Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.29 no.1 Bogotá Jan./Mar. 2014
Terapia endoscópica con argón plasma para tumores neuroendocrinos gástricos tipo I
Rodrigo Castaño, MD (1), Claudia Vargas, MD (1), Juan Camilo Pérez Cadavid, MD (1), Juan Pablo Dueñas, MD (1), Mario Hernán Ruiz, MD (1), Jorge A. Almenares, MD (1), Luis Miguel Ruiz, MD (1)
(1) Grupo antioqueño para el estudio de los tumores neuroendocrinos y GIST (GAE NET-GIST). Medellín-Colombia.
Fecha recibido: 12-08-13 Fecha aceptado: 19-12-13
Resumen
Antecedentes y objetivo: los datos con respecto a los carcinoides gástricos tipo I y su evolución en series prospectivas son escasos; por lo tanto, el tratamiento y el seguimiento no se han establecido unánimemente. Nuestro propósito es describir la aplicación de la coagulación por argón plasma (APC) para lograr la erradicación de múltiples carcinoides gástricos tipo I y observar el comportamiento en el tiempo después de la terapia. Métodos: durante un periodo de 7 años (julio 2005 – junio 2012) en dos centros de tercer nivel, 14 paciente fueron intervenidos por endoscopia al presentar tumores neuroendocrinos gástricos. Se les aplicó argón plasma para erradicar la presencia de múltiples carcinoides gástricos. Inmediatamente fueron sometidos a un programa de seguimiento endoscópico. Resultados: ninguno de los pacientes acusaba síntomas o signos específicos relacionados con la presencia de una gastritis crónica atrófica y el diagnóstico fue siempre un hallazgo incidental a la endoscopia. La biopsia endoscópica previa a la intervención mostró que los pólipos eran tumores neuroendocrinos tipo I intramucosos. La mediana del diámetro fue de 3,8 mm (rango 2-10 mm), la atrofia severa asociada estaba presente en siete casos (50%), mientras una atrofia multifocal se encontró en el 29%. El Helicobacter pylori (H pylori) se encontró en siete pacientes (50%). Durante un seguimiento promedio de 46 meses (intervalo de 17 a 84 meses) la sobrevida fue del 100% y la recurrencia estuvo presente en 10 pacientes (71%), sin embargo en todos ellos se erradicaron las lesiones. Enfermedades autoinmunes, gastrina, cromogranina A, índice de mitosis, y Ki 67 fueron evaluadas. No se presentaron complicaciones tipo sangrado o perforación. Conclusiones: la erradicación endoscópica completa con argón plasma de los tumores neuroendocrinos gástricos tipo I, es segura y sencilla.
Palabras claves
Tumores neuroendocrinos gástricos tipo I, endoscopia, argón plasma.
INTRODUCCIÓN
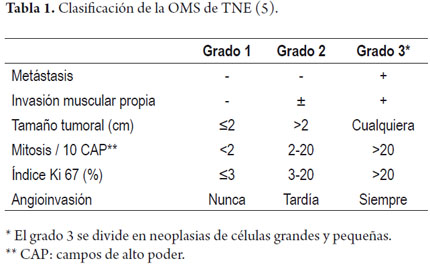
En general, la incidencia de tumores neuroendocrinos (TNE) se ha incrementado en los últimos 30 años (1). Los carcinoides gástricos o, como se denominan actualmente, tumores neuroendocrinos gástricos (TNE-G) (2) se originan de las células enterocromafines (CECA) productoras de histamina, aunque ocasionalmente pueden tener un fenotipo que sugieren otro origen; por ejemplo de CECA productoras de somatostatina o células productoras de Grelina (3). Las CECA se clasifican en dependientes o independientes de gastrina, aunque ambas expresan el receptor gastrina/CCK2 (4). Estas son lesiones raras; representan el 7% de todos los TNE y el 1% de los tumores gástricos. De acuerdo con la clasificación histológica de estos tumores por la OMS (5) en 2010 (tabla 1) se clasifican como se muestra a continuación:
1. TNE bien diferenciados de grado bajo o intermedio (G1, G2)
2. TNE pobremente diferenciados (G3, G4).
Los TNE-G dependientes de gastrina se relacionan con condiciones que inducen hipergastrinemia, como en la gastritis atrófica crónica (tipo I, 70%-80%) y los gastrinomas con síndrome de Zollinger Ellison (tipo II, 5%-6%), mientras los tumores independientes de la gastrina (tipo III, 20% y tipo IV, <5%) cursan con niveles normales de gastrina y no responden a la gastrina como promotora de la proliferación (6, 7). Los tumores tipo II se asocian a mutaciones del gen MEN-1, mientras que las lesiones independientes de gastrina no han sido investigadas suficientemente y su etiopatogenia es controvertida (8, 9).
Los TNE-G tipo I son generalmente asintomáticos, los tipo II pueden desarrollar enfermedad ulcerosa péptica por la hiperacidez, mientras que los tipos III y IV (indiferenciado) cursan con tumores grandes y ulcerados (6). Frecuentemente los TNE-G tipo I no muestran síntomas específicos asociados a la gastritis crónica atrófica y el diagnóstico es un hallazgo incidental durante la endoscopia alta. Estos TNE son bien diferenciados, con un bajo índice Ki-67, a menudo múltiples y en el estómago proximal. Se observan como pólipos de pequeño tamaño (<2 cm), pero hasta el 25% los TNE-G tipo I no son visibles macroscópicamente durante la endoscopia y solo son aparentes al estudio histológico, en estos casos se denominan "carcinoides intramucosos" (10).
Los estudio previos de TNE-G tipo I son retrospectivos y tienen un número escasos de pacientes; esto ocurre con todos los tipos. Se describe un curso indolente con escasos reportes de compromiso regional o metastásico (11-15).
El manejo de los TNE-G tipo I no ha sido establecido, se han sugerido diferentes alternativas. La gastrectomía se ha propuesto para las lesiones múltiples y/o grandes o para pacientes con recaídas luego de la resección endoscópica (16, 17). Los análogos de la somatostatina se han propuesto al disminuir el crecimiento tumoral tanto in vitro como in vivo (18-20). Una alternativa de manejo ya evaluada es la resección endoscópica con el seguimiento endoscópico subsiguiente. Sin embargo, entre los pocos estudios que han evaluado esta opción terapéutica, la mayoría tienen pocos pacientes y diferentes opciones de manejo; sumado a esto, cuentan con escasa información sobre recaídas (13, 15, 17, 21).
El manejo con argón plasma de los TNE se ha descrito como reporte de casos, también las primeras experiencias informadas de la terapia con argón plasma ha sido con TNE bronquiales; con buenos resultados (22-25). Los informes son muy pocos, con escasos números de pacientes y del uso de la terapia con argón plasma para TNE en el tracto digestivo (26, 27). Desde el año 2005 se implementó en dos centros de tercer nivel de la ciudad de Medellín la terapia con argón plasma para los TNE-G tipo I, con un seguimiento prospectivo de estos pacientes. Por lo tanto, el propósito de este estudio es evaluar el pronóstico clínico (sobrevida y progresión tumoral) como objetivo principal, y la tasa de recurrencia y los riesgos con la remoción endoscópica como objetivo secundario, en una serie consecutiva de pacientes con TNE-G tipo I manejados con argón plasma.
MÉTODOS
Pacientes y diseño del estudio
Los pacientes con diagnóstico de TNE-G tipo I con manejo endoscópico detectados entre julio de 2005 y junio de 2012 fueron ingresados en el estudio y seguidos prospectivamente con endoscopias.
En el momento de ingreso al estudio se registraron en un formulario desarrollado para tal efecto, y como fuente de alimentación para una base de datos, diferentes variables: sexo, edad, historia familiar de enfermedad ácido péptica, presencia de tiroiditis y/o diabetes mellitus tipo I, exámenes de laboratorio, grado de atrofia, estado de la CECA e infección por H pylori.
El diagnóstico de gastritis crónica atrófica se basó en la confirmación histológica con múltiples biopsias tomadas en el antro gástrico y el cuerpo. La gastritis se evaluó de acuerdo con el Sistema Sídney actualizado (28); la atrofia gástrica corporal se definió por el reemplazo focal o completo de las glándulas oxínticas por metaplasia intestinal; esta variable se graduó en una escala que va de la ausencia de atrofia (grado 0) a atrofia leve (grado 1), moderada (grado 2) o severa (grado 3). La atrofia antral se definió como completa o focal por la desaparición de las glándulas antrales o por ser reemplazadas por epitelio intestinal metaplásico.
Para definir el estado de la CECA se utilizó la clasificación de Solcia (29). Se consideraron hiperplásicas aqellas células proliferativas con un diámetro <150 µm, que pueden ser de patrón normal, simple o lineal, micronodular o adenomatoide. La displasia se diagnosticó con una proliferación >150 µm pero <500 µm, mientras una proliferación >500 µm se definió como un TNE-G tipo I.
El diagnóstico de anemia perniciosa se basó en la presencia de una anemia macrocítica (hemoglobina <13 g/dL en hombres y <12 g/dL en mujeres, con volumen corpuscular >100 fL, baja vitamina B12 (<197 pg/mL) que responde a B12 IM y diagnóstico de gastritis corporal atrófica (30).
El diagnóstico de tiroiditis autoinmune se basó en la presencia de autoanticuerpos tiroideos y ecografía sugerente de tiroiditis, independiente de la función tiroidea (31).
Las pruebas de laboratorio realizadas fueron hemograma, gastrina sérica, cromogranina A, ferritina y B12, la presencia del H pylori se estableció por la biopsia antral a la endoscopia. Una vez hecho el diagnóstico de presencia del H pylori, este se trató con la triple terapia estándar (omeprazol, claritromicina y amoxicilina), el control de la erradicación se realizó con el test de aliento un mes después de terminar la terapia. El síndrome de neoplasia endocrina múltiple se descartó con base en el estudio de los síntomas, la historia personal y familiar y pruebas de laboratorio.
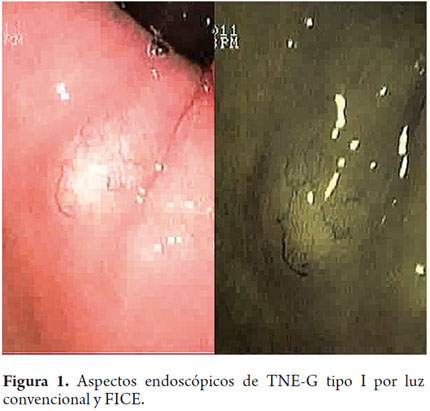
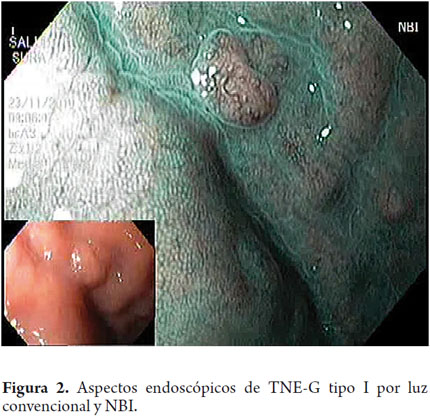
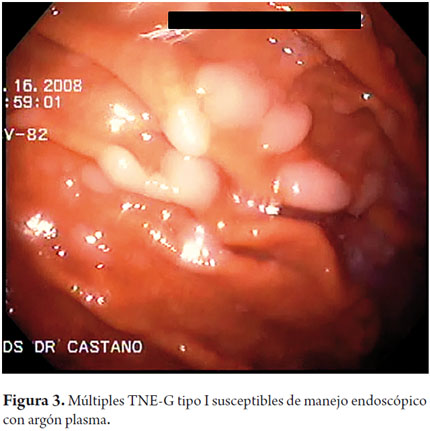
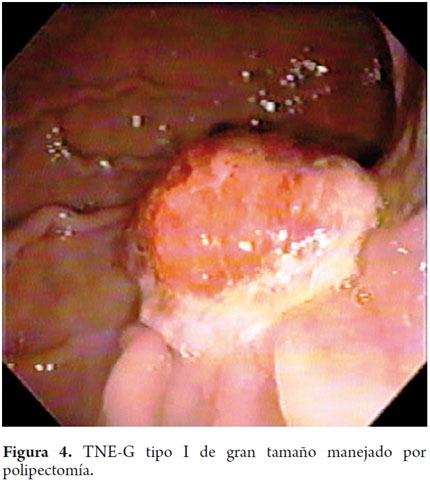
Característicamente a la endoscopia, los TNE-G tipo I son lesiones polipoides pequeñas (<1 cm) con aspecto de lesión subepitelial por presentar una mucosa normal o con aumento de la vascularización y una coloración amarillenta; cuando se observa depresión, erosión o ulceración se sugiere la posibilidad de carcinoma (figuras 1, 2, 3 y 4).
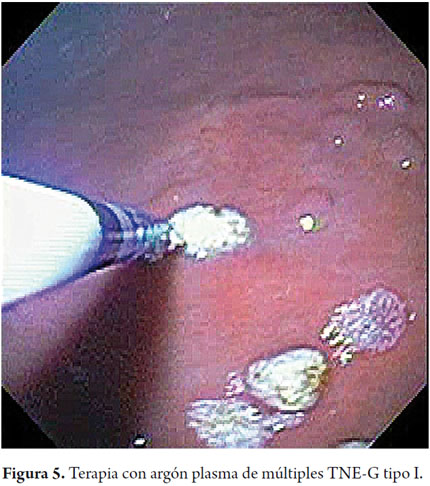
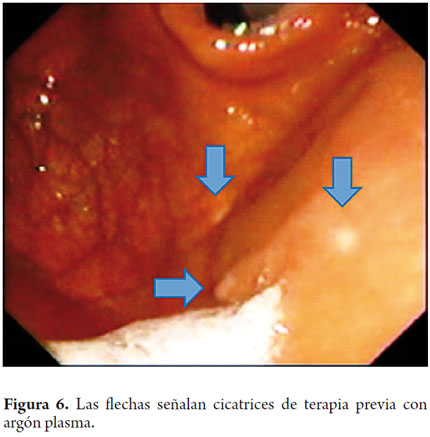
El procedimiento terapéutico endoscópico se realizó bajo sedación con midazolam más meperidina y todas las lesiones visibles fueron tratadas con argón plasma con parámetros predeterminados de potencia en 50 W y flujo de 1 L/min con una distancia del catéter de 2 a 4 mm y por pulsos de 1 a 2 segundos de duración, evitando el contacto con el tejido y tras un lavado para remover detritus, saliva o moco (figuras 5 y 6).
Además, se tomaron biopsias de cuerpo y antro con una pinza de biopsia estándar, oval y fenestrada. Ninguno de los pacientes fue estudiado con ultrasonido endoscópico. Los pacientes fueron controlados entre 4 a 6 meses después de la terapia inicial, se realizaron biopsias del antro y del cuerpo para tratar de identificar neoplasias endocrinas intramucosas (32). En los casos de remoción endoscópica de lesiones, las muestras fueron recogidas en formol bufferado al 10%, procesadas con secciones de 5 µm de espesor y teñidas con hematoxilina y eosina para la evaluación rutinaria. No se realizaron tinciones específicas para H pylori ni para la detección de la metaplasia intestinal.
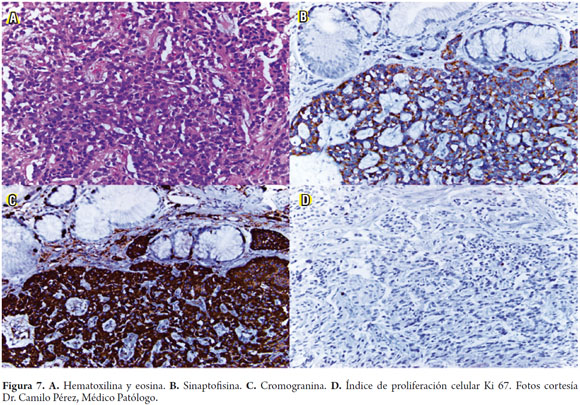
El estudio histológico se hizo con hematoxilina y eosina y diferentes tinciones específicas para estas neoplasias como la sinaptofisina, cromogranina y el índice de proliferación celular Ki 67 (figura 7).
El tiempo de seguimiento se considera desde la intervención endoscópica, en que se realiza la ablación de la lesión con argón plasma, hasta el último control. El tiempo de recurrencia se define como el intervalo entre la terapia con argón plasma y la detección de una nueva lesión al control endoscópico. Las complicaciones endoscópicas se registraron al momento de la intervención y durante el período de seguimiento.
Análisis de los datos y evaluación estadística
El análisis estadístico se realizó con un software dedicado, el IBM SPSS versión 18. Los datos fueron expresados como medianas (rango intercuartílico de 25 a 75). El análisis del tiempo libre de recurrencia se realizó con el método de Kaplan-Meier, el análisis univariado de los factores de riesgo se hizo con el modelo de riesgos proporcionales de Cox. La p fue considerada significativa cuando era <0,05.
RESULTADOS
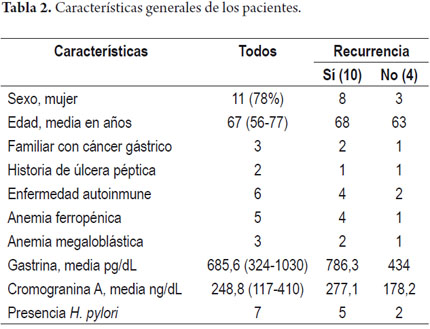
Se trataron por endoscopia con argón plasma 14 pacientes (11 mujeres-78%) con TNE-G tipo I, con un promedio de edad de 67 años y un promedio de gastrina de 685 pg/dL (tabla 2).
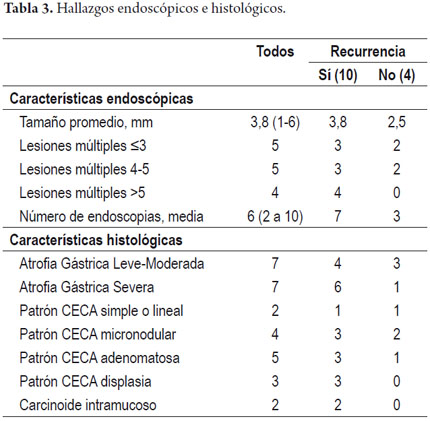
Al momento del diagnóstico el promedio del tamaño de las lesiones era de 3,8 mm y todos los pacientes tenían lesiones múltiples; en dos casos había carcinoides intramucosos (tabla 3).
Todos los pacientes fueron tratados endoscópicamente con argón plasma y no se presentaron complicaciones relacionadas con la terapia ni hubo necesidad de hospitalización de los pacientes.
El 50% de los pacientes tenían una atrofia leve-moderada y en el otro 50% era severa. En 4 pacientes también había atrofia antral lo que configura la atrofia multifocal (29%).
El seguimiento promedio fue de 46 meses (rango 18 a 84 meses) con una media de 6 endoscopias (rango de 2 a 10). No se registraron muertes relacionadas con el tumor. Durante el seguimiento por lo menos un estudio de imágenes se le realizó a los pacientes (tomografía o resonancia de abdomen) sin evidenciar compromiso local, regional o a distancia.
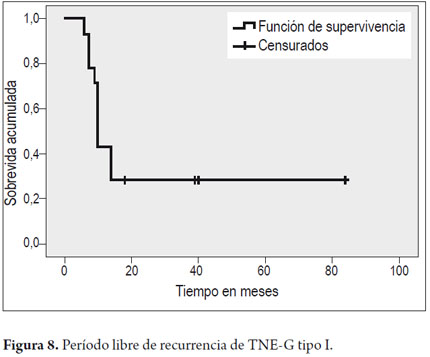
Después de la terapia inicial con argón plasma, durante el seguimiento se detectaron 10 de 14 pacientes con recaídas (71%), pero en 4 pacientes no se presentaron más lesiones. El promedio de la primera recaída fue de 6 meses y a un año la tasa de recaídas era del 42% (figura 8). Las recaídas fueron múltiples en nueve pacientes (tabla 4).
En la evaluación de los pacientes con recurrencia se encontró que la atrofia severa y la anemia (75%) son factores de riesgo para recurrencia (85,7%).
DISCUSIÓN
El presente estudio multicéntrico prospectivo muestra a través del seguimiento endoscópico de los pacientes con TNE-G tipo I tratados con ablación con argón plasma que este es un procedimiento seguro y efectivo, con una sobrevida del 100% y sin metástasis, sin complicaciones relacionadas con la intervención y que permite la detección temprana de neoplasias neuroendocrinas recurrentes que aparecen durante el seguimiento.
En este estudio se demuestra que esta neoplasia es altamente recurrente y que varios pacientes presentaron más de una recurrencia; esta situación ya ha sido sugerida por el estudio de Merola (21) en un grupo de pacientes manejados con la resección endoscópica de las lesiones (32 pacientes) con seguimiento prospectivo.
Los datos de diferentes estudios muestran que los pacientes con TNE-G tipo I se presentan con múltiples lesiones en el cuerpo y fondo gástrico y que con el seguimiento el comportamiento, como se sugiere en otras series retrospectivas y multicéntricas (13, 15, 21, 33-35), puede ser más agresivo y con una tasa de proliferación mayor.
La evaluación del comportamiento biológico de los TNE-G tipo I y la posibilidad de estandarizar su manejo ha sido difícil hasta la fecha, porque los estudios se basan en estudios con pocos pacientes o series de casos, retrospectivos, multicéntricos e incluyen todos los tipos de neoplasias: neuroendocrinas gástricas, analizando en forma conjunta tumores con diferentes pronósticos (13, 15, 33-37).
Algunos autores proponen la cirugía como única alternativa capaz de evitar la progresión tumoral y resolver definitivamente la hipergastrinemia (16, 17). Hay propuestas para el manejo de los TNE-G tipo I que incluyen diversas terapias con diferentes números de lesiones, desiguales tamaños, con cirugía en caso de pólipos grandes o recurrentes; limitando el manejo conservador en los casos de TNE-G tipo I pequeños (16, 38). Se han reportado promisorios resultados en la literatura con el uso de los análogos de somatostatina en pacientes con múltiples TNE-G tipo I sin ningún signo de invasión (18-20, 33, 39, 40).
Otra opción es el enfoque conservador con endoscopia y resección de las lesiones, sin embargo, no existen series que muestren su eficacia con un seguimiento a largo plazo (41-43). Los TNE-G tipo I son de un curso indolente, otros autores proponen un manejo expectante, limitar la resección a los pólipos grandes con signos de diseminación (12, 44). Sin embargo, los pacientes con gastritis atrófica corporal están en riesgo de desarrollar carcinoma, por lo que cualquier lesión levantada es mandatorio su resección; la incidencia anual de adenocarcinoma en estos pacientes es del 0,25% en los casos con metaplasia intestinal, de 0,6% cuando hay displasia leve a moderada y del 6% en caso de displasia severa (45, 46).
El objetivo principal del estudio fue determinar el pronóstico clínico de los pacientes con TNE-G tipo I que fueron manejados con la ablación endoscópica con argón plasma, demostrándose una sobrevida del 100% tras una mediana de casi 5 años de seguimiento, sin evidencia de compromiso metastásico local o a distancia. Estos hallazgos sugieren que el manejo endoscópico conservador es efectivo y seguro, ningún paciente tuvo complicaciones endoscópicas o necesidad de hospitalización. Por el contrario, la mayor morbimortalidad y el impacto desfavorable en la calidad de vida de los pacientes sometidos a gastrectomía deben ser tenidos en cuenta.
La cirugía se deja para pacientes con lesiones malignas (carcinoma o tumores neuroendocrinos mal diferenciados) si se detectan durante la evolución. En el presente estudio no se demostraron lesiones tipo carcinoma. El seguimiento estrecho permite la detección temprana del compromiso locorregional, evitando el tratamiento adyuvante.
Estos tumores también pueden detectarse como neoplasias intramucosas. Como muchos de ellos no son visibles, no se puede determinar cuáles son verdaderas recurrencias o que estuviesen presente en las endoscopias previas. En estos pacientes, el mapeo con biopsias gástricas durante las endoscopias de seguimiento incrementan la posibilidad de encontrar los tumores neuroendocrinos intramucosos (32, 46).
Se ha sugerido que los TNE-G tipo I se relacionan con atrofia gástrica de moderada a severa en el cuerpo gástrico, pero también se han encontrado con atrofia corporal leve (15, 19). En nuestra serie, el 50% cursó con atrofia gástrica leve/moderada. Este patrón histológico es aplicable a las CECA y la sola presencia de una hiperplasia lineal o simple asociada al TNE-G tipo I, lo que es consistente con reportes pequeños que muestran la relación de los TNE-G tipo I con la hiperplasia simple o linear (34).
Un segundo objetivo de evaluación fue la tasa de recurrencia. En esta serie de casos se encontró una recurrencia del 71% después de la resección inicial. Sin embargo, como se sugirió previamente, los TNE-G tipo I frecuentemente son múltiples y pequeños e incluso pueden haber carcinomas intramucosos, por lo que no se puede precisar cuántos fueron realmente recurrencia y cuántos no fueron vistos en la endoscopia inicial. El control endoscópico se realizó entre los 6 y 12 meses siguientes acorde sí había o no recurrencia. En pacientes sin recaídas el seguimiento se hace cada 12 meses y puede espaciarse a cada 2 a 4 años acorde si hay o no atrofia gástrica (21).
En los pacientes con recurrencias deben identificarse los factores de riesgo que determinan la recaída luego de la primera intervención, reservando el seguimiento endoscópico estricto para estos pacientes. La anemia (75%) y la atrofia severa (85,7%) estuvieron más presentes en los pacientes con recurrencia que sin ella.
Las principales limitaciones de este estudio son su corto número de pacientes y el relativo corto período de seguimiento. Sin embargo, debido a lo infrecuente de esta condición se requerirían de estudios multicéntricos y prospectivos para resolver estos problemas. Otro factor limitante es el concepto de recurrencia, por la posibilidad de multicentricidad o de lesiones residuales después de la terapia inicial. Sin embargo, un espacio de seguimiento de seis meses parece ser efectivo para controlar el crecimiento de las CECA, sin afectar la posibilidad de recurrencia.
CONCLUSIONES
Este estudio muestra una alta tasa de recurrencia de lesiones de este tipo, pero con un riesgo muy bajo de malignización; también muestra que el manejo endoscópico es seguro y efectivo, con un 100% de sobrevida. El seguimiento endoscópico permite la detección temprana de recaídas. Son necesario más estudios para determinar cuáles son los factores de riesgo de recurrencia en lo pacientes con TNE-G tipo I.
REFERENCIAS
1. Ter-Minassian M, Chan JA, Hooshmand SM, et al. Clinical presentation, recurrence, and survival in patients with neuroendocrine tumors: results from a prospective institutional database. Endocrine-related cancer 2013;20(2):187-96. [ Links ]
2. Modlin IM, Oberg K, Chung DC, et al. Gastroentero-pancreatic neuroendocrine tumours. The lancet oncology 2008;9:61-72. [ Links ]
3. Latta E, Rotondo F, Leiter LA, Horvath E, Kovacs K. Ghrelin- and serotonin-producing gastric carcinoid. J Gastrointest Cancer 2012;43:319-23. [ Links ]
4. Rindi G, Luinetti O, Cornaggia M, Capella C, Solcia E. Three subtypes of gastric argyrophil carcinoid and the gastric neuroendocrine carcinoma: a clinicopathologic study. Gastroenterology 1993;104:994-1006. [ Links ]
5. Klimstra DS, Modlin IR, Coppola D, Lloyd RV, Suster S. The pathologic classification of neuroendocrine tumors: a review of nomenclature, grading, and staging systems. Pancreas 2010;39:707-12. [ Links ]
6. Vargas CC, Castaño R. Tumores neuroendocrinos gastroenteropancreáticos. Rev Col Gastroenterol 2010;24:165-76. [ Links ]
7. Scherubl H, Cadiot G, Jensen RT, Rosch T, Stolzel U, Kloppel G. Neuroendocrine tumors of the stomach (gastric carcinoids) are on the rise: small tumors, small problems? Endoscopy 2010;42:664-71. [ Links ]
8. Nikou GC, Angelopoulos TP. Current concepts on gastric carcinoid tumors. Gastroenterology research and practice 2012;2012:287825. [ Links ]
9. Kidd M, Gustafsson BI. Management of gastric carcinoids (neuroendocrine neoplasms). Current gastroenterology reports 2012;14:467-72. [ Links ]
10. Delle Fave G, Capurso G, Milione M, Panzuto F. Endocrine tumours of the stomach. Best practice & research Clinical gastroenterology 2005;19:659-73. [ Links ]
11. Landry CS, Brock G, Scoggins CR, McMasters KM, Martin RC, 2nd. A proposed staging system for gastric carcinoid tumors based on an analysis of 1,543 patients. Ann Surg Oncol 2009;16:51-60. [ Links ]
12. Hosokawa O, Kaizaki Y, Hattori M, et al. Long-term follow up of patients with multiple gastric carcinoids associated with type A gastritis. Gastric cancer : official journal of the International Gastric Cancer Association and the Japanese Gastric Cancer Association 2005;8:42-6. [ Links ]
13. Jordan PH, Jr., Barroso A, Sweeney J. Gastric carcinoids in patients with hypergastrinemia. Journal of the American College of Surgeons 2004;199:552-5. [ Links ]
14. Gladdy RA, Strong VE, Coit D, et al. Defining surgical indications for type I gastric carcinoid tumor. Ann Surg Oncol 2009;16:3154-60. [ Links ]
15. Borch K, Ahren B, Ahlman H, Falkmer S, Granerus G, Grimelius L. Gastric carcinoids: biologic behavior and prognosis after differentiated treatment in relation to type. Annals of surgery 2005;242:64-73. [ Links ]
16. Modlin IM, Lye KD, Kidd M. Carcinoid tumors of the stomach. Surgical oncology 2003;12:153-72. [ Links ]
17. Dakin GF, Warner RR, Pomp A, Salky B, Inabnet WB. Presentation, treatment, and outcome of type 1 gastric carcinoid tumors. Journal of surgical oncology 2006;93:368-72. [ Links ]
18. Manfredi S, Pagenault M, de Lajarte-Thirouard AS, Bretagne JF. Type 1 and 2 gastric carcinoid tumors: long-term follow-up of the efficacy of treatment with a slow-release somatostatin analogue. Eur J Gastroenterol Hepatol 2007;19:1021-5. [ Links ]
19. Campana D, Nori F, Pezzilli R, et al. Gastric endocrine tumors type I: treatment with long-acting somatostatin analogs. Endocrine-related cancer 2008;15:337-42. [ Links ]
20. Grozinsky-Glasberg S, Kaltsas G, Gur C, et al. Long-acting somatostatin analogues are an effective treatment for type 1 gastric carcinoid tumours. European journal of endocrinology / European Federation of Endocrine Societies 2008;159:475-82. [ Links ]
21. Merola E, Sbrozzi-Vanni A, Panzuto F, et al. Type I gastric carcinoids: a prospective study on endoscopic management and recurrence rate. Neuroendocrinology 2012;95:207-13. [ Links ]
22. Cetinkaya E, Aras G, Sokucu SN, Ozgul A, Altin S. Treatment of endoluminal typical carcinoid tumor with bronchoscopic techniques. Tuberkuloz ve toraks 2009;57:427-30. [ Links ]
23. Karasulu L, Altin S, Dalar L, Sokucu S, Simsek N. [Two typical carcinoid cases treated by endobronchial approach]. Tuberkuloz ve toraks 2009;57:212-7. [ Links ]
24. Jabbardarjani H, Masjedi M, Herth F. Successful treatment of endobronchial carcinoid using argon plasma coagulation. Journal of bronchology & interventional pulmonology 2009;16:196-8. [ Links ]
25. Orino K, Kawai H, Ogawa J. Bronchoscopic treatment with argon plasma coagulation for recurrent typical carcinoids: report of a case. Anticancer Res 2004;24:4073-7. [ Links ]
26. Multiple gastric carcinoids type I. (en línea) GastroSource: (accesado 5 Feb 2013) Disponible en: http://www.gastrosource.com/Patient-Cases/Dr.Kruse/ [ Links ]
27. Green HL. Treatment of Duodenal Carcinoid with Argon Plasma Coagulation. Proc UCLA Healthcare 2003;7:37-8. [ Links ]
28. Dixon MF, Genta RM, Yardley JH, Correa P. Classification and grading of gastritis. The updated Sydney System. International Workshop on the Histopathology of Gastritis, Houston 1994. Am J Surg Pathol 1996;20:1161-81. [ Links ]
29. Solcia E, Bordi C, Creutzfeldt W, et al. Histopathological classification of nonantral gastric endocrine growths in man. Digestion 1998;41:185-200. [ Links ]
30. Lahner E, Caruana P, D'Ambra G, et al. First endoscopic-histologic follow-up in patients with body-predominant atrophic gastritis: when should it be done? Gastrointestinal endoscopy 2001;53:443-8. [ Links ]
31. Lahner E, Centanni M, Agnello G, et al. Occurrence and risk factors for autoimmune thyroid disease in patients with atrophic body gastritis. The American journal of medicine 2008;121:136-41. [ Links ]
32. Annibale B, Azzoni C, Corleto VD, et al. Atrophic body gastritis patients with enterochromaffin-like cell dysplasia are at increased risk for the development of type I gastric carcinoid. Eur J Gastroenterol Hepatol 2001;13:1449-56. [ Links ]
33. Granberg D, Wilander E, Stridsberg M, Granerus G, Skogseid B, Oberg K. Clinical symptoms, hormone profiles, treatment, and prognosis in patients with gastric carcinoids. Gut 1998;43:223-8. [ Links ]
34. Yu JY, Wang LP, Meng YH, Hu M, Wang JL, Bordi C. Classification of gastric neuroendocrine tumors and its clinicopathologic significance. World J Gastroenterol 1998;4:158-61. [ Links ]
35. Rindi G, Bordi C, Rappel S, La Rosa S, Stolte M, Solcia E. Gastric carcinoids and neuroendocrine carcinomas: pathogenesis, pathology, and behavior. World journal of surgery 1996;20:168-72. [ Links ]
36. Modlin IM, Lye KD, Kidd M. A 50-year analysis of 562 gastric carcinoids: small tumor or larger problem? Am J Gastroenterol 2004;99:23-32. [ Links ]
37. Rindi G, Azzoni C, La Rosa S, et al. ECL cell tumor and poorly differentiated endocrine carcinoma of the stomach: prognostic evaluation by pathological analysis. Gastroenterology 1999;116:532-42. [ Links ]
38. Ruszniewski P, Delle Fave G, Cadiot G, et al. Well - differentiated gastric tumors/carcinomas. Neuroendocrinology 2006;84:158-64. [ Links ]
39. Ferraro G, Annibale B, Marignani M, et al. Effectiveness of octreotide in controlling fasting hypergastrinemia and related enterochromaffin-like cell growth. The Journal of clinical endocrinology and metabolism 1996;81:677-83. [ Links ]
40. Fykse V, Sandvik AK, Qvigstad G, Falkmer SE, Syversen U, Waldum HL. Treatment of ECL cell carcinoids with octreotide LAR. Scandinavian journal of gastroenterology 2004;39:621-8. [ Links ]
41. Ichikawa J, Tanabe S, Koizumi W, et al. Endoscopic mucosal resection in the management of gastric carcinoid tumors. Endoscopy 2003;35:203-6. [ Links ]
42. Kokkola A, Sjoblom SM, Haapiainen R, Sipponen P, Puolakkainen P, Jarvinen H. The risk of gastric carcinoma and carcinoid tumours in patients with pernicious anaemia. A prospective follow-up study. Scandinavian journal of gastroenterology 1998;33:88-92. [ Links ]
43. Rappel S, Altendorf-Hofmann A, Stolte M. Prognosis of gastric carcinoid tumours. Digestion 1995;56:455-62. [ Links ]
44. Johnson FE, Smith JB, Janney CM, Ramrakhiani S. Multiple gastric carcinoids. Journal of the American College of Surgeons 2003;196:984-5. [ Links ]
45. de Vries AC, van Grieken NC, Looman CW, et al. Gastric cancer risk in patients with premalignant gastric lesions: a nationwide cohort study in the Netherlands. Gastroenterology 2008;134:945-52. [ Links ]
46. Bordi C, Azzoni C, Ferraro G, et al. Sampling strategies for analysis of enterochromaffin-like cell changes in Zollinger-Ellison syndrome. Am J Clin Pathol 2000;114:419-25. [ Links ]











 text in
text in