Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.29 no.2 Bogotá Apr./June 2014
Utilización de AINES y uso de IBP profilácticos en pacientes de medicina interna
álvaro Osorio MD. (1), William Otero Regino MD. (2), Martín Gómez Zuleta MD. (3)
(1) Residente de Medicina Interna, Universidad Nacional de Colombia. Bogotá, Colombia.
(2) Profesor de Medicina, Unidad de Gastroenterología, Universidad Nacional de Colombia, Gastroenterólogo, Clínica Fundadores. Bogotá, Colombia.
(3) Profesor de Medicina, Unidad de Gastroenterología, Universidad Nacional de Colombia, Gastroenterólogo, Hospital El Tunal, Hospital de Kennedy. Bogotá, Colombia.
Fecha recibido: 08-01-14 Fecha aceptado: 08-05-14
Resumen
Introducción: los antiinflamatorios no esteroideos (AINES) son prescritos con frecuencia en la práctica médica y sus eventos adversos gastrointestinales aumentan la morbimortalidad, la cual puede disminuir utilizando profilácticamente inhibidores de la bomba de protones (IBP), misoprostol o anti H2. Objetivo: estimar la prevalencia de consumo de AINES en una población de consulta externa de Medicina Interna y, en ellos, determinar la frecuencia de prescripción profiláctica de IBP en pacientes con riesgo de sangrado gastrointestinal.
Métodos: estudio prospectivo de prevalencia analítica con pacientes mayores de 18 años de la consulta externa de Medicina Interna de la Fundación Hospital San Carlos de Bogotá. Los pacientes consumidores de AINES fueron clasificados en tres grupos de riesgo de sangrado gastrointestinal con base en los factores de riesgo tradicionalmente descritos.
Resultados: de 140 pacientes incluidos, el 30% tomaban AINES. El 47,6% (n=20) fueron clasificados en el grupo de bajo riesgo, el 28,5% (n=12) en el grupo de riesgo intermedio y el 23,8% (n=10) en el grupo de alto riesgo. El 47% (20 pacientes) de los que consumían AINES tomaban simultáneamente IBP. Con respecto a los grupos de riesgo, consumían IBP el 80% de alto riesgo, el 50% de riesgo intermedio y el 30% de bajo riesgo.
Conclusión: en la población estudiada, la prescripción de IBP en pacientes de alto riesgo es superior a la informada en trabajos internacionales (80% versus menos del 50%). Hay formulación de IBP innecesaria en el 30% de los pacientes de bajo riesgo.
Palabras claves
AINES, IBP, profilaxis, gastroprotección.
INTRODUCCIÓN
Los antiinflamatorios no esteroideos (AINES) son medicamentos frecuentemente utilizados en diferentes condiciones inflamatorias, así como para el alivio sintomático de la fiebre y el dolor sin inflamación (1). Mundialmente están dentro de los medicamentos más prescritos. Se estima que en Estados Unidos se producen más de 100 millones de prescripciones anuales (2) con un costo aproximado de 4800 millones de dólares (2,3). Al lado de su demostrada eficacia analgésica y antiinflamatoria, tienen efectos adversos cardiovasculares y gastrointestinales que pueden tener complicaciones fatales (4-6) y, en la actualidad, se considera que los AINES y la aspirina causan la mayoría de úlceras pépticas sangrantes (7). El 25% de los usuarios crónicos de AINES desarrollan úlceras pépticas, del 2%-4% presentan sangrado o perforación y en USA esto origina más de 100 000 hospitalizaciones al año y de 10 000 a 17 000 muertes, especialmente en pacientes de la categoría de alto riesgo (8). Hay factores establecidos que aumentan el riesgo de sangrado por las úlceras pépticas en los consumidores de AINES, entre los cuales está la edad mayor de 65 años, antecedente de úlcera con o sin sangrado, uso concomitante de anticoagulantes o esteroides, comorbilidades graves o utilización de altas dosis de AINES (7,8). Hay suficiente evidencia de que la coprescripción de antisecretores disminuye el riesgo de sangrado por úlceras en pacientes de alto riesgo (9). Cuando se utiliza misoprostol 800 µg/día, anti H2 en doble dosis o inhibidores de la bomba de protones (IBP) con un RR: 0,17; RR: 0,44; RR: 0,40 respectivamente (9). Además, se han publicado diversas guías para la prevención de las complicaciones de úlceras por AINES (8, 10,11). No obstante, la amplia difusión de estas guías y varios estudios internacionales han demostrado que los medicamentos protectores en los pacientes con riesgo de complicaciones por AINES dejan de utilizarse en el 60%-80% de ellos y, en cambio, se utiliza gastroprotección exagerada en pacientes con bajo riesgo de complicaciones (12-14). En Colombia no se han realizado investigaciones sobre la prevalencia de prescripción de medicamentos protectores en pacientes que consumen crónicamente AINES, como tampoco sobre la población que utiliza estos medicamentos crónicamente. En un estudio reciente de Otero y colaboradores (15), se encontró que en pacientes con úlceras duodenales, el consumo de AINES o aspirina estaba presente en el 41% de estos. Teniendo en cuenta la importancia de la prescripción de antisecretores en pacientes que crónicamente utilizan AINES y la falta de información sobre el tema en el medio, se decidió realizar el presente trabajo de investigación.
MATERIALES Y MÉTODOS
Estudio prospectivo en pacientes mayores de 18 años, atendidos por el servicio de consulta externa de Medicina Interna de la Fundación Hospital San Carlos durante el período comprendido entre enero y abril de 2013. Se calculó un tamaño de muestra mínimo de 138 pacientes para estimar la prevalencia del consumo de AINES en la población atendida, tomando como base una prevalencia estimada de consumo de AINES del 10%, confianza del 95% y una precisión del 5%.
Durante el período del estudio los médicos que realizan la consulta externa de Medicina Interna (residentes y docentes) incluyeron los pacientes que asistieron a la consulta externa de Medicina Interna, que aceptaron participar en el estudio y firmaron el consentimiento informado. Para la recolección de los datos se diseñó un cuestionario en el cual se incluía: datos demográficos del paciente, indicación, dosis y duración del consumo de AINES/aspirina, diagnóstico actual o previo de úlceras pépticas complicadas o no complicadas, síntomas de reflujo gastroesofágico (pirosis y/o regurgitación), dispepsia (dolor o malestar en el abdomen superior con o sin náuseas o sensación de distensión abdominal o bloating), intolerancia a los AINES, utilización concomitante de IBP. No se registró la utilización de misoprostol ni de anti H2, debido a que el primero tiene formulación restringida por sus efectos abortivos y los anti H2 rara vez o nunca se formulan dos veces al día, que es la dosis protectora. También se consignaron las enfermedades concomitantes serias, las cuales están representadas por insuficiencia cardíaca congestiva, hipertensión arterial, accidente cerebrovascular, diabetes o hipercolesterolemia. También se consignó la utilización simultánea de anticoagulantes, esteroides o antiagregantes (clopidogrel) y consumo de dos o más AINES. Para disminuir o evitar el sesgo de memoria, en los consultorios en los que se iban a recolectar los pacientes, se tenían fotografías de los empaques de los diferentes AINES más frecuentemente utilizados, las cuales se mostraban a los pacientes cuando ellos tenían dudas de si estaban o no consumiendo estos medicamentos.
Se definió ingesta significativa de AINES como todo paciente que refiere consumo de AINES acumulado a las dosis referidas, igual o mayor a un mes en el último año, basado en definiciones usadas en estudio EPISER (16). La dosis de aspirina fue considerada antitrombótica cuando era menor a 300 mg/día y AINES cuando era superior a 300 mg/día (17). Los pacientes fueron estratificados en tres grupos de riesgo de sangrado: alto, medio o bajo, de acuerdo a la presencia de 2 o más factores de riesgo, un factor de riesgo o la ausencia de estos factores, respectivamente (8). Los residentes de Medicina Interna rotantes en el servicio de consulta externa que participaron en la recolección de datos recibieron una charla en la cual se desarrollaron los siguientes temas: importancia de la prescripción de AINES, gastrotoxicidad de los AINES, factores de riesgo para sangrado gastrointestinal en pacientes consumidores de AINES, gastroprotección en pacientes consumidores de AINES, socialización del protocolo, definiciones y socialización del instrumento de recolección de datos. El protocolo de investigación y el consentimiento informado fueron aprobados por el comité de ética de la institución.
Objetivos del estudio (end points)
Los principales objetivos del estudio fueron determinar la prevalencia del consumo de AINES en pacientes atendidos en la consulta externa de Medicina Interna general (por propia iniciativa o prescritos por el médico) y la utilización de medicamentos gastroprotectores de acuerdo a al tipo de riesgo (bajo, moderado o alto) para presentar complicaciones gastroduodenales.
Análisis estadístico
La base de datos analizada fue diseñada en programa Excel®, Licencia de Microsoft Office 2010, el programa estadístico empleado fue IBM® SPSS® Statistics Versión 18. Se realizó un análisis descriptivo de las variables demográficas y clínicas de los pacientes consumidores de AINES e IBP. La descripción de las variables demográficas y clínicas se expresó en las variables categóricas como frecuencias absolutas y relativas, las variables continuas se describieron usando medidas de tendencia central. Se realizaron pruebas de normalidad de las variables cuantitativas continuas. Para estimar la diferencia entre edad y el consumo de AINES se realizó análisis ANOVA con un nivel de significancia del 95% y un error máximo de 0,05. Para las variables dicotómicas se utilizó la prueba de Chi cuadrado.
RESULTADOS
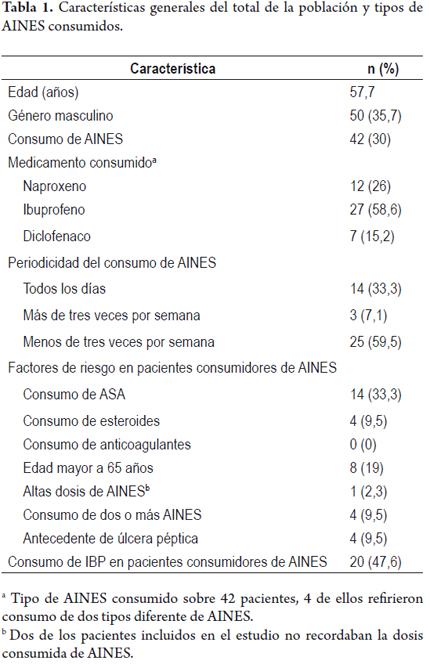
De un total de 450 pacientes atendidos en la consulta de Medicina Interna, durante el período de estudio, 140 cumplieron los criterios de inclusión y decidieron participar en el estudio, de estos 35,7% eran mujeres. La edad promedio fue 57,7 años (19-90 años). Entre los 140, 42 pacientes (30% IC 95%; 16-30) consumían AINES y de estos 29 (69%) eran mujeres. La edad promedio fue de 53,8 años (19-90 años). Las características generales de la población y la proporción del consumo de los diferentes tipos de AINES se muestran en la tabla 1.
Con relación a la frecuencia del consumo de AINES, 14 pacientes (33,3%) los consumía diariamente, 3 pacientes (7,1%) tres o más veces por semana y 25 pacientes (59,5%) menos de tres veces por semana. Del total de los pacientes, 27 (64,2%) tenía un consumo significativo de AINES en el último año (consumo por más de un mes en el último año al ingreso del estudio). Con respecto de los factores de riesgo se encontró que 14 pacientes (33,3%) tenían consumo concomitante de ácido acetilsalicílico a dosis de prevención cardiovascular primaria o secundaria, 8 (19%) eran mayores de 65 años, 4 pacientes (9,5%) consumían de esteroides, 4 (9,5%) tenían antecedente de úlcera péptica diagnosticada por endoscopia, 4 pacientes (9,5%) consumían dos o más AINES y 1 paciente tenía consumo alto de AINES. Dos pacientes no recordaban las dosis diarias del medicamento consumido, ningún paciente consumía anticoagulantes.
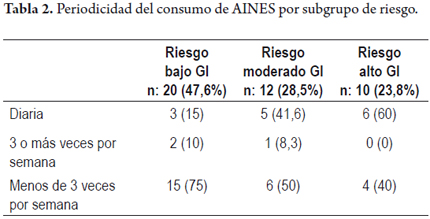
Con respecto a los factores de riesgo, 20 pacientes no tenían ningún factor de riesgo para sangrado gastrointestinal (bajo riesgo), 12 pacientes (28,5%) tenían un solo factor de riesgo (riesgo intermedio) 7 pacientes (16,6%) tenían dos factores de riesgo y 3 pacientes (7,1%) tenían más de dos factores de riesgo. Estos últimos diez pacientes clasificaron para alto riesgo. En la tabla 2 se muestra la periodicidad de consumo de AINES de acuerdo a los grupos de riesgo.
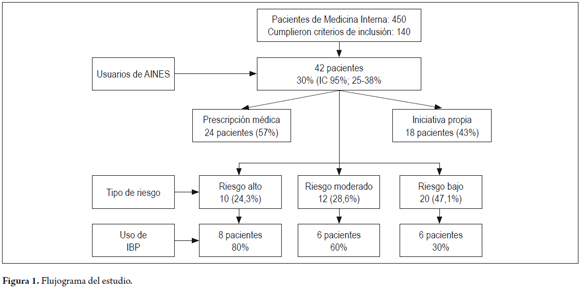
De los 42 pacientes que consumían AINES, 20 de ellos (47,6%) tomaban IBP. Estos corresponden a 8/10 (80%) de alto riesgo, 6/12 (50%) de riesgo moderado y 6/20 (33%) de riesgo bajo. La utilización de los AINES se hacía por prescripción médica en el 57% (24 pacientes), el resto lo hacía por su propia iniciativa. El flujograma del estudio se muestra en la figura 1.
Al analizar el promedio de edad estratificado por la condición de consumo, se encontró que el grupo de los consumidores poseen una edad media de 53,8 años, en contraste con el grupo de los no consumidores, que tiene una edad promedio de 59,48 años (p<0,05). No hubo diferencias estadísticamente significativas entre la proporción de mujeres y hombres, y el consumo de AINES.
DISCUSIÓN
En el presente estudio el 30% de los pacientes atendidos en consulta externa de Medicina Interna de la Fundación Hospital San Carlos, consumen AINES. Un estudio poblacional realizado en España con una muestra superior a 2900 sujetos, mostró que el 20,6% (IC 95%; 15,8-25,4) de la población incluida en el muestreo consumía AINES (18). En el estudio el 23,8% de los pacientes consumidores de AINES fueron considerados de alto riesgo, cifra que es similar a la encontrada en el estudio español LOGICA realizado en pacientes con osteoartritis, en el cual fue de 22,3% (17). Los resultados mostraron que la mayoría de los pacientes de alto riesgo (80%) tomaba IBP y también el 50% de los pacientes con riesgo moderado, cifras que son superiores a las encontradas en investigaciones internacionales, en los cuales la gastroprotección se hace sólo en el 20% a 45% (12-14,19-21) de los pacientes. En el presente estudio se evidencia una alta frecuencia de gastroprotección en los pacientes de alto riesgo, aunque lo ideal es que el 100% los pacientes con riesgo alto y riesgo moderado reciban la profilaxis.
En esta investigación, al igual que en otros trabajos (20,21), una proporción importante de pacientes sin riesgo (30%) recibían IBP, lo cual es innecesario ya que la profilaxis en este grupo no es costo-eficaz (22). Es posible que la alta prescripción de IBP en los grupos de riesgo alto o moderado se deba a la indiscriminada utilización de los IBP en el medio y, en este caso, esta práctica generalizada favorece a estos grupos de pacientes, aunque lo ideal es que los IBP se formulen de manera racional, es decir, solo para quienes lo necesitan, y se eviten en quienes la probabilidad de sangrado es mínima o inexistente, como los de bajo riesgo, que en el presente estudio significó la prescripción innecesaria en el 30% de estos pacientes, la cual es superior al 12% de sobreprescripción informada en la literatura (14). Se desconoce en qué proporción de los pacientes el consumo del IBP era sobreprescripción formulada conscientemente por el médico para evitar daño por AINES o era por otra indicación como el reflujo gastroesofágico o la dispepsia. Al igual que en otros estudios, en el presente se demuestra un alto consumo de AINES por iniciativa del paciente, lo cual refleja la facilidad de utilizarlos sin prescripción médica (5); y es probable que esta situación explique que en este trabajo los consumidores de AINES fueran de menor edad que los no consumidores, en contraste con lo encontrado en otras investigaciones (16,18).
Se reconoce que el presente estudio tiene limitaciones como las siguientes:
1. No disponer de una base de datos de prescripciones y dispensarios de medicamentos, para tener más certeza de la verdadera prevalencia del consumo de AINES.
2. La información recolectada fue a partir de los datos suministrados por el paciente al médico durante la consulta y esto puede llevar a sesgos de memoria en la recolección de los datos, no obstante, se disponía de fotografías de los empaques de los AINES prescritos con mayor frecuencia.
3. Aunque el cálculo de la muestra se realizó para el consumo de AINES en la población, probablemente el número de pacientes sería insuficiente para estudiar mejor los factores de riesgo y el consumo de IBP.
A pesar de las limitaciones, se considera que el presente estudio proporciona datos de relevancia tales como el alto consumo de AINES en la población de Medicina Interna (30%), donde casi la mitad se hace sin prescripción médica, también presenta información sobre la incompleta prescripción de profilaxis en pacientes con riesgo alto o moderado de sangrado. De igual manera informa sobre la prescripción innecesaria de IBP a la tercera parte de pacientes de bajo riesgo.
Con base en la información obtenida en este trabajo, se considera que sería clave la difusión de las guías de prevención de sangrado por úlceras pépticas en los usuarios de AINES (8,10,11). Otra gran ventana que queda por explorar es la carga y el impacto que la infección por Helicobacter pylori tiene en este tipo de pacientes. En la literatura se ha demostrado que esta infección es un factor de riesgo para el desarrollo de eventos adversos gastrointestinales en los pacientes consumidores de AINES y existe evidencia que demuestra la utilidad de la búsqueda activa y erradicación del H. pylori en los pacientes que van a recibir AINES/aspirina por primera vez, como ha sido recientemente recomendado por el IV Consenso de Maastricht (23) y el último Consenso de la China sobre el manejo de la infección por H. pylori (24). En Colombia se ha encontrado que esta infección es la principal causa de úlceras duodenales (73%), seguida por el consumo de AINES (41%) y ambos factores de riesgo en la tercera parte de los pacientes (15). La asociación de AINES y H. pylori, aumenta el riesgo de padecer úlcera péptica 64 veces y el riesgo de sangrado por úlceras más 6 veces (25). En el presente estudio, dado su diseño, fue imposible obtener los datos de infección por H. pylori, y se crea la inquietud al respecto, ya que en datos de otras poblaciones colombianas la prevalencia de esta infección oscila entre 77%-82% (26-28), aunque recientemente se encontró que en Bogotá la prevalencia es del 60% (29). En conclusión, la prescripción de IBP en pacientes de alto riesgo es superior a la informada en trabajos internacionales (80% versus menos del 50%) y al igual que en muchos de ellos, en el estudio también hay formulación innecesaria de profilaxis en pacientes sin riesgo de sangrado por úlceras. Se considera necesario un trabajo multicéntrico con mayor número de pacientes para estimar mejor la tasa del consumo de AINES en este tipo de pacientes.
REFERENCIAS
1. Tenenbaum J. The epidemiology of nonsteroidal anti-inflammatory drugs. Can J Gastroenterol J Can Gastroenterol. 1999;13(2):119-22. [ Links ]
2. Shaheen NJ, Hansen RA, Morgan DR, Gangarosa LM, Ringel Y, Thiny MT, et al. The burden of gastrointestinal and liver diseases, 2006. Am J Gastroenterol. 2006;101(9):2128-38. [ Links ]
3. Laine L. Approaches to nonsteroidal anti-inflammatory drug use in the high-risk patient. Gastroenterology. 2001;120(3):594-606. [ Links ]
4. Risser A, Donovan D, Heintzman J, Page T. NSAID prescribing precautions. Am Fam Physician. 2009;80(12):1371-8. [ Links ]
5. Lee I, Cryer B. Epidemiology and role of nonsteroidal antiinflammatory drugs in causing gastrointestinal bleeding. Gastrointest Endosc Clin N Am. 2011;21(4):597-612. [ Links ]
6. Lanas A, Hunt R. Prevention of anti-inflammatory drug-induced gastrointestinal damage: benefits and risks of therapeutic strategies. Ann Med. 2006;38(6):415-28. [ Links ]
7. Malfertheiner P, Chan FKL, McColl KEL. Peptic ulcer disease. Lancet. 2009;374(9699):1449-61. [ Links ]
8. Lanza FL, Chan FKL, Quigley EMM, Practice Parameters Committee of the American College of Gastroenterology. Guidelines for prevention of NSAID-related ulcer complications. Am J Gastroenterol. 2009;104(3):728-38. [ Links ]
9. Rostom A, Dube C, Wells G, Tugwell P, Welch V, Jolicoeur E, et al. Prevention of NSAID-induced gastroduodenal ulcers. Cochrane Database Syst Rev. 2002;(4):CD002296. [ Links ]
10. Abraham NS, Hlatky MA, Antman EM, Bhatt DL, Bjorkman DJ, Clark CB, et al. ACCF/ACG/AHA 2010 expert consensus document on the concomitant use of proton pump inhibitors and thienopyridines: a focused update of the ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use. Am J Gastroenterol. 2010;105(12):2533-49. [ Links ]
11. Lanza FL. A guideline for the treatment and prevention of NSAID-induced ulcers. Members of the Ad Hoc Committee on Practice Parameters of the American College of Gastroenterology. Am J Gastroenterol. 1998;93(11):2037-46. [ Links ]
12. Clinard F, Bardou M, Sgro C, Lefevre N, Raphael F, Paille F, et al. Non-steroidal anti-inflammatory and cytoprotective drug co-prescription in general practice. A general practitioner-based survey in France. Eur J Clin Pharmacol. 2001;57(10):737-43. [ Links ]
13. Abraham NS, El-Serag HB, Johnson ML, Hartman C, Richardson P, Ray WA, et al. National adherence to evidence-based guidelines for the prescription of nonsteroidal anti-inflammatory drugs. Gastroenterology. 2005;129(4):1171-8. [ Links ]
14. Valkhoff VE, van Soest EM, Sturkenboom MCJM, Kuipers EJ. Time-trends in gastroprotection with nonsteroidal anti-inflammatory drugs (NSAIDs). Aliment Pharmacol Ther. junio de 2010;31(11):1218-28. [ Links ]
15. Otero W, Gómez M, Ruiz X. Etiología de las úlceras duodenales en una población colombiana. Rev Col Gastroenterol 2009; 24: 266-271. [ Links ]
16. Ballina J, Carmona L, Laffon A, Grupo de Estudio EPISER. Impacto del consumo de AINES en la población general española. Resultados del estudio EPISER. Rev Esp Reumatol. 2002;29:337-42. [ Links ]
17. Lanas A, Tornero J, Zamorano JL. Assessment of gastrointestinal and cardiovascular risk in patients with osteoarthritis who require NSAIDs: the LOGICA study. Ann Rheum Dis. 2010;69(8):1453-8. [ Links ]
18. Talley NJ, Evans JM, Fleming KC, Harmsen WS, Zinsmeister AR, Melton LJ 3rd. Nonsteroidal antiinflammatory drugs and dyspepsia in the elderly. Dig Dis Sci. 1995;40(6):1345-50. [ Links ]
19. Ho CW, Tse YK, Wu B, Mulder CJJ, Chan FKL. The use of prophylactic gastroprotective therapy in patients with nonsteroidal anti-inflammatory drug- and aspirin-associated ulcer bleeding: a cross-sectional study. Aliment Pharmacol Ther. 2013;37(8):819-24. [ Links ]
20. Smalley W, Stein CM, Arbogast PG, Eisen G, Ray WA, Griffin M. Underutilization of gastroprotective measures in patients receiving nonsteroidal antiinflammatory drugs. Arthritis Rheum. 2002;46(8):2195-200. [ Links ]
21. Abraham NS, El-Serag HB, Johnson ML, Hartman C, Richardson P, Ray WA, et al. National adherence to evidence-based guidelines for the prescription of nonsteroidal anti-inflammatory drugs. Gastroenterology. 2005;129(4):1171-8. [ Links ]
22. Lanas A. Economic analysis of strategies in the prevention of non-steroidal anti-inflammatory drug-induced complications in the gastrointestinal tract. Aliment Pharmacol Ther. de 2004;20(3):321-31. [ Links ]
23. Malfertheiner P, Megraud F, O'Morain CA, Atherton J, Axon ATR, Bazzoli F, et al. Management of Helicobacter pylori infection--the Maastricht IV/ Florence Consensus Report. Gut. 2012;61(5):646-64. [ Links ]
24. Chinese Society of Gastroenterology, Chinese Study Group on Helicobacter pylori, Liu WZ, Xie Y, Cheng H, Lu NH, Hu FL, et al. Fourth Chinese National Consensus Report on the management of Helicobacter pylori infection. J Dig Dis. 2013;14(5):211-21. [ Links ]
25. Huang JQ, Sridhar S, Hunt RH. Role of Helicobacter pylori infection and non-steroidal anti-inflammatory drugs in peptic-ulcer disease: a meta-analysis. Lancet. 2002;359(9300):14-22. [ Links ]
26. Campuzano-Maya G, Hoyos-Castaño D, Calvo-Betancur VD, Suárez-Ramírez OA, Lizcano-Cardona D, Rojas-Arbeláez CA. [Prevalence of Helicobacter pylori infection in physicians in Medellín, Colombia]. Acta Gastroenterol Latinoam. junio de 2007;37(2):99-103. [ Links ]
27. Bravo LE, Cortés A, Carrascal E, Jaramillo R, García LS, Bravo PE, et al. Helicobacter pylori: patología y prevalencia en biopsias gástricas en Colombia. Col Med 2003; 34:124-31. [ Links ]
28. Porras C, Nodora J, Sexton R, Ferreccio C, Jimenez S, Dominguez RL, et al. Epidemiology of Helicobacter pylori infection in six Latin American countries (SWOG Trial S0701). Cancer Causes Control CCC. 2013;24(2):209-15. [ Links ]
29. Trespalacios AA, Rimbara E, Otero W, Mercado M, Caminos JE, Reddy R, Graham D. PCR Alelo-Específica para detección de resistencia de Helicobacter pylori a claritromicina y fluoroquinolonas en biopsias gástricas de Colombia incluyendo la identificación de una nueva mutación en gyrA; manuscrito en preparación. [ Links ]











 text in
text in