Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.29 no.2 Bogotá Apr./June 2014
Endometriosis en el colon y obstrucción intestinal: un caso clínico y revisión de la literatura
Dumar Rodríguez Tello MD. (1), William Otero Regino MD. (2), Martín Gómez Zuleta MD. (3)
(1) Médico de Urgencias, Clínica Fundadores. Bogotá, Colombia.
(2) Profesor de Medicina, Unidad de Gastroenterología, Universidad Nacional de Colombia. Gastroenterólogo, Clínica Fundadores. Bogotá, Colombia.
(3) Profesor de Medicina, Unidad de Gastroenterología Universidad Nacional de Colombia. Gastroenterólogo, Hospital El Tunal, Hospital de Kennedy. Bogotá, Colombia.
Fecha recibido: 27-08-13 Fecha aceptado: 08-15-14
Resumen
La endometriosis (EMT) es una patología que afecta principalmente a mujeres en edad reproductiva, siendo el tracto intestinal es el sitio extragenital más comúnmente afectado. Su presentación clínica es variada y raramente se presenta con obstrucción intestinal, que es difícil diferenciar de la malignidad antes de la cirugía. Cuando hay compromiso colorrectal, las manifestaciones pueden imitar o coexistir con diferentes enfermedades gastrointestinales crónicas que dificultan el diagnóstico. Se presenta un caso clínico de una mujer de 48 años, que ingresó con cuadro de obstrucción intestinal secundaria a endometriosis en colon sigmoide. Se realiza una revisión de la literatura de endometriosis intestinal, haciendo énfasis en el diagnóstico diferencial, y la participación de infecciones bacterianas en la etiología y reactivación de endometriosis.
Palabras claves
Endometriosis, obstrucción intestinal, infección.
INTRODUCCIÓN
La endometriosis (EMT) es definida como una condición inflamatoria crónica, que se caracteriza por la presencia de glándulas endometriales y estroma fuera del útero (1). El origen de su descubrimiento es controvertido; comúnmente se considera que fue John Sampson quién identificó la entidad con su descripción sobre la fisiopatología, sin embargo, esta no fue posible sin los aportes de Thomas Cullen (2). La EMT es una condición dependiente de estrógenos, comúnmente se asocia a dolor pélvico crónico e infertilidad, afecta entre 6% al 10% de las mujeres en edad reproductiva y su prevalencia aumenta hasta en 30% a 50% de mujeres con infertilidad (1). Comúnmente se presenta en el peritoneo, ovarios, septo rectovaginal, ligamentos uterosacros y tejidos extrapélvicos como el tracto gastrointestinal, tracto urinario, sistema pulmonar, sistema nervioso central, piel y músculo estriado (3,4).
El tracto intestinal es el sitio extragenital más comúnmente afectado (3,5). La prevalencia ha variado de 5,3% a 12% (4,6,7). La edad media de presentación es 39 años (5). La localización más frecuente es la rectosigmoide 71%, seguido por apéndice 19%, ilion terminal 6,7%, ciego 5,5% y colon trasverso 0,5% (3,4,6-8).
Cuando hay compromiso intestinal, el síntoma principal es el dolor abdominal, que se empeora durante el período menstrual (3,7-9), seguido por alteración del hábito intestinal, sangrado rectal cíclico, disquecia, tenesmo rectal, distención abdominal, diarrea o estreñimiento recurrente y, en ocasiones, obstrucción intestinal parcial o completa y masa abdominal palpable (6,8).
Se presenta el caso de una paciente quien presentó obstrucción intestinal por endometriosis en colón sigmoide, y se realiza una revisión de la literatura.
CASO CLÍNICO
Mujer de 48 años de edad, quien ingresó al servicio de urgencias de Clínica Fundadores de Bogotá, por cuadro de 10 días de evolución consistente en la disminución del calibre de las heces y, posteriormente, dolor abdominal difuso, vómito y distensión abdominal. Tenía antecedente de dismenorrea, miomatosis uterina, anemia ferropénica, urolitiasis izquierda. Mes y medio antes del cuadro clínico actual estuvo hospitalizada 12 días por pielonefritis por Escherichia coli (E. coli), siendo tratada con meropenem. En el postratamiento tuvo colitis secundaria a Clostridium difficile (C. difficile); recibió tratamiento inicial con metronidazol sin mejoría, por lo cual se cambió por vancomicina oral durante 10 días con la resolución del cuadro clínico.
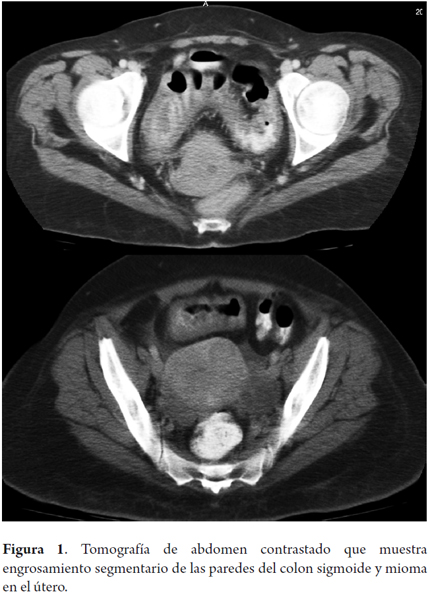
En la hospitalización actual, se le realizó colonoscopia, donde se encontró una estenosis en el sigmoides a 28 cm del recto, la cual no se pudo franquear. Se tomaron biopsias en ese sitio, las cuales no mostraron alteraciones. Para complementar la colonoscopia se le realizó colon por enema con doble contraste, el cual tuvo limitaciones por no poderse visualizar todo el colon. La tomografía de abdomen total simple y con contraste mostró engrosamiento de sigmoides (figura 1).
Con el diagnóstico de estenosis y obstrucción intestinal parcial, se le realizó una laparotomía con resección en bloque del colon sigmoide y una colostomía de Hartmann. En la cirugía se encontró, además, un proceso inflamatorio y fibrosis en la pelvis, por lo cual el área de ginecología le realizó una histerectomía y Salpingo-ooforectomía bilateral. Los resultados de patología fueron: endometriosis en colon sigmoides. La muscular tiene infiltración por estroma y glándulas endometriales, la mucosa tiene edema y congestión vascular. No se identifica proceso tumoral. Los ovarios y la trompa uterina izquierda con endometriosis.
OBSTRUCCIÓN INTESTINAL POR ENDOMETRIOSIS
La obstrucción intestinal secundaria a EMT es una patología infrecuente, que ocurre en menos de 1% de los casos (10). En un estudio con 163 pacientes que tenían EMT intestinal, 10 presentaron obstrucción intestinal parcial (11). En la mayoría de los casos, no se considera como diagnóstico inicial y son los resultados de patología los que finalmente aclaran el diagnóstico. La obstrucción intestinal puede ocurrir en pacientes que tienen EMT intestinal y concomitantemente presentan neoplasias en colon (12). En un estudio de 16 casos de obstrucción intestinal por endometriosis se mostró, microscópicamente, una mayor concentración de glándulas y estroma en la serosa y las capas musculares externas cuando había compromiso del íleon, mientras que la obstrucción en el sigmoides tenía una mayor implicación del músculo circular interno y la submucosa (13).
La EMT intestinal se presenta como lesiones superficiales o profundas. La capa intestinal más frecuentemente afectada es la serosa, seguida de la muscular propia (12,14). Las lesiones superficiales comprometen la serosa, por lo general, son del tamaño de la cabeza de un alfiler y están rodeadas por tejido fibrótico escaso (5). Las lesiones más profundas comprometen la muscular propia o incluso la submucosa y mucosa en pacientes con síntomas gastrointestinales (14,15). Este compromiso produce fibrosis secundaria, provocando un engrosamiento de la pared y disminuyendo el lumen intestinal. En las lesiones de endometriosis que afectan el recto y/o el colon sigmoides, más allá de la capa muscular interna, la circunferencia de estos órganos se compromete en más del 40%, de ahí la recomendación de resección segmentaria del intestino (16). En el caso descrito la endometriosis afectó la capa muscular del sigmoide.
DIAGNÓSTICO DIFERENCIAL
La EMT colorrectal puede imitar o coexistir con diferentes enfermedades gastrointestinales, que puede dificultar el diagnóstico, como es el caso de la enfermedad de Crohn, colitis ulcerativa, colitis isquémica, diverticulitis, síndrome de intestino irritable, e incluso simular tumores de colon y recto cuando hay endometriomas intraluminales, que pueden inducir a tratamiento quirúrgico agresivo, el cual se asocia con alta morbimortalidad (6,17,18). En un estudio de casos y controles de 5540 mujeres con endometriosis, comparadas con controles, tenían más probabilidades de ser diagnosticadas con síndrome de colon irritable (OR 3,5; IC 95%; 3,1-3,9). Del mismo modo, tenían más probabilidades de ser tratados como enfermedad pélvica inflamatoria antes (OR 5,9; IC 95%; 5,1-6,9) y después (OR 3,8; IC 95%; 3,1-4,6) de ser diagnosticadas con endometriosis (19). En un estudio de 7025 mujeres con endometriosis, 65% de las mujeres fueron mal diagnosticadas con otra condición y 46% fueron vistas por cinco o más médicos antes del diagnóstico (20). Cuando hay compromiso del íleon, el diagnóstico diferencial incluye fundamentalmente enfermedad de Crohn, ya que en ambas enfermedades se puede producir inflamación, induración, engrosamiento y estenosis del intestino delgado (21). Un estudio con una cohorte de 37 661 mujeres con endometriosis mostró un 50% de aumento del riesgo de enfermedad inflamatoria intestinal; el riesgo persistió después de 20 años de seguimiento (21).
La EMT es generalmente una enfermedad benigna, pero se estima que 1% de los casos se asocia a cáncer, especialmente cuando ambas condiciones están presentes en el ovario y afecta principalmente a mujeres posmenopáusicas (21). La frecuencia de la endometriosis y el cáncer en colon sigmoide fue calculada 1:156 (5). Hay que sospechar malignidad en los pacientes con dolor abdominal o sangrado rectal y una historia previa de endometriosis quiescente, sobre todo si han recibido tratamiento con estrógenos (12). Los carcinomas de colon primarios siempre involucran la mucosa y son, a menudo, asociados con cambios adenomatosos o un pólipo neoplásico en el epitelio adyacente. Se extienden desde la mucosa, a través de la pared intestinal, hasta la superficie serosa o la grasa adyacente (12). En contraste, la endometriosis y los cánceres que surgen en ella, con frecuencia, involucra las capas más externas de la pared del intestino (a menudo asociados con adherencias), es decir, la serosa, subserosa y muscular propia con sólo la extensión ocasional en la submucosa o mucosa (12). Las características generales útiles que ayudan a distinguir una endometriosis intestinal de una neoplasia, incluyen la ubicación característica dentro de la pared intestinal con una extensa afectación mural y cambios en la mucosa menos prominentes, asociación con una serositis o adherencias posoperatorias y la presencia de pequeños quistes murales o hemorragia (6).
ETIOLOGÍA
La etiología de la EMT es compleja y multifactorial. Diferentes teorías tratan de explican su fisiopatología. La teoría de la menstruación retrógrada propuesta por Sampson, en la década de 1920, afirma que fragmentos del endometrio se diseminaban dentro de la circulación venosa a la cavidad peritoneal durante la menstruación (22). La universalidad de este fenómeno es apoyada por el hallazgo de la sangre menstrual en el líquido peritoneal en 90% de mujeres sanas con trompas de Falopio permeables, que se les realiza laparoscopia durante el tiempo del ciclo premenstrual (23).
La teoría de la metaplasia celómica involucra la trasformación del tejido peritoneal a tejido endometrial ectópico, inducido por un estímulo hormonal o inmunológico endógeno (23). Otra consideración, es que los restos embrionarios de los conductos de Müller embrionarios migran y tienen la capacidad de desarrollar lesiones endometriales bajo la influencia de estrógenos, comenzando en la pubertad (23). Esta teoría está soportada por un estudio que encontró un riesgo relativo de 1,8 (IC 95%; 1,2–2,8) de desarrollar endometriosis en mujeres que estuvieron expuestas a dietilestilbestrol en útero (24). Una posibilidad más reciente sugiere que las células madre o progenitoras extrauterinas, procedentes de la médula ósea, pueden diferenciarse en el tejido endometrial (23). El apoyo a esta teoría se deriva de casos de endometriosis confirmada histológicamente en pacientes sin endometrio menstrual, tales como personas con síndrome de Rokitansky-Kuster-Hauser y hombres con cáncer de próstata, sometidos a tratamiento con estrógenos en dosis altas (23).
La EMT es una enfermedad inflamatoria crónica que involucra mediadores inflamatorios secundarios. Los mediadores inflamatorios primarios, como endotoxinas o lipopolisacáridos (LPS) de bacterias Gramnegativas, pueden ser los desencadenantes de mediadores inflamatorios secundarios como citoquinas, quimiocinas, factores de crecimiento por maduración o activación de macrófagos en la pelvis (25,26). La hipótesis bacteriana propone que la Shigella o bacterias similares pueden ser el detonante de los cambios inmunológicos en el peritoneo pélvico, que inician la etiopatogenia de la endometriosis (25). En algunos pacientes con EMT intestinal se ha encontrado sobrecrecimiento bacteriano y se especula que pueda ser secundario a la alteración neuromuscular que produce la entidad (26). La EMT en monos Rhesus se asocia con alteración de la microflora intestinal, hay baja concentración de lactobacilos y alta concentración de bacterias Gramnegativas (27). Khan y su equipo de investigadores realizaron un estudio donde demostraron, por primera vez, que la sangre menstrual de las mujeres con endometriosis está más contaminada con E. coli en comparación con las mujeres control y, además, con niveles más altos de endotoxina en la sangre menstrual y, por lo tanto, en el líquido peritoneal, debido al reflujo de la sangre menstrual en la pelvis (28). Esto puede promover el crecimiento de receptores Toll-4 (TLR4) mediado por la EMT, como se evidencia por el aumento del crecimiento de las células endometriales en respuesta a LPS y la supresión de estos efectos mediados por anticuerpo anti-TLR4 (28). En contraste, en un estudio experimental de endometriosis en ratones no hubo diferencia significativa en la carga total de bacterias y el número de lactobacilos en el colon frente al grupo control (29). La paciente presentada aquí, presentó pielonefritis por E. Coli y colitis seudomembranosa por C. difficile antes de la obstrucción intestinal por EMT, y existe la posibilidad de que la respuesta inflamatoria por estas entidades infecciosas pudiera ser un reactivador de la EMT, ocasionando aumento en el tamaño de las lesiones y desencadenando la obstrucción intestinal.
DIAGNÓSTICO
En la actualidad, el "gold standard" para el diagnóstico definitivo de EMT es mediante la inspección visual laparoscópica, preferiblemente con confirmación histológica, procedimiento que además permite un tratamiento ablativo y correctivo en el mismo procedimiento quirúrgico (30). La colonoscopia con histología es poco utilizada para diagnosticar endometriosis intestinal, a menos que se encuentren lesiones intraluminales sin compromiso evidente de la mucosa, pero tiene baja sensibilidad (31). Sin embargo, como en todo paciente con sangrado rectal es el examen de elección y más si es cíclico; es el primer examen realizado en pacientes con rectorragia, porque puede excluir malignidad u otras causas de sangrado, pero tiene baja sensibilidad para diagnosticar endometriosis colorrectal (32). El hallazgo más común es el engrosamiento excéntrico de la pared, seguido por lesiones polipoides. El rendimiento diagnóstico histológico de la biopsia endoscópica es alta cuando las lesiones se acompañan de nodularidades superficiales; cuando no están presentes, el diagnostico por biopsia endoscópica es bajo, probablemente porque la afectación de la mucosa del colon es rara (31). La colonoscopia con biopsia realizada a la paciente del caso descrito no evidenció EMT, lo cual se correlaciona con lo descrito en la literatura.
El colon por enema con doble contraste se ha utilizado para el diagnóstico de endometriosis intestinal (32,33). La principal limitación es la dificultad para diferenciar la endometriosis intestinal de otras patologías. Otras limitaciones son el uso de radiación ionizante en las mujeres en edad reproductiva, la imposibilidad de estimar el grado de infiltración de la pared del intestino y la identificación de la extensión a otros órganos pélvicos (33). La ultrasonografía endoscópica rectosigmoidea se utiliza para establecer la profundidad de infiltración de la EMT en la pared intestinal; si se realiza antes de la operación, hace que sea posible distinguir entre los pacientes en los que está indicada la resección intestinal y los que pueden ser tratados con cirugía laparoscópica sin abordar el intestino (32).
La resonancia magnética (RM) preoperatoria, después de la limpieza intestinal, permite una delimitación anatómica clara y precisa de las lesiones en el colon sigmoides y en el recto (33). Para nódulos endometriales, que aparecen en estrecho contacto con la pared intestinal, la profundidad de infiltración no puede determinarse con precisión en la RM (33). La tomografía axial computarizada (TAC) y la RM pueden revelar engrosamiento de la pared intestinal; sin embargo, estas modalidades no pueden proporcionar un diagnóstico del tejido, a menos que se solicita una biopsia dirigida (30). La ecografía transvaginal no tiene ningún valor en el diagnóstico de la endometriosis peritoneal, pero es una herramienta útil tanto para hacer y excluir el diagnóstico de un endometrioma ovárico (30). Un análisis multivariado de cuatro biomarcadores (anexina V, factor de crecimiento endotelial vascular [VEGF], CA-125 y molécula de adhesión celular I [sICAM-1] o glicodelina) en muestras de plasma, obtenidas durante la fase menstrual, realizan el diagnóstico de endometriosis no detectable por ultrasonografía, con una sensibilidad del 81%-90% y una especificidad del 63%-81% (20).
TRATAMIENTO
Las opciones de tratamiento consisten principalmente en una terapia con medicamentos y tratamiento quirúrgico (34,35). La resección segmentaria laparoscópica del recto y el colon sigmoide mejora los síntomas relacionados al dolor y cumple con el objetivo esencial del tratamiento de la endometriosis intestinal, y en consecuencia mejorar la calidad de vida de las pacientes de manera significativa (34,35). El tratamiento hormonal para la supresión de la función ovárica durante 6 meses, reduce el dolor asociado a la endometriosis. Los medicamentos hormonales frecuentemente utilizados son los anticonceptivos orales. Otros medicamentos como danazol, gestrinona, acetato de medroxiprogesterona y agonistas de hormona liberado de gonadotrofinas son igualmente eficaces, pero sus efectos secundarios y los perfiles de costos difieren (30).
Los pacientes con síntomas obstructivos por EMT intestinal deberían someterse a resección quirúrgica (4). En mujeres que desean preservar su vida reproductiva, la cirugía conservadora ha mostrado beneficios; de 54 mujeres a quienes les realizaron cirugía conservadora, 23 quedaron en embarazo (11). Al comparar la resección colónica laparoscópica frente a la laparotomía en pacientes con EMT intestinal, ambos enfoques conducen a mejorías sintomáticas similares después de la operación, aunque las que recibieron tratamiento por laparoscopia tuvieron tasas significativamente más bajas de complicaciones quirúrgicas, así como las tasas más altas de embarazos espontáneos (7,36).
CONCLUSIONES
La EMT intestinal es una patología que debe sospecharse clínicamente en mujeres en edad reproductiva como causa de síntomas de dolor abdominal difuso, rectorragia y obstrucción intestinal. Además la EMT intestinal puede imitar o coexistir con diferentes patologías del tracto gastrointestinal como neoplasias, enfermedad inflamatoria intestinal, síndrome de intestino irritable. Se deben realizar investigaciones adicionales para determinar el papel que pudieran tener las infecciones bacterianas en la fisiopatología de la EMT, ya que existe la posibilidad teórica de que puedan estar relacionadas con la etiología o reactivación del proceso inflamatorio que lleva a la EMT.
REFERENCIAS
1. Rogers PAW, D'Hooghe TM, Fazleabas A, Giudice LC, Montgomery GW, Petraglia F, et al. Defining future directions for endometriosis research: workshop report from the 2011 World Congress of Endometriosis In Montpellier, France. Reprod Sci Thousand Oaks Calif. 2013;20(5):483-99. [ Links ]
2. Benagiano G, Brosens I. Who identified endometriosis? Fertil Steril. 2011;95(1):13-6. [ Links ]
3. Veeraswamy A, Lewis M, Mann A, Kotikela S, Hajhosseini B, Nezhat C. Extragenital endometriosis. Clin Obstet Gynecol. 2010;53(2):449-66. [ Links ]
4. Prystowsky JB, Stryker SJ, Ujiki GT, Poticha SM. Gastrointestinal endometriosis. Incidence and indications for resection. Arch Surg Chic Ill 1960. 1988;123(7):855-8. [ Links ]
5. Bergqvist A. Different types of extragenital endometriosis: a review. Gynecol Endocrinol Off J Int Soc Gynecol Endocrinol. 1993;7(3):207-21. [ Links ]
6. Yantiss RK, Clement PB, Young RH. Endometriosis of the intestinal tract: a study of 44 cases of a disease that may cause diverse challenges in clinical and pathologic evaluation. Am J Surg Pathol. 2001;25(4):445-54. [ Links ]
7. Wills HJ, Reid GD, Cooper MJW, Tsaltas J, Morgan M, Woods RJ. Bowel resection for severe endometriosis: an Australian series of 177 cases. Aust N Z J Obstet Gynaecol. 2009;49(4):415-8. [ Links ]
8. Cameron IC, Rogers S, Collins MC, Reed MW. Intestinal endometriosis: presentation, investigation, and surgical management. Int J Colorectal Dis. 1995;10(2):83-6. [ Links ]
9. Kaufman LC, Smyrk TC, Levy MJ, Enders FT, Oxentenko AS. Symptomatic intestinal endometriosis requiring surgical resection: clinical presentation and preoperative diagnosis. Am J Gastroenterol. 2011;106(7):1325-32. [ Links ]
10. De Jong MJH, Mijatovic V, van Waesberghe JHTM, Cuesta MA, Hompes PGA. Surgical outcome and long-term follow-up after segmental colorectal resection in women with a complete obstruction of the rectosigmoid due to endometriosis. Dig Surg. 2009;26(1):50-5. [ Links ]
11. Weed JC, Ray JE. Endometriosis of the bowel. Obstet Gynecol.;69(5):727-30. [ Links ]
12. Yantiss RK, Clement PB, Young RH. Neoplastic and pre-neoplastic changes in gastrointestinal endometriosis: a study of 17 cases. Am J Surg Pathol. 2000;24(4):513-24. [ Links ]
13. Macafee CH, Greer HL. Intestinal endometriosis. A report of 29 cases and a survey of the literature. J Obstet Gynaecol Br Emp. 1960;67:539-55. [ Links ]
14. Kavallaris A, Köhler C, Kühne-Heid R, Schneider A. Histopathological extent of rectal invasion by rectovaginal endometriosis. Hum Reprod Oxf Engl. 2003;18(6):1323-7. [ Links ]
15. naf V, El Nakadi I, Simon P, Van de Stadt J, Fayt I, Simonart T, et al. Preferential infiltration of large bowel endometriosis along the nerves of the colon. Hum Reprod Oxf Engl. 2004;19(4):996-1002. [ Links ]
16. Abrão MS, Podgaec S, Dias JA Jr, Averbach M, Silva LFF, Marino de Carvalho F. Endometriosis lesions that compromise the rectum deeper than the inner muscularis layer have more than 40% of the circumference of the rectum affected by the disease. J Minim Invasive Gynecol. 2008;15(3):280-5. [ Links ]
17. Ong SY, Sim SY, Johnston M, Crowley P, Froomes P. Education and imaging. Gastrointestinal: refractory ulcerative colitis complicated by colonic stricturing endometriosis. J Gastroenterol Hepatol. 2012;27(1):181. [ Links ]
18. Samet JD, Horton KM, Fishman EK, Hruban RH. Colonic endometriosis mimicking colon cancer on a virtual colonoscopy study: a potential pitfall in diagnosis. Case Rep Med. 2009;2009:379578. [ Links ]
19. Seaman HE, Ballard KD, Wright JT, de Vries CS. Endometriosis and its coexistence with irritable bowel syndrome and pelvic inflammatory disease: findings from a national case-control study--Part 2. BJOG Int J Obstet Gynaecol. 2008;115(11):1392-6. [ Links ]
20. Vodolazkaia A, El-Aalamat Y, Popovic D, Mihalyi A, Bossuyt X, Kyama CM, et al. Evaluation of a panel of 28 biomarkers for the non-invasive diagnosis of endometriosis. Hum Reprod Oxf Engl. 2012;27(9):2698-711. [ Links ]
21. Jess T, Frisch M, Jørgensen KT, Pedersen BV, Nielsen NM. Increased risk of inflammatory bowel disease in women with endometriosis: a nationwide Danish cohort study. Gut. 2012;61(9):1279-83. [ Links ]
22. Sampson JA. Metastatic or Embolic Endometriosis, due to the Menstrual Dissemination of Endometrial Tissue into the Venous Circulation. Am J Pathol. 1927;3(2):93-110.43. [ Links ]
23. Burney RO, Giudice LC. Pathogenesis and pathophysiology of endometriosis. Fertil Steril. 2012;98(3):511-9. [ Links ]
24. Missmer SA, Hankinson SE, Spiegelman D, Barbieri RL, Michels KB, Hunter DJ. In utero exposures and the incidence of endometriosis. Fertil Steril. 2004;82(6):1501-8. [ Links ]
25. Kodati VL, Govindan S, Movva S, Ponnala S, Hasan Q. Role of Shigella infection in endometriosis: a novel hypothesis. Med Hypotheses. 2008;70(2):239-43. [ Links ]
26. Mathias JR, Franklin R, Quast DC, Fraga N, Loftin CA, Yates L, et al. Relation of endometriosis and neuromuscular disease of the gastrointestinal tract: new insights. Fertil Steril. 1998;70(1):81-8. [ Links ]
27. Bailey MT, Coe CL. Endometriosis is associated with an altered profile of intestinal microflora in female rhesus monkeys. Hum Reprod Oxf Engl. 2002;17(7):1704-8. [ Links ]
28. Khan KN, Kitajima M, Hiraki K, Yamaguchi N, Katamine S, Matsuyama T, et al. Escherichia coli contamination of menstrual blood and effect of bacterial endotoxin on endometriosis. Fertil Steril. 2010;94(7):2860-2863.e1-3. [ Links ]
29. Appleyard CB, Cruz ML, Rivera E, Hernández GA, Flores I. Experimental endometriosis in the rat is correlated with colonic motor function alterations but not with bacterial load. Reprod Sci Thousand Oaks Calif. 2007;14(8):815-24. [ Links ]
30. Kennedy S, Bergqvist A, Chapron C, D'Hooghe T, Dunselman G, Greb R, et al. ESHRE guideline for the diagnosis and treatment of endometriosis. Hum Reprod Oxf Engl. 2005;20(10):2698-704. [ Links ]
31. Kim K-J, Jung S-S, Yang S-K, Yoon SM, Yang D-H, Ye BD, et al. Colonoscopic findings and histologic diagnostic yield of colorectal endometriosis. J Clin Gastroenterol. 2011;45(6):536-41. [ Links ]
32. Roseau G, Dumontier I, Palazzo L, Chapron C, Dousset B, Chaussade S, et al. Rectosigmoid endometriosis: endoscopic ultrasound features and clinical implications. Endoscopy. 2000;32(7):525-30. [ Links ]
33. Loubeyre P, Copercini M, Frossard JL, Wenger JM, Petignat P. Pictorial review: rectosigmoid endometriosis on MRI with gel opacification after rectosigmoid colon cleansing. Clin Imaging. 2012;36(4):295-300. [ Links ]
34. Keckstein J, Wiesinger H. Deep endometriosis, including intestinal involvement--the interdisciplinary approach. Minim Invasive Ther Allied Technol MITAT Off J Soc Minim Invasive Ther. 2005;14(3):160-6. [ Links ]
35. Bassi MA, Podgaec S, Dias JA Jr, D'Amico Filho N, Petta CA, Abrao MS. Quality of life after segmental resection of the rectosigmoid by laparoscopy in patients with deep infiltrating endometriosis with bowel involvement. J Minim Invasive Gynecol. 2011;18(6):730-3. [ Links ]
36. Ruffo G, Scopelliti F, Scioscia M, Ceccaroni M, Mainardi P, Minelli L. Laparoscopic colorectal resection for deep infiltrating endometriosis: analysis of 436 cases. Surg Endosc. 2010;24(1):63-7. [ Links ]











 text in
text in