Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.30 no.1 Bogotá Jan./Mar. 2015
Hiponatremia dilucional y trasplante hepático. Revisión
Edilberto E. Núñez C. MD. (1), Juan C. Restrepo G. MD. (2), Rodrigo Castaño Llano MD. (3)
(1) Médico Internista. Universidad Pontificia Bolivariana. Fellow de Gastroenterología, Pontificia Universidad Javeriana. Bogotá, Colombia.
(2) Grupo de Gastrohepatología, Universidad de Antioquia. Unidad de Hepatología y Trasplante Hepático, Universidad de Antioquia y Hospital Pablo Tobón Uribe. Medellín, Colombia.
(3) Grupo de Gastrohepatología, Universidad de Antioquia. Jefe de Posgrado Cirugía General, Universidad Pontificia Bolivariana. Instituto de Cancerología Clínica Las Américas. Medellín, Colombia.
Fecha recibido: 26-03-14 Fecha aceptado: 02-02-15
Resumen
Los pacientes con hepatopatías avanzadas pueden presentar estados de hipervolemia que los puede llevar a desarrollar hiponatremia dilucional, la cual se origina principalmente a niveles persistentemente aumentados de hormona antidiurética. El trasplante hepático es la terapia de elección en pacientes con hepatopatías terminales con excelentes sobrevidas en el tiempo. La hiponatremia dilucional ha demostrado ser un factor pronóstico en pacientes con cirrosis e incluso de mortalidad en pacientes en lista de espera para trasplante de hígado. Por tal razón, actualmente hace parte de los puntajes de clasificación de lista de espera de trasplante hepático en pacientes con hepatopatías avanzadas. El papel de la hiponatremia pretrasplante en el pronóstico de pacientes que serán llevados a trasplante hepático es tema de renovado interés, con datos en la literatura bastante contradictorios. Hasta hace poco, solo la restricción hídrica era el tratamiento contra la hiponatremia dilucional; sin embargo, actualmente se dispone de tratamientos dirigidos contra la hiponatremia dilucional en pacientes con cirrosis con resultados algo alentadores, aunque poco se sabe sobre su efecto en pacientes con cirrosis que serán llevados a trasplante hepático.
Palabras clave
Hiponatremia, cirrosis, trasplante hepático, pronóstico.
INTRODUCCIÓN
La hiponatremia en la cirrosis definida arbitrariamente como una concentración plasmática de sodio sérico menor de 130 mEq/L es una complicación bastante frecuente (1). La hiponatremia hipovolémica que está asociada con importantes pérdidas de fluidos extracelulares y la hiponatremia hipervolémica, también conocida como hiponatremia dilucional, en la cual existe una retención desproporcionada de agua en comparación con el sodio y para que esta última se presente los pacientes deben cursar con ascitis y no mostrar signos clínicos de deshidratación (2). Se ha reportado que en pacientes con cirrosis, la hiponatremia dilucional puede presentarse hasta en un 21,6% de los casos al momento del diagnóstico (3). En pacientes con cirrosis, el riesgo de desarrollar hiponatremia dilucional es del 14% al año y del 37% a los 5 años (4).
ORIGEN DE LA HIPONATREMIA DILUCIONAL
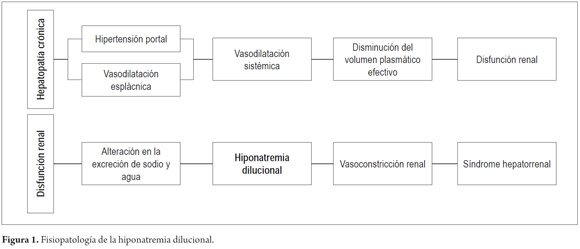
El desarrollo de hiponatremia en el paciente cirrótico es secundario a una disfunción circulatoria y renal severa (1, 2). Al inicio, los pacientes con hepatopatía avanzada pierden la capacidad renal para excretar sodio, seguida subsecuentemente por una limitación para eliminar agua libre de solutos (1, 5, 6); lo anterior lleva a un estado de hipervolemia que causa hiponatremia dilucional e hipoosmolaridad, que clínicamente se manifiesta como la presencia de ascitis y edemas periféricos en los pacientes (5). En estadios más avanzados se producirá vasoconstricción renal que puede llegar a convertirse en un síndrome hepatorrenal (SHR) (figura 1) (2).
Aunque la patogenia de la retención de agua en la cirrosis es compleja, se cree que la acción de la hormona antidiurética, también conocida como arginina-vasopresina (AVP), cumple un papel fundamental en su génesis (7). En pacientes con cirrosis se han documentado niveles séricos aumentados de AVP por medio de una secreción no osmótica de esta, la cual es secundaria a la vasodilatación esplácnica y que tiene la finalidad de mantener la perfusión sistémica (5, 8). La AVP cumple su papel patogénico a través de dos formas: primero, estimula a las células ubicadas en el túbulo contorneado distal y en el túbulo colector por medio de los receptores V2 para que reabsorban agua libre; segundo, a través de los receptores V1 ubicados en la musculatura lisa de los vasos sanguíneos, estimula la vasoconstricción afectando la perfusión renal (1). La perpetuación del estímulo de la AVP favorecerá la hipervolemia y, por ende, la hiponatremia dilucional (8).
Concomitante con la AVP también se ha demostrado la liberación de otras sustancias vasoactivas, como la noradrenalina y el sistema renina-angiotensina-aldosterona (8). Adicionalmente el uso de diuréticos en estos pacientes puede contribuir de manera importante en el desarrollo de hiponatremia dilucional en los pacientes con cirrosis e insuficiencia hepática avanzada (9).
MANIFESTACIONES CLÍNICAS DE LA HIPONATREMIA DILUCIONAL EN CIRROSIS
Los datos sobre las manifestaciones clínicas de los pacientes con hiponatremia dilucional en cirrosis son limitados (2). Los síntomas de la hiponatremia son predominantemente neurológicos, reportándose en un amplio espectro que va desde hallazgos inespecíficos como anorexia, letargia, náuseas y dificultades para la concentración, hasta manifestaciones severas como déficits neurológicos focales, convulsión o coma, aunque estos últimos bastante infrecuentes (10). Usualmente es difícil diferenciar si los síntomas de los pacientes son secundarios a su hiponatremia o si realmente se trata de un cuadro de encefalopatía hepática (2). Se sabe que los pacientes con hiponatremia, por lo general en estados avanzados de su enfermedad hepática, podrán tener una mayor predisposición a sufrir de encefalopatía hepática (11).
Hiponatremia dilucional en el pretrasplante hepático
Desde hace ya varias décadas, el trasplante hepático se ha convertido en el tratamiento ideal de pacientes con enfermedad hepática avanzada, insuficiencia hepática aguda con indicadores de mal pronóstico, algunas enfermedades metabólicas con afectación del hígado y algunos tumores primarios del hígado (12). En nuestro medio, la causa más frecuente de trasplante hepático es la hepatopatía alcohólica (12). En 2002 se implementó en los Estados Unidos el puntaje MELD (del inglés Model End Liver Disease) para designar el proceso de distribución de los órganos de pacientes fallecidos, aunque este puntaje inicialmente habido sido diseñado para predecir la sobrevida de los pacientes llevados a derivación portosistémica transyugular intrahepática (TIPS) y está basado en un cálculo logarítmico que toma en cuenta la bilirrubina, la creatinina y el INR (13).
Recientemente se ha reanalizado el papel pronóstico de la hiponatremia en el contexto de los pacientes candidatos a trasplante hepático (1, 2). El estudio de Kim y colaboradores intentó predecir la mortalidad en los primeros 90 días de los pacientes que habían sido registrados en una lista de espera para trasplante hepático (14). Para ello, se tomó la lista de espera de todos los pacientes candidatos a trasplante de hígado registrados en Estados Unidos entre los años 2005 y 2006. El hazard ratio (HR) para morir en lista de espera para el 2005 fue de 1,05 con intervalo de confianza del 95% (IC 95%) de 1,03 a 1,08 por cada disminución en 1 mmol/L en los valores de sodio entre 125 y 140 mmol/L. Para el 2006, la medición combinada del MELD y el sodio (MELD-Na) (véase más adelante) demostró ser mejor predictor de desenlaces adversos que el MELD convencional (14). La serie de Moini y colaboradores también reportó que los pacientes con hiponatremia en el momento en que estaban en lista de espera para trasplante de hígado tenían un mayor riesgo de morir que los pacientes eunatrémicos también enlistados (15). Los niveles de sodio menores de 130 mEq/L incrementaban la mortalidad a 90 y 180 días con un odds ratio (OR) de 4,519 (IC 95%, 1,956-10,439) y un OR de 2,667 (IC 95%, 1,554-4,579) respectivamente. Ajustados por el MELD, una disminución de 1 mEq/L significa un aumento del riesgo de muerte de un 6% y 7% a los días 90 y 180, respectivamente (15).
En población pediátrica también se demostró que los bajos niveles de sodio y la presencia de ascitis, junto con altos niveles de bilirrubinas y categorización de la edad (0 a 1 año versus mayores de 1 año) son predictores independientes de mortalidad a 90 días de pacientes en lista de espera (16).
El papel del MELD-Na en el pretrasplante hepático
Al demostrarse que en los pacientes con cirrosis la hiponatremia predice de forma independiente los desenlaces adversos en pacientes en lista de espera para trasplante hepático (17), era lógico pensar que adicionar el sodio sérico a la ecuación MELD, conocida como MELD-Na, podría mejorar el poder predictivo de sobrevida en estos pacientes (18). Incluso se ha planteado la posibilidad de usar la ecuación MELD-Na para adjudicar los mejores candidatos a trasplante (18, 19). Sin embargo, aún existe polémica con respecto al uso generalizado de la ecuación del MELD-Na, ya que el sodio sérico en realidad puede ser una variable fácilmente modificable y es posible que no solo sea manifestación del grado avanzado de la enfermedad hepática (1, 2).
Hiponatremia dilucional pretrasplante como indicador pronóstico del postrasplante hepático
En el postrasplante hepático, la hiponatremia pretrasplante también se ha relacionado con desenlaces adversos (2). No obstante, la literatura aún es controversial.
Estudios que apoyan la hiponatremia dilucional como factor pronóstico
Londoño y colaboradores publicaron una serie de 241 pacientes consecutivos que fueron llevados a trasplante hepático. Retrospectivamente demostraron que los pacientes con niveles de sodio sérico menores de 130 mEq/L (8% del total de pacientes) pretrasplante tenían una menor sobrevida a 3 meses postrasplante en comparación con los pacientes sin hiponatremia (84% versus 95%, respectivamente, p <0,05) (20).
Karapanagiotou y colaboradores publicaron un estudio en el que evaluaron el desenlace en pacientes sometidos a trasplantes ortotópico de hígado (21). En este estudio, la tasa de complicaciones neurológicas, lesión renal aguda y mortalidad en la unidad de cuidados intensivos (UCI) fue menor en pacientes con hiponatremia comparados con eunatremia, con diferencias estadísticamente significativas. La sobrevida a 30 días y al año también fue menor para el grupo de pacientes con hiponatremia (62,5% versus 88,5% y 60,9% versus 88,5%, respectivamente). La regresión logística multivariada demostró que tanto la lesión renal aguda como la hiponatremia pretrasplante fueron factores predictores independientes de sobrevida a los 30 días y al primer año del trasplante de hígado (21).
Boin y colaboradores también demostraron en su cohorte que los pacientes que tenían niveles de sodio menores de 130 mEq/L presentaban un peor pronóstico, con una sobrevida en meses mucho menor para dicho grupo comparado con el control (una media de 37,2+51,2 meses contra un 51,2+54,1 meses respectivamente, p <0,05) (22).
Li y colaboradores revisaron de manera retrospectiva la información de 207 pacientes trasplantados de hígado de donantes vivos. Los autores demostraron que la hiponatremia pretrasplante, definida como unos valores séricos menores de 130 mEq/L, era un factor independiente de infecciones bacterianas en el posoperatorio del trasplante (23).
En un estudio japonés en el que se revisaron retrospectivamente a 134 pacientes, aquellos con niveles de sodio pretrasplante menores de 130 mEq/L mostraron una sobrevida a 3 meses y a 1 año mucho menor que los pacientes con niveles de sodio por encima de ese valor (97% versus 74% y 96% versus 58%, respectivamente p <0,001). En su análisis multivariado, los niveles de sodio predijeron la sobrevida del injerto en el postrasplante (p = 0,005) (24).
Finalmente, el estudio de Abdalla y colaboradores documentó que los pacientes con niveles de sodio sérico por debajo de 135 mEq/L estaban relacionados más frecuentemente con pérdida del injerto a 3 meses del postrasplante comparados con los pacientes sin hiponatremia (p = 0,01) (25).
Estudios que no apoyan la hiponatremia dilucional como factor pronóstico
Leise y colaboradores publicaron su experiencia en el manejo de pacientes trasplantados de hígado con hiponatremia pretrasplante (26). En su estudio, que incluía a 19 357 pacientes, se demostró que la probabilidad de sobrevida fue similar entre los grupos de pacientes con hipo y normonatremia (94,7% y 94,0%, respectivamente).
Un estudio coreano trató de demostrar el impacto pronóstico de la hiponatremia pretrasplante y su corrección en el desenlace de pacientes llevados a trasplante hepático (27). En este estudio se incluyó una nueva variable, conocida como el delta de sodio, que medía las concentraciones séricas de sodio en las primeras 48 horas del trasplante hepático. En su estudio, que incluyó a 512 pacientes con trasplante ortotópico de hígado, se demostró que los casos con hiponatremia pretrasplante severa, definida como unos niveles de sodio sérico menores de 125 mmol/L, estaban relacionados con tasas más altas de mortalidad intrahospitalaria (9,6%), delirio (54,8%), complicaciones neurológicas (24,7%) y lesión renal aguda, todas con significancia estadística. Sin embargo, en la regresión logística multivariada, ni las concentraciones de sodio ni el delta de sodio estuvieron relacionados con mortalidad intrahospitalaria.
Tratamiento de la hiponatremia dilucional en los pacientes candidatos a trasplante hepático
Poco se sabe sobre la ventaja del tratamiento de los pacientes con hiponatremia antes del trasplante hepático para mejorar su pronóstico y convertirse así en una modalidad terapéutica (1, 2). Según el estudio de Fukuhara y colaboradores (24), en los pacientes con hiponatremia, en quienes se corrigieron los niveles de sodio a velocidades que evitaran el desarrollo de un síndrome de desmielinización osmótica, el pronóstico fue similar al de los pacientes en los que no se logró la corrección de dichos niveles (24).
Actualmente el tratamiento de la hiponatremia dilucional en cirrosis es manejado con restricción de líquidos y terapia diurética en aquellos pacientes con sobrecarga de volumen (28). El régimen terapéutico más exitoso es la combinación de espironolactona en 100 mg/día y furosemida en 40 mg/día, con dosis que son tituladas de manera paulatina y mantenimiento de la misma relación de dosis con miras a conservar unos niveles de potasio normales. No obstante, en algunos casos, el uso de estos diuréticos somete al paciente a graves complicaciones como son lesión renal y alteraciones hidroelectrolíticas, lo que limita su utilidad (29).
Vaptanes
Recientemente salió al mercado un nuevo grupo de medicamentos que antagonizan el efecto de la AVP. Estos medicamentos, conocidos como vaptanes (conivaptan, lixivaptan, satavaptan y tolvaptan), han demostrado que pueden corregir los niveles de sodio en pacientes con hiponatremia euvolémica o hipervolémica (28). Su utilidad se restringe a los pacientes con estados de secreción persistente de hormona antidiurética a pesar de una osmolalidad plasmática baja (28).
Algunos estudios han demostrado que el conivaptan y el lixivaptan pueden ser útiles en los pacientes con cirrosis e hiponatremia dilucional (30-32). También pequeños ensayos clínicos comprobaron que el lixivaptan y el satavaptan son más efectivos que el placebo para corregir los niveles de sodio, aunque sugieren que su efecto sobre la hiponatremia puede ser menor en pacientes con cirrosis comparados con pacientes con hiponatremia por otras causas (30, 33). Incluso un análisis de subgrupos del estudio SALT (Study of Ascending Levels of Tolvaptan), en el que se incluyó un grupo de pacientes con cirrosis, también soporta esta observación (34). Algunos autores proponen que la respuesta limitada en estos pacientes sea el efecto de una reabsorción proximal de solutos que lleva a la disminución de la cantidad de filtrado glomerular en la nefrona distal (35), aunque esta posibilidad no ha sido estudiada; otros, por su parte, proponen que la regulación de la acuaporina 2 en pacientes con cirrosis está regulada por una vía independiente de los receptores V2 de la AVP (36). Con respecto al satavaptan, aunque los estudios iniciales demostraron que podría ser útil, los estudios fase 3 no tuvieron los resultados esperados. Un estudio fase 3 del satavapatan demostró que la mortalidad aumenta en pacientes con cirrosis en quienes se administraba el medicamento (37), razón por la cual sus investigaciones fueron suspendidas en el 2008 (28).
El tolvaptan tiene la ventaja de no requerir ajuste según la edad, el género, la raza, la función cardiovascular, las alteraciones hepáticas o renales (tasa de filtración glomerular >10 mL/min). Sin embargo, está contraindicado en los siguientes casos: hiponatremia hipovolémica; alteración en el centro de la sed o pacientes que no puedan acceder a líquidos orales en caso de requerirlos; hiponatremia aguda sintomática; anuria; y pacientes que estén en tratamiento con inhibidores potentes de la isoenzima CYP3A4 (28). Por otro lado, a pesar de que el tolvaptan es de uso oral, al iniciarlo deben controlarse concomitantemente los niveles séricos de sodio y el cambio de este en el tiempo, para lo que sería ideal que el paciente estuviera hospitalizado. También debe recordarse que solo existe evidencia para utilizar el tolvaptan hasta máximo de 30 días, ya que no hay estudios que avalen su uso de forma prolongada (38).
La administración de tolvaptan en pacientes con hepatopatía crónica ha generado algunas inquietudes en relación con la seguridad debido a que en un ensayo clínico aumentó la tasa de episodios de sangrado digestivo (34, 39). Sin embargo, muy recientemente Sakaida y colaboradores demostraron la utilidad del tolvaptan en el manejo de los edemas en pacientes con cirrosis (40). Este estudio comprobó que el tolvaptan, en dosis de 7,5 mg/día durante 7 días, puede mejorar los niveles de sodio sérico a razón de 1 mmol/L, sin desviaciones de los rangos normales, por lo que podría ser útil para el manejo de la hiponatremia de los pacientes con hepatopatía crónica (40). Sin embargo, en el estudio se reportaron 2 episodios de complicaciones graves, 1 cuadro de sangrado digestivo de origen variceal al día 14 de tratamiento y 1 paciente que desarrolló encefalopatía hepática a los 3 días de iniciada la terapia (40).
Se requieren más estudios que soporten el uso de los vaptanes en pacientes con cirrosis e insuficiencia hepática avanzada y adicionalmente en el perioperatorio de pacientes que serán llevados a trasplante hepático, para demostrar su utilidad y verdadero impacto sobre la mejoría en el desenlace de pacientes hiponatrémicos con cirrosis avanzada. Los vaptanes no están disponibles en nuestro medio.
CONCLUSIONES
La hiponatremia dilucional en los pacientes con hepatopatía crónica es un indicador de severidad y un marcador de pronóstico adverso, debido a que es una consecuencia fisiopatológica de un estadio avanzado de disfunción hemodinámica y renal producido por la cirrosis. Utilizar este marcador pronóstico para designar la lista de pacientes candidatos a trasplante hepático ha sido de utilidad; sin embargo, poco se sabe sobre si la hiponatremia pretrasplante puede ser un indicador adverso en pacientes que son trasplantados de hígado. En nuestro grupo, en estos momentos se está llevando a cabo un estudio con la finalidad de aclarar dicha pregunta en una serie local.
Hasta ahora, la única manera de revertir el proceso que lleva a la hiponatremia es el trasplante como tal, aunque se han implementado algunas medidas no farmacológicas y farmacológicas como los vaptanes, medicamentos prometedores, pese a que faltan muchos estudios que avalen su uso. Para los autores, su administración aún no debe recomendarse.
REFERENCIAS
1. Guevara M, Gines P. Hyponatremia in liver cirrhosis: pathogenesis and treatment. Endocrinol Nutr 2010;57(Suppl 2):15-21. [ Links ]
2. Cardenas A, Gines P. Dilutional hyponatremia, hepatorenal syndrome and liver transplantation. Gastroenterol Hepatol 2008;31:29-36. [ Links ]
3. Angeli P, Wong F, Watson H, Gines P. Hyponatremia in cirrhosis: results of a patient population survey. Hepatology 2006;44:1535-42. [ Links ]
4. Planas R, Montoliu S, Balleste B, et al. Natural history of patients hospitalized for management of cirrhotic ascites. Clin Gastroenterol Hepatol 2006;4:1385-94. [ Links ]
5. Schrier RW, Arroyo V, Bernardi M, Epstein M, Henriksen JH, Rodes J. Peripheral arterial vasodilation hypothesis: a proposal for the initiation of renal sodium and water retention in cirrhosis. Hepatology 1988;8:1151-7. [ Links ]
6. Epstein M. Deranged sodium homeostasis in cirrhosis. Gastroenterology 1979;76:622-35. [ Links ]
7. Arroyo V, Claria J, Salo J, Jimenez W. Antidiuretic hormone and the pathogenesis of water retention in cirrhosis with ascites. Semin Liver Dis 1994;14:44-58. [ Links ]
8. Schrier RW. Water and sodium retention in edematous disorders: role of vasopressin and aldosterone. Am J Med 2006;119:S47-53. [ Links ]
9. Bichet DG, Van Putten VJ, Schrier RW. Potential role of increased sympathetic activity in impaired sodium and water excretion in cirrhosis. N Engl J Med 1982;307:1552-7. [ Links ]
10. Gines P, Berl T, Bernardi M, et al. Hyponatremia in cirrhosis: from pathogenesis to treatment. Hepatology 1998;28:851-64. [ Links ]
11. Haussinger D, Kircheis G, Fischer R, Schliess F, vom Dahl S. Hepatic encephalopathy in chronic liver disease: a clinical manifestation of astrocyte swelling and low-grade cerebral edema? J Hepatol 2000;32:1035-8. [ Links ]
12. Santos O, Marín J, Muñoz O, et al. Trasplante hepático en adultos: Estado del arte. Rev Col Gastroenterol 2012;27: 21-31. [ Links ]
13. Malinchoc M, Kamath PS, Gordon FD, Peine CJ, Rank J, ter Borg PC. A model to predict poor survival in patients undergoing transjugular intrahepatic portosystemic shunts. Hepatology 2000;31:864-71. [ Links ]
14. Kim WR, Biggins SW, Kremers WK, et al. Hyponatremia and mortality among patients on the liver-transplant waiting list. N Engl J Med 2008;359:1018-26. [ Links ]
15. Moini M, Hoseini-Asl MK, Taghavi SA, et al. Hyponatremia a valuable predictor of early mortality in patients with cirrhosis listed for liver transplantation. Clin Transplant 2011;25:638-45. [ Links ]
16. Pugliese R, Fonseca EA, Porta G, et al. Ascites and serum sodium are markers of increased waiting list mortality in children with chronic liver failure. Hepatology 2013. [ Links ]
17. Londoño MC, Cárdenas A, Guevara M, et al. MELD score and serum sodium in the prediction of survival of patients with cirrhosis awaiting liver transplantation. Gut 2007;56:1283-90. [ Links ]
18. Ruf AE, Kremers WK, Chavez LL, Descalzi VI, Podesta LG, Villamil FG. Addition of serum sodium into the MELD score predicts waiting list mortality better than MELD alone. Liver Transpl 2005;11:336-43. [ Links ]
19. Biggins SW, Rodriguez HJ, Bacchetti P, Bass NM, Roberts JP, Terrault NA. Serum sodium predicts mortality in patients listed for liver transplantation. Hepatology 2005;41:32-9. [ Links ]
20. Londoño MC, Guevara M, Rimola A, et al. Hyponatremia impairs early posttransplantation outcome in patients with cirrhosis undergoing liver transplantation. Gastroenterology 2006;130:1135-43. [ Links ]
21. Karapanagiotou A, Kydona C, Papadopoulos S, et al. The effect of hyponatremia on the outcome of patients after orthotopic liver transplantation. Transplant Proc 2012;44:2724-6. [ Links ]
22. Boin IF, Capel C, Jr., Ataide EC, Cardoso AR, Caruy CA, Stucchi RS. Pretransplant hyponatremia could be associated with a poor prognosis after liver transplantation. Transplant Proc 2010;42:4119-22. [ Links ]
23. Li C, Wen TF, Mi K, Wang C, Yan LN, Li B. Analysis of infections in the first 3-month after living donor liver transplantation. World J Gastroenterol 2012;18:1975-80. [ Links ]
24. Fukuhara T, Ikegami T, Morita K, et al. Impact of preoperative serum sodium concentration in living donor liver transplantation. J Gastroenterol Hepatol. 2010;25: 978-984. [ Links ]
25. Abdalla S, Alves RCP, Fonseca EA, Vicenzi R, Gonçalves JE, Waisberg J. A hiponatremia como fator preditivo da perda precoce do transplante hepático na modalidade intervivos. Arq Bras Ciênc Saúde 2012;37:76-80. [ Links ]
26. Leise MD, Yun BC, Larson JJ, et al. The effect of pretransplant serum sodium concentration on outcome following liver transplantation. Liver Transpl 2014. [ Links ]
27. Lee J, Kim DK, Lee JW, et al. Rapid correction rate of hyponatremia as an independent risk factor for neurological complication following liver transplantation. Tohoku J Exp Med 2013;229:97-105. [ Links ]
28. Gaglio P, Marfo K, Chiodo J, 3rd. Hyponatremia in cirrhosis and end-stage liver disease: treatment with the vasopressin V(2)-receptor antagonist tolvaptan. Dig Dis Sci 2012;57:2774-85. [ Links ]
29. Ishikawa T. Novel additional indication of tolvaptan: Can tolvaptan provide a beneficial therapeutic option in cirrhotic patients with ascites? Hepatol Res 2014;44:70-2. [ Links ]
30. Gerbes AL, Gulberg V, Gines P, et al. Therapy of hyponatremia in cirrhosis with a vasopressin receptor antagonist: a randomized double-blind multicenter trial. Gastroenterology 2003;124: 933-9. [ Links ]
31. Guyader D, Patat A, Ellis-Grosse EJ, Orczyk GP. Pharmacodynamic effects of a nonpeptide antidiuretic hormone V2 antagonist in cirrhotic patients with ascites. Hepatology 2002;36:1197-205. [ Links ]
32. OLeary JG, Davis GL. Conivaptan increases serum sodium in hyponatremic patients with end-stage liver disease. Liver Transpl 2009;15:1325-9. [ Links ]
33. Gines P, Wong F, Watson H, Milutinovic S, del Arbol LR, Olteanu D. Effects of satavaptan, a selective vasopressin V(2) receptor antagonist, on ascites and serum sodium in cirrhosis with hyponatremia: a randomized trial. Hepatology 2008;48:204-13. [ Links ]
34. Cárdenas A, Gines P, Marotta P, et al. Tolvaptan, an oral vasopressin antagonist, in the treatment of hyponatremia in cirrhosis. J Hepatol 2012;56:571-8. [ Links ]
35. Lehrich RW, Ortiz-Melo DI, Patel MB, Greenberg A. Role of vaptans in the management of hyponatremia. Am J Kidney Dis 2013;62:364-76. [ Links ]
36. Krag A, Moller S, Pedersen EB, Henriksen JH, Holstein-Rathlou NH, Bendtsen F. Impaired free water excretion in child C cirrhosis and ascites: relations to distal tubular function and the vasopressin system. Liver Int 2010;30:1364-70. [ Links ]
37. Wong F, Gines P, Watson H, et al. Effects of a selective vasopressin V2 receptor antagonist, satavaptan, on ascites recurrence after paracentesis in patients with cirrhosis. J Hepatol 2010;53: 283-90. [ Links ]
38. Boyer TD. Tolvaptan and hyponatremia in a patient with cirrhosis. Hepatology 2010;51:699-702. [ Links ]
39. Schrier RW, Gross P, Gheorghiade M, et al. Tolvaptan, a selective oral vasopressin V2-receptor antagonist, for hyponatremia. N Engl J Med 2006;355:2099-112. [ Links ]
40. Sakaida I, Kawazoe S, Kajimura K, et al. Tolvaptan for improvement of hepatic edema: A phase 3, multicenter, randomized, double-blind, placebo-controlled trial. Hepatol Res 2014;44:73-82. [ Links ]











 text in
text in