Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.30 no.1 Bogotá Jan./Mar. 2015
Manejo de un sangrado por úlcera posligadura de várices esofágicas mediante prótesis metálica autoexpandible: reporte de un caso y revisión de la literatura
Margarita Rey MD. (1), Jaime Solano MD. (1), Fernando Sierra A. MD. (1), Luis Felipe Cabrera V. MD. (2)
(1) Fundación Santa Fe de Bogotá, Servicio de Gastroenterología. Bogotá, Colombia.
(2) Universidad El Bosque, Cirugía General. Bogotá, Colombia.
Fecha recibido: 15-05-14 Fecha aceptado: 02-02-15
Resumen
Los inicios del manejo del sangrado variceal con compresión directa datan de 1930 por Westphal y colaboradores. Después, en 1950, se desarrolló el balón de Sengstaken-Blakemore, definido por Panes y colaboradores como la primera línea de terapia; en 1980, a nivel de várices esofágicas y en várices gástricas, se empleaba el balón de Linton-Nachlass (1, 2). Se presenta el caso clínico de un paciente con cirrosis hepática por hepatitis C, Child B, con várices esofágicas, a las cuales se les realizó ligadura en dos ocasiones por sangrado y en la segunda ocasión por inminencia de ruptura, esta última llevada a cabo dos semanas antes del evento. El paciente muestra un cuadro clínico compatible con hemorragia de vías digestivas altas masiva, con evidencia endoscópica de úlcera esofágica sangrante que no mejora con terlipresina, ni escleroterapia con adrenalina, ni compresión local con balón de acalasia. En consecuencia, como terapia de rescate se decide colocar un stent esofágico metálico autoexpandible parcialmente recubierto (por no contar con totalmente recubierto en el momento), con control parcial del sangrado. Es recomendable el uso del stent como terapia de rescate para el sangrado por várices esofágicas refractarias. Debe emplearse el diseñado especialmente para esta indicación (SX-Ella Danis), como un puente para poder estabilizar al paciente y realizar una terapia definitiva como la TIPS, tal cual como se procedió en un nuestro paciente.
Palabras clave
Stent esofágico, hemorragia variceal refractaria, úlcera esofágica.
INTRODUCCIÓN
Los inicios del manejo del sangrado variceal con compresión directa datan de 1930 por Westphal y colaboradores. Después, en 1950, se desarrolló el balón de Sengstaken-Blakemore, definido por Panes y colaboradores como la primera línea de terapia; en 1980, a nivel de várices esofágicas y en várices gástricas, se empleaba el balón de Linton-Nachlass (1, 2), con un muy variable control a corto plazo del sangrado (del 50% al 91,5%) y con complicaciones como neumonía aspirativa, úlceras esofágicas gigantes, desgarros esofágicos y obstrucción de la vía aérea. Además los pacientes manejados con terapia compresiva de balón resangraban en un 50% al momento de retirar el dispositivo (3, 4). El sangrado variceal presenta una mortalidad a 6 semanas del 15% al 20% según la severidad de la enfermedad hepática concomitante. El manejo actual comprende la combinación de medicamentos vasoactivos locales y sistémicos, terapia endoscópica con ligadura con bandas y administración de antibióticos (1). Asociado con este tratamiento, García-Pagan y colaboradores demostraron que la realización temprana de derivación portosistémica intrahepática transyugular (TIPS), durante las primeras 72 horas y en pacientes con alto riesgo de falla del manejo estándar, reduce de manera significativa la mortalidad. Hasta el momento, el taponamiento con balón solamente está indicado en sangrado masivo no controlado, por un máximo de 24 horas y como puente para una terapia definitiva (2).
CASO CLÍNICO
Paciente masculino de 53 años de edad, con cuadro clínico de 1 hora de evolución, consistente en hematemesis de 300 mL aproximadamente y con lipotimia posterior, motivo de la consulta. Como antecedente importante, se trata de un paciente con cirrosis hepática por hepatitis C, Child B, en valoración pretrasplante hepático, con dos cordones varicosos que fueron llevados a ligadura en dos ocasiones por sangrado, la segunda vez por inminencia de ruptura, esta última realizada dos semanas antes del evento. Presenta además toxoplasmosis ocular tratada con clindamicina más trimetropin-sulfametoxazol durante 30 días, hipertensión arterial diagnosticada desde hace 2 años y que recibe manejo crónico farmacológico con enalapril 5 mg/día, omeprazol 20 mg/día y propranolol 20 mg cada 12 horas. Ingresa con hemoglobina de 10,2 mg/dL, se reserva y se inicia manejo con terlipresina y ceftriaxona. Después, en la sala de urgencias, el paciente presenta un episodio de hematemesis masiva que le genera inestabilidad hemodinámica dada por hipotensión y dificultad respiratoria, por lo cual requiere intubación orotraqueal, 3 unidades de glóbulos rojos y soporte vasopresor con noradrenalina. Se realiza endoscopia de vías digestivas altas que muestra: sangrado en jet a nivel del tercio distal del esófago, desgarro sin evidencia de perforación, sangrado activo y úlcera con vaso expuesto. Se lleva a cabo hemostasia con adrenalina aunque sin éxito en el control de la hemorragia, por lo que se procede a emplear el balón de acalasia, que inicialmente controla el sangrado, aunque después continúa siendo activo. Dado lo anterior, se coloca un stent esofágico metálico autoexpandible parcialmente recubierto (por no contar con uno totalmente recubierto en el momento) como terapia de rescate, con el que se logra un control parcial de la hemorragia. Luego de la estabilización, el paciente es trasladado a la unidad de cuidados intensivos (UCI). A las 24 horas presenta un pico febril y leucocitosis, se toma una TAC contrastada de tórax que evidencia neumomediastino y derrame pleural izquierdo.
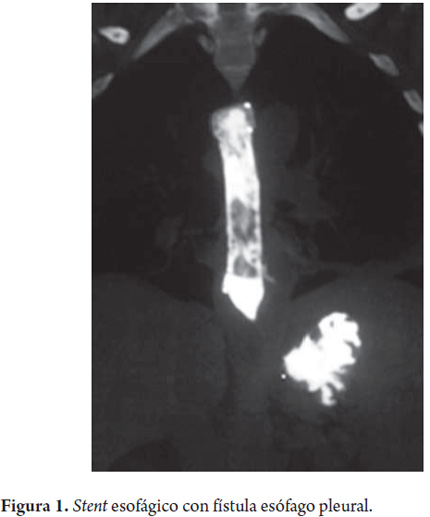
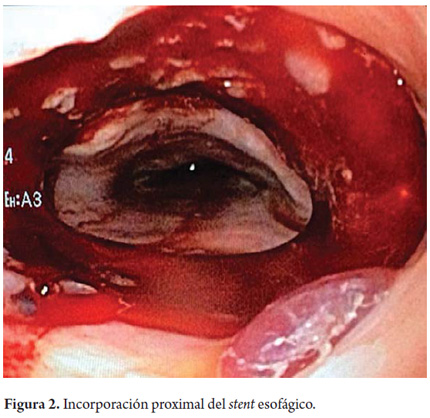
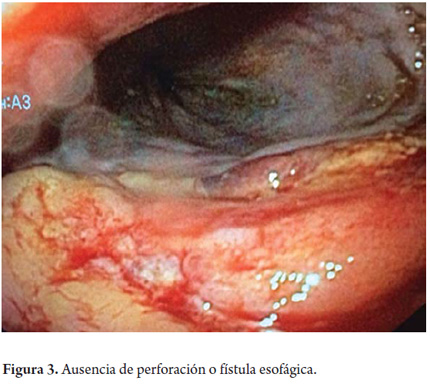
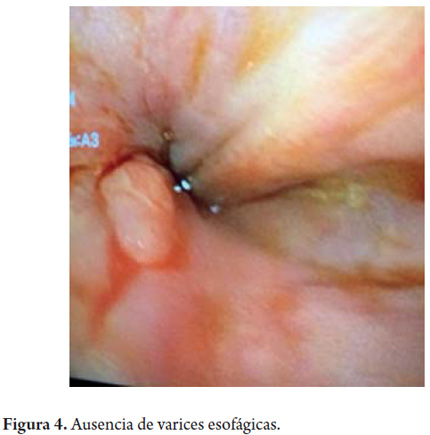
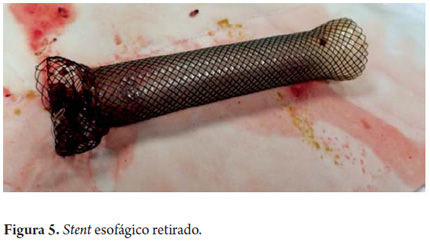
Se considera perforación esofágica y el paciente es llevado a cirugía para drenaje por mediastinitis aguda, esofagorrafia más rotación de colgajo del músculo intercostal y decorticación pleural. Se inicia manejo antibiótico con linezolid y meropenem. En su evolución hay evidencia de formación de una fístula esofágica con subsecuente resolución a la tercera semana de tratamiento médico (figura 1). El paciente es sometido a TIPS, sin complicaciones. A la cuarta semana se retira el stent esofágico parcialmente recubierto, bajo anestesia general y guía radiográfica que muestra incorporación proximal del stent en la pared esofágica (figura 2), el cual se libera con tracción progresiva y extracción del mismo sin complicaciones. Se revisa el esófago y se observa que hay ausencia de úlceras o várices esofágicas y que la perforación está resuelta (figuras 3, 4 y 5). A las 24 horas, el paciente tolera la vía oral y es dado de alta.
DISCUSIÓN
Aproximadamente del 10% al 20% de los pacientes con sangrado variceal esofágico no mejoran con la terapia estándar combinada con medicamentos y terapia endoscópica, y son llevados a terapias de rescate como taponamiento con balón, TIPS o derivación portosistémica quirúrgica (1).
El balón de Sengstaken-Blakemore es un tubo multiluminal con dos balones inflables, uno esofágico y otro gástrico, de 250 mL, que se utiliza en los casos de sangrado persistente; dicho balón presenta variaciones en su morfología, como el de Minnesota, por ejemplo, el cual contiene un puerto de succión a nivel esofágico (2, 3). El porcentaje promedio de control del sangrado con este dispositivo es del 80%; en casos de resangrado, como ya se mencionó, es del 50%, al retiro del balón (4). En estos pacientes se ha podido identificar que el principal error en la falla del control de la hemorragia es la ubicación del balón a nivel de la unión gastroesofágica. Se debe tener presente que se trata de una terapia puente por un máximo de 24 horas y que su eficacia depende del operador, con un 6% a 20% de complicaciones fatales, como la perforación esofágica, y un 10% a 20% de riesgo de broncoaspiración asociado con encefalopatía de base (1). En nuestro caso, al no contar con un balón de Sengstaken-Blakemore, se intentó emplear el balón de dilatación de acalasia con el mismo principio de acción, sin tener éxito en el control del sangrado.
Con respecto al manejo quirúrgico, su realización ha disminuido debido a los avances en las técnicas endoscópicas, a la TIPS y al trasplante hepático; sin embargo, solo es una terapia efectiva en algunos pacientes seleccionados. Se divide en dos categorías: los procedimientos sin cortocircuito, que incluyen la transección esofágica y la devascularización gastroesofágica; y los procedimientos con cortocircuito, en los cuales tenemos los selectivos, como el cortocircuito esplenorrenal (procedimiento de Warren), parciales, con cortocircuitos portocava de vasos de pequeño calibre, y no selectivos, como los cortocircuitos portocava (2, 5). El cortocircuito esplenorrenal es efectivo en el control del sangrado y protege más para el resangrado que la devascularización gastroesofágica. El procedimiento de Sugiura modificado, el cual consiste en devascularización de la unión gastroesofágica más transección esofágica con sutura mecánica y esplenectomía, puede ser una terapia de salvación en hospitales sin experiencia en cortocircuitos portocava (6, 7). A pesar de la efectividad quirúrgica, la mortalidad de estos procedimientos oscila entre un 45% y un 75% (2).
La TIPS se introdujo en el año de 1990 como una alternativa a los procedimientos quirúrgicos; hasta la fecha, en la mayoría de los centros de alta complejidad, los ha reemplazado. Consiste en comunicar las venas suprahepáticas con la vena porta a través de un stent metálico autoexpandible recubierto de 8 a 12 mm de diámetro (2). Está indicada en pacientes con hemorragia variceal no controlada o recurrente a pesar del manejo farmacológico y endoscópico, con una efectividad alta del 95% y un riesgo de resangrado solamente del 18%. Sin embargo, presenta una incidencia del 30% al 35% de encefalopatía como efecto adverso (8). En nuestro paciente, luego de la colocación del stent esofágico y cumpliendo 4 semanas de manejo asociado con perforación esofágica, se decide colocar este tipo de dispositivo para disminuir el riesgo de resangrado durante el retiro del stent y dar un manejo definitivo a las várices. En cuanto a las otras posibilidades de manejo definitivo para el sangrado variceal, tenemos la desconexión laparoscópica del sistema ácigos, la ligadura con bandas y el trasplante hepático.
Debido a las anteriores limitaciones de las terapias de rescate mencionadas, desde el 2003 Hubmann y colaboradores introdujeron una nueva terapia para el manejo del sangrado variceal esofágico, con base en los resultados obtenidos en oncología con los cánceres esofágicos estenosantes que usaron stents metálicos autoexpandibles (1, 9). De esta forma, se desarrolló un stent metálico autoexpandible completamente recubierto como alternativa a la terapia de taponamiento con balón en el sangrado variceal refractario agudo. Hasta el momento, este dispositivo cuenta con cuatro estudios realizados, el mayor de ellos con 34 pacientes y que ha demostrado resultados favorables en términos de control inmediato de la hemorragia, con un 77% a 100% de éxito y baja proporción de complicaciones, como técnica de salvación (9, 10). En el caso especial de las várices gástricas, el balón de Linton-Nachlass todavía desempeña un papel importante (11).
El stent metálico autoexpandible completamente recubierto recomendado es el SX ELLA Danis, el cual puede colocarse sin necesidad de endoscopia ni guía radiográfica, con bordes atraumáticos, marcadores distales radiolúcidos y asa de extracción, como lo reportan Wright y colaboradores. Con estas características se da la posibilidad de salvar vidas en la fase prehospitalaria; sin embargo, en el hospital es obligatoria la realización de una endoscopia de vías digestivas altas, ya que el empleo del stent no permite controlar las várices gástricas y en este caso debe combinarse con el balón de Linton-Nachlass (12). El stent se avanza hasta el estómago y el balón gástrico se insufla y se retrae hasta que haya resistencia, que es indicativa de que se está en la unión gastroesofágica y se puede desplegar el stent. Ya en el esófago, el stent puede mantenerse por un tiempo promedio de 2 semanas para disminuir la posibilidad de migración y lesión de la pared esofágica por isquemia (1, 2, 9). Este dispositivo permite, además, mantener permeable el tracto gastrointestinal y disminuye la posibilidad de neumonía aspirativa (3). En nuestro caso, se colocó un stent esofágico de uso convencional parcialmente recubierto ante la no disponibilidad en el momento de uno totalmente recubierto y como medida de rescate, el cual se mantuvo por más de 2 semanas debido a la perforación esofágica que se presentó asociada.
Según el consenso de Baveno V, el éxito del manejo de una hemorragia aguda se evalúa en los 5 días posteriores al evento (1). De esta forma se establecen como predictores de falla del tratamiento un gradiente de presión venoso-hepático mayor de 20 mm Hg, clasificación Child Pugh C y un sangrado activo al momento de la endoscopia (2, 3). El riesgo de mortalidad a las 6 semanas empleando la terapia con stent aumenta considerablemente de un 30% a un 50% con respecto a la terapia estándar combinada; sin embargo, esto se debe a que los pacientes que requieren stent muestran una mayor severidad de su enfermedad hepática y comorbilidades (13). En nuestro caso, a pesar de la alta morbilidad asociada, no se presentó mortalidad y el paciente evolucionó de forma satisfactoria y se pudo dar de alta.
La colocación del stent específico para el control del sangrado variceal requiere entrenamiento y experiencia para prevenir complicaciones como la broncoaspiración, con plena seguridad de que la posición del balón en la unión gastroesofágica es adecuada (2, 3). También se ha descrito la migración del stent hacia el estómago, aunque no generó ninguna complicación asociada; en un paciente se describió la presencia de compresión extrínseca del bronquio fuente izquierdo, que mejoró con el retiro del stent (9, 10). En nuestro caso, no se presentaron complicaciones relacionadas con la colocación o el retiro del stent.
Es importante aclarar que en nuestro caso clínico no hubo un sangrado secundario a várices esofágicas sino a úlcera en el lecho de una várice esofágica ligada 3 semanas antes, la cual no cuenta con reporte de ningún caso manejado con stent metálico autoexpandible y cuya mortalidad es mucho mayor que la reportada en los sangrados variceales no controlados con terapia usual.
CONCLUSIONES
Es recomendable el uso del stent como terapia de rescate para el sangrado por várices esofágicas refractarias. Debe emplearse el stent diseñado especialmente para esta indicación (SX-Ella Danis) como un puente para poder estabilizar al paciente y realizar una terapia definitiva como la TIPS, tal cual como se llevó a cabo en nuestro paciente. Sin embargo, como ya se mencionó, la mortalidad sigue siendo elevada por la severidad de las comorbilidades del paciente. Se requieren estudios clínicos aleatorizados para confirmar la seguridad y eficacia de este manejo.
REFERENCIAS
1. Fierz F. Treatment of esophageal variceal hemorrhage with self-expanding metal stents as a rescue maneuver in a Swiss multicentric cohort. Case Rep Gastroenterol 2013;7:97-105. [ Links ]
2. Maufa F, Al-Kawas FH. Role of self-expandable metal stents in acute variceal bleeding. Int J Hepatol 2012;418369. [ Links ]
3. Escorsell A, Bosch J. Self-expandable metal stents in the treatment of acute esophageal variceal bleeding. Gastroenterol Res Pract 2011;910986. [ Links ]
4. Feneyrou B. Initial control of bleeding from esophageal varices with the Sengstaken-Blakemore tube. Experience in 82 patients. Am J Surg 1988;155(3):509-11. [ Links ]
5. Chong C. Esophageal rupture due to Sengstaken-Blakemore tube misplacement. World J Gastroenterol 2005;11(41):6563-5. [ Links ]
6. Rikkers L. The changing spectrum of treatment for variceal bleeding. Ann Surg 1998;228(4):536-46. [ Links ]
7. Voros D. Long term results with the modified Sugiura procedure for the management of variceal bleeding: standing the test of time in the treatment of bleeding esophageal varices. World J Surg 2012;36(3):659-66. [ Links ]
8. Punamiya S. Role of TIPS in improving survival of patients with decompensated liver disease. Int J Hepatol 2011;398291. [ Links ]
9. Hubmann R. The use of self-expanding metal stents to treat acute esophageal variceal bleeding. Endoscopy 2006;38(9):896-901. [ Links ]
10. Zehetner J. Results of a new method to stop acute bleeding from esophageal varices: implantation of a self-expanding stent. Surg Endosc 2008;22(10):2149-52. [ Links ]
11. Dechene A. Acute management of refractory variceal bleeding in liver cirrhosis by self-expanding metal stents. Digestion 2012;85(3):185-91. [ Links ]
12. Wright G, Lewis H, Hogan B, Burroughs A, Patch D, O´Beirne J. A self-expanding metal stent for complicated variceal hemorrhage: experience at a single center. Gastrointest Endosc 2010;71(1):71-8. [ Links ]
13. De Francis R. Baveno V faculty: revising consensus in portal hypertension: report of the Baveno V consensus workshop on methodology of diagnosis and therapy in portal hypertension. J Hepatol 2010;53:762-8. [ Links ]











 text in
text in