Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista colombiana de Gastroenterología
versión impresa ISSN 0120-9957
Rev Col Gastroenterol vol.30 no.2 Bogotá abr./jun. 2015
Neoplasias hepáticas malignas: 1ª. parte.
Hepatocarcinoma: papel de la biopsia hepática, estudios de inmunohistoquímica y otros aspectos importantes
Rocío del Pilar López Panqueva MD. (1)
(1) Médica patóloga. Hospital Universitario Fundación Santa Fe de Bogotá, Sección Anatomía Patológica. Profesora, Facultad de Medicina, Universidad de los Andes. Bogotá, Colombia.
Fecha recibido: 08-05-15 Fecha aceptado: 22-05-15
Resumen
Continuamos con la revisión de los tumores hepáticos. Nos referiremos a los tumores hepáticos primarios malignos más frecuentes. Tal como lo mencionamos anteriormente, los tumores malignos hepatobiliares son un espectro de tumores invasivos que reciben su nombre dependiendo de su célula de origen. De acuerdo con la Agencia Internacional para el Estudio del Cáncer (IARC), los tumores hepáticos malignos constituyen la segunda causa de muerte en el mundo, con aproximadamente 745 000 muertes/año (1).
Al igual que en el artículo anterior, el objetivo es identificar aquellos aspectos más relevantes de estas neoplasias, en especial los hallazgos morfológicos que generan mayor problema diagnóstico en la utilidad de los estudios de inmunohistoquímica y sus diagnósticos diferenciales.
La primera parte de esta revisión se centrará en el hepatocarcinoma, el más frecuente de los tumores hepáticos epiteliales malignos, algunas de sus variantes y sus lesiones precursoras. También en el controvertido papel de la biopsia hepática para su diagnóstico.
Palabras clave
Tumores hepáticos malignos, hepatocarcinoma, carcinoma hepatocelular, nódulos displásicos, hepatocarcinoma fibrolamelar, biopsia hepática percutánea, biopsia por aspiración, inmunohistoquímica.
CARCINOMA HEPATOCELULAR O HEPATOCARCINOMA: ASPECTOS GENERALES
El carcinoma hepatocelular (CHC) o hepatocarcinoma (HCC) es el tumor primario hepático maligno más frecuente en el mundo. El 85% se desarrolla en el contexto de la enfermedad hepática crónica y cirrosis de cualquier etiología, especialmente la asociada con infección por los virus de la hepatitis B y C (VHB y VHC). Solamente un 15% se presenta en hígados no cirróticos. Es de pobre pronóstico y constituye la segunda causa de muerte relacionada con cáncer en hombres y la sexta en mujeres (2).
Tiene una incidencia muy variable según la edad y zona geográfica: es más frecuente en población mayor de los 65 años de edad. El 80% de todos los HCC ocurre en los países en vía de desarrollo, con una alta incidencia en Asia y en el África Subsahariana, donde puede llegar a 80/100 000 habitantes/año en mujeres y más de 110/100 000 habitantes/año en hombres; la mitad de las muertes ocurre en China. En áreas de baja incidencia, como son los países desarrollados, incluidos Estados Unidos, Europa, Australia y Nueva Zelandia, es de 6,8/100 000 en hombres y de 2,2/100 000 en mujeres (3).
Colombia es un país de baja prevalencia. En Globocan 2012, los datos de la Agencia Internacional para el Estudio del Cáncer (IARC) muestran que en nuestro país la incidencia de "cáncer hepático", sin especificar el subtipo tumoral, es de 2,8 y 3,2/100 000 habitantes; la mortalidad femenina ajustada a la edad es de 3,5-4,0/100 000 habitantes, y la masculina es un poco mayor, siendo de 4,1-4,5/100 000 habitantes. Además establecen que el número estimado de nuevos casos para el año 2015 será de 1462 (1).
El HCC se desarrolla especialmente en el contexto de la enfermedad hepática crónica y cirrosis. Numerosos factores de riesgo han sido identificados; sin embargo, son el VHB, el VHC y el alcohol los de mayor prevalencia en el mundo. El desarrollo del HCC es similar al de otros tumores sólidos, y especialmente en hígados cirróticos existe la presencia de nódulos hiperplásicos, con progresión a nódulos con cambio displásico de bajo grado, luego de alto grado, hasta HCC tempranos y HCC con mayor grado de desdiferenciación (3). Estos cambios dependen de una compleja interacción entre el huésped, la enfermedad de base y los factores ambientales. La modificación de estos es lo que podrá lograr disminuir la tasa mundial de mortalidad. El estrés oxidativo desempeña también un papel importante tanto en la carcinogénesis como en la recurrencia tumoral. Lo apoya el hecho de encontrar niveles séricos derivados de metabolitos de oxígeno reactivos (d-ROM), los cuales son predictores independientes de recurrencia del HCC (p = 0,0185) (4).
Estas variaciones en la incidencia global reflejan la variación en los factores de riesgo, dado que son los países de alta incidencia donde la prevalencia de infecciones virales como VHB y VHC es muy alta y son los responsables del 75%-80% del total de los casos. Cabe señalar que el VHB causa el 60% de los casos en países en vía de desarrollo y solo el 23% en los países desarrollados (3). Aproximadamente el 85% de los casos ocurre en pacientes con cirrosis de cualquier etiología. En Estados Unidos la hepatitis C es una de sus principales causas, aunque el aumento de la prevalencia del síndrome metabólico, la diabetes mellitus, la obesidad y la esteatohepatitis alcohólica y no alcohólica contribuyen ahora al aumento de la incidencia de estas otras etiologías (5).
Estas variaciones parecen estar relacionadas con las diversas etiologías y los diferentes factores de riesgo, principalmente asociados con inflamación del parénquima y con la infección por VHB y VHC. El papel de otros factores tanto genéticos como epigenéticos, de la activación de oncogenes o, por el contrario, la inactivación de genes supresores tumorales está siendo muy estudiado. Un ejemplo de esto es la desregulación de la vía Wnt/β-catenina asociada con el desarrollo de HCC en Europa y un poco menos en Asia. En Colombia, un estudio realizado por el Grupo de Gastrohepatología de la Universidad de Antioquia demostró que la señalización de la Wnt/β-catenina se activa en el 42,6% de las muestras de HCC principalmente asociado de la infección por VHB, uno de los factores de riesgo más importantes de HCC en nuestro país (6). Las aflatoxinas en la dieta tienen un papel relevante en la carcinogénesis del HCC en algunas poblaciones de África Subsahariana, China y Asia; sin embargo, esto no se ha demostrado en Colombia, donde el estudio de Navas y colaboradores encontró solo un 10,5% de mutaciones del codón 249 (mutación "hotspot" aflatoxina común) del gen p53, el cual es un gen supresor tumoral (7, 8).
Es interesante ver cómo el cambio del estilo de vida y la modificación de los factores ambientales en los países occidentales, más el aumento de las tasas de vacunación neonatal contra la hepatitis B y la disminución de la exposición a las aflatoxinas de la dieta en los países en desarrollo están cambiando la evolución de la epidemiología de este tumor (2).
Las guías sugeridas por las Asociaciones Americana (AASLD) y Europea (EASL) para el estudio de las enfermedades hepáticas han formulado algunas estrategias a seguir, dado que el tratamiento depende de un diagnóstico temprano del HCC, especialmente en aquellos pacientes de alto riesgo. Estas guías se basan en el tamaño de los nódulos hepáticos y en su identificación con imágenes (9, 10).
¿Cuándo, entonces, debemos realizar una biopsia?
El diagnóstico histológico no es necesario cuando el diagnóstico de HCC por imágenes es claro. Esto es considerado como grado de recomendación A, con un nivel de evidencia 1a. El diagnóstico histológico por biopsia está indicado cuando los hallazgos de imagen son atípicos, lo que constituye un grado de recomendación C con un nivel de evidencia 3b (9).
En lesiones indeterminadas se recomienda el seguimiento con imágenes o realizar una biopsia de acuerdo con el nivel de sospecha de malignidad. Algunos estudios han demostrado la utilidad de combinar el estudio radiológico y la biopsia, lo que mejora la sensibilidad sin perjudicar la especificidad o el valor predictivo positivo o negativo para el diagnóstico de HCC en pacientes con cirrosis y nódulos de 20 mm o más pequeñas. Aun cuando el diagnóstico más frecuente es el HCC, por estudio histopatológico también se han diagnosticado colangiocarcinomas intrahepáticos o lesiones benignas, metástasis que aunque son inusuales en hígados cirróticos, han sido encontradas; de igual manera están descritas metástasis de tumores neuroendocrinos, carcinomas de colon y de glándula mamaria, entre muchos otros (11).
Dada la heterogeneidad clínica, patológica y molecular del CHC, hay varias modalidades terapéuticas disponibles que pueden ser curativas, como son la resección quirúrgica o el trasplante hepático, o paliativas, como la ablación local, las terapias dirigidas por catéter o la terapia sistémica.
¿Por qué no hacer estudio histopatológico?
Al respecto existe mucha controversia, en especial porque las imágenes diagnósticas han demostrado tener una alta precisión, con excelente sensibilidad y especificidad en el diagnóstico de las masas hepáticas (12). La tasa global de complicaciones de una biopsia es del 29%, el 90% de las cuales son complicaciones menores e incluyen dolor e hipotensión transitoria. También hay complicaciones mayores como hemorragia intrahepática o intraperitoneal, hemotórax, neumotórax, lesión de órganos vecinos y fístulas arteriovenosas. El riesgo de siembra en el trayecto de la aguja, la diseminación hematógena intraprocedimiento y de recurrencia postrasplante tienen una tasa de prevalencia de 0,003%-5%. Se informa que la tasa de mortalidad después de la biopsia hepática está entre el 0% y el 0,18%, atribuible a hemorragia significativa y peritonitis (13).
En consecuencia nos planteamos: ¿cuál es el reto diagnóstico en un paciente cirrótico? ¿Cuándo un paciente se beneficia de un estudio histopatológico?
En la actualidad muy frecuentemente se realiza en aquellos pacientes que muestran imágenes atípicas y que no permiten diferenciar un HCC. Por tanto, solo un juicioso criterio clínico y la individualización de cada uno determinará la exacta indicación y beneficio de la biopsia.
Son 4 los mayores retos del diagnóstico de una masa hepática, a saber (14, 15):
- Lograr diferenciarlo de una lesión nodular hepatocelular benigna, sea un nódulo regenerativo grande, un nódulo displásico, hiperplasia nodular focal, adenoma hepatocelular o simplemente hepatocitos reactivos.
- Diferenciar el HCC del colangiocarcinoma intrahepático o de los tumores metastásicos.
- Determinar la histogénesis de un tumor maligno.
- Establecer el sitio de origen primario de un tumor hepático metastásico.
¿Cuál método es mejor y por qué? ¿La citología o biopsia por aspiración con aguja fina o la biopsia percutánea?
La biopsia por aspiración con aguja fina (BAAF) guiada por imágenes es segura, mínimamente invasiva, útil en pacientes con comorbilidades importantes y enfermedad avanzada. Tiene buena sensibilidad (91,5%) y precisión global de diagnóstico (92,4%), con excelente especificidad (100%) y valor predictivo positivo (100%), con aceptable valor predictivo negativo (59,1%). Además tiene una buena correlación de malignidad/citología por aspiración y los niveles de alfafetoproteína (AFP) ≥400 µg/L (14). Si se utiliza citología en base líquida y/o bloque celular o combinación con biopsia, pueden realizarse fácilmente estudios adicionales de histoquímica, como el retículo, o de inmunofenotipo, los cuales resultan muy útiles en el diagnóstico de HCC (16, 17).
La principal complicación es el sangrado; ocurre más en el HCC de localización superficial, en tumores grandes y cirrosis grave. Las metástasis de implantación forman un nódulo subcutáneo en el sitio o trayecto de la biopsia previa, aunque tienen poco efecto en el pronóstico y pueden ser tratadas con resección o radioterapia.
El papel de la BAAF ha cambiado en la última década a pesar de que usualmente el material citológico es escaso, hemorrágico y se centra más en la morfología celular, siendo los cambios arquitecturales sutiles o muy difíciles de identificar. Este método tiene pocos riesgos, mínima morbilidad, es económico y proporciona un rápido resultado. Los resultados óptimos dependen más de un trabajo en equipo radiólogo-citopatólogo, ambos expertos y con entrenamiento especializado. Es ideal contar con un servicio de citopatología en el mismo lugar donde se realiza el procedimiento o in situ, posibilidad de realizar estudios de inmunohistoquímica y una adecuada correlación clinicopatológica; es además una metodología segura, rápida y económica. Estos beneficios hacen que la BAAF muy probablemente sea incorporado rápidamente como un punto de partida hacia la medicina personalizada en el diagnóstico de las masas hepáticas, además de estar recomendada en las guías de la AASLD (12).
Los patólogos preferimos la biopsia Trucut o percutánea ya que se obtiene mayor cantidad de tejido donde no solo se puede analizar la morfología celular, sino que las alteraciones arquitecturales son más evidentes y pueden realizarse con mayor precisión técnicas de histoquímica e inmunohistoquímica, estudios moleculares, en algunos casos indispensables para el diagnóstico, y a la luz de las nuevas terapias dirigidas está demostrando su gran utilidad pronóstica y predictiva.
En términos generales, se requiere de la confirmación de un tumor maligno para el inicio de cualquier terapia, sea curativa o paliativa. Varios estudios muestran falsos positivos hasta en el 20% de los casos (7%-31%) cuando solo se utilizan estudios no invasivos. La recomendación de estudio histopatológico se dirige a los casos que muestren características radiológicas atípicas en al menos dos estudios consecutivos. Esta evaluación puede diferenciar entre lesiones premalignas, como son los nódulos displásicos de célula grande y de célula pequeña, y el HCC precoz, además de las variantes atípicas de HCC que deben ser reconocidas morfológicamente ya que confieren un importante valor pronóstico, así como un manejo terapéutico diferente (18-20). Algunos grupos han demostrado que la biopsia preoperatoria no influye negativamente el curso oncológico de los pacientes que van a ser llevados a un trasplante hepático y esto es importante para apoyar su uso y no restringirla en situaciones dudosas (21).
ASPECTOS PATOLÓGICOS DE IMPORTANCIA
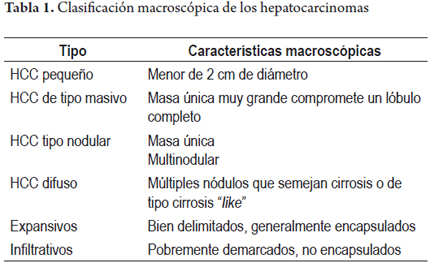
La clasificación basada en la imagen macroscópica ha sido descrita por numerosos autores desde hace más de 1 siglo. Generalmente requiere el examen de todo el tumor y por sí sola no aporta información útil pronóstica y predictiva ni tampoco proporciona claves para explicar su patogénesis.
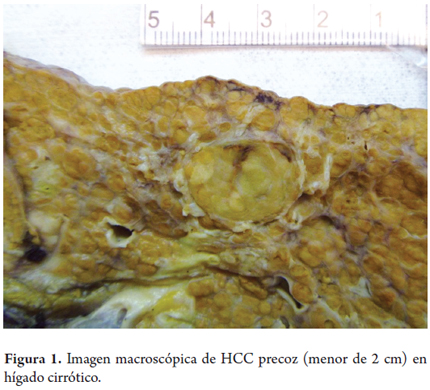
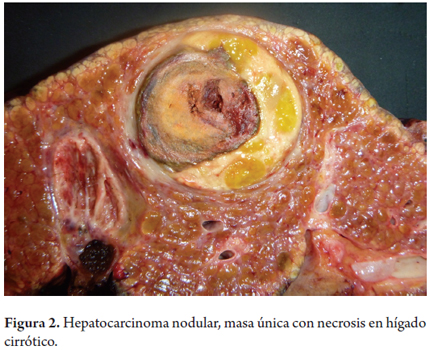
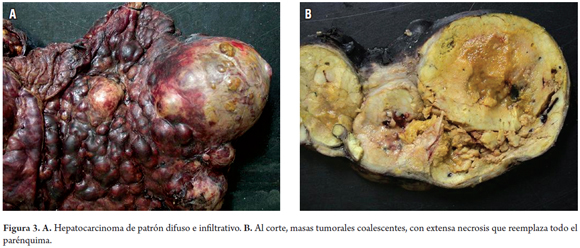
En la tabla 1 se resume las clasificaciones macroscópicas existentes. Los tumores pequeños, encapsulados o los pedunculados, sin evidencia de invasión vascular y aquellos no asociados con cirrosis tienen mejor pronóstico. Los tumores grandes, con necrosis, invasión vascular o de la vía biliar empobrecen el pronóstico. En las figuras 1, 2 y 3 se muestran las imágenes macroscópicas de un HCC precoz (menor de 2 cm), nodular con masa única y patrón difuso e infiltrativo.
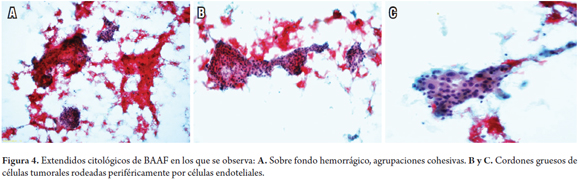
En el estudio citológico (BAAF) las principales características son la presencia de células poligonales de amplio citoplasma eosinofílico, núcleos vesiculosos o hipercromáticos, variables según el grado de diferenciación, nucléolo prominente, y dispuestas en agrupaciones tridimensionales. Pueden observarse la disposición trabecular o pseudoglandular o la presencia de pigmento biliar. Las agrupaciones son cohesivas con proyecciones arborescentes y cordones gruesos de células tumorales. Pueden estar rodeadas periféricamente por células endoteliales (figura 4).
Plantean un problema en el diagnóstico diferencial con lesiones hepatocelulares bien diferenciadas, y los tumores metastásicos con el HCC pobremente diferenciado. La presencia de necrosis puede sugerir un absceso o la atipia reactiva de los hepatocitos vecinos a las lesiones metastásicas puede confundirse con el HCC. La ayuda de métodos de inmunohistoquímica es útil e indispensable (22, 23). Sin embargo, usualmente su uso está limitado por la ausencia de material suficiente en los aspirados citológicos.
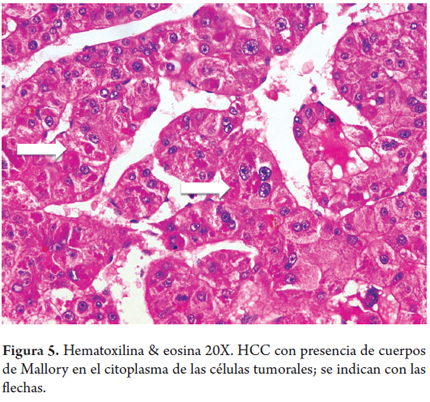
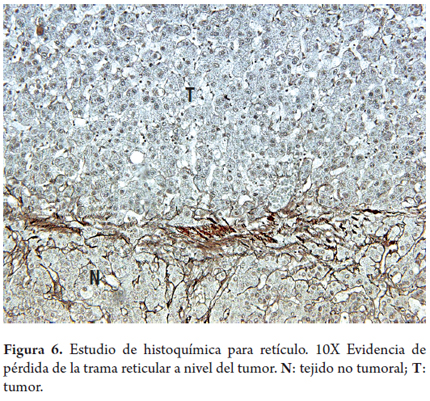
En el estudio histopatológico de las biopsias o resecciones, las células tumorales del HCC semejan a las células hepáticas normales. La atipia celular dependerá del grado de diferenciación del tumor. Los hepatocitos tumorales se disponen en trabéculas o hileras de más de dos células, sus núcleos varían de tamaño y forma, con hipercromasia e irregularidad de la membrana, lo que aumenta la relación núcleo-citoplasma con nucléolo prominente y eosinofilia citoplasmática. Los HCC pueden contener los productos celulares normales del hígado como glicoproteínas o bilis, u otros como grasa, cuerpos de Mallory (figura 5), glóbulos de alfa-1-antitripsina, fibrinógeno u otras proteínas celulares. Frecuentemente se observan canalículos biliares que rodean a las células tumorales o con tapones biliares en canalículos dilatados. Esta condición es muy útil en el diagnóstico diferencial de tumores pobremente diferenciados o en los metastásicos. La trama reticular se pierde en los HCC (figura 6) (24, 25).
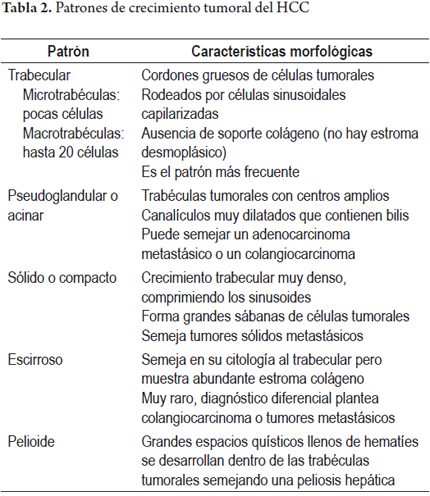
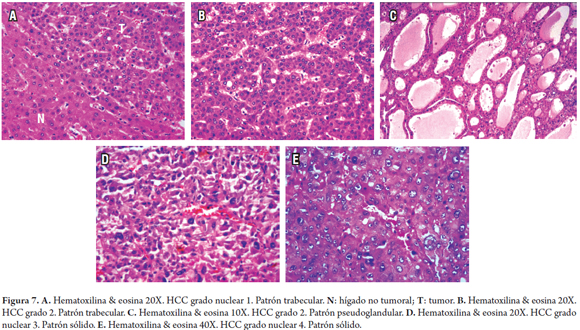
Son varios los patrones arquitecturales que pueden ser observados en un hepatocarcinoma. En la tabla 2 se resumen las principales características de los patrones más observados. La graduación microscópica está basada en las alteraciones nucleares. En 1954, Edmondson y Steiner propusieron una escala de I a IV, donde se tiene en cuenta el tamaño e irregularidad nuclear, la hipercromasia, la relación núcleo-citoplasma, asociado con la diferenciación tumoral (figura 7). El grado I resulta imposible de diferenciar citológicamente de un adenoma hepatocelular; por tanto, el diagnóstico se hace basado en los cambios de arquitectura, el patrón de crecimiento, la invasión vascular o la metástasis.
La necrosis e invasión vascular son frecuentes. Esta última es observada en las resecciones y explantes por trasplante, aunque es inusual de encontrar en las biopsias. Las metástasis intrahepáticas ocurren en el 60% de los tumores menores de 5 cm y en más del 95% en las de mayor tamaño. La invasión del ducto biliar es rara y ocurre en menos del 5% de los casos.
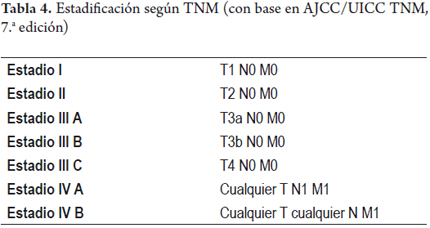
La clasificación TNM y su estadificación debe ser codificada según las recomendaciones del Comité Conjunto para el Estudio del Cáncer y la Unión Internacional para el Control del Cáncer (AJCC/UICC) y el Colegio Americano de Patología (CAP) (tablas 3 y 4).
VARIANTES DEL HCC
Se reconocen algunas variantes morfológicas del HCC como son el carcinoma escirroso, sarcomatoide, de célula clara, inflamatorio, linfoepitelioma "like" o medular, con diferenciación de tipo biliar. Usualmente estas acompañan la forma clásica, con presentación de focos de estas variantes o combinaciones de ellas. También se observan tumores mixtos como hepatocolangiocarcinoma.
Algunas como la variante de célula clara, en la cual el aspecto de las células tumorales con citoplasma amplio claro y transparente es dado por el abundante contenido de glucógeno, pueden causar problemas en el diagnóstico ya que esta semeja un carcinoma adrenal cortical, un carcinoma renal de célula clara metastásico o un carcinoma neuroendocrino.
También se observa el HCC escirroso con abundante estroma fibroso que semeja sarcomas, colangiocarcinoma o un adenocarcinoma metastásico. En estos casos, resulta de gran utilidad el uso de los estudios de inmunohistoquímica.
HEPATOCARCINOMA FIBROLAMELAR
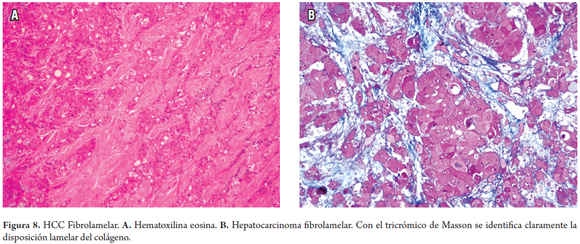
Corresponde a un subgrupo de HCC. Difiere de los anteriormente descritos ya que presenta unas características clínicas y pronósticas muy diferentes. Por lo general ocurre en los adultos jóvenes y adolescentes, con una media de 23 años de edad, igual hombres que mujeres y no tiene asociación con enfermedad crónica del hígado, cirrosis, ni se conoce otro factor de riesgo asociado. Además, su crecimiento es lento en comparación con otros tipos y tiene un mejor pronóstico con un 50%-70% de supervivencia a los 5 años. En esta variante, las células tienen abundante citoplasma eosinófilo y granular, núcleos redondeados, frecuentemente con inclusiones y nucléolo prominente; lo más característico es la disposición del colágeno, el cual es abundante y forma láminas paralelas, "lamelar", entre las trabéculas o los nidos de las células hepatocitarias tumorales (figura 8).
Los principales diagnósticos diferenciales de las masas en el hígado no cirrótico en personas jóvenes incluyen las descritas en nuestro anterior artículo, como son el adenoma, la hiperplasia nodular focal y la hiperplasia nodular regenerativa. Las variantes escirrosa y el carcinoma esclerosante asociado con hipercalcemia también debe ser planteado en el diferencial del HCC variante fibrolamelar (24). Recientemente hemos descrito una variante inusual de HCC mixto con componente clásico y fibrolamelar (26).
Es en estos casos donde el estudio histopatológico resulta fundamental para determinar la histogénesis de una lesión nodular hepática. Se prefiere la biopsia o la resección completa de la lesión ya que la BAAF el componente fibrolamelar no se desprende fácilmente en las citopunciones y es poco celular, por lo cual se dificulta el diagnóstico o no es definitivo (24).
LESIONES PRECURSORAS: NÓDULOS DISPLÁSICOS
Nódulo displásico (ND) es el término usado para identificar una lesión benigna que se puede confundir con HCC. Abarca las lesiones anteriormente descritas, como son la hiperplasia adenomatosa, los nódulos macrorregenerativos o cualquier nódulo en un hígado cirrótico, que son macroscópicamente diferentes en su forma, color y tamaño de los nódulos cirróticos circundantes y que son detectados por estudios de imágenes. Aquí es donde el examen histológico es necesario. Se clasifican como de bajo grado o de alto grado con base en las características morfológicas.
Las de bajo grado son ND que contienen áreas portales dentro de los nódulos y se componen de células hepáticas que son muy semejantes a las normales con relación núcleo-citoplasma normal o ligeramente aumentada, mínima atipia nuclear y sin mitosis.
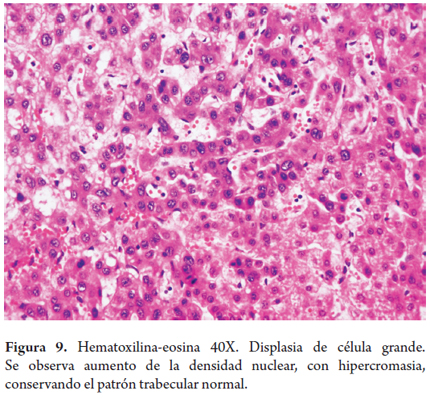
Las de alto grado son ND que se caracterizan por el cambio de células pequeñas. Son consideradas como lesiones preneoplásicas en las cuales los hepatocitos son considerablemente más pequeños que las células normales y aparecen como una zona de aglomeración nuclear, con aumento de la densidad nuclear, o pueden estar dispuestas aisladamente. El citoplasma es más basófilo que en los hepatocitos normales, aunque no hay atipia nuclear significativa, ni tampoco invasión al estroma (figura 9). Pueden tener disposición pseudoglandular o dar la apariencia de un nódulo dentro de otro nódulo. En algunos casos puede ser extremadamente difícil o imposible diferenciar entre un ND de alto grado y un HCC, especialmente en biopsias con aguja (21, 22).
Un estudio que puede ayudar es el retículo. Su trama está preservada o solo muy focalmente está ausente. La CK7 muestra reactividad en ductos proliferados en la periferia del nódulo en más del 95% de los casos de ND de alto grado, mientras que en el HCC esta reacción ductular está ausente o es focal con la tinción CK7.
ESTUDIOS DE INMUNOHISTOQUÍMICA ÚTILES EN EL DIAGNÓSTICO DE HCC
Existen múltiples marcadores de inmunohistoquímica que pueden ser útiles en casos seleccionados de difícil interpretación para confirmar el diagnóstico de HCC. Enumeraremos solo los más utilizados (27-32) y en la tabla 5 se muestran los puntos clave a tener en cuenta.
- El antígeno carcinoembrionario policlonal (pCEA) es útil para demostrar canalículos biliares, tanto en hígado normal como en HCC.
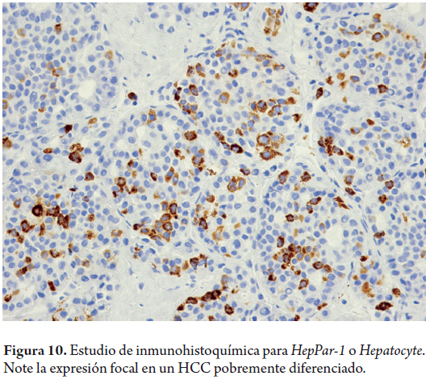
- El HepPar-1 o Hepatocyte es un anticuerpo monoclonal que reacciona con un epítope de las mitocondrias del hígado, produce una tinción positiva en aproximadamente el 90% de los casos de HCC, aun cuando no es exclusivo de tumores hepatocelulares, y debe ser interpretado en un contexto clínico y morfológico adecuado (figura 10).
- La alfa-fetoproteína (AFP) frecuentemente está elevada en el suero de los pacientes con HCC. Incluso cuando el tumor es negativo por inmunotinción, se ha encontrado tinción en parches en más del 50% de los HCC.
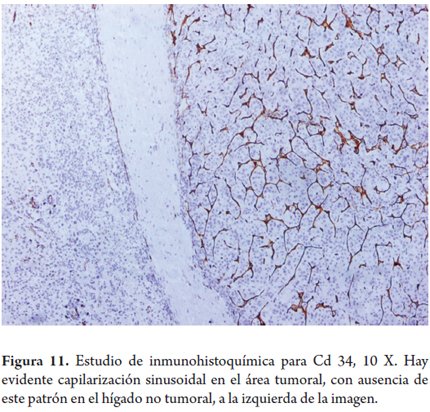
- El CD34 es un marcador de células endoteliales, aunque en el hígado el endotelio sinusoidal especializado normalmente no expresa este marcador. En el HCC existe el fenómeno conocido como capitalización sinusoidal y las células que rodean las trabéculas de HCC son generalmente positivas para CD34, mientras que lesiones hepatocelulares benignas tienen típicamente CD34 positivo solo en las zonas periféricas o cerca de los septos fibrosos. La reactividad difusa en los sinusoides para CD34 puede ser útil para distinguir un nódulo cirrótico de un HCC bien diferenciado (figura 11).
- La proteína HSP70 es una proteína que desempeña un papel importante en la regulación celular y la progresión del ciclo, se expresa en más del 80% de los HCC tempranos.
- La glutamina-sintetasa (GS) es el resultado de la translocación nuclear de la β-catenina y se correlaciona con su activación en los HCC. La expresión difusa se encuentra hasta en el 70% de los HCC y además tempranamente en los ND de alto grado, aunque es focal y en menos del 15% de los casos.
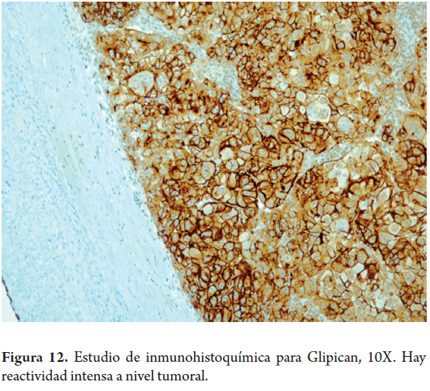
- El glipican-3 (GPC-3) es una oncoproteína que se identifica en la mayoría de los HCC. Es un buen marcador de diferenciación hepatocelular en neoplasias hepáticas primarias malignas, no se expresa en el tejido normal, ni en las neoplasias benignas hepatocelulares, ni tampoco en las lesiones pseudotumorales, y existe inmunotinción solo focalmente en algunos ND y en el tejido de hepatitis con marcada actividad inflamatoria (figura 12).
- La arginasa-1 (Arg-1) es un marcador muy sensible de hepatocitos benignos y malignos que puede ser una herramienta diagnóstica útil en la práctica. La patología hepática tumoral se detecta en el 96% casos de HCC y en el 0% de los casos de tumores metastásicos.
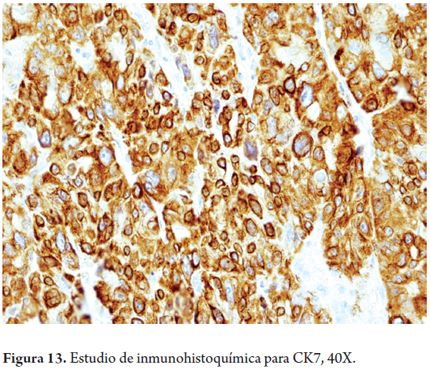
- Las citoqueratinas de bajo peso molecular como la CAM5.2 y las citoqueratinas 8 y 18 muestran reactividad mientras que usualmente las citoqueratinas 7, 20 y AE1/AE3 son negativas en el HCC clásico. Solo la variante fibrolamelar muestra expresión para la CK7 (figura 13).
- El receptor del factor de crecimiento epidérmico (EGFR) ha mostrado utilidad como biomarcador predictivo de respuesta a los antagonistas EGFR en el carcinoma fibrolamelar.
Los diagnósticos diferenciales se plantean usualmente entre carcinoma hepatocelular bien diferenciado versus adenoma, carcinoma hepatocelular versus colangiocarcinoma y carcinoma hepatocelular versus tumores metastásicos. Es precisamente en estos casos donde los estudios de inmunohistoquímica son útiles. Obviamente la interpretación debe realizarse en conjunto con la historia clínica, las imágenes, el patrón morfológico, la combinación de histoquímica para retículo y dos o más de los estudios de inmunohistoquímica.
CONCLUSIÓN
Los tumores malignos más frecuentes en el hígado son los tumores metastásicos o secundarios y en segundo lugar el hepatocarcinoma como tumor primario, especialmente en pacientes cirróticos de cualquier etiología. A la luz de la medicina actual, cada vez con mejores técnicas de imagen y el auge de las terapias dirigidas a la necesidad del paciente, decidir hacer una biopsia tal vez sea una necesidad ética, que beneficie y ayude a optimizar la interpretación de los resultados, definir subgrupos de pacientes que puedan beneficiarse de una u otra terapia, evitar así la posibilidad de efectos secundarios y disminuir los costos al sistema de salud. En este escenario resulta un gran reto clínico, que puede ser para el patólogo muy sencillo o, por el contrario, ser uno de los especímenes más desafiantes en la patología quirúrgica, incluso para los patólogos más especializados. Requiere un estudio detallado y muy cuidadoso de la citología y arquitectura tumoral con coloraciones de rutina de hematoxilina & eosina, frecuentemente acompañado de estudios adicionales de histoquímica, como el retículo, un panel de estudios de inmunohistoquímica y obviamente el conocimiento de la historia clínica, de los estudios imagenológicos y de la epidemiologia.
REFERENCIAS
1. Ferlay J, Soerjomataram I, Dikshit R, Eser S, Mathers C, Rebelo M, et al. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer. 2015;136:E359-86. [ Links ]
2. Wallace MC, Preen D, Jeffrey GP, Adams LA. The Evolving epidemiology of hepatocellular carcinoma: a global perspective. Expert Rev Gastroenterol Hepatol. 2015;1:1-15. [ Links ]
3. Jemal A, Bray F, Center MM, et al. Global cancer statistics. CA Cancer J Clin. 2011;61:69. [ Links ]
4. Suzuki Y, Imai K, Takai K, et al. Hepatocellular carcinoma patients with increased oxidative stress levels are prone to recurrence after curative treatment: a prospective case series study using the d-ROM test. J Cancer Res Clin Oncol. 2013;139(5):845-52. [ Links ]
5. Yazici C, Niemeyer DJ, Iannitti DA, Russo MW. Hepatocellular carcinoma and cholangiocarcinoma: an update. Expert Review of Gastroenterology & Hepatology. 2014;8(1):63-82. [ Links ]
6. Suarez I, Uribe D, Jaramillo CM, Osorio G, Pérez JC, López R, et al. Wnt/β-catenin signaling pathway in hepatocellular carcinomas cases from Colombia. Ann Hepathol. 2015;14(1):54-64. [ Links ]
7. Kew MC. Aflatoxins as a cause of hepatocellular carcinoma. J Gastrointestin Liver Dis. 2013;22(3):305-10. [ Links ]
8. Navas MC, Suárez I, Carreño A, Uribe D, Ríos WA, Cortés-Mancera F, et al. Hepatitis B and hepatitis C infection biomarkers and TP53 mutations in hepatocellular carcinomas from Colombia. Hepat Res Treat. 2011;2011:582945. [ Links ]
9. Vilarinho S, Taddei T. Therapeutic strategies for hepatocellular carcinoma: new advances and challenges. Curr Treat Options Gastroenterol. 2015;13(2):219-34. [ Links ]
10. Deepali Jain. Tissue diagnosis of hepatocellular carcinoma. J Clin Exp Hepatol. 2014;4:S67-73. [ Links ]
11. Darnell A, Forner A, Rimola J, Reig M, García-Criado Á, Ayuso C, et al. Liver imaging reporting and data system with MR imaging: evaluation in nodules 20 mm or smaller detected in cirrhosis at screening US. Radiology. 2015;141132. [ Links ]
12. Wee A. Fine needle aspiration biopsy of hepatocellular carcinoma and hepatocellular nodular lesions: role, controversies and approach to diagnosis. Cytopathology. 2011;22(5):287-305. [ Links ]
13. Molla N, AlMenieir N, Simoneau E, Aljiffry M, Valenti D, Metrakos P, et al. The role of interventional radiology in the management of hepatocellular carcinoma. Current Oncology. 2014;21(3):480-92. [ Links ]
14. Wang P, Meng ZQ, Chen Z, et al. Diagnostic value and complications of fine needle aspiration for primary liver cancer and its influence on the treatment outcome. A study based on 3011 patients in China. Eur J Surg Oncol. 2008;34:541-6. [ Links ]
15. Stigliano R, Marelli L, Yu D, et al. Seeding following percutaneous diagnostic and therapeutic approaches for hepatocellular carcinoma. What is the risk and the outcome? Seeding risk for percutaneous approach of HCC. Cancer Treat Rev. 2007;33:437-47. [ Links ]
16. Kuo FY, Chen WJ, Lu SN, Wang JH, Eng HL. Fine needle aspiration cytodiagnosis of liver tumors. Acta Cytol. 2004;48(2):142-8. [ Links ]
17. Castro-Villabón D, Avello Y, Ruiz N, Rodríguez-Urrego PA. Implementation of routine thromboplastin-plasma cell block technique in the evaluation of non-gynecologic specimens: A methodologic comparison with conventional cytology. J Microscopy Ultrastructure. 2014;2(3):177-81. [ Links ]
18. Jain D. Tissue diagnosis of hepatocellular carcinoma. J Clin Exp Hepatol. 2014;4(Suppl 3):S67-73. [ Links ]
19. Compagnon P, Grandadam S, Lorho R, et al. Liver transplantation for hepatocellular carcinoma without preoperative tumor biopsy. Transplantation. 2008;86:1068-76. [ Links ]
20. International Consensus Group for Hepatocellular Neoplasia. International consensus on the pathologic diagnosis of early hepatocellular carcinoma: a report of the International Consensus Group for Hepatocellular Neoplasia. Hepatology. 2009;49:658-64. [ Links ]
21. Fuks D, Cauchy F, Fusco G, Paradis V, Durand F, Belghiti J. Preoperative tumour biopsy does not affect the oncologic course of patients with transplantable HCC. J Hepatol. 2014;61(3):589-93. [ Links ]
22. Barbhuiya M, Bhunia S, Kakkar M, Shrivastava B, Tiwari PK, Gupta S. Fine needle aspiration cytology of lesions of liver and gallbladder: An analysis of 400 consecutive aspirations. J Cytol. 2014;31(1):20-4. [ Links ]
23. Saleh HA, Aulicino M, Zaidi SY, Khan AZ, Masood S. Discriminating hepatocellular carcinoma from metastatic carcinoma on fine-needle aspiration biopsy of the liver: the utility of immunocytochemical panel. Diagn Cytopathol. 2009;37(3):184-90. [ Links ]
24. Goodman ZD. Neoplasms of the liver. Modern Pathology. 2007;20:S49-60. [ Links ]
25. Ferrell L. Liver pathology: cirrhosis, hepatitis, and primary liver tumors. Update and diagnostic problems. Mod Pathol. 2000;13(6):679-704. [ Links ]
26. Castro-Villabón D, Barrera-Herrera LE, Rodríguez-Urrego PA, Hudacko R, Vera A, Álvarez J, et al. Hepatocellular carcinoma with both fibrolamellar and classical components: an unusual morphological pattern. Case Rep Pathol. 2015;2015;609780. [ Links ]
27. Shafizadeh N, Kakar S. Diagnosis of well-differentiated hepatocellular lesions: role of immunohistochemistry and other ancillary techniques. Adv Anat Pathol. 2011;18:438-45. [ Links ]
28. Geller SA, Dhall D, Alsabeh R. Application of immunohistochemistry to liver and gastrointestinal neoplasms liver, stomach, colon, and pancreas. Arch Pathol Lab Med. 2008;132:490-9. [ Links ]
29. Krings G, Ramanchandran R, Jain D, Wu TT, Yeh MM, Torbenson M, et al. Immunohistochemical pitfalls and the importance of glypican 3 and arginase in the diagnosis of scirrhous hepatocellular carcinoma. Modern Pathology. 2013;26:782-91. [ Links ]
30. Kandil SK, Cooper K. Glypican-3: a novel diagnostic marker for hepatocellular carcinoma and more. Adv Anat Pathol. 2009;16:125-9. [ Links ]
31. Yan BC, Gong C, Song J, Krausz T, Tretiakova M, et al. Arginase-1: a new immunohistochemical marker of hepatocytes and hepatocellular neoplasms. Am J Surg Pathol. 2010;34(8):1147-54. [ Links ]
32. Lagana SM, Salomao M, Bao F, Moreira RK, Lefkowitch JH, Remotti HE. Utility of an immunohistochemical panel consisting of glypican-3, heat-shock protein-70, and glutamine synthetase in the distinction of low-grade hepatocellular carcinoma from hepatocellular adenoma. Appl Immunohistochem Mol Morphol. 2013;21(2):170-6. [ Links ]











 texto en
texto en