Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.30 supl.1 Bogotá Dec. 2015
Guía de práctica clínica para la prevención, diagnóstico y tratamiento del cáncer gástrico temprano - 2015
Clinical Practice Guideline for Diagnostics, Prevention and Management for early Gastric Cancer - 2015
Martín Alonso Gómez Zuleta MD1, Javier Humberto Riveros Vega MD2, Oscar Ruiz MD2, Alejandro Concha MD3, Diana María Ángel Betancur MD4, Marcela Torres Amaya QF5, Rodrigo Pardo MD6, William Otero R. MD7, Luis Sabbagh MD8
1 Profesor unidad de gastroenterología, Universidad Nacional de Colombia. Gastroenterólogo Hospital el Tunal y Hospital de Kennedy, UGEC (Unidad de Gastroenterología y Ecoendoscopia). Bogotá-Colombia.
2 Gastroenterólogo Hospital el Tunal y Hospital de Kennedy. Bogotá-Colombia.
3 Coordinador de Gastroenterología Salud SURA calle 100. Gastroenterólogo Fundación Clínica Shaio y Hospital de Kennedy. Bogotá-Colombia.
4 Médica pediatra Maestría en Epidemiología Clínica. Facultad de Medicina Universidad Nacional. Instituto de Investigaciones Clínicas. Universidad Nacional de Colombia. Bogotá-Colombia.
5 Gerente Editorial del Grupo Cochrane de Infecciones Transmisión Sexual. Bogotá-Colombia.
6 Médico internista, epidemiólogo. Director del Instituto de Investigaciones Clínicas, Universidad Nacional de Colombia. Bogotá-Colombia.
7 Profesor titular de medicina, Coordinador de Gastroenterología, Universidad Nacional de Colombia. Ex-presidente Asociación Colombiana de Gastroenterología, Ex-presidente Asociación Colombiana de Endoscopia Digestiva. Miembro honorario Sociedad Dominicana de Gastroenterología. Miembro Honorario Sociedad Venezolana de Endoscopia Digestiva, Gastroenterólogo, Clínica Fundadores. Bogotá, Colombia.
8 Presidente de la Organización Panamericana de Gastroenterología. Presidente de la Asociación Colombiana de Gastroenterología. Expresidente de la Asociación Colombiana de Endoscopia Digestiva. Director del Posgrado en Gastroenterología, Fundación Universitaria Sánitas. Bogotá-Colombia.
Resumen
Objetivo: proporcionar una guía de práctica clínica basada en la evidencia más reciente para la detección oportuna, diagnóstico y tratamiento del cáncer gástrico temprano teniendo en cuenta la eficacia y seguridad de las intervenciones dirigidas a pacientes, personal asistencial, administrativo y entes gubernamentales de cualquier servicio de atención en Colombia.
Materiales y métodos: esta guía fue desarrollada por un equipo multidisciplinario con apoyo de la Asociación Colombiana de Gastroenterología, el Grupo Cochrane ITS y el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia. Se desarrollaron preguntas clínicas relevantes y se realizó la búsqueda de guías nacionales e internacionales en bases de datos especializadas. Las guías existentes fueron evaluadas en términos de calidad y aplicabilidad; ninguna de ellas cumplió con el criterio de adaptación, por lo que se decidió construir una guía de novo. El Grupo Cochrane realizó la búsqueda sistemática de la literatura. Las tablas de evidencia y recomendaciones fueron realizadas con base en la metodología GRADE. Las recomendaciones de la guía fueron socializadas dentro del marco del VII curso de gastroenterología de la Policía Nacional que incluyó la presencia del Dr. K. Yao, y en una reunión de expertos con entes gubernamentales y pacientes.
Resultados: se desarrolló una guía de práctica clínica basada en la evidencia para la detección oportuna, diagnóstico y tratamiento del cáncer gástrico temprano en Colombia.
Conclusiones: la detección y el manejo oportuno de lesiones premalignas y malignas del cáncer gástrico temprano son estrategias que contribuyen a mejorar la incidencia, calidad de vida y desenlaces de la enfermedad.
Palabras clave
Guía de práctica clínica, neoplasias gástricas, cáncer gástrico.
Abstract
Objective: To provide an evidence-based clinical practice guideline for detection, diagnosis and treatment of early gastric cancer considering the efficacy and safety and interventions for patients, caregivers, administrative and government bodies at all levels of care in Colombia.
Materials and Methods: This guide was developed by a multidisciplinary team with the support of the Colombian Association of Gastroenterology, Cochrane STI Group and Clinical Research Institute of the Universidad Nacional de Colombia. Relevant clinical questions were developed and the search for national and international guidelines in databases was performed. Existing guidelines were evaluated quality and usability. None of the guidelines met criteria for adaptation, so the group decided to develop a de novo guideline. Systematic literature searches were conducted by Cochrane STI. The tables of evidence and recommendations were developed based on the GRADE approach.
Results: A Clinical Practice Guidelines for the detection, diagnosis and treatment of early gastric cancer was developed for the Colombian context.
Conclusions: The opportune detection and appropriate management of premalignant and malignant lesions of early gastric cancer would impact the burden of the disease.
Keywords
Clinical practice guidelines, stomach neoplasms, gastric cancer.
PROPÓSITO
El propósito de la presente guía es brindar al área de la salud la evidencia más reciente en cuanto a la efectividad y seguridad de las diferentes estrategias para prevención, detección temprana, estadificación, manejo endoscópico y seguimiento del cáncer gástrico temprano en cualquier servicio de atención del país. No fue incluido el manejo oncológico, quirúrgico y paliativo, como tampoco el cáncer de la unión gastroesofágica, cáncer gástrico hereditario, metástasis gástricas de tumores primarios localizados en otro órgano ni el cáncer gástrico avanzado. Las recomendaciones fueron realizadas para los servicios de atención primaria, secundaria y terciaria, así como para pacientes adultos, con dispepsia, mayores de 35 años, con antecedente familiar en primer grado de cáncer gastico, atrofia, metaplasia intestinal, displasia y cáncer gástrico temprano. Con el objetivo de disminuir la variabilidad en la práctica sobre el manejo del paciente con lesiones gástricas premalignas y malignas, esta guía está dirigida a todo el personal en salud asistencial y administrativo así como para aquellos que toman decisiones en salud, aseguradoras, pagadores del gasto en salud y a quienes generan políticas en salud; además, fue realizada con la evidencia más reciente, teniendo en cuenta la efectividad y seguridad de las diferentes intervenciones disponibles para la detección oportuna, diagnóstico y tratamiento del cáncer gástrico temprano.
INTRODUCCIÓN Y JUSTIFICACIÓN DE LA GUÍA
En el 2012, se presentaron 952000 casos nuevos de cáncer gástrico (CG) en el mundo, lo cual representa el quinto cáncer más frecuente después del cáncer de pulmón, cáncer de seno, y cáncer colorrectal y próstata; asimismo, se reportaron 738000 muertes, constituyendo la tercera causa de muerte por cáncer (1). Las tasas de incidencia de cáncer gástrico son de 2 a 3 veces mayores en los hombres que en las mujeres (2). En Colombia, es la primera causa de muerte por cáncer en hombres y la tercera en las mujeres (1); además, está entre los países con más alta tasa de incidencia (17,4 a 48,2 por 100000 habitantes), similar a la de Costa Rica, Chile, Japón, Corea y China. Teniendo en cuenta la alta incidencia de CG así como la mortalidad originada por el mismo, este tumor representa para el país un verdadero problema de salud pública (3, 4).
La mayoría de los canceres gástricos son esporádicos, pero aproximadamente el 10% tiene agrupación familiar y de estos, del 10% al 30% son hereditarios. Los de tipo intestinal son los más frecuentes en los sitios de alta prevalencia de CG, tienen mejor pronóstico y ocurren más a menudo en hombres, a partir de los 50 años, aunque en sitios de alta prevalencia aparece a menor edad (5, 6). Este tipo de CG aparece en estómagos que tienen gastritis atrófica y metaplasia intestinal, y el mayor número de casos ocurre en países de bajos ingresos (7). El CG de tipo intestinal tiene un largo período de inflamación crónica que precede la aparición del tumor, por lo cual es susceptible de ser intervenido tempranamente a través de la endoscopia digestiva alta, con el fin de detectarlo precozmente y así ofrecerle al paciente un tratamiento endoscópico o quirúrgico oportuno (8). Las tasas altas de supervivencia pueden deberse a la eficacia de los programas de tamización en países desarrollados como Estados Unidos y Japón (9).
Aunque el cáncer gástrico es una entidad multifactorial, se ha demostrado el papel decisivo de la infección por Helicobacter pylori (H. pylori), por lo que su detección y erradicación es importante tanto para la prevención y como para el manejo (10). El CG es un tumor que no tiene síntomas típicos o característicos que permitan una identificación temprana (11); en los estadios iniciales y ocasionalmente en estados avanzados, puede ser asintomático o tener como única manifestación dolor o malestar en el epigastrio, conformando el cuadro de dispepsia (11, 12). En estados avanzados se presenta dolor moderado en epigastrio, anemia, anorexia, pérdida de peso, sangrado, obstrucción gástrica (síndrome pilórico) y muy ocasionalmente, perforación. Al examen físico puede ser normal y en estados avanzados pueden encontrarse adenomegalias axilares (ganglio de Irish) o supraclavicular izquierda (ganglio de Virchow), y hepatomegalia o esplenomegalia (11). Los CG tempranos están localizados en la mucosa y submucosa, con o sin compromiso de nódulos linfáticos (12); en la estatificación TNM serían T1, independientemente de cualquier N. Este tipo de CG se trata endoscópicamente mediante mucosectomía o disección endoscópica de la submucosa, dependiendo del tamaño y las características morfológicas. Finalmente, el pronóstico depende de su detección en estados tempranos (11, 12). La falta de síntomas específicos puede llevar a un retraso en el diagnóstico debido a que aproximadamente el 80% de los pacientes son diagnosticados en etapas avanzadas, principalmente por ausencia programas de detección precoz (4, 12).
Teniendo en cuenta el gran impacto epidemiológico del cáncer gástrico no solo en Colombia sino mundial, así como la ausencia de guías de práctica clínica (GPC) en nuestro medio, resulta necesario el desarrollo de un documento que ayude al clínico a abordar de forma adecuada a los pacientes con cáncer gástrico temprano, y aumentar las tasas de sobrevida por esta enfermedad para llevarlas en Colombia a los niveles internacionales.
MATERIALES Y MÉTODOS
El grupo desarrollador de la guía (GDG) implementó una metodología rápida para la elaboración de esta guía. Para mayor información, la versión larga se encuentra en: http://www.gastrocol.com/. El GDG contó con la participación de expertos temáticos en gastroenterología, endoscopia, medicina interna, nutrición, química farmacéutica, salud pública y diseño de políticas, así como expertos epidemiólogos. Además, el GDG recibió apoyo por parte de la Asociación Colombiana de Gastroenterología, el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia y el Grupo Cochrane STI; este último realizó la búsqueda sistemática de la literatura y la consecución de los artículos de estudios primarios.
El GDG realizó una búsqueda sistemática de la literatura con el objeto de identificar todas las GPC nacionales e internacionales que abordarán el manejo de pacientes con cáncer gástrico temprano. La búsqueda se realizó en TRIP Database, Medline, EMBASE, Biblioteca Cochrane, Lilacs y literatura gris. Se evaluó la calidad de las GPC recuperadas con el instrumento AGREE II (13). Una vez se obtuvo la calidad global de cada una, se construyó una matriz de decisión que considera el tipo de guía, fecha de publicación, concordancia de los objetivos y alcance de la misma. Con base en los resultados de la matriz, se consideró que la guía sería desarrollada de novo.
Todas las preguntas a desarrollar se estructuraron en formato PICO (población, intervención, comparación y desenlaces). El primer paso fue la búsqueda metódica de revisiones sistemáticas publicadas de las bases de datos especializadas hasta mayo de 2015. Las revisiones sistemáticas (RS) identificadas fueron evaluadas con la herramienta AMSTAR (14) La síntesis de los estudios seleccionados se realizó a través de la construcción de los perfiles de evidencia en www.guidleinedevelopment.org y los niveles de evidencia fueron graduados según la clasificación GRADE (alta, moderada, baja y muy baja) (15).
NIVEL DE EVIDENCIA
Calidad Global de la evidencia GRADE
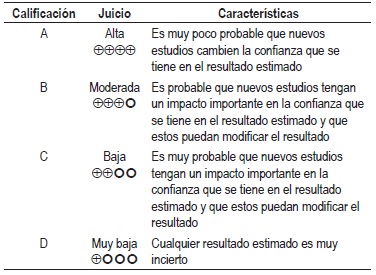
La graduación de la fuerza y dirección de cada recomendación se determinó con base en el nivel de evidencia y otras consideraciones adicionales que fueron revisadas en pleno por el GDG, el ente gestor y los grupos de interés. Este ejercicio se desarrolló mediante la construcción de una mesa de trabajo que generó la fuerza de la recomendación de acuerdo con:
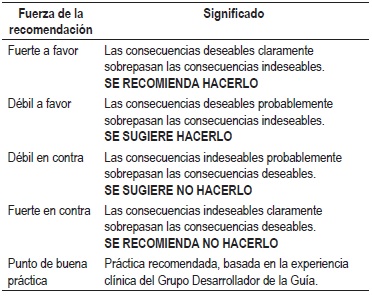
Las recomendaciones de la guía fueron socializadas dentro del marco del VII curso de gastroenterología de la Policía Nacional que incluyó la presencia del Dr. K. Yao, y en una reunión de expertos, entes gubernamentales y pacientes.
RECOMENDACIONES GENERALES
Pregunta 1: ¿cuáles son las indicaciones de la vigilancia endoscópica en Colombia?
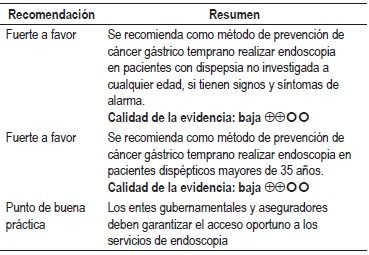
Una RS del 2014 evaluó la utilidad de la endoscopia como estrategia inicial en pacientes con dispepsia no investigada (DNE) en Asia. La revisión incluyó 18 estudios observacionales con 142802 pacientes adultos con DNE; entre aquellos con cáncer y síntomas dispépticos, el 17% (IC 95% con rango de 10,9 – 29,0) fueron menores de 45 años de edad y el 3,0% (IC 95% con rango de 2,5 – 3,5) fueron menores de 35. La edad >35 años tuvo una precisión diagnóstica para malignidad mejor que la edad >45 años (DOR = 9,41 vd DOR = 3,5, p >0,05). Los síntomas y signos de alarma tienen un poder muy limitado de predicción para la enfermedad orgánica: sensibilidad de 51,9%, IC 95% (50,4 – 53,4) y especificidad de 85,1%, IC 95% (84,9 – 85,3). Calidad de la evidencia: baja (16).
Pregunta 2: ¿cuál es la utilidad diagnóstica de los niveles de pepsinógeno para la predicción de lesiones gástricas precancerosas y cancerosas?
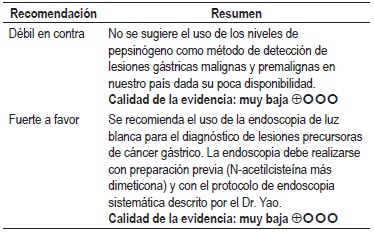
Una RS desarrollada para la Guía de Práctica Clínica de la Sociedad de Europea de Gastroenterología evaluó la utilidad de los niveles de pepsinógeno para predecir lesiones gástricas preneoplásicas y neoplásicas y se encontraron limitaciones en los estudios dado que la mayoría son provenientes del Japón, donde utilizan diferentes métodos de laboratorio, puntos de corte de los resultados y poblaciones diferentes, y concluyeron que los niveles bajos de pepsinógeno (PG) más que ser un valor, pueden predecir gastritis atrófica extensa (17). En Colombia, un estudio realizado por el Instituto Nacional de Cancerología en el 2010 cuyo objetivo era determinar los niveles de PG y su capacidad diagnóstica para la atrofia gástrica en diferentes poblaciones colombianas (mayores de 29 años de edad, 544 muestras) encontró que los niveles de PG difieren según la zona de riesgo de procedencia, edad, sexo, serología de H. pylori, localización gástrica de la atrofia, severidad de la atrofia y algunos estilos de vida como fumar. El PGI ≤86,68 y PGI/PGII ≤3,19 con un área bajo la curva de 0,76, identificó pacientes con atrofia severa multifocal, serología positiva para H. pylori y procedentes de zona de riesgo alto (Tunja, Bogotá), con sensibilidad de 77,5% y especificidad de 71,74%, por consiguiente, el beneficio de esta prueba estaría en la detección de lesiones avanzadas y no en lesiones tempranas (18). Calidad de la evidencia: muy baja.
Dentro del marco del VII curso de gastroenterología de la Policía Nacional, que incluyó la presencia del Dr. K. Yao, un consenso de expertos determinó que para Colombia la endoscopia debe realizarse con preparación previa y con el protocolo de endoscopia sistemática descrita por el Dr. Yao (19).
Pregunta 3: ¿cuál es la exactitud diagnóstica de los diferentes métodos endoscópicos para la detección temprana de lesiones gástricas premalignas y malignas?
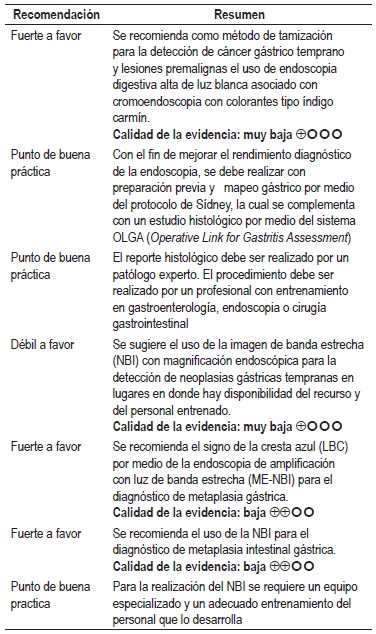
Una RS del 2015 evaluó la exactitud diagnóstica de la imagen convencional de luz blanca (4 estudios, 434 pacientes, 528 lesiones) y encontró una sensibilidad de 48% (IC 95% con rango de 39–57), especificidad de 67% (IC 95% con rango de 62–71) y RR diagnóstico 2,10 (IC 95%, con rango de 0,53–8,39) para detectar cáncer gástrico temprano (18). Una revisión realizada por la GPC de la Sociedad Europea de Gastroenterología identificó 3 estudios vinculados con el uso de la cromoendoscopia para ayudar a identificar las lesiones con metaplasia intestinal y displasia, y encontró que su uso puede ser reproducible y preciso, aunque prolonga el tiempo del procedimiento endoscópico, carga laboral y puede tener eventos adversos en relación con la tolerancia y sedación de los pacientes, por lo que recomiendan realizarlo en centros con experiencia (20). En Colombia, se realizó un estudio para la evaluar la utilidad de la cromoendoscopia sistemática y toma de muestras de lesiones sospechosas en la prevalencia de cáncer gástrico temprano y lesiones premalignas con un análisis histológico de las lesiones. En relación con las lesiones gástricas premalignas (LGP), se observó atrofia no metaplásica y metaplásica en el 14,5% (94/650) y 15,5% (101/650) respectivamente; la prevalencia total de LGP fue de 30% (195/650), diagnosticadas por histología. Aunque no se realizó un análisis de costo/efectividad, los autores estimaron disminución en los gastos por el hecho de haber diagnosticado 2 lesiones en estado 0 en 650 voluntarios y haber realizado mucosectomía curativa, evitándose la cirugía convencional (21). Calidad de la evidencia: muy baja.
Una RS del 2014 evaluó la exactitud diagnóstica de la magnificación endoscópica con imagen de banda estrecha (ME-NBI) para la detección de neoplasia gástrica en población adulta (8 estudios, 2151 lesiones) y encontró que tuvo un buen desempeño al momento de detectar lesiones neoplásicas gástricas con una sensibilidad de 85% (IC 95%, 81%–89%), especificidad de 96% (IC 95%, 95%–97%) y RR diagnóstico de 106,25 (IC 95%, 47,03–240,01). Cuando se evaluó la capacidad diagnostica de la ME-NBI versus la imagen convencional de luz blanca (WLI) se encontró que presentó un buen desempeño y capacidad discriminativa para la detección de neoplasias gástricas (22). Otra RS del 2014 evaluó la exactitud diagnóstica de signo de la cresta azul (LBC) por medio de la ME-NBI para la detección de metaplasia intestinal gástrica (4 estudios, 949 muestras de 285 pacientes) y se encontró una sensibilidad de 86% (IC 95% con rango de 83-89) y especificidad de 88% (IC 95% con rango de 84–91) (23). Otra RS del 2014 evaluó la exactitud diagnóstica de la NBI para la detección de metaplasia intestinal gástrica (347 sujetos, 887 lesiones, 6 estudios) y encontró una sensibilidad de 65% (IC 95%, con rango de 56–74), especificidad de 93% (IC 95%, con rango de 88–97) y RR diagnóstico de 28,06 (IC 95% con rango de 12,02–65,55); este desempeño mejoró al realizar la ME-NBI presentando una sensibilidad de 76% (IC 95% con rango de 61–87) (24). Calidad de la evidencia: baja.
Pregunta 4: ¿cuál es la eficacia y seguridad del tratamiento para la erradicación del Helicobacter pylori en la prevención de lesiones gástricas malignas y premalignas?
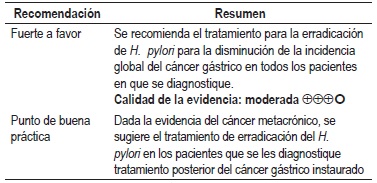
Una RS del 2015 evaluó la eficacia del tratamiento de erradicación de H. pylori en la disminución de la incidencia de cáncer gástrico en pacientes adultos (7953 participantes) con lesiones iguales o mayores, y menores a metaplasia intestinal. El tratamiento para la erradicación del H. pylori redujo la incidencia total de cáncer gástrico con RR 0,70 (IC 95% con rango de 0,49 a 0,99), cáncer gástrico metacrónico con RR 0,52 (IC 95% con rango de 0,31 a 0,87), atrofia con RR 0,25 (IC 95% con rango de 0,08 a 0,81), y progresión histológica de la atrofia gástrica con RR 0,82 (IC 95% con rango de 0,68 a 0,99). No se observó efecto en la ya instaurada metaplasia intestinal, progresión histológica por MI, progresión histológica por puntaje ≥ MI ni progresión histológica por step < MI (p >0,05) (25). Otra RS del 2014 encontró disminución de la ocurrencia de cáncer gástrico con esta intervención con RR 0,66 (IC 95% con rango de 0,46 a 0,95) (26). Una RS Cochrane (6 ensayos clínicos aleatorizados [ECA] con 6497 participantes) también encontró una reducción en cáncer gástrico con el tratamiento para H. pylori (RR: 0,66, IC 9% 0,46-0,95). No se encontró efecto en la mortalidad (p >0,05) (27). Calidad de la evidencia: moderada.
Pregunta 5: ¿cuál es la exactitud diagnóstica de la ecoendoscopia para la estadificación locorregional preoperatoria del cáncer gástrico?
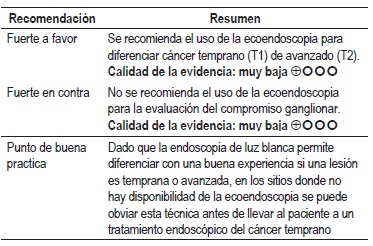
Una RS Cochrane del 2015 evaluó la exactitud diagnóstica de la ecoendoscopia para la estadificación locorregional del cáncer gástrico primario temprano con 7747 pacientes, encontrando un buen desempeño al momento de discriminar el cáncer gástrico en T1 - T2 (superficial) versus T3 - T4 (avanzado). Se reportó una sensibilidad de 86% (IC 95% con rango de 81-90), especificidad de 90% (IC 95% con rango de 87-93) y RR de 56 (IC 95% con rango de 37 a 85). Adicionalmente, al diferenciar las estadificaciones tempranas de la enfermedad (T1 cáncer gástrico temprano versus T2 infiltración muscular) se encontró una sensibilidad de 85% (IC 95% con rango de 78-91) y especificidad de 90% (IC 95% con rango de 85-93). Se reportó menor desempeño para distinguir cánceres T1a (mucosa) versus T1b (submucosa) y para evaluar el compromiso ganglionar, con una sensibilidad de 83% (IC 95% con rango de 79-87), especificidad de 67% (IC 95% con rango de 61-72) (28). Calidad de la evidencia: muy baja.
Pregunta 6: ¿cuál es la intervención endoscópica más efectiva y segura para el tratamiento del cáncer gástrico temprano?
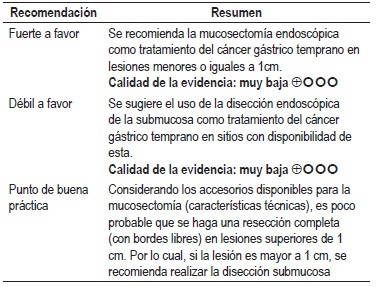
Una RS del 2014 evaluó la seguridad y efectividad de la disección endoscópica de la submucosa (DES) comparada con la resección de mucosa endoscópica (REM o mucosectomía) para el tratamiento de cáncer gástrico temprano (10 estudios de casos y controles de 4328 lesiones) y encontró que la DES consumió mayor tiempo quirúrgico con SMD 1,73 (IC 95% con rango de 0,52-2,95), presentó mayor tasa de resección en bloque con RR 9,69 (IC 95% con rango de 7,74-12,13), mayor resección histológica completa con OR 5,66 (IC 95% con rango de 2,92 a 10,96) y perforación luego del procedimiento con OR 4,67 (IC 95% con rango de 2,77-7,87); sin embargo, presentó menor recurrencia de la lesión con OR 0,09 (IC 95% con rango de 0,05-0,17). No se reportaron diferencias en la tasa de sangrado (29). En Colombia se realizó un estudio con 11 pacientes con tratamiento con mucosectomía para cáncer gástrico temprano y se realizó seguimiento y vigilancia endoscópica durante 5 años, no se evidenció recaída de la lesión (30). Calidad de la evidencia: muy baja.
Pregunta 7: ¿cuál debe ser el seguimiento endoscópico en los pacientes adultos con lesiones gástricas premalignas o malignas?

Se ha reportado una progresión rápida anual en la tasa de displasia severa (o de alto grado) a cáncer gástrico, con una incidencia anual de cáncer gástrico de 0,6% para displasia leve a moderada y del 1,4% a 6% para displasia severa en un seguimiento de 5 años. En el mismo estudio se encontró que la tasa de progresión a cáncer gástrico de pacientes con gastritis atrófica y metaplasia intestinal varía entre 0% a 1,8 % y 0% a 10% por año, respectivamente; deben identificarse factores de riesgo adicionales para su seguimiento (distribución intragástrica y extensión de la metaplasia) (31). Expertos recomiendan el seguimiento de los pacientes tratados por cáncer gástrico en donde pueda realizarse una endoscopia cada 3 a 6 meses por 1 a 2 años, luego cada 6 a 12 meses por 3 a 5 años, y finalmente cada año (30). Calidad de la evidencia: muy baja.
ALGORITMO 1.
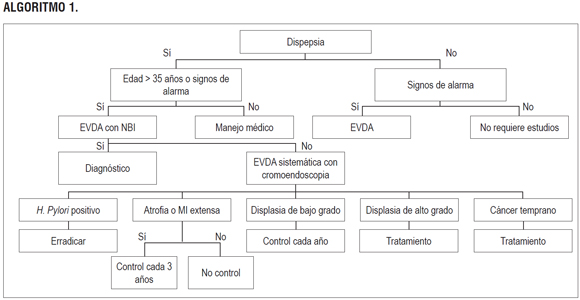
ALGORITMO 2.
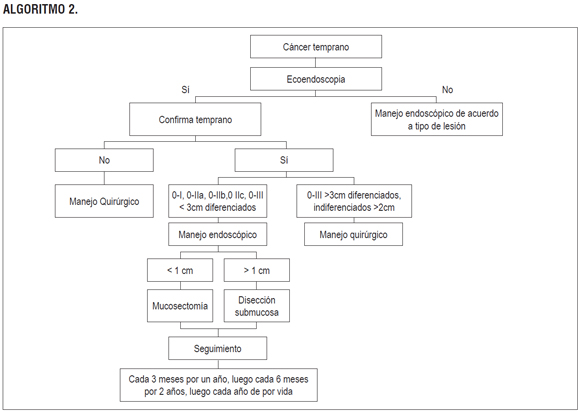
DECLARACIÓN DE CONFLICTOS DE INTERÉS
Los autores declaran no tener conflictos de interés, no estar involucrados como investigadores en ensayos clínicos en curso sobre el tema, y no haber recibido donaciones o beneficios por parte de los grupos interesados en las recomendaciones.
FUENTE DE FINANCIACIÓN
La presente guía fue desarrollada mediante un convenio de extensión entre la Asociación Colombiana de Gastroenterología y la facultad de Medicina de la Universidad Nacional.
REFERENCIAS
1. Ferlay J, Soerjomataram I, Ervik M, Shin HR, Bray F, Forman D, Mathers C, Parkin DM. Estimates of worldwide burden of cancer in 2012: GLOBOCAN 2012. Int J Cancer. 2010 Dec 15;127(12):2893-917. PubMed PMID: 21351269. [ Links ]
2. Karimi P, Islami F, Anandasabapathy S, Freedman ND, Kamangar F. Gastric cancer: Descriptive epidemiology, risk factors, screening, and prevention. Cancer Epidemiol Biomarkers Prev. 2014 May;23(5):700-13. [ Links ]
3. Otero W, Gomez M, Castro D. Carcinogénesis Gástrica. Rev Col Gastroenterol 2009; 24:314-28. [ Links ]
4. González CA, Sala N, Rokkas T. Gastric cancer: Epidemiologic aspects. Helicobacter. 2013 Sep;18 Suppl 1:34-8. [ Links ]
5. Correa P. Gastric Cancer: Overview. Gastroenterol Clin N. 2013 6//;42(2):211-7. [ Links ]
6. Correa P, Chen VW. Gastric cancer. Cancer surveys. 1994;19-20:55-76. PubMed PMID: 7534641. [ Links ]
7. Zuleta G, Otero R, Ruiz L. Factores de riesgo para cáncer gástrico en pacientes colombianos. Rev Col Gastroenterol. 2009;24:134-43. [ Links ]
8. Chen J, Cheong JH, Yun MJ, Kim J, Lim JS, Hyung WJ, et al. Improvement in preoperative staging of gastric adenocarcinoma with positron emission tomography. Cancer. 2005 Jun 1;103(11):2383-90. [ Links ]
9. Isobe Y, Nashimoto A, Akazawa K, Oda I, Hayashi K, Miyashiro I, et al. Gastric cancer treatment in Japan: 2008 annual report of the JGCA nationwide registry. Gastric Cancer 2011; Oct;14(4):301-16. [ Links ]
10. González CA1, Agudo A. Carcinogenesis, prevention and early detection of gastric cancer: Where we are and where we should go. Int J Cancer. 2012 Feb 15;130(4):745-53. [ Links ]
11. Mostacero Tapia S, Ferrández Á. Cáncer gástrico. Medicine-Programa de Formación Médica Continuada acreditado. 2012;11(3):149-57. [ Links ]
12. Venerito M, Nardone G, Selgrad M, Rokkas T, Malfertheiner P. Gastric cancer-epidemiologic and clinical aspects. Helicobacter. 2014 Sep;19 Suppl 1:32-7. [ Links ]
13. AGREE C. INSTRUMENTO AGREE II. Instrumento para la evaluación de guías de práctica clínica [en línea] GuíaSalud. 2009. [acceso, mayo de 2015] [ Links ].
14. Shea BJ, Grimshaw JM, Wells GA, Boers M, Andersson N, Hamel C, et al. Development of AMSTAR: A measurement tool to assess the methodological quality of systematic reviews. BMC Med Res Methodol. 2007;7(1):10. [ Links ]
15. Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, et al. GRADE: An emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 2008;336(7650):924-6. [ Links ]
16. Chen SL, Gwee KA, Lee JS, Miwa H, Suzuki H, Guo P, Hao YT, Chen MH. Systematic review with meta-analysis: prompt endoscopy as the initial management strategy for uninvestigated dyspepsia in Asia. Aliment Pharmacol Ther. 2015 Feb;41(3):239-52. [ Links ]
17. Dinis-Ribeiro, M Areia, A C de Vries, R. Marcos-Pinto M Monteiro-Soares, A OConnor, et al Management of precancerous conditions and lesions in the stomach (MAPS): Guideline from the European Society of Gastrointestinal Endoscopy (ESGE), European Helicobacter Study Group (EHSG), European Society of Pathology (ESP), and the Sociedad Portuguesa de Endoscopia Digestiva (SPED). Endoscopy. 2012; 44: 74–94. [ Links ]
18. Martínez T, Bravo M, Núnez D, Hernández G y Camorlingac M. Niveles séricos de pepsinógeno y su capacidad diagnóstica de atrofia gástrica en diferentes poblaciones colombianas. Rev Colomb Cancerol. 2014;18(4):166-178. [ Links ]
19. Yao K. The endoscopic diagnosis of early gastric cancer. Ann Gastroenterol. 2013; 26 (1): 11-22. [ Links ]
20. Zhang Q,Wang F,Chen ZY, Wang Z, Fa-Chao Z, Si-De L, Bai Y. Comparison of the diagnostic efficacy of white light endoscopy and magnifying endoscopy with narrow band imaging for early gastric cancer: A meta-analysis. Gastric Cancer. 2015 Apr 29 DOI 10.1007/s10120-015-0500-5. [ Links ]
21. Emura F, Mejía J, Mejía M, Osorio C, Hernández C, González I, Malaver O, Rodríguez C, Oda I, Correa P. Utilidad de la cromoendoscopia sistemática en el diagnóstico del cáncer temprano y lesiones gástricas premalignas. Resultado de dos campañas masivas consecutivas de tamización en Colombia (2006-2007). Rev Col Gastroenterol. 2010 ; 25 (1):18-28. [ Links ]
22. Lv X, Wang C, Xie Y, Yan Z. Diagnostic Efficacy of Magnifying Endoscopy with Narrow-Band Imaging for Gastric Neoplasms: A Meta-Analysis. DOI:10.1371/journal.pone.0123832 April 9, 2015 [ Links ]
23. Wang L., Huang W., Du J, Chen J,Yang J. Diagnostic Yield of the Light Blue Crest Sign in Gastric Intestinal Metaplasia: A Meta-Analysis. March 2014.Volume 9.Issue 3.e92874. PLOS ONE .www.plosone.org. [acceso, mayo de 2015] [ Links ].
24. Song J, Zhang J,Wang J, Guo X, Wang J,Liu Y, Dong W. Meta-Analysis: Narrow Band Imaging for Diagnosis of Gastric Intestinal Metaplasia. PLOS ONE. www.plosone.org April 2014, Volume 9, Issue 4, e94869 .[acceso, mayo de 2015] [ Links ].
25. Chen HN, Xiao Z, Zhou L. Helicobacter pylori eradication cannot reduce the risk of gastric cancer in patients with intestinal metaplasia and dysplasia: Evidence from a meta-analysis Gastric Cancer. 2015 DOI 10.1007/s10120-015-0462-7. [ Links ]
26. Ford A, Forman D, Hunt R, Yuan Y, Moayyedi P. Helicobacter pylori eradication therapy to prevent gastric cancer in healthy asymptomatic infected individuals: Systematic review and meta-analysis of randomized controlled trials. BMJ. 2014;348:g3174. [ Links ]
27. Ford A, Forman D, Hunt R, Yuan Y, Moayyedi P. Helicobacter pylori eradication for the prevention of gastric neoplasia. Cochrane 2015. DOI: 10.1002/14651858.CD005583.pub2 [ Links ]
28. Mocellin S, Pasquali S. Diagnostic accuracy of endoscopic ultrasonography (EUS) for the preoperative locoregional staging of primary gastric cancer. Cochrane Database of Systematic Reviews 2015, Issue 2. Art. No.: CD009944. [ Links ]
29. Facciorusso A, Antonino M, Di Maso M, Muscatiello N. Endoscopic submucosal dissection versus endoscopic mucosal resection for early gastric cancer: A meta-analysis World J Gastrointest Endosc. 2014 November 16; 6(11): 555-563. [ Links ]
30. Gómez M, Otero W, Arbeláez V. Tratamiento endoscópico de cáncer gástrico temprano en Colombia con seguimiento a cinco años. Rev Col Gastroenterol. 2009. 24 (4)347-352. [ Links ]
31. The National Comprehensive Cancer Network guidelines [pagina web] NCCN Clinical Practice Guidelines in oncology Gastric cancer. NCCN Guidelines [actualizada el 23 de marzo 2015 bajada el 26 junio 2015]. Disponible en http://www.nccn.org/professionals/physician_gls/pdf/gastric.pdf [ Links ]
32. Ono H, Yao K, Fujishiro M, Oda I, Nimura S, Yahagi N, Iishi H, Oka M, Ajioka Y, Ichinose M, Matsui T. Guidelines for ESD and EMR for Early Gastric Cancer. Dig Endosc. 2015 Aug 1. doi: 10.1111/den.12518. [Epub ahead of print] [ Links ].













