Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.30 supl.1 Bogotá Dec. 2015
Guía de práctica clínica para el diagnóstico y tratamiento del síndrome de intestino irritable en población adulta
Clinical Practice Guideline for the Diagnosis and Management of Adult Patients with Irritable Bowel Syndrome
Jaime Alvarado B. MD1, William Otero R. MD2, Mario Andrés Jaramillo Santos MD3, Paola Andrea Roa B. MD4, Gerardo Andrés Puentes L., MD5, Ana María Jiménez F., MD6, Carlos Fernando Grillo A., MD7, Rodrigo Pardo MD8, Luis Sabbagh MD.9
1 Especialista en medicina interna, especialista en gastroenterología. Profesor titular, Pontificia Universidad Javeriana, Bogotá-Colombia.
2 Profesor titular de medicina, Coordinador de Gastroenterología, Universidad Nacional de Colombia. Ex-presidente Asociación Colombiana de Gastroenterología, Ex-presidente Asociación Colombiana de Endoscopia Digestiva. Miembro honorario Sociedad Dominicana de Gastroenterología. Miembro Honorario Sociedad Venezolana de Endoscopia Digestiva, Gastroenterólogo, Clínica Fundadores.
3 Médico internista Universidad Nacional de Colombia. Fellow de Gastroenterologia, Universidad Nacional de Colombia. Hospital El Tunal. Bogotá-Colombia.
4 Especialista en medicina interna, especialista en gastroenterología. Profesora Ad Honorem Pontificia Universidad Javeriana, Bogotá-Colombia.
5 Especialista en medicina interna, fellowship de gastroenterología y endoscopia, Pontificia Universidad Javeriana, Bogotá-Colombia.
6 Especialista en pediatría, candidata a magíster en epidemiología clínica, Pontificia Universidad Javeriana, Bogotá-Colombia.
7 Médico cirujano, especialista en obstetricia y ginecología, magíster en epidemiología clínica. Profesor departamento de ginecología y obstetricia, Instituto de Investigaciones Clínicas, Universidad Nacional de Colombia, Bogotá-Colombia.
8 Médico internista, epidemiólogo, director del Instituto de Investigaciones Clínicas Universidad Nacional de Colombia. Bogotá-Colombia.
9 Presidente de la Organización Panamericana de Gastroenterología, presidente de la Asociación Colombiana de Gastroenterología, expresidente de la Asociación Colombiana de Endoscopia Digestiva, director del posgrado en Gastroenterología, Fundación Universitaria Sánitas. Bogotá-Colombia.
Contacto: William Otero watoteror@gmail.com
Resumen
Objetivo: diseñar una guía de práctica clínica para disminuir la variabilidad injustificada en el diagnóstico y tratamiento de los pacientes mayores de 18 años con síndrome de intestino irritable en Colombia mediante un diagnóstico orientado y unas pautas terapéuticas establecidas.
Materiales y métodos: el equipo multidisciplinario que conformó el presente Grupo Desarrollador contó con apoyo de la Asociación Colombiana de Gastroenterología, el Grupo Cochrane ITS y el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia. Se desarrollaron preguntas clínicas relevantes y se realizó la búsqueda de guías nacionales e internacionales en bases de datos especializadas. Las guías existentes fueron evaluadas en términos de calidad y aplicabilidad; ninguna de ellas cumplió el criterio de adaptación, por lo que se decidió desarrollar una guía de novo. El Grupo Cochrane realizó la búsqueda sistemática de la literatura. Las tablas de evidencia y recomendaciones fueron realizadas usando la metodología GRADE.
Resultados: se desarrolló una guía de práctica clínica basada en la evidencia para el diagnóstico y tratamiento farmacológico de los pacientes mayores de 18 años con síndrome de intestino irritable en Colombia.
Conclusiones: se establecieron los criterios clínicos y signos de alarma, las pruebas diagnósticas y las aproximaciones terapéuticas de acuerdo con el síntoma predominante en los pacientes con síndrome de intestino irritable en Colombia.
Palabras clave
Síndrome del colon irritable, diagnóstico, terapéutica, guía de práctica clínica.
Abstract
Objective: To design a clinical practice guideline to reduce unwarranted variation in the diagnosis and treatment of patients over 18 years old with irritable bowel syndrome in Colombia through targeted diagnosis and a treatment guidelines established.
Materials and Methods: This guide was developed by a multidisciplinary team with the support of the Colombian Association of Gastroenterology, Cochrane STI Group and Clinical Research Institute of the Universidad Nacional de Colombia. Relevant clinical questions were developed and the search for national and international guidelines in databases was performed. Existing guidelines were evaluated quality and applicability. No guideline met the criteria for adaptation, so the group decided to develop the guideline de novo. Systematic literature searches were conducted by the Cochrane Group. The tables of evidence and recommendations were made based on the GRADE methodology.
Results: An evidence-based Clinical Practice Guidelines for the diagnosis and treatment of irritable bowel syndrome in patients over 18 years old was developed for the Colombian context.
Conclusions: the clinical criteria and warning signs, diagnostic tests and therapeutic approaches were established in accordance with the predominant symptom in patients with irritable bowel syndrome in Colombia.
Keywords
Irritable bowel syndrome, diagnosis, therapy, clinical practice guideline.
PROPÓSITO Y ALCANCE
Esta guía de práctica clínica (GPC) está dirigida a los profesionales de la salud que atienden directamente a los pacientes con síndrome de intestino irritable (SII) con el propósito de disminuir la variabilidad injustificada en el diagnóstico y tratamiento mediante la generación de recomendaciones basadas en la mejor evidencia disponible en los aspectos de diagnóstico y tratamiento de los pacientes con este síndrome. Su enfoque está dirigido hacia aspectos relacionados con el diagnóstico, tratamiento farmacológico y no farmacológico. La población objetivo son pacientes mayores de 18 años con diagnóstico de SII, no incluyendo dentro del alcance de la presente guía pacientes con patología tumoral del tracto gastrointestinal, enfermedad inflamatoria intestinal, colitis infecciosa, enfermedad celíaca, pacientes que presenten eventos adversos al tratamiento del SII, y gestantes o pacientes en lactancia.
La guía brinda recomendaciones en aspectos de diagnóstico y tratamiento que buscan apoyar al personal de salud que atiende pacientes mayores de 18 años con diagnóstico de estreñimiento crónico funcional en todos los servicios de atención, independientemente de su vinculación al Sistema General de Salud.
INTRODUCCIÓN
El síndrome de intestino irritable (SII) es una entidad que afecta al 11% de la población, siendo una entidad funcional, compleja, crónica, recurrente, que puede persistir toda la vida (1, 2). Tiene diversas manifestaciones clínicas, dificultando su diagnóstico y su tratamiento, junto a una insatisfacción por parte de los pacientes frente al tratamiento recibido y un incumplimiento de las recomendaciones internacionales por los profesionales en la práctica cotidiana (1, 2). Se caracteriza por dolor o malestar abdominal asociados con alteración de la frecuencia y/o de la forma de deposiciones dando estreñimiento, diarrea o ambas con ausencia de alteraciones estructurales evidentes (1, 2).
Al ser una entidad con sintomatología variable, esta patología representa una importante carga para los sistemas en salud representando más del 30% de las consultas de gastroenterología, el 12% de la población que asiste a cuidado primario (3). En cuanto a costos, en Estados Unidos el SII presenta gastos superiores a los 33 billones de dólares al año, de los cuales 8 billones corresponden a gastos directos (4). Adicionalmente, esta patología genera errores de diagnóstico haciendo que estos pacientes sean operados casi 2 veces más de apendicectomía, histerectomía y colecistectomía, y 50% más de cirugías de la columna vertebral (5, 6), con una severa alteración en la calidad de vida y múltiples ausencias laborales (7, 8) reflejadas en la pérdida de más de 10 horas semanales de trabajo por incapacidades y menor desempeño (9).
El diagnóstico del SII está basado en síntomas, los cuales se interpretan "en paralelo" de acuerdo con los criterios para el diagnóstico (2), ya que hasta el momento no hay marcadores biológicos ni exámenes paraclínicos específicos para confirmarlo (2, 10). Las opciones de tratamiento son variadas e incluyen diferentes enfoques terapéuticos, con el desconocimiento de cuál de todas ellas es efectiva para las variedades sintomáticas que presenta esta enfermedad.
Al tener en cuenta lo anterior, se decidió realizar esta guía de práctica clínica con el propósito de disminuir la variabilidad injustificada en las etapas de diagnóstico y tratamiento, contribuyendo al uso racional y pertinente de recursos destinados al cuidado de los pacientes con síndrome de intestino irritable.
METODOLOGÍA
El grupo desarrollador de la guía (GDG) diseñó una metodología rápida para la elaboración de esta guía. Para mayor información, la versión larga de la guía se encuentra en: http://www.gastrocol.com/. El GDG contó con la participación de expertos que incluyeron las áreas de gastroenterología, medicina interna, coloproctología y epidemiología clínica, los cuales declararon no tener conflictos de interés frente a las intervenciones evaluadas en esta guía. El GDG recibió apoyo por parte de la Asociación Colombiana de Gastroenterología, el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia y el Grupo Cochrane STI; este último realizó la búsqueda sistemática de la literatura y la consecución de los artículos de estudios primarios.
El GDG realizó una búsqueda sistemática de la literatura con el objeto de detectar todas las GPC nacionales e internacionales que abordaran el manejo de pacientes con síndrome de intestino irritable. La búsqueda se realizó en TRIP database, Medline, EMBASE, Biblioteca Cochrane, LILACS y agencias especializadas. Se evaluó la calidad de las GPC recuperadas con el instrumento AGREE II (11). Una vez se obtuvo la calidad global de cada guía, se construyó una matriz de decisión que considera el tipo de guía, fecha de publicación, concordancia de los objetivos y alcance de la GPC. Con base en los resultados de la matriz de decisión se consideró que la guía sería desarrollada de novo.
Todas las preguntas a desarrollar se estructuraron en formato PICO (población, intervención, comparación y desenlaces). El primer paso fue la búsqueda metódica de revisiones sistemáticas publicadas de las bases de datos especializadas hasta mayo de 2015. Las revisiones sistemáticas (RS) identificadas fueron evaluadas con la herramienta AMSTAR (12). La síntesis de los estudios seleccionados se realizó a través de la construcción de los perfiles de evidencia en www.guidleinedevelopment.org y los niveles de evidencia fueron graduados según la clasificación GRADE (alta, moderada, baja y muy baja) (13, 14).
NIVEL DE EVIDENCIA
Calidad Global de la evidencia GRADE
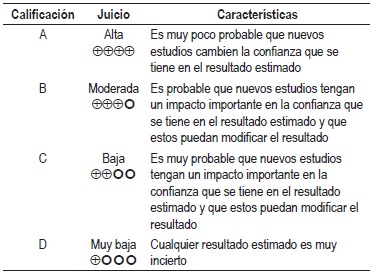
La graduación de la fuerza y dirección de cada recomendación se determinó con base en el nivel de evidencia y otras consideraciones adicionales que fueron revisadas en pleno por el GDG, el ente gestor y los grupos de interés. Este ejercicio se desarrolló mediante la construcción de una mesa de trabajo que generó la fuerza de la recomendación de acuerdo con:
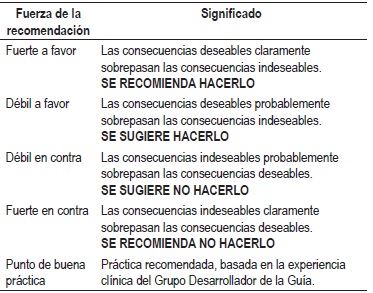
Las recomendaciones de la guía fueron socializadas en una reunión de expertos, entes gubernamentales y pacientes.
RECOMENDACIONES GENERALES
Diagnóstico
Pregunta 1: ¿cuáles son los signos y síntomas que hacen sospechar la presencia de síndrome de intestino irritable en población adulta?

Una RS de la literatura evaluó la exactitud diagnóstica de la historia clínica y el examen físico para establecer el diagnóstico de SII y descartar patología orgánica en pacientes con síntomas abdominales bajos usando como patrón de oro la combinación de enema de bario, colonoscopia y tomografía axial computarizada. La revisión encontró que los signos y síntomas sugestivos de SII poseen un discreto desempeño para confirmar la presencia de la enfermedad descartando patología orgánica. Calidad de la evidencia: muy baja (15).
Pregunta 2: ¿cuál es la exactitud de los criterios clínicos basados en síntomas para el diagnóstico del síndrome de intestino irritable en población adulta?

Criterios diagnósticos: una RS evaluó la exactitud diagnóstica de los criterios basados en síntomas para establecer el pronóstico del SII en pacientes mayores de 18 años con síntomas abdominales mayores de 2 semanas, usando como patrón de oro el seguimiento clínico por más de 1 año. La revisión reportó un discreto desempeño operativo de las clasificaciones evaluadas (Bellentani, Kruis, Manning, Mazumdar, Talley, Wasson, Roma I y Roma II). Calidad de la evidencia: muy baja (16).
Criterios de Roma III: un estudio de pruebas diagnósticas evaluó la exactitud de los criterios de Roma III en población adulta con sintomatología gastrointestinal no aguda usando como patrón de oro la colonoscopia con o sin biopsia. El estudio encontró un moderado desempeño de los criterios para descartar patología orgánica gastrointestinal (sensibilidad de 68%, IC 95% con rango de 63% a 73%, especificidad de 79%, IC 95% con rango de 77% a 81%, LR+ de 3,35, IC 95% con rango de 2,97 a 3,79, LR negativo de 0,39, IC 95% con rango de 0,34 a 0,46). Calidad de la evidencia: moderada (17).
Pregunta 3: ¿cuál es la utilidad de realizar estudios complementarios para confirmar el diagnóstico de síndrome de intestino irritable en población adulta?

Una RS de la literatura evaluó la prevalencia de la patología orgánica en pacientes con diagnóstico de SII en quienes realizaron paraclínicos, imágenes o cualquier otra ayuda diagnóstica de forma rutinaria. Calidad de la evidencia: muy baja (18).
- Hemograma y química sanguínea: la revisión encontró que el hemograma no modificó el diagnóstico final o la conducta, junto con una prevalencia del 1% de alteración hepática y 6% de la función tiroidea
- Estudios de materia fecal: la revisión encontró una prevalencia del 1,7% de colonización por Blastocystis hominis y otro estudio reportó la ausencia de alteraciones
- Ecografía abdominal: la revisión encontró un estudio que reportó una prevalencia del 20% en mujeres y 8% en hombres en hallazgos anormales, sin modificación del diagnóstico o tratamiento de estos
- Colonoscopia, sigmoidoscopia o enema de bario: la revisión encontró 4 estudios observacionales con prevalencia de anormalidades entre el 0% al 1,3%
- Biopsia rectal: la revisión reportó una prevalencia de 0 patologías orgánicas en el estudio que evaluó esta prueba.
Prueba de aliento: una RS evaluó el desempeño de la prueba de aliento para confirmar el diagnóstico de SII en población adulta usando como patrones de oro el diagnóstico previo de trastorno intestinal funcional, el diagnóstico clínico de exclusión o el uso de los criterios de Roma I-II-III. La revisión reportó que esta prueba posee un pobre desempeño para confirmar SII (sensibilidad 39%, especificidad 84%), siendo estos hallazgos consistentes en el análisis de subgrupos realizado por el tipo de sustrato utilizado. Calidad de la evidencia: muy baja (19).
Pregunta 4: ¿cuál es la utilidad diagnóstica de los paraclínicos utilizados para descartar la presencia de enfermedad inflamatoria intestinal en pacientes con síntomas sugestivos de síndrome de intestino irritable?

Calprotectina fecal: una RS evaluó la exactitud diagnóstica de los niveles de calprotectina fecal para establecer el diagnóstico diferencial entre la enfermedad inflamatoria intestinal y el síndrome de intestino irritable en población adulta con síntomas gastrointestinales menores crónicos persistentes usando como patrón de oro la combinación de colonoscopia, histología, ultrasonido y endoscopia. Cuando se estableció un punto de corte de 50 μg/g, la prueba presentó un adecuado desempeño (curva ROC de 97%, IC 95% con rango de 95% a 98%, sensibilidad de 93% y especificidad de 94%). Calidad de la evidencia: moderada.
En la comparación de SII versus otra enfermedad orgánica, el punto de corte de 50 μg/g presentó un menor rendimiento operativo (DOR 3,3, IC 95% con rango de 2,2 a 4,7, LR+ 2,27, LR negativo de 0,16). Calidad de la evidencia: muy baja (20).
Lactoferrina fecal: una RS evaluó la exactitud diagnóstica de la lactoferrina fecal para el diagnóstico diferencial de SII y enfermedad inflamatoria en población adulta con síntomas gastrointestinales usando como patrón de oro endoscopia + histología. Cuando el punto de corte es de 4 a 7 μg/ml, la prueba tiene un desempeño adecuado (curva ROC de 94%, sensibilidad de 78%, IC 95% con rango de 75% a 82%, especificidad de 94%, IC 95% con rango de 91% a 96%, LR+ de 12,31, LR negativo de 0,23). Calidad de la evidencia: baja (21).
Pregunta 5: ¿cuáles son las manifestaciones clínicas que obligan a descartar la presencia de patología orgánica en pacientes con signos y síntomas sugestivos de síndrome de intestino irritable?

Una RS evaluó la exactitud diagnóstica de los signos y síntomas de alarma para el diagnóstico de carcinoma colorrectal o pólipos colorrectales en población mayor de 15 años usando como patrones de oro la colonoscopia, sigmoidoscopia o el seguimiento clínico. Algunos signos y síntomas están descritos en la guía de estreñimiento crónico funcional (sangrado rectal oscuro, cambios en el hábito intestinal, sangrado rectal, presencia de sangre en heces, pérdida de peso). El síntoma "dolor abdominal" presentó un bajo desempeño operativo (curva ROC de 0,45, sensibilidad de 19%, IC 95% con rango de 13% a 28%, especificidad de 76%, IC 95% con rango de 67% a 83%, LR+ de 0,8, LR negativo de 1,1). Calidad de la evidencia: muy baja (22).
Del mismo modo, otra revisión sistemática (23) evaluó la exactitud diagnóstica de otras "banderas rojas" no consideradas al interior del estudio de Adelstein y colaboradores, registrada detalladamente en el reporte de la guía de estreñimiento crónico funcional. Calidad de la evidencia: muy baja.
Síntoma predominante: dolor
El dolor es un síntoma que altera notablemente la calidad de vida de los pacientes con SII (1-3). Con frecuencia obliga a los pacientes a acudir a los servicios de urgencias y es también una de las principales causas de ausentismo laboral (3,4). No se conoce con exactitud la causa del mismo, sin embargo, se considera que en su origen participa una hipersensibilidad visceral y también contracciones del musculo liso del colon (4,5). Para su alivio se han utilizado antiespasmódicos, antidepresivos tricíclicos e inhibidores selectivos de la recaptación de serotonina (5-7). Se considera que los medicamentos que actúan en los receptores 5-HT pueden controlar los espasmos musculares, el dolor abdominal y controlar el hábito intestinal en el SII (4). Así mismo dentro de los medicamentos usualmente utilizados para el manejo del dolor están los relajantes del musculo liso o antiespasmódicos, que alivian los espasmos del musculo liso y la hipersensibilidad visceral (5). Debido a las limitaciones que ofrecen las intervenciones farmacológicas para el tratamiento del SII, y teniendo en cuenta la asociación de esta entidad con factores psicológicos, se ha propuesto que el uso de antidepresivos podría ofrecer beneficios adicionales al actuar modulando el dolor y la ansiedad (6,7).
Evidencia clínica: antiespasmódicos
Una revisión sistemática de la literatura (8) puntaje AMSTAR 9/11 evaluó la efectividad del uso de antiespasmódicos para el tratamiento de los pacientes con síndrome de intestino irritable. Los desenlaces evaluados fueron el porcentaje de pacientes con resolución del dolor abdominal, la magnitud del dolor y la proporción de pacientes con mejoría global de los síntomas. Los pacientes fueron evaluados a través de cuestionario de síntomas con un rango de seguimiento de 1 a 24 semanas.
Se recuperaron 13 ensayos clínicos controlados para un total de 1392 participantes. Cuando se comparó frente al placebo, el uso de cualquier medicamento antiespasmódico incremento la frecuencia de pacientes que reportaron ausencia de dolor abdominal (RR 1,32; IC 95% 1,12 a 1,55) o que experimentaron mejoría global de los síntomas (RR 1,49; IC 95% 1,25 a 1,77). El uso de antiespasmódicos también se asoció a mejores puntajes en la escala de dolor abdominal (DME 1,14; IC 95% 0,47 a 1,81).
Ahora bien, esta revisión sistemática realizó un análisis de subgrupos dirigido a evaluar la efectividad de cada uno de los antiespasmódicos. Cuando se evaluó la efectividad de la administración de aceite elemental de menta, el uso de esta intervención incrementó la proporción de pacientes con mejoría del dolor abdominal (RR 2,15; IC 95% 1,54 a 3,0) y que reportaron mejoría global de los síntomas (RR 2,25; IC 95% 1,7 a 2,98), al tiempo que mejoró los puntajes alcanzados en la escala de dolor abdominal (DME 3,88; IC 95% 2,98 a 4,79). Estos hallazgos son similares a los observados con la administración cimetropio/diciclomina, que también incremento la probabilidad de presentar mejoría del dolor abdominal (RR 1,56; IC 95% 1,06 a 2,28) y global de los síntomas (RR 1,78; IC 95% 1,15 a 2,75).
Para la administración de bromuro de pinaverio, trimebutina y de bromuro de otilonio los hallazgos fueron menos consistentes. La administración de bromuro de pinaverio incrementó la proporción de pacientes que reportaron mejoría del dolor (RR 1,57; IC 95% 1,08 a 2,26) y global de los síntomas (RR 1,66; IC 95% 1,25 a 2,19) sin que esto se viera asociado con mejores resultados en la escala de dolor abdominal (DME 0,44; IC 95% -0,2 a 1,08). Por otra parte, la trimebutina incrementó la proporción de pacientes sin dolor (RR 1,32; IC 95% 1,07 a 1,64), pero no la de pacientes con mejoría global de los síntomas (RR 0,97; IC 95% 0,68 a 1,38). Con respecto al bromuro de Otilonio, su uso no redujo la frecuencia de pacientes que reportaron dolor abdominal (RR 1,27; IC 95% 0,96 a 1,68) pero sí con mejoría global de los síntomas (RR 1,79; IC 95% 1,31 a 2,44). Finalmente, la mebeverina no incrementó la proporción de pacientes que experimentaron mejoría de dolor (RR 0,82; IC 95% 0,38 a 1,76) o global de los síntomas (RR 0,42; IC 95% 0,16 a 1,07). Esta revisión sistemática no evaluó los efectos adversos de la intervención. La calidad de la evidencia fue baja por limitaciones en la precisión y el riesgo de sesgos.
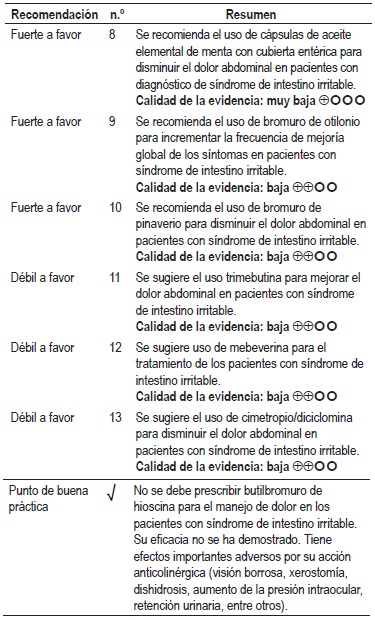
Evidencia clínica: antidepresivos
Una revisión sistemática de la literatura (9) puntaje AMSTAR 9/11 evaluó la seguridad y la efectividad de los antidepresivos para el tratamiento de los pacientes con síndrome de intestino irritable diagnosticado según concepto de un experto gastroenterólogo, o bien mediante el uso de criterios clínicos (Manning, Kruis, Roma I, II, o III). Los desenlaces evaluados fueron la no mejoría global de los síntomas o del dolor abdominal (reportado por el paciente o por el médico), la no mejoría del dolor abdominal (reportado por el paciente o por el médico) y la presencia de eventos adversos de cualquier tipo reportados por los pacientes.
Teniendo en cuenta los diferentes tipos de antidepresivos evaluados (desipramina, trimipramina, amitriptilina, doxepina, fluoxetina, proxetina, citalopram e imipramina), esta revisión sistemática incorporó las siguientes comparaciones
1. Cualquier antidepresivo versus placebo
2. Antidepresivos tricíclicos versus placebo
3. Antidepresivos inhibidores de la recaptación de serotonina versus placebo
Comparación 1 - Cualquier antidepresivos versus placebo
Se recuperaron 17 ensayos clínicos controlados (10 estudios evaluaron tricíclicos, 6 inhibidores de la receptación de serotonina y 1 estudio ambos antidepresivos) para un total de 1100 pacientes (592 recibieron cualquier antidepresivos y 508 recibieron placebo) en donde se evaluó la intervención de interés con un seguimiento de 4 a 12 semanas en cualquier nivel de complejidad (primer, segundo y tercer nivel). Cuando se comparó frente al placebo, para el tratamiento de los pacientes con síndrome de intestino irritable, el uso de antidepresivos redujo la frecuencia de no mejoría global en los síntomas (RR 0,67; IC 95% 0,58 a 0,77) y disminuyó la posibilidad de no experimentar mejoría del dolor abdominal (RR 0,62; IC 95% 0,43 a 0,88) a costa de un incremento en la frecuencia de eventos adversos (RR 1,63; IC 95% 1,18 a 2,25) siendo la somnolencia y la sensación de boca seca los reportados con mayor frecuencia. Cuando se realizó un análisis de sensibilidad limitado a estudios de alta calidad metodológica, no se encontraron diferencias estadísticamente significativas en términos de la frecuencia de mejoría global de los síntomas (3 estudios, RR 0,76; IC 95% 0,46 a 1,27). La calidad de la evidencia fue muy baja por algunas limitaciones en el riesgo de sesgos, la precisión y la consistencia de los resultados.
Comparación 2 - Antidepresivos tricíclicos versus Placebo
Se recuperaron 11 ensayos clínicos controlados para un total de 744 pacientes, donde se evaluó el uso de antidepresivos tricíclicos con un seguimiento de 4 a 12 semanas en cualquier nivel de complejidad (primer, segundo y tercer nivel). Comparado frente al placebo, el tratamiento con antidepresivos tricíclicos redujo la posibilidad de no alcanzar una mejoría global en el alivio de los síntomas con un 43,3% frente a un 63,7% de los participantes para el grupo de intervención y placebo respectivamente (RR 0,66; IC 95% 0,56 a 0,79). La revisión sistemática no reportó la frecuencia de eventos adversos por tipo de antidepresivo. La calidad de la evidencia fue muy baja por limitaciones en el riesgo de sesgos y la inconsistencia de los resultados.
Comparación 2 - Antidepresivos inhibidores de la recaptación de serotonina versus Placebo
Se recuperaron 7 ensayos clínicos controlados para un total de 356 pacientes, donde se evaluaron inhibidores de la recaptación de serotonina con un seguimiento de 4 a 12 semanas en cualquier nivel de atención (primer, segundo y tercer nivel). Los pacientes asignados al grupo de tratamiento con inhibidores de la recaptación de serotonina reportaron una menor frecuencia de no mejoría durante la evaluación global de los síntomas cuando se compararon frente al grupo control (45,5% versus 67,2% respectivamente) con un RR 0,68 (IC 95% 0,51 a 0,91). La revisión sistemática no reportó la frecuencia de eventos adversos por tipo de antidepresivo. La calidad de la evidencia fue muy baja por limitaciones en el riesgo de sesgos y la consistencia de los resultados.

Evidencia clínica: probióticos, prebióticos y simbióticos
Una revisión sistemática de la literatura (10) con puntaje AMSTAR 8/11 evaluó la efectividad y la seguridad del uso de probióticos, prebióticos y simbióticos (Streptococcus faecium, Lactobacillus plantarum, VSL#3, Lactobacillus rhamnosus, Propionibacterium Freudenreichii, Bifidobacterium breve, Lactobacillus reuteri, Lactobacillus salivarius, Bifidobacterium infantis, Bifidobacterium Animalis, Streptococcus thermophilus, Lactobacillus bulgaricus, Bifidobacterium longum, Lactobacillus acidophilus, Lactobacillus lactis, Escherichia coli DSM17252, Lactobacillus paracasei ssp. paracasei, Saccharomyces boulardii, entre otros) para el tratamiento de los pacientes con síndrome de intestino irritable. Los desenlaces evaluados fueron el control global de los síntomas, el cambio en el puntaje de distensión, de dolor abdominal o de flatulencias y la frecuencia de eventos adversos no serios derivados de la intervención. Se recuperaron 43 ensayos clínicos controlados para un total de 2575 participantes en donde se evaluó la intervención de interés con un rango de seguimiento de 2 a 26 semanas.
Cuando se comparó frente al placebo, la administración de probióticos redujo la proporción de pacientes que no experimentaron mejoría sintomática (RR 0,79; IC 95% 0,7 a 0,89) al igual que los índices de dolor (diferencia de medias estandarizadas (DME -0,25; IC 95% -0,36 a -0,14), distensión abdominal (DME -0,15; IC 95% -0,27 a -0,03) y de flatulencias (DME -0,23; IC 95% -0,38 a -0,07). La calidad de la evidencia fue moderada por algunas limitaciones en la consistencia y el riesgo de sesgos de los estudios incluidos. Se recuperaron dos ensayos clínicos (10,11) controlados para un total de 198 participantes en donde se evaluó el uso de simbióticos para el tratamiento de los pacientes con síndrome de intestino irritable. El seguimiento se realizó de 8 a 12 semanas y el desenlace de interés fue el índice de mejoría sintomática después de la intervención. Comparado frente al placebo, la administración de simbióticos no se asoció con un mayor o menor índice de mejoría sintomática en los pacientes que recibieron la intervención (DME -1,73; IC 95% -3,73 a 0,27). La calidad de la evidencia fue muy baja por limitaciones en la consistencia y la precisión de los resultados.
Con respecto al uso de prebióticos en pacientes con síndrome de intestino irritable, esta revisión sistemática incluyó un ensayo clínico controlado (12) que reclutó 63 participantes con un seguimiento de 3 semanas. El uso de prebióticos no incrementó la proporción de pacientes que reportaron mejoría sintomática (32% versus 31%) y el número de movimientos intestinales por semana no fue estadísticamente diferente entre los grupos (5,95±2,50 en el grupo prebiótico, comparado con 6,70±3,83 en el grupo control).
23 estudios incluidos en esta revisión (2406 participantes) evaluaron la frecuencia de eventos adversos asociados con el uso de los probióticos, prebióticos y simbióticos. Comparados con al grupo control, el tratamiento con probióticos, prebióticos o simbióticos incrementó la frecuencia de eventos adversos no serios (RR 1,21; IC 95% CI 1,02 a 1,44) tales como vértigo, vómito, diarrea, sensación de palpitaciones o dolor abdominal entre otros. La calidad de la evidencia fue muy baja por limitaciones en la precisión y el riesgo de sesgos.
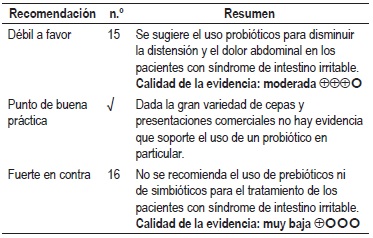
Tratamiento
Pregunta 6: ¿cuáles son las intervenciones farmacológicas más efectivas y seguras para el tratamiento de los diferentes síntomas en pacientes con síndrome de intestino irritable?
¿Cuál es el tratamiento cuando el síntoma predominante es diarrea?

Medicamentos antimotilidad: una RS desarrollada por el GDG NICE (24) evaluó la efectividad y seguridad del uso de medicamentos antimotilidad (loperamida y difenoxilato + atropina –lomotil–) como terapia aguda y de mantenimiento para el tratamiento de los pacientes con síndrome de intestino irritable con diarrea como síntoma predominante. Al comparar lomotil versus loperamida, se encontró que el grupo que recibió el primero presentó una menor efectividad en la ausencia de deposiciones diarreicas a las 24 horas (RR 0,78, IC 95% con rango de 0,62 a 0,98), 48 horas (RR 0,81, IC 95% con rango de 0,73 a 0,89) y 72 horas (RR 0,89, IC 95% con rango de 0,84 a 0,94). Como terapia de mantenimiento, se encontró que la loperamida se asoció con una mejoría en la frecuencia de deposiciones (RR 2,38, IC 95% con rango de 1,53 a 3,70), en el número de deposiciones formadas (RR 9,22, IC 95% con rango de 4,48 a 18,98) y en los episodios de urgencia (RR 3,0, IC 95% con rango de 1,07 a 8,43) sin encontrar diferencias en la consistencia de las deposiciones o la frecuencia de eventos adversos (RR 3, IC 95% con rango de 0,13 a 67,06). Calidad de la evidencia: muy baja (24).
Antibióticos: una RS evaluó la efectividad del uso de antibióticos para el tratamiento de los pacientes con síndrome de intestino irritable. Comparado frente al placebo, la administración de antibióticos (neomicina o rifaximina) incrementó la frecuencia de mejoría sintomática durante el tratamiento (RR 2,06, IC 95% con rango de 1,30 a 3,27) sin reportar información sobre eventos adversos. Calidad de la evidencia: baja (25).
Rifaximina: otra RS evaluó la eficacia de la rifaximina en pacientes con síndrome de intestino irritable. Cuando se comparó frente al placebo, este tratamiento se asoció con una mejoría global de los síntomas (OR 1,57, IC 95% con rango de 1,22 a 2,01) y con la disminución en la distensión abdominal (OR 1,55, IC 95% con rango de 1,23 a 1,96) sin información sobre seguridad. Calidad de la evidencia: moderada (26).
Antagonistas 5HT: una RS evaluó la efectividad y seguridad del uso de antagonistas 5HT3 o agonistas 5HT4 para el tratamiento de los pacientes con síndrome de intestino irritable. Con base en este estudio se pudo evidenciar que los antagonistas 5HT3 (alosetrón, cilasetrón) reducen la proporción de pacientes que no experimentan mejoría sintomática (RR 0,78, IC 95% con rango de 0,71 a 0,86) y aumentan los eventos adversos (RR 1,19, IC 95% con rango de 1,09 a 1,30) y el estreñimiento (RR 4,4, IC 95% con rango de 3,11 a 6,53). En cuanto al uso combinado (antagonistas 5HT3 y agonistas 5HT4), no se encontraron diferencias en la mejoría sintomática (RR 0,94, IC 95% con rango de 0,76 a 1,17) ni en la frecuencia global de eventos adversos (renzaprida 68% versus placebo 67%; cisaprida versus placebo: RR 0,73, IC 95% con rango de 0,29 a 1,80). Calidad de la evidencia: muy baja (27).
Ondansetrón: un ensayo clínico aleatorizado evaluó la efectividad y seguridad del ondansetrón para el tratamiento de pacientes con síndrome de intestino irritable con diarrea, diagnosticado según criterios de Roma III. El estudio reportó que mejoró la consistencia de las heces (DM −0,9, IC 95% con rango de -1,1 a -0,6), el puntaje de urgencia fecal (DM -1,1, IC 95% con rango de -1,5 a -0,6), el porcentaje de deposiciones (-11%, IC 95% con rango de -4% a -18%), sin encontrar diferencias en dolor, distensión abdominal o eventos adversos (RR 4,61, IC 95% con rango de 0,56 a 38,01). Calidad de la evidencia: baja (28).
Ramosetrón: un ensayo clínico controlado aleatorizado evaluó la efectividad y seguridad del uso del ramosetrón para el tratamiento de los pacientes con síndrome de intestino irritable. Cuando se comparó frente a placebo, el ramosetrón se asoció con mejoría en la consistencia de las heces (RR 2,57, IC 95% con rango de 1,79 a 3,7) sin encontrar diferencias en el dolor abdominal o en los eventos adversos (RR 1,07, IC 95% con rango de 0,82 a 1,39). Calidad de la evidencia: moderada (29).
¿Cuál es el tratamiento cuando el síntoma predominante es estreñimiento?

Laxantes estimulantes: una RS realizada por el GDG NICE evaluó la efectividad y seguridad del uso de laxantes estimulantes (bisacodilo o picosulfato de sodio) para el tratamiento de los pacientes con síndrome de intestino irritable con episodio agudo de estreñimiento. El estudio encontró que los pacientes asignados al brazo de laxantes estimulantes tuvieron una mayor probabilidad de mejorar su hábito intestinal (RR 1,34, IC 95% con rango de 1,02 a 1,76) con mejoría en la consistencia (RR 1,51, IC 95% con rango de 1,06 a 2,15) y la frecuencia de las heces (DM 0,85, IC 95% con rango de 0,24 a 1,46) sin diferencias en la presencia de eventos adversos (RR 0,73, IC 95% con rango de 0,17 a 3,08). Calidad de la evidencia: muy baja (24).
Laxantes osmóticos: una revisión sistemática de la literatura realizada por el GDG NICE evaluó la efectividad de la terapia de mantenimiento con laxantes osmóticos (polietilenglicol) para el tratamiento de los pacientes con síndrome de intestino irritable con estreñimiento. El estudio reportó su uso se asoció con un uso de laxantes de rescate (RR 0,33, IC9 5% con rango de 0,12 a 0,9) con mejoría del hábito intestinal (RR 3,95, IC 95% con rango de 1,86 a 8,42), reducción del abandono por no respuesta clínica (RR 0,13, IC 95% con rango de 0,03 a 0,53), sin encontrar diferencias en la mejoría del dolor o la distensión abdominal. Los estudios no evaluaron desenlaces de seguridad. Calidad de la evidencia: muy baja (24).
Antagonistas 5HT: una RS evaluó la efectividad y seguridad del uso de antagonistas 5HT3 o agonistas 5HT4 para el tratamiento de los pacientes con síndrome de intestino irritable. El estudio encontró que el uso de los últimos se asoció con menor probabilidad de no experimentar mejoría sintomática (RR 0,85, IC 95% con rango de 0,8 a 0,9), sin diferencias en eventos adversos globales (RR 1,07, IC 95% con rango de 1,0 a 1,15). Calidad de la evidencia: baja.
Para el uso combinado de antagonistas 5HT3 y agonistas 5HT4 no se encontraron diferencias en la mejoría sintomática (RR 0,94, IC 95% con rango de 0,76 a 1,17) con frecuencias de eventos adversos similares (68% versus 67%). Calidad de la evidencia: muy baja (27).
Linaclotide: una RS evaluó la seguridad y efectividad del linaclotide para el tratamiento de los pacientes mayores de 18 años con síndrome de intestino irritable de predominio estreñimiento. La revisión encontró que este redujo la frecuencia de pacientes que no experimentaron mejoría (RR 0,8, IC 95% con rango de 0,76 a 0,85) o alivio de los síntomas (RR 0,73, IC 95% con rango de 0,65 a 0,82), redujo la proporción de pacientes que no reportaron incremento en su calidad de vida (RR 0,78, IC 95% con rango de 0,72 a 0,86) con un aumento en la suspensión del tratamiento por diarrea (RR 14,7, IC 95% con rango de 4,0 a 53,8). Calidad de la evidencia: baja (30).
Lubiprostone: un ensayo clínico aleatorizado evaluó la efectividad y seguridad del lubiprostone para el tratamiento de pacientes con síndrome de intestino irritable con estreñimiento. El estudio reportó mejoría asociada con el lubiprostone en dolor abdominal (16 μg/día DM -0,58, IC 95% con rango de -0,38 a -0,78), distensión abdominal (16 μg/día DM -0,58, IC 95% con rango de -0,36 a -0,78), grado de esfuerzo defecatorio (16 μg/día DM -0,72, IC 95% con rango de -0,55 a -0,95), severidad del estreñimiento (16 μg/día DM -0,55, IC 95% con rango de -0,33 a -0,79), consistencia de las deposiciones (16 μg/día DM -0,52, IC 95% con rango de -0,37 a -0,78), y reducción de las deposiciones semanales (16 μg/día 1,8 veces por semana, IC 95% con rango de 1,1 a 2,8); no se encontraron diferencias en la frecuencia de eventos adversos (p >0,05). Calidad de la evidencia: baja (31).
Pregunta 7: ¿cuáles son las intervenciones no farmacológicas más efectivas y seguras para el tratamiento de los pacientes con síndrome de intestino irritable?

Placebo: una RS evaluó la efectividad del placebo en pacientes con síndrome de intestino irritable y encontró una mejoría global de síntomas del 37,5% (IC 95% con rango de 34,4% a 40,6%). Calidad de la evidencia: baja (32).
Dieta FODMAP: una revisión sistemática evaluó la efectividad de la dieta baja en FODMAP para el tratamiento de los pacientes con síndrome de intestino irritable y reportó reducción de los síntomas globales asociados con la dieta (OR 1,81, IC 95% con rango de 1,11 a 2,95), el dolor (OR 1,81, IC 95% con rango de 1,13 a 2,88), la distensión abdominal (OR 1,75, IC 95% con rango de 1,07 a 2,87) y la severidad de los síntomas (OR 0,44, IC 95% con rango de 0,25 a 0,76). Calidad de la evidencia: baja (33).
Fibra: una RS evaluó la seguridad y la efectividad de la fibra para el tratamiento de los pacientes con síndrome de intestino irritable. Los resultados globales mostraron que la fibra se asoció con la reducción de la no mejoría (RR 0,86, IC 95% con rango de 0,8 a 0,94) sin encontrar diferencias en la frecuencia de eventos adversos (RR 1,06, IC 95% con rango de 0,92 a 1,22). Calidad de la evidencia: muy baja (34).
Moxibustión: una RS evaluó la efectividad de la moxibustión para el tratamiento de los pacientes con síndrome de intestino irritable y encontró que su uso solo (RR 1,33, IC 95% con rango de 1,15 a 1,55) o con acupuntura (RR 1.24, IC 95% con rango de 1,09 a 1,41) se asoció con la mejoría global de los síntomas, sin encontrar diferencias en la severidad de los síntomas. Calidad de la evidencia: muy baja (35).
Acupuntura: una RS evaluó la efectividad de la acupuntura para el tratamiento de los pacientes con síndrome de intestino irritable. Al comparar la acupuntura versus otras terapias, se encontró que la primera se asoció con mejoría de los síntomas (versus farmacoterapia: RR 1,28, IC 95% con rango de 1,12 a 1,45), sin encontrar diferencias en la mejoría clínica en las comparaciones contra placebo, Bifidobacterium y psicoterapia. Calidad de la evidencia: muy baja (36).
Hipnoterapia: la RS evaluó la eficacia de la hipnoterapia para el tratamiento de los pacientes con síndrome de intestino irritable y encontró diferencias en favor de la hipnoterapia al compararla con biofeedback, terapia cognitiva comportamental, terapia psicodinámica, y terapia de relajación, pero no encontró diferencias en los desenlaces de distensión abdominal, dolor (DME -0,46, IC 95% con rango de -1,15 a 0,23), depresión, calidad de vida relacionada con la salud y tolerabilidad de los síntomas. Calidad de la evidencia: muy baja (37).
Homeopatía: una RS evaluó la efectividad de la homeopatía para el tratamiento de los pacientes con síndrome de intestino irritable. Se encontró que la homeopatía se asoció con la mejoría global de los síntomas (RR 1,61, IC 95% con rango de 1,18 a 1,28) sin encontrar diferencias en la percepción de bienestar. No fueron evaluados desenlaces de seguridad. Calidad de la evidencia: muy baja (38).
ALGORITMO 1. DIAGNÓSTICO DEL SÍNDROME DE INTESTINO IRRITABLE
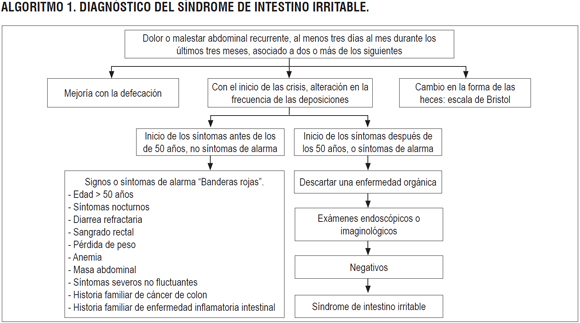
ALGORITMO 2. TRATAMIETO DEL SÍNDROME DE INTESTINO IRRITABLE
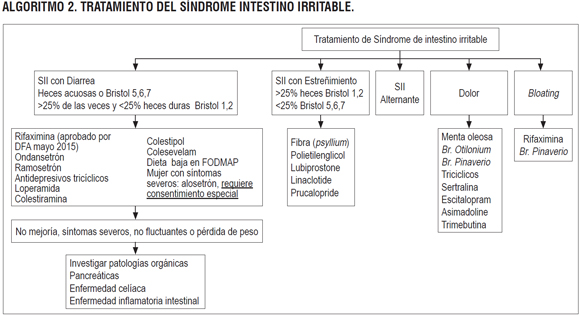
DECLARACIÓN DE CONFLICTOS DE INTERÉS
Los autores declaran no tener conflictos de interés, no estar involucrados como investigadores en ensayos clínicos en curso sobre el tema, y no haber recibido donaciones o beneficios por parte de los grupos interesados en las recomendaciones. El doctor William Otero, declara haber sido conferencista de los laboratorios: Abbott-Lafrancol. Janssen, Procaps, Tecnofarma, Biotoscana y Takeda.
FUENTE DE FINANCIACIÓN
La presente guía fue desarrollada mediante un convenio de extensión entre la Asociación Colombiana de Gastroenterología y la facultad de Medicina de la Universidad Nacional.
REFERENCIAS
1. Lovell RM, Ford AC. Global prevalence of and risk factors for irritable bowel syndrome: A meta-analysis. Clin Gastroenterol Hepatol. 2012 Jul;10(7):712-21 e4. [ Links ]
2. Longstreth GF, Thompson WG, Chey WD, Houghton LA, Mearin F, Spiller RC. Functional bowel disorders. Gastroenterology. 2006 Apr;130(5):1480-91. [ Links ]
3. Drossman DA, Camilleri M, Mayer EA, Whitehead WE. AGA technical review on irritable bowel syndrome. Gastroenterology. 2002 Dec;123(6):2108-31. [ Links ]
4. Hahn BA, Yan S, Strassels S. Impact of irritable bowel syndrome on quality of life and resource use in the United States and United Kingdom. Digestion. 1999 Jan-Feb;60(1):77-81. [ Links ]
5. Longstreth GF, Yao JF. Irritable bowel syndrome and surgery: A multivariable analysis. Gastroenterology. 2004 Jun;126(7):1665-73. [ Links ]
6. Talley NJ. Unnecessary abdominal and back surgery in irritable bowel syndrome: time to stem the flood now? Gastroenterology. 2004 Jun;126(7):1899-903. [ Links ]
7. Frank L, Kleinman L, Rentz A, Ciesla G, Kim JJ, Zacker C. Health-related quality of life associated with irritable bowel syndrome: Comparison with other chronic diseases. Clin Ther. 2002 Apr;24(4):675-89; discussion 4. [ Links ]
8. Chang JY, Locke GR, 3rd, McNally MA, Halder SL, Schleck CD, Zinsmeister AR, et al. Impact of functional gastrointestinal disorders on survival in the community. Am J Gastroenterol. 2010 Apr;105(4):822-32. [ Links ]
9. Brandt LJ, Chey WD, Foxx-Orenstein AE, Schiller LR, Schoenfeld PS, Spiegel BM, et al. An evidence-based position statement on the management of irritable bowel syndrome. Am J Gastroenterol. 2009 Jan;104 Suppl 1:S1-35. [ Links ]
10. Chang L, Lembo A, Sultan S. American Gastroenterological Association Institute Technical Review on the pharmacological management of irritable bowel syndrome. Gastroenterology. 2014 Nov;147(5):1149-72 e2. [ Links ]
11. AGREE C. Instrumento AGREE II Instrumento para la evaluación de Guías de Práctica Clínica. Guiasalud; 2009 [updated 2009; cited 2015]; Available from: http://www.guiasalud.es/contenidos/documentos/Guias_Practica_Clinica/Spanish-AGREE-II.pdf. [ Links ]
12. Shea BJ, Grimshaw JM, Wells GA, Boers M, Andersson N, Hamel C, et al. Development of AMSTAR: A measurement tool to assess the methodological quality of systematic reviews. BMC Med Res Methodol. 2007;7:10. [ Links ]
13. Brozek JL, Akl EA, Alonso-Coello P, Lang D, Jaeschke R, Williams JW, et al. Grading quality of evidence and strength of recommendations in clinical practice guidelines. Part 1 of 3. An overview of the GRADE approach and grading quality of evidence about interventions. Allergy. 2009 May;64(5):669-77. [ Links ]
14. Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, et al. GRADE: An emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 2008 Apr 26;336(7650):924-6. [ Links ]
15. Ford AC, Talley NJ, Veldhuyzen van Zanten SJ, Vakil NB, Simel DL, Moayyedi P. Will the history and physical examination help establish that irritable bowel syndrome is causing this patients lower gastrointestinal tract symptoms? JAMA. 2008 Oct 15;300(15):1793-805. [ Links ]
16. Jellema P, van der Windt DA, Schellevis FG, van der Horst HE. Systematic review: accuracy of symptom-based criteria for diagnosis of irritable bowel syndrome in primary care. Aliment Pharmacol Ther. 2009 Oct;30(7):695-706. [ Links ]
17. Ford AC, Bercik P, Morgan DG, Bolino C, Pintos-Sanchez MI, Moayyedi P. Validation of the Rome III criteria for the diagnosis of irritable bowel syndrome in secondary care. Gastroenterology. 2013 Dec;145(6):1262-70.e1. [ Links ]
18. Cash BD, Schoenfeld P, Chey WD. The utility of diagnostic tests in irritable bowel syndrome patients: A systematic review. Am J Gastroenterol. 2002 Nov;97(11):2812-9. [ Links ]
19. Shah ED, Basseri RJ, Chong K, Pimentel M. Abnormal breath testing in IBS: A meta-analysis. Dig Dis Sci. 2010 Sep;55(9):2441-9. [ Links ]
20. Waugh N, Cummins E, Royle P, Kandala NB, Shyangdan D, Arasaradnam R, et al. Faecal calprotectin testing for differentiating amongst inflammatory and non-inflammatory bowel diseases: Systematic review and economic evaluation. Health Technol Assess. 2013 Nov;17(55):xv-xix, 1-211. [ Links ]
21. Zhou XL, Xu W, Tang XX, Luo LS, Tu JF, Zhang CJ, et al. Fecal lactoferrin in discriminating inflammatory bowel disease from irritable bowel syndrome: A diagnostic meta-analysis. BMC Gastroenterol. 2014;14:121. [ Links ]
22. Adelstein BA, Macaskill P, Chan SF, Katelaris PH, Irwig L. Most bowel cancer symptoms do not indicate colorectal cancer and polyps: A systematic review. BMC Gastroenterol. 2011;11:65. [ Links ]
23. Jellema P, van der Windt DA, Bruinvels DJ, Mallen CD, van Weyenberg SJ, Mulder CJ, et al. Value of symptoms and additional diagnostic tests for colorectal cancer in primary care: Systematic review and meta-analysis. BMJ. 2010;340:c1269. [ Links ]
24. (NICE) Nccfnasc. Irritable Bowel Syndrome in Adults: Diagnosis and Management of Irritable Bowel Syndrome in Primary Care. London: Royal College of Nursing (UK); 2008 [citado mayo 20, 2015]. Available from: http://www.ncbi.nlm.nih.gov/books/NBK51953/. [ Links ]
25. Rezaie A, Nikfar S, Abdollahi M. The place of antibiotics in management of irritable bowel syndrome: A systematic review and meta-analysis. Arch Med Sci. 2010 Mar 1;6(1):49-55. [ Links ]
26. Menees SB, Maneerattannaporn M, Kim HM, Chey WD. The efficacy and safety of rifaximin for the irritable bowel syndrome: A systematic review and meta-analysis. Am J Gastroenterol. 2012 Jan;107(1):28-35; quiz 6. [ Links ]
27. Ford AC, Brandt LJ, Young C, Chey WD, Foxx-Orenstein AE, Moayyedi P. Efficacy of 5-HT3 antagonists and 5-HT4 agonists in irritable bowel syndrome: Systematic review and meta-analysis. Am J Gastroenterol. 2009 Jul;104(7):1831-43; quiz 44. [ Links ]
28. Garsed K, Chernova J, Hastings M, Lam C, Marciani L, Singh G, et al. A randomised trial of ondansetron for the treatment of irritable bowel syndrome with diarrhoea. Gut. 2014 Oct;63(10):1617-25. [ Links ]
29. Fukudo S, Ida M, Akiho H, Nakashima Y, Matsueda K. Effect of ramosetron on stool consistency in male patients with irritable bowel syndrome with diarrhea. Clin Gastroenterol Hepatol. 2014 Jun;12(6):953-9 e4. [ Links ]
30. Atluri DK, Chandar AK, Bharucha AE, Falck-Ytter Y. Effect of linaclotide in irritable bowel syndrome with constipation (IBS-C): A systematic review and meta-analysis. Neurogastroenterol Motil. 2014 Apr;26(4):499-509. [ Links ]
31. Johanson JF, Drossman DA, Panas R, Wahle A, Ueno R. Clinical trial: phase 2 study of lubiprostone for irritable bowel syndrome with constipation. Aliment Pharmacol Ther. 2008 Apr;27(8):685-96. [ Links ]
32. Ford AC, Moayyedi P. Meta-analysis: Factors affecting placebo response rate in the irritable bowel syndrome. Aliment Pharmacol Ther. 2010 Jul;32(2):144-58. [ Links ]
33. Marsh A, Eslick EM, Eslick GD. Does a diet low in FODMAPs reduce symptoms associated with functional gastrointestinal disorders? A comprehensive systematic review and meta-analysis. Eur J Nutr. 2015 May 17. [ Links ]
34. Moayyedi P, Quigley EM, Lacy BE, Lembo AJ, Saito YA, Schiller LR, et al. The effect of fiber supplementation on irritable bowel syndrome: A systematic review and meta-analysis. Am J Gastroenterol. 2014 Sep;109(9):1367-74. [ Links ]
35. Park JW, Lee BH, Lee H. Moxibustion in the management of irritable bowel syndrome: Systematic review and meta-analysis. BMC Complement Altern Med. 2013;13:247. [ Links ]
36. Manheimer E, Cheng K, Wieland LS, Min LS, Shen X, Berman BM, et al. Acupuncture for treatment of irritable bowel syndrome. Cochrane Database Syst Rev. 2012;5:CD005111. [ Links ]
37. Schaefert R, Klose P, Moser G, Hauser W. Efficacy, tolerability, and safety of hypnosis in adult irritable bowel syndrome: Systematic review and meta-analysis. Psychosom Med. 2014 Jun;76(5):389-98. [ Links ]
38. Peckham EJ, Nelson EA, Greenhalgh J, Cooper K, Roberts ER, Agrawal A. Homeopathy for treatment of irritable bowel syndrome. Cochrane Database Syst Rev. 2013;11:CD009710. [ Links ]













