Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.30 supl.1 Bogotá Dec. 2015
Guía de práctica clínica para la tamización del cáncer colorrectal - 2015
Clinical Practice Guideline for the screening of colorectal cancer-2015
Fabio Leonel Gil Parada, MD 1, Marcela Torres Amaya, QF,2 Sandra Viviana Riveros Santoya, MD,3, Rodrigo Castaño Llano, MD,4, Heinz Ibáñez, MD,5, Margarita María Huertas Quintero, MD6, Rafael Carmona, MD7, Rodrigo Pardo MD8, William Otero MD9, Luis Sabbagh, MD.10.
1Gastroenterólogo, Clínica Universitaria Colombia – Organización Sánitas Internacional.
2Química farmacéutica. MsC, PhD (E). Gerente editorial Grupo Cochrane STI.
3 Médica cirujana, Universidad Nacional de Colombia. Epidemióloga clínica, Universidad del Rosario - CES (C).
4 Cirugía gastrointestinal y endoscopia, grupo de gastrohepatología, Universidad de Antioquia. Instituto de Cancerología, Clínica las Américas, jefe de posgrado. Cirugía General, UPB.
5 Coloproctólogo, Hospital Militar. Presidente de la Asociación Colombiana de Coloproctología.
6 Médico, cirujano, gastroenterología y endoscopia digestiva, Fundación Universitaria Sánitas. Gastroenterología en Clínica Colombia y Clínica Reina Sofía.
7 Gastroenterólogo, Clínica Madre Bernarda, Clínica Medihelp Servicios, Cartagena.
8 Médico internista, epidemiólogo. Director del Instituto de Investigaciones Clínicas, Universidad Nacional de Colombia.
9 Profesor titular de medicina, Coordinador de Gastroenterología, Universidad Nacional de Colombia. Ex-presidente Asociación Colombiana de Gastroenterología, Ex-presidente Asociación Colombiana de Endoscopia Digestiva. Miembro honorario Sociedad Dominicana de Gastroenterología. Miembro Honorario Sociedad Venezolana de Endoscopia Digestiva, Gastroenterólogo, Clínica Fundadores.
10Presidente de la Organización Panamericana de Gastroenterología. Presidente de la Asociación Colombiana de Gastroenterología. Expresidente de la Asociación Colombiana de Endoscopia Digestiva. Director del posgrado en gastroenterología, Fundación Universitaria Sánitas.
Contacto: Dr. Fabio Gil. fabiogilp@gmail.com
Resumen
Objetivo: desarrollar una guía de práctica clínica con la evidencia más reciente para la tamización de cáncer de colon y recto en población asintomática de riesgo promedio, dirigida a pacientes, personal asistencial, administrativo y entes gubernamentales de cualquier servicio de atención en Colombia.
Materiales y métodos: esta guía fue desarrollada por un equipo multidisciplinario con apoyo de la Asociación Colombiana de Gastroenterología, el Grupo Cochrane ITS y el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia. Se desarrollaron preguntas clínicas relevantes y se realizó la búsqueda de guías nacionales e internacionales en bases de datos especializadas. Las guías existentes fueron evaluadas en términos de calidad y aplicabilidad; ninguna de ellas cumplió el criterio de adaptación, por lo que se decidió construir una guía de novo. El Grupo Cochrane realizó la búsqueda sistemática de la literatura. Las tablas de evidencia y recomendaciones fueron realizadas con base en la metodología GRADE. Las recomendaciones de la guía fueron socializadas en una reunión de expertos con entes gubernamentales y pacientes.
Resultados: se desarrolló una guía de práctica clínica basada en la evidencia para la tamización del cáncer de colon y recto en Colombia.
Conclusiones: la tamización de pacientes asintomáticos de riesgo promedio en Colombia en forma adecuada con estándares de calidad tiene el potencial de impactar la carga de cáncer de colon en el país.
Palabras clave
Guía de práctica clínica, cáncer colorrectal, tamización.
Abstract
Objective: To provide an evidence-based clinical practice guideline for the screening of colon and rectal cancer for patients, caregivers, administrative and government bodies at all levels of care in Colombia.
Materials and Methods: This guide was developed by a multidisciplinary team with the support of the Colombian Association of Gastroenterology, Cochrane STI Group and Clinical Research Institute of the Universidad Nacional de Colombia. Relevant clinical questions were developed and the search for national and international guidelines in databases was performed. Existing guidelines were evaluated for quality and applicability. None of the guidelines met the criteria for adaptation, so the group decided to develop a de novo guideline. Systematic literature searches were conducted by the Cochrane Group. The tables of evidence and recommendations were made based on the GRADE methodology. The recommendations of the guide were socialized in a meeting of experts with government agencies and patients.
Results: An evidence-based Clinical Practice Guidelines for the screening of colorectal cancer was developed for the Colombian context.
Conclusions: The opportune detection of colon cancer would have an impact of the disease in Colombia.
Keywords
Clinical practice guidelines, colorectal cancer, screening.
PROPÓSITO
El propósito de esta guía es brindar al área de la salud la evidencia más reciente en cuanto a la efectividad y seguridad de las diferentes estrategias para la tamización de cáncer colorrectal (CCR) en cualquier servicio de atención del país. Las recomendaciones fueron realizadas para los servicios de atención primaria, secundaria y terciaria que atienden individuos asintomáticos con edad cumplida mayor o igual a 50 años, de ambos sexos y sin factores de riesgo relacionados. No se incluirán pacientes con manifestaciones clínicas o relacionados con síndromes genéticos, poliposis múltiples heredofamiliares o con factores de riesgo identificados para CCR.
Con el objetivo de brindar recomendaciones para la mejor estrategia de tamización de CCR en Colombia, esta guía está dirigida a todo el personal en salud asistencial y administrativo así como para tomadores de decisiones en salud, aseguradoras, pagadores del gasto en salud y a aquellos que generan políticas en salud.
INTRODUCCIÓN Y JUSTIFICACIÓN DE LA GUÍA
El cáncer colorrectal es un problema mundial, con una incidencia anual de aproximadamente 21 casos por cada 100000 habitantes, y 752731 muertes en 2012; es la tercera causa más común de cáncer en hombres y segunda en mujeres, y la segunda causa en frecuencia de mortalidad por cáncer entre hombres y mujeres a nivel mundial (1). En Colombia es la cuarta causa en incidencia y mortalidad por cáncer, con una incidencia aproximada de 16 casos por cada 100000 habitantes y 9 muertes por cada 100000 habitantes. En los países en vía de desarrollo, como los latinoamericanos, se viene presentando un incremento en la incidencia de todos los tipos de cáncer, y en particular del colorrectal, en relación con el aumento de la población, cambio en los hábitos alimentarios y envejecimiento, entre otras (2).
El CCR es una entidad prevenible en la mayoría de casos si se realizan pruebas para la detección de lesiones precursoras. Se considera, por lo tanto, de gran importancia generar pautas para su prevención y detección temprana con las alternativas de tamización disponibles para su aplicación en la población colombiana (3). La evidencia científica actual ha demostrado que estas estrategias disminuyen la incidencia, morbilidad y mortalidad del CCR; además de ser una estrategia favorable en salud, también lo es desde el punto de vista social, con la esperanza que todos los colombianos con indicación puedan acceder al beneficio presentado con la certeza que el CCR es una enfermedad prevenible, y este debería ser un mensaje de pleno conocimiento público. También es importante insistir en el alcance del beneficio de la tamización, ya que se reconoce que hay diferencias en las tasas de prevención y resultados en la mortalidad en relación con la situación socioeconómica y tipo de cobertura por los prestadores de servicios de salud (4).
Por lo tanto, esta guía de práctica clínica (GPC) ofrece una posibilidad más para concientizar al personal de la salud en el énfasis de una prevención primaria que ayude a nuestra población a mantener su estado de salud. Adicionalmente, se busca mejorar la calidad de la colonoscopia con el fin de aumentar su utilidad en la prevención del CCR, por lo cual se deben implementar y monitorizar periódicamente las recomendaciones que la favorecen, ofrecer un servicio competente, personalizado, de alta calidad, que garantice que un paciente reciba un procedimiento apropiadamente indicado y seguro, con un mínimo riesgo.
MATERIALES Y MÉTODOS
El grupo desarrollador de la guía (GDG) diseñó una metodología rápida para la elaboración de esta guía. Para mayor información, la versión larga de la guía se encuentra en http://www.gastrocol.com/. El GDG contó con la participación de expertos temáticos en gastroenterología, cirugía, cirugía gastrointestinal, endoscopia, medicina interna, química farmacéutica, salud pública y diseño de políticas, así como expertos epidemiólogos. Además, el GDG recibió apoyo por parte de la Asociación Colombiana de Gastroenterología, el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia y el Grupo Cochrane STI; este último realizó la búsqueda sistemática de la literatura y la consecución de los estudios.
El GDG realizó una búsqueda sistemática de la literatura con el objeto de identificar todas las GPC nacionales e internacionales que abordaran la tamización de cáncer colorrectal. La búsqueda se realizó en TRIP database, Medline, EMBASE, biblioteca Cochrane, Lilacs y agencias especializadas, y se evaluó la calidad de las GPC recuperadas con el instrumento AGREE II (5). Una vez se obtuvo la calidad global de cada guía, se construyó una matriz de decisión que considera el tipo de guía, fecha de publicación, concordancia de los objetivos y alcance de la misma. Con base en los resultados de la matriz, se consideró que la guía sería desarrollada de novo.
Todas las preguntas a desarrollar se estructuraron en formato PICO (población, intervención, comparación y desenlaces). El primer paso fue la búsqueda de revisiones sistemáticas (RS) publicadas en las bases de datos especializadas hasta mayo de 2015. Las revisiones sistemáticas identificadas fueron evaluadas con la herramienta AMSTAR (6). La síntesis de los estudios seleccionados se realizó a través de la construcción de los perfiles de evidencia en www.guidleinedevelopment.org y los niveles de evidencia fueron graduados según la clasificación GRADE (alta, moderada, baja y muy baja) (7).
NIVEL DE EVIDENCIA
Calidad Global de la evidencia GRADE
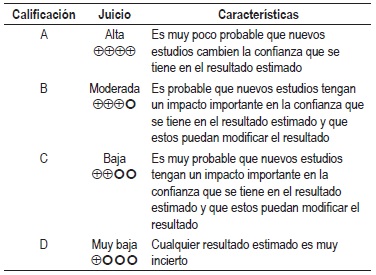
La graduación de la fuerza y dirección de cada recomendación se determinó con base en el nivel de evidencia y otras consideraciones adicionales que fueron revisadas en pleno por el GDG, el ente gestor y los grupos de interés. Este ejercicio se desarrolló mediante la construcción de una mesa de trabajo que generó la fuerza de la recomendación de acuerdo con:
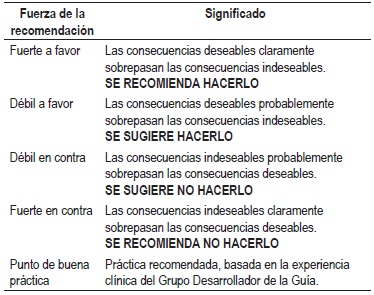
Las recomendaciones de la guía fueron socializadas en una reunión de expertos, entes gubernamentales y pacientes.
RECOMENDACIONES GENERALES
Pregunta 1: ¿cuál es la utilidad y seguridad de las pruebas para la tamización de cáncer colorrectal en pacientes adultos asintomáticos?
¿Cuál es la utilidad de la colonoscopia en la tamización de cáncer colorrectal en pacientes adultos asintomáticos?

Se desarrolló una RS en 2012 con el objetivo de comparar la efectividad y las tasas de adherencia de las diferentes opciones de tamización para la detección de neoplasias. Se incluyeron 14 ensayos clínicos aleatorizados (ECA) con un total de 197910 pacientes, y se identificaron las siguientes comparaciones:
- Sangre oculta en las heces por inmunoquímica (FIT) versus sangre oculta en las heces detectada con la técnica de guayaco (g-SOMF): la tasa de detección de neoplasias avanzadas es mayor con FIT (RR 1,94, IC 95% con rango de 1,37-2,76). La tasa de participación también fue más alta con FIT (RR 1,16, IC 95% con rango de 1,03-1,30)
- Colonoscopia versus sangre oculta detectada con guayaco: la colonoscopia se asoció con menor tasa de participación que las pruebas fecales (RR 0,67, IC 95% con rango de 0,56-0,80) pero representa una tasa de detección de neoplasias avanzadas más alta (RR 4,65, IC 95% con rango de 3,67-5,90)
- Colonoscopia versus g-SOMF/FIT: la detección de neoplasias fue mayor con colonoscopia (RR 5,91, IC 95% con rango de 3,35-10,42) pero las tasas de adherencia son mayores para g-SOMF/FIT (RR 0,57, IC 95% con rango de 0,42-0,78). Calidad de la evidencia: muy baja (12).
Un metaanálisis de 2014 comparó la técnica inmunológica de alta exactitud (TIAE) y la basada en guayaco para el análisis de sangre oculta en heces en 114764 pacientes mayores de 40 años, usando la colonoscopia como la prueba de oro. Los resultados mostraron que el método de detección inmunoquímico presentó mejor sensibilidad siendo de 0,872 (IC 95% con rango de 0,725-0,947) comparado con la técnica de guayaco con 0,668 (IC 95% con rango de 0,589-0,739) (13). Calidad de la evidencia: muy baja.
En el metaanálisis del 2014 se evaluó la efectividad de colonografía comparada con colonoscopia para la tamización de cáncer colorrectal con 5640 pacientes asintomáticos con edades entre los 57-65 años y con riesgos de CCR diferentes. La sensibilidad de la colonografía fue 66,8% (IC 95% con rango de 62,7-70,8) y para colonoscopia de 92,5% (IC 95% con rango de 89-95,2). La especificidad fue 80,3% (IC 95% con rango de 77,7-82,8) y de 73,2% (IC 95% con rango de 67,7-78,1) respectivamente. Se reportaron eventos adversos en 7 pacientes (0,21%) (8). Calidad de la evidencia: moderada.
En una RS de 2012 se incluyeron 16 estudios observacionales comparando la preferencia de los pacientes por colonoscopia versus colonografía por tomografía computarizada.(CTC) Algunas de las ventajas de la colonoscopia mencionadas por los pacientes es que se presenta la capacidad de visualizar directamente durante el examen, lo que permite una retroalimentación de los resultados; tiene la posibilidad de tomar biopsia o realizar polipectomía durante la misma sesión y tienen la posibilidad de dormir durante el examen. Las ventajas de la CTC incluyen que no es invasiva, es de corta duración, relativo menos dolor y es una nueva tecnología (9). Calidad de la evidencia: moderada.
Barreras y experiencias en la tamización con colonoscopia
Una RS del 2012 identificó las experiencias de los pacientes durante la tamización con colonoscopia. Se identificaron 56 estudios cualitativos y cuantitativos (10). Las principales barreras identificadas para realizar la tamización fueron:
- Molestias asociadas con el laxante
- Restricción en la dieta antes del procedimiento
- Ansiedad antes del procedimiento y anticipación del dolor, que fue menor de lo esperado cuando fueron entrevistados después del procedimiento
- Las mujeres se sienten más vulnerables
- Las mujeres prefieren mujeres endoscopistas y pueden esperar más tiempo la cita
- Los pacientes no tienen información sobre la importancia de seguir las recomendaciones y la importancia de la tamización
- Algunos pacientes reportan miedo de un resultado positivo
- Los pacientes consideran que toma tiempo laboral
- Los pacientes cuyos doctores recomiendan la tamización tienen un 30% más de probabilidad de programar la cita
Calidad de la evidencia: moderada.
¿Cuál es la utilidad de la copa transparente en el desempeño de la colonoscopia?
En una RS del 2013 se evaluó si la colonoscopia con copa transparente es mejor que la colonoscopia tradicional y mejora los tiempos de intubación cecal y la detección de pólipos. Se escogieron 14 ECA con 6713 pacientes. Se comparó el tiempo de intubación cecal (TCC) evidenciando que fue menor con TCC: -0,80 min (IC 95% con rango de 1,31-0,30) (11). Calidad de la evidencia: moderada.
Pregunta 2: ¿cuál es la utilidad de la prueba de sangre oculta para la tamización de cáncer de colon en población asintomática?
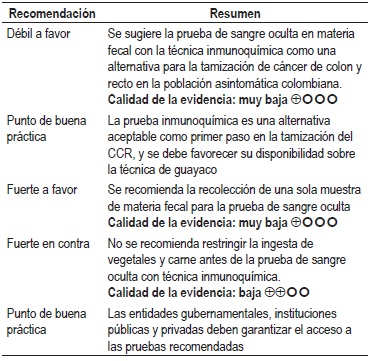
Restricciones para pacientes que son sometidos a sangre oculta
Una de las barreras de la prueba de sangre oculta son las restricciones en la dieta. Se identificó una RS del 2010 que evaluó si estas afectan la especificidad de la prueba de sangre oculta detectada con guayaco. Se identificaron 15 estudios observacionales, 4 ECA y un metaanálisis; los resultados no encontraron efectos en la ingesta de frutas y vegetales con alto contenido de peroxidasa; los ECA no mostraron efecto en la tasa de falsos positivos con o sin restricción dietaria (p >0,05) (14). Calidad de la evidencia: baja.
Pregunta 3: ¿cuál es la utilidad de los biomarcadores para la tamización de cáncer colorrectal en población asintomática?

Se encontró una RS del 2014 que evaluó la exactitud diagnóstica de los biomarcadores para la detección temprana de cáncer colorrectal y/o pólipos colorrectales en 9908 pacientes. La sensibilidad global para la detección de CCR de los marcadores fecales de ADN se encuentra entre el 53% y 87%; los biomarcadores en sangre (cambios epigenéticos) presentan una sensibilidad entre el 30% y 94%. Se concluye que los biomarcadores aún no tienen la sensibilidad y especificidad requerida para ser usados como prueba de primera elección para tamización de CCR (15). Calidad de la evidencia: baja.
Pregunta 4: ¿cuál es la utilidad de la colonografía virtual como prueba de tamización de cáncer colorrectal?

Se utiliza el término virtual para referirse a la colonografía por tomografía computarizada o resonancia magnética (RM). Una RS de 1285 pacientes evaluó la utilidad de la colonografía por RM (1,5T o 3T) para la detección de lesiones colorrectales en pacientes con riesgo promedio o riesgo aumentado de CCR comparado con colonoscopia. La sensibilidad global fue reportada en 86% (IC 95% con rango de 79-91) y la especificidad en 58% (IC 95% con rango de 28-76). Para pólipos con un tamaño de más de 10 mm, la sensibilidad fue de 88% (IC 95% con rango de 63-97) y especificidad de 99% (IC 95% con rango de 95-100); el 84% se consideraron de alta calidad (16). Calidad de la evidencia: muy baja.
Una RS del 2014 evaluó la tasa de perforación de colonografía CT y los predictores técnicos de complicaciones. Se incluyeron 103399 pacientes de Estados Unidos, Holanda, Italia, Australia, Inglaterra e Israel, de 121 centros. La tasa de perforación de colonografía CT global correspondió al 0,04% (IC 95% con rango de 0,00-0,10), siendo de 0,02% para pacientes asintomáticos y de 0,08% para pacientes sintomáticos. La tasa de perforación de pacientes con distensión manual del colon fue de 0,034% y de 0,032% en pacientes con insuflador de CO2 (p <0,05) (17). Calidad de la evidencia: baja.
Pregunta 5: ¿cuáles deben ser los intervalos de tamización de cáncer de colon después de una prueba negativa?

Una RS del 2012 evaluó el tiempo necesario para observar un beneficio en la sobrevida después de la tamización de CCR. Se identificaron 2 metaanálisis (Cochrane 2008 y US Preventive Task Force 2008) y 4 ensayos clínicos con 5000 pacientes mayores de 50 años que se sometieron a tamización con sangre oculta fecal o examen de sangre. Se encontró, después de 5 años de la tamización, que se previnieron 2,8 muertes (IC 95% con rango de 1,2-6,8) por cada 10000 personas tamizadas. El beneficio fue mayor 10 años después dado que se encontró la prevención de 23 muertes (IC 95% con rango de 3-42) por cada 10000 personas tamizadas. La RS recomienda que, para pacientes con una expectativa de vida menor a 10 años (75 años), no es necesario realizar tamización dado que los riesgos son mayores que los beneficios (18). Calidad de la evidencia: baja.
Una RS del 2014 determinó la prevalencia y factores de riesgo de cáncer colorrectal de intervalo (CCR que surge 6 a 36 meses después de la colonoscopia de tamización). Se incluyeron 12 estudios observacionales (139813 casos de CCR y 7912 de CRC de intervalo) que reportaron CCR en los pacientes 3 años después de la colonoscopia; la prevalencia de CRC de intervalo correspondió al 3,7% (IC 85% con rango de 2,8-4,9) (19). Calidad de la evidencia: baja.
Impacto de la calidad de la preparación de la colonoscopia en el tiempo de intervalo de la misma
Una RS del 2014 evaluó si los diferentes niveles de calidad de la preparación para la colonoscopia están asociados con las tasas de detección de adenomas, con el fin de apoyar la decisión de ajustar el intervalo de la colonoscopia. Se incluyeron 9 estudios (238 pacientes) donde se compararon los diferentes niveles de calidad de la preparación (alto, intermedio, bajo) y se encontró asociación entre la adecuada detección de adenocarcinomas y la preparación de calidad intermedia (OR 1,39, IC 95% con rango de 1,08-1,79) y alta (OR 1,41, IC 95% con rango de 1,21-1,64); no se encontraron diferencias entre la calidad de la preparación y los carcinomas en estadio avanzado. Con el fin de asegurar una adecuada tamización en pacientes que recibieron una preparación de calidad baja, se recomienda un intervalo más corto para repetir el procedimiento (20). Calidad de la evidencia: baja.
Pregunta 6: ¿cuál debe ser la preparación del intestino para la realización de la colonoscopia de tamización?

Una RS del 2013 evaluó la eficacia de la preparación en dosis dividida comparada con la preparación sin dividir tomada el día antes de la colonoscopia, se incluyeron 29 ECA con un total de 7719 participantes y se encontró que una adecuada preparación para la colonoscopia fue asociada de forma mayor con los pacientes que recibieron el régimen de dosis dividida (OR 0,85, IC 95% con rango de 0,82-0,88) comparada con los que recibieron la dosis completa (OR 0,63, IC 95% con rango de 0,55-0,71). La adherencia es mayor con el régimen de dosis dividida y sulfato de sodio (p <0,01) (21). Calidad de la evidencia: moderada.
Una RS del 2014 evaluó si los diferentes niveles de calidad de la preparación para la colonoscopia están asociados con las tasas de detección de adenomas, con el fin de apoyar la decisión de ajustar el intervalo de la colonoscopia. Se incluyeron 9 estudios (238 pacientes) donde se compararon los diferentes niveles de calidad de la preparación (alto, intermedio, bajo) y se encontró que no existen diferencias en la detección de adenocarcinomas con preparación de calidad alta o intermedia (OR 0,94, IC 95% con rango de 0,80-1,10). No se encontraron diferencias entre la calidad de la preparación y los carcinomas en estadio avanzado (20). Calidad de la evidencia: baja.
Una RS del 2014 desarrollada para el diseño de los estándares de colonoscopía del Centro de Cuidado de Cáncer de Ontario indica cuáles son los criterios de calidad para la ejecución de colonoscopias. En relación con el entrenamiento del personal, la evidencia encontrada de 3 GPC y 6 estudios primarios es consistente con respeto al perfil profesional del especialista que debe realizar las colonoscopias (gastroenterólogos entrenados con por lo menos 2 años de experiencia en centros certificados). También se identifica la relevancia de que todos los pacientes deben desarrollar protocolos para la preparación del paciente (evidencia de 5 GPC y 11 estudios primarios) que incluyan: evaluación de riesgo del paciente, consentimiento informado, prevención de infecciones, adecuado uso de la sedación, monitorización durante y después de la administración de la sedación, monitorización durante la recuperación, capacidad de reanimación, calidad de la endoscopia (22). Calidad de la evidencia: muy baja.
Pregunta 7: ¿cuál es la utilidad de colonografía por tomografía computarizada (CTC) luego de una prueba de sangre oculta fecal positiva en seguimiento?

Un metaanálisis del 2014 incluyó 622 pacientes con prueba de sangre oculta en heces positiva a quienes se les realizó una CTC de seguimiento, evidenciando una alta sensibilidad con 88,8% (IC 95% con rango de 83,6%-92,5%) para adenomas mayores de 6 mm o cáncer colorrectal, con baja heterogeneidad entre los estudios. La especificidad para la detección de adenomas y cáncer colorrectal fue menor y con mayor heterogeneidad entre los estudios, siendo de 75,4% (IC 95% con rango de 58,6-86,8%) (23). Calidad de la evidencia: baja.
ALGORITMO 1.
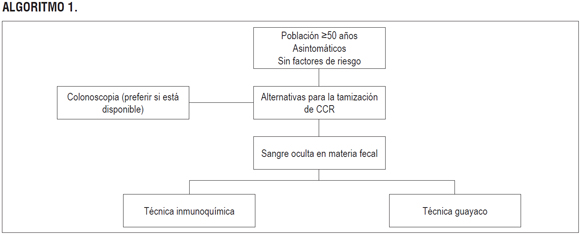
ALGORITMO 2.
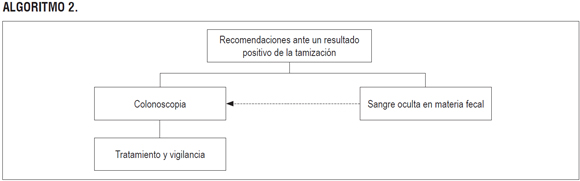
ALGORITMO 3.
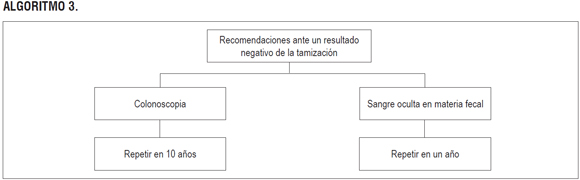
DECLARACIÓN DE CONFLICTOS DE INTERÉS
Los autores declaran no tener conflictos de interés, no estar involucrados como investigadores en ensayos clínicos en curso sobre el tema, y no haber recibido donaciones o beneficios por parte de los grupos interesados en las recomendaciones.
FUENTE DE FINANCIACIÓN
La presente guía fue desarrollada mediante un convenio de extensión entre la Asociación Colombiana de Gastroenterología y la facultad de Medicina de la Universidad Nacional.
REFERENCIAS
1. GLOBOCAN. Cancer Incidence, Mortality and Prevalence Worldwide. Descargado el 25 de Junio dee 2015 http://globocan.iarc.fr/old/burden.asp?selection_pop=40170&Text-p=Colombia&selection_cancer=5060&Textc=Colorectum&pYear=3&type=0&window=1&submit=%C2%A0Execute%C2%A0 [ Links ]
2. Winawer S, Zauber A, Ho M. Prevention of colon-rectal cancer by colonoscopic polypectomy. N Eng J Med. 1993;329:1977–81. [ Links ]
3. Zauberg A, Winawer SJ, OBrien M. Colonoscopic polypectomy and long-term prevention of colorectal-cancer deaths. N Eng J Med. 2012;366:687–96. [ Links ]
4. Citarda F, Tomaselli G, Capocaccia R, Barcherini S, Crespi M. Italian Multicentre Study Group. Efficacy in standard clinical practice of colonoscopic polypectomy in reducing colorectal cancer incidence. Gut. 2001;48:812–5. [ Links ]
5. AGREE C. INSTRUMENTO AGREE II. Instrumento para la evaluación de guías de práctica clínica [en línea] GuíaSalud. 2009. [acceso mayo 15 de 2015] [ Links ].
6. Shea BJ, Grimshaw JM, Wells GA, Boers M, Andersson N, Hamel C, et al. Development of AMSTAR: A measurement tool to assess the methodological quality of systematic reviews. BMC Med Res Methodol.2007;7(1):10. [ Links ]
7. Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, et al. GRADE: An emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 2008;336(7650):924-6. [ Links ]
8. Martín-López JE1, Beltrán-Calvo C, Rodríguez-López R, Molina-López T. Comparison of the accuracy of CT colonography and colonoscopy in the diagnosis of colorectal cancer. Colorectal Dis. 2014;16(3):O82-9. [ Links ]
9. McLachlan SA, Clements A, Austoker J. Patients experiences and reported barriers to colonoscopy in the screening context-a systematic review of the literature. Patient Educ Couns. 2012;86(2):137-46. [ Links ]
10. Lin OS, Kozarek RA, Gluck M, Jiranek GC, Koch J, Kowdley KV, Irani S, Nguyen M, Dominitz JA. Preference for colonoscopy versus computerized tomographic colonography: A systematic review and meta-analysis of observational studies. J Gen Intern Med. 2012;27(10):1349-60. [ Links ]
11. Westwood D, Alexakis N, Connor SJ. Transparent cap-assisted colonoscopy versus standard adult colonoscopy: A systematic review and meta-analysis. Dis Colon Rectum. 2012;55(2):218-12. [ Links ]
12. Hassan C, Rossi P, Camilloni L, Rex DK, Jimenez-Cendales B, Ferroni E, Borgia P, Zullo A, Guasticchi G; HTA Group. Meta-analysis: Adherence to colorectal cancer screening and the detection rate for advanced neoplasia, according to the type of screening test. Aliment Pharmacol Ther. 2012;36(10):929-40. [ Links ]
13. Launois R, Le Moine JG, Uzzan B, Fiestas Navarrete LI, Benamouzig R. Systematic review and bivariate/HSROC random-effect meta-analysis of immunochemical and guaiac-based fecal occult blood tests for colorectal cancer screening. Eur J Gastroenterol Hepatol. 2014; 26(9):978-89. [ Links ]
14. Konrad G. Dietary interventions for fecal occult blood test screening: systematic review of the literature. Can Fam Physician. 2010;56(3):229-38. [ Links ]
15. Shah R, Jones E, Vidart V, Kuppen PJ, Conti JA, Francis NK. Biomarkers for early detection of colorectal cancer and polyps: systematic review. Cancer Epidemiol Biomarkers Prev. 2014;23(9):1712-28. [ Links ]
16. Zijta F, Bipat S, Stoker J. Magnetic resonance (MR) colonography in the detection of colorectal lesions: A systematic review of prospective studies. Eur Radiol. 2010;20(5):1031-46. [ Links ]
17. Bellini D, Rengo M, De Cecco CN, Iafrate F, Hassan C, Laghi A. Perforation rate in CT colonography: a systematic review of the literature and meta-analysis. Eur Radiol. 2014; 24(7):1487-96. [ Links ]
18. Lee SJ, Boscardin WJ, Stijacic-Cenzer I, Conell-Price J, OBrien S, Walter LC. Time lag to benefit after screening for breast and colorectal cancer: meta-analysis of survival data from the United States, Sweden, United Kingdom, and Denmark. BMJ. 2013;346:e8441. [ Links ]
19. Singh S, Singh P, Murad M, Singh H, Samadder N. Prevalence, risk factors, and outcomes of interval colorectal cancers: A systematic review and meta-analysis. Am J Gastroenterol. 2014;109(9):1375-89. [ Links ]
20. Clark B, Rustagi T, Laine L. What level of bowel prep quality requires early repeat colonoscopy?: Systematic review and meta-analysis of the impact of preparation quality on adenoma detection rate. Am J Gastroenterol. 2014;109(11):1714-23. [ Links ]
21. Bucci C, Rea M, Ciacci C, Marmo R. Low Volume Split-Dose Before Colonoscopy for Bowel Preparation: A Systematic Review and a Series of Meta-Analysis of Randomized Controlled Clinical Trials. Gastroenterology. 2014;146(5): S736. [ Links ]
22. Tinmouth J, Kennedy E, Baron D, Burke M, Feinberg S, Gould M, Baxter N, Lewis N. Colonoscopy quality assurance in Ontario: Systematic review and clinical practice guideline. Can J Gastroenterol Hepatol. 2014;28(5):251-74. [ Links ]
23. Plumb A, Halligan S, Pendsé DA, Taylor SA, Mallett S. Sensitivity and specificity of CT colonography for the detection of colonic neoplasia after positive fecal occult blood testing: Systematic review and meta-analysis. Eur Radiol. 2014;24 (5):1049-58. [ Links ]













