Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.30 supl.1 Bogotá Dec. 2015
Guía de práctica clínica para la enfermedad hepática grasa no alcohólica
Clinical practice guideline for nonalcoholic fatty liver disease
Oscar A. Beltrán Galvis, MD,1 Andrés Galindo, MD2 Yuly Mendoza, MD,3 Geovanny Hernández, MD,4 Adriana Varón P. MD,5 Martín A. Garzón, MD6 Jhon Edison Prieto, MD,7 Rodrigo Pardo, MD,8, William Otero R. MD9, Luis Sabbagh MD.10
1Coordinador programa de gastroenterología, Fundación CardioInfantil. Profesor titular de gastroenterología, Universidad del Rosario. Bogotá-Colombia.
2Asistente de búsquedas del Grupo Cochrane de Infecciones Transmisión Sexual. Bogotá-Colombia.
3Fellow de gastroenterología, Universidad del Rosario. Bogotá-Colombia.
4Gastroenterólogo, Fundación CardioInfantil. Bogotá-Colombia.
5Profesor titular de gastroenterología, Universidad del Rosario. Jefe del servicio de hepatología, Fundación CardioInfantil. Bogotá-Colombia.
6Profesor titular de gastroenterología, Universidad del Rosario. Bogotá-Colombia.
7Profesor titular de gastroenterología, Fundación Universitaria Sánitas. Bogotá-Colombia.
8Director del Instituto de Investigaciones Clínicas, Universidad Nacional de Colombia. Bogotá-Colombia.
9Profesor titular de medicina, Coordinador de Gastroenterología, Universidad Nacional de Colombia. Ex-presidente Asociación Colombiana de Gastroenterología, Ex-presidente Asociación Colombiana de Endoscopia Digestiva. Miembro honorario Sociedad Dominicana de Gastroenterología. Miembro Honorario Sociedad Venezolana de Endoscopia Digestiva, Gastroenterólogo, Clínica Fundadores.
10Presidente de la Asociación Colombiana de Gastroenterología.
Contacto: Oscar Beltrán oscarbeltrangalvis@gmail.com
Resumen
Objetivo: brindar una guía de práctica clínica basada en la evidencia más reciente para el diagnóstico y tratamiento de la enfermedad hepática grasa no alcohólica teniendo en cuenta la efectividad y seguridad de las intervenciones dirigidas a pacientes, personal asistencial, administrativo y entes gubernamentales de cualquier servicio de atención en Colombia.
Materiales y métodos: esta guía fue desarrollada por un equipo multidisciplinario con apoyo de la Asociación Colombiana de Gastroenterología, el Grupo Cochrane ITS y el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia. Se desarrollaron preguntas clínicas relevantes y se realizó la búsqueda de guías nacionales e internacionales en bases de datos especializadas. Las guías existentes fueron evaluadas en términos de calidad y aplicabilidad; una guía cumplió los criterios de adaptación, por lo que se decidió adaptar 3 preguntas clínicas. El Grupo Cochrane realizó la búsqueda sistemática de la literatura. Las tablas de evidencia y recomendaciones fueron realizadas con base en la metodología GRADE. Las recomendaciones de la guía fueron socializadas en una reunión de expertos con entes gubernamentales y pacientes.
Resultados: se desarrolló una guía de práctica clínica basada en la evidencia para el diagnóstico y tratamiento de la enfermedad hepática grasa no alcohólica en Colombia.
Conclusiones: el diagnóstico y manejo oportuno de la enfermedad hepática grasa no alcohólica contribuirá a disminuir la carga de la enfermedad en Colombia, así como de las enfermedades asociadas.
Palabras clave
Hígado graso, enfermedad hepática, guía de práctica clínica (DeCS).
Abstract
Objective: To provide a clinical practice guideline with the latest evidence for diagnosis and treatment of nonalcoholic fatty liver disease for patients, caregivers, administrative and government bodies at all levels of care in Colombia.
Materials and Methods: This guide was developed by a multidisciplinary team with the support of the Colombian Association of Gastroenterology, Cochrane STI Group and Clinical Research Institute of the Universidad Nacional de Colombia. Relevant clinical questions were developed and the search for national and international guidelines in databases was performed. Existing guidelines were evaluated about quality and applicability. One guideline met the criteria for adaptation, so the group decided to adapt 3 clinical questions. Systematic literature searches were conducted by the Cochrane Group. The tables of evidence and recommendations were made based on the GRADE methodology. The recommendations of the guide were socialized in a meeting of experts with government agencies and patients.
Results: An evidence-based Clinical Practice Guidelines for the diagnosis and treatment of nonalcoholic fatty liver disease was developed for the Colombian context.
Conclusions: The opportune detection and appropriate management of nonalcoholic fatty liver disease would contribute to the burden of the disease in Colombia
Keywords
Fatty liver, hepatic disease, clinical practice guideline (DeCS).
ALCANCE
Esta guía de práctica clínica está dirigida a los profesionales de la salud que atienden directamente a los pacientes diagnosticados o con sospecha de enfermedad hepática grasa no alcohólica (EHGNA) en cualquier servicio de atención del país. Aborda aspectos relacionados con el diagnóstico, tratamiento y seguimiento de esta condición con el propósito de otorgar a los profesionales de la salud la más reciente evidencia respecto al diagnóstico, efectividad y seguridad de las diversas opciones terapéuticas, y establecer pautas de seguimiento.
La población objetivo de esta guía son los pacientes mayores de 18 años con sospecha diagnóstica o infección confirmada por EHGNA que sean tratados en cualquier nivel de atención. La guía no incluyó el manejo de pacientes con eventos adversos al tratamiento o pacientes gestantes o en lactancia.
Con el objetivo de brindar recomendaciones para el mejor manejo de la infección de la EHGNA en Colombia, esta guía está dirigida a todo el personal en salud asistencial y administrativo así como para quienes toman decisiones en salud, aseguradoras, pagadores del gasto en salud y aquellos que generan políticas en salud.
INTRODUCCIÓN Y JUSTIFICACIÓN
La enfermedad hepática grasa no alcohólica (EHGNA) es una de las enfermedades hepáticas más comunes en el mundo y la principal de los países occidentales (2). En comparación con décadas pasadas, la prevalencia de la EHGNA se incrementó de 2,8% a 46% y está asociada con la epidemia de obesidad y diabetes a nivel mundial. Asimismo, en el 2008 representó el 75% de todas las enfermedades hepáticas crónicas (1).
La definición de EHGNA requiere: a) evidencia de esteatosis hepática ya sea por imagenología o por histología, y b) que no existan causas secundarias de acumulación de grasa en el hígado como consumo de alcohol, uso de medicación esteatogénica o enfermedades hereditarias. En la mayoría de los pacientes, la EHGNA está asociada con obesidad, diabetes mellitus y dislipidemia. La EHGNA es histológicamente categorizada como hígado graso y esteatohepatitis no alcohólica; el hígado graso se define como la presencia de esteatosis hepática sin evidencia de daño hepatocelular, y la esteatohepatitis se define como la presencia de esteatosis hepática e inflamación con daño hepatocelular (balonamiento de los hepatocitos) con o sin fibrosis. Ella puede progresar a cirrosis, falla hepática y rara vez, a cáncer hepático (3).
Nos enfrentamos ante una entidad frecuente pero poco diagnosticada y manejada (1), es por ello que el desarrollo de la presente guía pretende reflejar mejores abordajes diagnósticos, enfoques terapéuticos y aspectos preventivos para médicos y profesionales de la salud, teniendo en cuenta la mejor evidencia basada en la literatura actual.
MATERIALES Y MÉTODOS
El grupo contó con la participación de expertos temáticos en gastroenterología, endoscopia, medicina interna, nutrición, química farmacéutica, salud pública y diseño de políticas. El Grupo Desarrollador de la Guía (GDG) recibió apoyo por parte de la Asociación Colombiana de Gastroenterología, el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia y el Grupo Cochrane STI; este último realizó la búsqueda sistemática de la literatura y la consecución de los artículos.
El GDG realizó una búsqueda sistemática de la literatura con el objeto de identificar todas las GPC nacionales e internacionales que abordaran el manejo de pacientes adultos con EHGNA. Se evaluó la calidad de las GPC recuperadas con el instrumento AGREE II (4); una vez se obtuvo la calidad global de cada guía, se construyó una matriz de decisión que considera el tipo de guía, fecha de publicación y concordancia de los objetivos y alcance de la misma (5). Con base en los resultados de la matriz de decisión, se consideró que la guía Korean Association for the Study of the Liver (KASL). KASL clinical practice guidelines: management of nonalcoholic fatty liver disease era la adecuada para ser sometida a proceso de adaptación al contexto colombiano.
Todas las preguntas a desarrollar (adaptadas o de novo) se estructuraron en formato PICO (población, intervención, comparación y desenlaces). El primer paso desarrollado fue la búsqueda metódica de revisiones sistemáticas publicadas en las bases de datos especializadas hasta mayo de 2015.
Las revisiones sistemáticas (RS) identificadas fueron evaluadas con la herramienta AMSTAR (6). En caso de no identificar revisiones sistemáticas de alta calidad, se procedió a la evaluación de estudios primarios utilizando la herramienta de riesgo de sesgos de Cochrane (7). La síntesis de los estudios seleccionados se realizó a través de la construcción de los perfiles de evidencia en www.guidleinedevelopment.org y los niveles de evidencia fueron graduados según la clasificación GRADE (alta, moderada, baja y muy baja) (8, 9).
NIVEL DE EVIDENCIA
Calidad Global de la evidencia GRADE
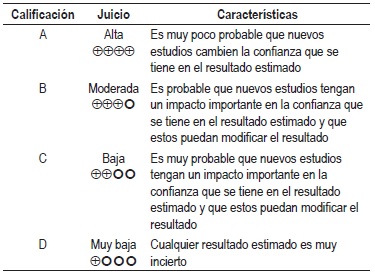
La graduación de la fuerza y dirección de cada recomendación se determinó con base en el nivel de evidencia y otras consideraciones adicionales que fueron revisadas en pleno por el GDG.
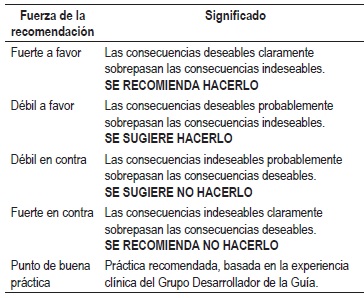
Las recomendaciones de la guía fueron socializadas en una reunión de expertos, entes gubernamentales y pacientes.
RECOMENDACIONES GENERALES
Pregunta 1: ¿cuál es la utilidad de las pruebas diagnósticas para predecir fibrosis hepática severa en los pacientes con EHGNA?

Dos revisiones sistemáticas (RS) (2011 y 2014) evaluaron las diferentes pruebas no invasivas para estadificar la EHGNA en comparación con la biopsia hepática y encontraron una muy buena precisión diagnóstica y reproducibilidad del FibroScan con curva ROC 0,94 (0,90-0,99), sensibilidad de 94% y especificidad de 95% para fibrosis avanzada (F3+). El único método no invasivo validado extensamente para detectar fibrosis avanzada fue el NALFD Fibrosis Score, que incluyó 13 estudios y mostró un resultado para fibrosis avanzada de con curva ROC 0,85 (0,80-0,93), sensibilidad de 90% y especificidad de 97% (10). La otra RS demostró con el FibroScan una moderada precisión para detectar fibrosis (F2+), con valores de sensibilidad y especificidad <80% y curva ROC de 0,79-0,87; la precisión mejoró con la detección de fibrosis F3+, con sensibilidad de 85%, especificidad 82% y curva ROC 0,76-0,98, y con la detección de cirrosis con sensibilidad y especificidad de 92%, curva ROC 0,91-0,99, y PPVs 41%-86%, NPVs 91%-100%. Calidad de la evidencia: moderada (11).
Pregunta 2: ¿cuál es la efectividad y seguridad de las intervenciones farmacológicas que disminuyen el riesgo de fibrosis hepática en los pacientes con EHGNA?
¿Cuál es la efectividad y seguridad de los sensibilizadores de la insulina en los pacientes con EHGNA?
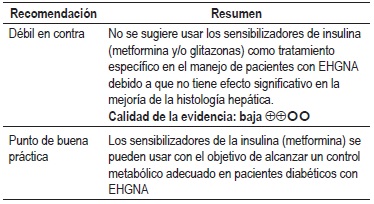
Una RS del 2013 evaluó 9 ensayos clínicos aleatorizados (ECA), 6 fueron en EHGNA y 3 en esteatohepatitis no alcohólica, donde se comparó la metformina con placebo u otra intervención para el tratamiento de EHGNA; no se observó mejoría en las variables de esteatosis, inflamación, balonización y fibrosis. En los resultados secundarios en los que se evaluaron las variables bioquímicas, los pacientes tratados con metformina mostraron reducción estadísticamente significativa de las aminotransferasas, en el modelo de homeostasis que valora la resistencia a la insulina (HOMA-IR) y en el IMC; sin embargo, la mejoría bioquímica en la reducción de ALT no se correlacionó con los hallazgos histológicos. Calidad de la evidencia: baja (12).
¿Cuál es la efectividad y seguridad de la vitamina E, vitamina D, pentoxifilina y ácido ursodesoxicólico (UDCA) en los pacientes con EHGNA?

Un ECA comparó la pioglitazona con vitamina E versus placebo para el tratamiento de EHGNA, en pacientes sin diabetes con esteatohepatitis confirmada con biopsia (n=247), mostrando un beneficio histológico. La vitamina E en altas dosis (800 U/día) fue efectiva y presentó mejoría de la esteatohepatitis, específicamente en la balonización hepatocelular, comparado con el grupo control (43% versus 19%, p = 0,001). Calidad de la evidencia: muy baja (13).
Una RS del 2014 incluyó 5 ECA que evaluaron los efectos de la pentoxifilina, 3 estudios homogéneos valoraron su efecto en los niveles séricos de AST (WMD: -9,70, IC 95% con rango de -15,24 a -4,16). Asimismo, los estudios mostraron reducción en el factor de necrosis tumoral alfa (FNT-α) (WMD: -0,66, IC 95%, con rango de -1,14 a -0,18) (14). Otra RS de 2014 mejoró los parámetros histológicos, la esteatosis (WMD = – 0,68; IC 95% con rango de 1,01 – 0,34), la inflamación lobular (WMD = – 0,49; IC 95%, con rango de 0,86 – 0,12), y la fibrosis (WMD = – 0,60; IC 95%, con rango de 0,99 – 0,21), así como también el IMC. Calidad de la evidencia: muy baja (15).
Una RS del 2012 incluyó 3 ECA, los cuales evaluaron el efecto del tratamiento con UDCA en dosis altas (12 – 28 mg/kg/día). Entre la respuesta histológica se observó solo mejoría en la inflamación lobular (WMD: - 0,23, IC 95%, con rango de -0,40 a -0,06). En conclusión, el UDCA no tiene un efecto positivo sustancial en la esteatohepatitis no alcohólica. Calidad de la evidencia: baja (16).
Una RS del 2013 evaluó la asociación entre los niveles de vitamina D, medidos como 25-hidroxivitamina D, y la EHGNA, encontrando que los pacientes con EHGNA tuvieron 1,26 veces más probabilidad de tener deficiencia de vitamina D (RR 1,26, IC 95% con rango de 1,17 - 1,35) comparado con sus controles. Al demostrar que el déficit de vitamina D es más prevalente en pacientes con EHGNA, se sugiere que esta vitamina juega un rol en esta enfermedad. Calidad de la evidencia: muy baja (19).
¿Cuál es la efectividad y seguridad de los probióticos en los pacientes con EHGNA?
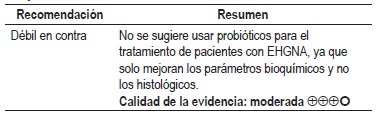
Una RS del 2013 evaluó el efecto de los probióticos en la EHGNA, los resultados mostraron que la terapia probiótica disminuyó significativamente la ALT (DMP -23,17, IC 95% con rango de -33,46 a -13,95, p <0,00001), el colesterol (DMP -0,28, IC 95% con rango de 0,55 a -0,01, p 0,04), la HDL (DMP -0,09, IC 95% con rango de -0,16 a 0,01, p 0,03), el FNT-α (DMP -0,32, IC 95% con rango de -0,48 a -0,17, p <0,0001) y el HOMA-IR (DMP -0,46, IC 95% con rango de -0,73 a -0,19, p 0,0008). Sin embargo, el uso de los probióticos no se asoció con cambios en el IMC (DMP 0,05, IC 95% con rango de -0,18 a 0,29, p 0,64), glucosa (DMP 0,05, IC 95% con rango de -0,25 a 0,35, p 0,76) y las lipoproteínas de baja densidad (LDL) (DMP -0,38, IC 95% con rango de -0,78 a 0,02, p 0,06), aunque este metaanálisis incluyó estudios que no evaluaron parámetros histológicos. Calidad de la evidencia: moderada (17).
¿Cuál es la efectividad y seguridad de las estatinas en los pacientes con EHGNA?

Una RS del 2013, que incluyó 2 ECA, evaluó los efectos benéficos o nocivos de la estatinas en pacientes con EHGNA. Los 2 ensayos clínicos mostraron que estas pueden mejorar los niveles de transaminasas séricas, así como los hallazgos ecográficos en pacientes con EHGNA; sin embargo, ninguno de los ensayos informó acerca de los cambios histológicos, morbilidad o mortalidad hepática relacionada. Calidad de la evidencia: baja (18).
¿Cuál es la efectividad y seguridad de la cirugía bariátrica en los pacientes con EHGNA?
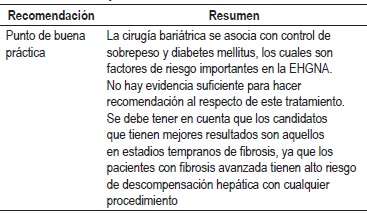
Dos RS del 2008 evaluaron el efecto de la cirugía bariátrica en la histología hepática de pacientes con EHGNA y mostraron que la esteatosis, esteatohepatitis y fibrosis mejoran después de la cirugía bariátrica (20); sin embargo, un metaanálisis Cochrane concluye que la falta de ensayos clínicos aleatorizados impide la evaluación definitiva de los beneficios y los efectos adversos de la cirugía bariátrica como enfoque terapéutico para los pacientes con EHGNA (21).
Pregunta 3: ¿cuál es la eficacia de las intervenciones no farmacológicas para disminuir el riesgo de fibrosis hepática severa en los pacientes con EHGNA?
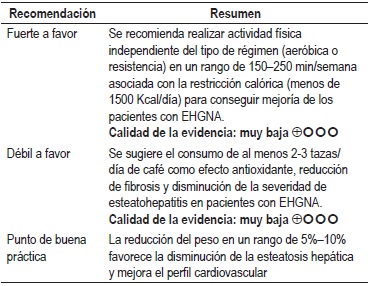
Una RS del 2012 evaluó las intervenciones con solo dieta, solo ejercicio y la combinación de dieta y ejercicio. Los estudios mostraron una fuerte correlación en la reducción en la grasa hepática y el descenso de la concentración de las aminotransferasas con la disminución de peso. Algunos estudios que reportaron cambios histológicos mostraron una tendencia a la disminución de la inflamación, y solo 1 estudio mostró una reducción significativa en la fibrosis. La mayoría de estudios mostraron mejoría en los controles de glucemia y en la sensibilidad a la insulina. Una reducción de peso de 4%-14% resultó en una reducción del 35%-81% de los triglicéridos intrahepáticos (TAGIH) (p <0,05). Calidad de la evidencia: muy baja (22).
Una RS del 2012 evaluó la eficacia del ejercicio aeróbico solo y/o entrenamiento de resistencia progresiva para la disminución de grasa en el hígado y de los niveles de la ALT en los adultos con EHGNA. Mostró un tamaño del efecto (TE) significativo en el subgrupo de ejercicio (TE = -0,37, IC 95% con rango de -0,06 a -0,69, p = 0,02); también demostró que las intervenciones de ejercicio per se reducen la grasa en el hígado a pesar de una mínima o ninguna pérdida de peso. Calidad de la evidencia: muy baja (23).
Una RS del 2014 evaluó el efecto de la fructosa como indicador de EHGNA. Aunque no presentó un efecto significativo en los estudios isocalóricos, en los lípidos intrahepatocelulares, ni efecto en los niveles séricos de ALT, la fructosa en los estudios hipercalóricos incrementó los lípidos intrahepatocelulares (DME 0,45, IC 95% con rango de 0,18 a 0,72) y los niveles de ALT (DM 4,94 U/L, IC 95% con rango de 0,03 a 9,85). Calidad de la evidencia: muy baja (24).
Un estudio prospectivo de 2015 evaluó la asociación entre el consumo de café y el inicio de EHGNA y no se encontró relación, pero sí evidenció que el consumo elevado de café se asoció con una menor proporción de fibrosis >F2 (8,8% versus 16,3%, p = 0,038); de igual forma, el análisis de regresión logística multivariado evidenció que un alto consumo de café está asociado con una probabilidad más baja de fibrosis (RR: 0,49, IC 95% con rango de 0,25-0,97, p= 0,041). Calidad de la evidencia: muy baja (25).
Pregunta 4: ¿cuál es pronóstico de los pacientes con EHGNA en relación con el riesgo de hepatocarcinoma, trasplante hepático, mortalidad cardiovascular y por enfermedad hepática en pacientes mayores de 18 años?
Mortalidad cardiovascular y por enfermedad hepática
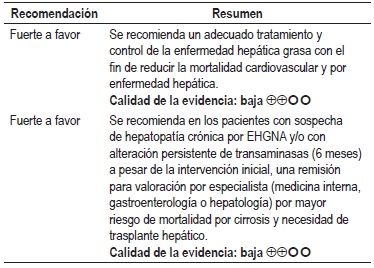
Una RS del 2011 determinó un aumento en la mortalidad en los pacientes con EHGNA comparado con la población general, con un RR 1,57 (IC 95% con rango de 1,18 a 2,10). Asimismo, cuando se realiza un análisis por subgrupos diferenciando la esteatosis simple y la esteatohepatitis no alcohólica (NASH) se observa un aumento en la mortalidad por enfermedad hepática en el grupo de pacientes con NASH, con un RR 5,71 (IC 95% con rango de 2,31 a 14,13). Sin embargo, esta diferencia no se observa cuando se estudia la mortalidad originada por enfermedad cardiovascular en estos 2 grupos (RR 0,91, IC 95% con rango de 0,42 a 1,98). Calidad de la evidencia: baja (26).
Trasplante hepático
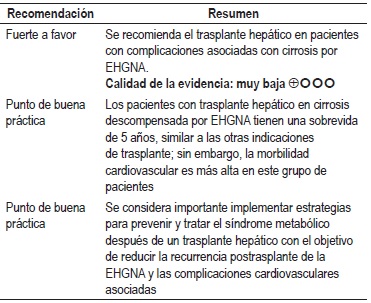
Una RS del 2014 evaluó los resultados en el postrasplante de pacientes sin EHGNA comparado con EHGNA y no se encontraron diferencias significativas en la sobrevida de los pacientes en 5 años en los 2 grupos (RR 1,09, IC 95% con rango de 0,77 a 1,56). Cuando se comparó la tasa de eventos cardiovasculares en estos 2 grupos, se observó la presencia de un desenlace más fuerte en los pacientes trasplantados hepáticos por EGNHA con un RR 1,65 (IC 95% con rango de 1,01 a 2,70). Finalmente, cuando se compara la mortalidad por falla del órgano trasplantado, se observa una baja mortalidad en el grupo de EHGNA, con RR 0,21 (IC 95% con rango de 0,05 a 0,89). Calidad de la evidencia: muy baja (27).
ALGORITMO 1.
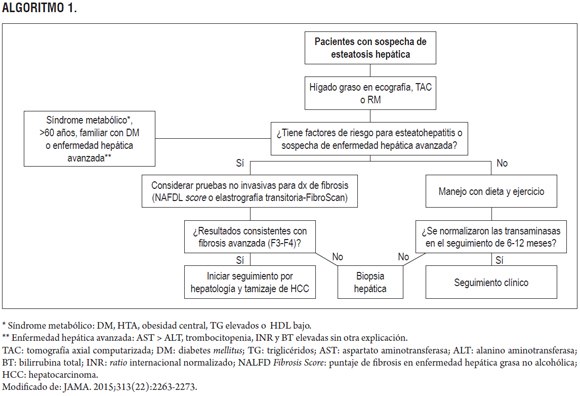
DECLARACIÓN DE CONFLICTOS DE INTERÉS
Los autores declaran no tener conflictos de interés, no estar involucrados como investigadores en ensayos clínicos en curso sobre el tema, y no haber recibido donaciones o beneficios por parte de los grupos interesados en las recomendaciones.
FUENTE DE FINANCIACIÓN
La presente guía fue desarrollada mediante un convenio de extensión entre la Asociación Colombiana de Gastroenterología y la facultad de Medicina de la Universidad Nacional.
REFERENCIAS
1. Diagnóstico y Tratamiento de la Enfermedad Hepática Grasa No Alcohólica del Adulto. México: Secretaría de Salud; 08/07/2014. Disponible en: http://www.cenetec.salud.gob.mx/descargas/gpc/CatalogoMaestro/719_GPC_enfermedad_hepatica_grasa_no_alcoholica/719GER.pdf [acceso 15 de mayo de 2015] [ Links ].
2. Méndez N, Gutiérrez Y, Chávez N et al. Hígado graso no alcohólico y esteatohepatitis no alcohólica. Conceptos actuales. Rev Gastroenterol México. 2010;75:143S-148S. [ Links ]
3. Chalasani N., Younossi Z., Lavine J., Mae Diehl A., Brunt A., Cussi K., Charlton M., Sanyal A. The diagnosis and Management of Non-alcoholic fatty liver disease: Practice Guideline by the American Association for the study of Liver Disease, American College of Gastroenterology, and The American Gastroenterological Association. Hepatology. 2012;55:2005-2023. [ Links ]
4. AGREE C. INSTRUMENTO AGREE II. Instrumento para la evaluación de guías de práctica clínica [en línea] GuíaSalud. 2009. [acceso 15 de mayo de 2015] [ Links ].
5. Guía Metodológica para la elaboración de Guías de Práctica Clínica con Evaluación Económica en el Sistema General de Seguridad Social en Salud Colombiano. In: Ministerio de la Protección Social, Centro de Estudios e Investigación en Salud de la Fundación Santa Fe de Bogotá editor. Bogotá, D.C.2013. [ Links ]
6. Shea BJ, Grimshaw JM, Wells GA, Boers M, Andersson N, Hamel C, et al. Development of AMSTAR: A measurement tool to assess the methodological quality of systematic reviews. BMC Med Res Methodol.2007;7(1):10. [ Links ]
7. Higgins JP, Green S. Cochrane handbook for systematic reviews of interventions: Wiley Online Library; 2008. [acceso 15 de mayo de 2015] [ Links ].
8. Brozek JL, Akl EA, Alonso-Coello P, Lang D, Jaeschke R, Williams JW, et al. Grading quality of evidence and strength of recommendations in clinical practice guidelines. Part 1 of 3. An overview of the GRADE approach and grading quality of evidence about interventions. Allergy. 2009;64(5):669-77. [ Links ]
9. Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, et al. GRADE: An emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 2008;336(7650):924-6. [ Links ]
10. Musso G, Gambino R, Cassader M, Pagano G. Meta-analysis: natural history of non-alcoholic fatty liver disease (NAFLD) and diagnostic accuracy of non-invasive tests for liver disease severity. Ann Med. 2011 Dec;43(8):617-49. [ Links ]
11. Kwok R, Tse YK, Wong GL, Ha Y, Lee AU, Ngu MC, Chan HL, Wong VW. Systematic review with meta-analysis: non-invasive assessment of non-alcoholic fatty liver disease-the role of transient elastography and plasma cytokeratin-18 fragments. Aliment Pharmacol Ther. 2014 Feb;39(3):254-69. [ Links ]
12. Li Y, Liu L, Wang B, Wang J, Chen D. Metformin in non-alcoholic fatty liver disease: A systematic review and meta-analysis. Biomedical Report. I: 2013;57-64. [ Links ]
13. Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, Bass NM, et al. Pioglitazone, vitamin E, or placebo for nonalcoholic steatohepatitis. N Engl J Med. 2010;362:1675-1685. [ Links ]
14. Du J, Ma Y, Yu CH, Li YM. Effects of pentoxifylline on nonalcoholic fatty liver disease: A meta-analysis. World J Gastroenterol. 2014; 20(2): 569-577. [ Links ]
15. Zeng T, Zhang CL, Zhao XL, Xie KQ. Pentoxifylline for the treatment of nonalcoholic fatty liver disease: A meta-analysis of randomized double-blind, placebo-controlled studies. Eur J Gastroenterol Hepatol. 2014 Jun;26(6):646-53. [ Links ]
16. Wu S, Li L, Wang J. Ursodeoxycholic acid for nonalcoholic seatohepatitis. Eur J Gastroenterol Hepatol. 2012, 24:1247–1253. [ Links ]
17. Ma YY, Li L, Yu CH, Shen Z, Chen LH, Li YM. Effects of probiotics on nonalcoholic fatty liver disease: A meta-analysis. World J Gastroenterol. 2013; 19(40): 6911-6918. [ Links ]
18. Eslami L, Merat S, Malekzadeh R, Nasseri-Moghaddam S, Aramin H. Statins for non-alcoholic fatty liver dis- ease and non-alcoholic steatohepatitis. Cochrane Database of Systematic Reviews 2013. [ Links ]
19. Eliades M et al. Meta-analysis: Vitamin D and non-alcoholic fatty liver disease. Aliment Pharmacol Ther. 2013; 38: 246–254. [ Links ]
20. Mummadi RR, Kasturi KS, Chennareddygair S, Sood GK. Effect of bariatric surgery on nonalcoholic fatty liver disease: Systematic review and meta-analysis. Clinical Gastro and Hepatol. 2008;6:1396-1402. [ Links ]
21. Chavez-Tapia NC, Tellez-Avila FI, Barrientose-Gutierrez T, Mendez- Sanchez N, Lizardi-Cervera J, Uribe M. Bariatric surgery for non-alcoholic steatohepatitis in obese patients. Cochrane Database of Systematic Reviews 2010, Issue 1. Art No: CD007340. DOI:10:1002/14641858. [ Links ]
22. Thoma C, Day CP,Trenell MI. Lifestyle interventions for the treatment of non-alcoholic fatty liver disease in adults: A systematic review. J Hepatol. 2012;56:255-266. [ Links ]
23. Keating SE, Hackett DA, George J, Johnson NA. Exercise and non- alcoholic fatty liver disease: A systematic review and meta-analysis. J Hepatol. 2012;57:157-166. [ Links ]
24. Chiu S, Sievenpiper JL, Souza RJ, et al. Effect of fructose on markers of non-alcoholic fatty liver disease (NAFLD): A systematic review and meta-analysis of controlled feeding trials. Eur J Clin Nutr. 2014;68:416–423. [ Links ]
25. Zelber-Sagi S. et al. Coffee consumption and nonalcoholic fatty liver onset: A prospective study in the general population. Translational Res. 2015: 165 (3):428- 435 [ Links ]
26. Musso G, Gambino R, Cassader M, Pagano G. Meta-analysis: Natural history of non-alcoholic fatty liver disease (NAFLD) and diagnostic accuracy of non-invasive tests for liver disease severity. Ann Med. 2011;43(8):617-649. [ Links ]
27. Wang X, Li J, Riaz DR, Shi G, Liu C, Dai Y. Outcomes of liver transplantation for nonalcoholic steatohepatitis: A systematic review and meta-analysis. Clin Gastroenterol Hepatol. 2014;12(3):394-402. [ Links ]













