Introducción
Las preparaciones herbales se utilizan desde el Antiguo Egipto y, desde entonces, sus formulaciones se han mantenido por siglos de forma empírica y por tradición oral 1. Los productos a base de plantas están disponibles en forma de raíces, semillas, hojas, tés, polvos, aceites, cremas, cápsulas e incluso inyectables 2. En las últimas 2 décadas su uso se ha incrementado a nivel mundial de manera exponencial, y en la actualidad se estima que más de 60 millones de personas los utilizan con costos que superan los 30 000 millones de dólares 3. Este impresionante mercado se debe fundamentalmente a que médicos y pacientes consideran que los remedios naturales están completamente libres de efectos secundarios por ser naturales.
Al respecto, con frecuencia se le explica a los pacientes que, aunque la gasolina proviene del petróleo (que es un producto natural), este último no se pude utilizar en los vehículos automotores porque primero debe ser sometido a complejos procesos de purificación para extraer la gasolina (que es el producto final). Así mismo, si en los componentes de las plantas existen sustancias benéficas, estas deber ser extraídas y purificadas para separarlas de otras sustancias tóxicas que también podrían estar presentes.
Es muy preocupante que se ignore el potencial hepatotóxico de esas sustancias, ya sea por un efecto directo o por interacción con otras sustancias o con medicamentos 4. Más de 1000 productos naturistas se han asociado con hepatotoxicidad y la lista continúa creciendo. Por su magnitud, se introdujo el término injuria hepática inducida por productos herbales (HILI), el cual es diferente a injuria hepática inducida por drogas (DILI) 5. La Red de Lesión Hepática Inducida por Drogas de los Estados Unidos encontró que aproximadamente el 15 % al 20 % de los casos reportados de lesión hepática inducida por medicamentos corresponden realmente al uso de productos naturistas 5,6. Datos globales revelan que la HILI aumentó de 7 % a 20 % entre 2004 y 2013 7. Sin embargo, no existen datos precisos de su frecuencia, debido a que los pacientes no reportan su uso, se automedican o son prescritos por personas sin formación 8. Es por esto que la hepatotoxicidad asociada con el uso de estos remedios muchas veces no se sospecha, se desconoce y puede pasar desapercibida. 9.
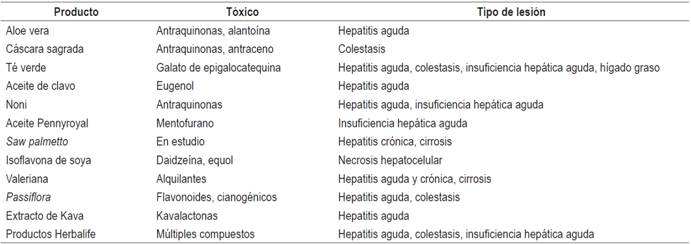
Por el gran peligro de esas sustancias y la preocupación al respecto se impulsó la creación del portal http://www.livertox.nih.gov/, que es una base de datos, con actualización permanente, en la cual se muestra en orden alfabético los diferentes productos implicados en el daño hepático y también los posibles mecanismos implicados en el mismo. En la Tabla 1 se muestran algunos de los productos más populares que se encuentran en esa lista.
Epidemiología
Se desconoce la verdadera incidencia de lesión hepática inducida por medicamentos naturistas y suplementos dietéticos, y los datos encontrados probablemente subestiman la realidad 10. La agencia de farmacovigilancia de Estados Unidos (EE. UU.) determinó que la incidencia anual en ese país es de 2,7 casos por cada 100 000 adultos 11. En un estudio de Corea que incluyó 371 casos reportados por 17 hospitales entre 2005 y 2007, la tasa de incidencia de pacientes con HILI que requirieron hospitalización fue de 5,8 pacientes por año 12. En Islandia hay datos confiables que muestran que la incidencia de HILI es de 3 casos por cada 100 000 personas 13. En el registro español se reportaron cifras más bajas, pero crecientes de HILI, oscilando entre el 2 % en 1998 y el 6 % en 2016 14.
En Alemania, un estudio que incluyó 51 hospitales de Berlín entre 2002 y 2011 reveló que 10 de los 198 casos de hepatotoxicidad se atribuyeron a productos naturales, lo cual corresponde al 5 % de los casos 15. En China, en una revisión que incluyó a 21 789 pacientes, los remedios naturales ocuparon el segundo lugar como causa de lesión hepática, solamente seguidos por los fármacos antituberculosos 16. En América Latina, los datos preliminares de la Red LATIN DILI mostraron que el 10 % de los casos de lesiones hepáticas agudas se atribuyó a productos naturistas, configurándose un problema de salud pública a nivel mundial 17.
Factores de riesgo para hepatotoxicidad
A diferencia de las medicinas convencionales, las preparaciones basadas en hierbas contienen diversos ingredientes en concentraciones desconocidas 18. El aumento inusitado de su consumo se puede atribuir a diversos factores que incluyen, entre otros, los siguientes: insatisfacción de los pacientes con el tratamiento médico y sus efectos adversos; y el fácil acceso a estos productos, ya que además de su bajo costo, no se requiere una fórmula médica para su adquisición 19.
El hígado es el principal órgano blanco involucrado en el desarrollo de toxicidad por remedios naturistas, esto se explica por los procesos metabólicos que allí ocurren 20. Esta alteración presenta un curso insidioso, caracterizado por un desenlace clínico variable e inespecífico. Hay varios casos reportados en los cuales algunos de ellos requirieron trasplante de hígado y otros murieron 5.
A diferencia de lo que se cree en la población general e incluso en algunos sectores de sociedades pseudocientíficas, las plantas tienen ingredientes activos o producen metabolitos secundarios que son tóxicos 21. El riesgo es aún mayor cuando se utilizan preparaciones que mezclan diferentes productos naturistas 22. Otras variables determinantes en el desarrollo de lesión y posterior daño hepático son el consumo excesivo, en dosis altas, o la toma de sustancias que omiten en la etiqueta su composición 23. Menos del 10 % de los productos a base de compuestos naturistas está verdaderamente estandarizado con el conocimiento de sus componentes activos 24. Adicional a todos estos factores mencionados, al interior de las compañías que fabrican remedios naturistas existe la creencia de que los metales pesados como el plomo, el mercurio, el cadmio o el arsénico podrían mejorar la efectividad de los productos y son utilizados frecuentemente como parte de sus ingredientes 25.
Patogénesis y clasificación
La hepatotoxicidad es la reacción adversa más frecuente a los remedios naturistas y ocurre en individuos susceptibles 26. Las alteraciones generalmente son transitorias y autolimitadas, aunque se han descrito casos de enfermedad hepática crónica e insuficiencia hepática aguda 27. Clínicamente son similares a las producidas por medicamentos 28. Ambas categorías de daño hepático tienen en común que son originadas por sustancias químicas de productos naturales o sintetizadas, las cuales son extrañas al organismo y requieren ser metabolizadas para su eliminación 29. En muchas de esas preparaciones hay 2 componentes biológicos principales que están asociados con el daño hepático, los alcaloides y los flavonoides 30. Su interacción con las diferentes isoformas del citocromo P-450 desencadenan actividades inflamatorias y oxidativas como la principal vía de injuria hepática 31.
Dependiendo del mecanismo involucrado existen 2 tipos de HILI: la idiosincrática, caracterizada por ser impredecible, de curso largo y dependientes de la dosis; y la intrínseca, que se desarrolla como una reacción predecible a una dosis terapéutica o sobredosis con cortos períodos de latencia y alta incidencia entre los consumidores de productos naturistas 32.
La instauración de la HILI en relación con la temporalidad de su instauración también puede ser aguda o crónica dependiendo de que la alteración o daño hepático tenga una evolución menor a 6 meses o mayor a 6 meses, respectivamente 33. Desde el punto de vista bioquímico, el daño puede ser predominantemente hepatocelular (elevación de aminotransferasas), colestásico (elevación de fosfatasa alcalina) o mixto 34.
Una consideración importante en el manejo de la HILI es que la posibilidad y el porcentaje de individuos en quienes la lesión se vuelve crónica es más alto que el daño hepático inducido por drogas (DILI) 35.
Manifestaciones clínicas
El espectro de la enfermedad es variable, su presentación clínica es inespecífica, los síntomas predominantes son gastrointestinales e incluyen náuseas, vómitos y dolor abdominal; pueden ocurrir alteraciones asintomáticas del perfil hepático hasta casos severos con injuria hepática aguda, insuficiencia hepática fulminante 36 o complicaciones derivadas de enfermedad hepática avanzada o cirrosis 37. Cuando los pacientes dejan de usar el producto, los signos clínicos comienzan a disminuir con posterior normalización del perfil hepático 38. En una serie de 27 casos de HILI por medicamentos naturistas, el patrón de daño hepático fue el siguiente: 82 % hepatocelular, 11 % colestásico, y mixto en el 7 % 39.
Diagnóstico
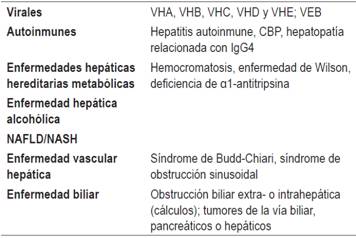
La HILI es un diagnóstico de exclusión que implica una alta sospecha clínica, seguida de una evaluación del perfil hepático para establecer el tipo de lesión 19. Sus manifestaciones clínicas e histopatológicas son similares a las demás causas de enfermedad hepática aguda o crónica (Tabla 2) 40, las cuales deberán ser descartadas dependiendo de las características del paciente.
CBP: colangitis biliar primaria; NAFLD: enfermedad del hígado graso no alcohólica; NASH: esteatohepatitis no alcohólica; VEB: virus de Epstein-Barr; VHA: virus de la hepatitis A; VHB: virus de la hepatitis B; VHC: virus de la hepatitis C; VHD: virus de la hepatitis D; VHE: virus de la hepatitis E.
Las características que sugieren hepatotoxicidad inducida por remedios homeópatas incluyen la ausencia de enfermedad antes de ingerir el medicamento naturista, el desarrollo de la enfermedad o de las alteraciones bioquímicas después de comenzar su uso y la mejoría que ocurre después de retirar el producto 41. No existe un estándar de oro, ni pruebas específicas, ni biomarcadores séricos para confirmar un diagnóstico de lesión hepática inducida por remedios naturistas. Se han validado varias herramientas de diagnóstico, pero todavía es difícil probar la causalidad relacionada con un fármaco específico; por ende, se debe procurar descartar otras causas de enfermedad hepática 20.
Es imperativo que en la anamnesis se pregunte específicamente sobre el consumo de tales sustancias, ya que los pacientes no las reconocen como medicamentos y usualmente las consideran tan inofensivas que es innecesario mencionarlas. Además, no es infrecuente que los pacientes estén tomando múltiples preparaciones, lo que hace imposible la identificación de un solo tóxico causal 42. Además, se ha encontrado que, en el curso agudo del daño hepático, el paciente motu proprio incremente las dosis de los mismos para ayudar a tratar los nuevos síntomas 43.
Se han desarrollado varias escalas que intentan codificar la causalidad de la toxicidad del fármaco con criterios objetivos. Las más conocidas son la de Naranjo (Tabla 3) y el método de evaluación de la causalidad de Roussel Uclaf (RUCAM; disponible en http://www.rccc.eu/scores/RUCAM.html). Los estudios que han comparado estos modelos sugieren que la escala RUCAM puede tener mejor capacidad discriminatoria. Aunque estas escalas no han sido validadas en el ámbito de los medicamentos herbales, con frecuencia son utilizadas como una ayuda clínica 44.
*La relación de causalidad de una reacción adversa está determinada por el puntaje total, el cual puede obtener un valor entre 4 y +13, considerándose probada o definida un puntaje >9; probable, 5-8; posible, 1-4 puntos; o dudosa 0 o menos. Tomado de: Naranjo CA, du Souich P, Busto UE. Métodos en farmacología clínica. OPS; 1992.
Biopsia hepática
En las series de casos reportados con HILI se han hecho descripciones histológicas detalladas de los hallazgos patológicos más frecuentes como hepatitis, necrosis, infiltrados de esosinófilos, fibrosis y colestasis 45. Sin embargo, la biopsia hepática no se considera rutinariamente útil 46 ya que no aporta información relevante para el manejo de los pacientes y puede generar complicaciones adicionales 47, por lo que no se recomienda como método rutinario de apoyo para evaluar los casos de HILI y se reserva solo a los casos de presentación clínica atípica 48.
Tratamiento
El pilar del tratamiento es retirar el tóxico administrado y vigilar al paciente estrechamente, hasta la resolución de los síntomas 49. La identificación temprana es fundamental, ya que puede modificar el pronóstico y la evolución de la enfermedad 50. En la mayoría de los pacientes la recuperación ocurre después de descontinuar el producto y el manejo médico recomendado es sintomático 51.
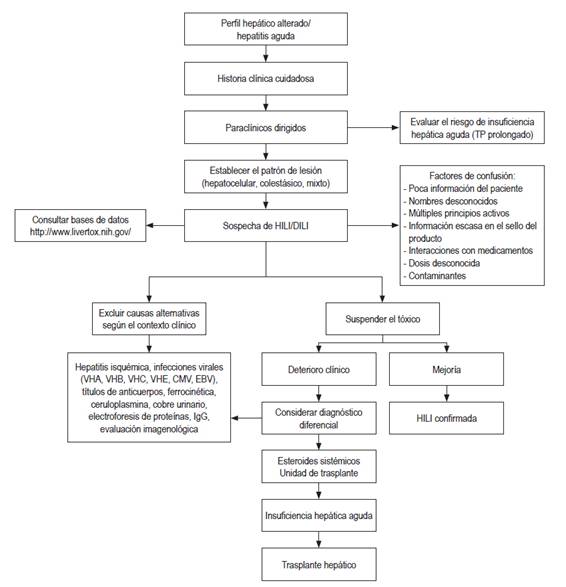
Los esteroides sistémicos, aunque son utilizados frecuentemente, no tienen beneficio comprobado en la mayoría de las formas de hepatotoxicidad; aunque podrían ser útiles en el tratamiento de pacientes con reacciones de hipersensibilidad 52. Los casos severos con insuficiencia hepática fulminante requieren manejo en unidades de trasplante hepático, ya que la mortalidad sin trasplante es cercana al 80 % 53. Hay alteraciones del perfil hepático que orientan hacia la posibilidad de progresar a insuficiencia hepática aguda en el contexto de HILI 54, y son la elevación de la bilirrubina total 2 veces por encima del límite superior normal asociado con una elevación de las aminotransferasas 3 veces por encima del límite superior. Estos hallazgos obligan a una hospitalización para garantizar una vigilancia más estrecha 55. En la Figura 1 se muestra un algoritmo sugerido para el manejo de los pacientes.
Conclusión
El público no médico tradicionalmente considera que los productos herbales son seguros porque son naturales. Sin embargo, tal creencia es absolutamente errónea, ya que tales sustancias, o remedios naturistas, pueden producir reacciones adversas graves e incluso fatales. Lamentablemente, se distribuyen en el mercado sin el respaldo de ensayos clínicos controlados que demuestren su eficacia y su seguridad, y más grave aún, sin la supervisión rigurosa de los entes reguladores que tengan la capacidad científica para entender la problemática y que tengan el conocimiento suficiente para entender las características químicas de sus principios activos y el metabolismo de los mismos, tal y como ocurre con medicamentos convencionales alopáticos.
Su composición y calidad es variable, por lo que la evaluación de la causalidad es un verdadero reto diagnóstico. Los productos que contienen múltiples ingredientes pueden causar daños hepáticos más graves, en comparación con los que tienen un solo ingrediente. Se han creado registros nacionales y redes de investigación multicéntricos para superar limitaciones como un amplio espectro de fenotipos, gravedad, reacciones idiosincrásicas y susceptibilidad individual.
La eficacia y seguridad de los productos a base de hierbas siguen siendo inciertas hasta el momento. Las repercusiones clínicas pueden ser graves e incluso letales, siendo el hígado el principal órgano comprometido.
Aún se necesitan muchos estudios clínicos para determinar su eficacia, aclarar sus mecanismos de acción y los riesgos derivados de su uso. Por lo anterior, nuestra recomendación es que se suspenda de manera inmediata la comercialización, prescripción y usos de tales compuestos. Los respectivos permisos para su uso y prescripción deben esperar los resultados de ensayos clínicos rigurosos que demuestren su potencial terapéutico. Así mismo, motivar a los médicos para que informen y registren a los pacientes con hepatotoxicidad secundaria a HILI que con frecuencia son identificados. También deben informarse a los entes reguladores todas las reacciones adversas documentadas relacionadas con esas sustancias.











 texto em
texto em