Introducción
En el intestino delgado (ID) se producen de 2 %-10 % de los sangrados gastrointestinales (SGI) 1,2,3. Sin embargo, cuando la endoscopia digestiva alta (EVDA) y la colonoscopia total (CLNT) no identifican su lugar de origen, en el 77 % de los casos será el ID 4-7.
En el pasado, cuando los exámenes endoscópicos iniciales no encontraban la etiología del sangrado, el cuadro se denominaba sangrado gastrointestinal de origen oscuro (SGIO) 8. A su vez, el SGIO podía ser oculto si su manifestación era anemia ferropénica o se detectaba sangre oculta en las heces, o manifiesto si había manifestaciones clínicas del sangrado como melenas, rectorragia o hematoquecia 8. Actualmente la nomenclatura ha cambiado: cuando los procedimientos endoscópicos son negativos, el cuadro se denomina posible sangrado de intestino delgado (PSID), reservándose el término SGIO para la situación en la cual la EVDA, la CLNT y los exámenes que evalúan el ID son negativos 9.
Las causas más comunes de sangrado de ID en pacientes con PSID son las angiectasias (20 %-55 %), especialmente en ancianos, seguidas por los tumores (10 %-20 %) y la enfermedad de Crohn (EC) (2 %-10 %) 10. Otras causas menos frecuentes incluyen la enfermedad celíaca, divertículo de Meckel, enteropatía por antiinflamatorios no esteroideos (AINE), lesión de Dieulafoy, várices ectópicas, enteropatía hipertensiva portal o enteritis por radiación 10.
La evaluación del ID se puede realizar con diferentes métodos, principalmente enteroscopias, enterorresonancia y videocápsula endoscópica (VCE) 9. Desde su introducción, la VCE ha facilitado la evaluación del ID y en la actualidad se le considera el examen de elección para el estudio de enfermedades de este segmento 11,12. No obstante, varios autores y guías recomiendan repetir la EVDA y la CLNT antes de iniciar el estudio del ID en varios pacientes con PSID 9,13. Este abordaje surge de varios estudios en estos pacientes en quienes con diferentes métodos de evaluación del ID se ha encontrado la causa del sangrado al alcance de la EVDA o de la CLNT en el 2 %-25 % y 6 %-23 %, respectivamente 14,15,16. Publicaciones de nuestro medio también recomiendan ese abordaje 17. Sin embargo, ese enfoque ha sido controvertido por varios autores, incluyendo algunos de nuestro país, quienes consideran la VCE como primera línea de evaluación en este grupo de pacientes 10,18,19.
El objetivo de la presente revisión es la descripción y evaluación de la utilidad de la VCE como método de estudio de elección del PSID, después de un primer examen endoscópico alto y bajo negativos, comparándola con el abordaje más tradicional de una segunda endoscopia alta y baja, y también con otros métodos de evaluación del ID.
Metodología
Se realizó una búsqueda bibliográfica en la base de datos PubMed desde los últimos 5 años hasta el 14 de mayo de 2018 utilizando los siguientes términos y metodología “(((((Capsule Endoscopes OR Capsule Endoscope OR Endoscope, Capsule OR Endoscopes, Capsule OR Video Capsule Endoscopes OR Capsule Endoscope, Video OR Capsule Endoscopes, Video OR Endoscope, Video Capsule OR Endoscopes, Video Capsule OR Video Capsule Endoscope))) AND ((Endoscopy, Digestive System OR Digestive System Endoscopies OR Digestive System Endoscopy OR Endoscopies, Digestive System OR Digestive System Endoscopic Surgical Procedures OR Endoscopic, Digestive System, Surgery OR Endoscopic, Digestive System, Surgical Procedure OR Procedure, Digestive System, Endoscopic, Surgical OR Surgical Procedures, Endoscopic, Digestive System OR Procedures, Digestive System, Endoscopic, Surgical OR Procedures, Endoscopic, Digestive System, Surgical OR Surgery, Digestive System Endoscopic OR Surgery, Endoscopic, Digestive System OR Surgical Procedure, Endoscopic, Digestive System OR Digestive System Endoscopic Surgery OR Procedure, Endoscopic, Digestive System, Surgical OR Esophagogastroduodenoscopy OR Esophagogastroduodenoscopies OR Colonoscopy OR Colonoscopies OR Colonoscopic Surgical Procedures OR Colonoscopic Surgical Procedure OR Procedure, Colonoscopic Surgical OR Procedures, Colonoscopic Surgical OR Surgical Procedure, Colonoscopic OR Surgery, Colonoscopic OR Surgical Procedures, Colonoscopic OR Colonoscopic Surgery OR Colonoscopic Surgeries OR Surgeries, Colonoscopic)))) AND ((((Intestine, Small OR Intestines, Small OR Small Intestines OR Small Intestine OR Duodenum OR Ileum OR Jejunum OR Small Bowel))) AND ((Hemorrhage OR Hemorrhages OR Bleeding)))”, especificando la presencia en el título o resumen para cada uno de los términos de la búsqueda, sin límite de fechas, solo en los idiomas español o inglés. Posteriormente, se revisaron los títulos y resúmenes de todos los resultados para identificar los artículos que al concepto de los autores merecieran su revisión total. Adicionalmente, se revisaron algunas referencias de los artículos seleccionados y algunos artículos y guías del conocimiento de los autores.
Resultados
VCE
La VCE se concibió hace más de 30 años y, posteriormente, desarrolló de forma simultánea por dos grupos independientes, uno israelí y otro inglés 20,21,22. Desde entonces se ha convertido en un excelente método de visualización del tracto gastrointestinal, especialmente del ID, donde otros métodos tienen problemas de rendimiento o de facilidades logísticas en su aplicación 17,23. Su refinamiento tecnológico no ha cesado desde su concepción y los nuevos modelos permiten un mejor desempeño y diferentes utilidades 11,24,25. En la actualidad hay varios modelos disponibles para examinar los diferentes segmentos gastrointestinales, de los cuales PillCam es el primero y el más estudiado (GivenImaging®; Yoqneam, Israel) (Tabla 1) 26.
Tabla 1 VCE disponibles en el mercado 22
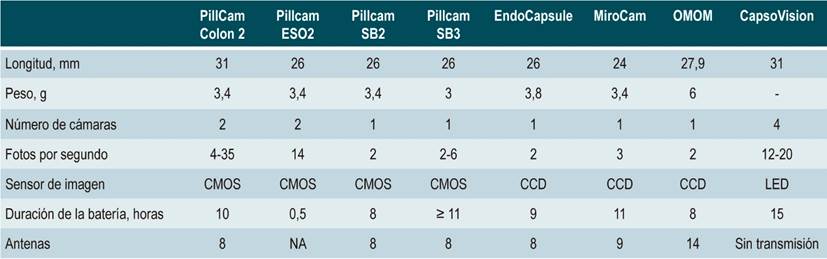
CCD: dispositivo de carga acoplada; CMOS: semiconductor complementario de óxido metálico; ESO: esófago; LED: diodo emisor de luz; SB: small bowel. Modificado de: Gerber J et al. Gastrointest Endosc. 2007;66(6):1188-95.
Con el paso de los años la visualización del ID por la VCE ha venido encontrando aplicaciones en el diagnóstico y seguimiento de diversas patologías como la EC, enfermedad celíaca, tumores del ID y enteropatía inducida por los AINE, entre otras 27-30. Así mismo, este método permite identificar la causa de la anemia ferropénica hasta en el 66 % de los pacientes que no tienen una causa aparente de la misma 31-33. En la última década se ha ampliado su uso, sugiriéndola incluso como una estrategia para la tamización de cáncer colorrectal 26,34, esófago de Barrett 35-37 y várices esofágicas 38,39, entre otras 40. Más recientemente se ha estudiado la posibilidad de utilizarla, adicionalmente, como un instrumento terapéutico en la hemorragia de vías digestivas, como una VCE intraoperatoria en tiempo real 41. Estas utilidades dependerán de que se logren los refinamientos tecnológicos necesarios, cuyo desarrollo es un foco de intensa investigación 11,25.
Por su alta sensibilidad en la evaluación del ID, en 2003 la Food and Drug Administration (FDA) removió su indicación previa como método coadyuvante para el estudio intraluminal del ID, designándolo como primera línea 12. En 2006 el comité de tecnología de la American Society for Gastrointestinal Endoscopy (ASGE) concluyó que la VCE tenía un rendimiento superior a los estudios radiológicos con contraste y a la enteroscopia de empuje (EE) en evaluación de PSID 33. Desde entonces, se ha insistido en que es el método de elección para la visualización del ID después de descartar que la fuente del SGI sea alta o baja 13,33,42, siendo incluso considerada el estándar de oro en PSID por algunos 23,43. Como tal, el PSID actualmente es la indicación más frecuente de VCE (66 %) 11,44. La posibilidad de encontrar la causa del sangrado en el ID en estos pacientes oscila entre 35 %-77 % 6, dependiendo de si el sangrado es oculto o manifiesto. En una serie de 100 pacientes con PSID se encontró una causa de sangrado en el 12 % de los pacientes con sangrado manifiesto previo, en el 44 % de los pacientes con sangre oculta en las heces y anemia ferropénica, y en el 92 % de los pacientes con sangrado manifiesto actual 45.
Evaluación del ID frente a una segunda endoscopia alta o baja
Cuando un examen endoscópico previo alto y bajo es negativo, la posibilidad de que la fuente sea el ID es mayor a que sea el tracto gastrointestinal superior o inferior (Tabla 2) 10. Por lo tanto, se ha considerado que el ID debería ser el próximo órgano a estudiar, lo que ha sido corroborado por la frecuencia con la que se encuentran causas de sangrado en los pacientes sometidos a VCE en comparación con los que se someten a una segunda EVDA y CLNT. Un estudio australiano encontró que al repetir la EVDA y CLNT solo encontraba una lesión pasada por alto en el 4 % de los pacientes, mientras que la VCE encontró alguna lesión causante probable o posible en por lo menos el 62 % 18.
Por su parte, en casos de PSID se ha encontrado que la EE identifica lesiones que estaban al alcance de la EVDA en el 10 %-64 % de los casos 14,15,46,47. Así mismo, con la enteroscopia con doble balón (EDB), se identifican lesiones en el 24 %-25 % que también estaban al alcance de una EVDA 5,48 y en el 7 % de los casos al alcance de una CLNT 5. Con la VCE ocurre algo similar, al encontrar que en el 2 %-14 % de los pacientes, las causas estaban al alcance de una EVDA 45,49-55. No obstante, es necesario tener en cuenta dos elementos fundamentales: el primero, que el rendimiento de la VCE y otros métodos de estudio del ID sigue siendo mayor a una segunda endoscopia en casi la totalidad de escenarios 18,42; y el segundo, aunque esas lesiones estaban al alcance de una posible nueva endoscopia, estos estudios no demostraron que las mismas fueran encontradas con la endoscopia, sino con un método alternativo.
Tabla 2 Causas de sangrado en PSID 10
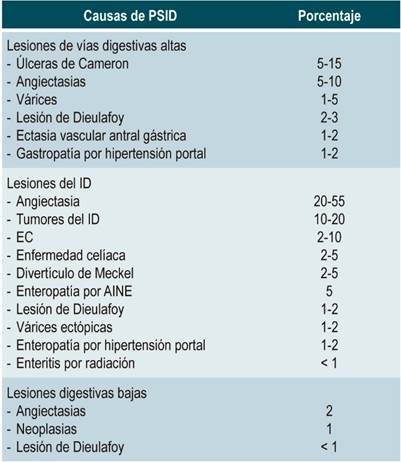
Modificado de: Liu K et al. Aliment Pharmacol Ther. 2011;34(4):416-23.
Dentro de las causas del rendimiento de la VCE se ha propuesto que al no insuflar aire y no distender los segmentos gastrointestinales, este examen sería una endoscopia fisiológica y tendría más posibilidades de identificar lesiones como ectasias vasculares, las cuales la endoscopia convencional no identificaría. Así mismo, para la visualización de muchas de estas lesiones, se necesita perseverancia, dedicación y tiempo. Los endoscopistas atareados frecuentemente no disponen del tiempo suficiente para inspeccionar minuciosamente el estómago, incluida una adecuada retrovisión y, en el caso del colon, puede suceder que no se cercioren de que realmente han alcanzado el ciego 42,51.
En 2010 la Sociedad Americana de Endoscopia Gastrointestinal recomendó repetir la EVDA en casos de PSID si la presentación era sospechosa de sangrado alto, repetir la colonoscopia si era sospechosa de sangrado bajo o proceder inmediatamente con la VCE si no se sugería ninguno de los dos 56. Sin embargo, indicó también que en la mayoría de casos la VCE era una primera opción razonable 56. Otros autores han sugerido repetir las endoscopias alta y baja solo si el endoscopista es consciente de no haber realizado una adecuada visualización de las vías digestivas altas o bajas, respectivamente 10.
La Sociedad Europea de Endoscopia Gastrointestinal publicó en 2006 una actualización de sus guías, en la cual sugiere ambiguamente que la VCE es el método de elección en PSID 57. Finalmente, las guías más recientes del Colegio Americano de Gastroenterología (ACG) sobre diagnóstico y manejo de sangrado de ID, publicadas en 2015, recomiendan repetir la EVDA en PSID si el paciente presenta melenas o hematemesis, así como también si en la primera EVDA no se visualizó adecuadamente la mucosa, y repetir la colonoscopia si hay hematoquecia recurrente, sospecha de origen bajo o, nuevamente, si en la primera colonoscopia no hubo adecuada inspección de la mucosa 57. Sin embargo, como lo reconocen los autores de las guías, tales recomendaciones tienen un nivel de evidencia “bajo” o “muy bajo” y están basadas en los hallazgos de causas de PSID que estaban al alcance de los métodos endoscópicos convencionales al usar métodos de estudio del ID 5,14,15,45-55, lo que comentamos previamente. Así mismo, estas guías sugieren proceder directamente con la VCE si no existen las indicaciones descritas para la segunda endoscopia 9. Sin embargo, la escasez de evidencia se manifiesta al reconocer dentro del texto de estas guías que una EE puede ser considerada en lugar de una segunda EVDA y que la VCE puede utilizarse sin una segunda endoscopia previa para acelerar el abordaje, más aún, teniendo en cuenta la aparente no costo-efectividad del abordaje con una segunda endoscopia 9.
Rendimiento de la videocápsula frente a la EE
Una publicación de 2005 evaluó el rendimiento de la VCE contra la EE en 7 estudios prospectivos publicados hasta entonces sobre PSID, encontrando un rendimiento de la VCE de 71 % contra 29 % para la EE 58. Un metaanálisis del mismo año que incluyó 14 estudios encontró un rendimiento del 63 % para la VCE y solo del 28 % para la EE 3. En un segundo metaanálisis con 17 estudios se encontró una diferencia de 37 % a favor de la VCE en PSID cuando se comparó con otros métodos, siendo la EE el principal comparador 59. El Odds ratio (OR) de la VCE para un hallazgo positivo fue 4,3 (intervalo de confianza [IC] 95 %: 3,1-6,0) 59. Más recientemente, un estudio aleatorizado confirmó esos hallazgos con una causa identificada en el 50 % de los casos con VCE y en el 24 % con EE (p = 0,02) 60.
Saurin y colaboradores 61 utilizaron como estándar de oro el diagnóstico clínico final, encontrando que la VCE tuvo sensibilidad y especificidad de 92 % y 48 %, respectivamente, frente al 80 % y 69 % para la EE.
Rendimiento de la videocápsula frente a la enteroscopia con doble balón (EDB)
Algunos estudios pequeños han comparado directamente la VCE y EDB. Uno de ellos, que incluyó 13 pacientes, encontró que en el PSID el valor diagnóstico fue similar con ambos métodos 62. Un metaanálisis posterior, que incluía 227 pacientes en los que se comparaba el rendimiento de ambos métodos, encontró que la VCE detectaba más causas que la EDB cuando esta última no se hacía combinando el abordaje anal y oral (OR: 1,61; IC 95 %: 1,07-2,43), pero menos cuando la EDB se hacía con tal abordaje 63. Sin embargo, un estudio de ese mismo año concluyó que la VCE más frecuentemente tuvo un diagnóstico etiológico que la EDB por abordaje anal y oral (59 % frente al 42 %), aunque la diferencia no fue estadísticamente significativa (p = 0,30), probablemente por el pequeño número de pacientes (n = 32) 64. En general, el rendimiento de ambos métodos se considera similar, con la ventaja de que la VCE es un método no invasivo y con menos efectos colaterales 13,65-67.
Rendimiento de la videocápsula frente a la enteroscopia intraopertatoria (EIOP)
La enteroscopia intraoperatoria (EIOP) es considerada por algunos como el mejor método para estudiar completamente el ID y el que tiene el mayor rendimiento etiológico (58 %-88 %) 9,68. Existen pocos estudios que comparan la VCE con la EIOP. Uno de los estudios que se destacan es el de Hartmann y colaboradores 69, en el cual la VCE encontró la causa del sangrado en el 74 % frente al 72 % con la EIOP, sin diferencias estadísticamente significativas. En el metaanálisis mencionado de Triester y colaboradores 3, se encontró un solo estudio que comparara ambos métodos y concluyó un rendimiento similar (83 %), por lo cual la VCE sería el método preferido, ya que no es invasiva y carece de las complicaciones y riesgos de la EIOP 17,69.
Rendimiento de la videocápsula frente a otros métodos
En algunos estudios pequeños, se ha encontrado que la VCE identifica más frecuentemente causas de sangrado que la enteroclisis por la tomografía axial computarizada (TAC) (n = 8) 70 o por resonancia magnética nuclear (RMN) (n = 14) 71. Por su parte, la enteroclisis convencional tiene un rendimiento de 0 %-21 % 72-75. En el metaanálisis mencionado previamente se encontraron 3 estudios que comparaban la VCE con enteroclisis convencional, encontrando una posible causa en el 67 % de los casos con la primera y en el 8 % con la segunda 3. Así mismo, se ha calculado que la VCE permite modificar el tratamiento en el 66 % de los pacientes con PSID 76, comparado con 10 % al utilizar la enteroclisis convencional 72, con las limitaciones de hacer este tipo de comparaciones en poblaciones diferentes.
También se ha demostrado la superioridad de la VCE comparada con la angiografía estándar, con rendimientos de 53 % y 20 %, respectivamente 77. Saperás y colaboradores 78 encontraron que la VCE tenía un rendimiento de 72 %, frente al 24 % con angiografía por TAC y 56 % con la angiografía estándar.
Inconvenientes de la videocápsula
La principal complicación de la VCE es la posibilidad de su retención a lo largo del tracto gastrointestinal 44, la cual puede ocurrir por cicatrices, masas y otras causas de estenosis del lumen, sin una forma adecuada de predecirla con certeza en la actualidad, a excepción de la presencia de signos y síntomas sugestivos de obstrucción intestinal 17,19. La retención de la VCE puede ocurrir en 0 % a 21 % de los pacientes, dependiendo de la población, siendo más frecuente en EC, entre otras 13,59,80. En caso de sospecha clínica de riesgo de retención, se recomienda una enteroTAC o enterorresonancia como métodos imagenológicos para evaluar tal riesgo, o la “cápsula de patencia”, la cual identificaría la estenosis, pero al desintegrarse espontáneamente no originaría una emergencia por la obstrucción total del ID 13,81.
Otros posibles eventos adversos están relacionados con dificultades técnicas e incluyen mal funcionamiento de la cápsula por problemas con la batería y problemas con la transferencia de datos 76,82-84. En casos de vaciamiento gástrico demorado, puede permanecer mucho tiempo en el estómago, con consumo innecesario de la batería, la cual se puede consumir, antes de que examine completamente el ID 82,83. Dado que no insufla aire, no tiene la capacidad de distender el ID y, por lo tanto, habrá zonas en las cuales no hay una adecuada exposición de la superficie mucosa y no identificaría lesiones en esos sitios 13,22. Una limitación inherente a la VCE es que en la actualidad sigue siendo un método diagnóstico, sin la posibilidad de tomar biopsias o realizar intervenciones terapéuticas 13. Adicionalmente, tiene contraindicaciones, que incluyen el embarazo (no hay investigaciones en este grupo) y los problemas de deglución por el riesgo de aspiración traqueal, por lo que es necesario avanzarla endoscópicamente en este último caso 6,26.
A pesar de las limitaciones mencionadas, entre todos los métodos de evaluación del ID que pudieran tener un rendimiento similar, la VCE es el más seguro. Por ejemplo, la EIOP se ha asociado con múltiples complicaciones, que incluyen lesión de los vasos mesentéricos, íleo prolongado, hematoma, infección, perforación e incluso mortalidad por complicaciones postoperatorias 17,69. Así mismo, la EDB, por su naturaleza invasiva, menor tolerabilidad y necesidad de sedación o anestesia, en la actualidad se recomienda solo cuando la VCE haya encontrado lesiones tratables con la EDB, cuando se requieran biopsias o si luego de una VCE sin hallazgos persiste la sospecha de sangrado de ID 65-67,85-87.
Costo-efectividad de la videocápsula frente a una nueva endoscopia alta o baja
Una variable que puede ayudar a decidir entre estas dos estrategias son los costos. Un estudio retrospectivo realizado en Grecia evaluó el rendimiento de la VCE en PSID y concluyó que esta es más costo-efectiva que repetir la EVDA y CLNT 42. Realizar una nueva EVDA y CLNT a todos los pacientes hubiese costado € 50,050 (143 pacientes x € 350), lo que habría evitado 9 VCE innecesarias, con un gasto de € 80,400 por las VCE necesarias (134 pacientes X € 600), para un total de € 130,450 con esta estrategia. La estrategia inversa, con realización de VCE a todos los pacientes, tuvo un costo de € 85,800 (143 pacientes x € 600). Esto representa un ahorro de € 312,2 por paciente. Debe destacarse que estos pacientes habían sido evaluados en el pasado en promedio con 2 EVDA (Rango 1-3) y 2 colonoscopias (rango 1-3), por lo que no puede descartarse que, en caso de menos evaluaciones endoscópicas previas, se hubieran encontrado más causas al alcance de estos métodos tradicionales.
Se podría intentar extrapolar los datos mencionados a los costos locales de estos métodos diagnósticos, conscientes de las claras limitaciones de este tipo de extrapolaciones. Para los cálculos se tendrán en cuenta las tarifas que el Hospital Universitario de la Universidad Nacional le ofrece a las entidades que le remiten sus pacientes: EVDA con sedación: $ 375 000, CLNT con sedación: $ 413 000 y VCE: $ 6 000 000. En caso de hacerlo, se tendría que el abordaje inicial con una segunda endoscopia alta y baja, seguidas por VCE en casos de no hallazgos, tendría un costo de $ 916 684 000 (143 X $ 788 000 + 134 X $ 6 000 000). Por su parte, la realización de VCE directamente a todos los pacientes costaría $ 858 000 000 (143 X $ 6 000 000), representando un ahorro de $ 410 377,6 por paciente.
En el estudio australiano mencionado previamente se encontró también un costo mayor en la estrategia de repetir la endoscopia alta y baja y, en caso de no hallazgos, proceder a la VCE, que con el uso de la estrategia inversa (el uso de la VCE directamente para todos los pacientes) 18. Con la primera estrategia se evaluaban 50 pacientes con ambas endoscopias ($ 1273 por paciente) y 47 pacientes con VCE ($ 1801,9 por paciente); con la segunda se realizaban 50 VCE y, a lo sumo, 26 nuevas endoscopias altas y bajas. Esto llevaba a un gasto total de $ 148 364 al proceder a segunda endoscopia alta y baja, mientras que el gasto era de $ 123 199 con una VCE inmediata, representando un ahorro de $ 503 000 por paciente. Si se extrapolaran los hallazgos de este estudio a los costos de nuestra institución se tendría que la estrategia inicial de una nueva EVDA y CLNT costaría $ 321 400 000 (50 X $ 788 000 + 47 X $ 6 000 000), mientras que la estrategia inversa, con VCE inicial seguida por nuevas endoscopias en caso de no hallazgos costaría $ 320 488 000 (50 X $ 6 000 000 + 26 X $ 788 000). En este caso se tendría un ahorro de $ 18 240 por paciente con la VCE como estrategia inicial.
Un tercer estudio internacional, en este caso italiano, encontró también una mejor costo-efectividad con el uso de VCE en el estudio del PSID al compararla con los demás métodos de evaluación de estos pacientes, incluidos EE, enteroclisis, EVDA, colonoscopia, TAC, angiografía, RMN, ecografía, gammagrafía y EIOP 43. El costo promedio de la VCE para llegar a un diagnóstico fue de € 2091, mientras que el de los otros métodos fue € 3829.
En Colombia no hay estudios que comparen los diferentes métodos para investigar el PSID, mucho menos estudios de costo-efectividad al respecto. Sin embargo, se han publicado dos series de casos retrospectivas que describen el uso de VCE en 97 19 y 50 pacientes (88) con PSID. En esos estudios, la causa del sangrado fue identificada en 91,7 % (89/97) y 58 % (29/50), respectivamente. En el estudio de Galiano y colaboradores (19), las lesiones encontradas estaban al alcance del endoscopio estándar en el 24,7 % de los pacientes con PSID (24/97): esófago: 1, estómago: 10, duodeno: 8 y colon: 5. Para el caso del estudio de García del Risco y colaboradores 88, 14 % de los pacientes presentó lesiones al alcance del endoscopio estándar (7/50), distribuidas de la siguiente manera: una en el esófago, dos en el estómago, una en el duodeno y tres en el colon derecho.
Al realizar un análisis de costo-efectividad con estos datos, si se procediera con una nueva EVDA y CLNT para todos los pacientes del primer estudio 19 se gastarían COP $ 76 436 000 en endoscopias (97 X COP $ 788 000), lo que evitaría el uso de 24 VCE, con un gasto por VCE entonces de $438 000 000 (73 X $6,000,000), para un total de $ 514 436 000 con esta estrategia. Por el contrario, la realización directa de VCE a todos los pacientes costaría $ 582 000 000 (97 X $ 6 000 000), representando un gasto adicional de $ 696 536 por paciente con el uso inmediato de la VCE. Para el segundo estudio 88, la realización de una nueva EVDA y CLNT, seguidas por VCE en caso de no hallazgo de la causa del PSID, costaría $ 297 400 000 (50 X $ 788 000 + 43 X $ 6 000 000), mientras que la realización directa de la VCE costaría $300 000 000 (50 X $ 6 000 000). Esto representa un costo adicional de $ 52 000 por paciente si se procede inmediatamente con la VCE. Sin embargo, debe recalcarse que estos estudios no fueron diseñados para análisis de costo-efectividad y que además de esos no existen otros estudios que permitan hacer un adecuado análisis de este tipo a nivel local.
Si se extrapolan los hallazgos internacionales a los costos locales también se encuentra un mejor costo-efectividad con la VCE como estrategia inicial después de los exámenes endoscópicos iniciales negativos. Sin embargo, si los cálculos se realizan teniendo en cuenta los rendimientos de las dos series colombianas publicadas, esta estrategia podría ser menos costo-efectiva. El costo de la VCE en otros países es menos del doble de una nueva EVDA y colonoscopia, escenario en el cual parece evidente la mejor costo-efectividad de la VCE como estrategia inicial de estudio de los pacientes con PSID, lo que se ha manifestado en los tres estudios internacionales que hasta el momento han hecho análisis económicos al respecto (18, 42, 43). Por el contrario, en nuestro medio la VCE es alrededor de 7,6 veces más costosa que una segunda endoscopia alta y baja, de modo que la relación del costo de la VCE con los estudios endoscópicos es muy superior a lo que sucede internacionalmente. Dada esta alta relación no se puede asegurar el costo-efectividad de la VCE si se evitara una segunda EVDA y CLNT. Por lo anterior, consideramos que, en nuestro medio, se necesitan estudios específicos sobre el costo-efectividad de estos métodos.
Conclusiones
La VCE es un excelente método de evaluación del ID, reconocido como tal por las principales sociedades científicas a nivel mundial. Su rendimiento en PSID es excelente, e incluso considerado el estándar de oro por algunos. Así mismo, es evidente que su rendimiento es mayor al de una segunda endoscopia alta y baja en estos pacientes, detectando incluso causas al alcance de estos procedimientos endoscópicos iniciales pasadas por alto durante ellos. Ante este rendimiento y ante su seguridad y naturaleza no invasiva en relación con otros, este método parece ser la mejor opción para el estudio del PSID luego de una primera EVDA y colonoscopia a la luz de la literatura científica mundial publicada hasta el momento. Así mismo, la mejor costo-efectividad de la VCE ha sido claramente demostrada en el ámbito internacional. Sin embargo, en nuestro medio la VCE es 7,6 veces más costosa que una segunda EVDA y CLNT, por lo que se generan dudas sobre cuál de las dos estrategias es más costo-efectiva en nuestro país. Esta incertidumbre solo cambiará si los precios de la VCE se hacen más competitivos a nivel local o si se realizan estudios prospectivos locales adecuadamente diseñados. Una recomendación que se desprende de los hallazgos internacionales y locales con la VCE es la necesidad de que las EVDA y las CLNT realizadas en pacientes con sangrado manifiesto u oculto se realicen con el más alto estándar de calidad para evitar pasar por alto las lesiones que han detectado las VCE al alcance de esos procedimientos endoscópicos.











 text in
text in 


