Introducción
COVID-19 es una enfermedad producida por el coronavirus SARS-CoV-2, un virus ARN cuyo nombre deriva de la morfología de su envoltura en forma de “corona”; este se originó en Wuhan, capital de la provincia de Hubei (China), desde diciembre de 2019 1. El 7 de enero de 2020 fue aislado en muestras del tracto respiratorio de 4 pacientes, en las que se encontró que es un poco diferente y más contagioso que las otras dos cepas de coronavirus causantes de epidemias previas, el SARS-CoV (severe acute respiratory syndrome) y el MERS-CoV (Middle East respiratory syndrome) 2.
El SARS-CoV-2 se ha diseminado por todo el mundo, por lo cual el 11 de marzo de 2020 la Organización Mundial de la Salud (OMS) declaró la pandemia 3. Para el 15 de abril de 2020, tenemos 185 países afectados, con 2 049 888 personas infectadas en el mundo y 133 572 muertos, lo que da una mortalidad global de 6,5 % 4.
La ruta principal de contaminación es por microgotas de saliva y partículas aerosolizadas (<5 μm) cargadas de virus y que se desplazan por el aire; sin embargo, tocar superficies contaminadas con dichas partículas y tener contacto persona a persona también pueden transmitir el virus. Se ha demostrado que el virus SARS-CoV-2 puede permanecer viable en superficies como plásticos y acero inoxidable hasta por 72 horas 5. El promedio de incubación es de 5,1 días (intervalo de confianza [IC] 95 %, 4,5-5,8 días), y el 97,5 % de los pacientes desarrollan síntomas en promedio dentro de 11,5 días (IC 95 %, 8,2-15,6 días) posterior al contagio 6. En un estudio en China, se documentó la presencia del SARS-CoV-2 en la materia fecal en el 53 % de 73 pacientes hospitalizados con COVID-19, lo que abre la posibilidad de una transmisión oro-fecal, aunque esto aún no ha sido demostrado 7. El primer caso en Estados Unidos se detectó en el estado de Washington el 20 de enero de 2020; el paciente presentó síntomas gastrointestinales como náuseas, vómito, diarrea y molestia abdominal, y se le realizó una prueba para SARS-Cov-2 en materia fecal al séptimo día del comienzo de la infección, la cual fue positiva 8.
Las manifestaciones clínicas de COVID-19 son variables. Un reciente metaanálisis de 60 estudios con 59 254 pacientes de 11 países encontró que los síntomas más frecuentes son: fiebre (82 %), tos seca (61 %), fatiga y mialgias (36 %), disnea (26 %), cefalea (12 %), dolor de garganta (10 %) y síntomas gastrointestinales (9 %) 9. En cuanto al espectro clínico de COVID-19 en 44 672 casos confirmados en China, la mayoría (75 %) proveniente de la provincia de Hubei, fue el siguiente: 81 % fueron leves (sin neumonía o neumonía leve), 14 % con neumonía grave (disnea, frecuencia respiratoria ≥30 respiraciones/min, saturación de oxígeno en sangre ≤93 %, presión parcial de oxígeno arterial a fracción de oxígeno inspirado <300, y/o infiltrados pulmonares >50 % en 24-48 horas), y 5 % críticos (falla respiratoria, choque séptico, y/o disfunción multiorgánica) 10.
En otro metaanálisis de 60 estudios con 4243 pacientes se encontraron síntomas gastrointestinales en 17,6 % de individuos (IC 95 %, 12,3 %-24,5 %); en aquellos con COVID-19 no graves, el 11,8 % (IC 95 %, 4,1 %-29,1 %) presentaban síntomas gastrointestinales, mientras que 17,1 % (IC 95 %, 6,9 %-36,7 %) de individuos con COVID-19 grave tenían síntomas gastrointestinales. La prevalencia del SARS-CoV-2 en muestras de materia fecal fue de 48,1 % (IC 95 %, 38,3 %-57,9 %). De estas muestras, el 70,3 % fueron recolectadas después de tener resultados negativos en las pruebas de tracto respiratorio 11.
¿Existe un mayor riesgo de infección por SARS-CoV-2 en pacientes con enfermedad inflamatoria intestinal?
La enfermedad inflamatoria intestinal (EII) comprende dos entidades: la colitis ulcerativa (CU) y la enfermedad de Crohn (EC), las cuales son patologías inflamatorias crónicas del tracto gastrointestinal, poco comunes, que afectan primordialmente el colon y el intestino delgado, y cuya etiología es multifactorial 12,13. Su curso clínico se caracteriza por presentar múltiples recaídas; durante los últimos años, se ha detectado un aumento en la frecuencia de aparición tanto a nivel mundial como en Latinoamérica 14,15. La EII es una enfermedad discapacitante, con daño tisular y alteración en la respuesta inmunológica, lo cual, asociado a los medicamentos que se utilizan para su tratamiento, ponen al paciente en riesgo de desarrollar infecciones y complicaciones 16-19.
Los pacientes con EII pueden, hipotéticamente, tener un riesgo incrementado de COVID-19. El receptor del SARS-CoV-2 en la célula blanco es el receptor tipo 2 de la enzima convertidora de angiotensina (ECA), y necesita también a la proteasa TMPRSS2 para poder entrar a la célula. El receptor de la ECA tipo 2, además de expresarse en el tracto respiratorio superior, los pulmones (neumocitos tipo II), el corazón, los vasos sanguíneos y el riñón, se encuentra en el tracto digestivo, con una mayor concentración en el esófago, el íleon terminal y en el colon 7,20. Lo anterior podría explicar el alto porcentaje del SARS-CoV-2 positivo en heces y los síntomas gastrointestinales asociados a esta infección 7,11,21. Adicionalmente, se ha documentado un incremento en la expresión del receptor de ECA tipo 2 en el intestino inflamado de pacientes con EII 22. Todas estas observaciones sugieren que el intestino inflamado de los pacientes con EII puede facilitar la entrada del SARS-CoV-2 en el organismo; sumado a esto, los pacientes con EII reciben medicamentos que se asocian con un incremento en el riesgo de infecciones 16-19. A pesar de lo anterior, hasta el momento no hay estudios publicados en pacientes con EII y COVID-19; por lo tanto, no se pueden hacer recomendaciones específicas basadas en evidencia clínica directa 23.
Recientemente fue creado un registro internacional de pacientes con EII denominado SECURE-IBD (Surveillance Epidemiology of Coronavirus Under Research Exclusion - Inflammatory bowel disease), que incluye tanto adultos como niños y sirve para monitorizar y mostrar resultados de COVID-19 en individuos con EII. Para abril 15 de 2020 se han registrado 525 casos en 35 países del mundo, 33,5 % provienen de Estados Unidos y 16,7 % de España, con una mortalidad de 2 % en EC y 5 % en CU, la cual es mayor en hombres (4 % frente a 2 %), en fumadores (4 % frente a 3 %) y en pacientes >60 años o con comorbilidades. La mortalidad observada en individuos tratados con ácido 5-aminosalicílico (5-ASA) es de 8 %, budesonida 6 %, esteroides 11 %, azatioprina 2 %, metotrexato 0 %, monoterapia con un antagonista del factor de necrosis tumoral alfa (anti-FNTα) 1 %, terapia combinada con inmunosupresores 4 %, anti-integrinas 0 %, y anti-interleucina (IL)-12/23 0 % 24. A pesar de las tendencias presentadas, se debe esperar tener resultados con un mayor número de pacientes para sacar conclusiones definitivas de este interesante registro.
Recomendaciones para pacientes con enfermedad inflamatoria intestinal durante la pandemia por COVID-19
La pandemia por COVID-19 ha tenido una diseminación muy rápida, y aún se encuentra en evolución; por lo tanto, aún no están disponibles datos amplios de incidencia o factores de riesgo en pacientes con EII. El centro de EII de la Universidad Humanitas de Milán (Italia) 25 y, más recientemente, la Organización Internacional para el estudio de EII (IOIBD) 26, teniendo en cuenta que COVID-19 no es una infección oportunista y que es extremadamente contagiosa, sugieren seguir las mismas instrucciones de medidas protectoras básicas recomendadas por la OMS para la población general en los pacientes con EII 27:
Limpie sus manos regularmente y a fondo con un desinfectante para manos a base de alcohol, o lávelas con agua y jabón.
Limpie las superficies con un desinfectante a base de alcohol dónde crea que pueda haber gotas de saliva.
Mantenga al menos 1 metro de distancia de cualquier persona que esté tosiendo o estornudando.
Evite tocarse los ojos, la nariz y la boca (un tapabocas puede ayudar en esto).
Asegúrese de que usted y las personas que lo rodean sigan una buena higiene respiratoria. Esto significa cubrirse la boca y la nariz con el codo o un pañuelo doblado cuando tosa o estornude.
Quédese en casa si no se siente bien. Si tiene fiebre, tos y dificultad para respirar, busque atención médica.
Use un tapabocas para evitar infectar a otras personas, incluso en caso de que presente síntomas leves.
Use guantes cuando vaya de compras, cuando use la bomba de gasolina, y en todas las demás actividades externas que impliquen riesgo de contaminación de manos.
Evite usar baños públicos tanto como sea posible, ya que el inodoro, el lavamanos y la manija de la puerta pueden estar contaminados.
Manténgase actualizado sobre los últimos sitios críticos de COVID-19. Si es posible, evite viajes no urgentes, especialmente si es una persona mayor o tiene diabetes, enfermedades cardíacas o pulmonares.
Adicionalmente, en el centro de EII Humanitas en Italia considera que mantener la comunicación con los pacientes es fundamental, ya sea por correo electrónico o por vía telefónica, y que el papel de la enfermera es clave. Se les insiste a los pacientes continuar con su mismo tratamiento, sobre todo si están en remisión, y seguir las recomendaciones de la asociación nacional de pacientes de Italia. Además, durante esta pandemia, la farmacia se encarga de suministrar medicamentos a domicilio por un período de hasta 4 meses, incluyendo aquellos de aplicación subcutánea para administrar en casa 28.
Recomendaciones para los centros de enfermedad inflamatoria intestinal durante la pandemia por COVID-19
El centro de EII de la Universidad Humanitas de Milán (Italia) atiende más de 5000 pacientes de todo el país y, por la pandemia COVID-19, se ha convertido en una clínica de atención virtual; las cirugías electivas fueron aplazadas, y solamente se manejan en forma presencial los casos clínicos y quirúrgicos urgentes, u oncológicos, lo cual tiene como desventaja una posible progresión de la enfermedad, y resultados quirúrgicos quizá no tan favorables por aplazar dichos procedimientos. Toda esta situación genera ansiedad en los pacientes, pero hay que insistirles en que esta pandemia es temporal, y que es necesario que se mantengan en contacto con el centro para suministrarles todo el soporte necesario 28.
Todos los trabajadores de la salud y los pacientes son interrogados a la entrada del hospital; se les pregunta por síntomas como tos y fiebre en las últimas dos semanas, o si han tenido contacto cercano con familiares con estos síntomas, o conocidos infectados por SARS-CoV-2. Los pacientes que ingresan para procedimientos de estudios clínicos o para infusión de medicamentos son atendidos en forma presencial, pero sin acompañantes, y las sillas para infusión de medicamentos están separadas a una distancia segura (1-2 metros) 28. A los pacientes se les coloca tapabocas quirúrgico, y todo el personal de salud cuenta con equipo de protección personal (EPP) y siguen las recomendaciones de la OMS anteriormente descritas 27. El uso de esteroides en la infección por COVID-19 es controversial 29, razón por la cual intentan usar dosis bajas (<20 mg/día) y por corto tiempo solo en caso de recaídas. Adicionalmente, sugieren evitar el inicio de terapia biológica durante esta pandemia en pacientes asintomáticos, por ejemplo, en la prevención de recurrencia posquirúrgica en EC de riesgo bajo a moderado, y tampoco recomiendan cambiar de terapia biológica de presentación intravenosa a una subcutánea en pacientes en remisión 25.
Hasta el momento, no hay recomendaciones basadas en evidencia clínica durante esta pandemia por COVID-19 para pacientes en inmunosupresión, como es el caso de la EII. La IOIBD está conformada por 89 miembros expertos en EII de 26 diferentes países del mundo, y ha publicado una serie de recomendaciones basadas en la opinión de expertos por medio de votación virtual el día 27 de marzo de 2020, relacionadas con el riesgo de infección por el SARS-CoV-2, el desarrollo de COVID-19, y el manejo de la EII en diferentes escenarios clínicos. A cada declaración se le daba un puntaje de 1 a 9: un puntaje promedio de 1 a 3 se consideró no apropiada, de 4 a 6 incierta y de 7 a 9 apropiada. En total se votaron 76 declaraciones, de las cuales 26 fueron apropiadas, 19 inciertas y 31 no apropiadas 26. Se consideró apropiada la declaración de que no hay riesgo adicional de contraer la infección por el virus SARS-CoV-2 en pacientes con EII en comparación con la población general, y que no existen diferencias en cuanto al riesgo de pacientes con EC y CU; sin embargo, consideran incierta la posibilidad de que los pacientes con EII activa con inflamación puedan tener mayor riesgo de infección por el SARS-CoV-2.
Adicionalmente, el panel consideró apropiado aplazar procedimientos endoscópicos y quirúrgicos no urgentes, suspender viajes no esenciales, continuar con el tratamiento inmunosupresor en pacientes con EII si se encuentran en remisión; si están en terapia combinada (anti-FNT más inmunosupresor) y contraen la infección por el SARS-CoV-2, pero no desarrollan COVID-19, se debe suspender el inmunosupresor. A pesar de que las tiopurinas se han asociado a infecciones virales 17-19, el panel considera continuarlas, ya que suspenderlas no ayudaría a corto plazo debido a que tienen una vida media larga de eliminación. En caso de suspender el medicamento por contraer COVID-19, se debe reiniciar después de 14 días cuando el paciente se encuentre asintomático, y después de dos muestras negativas de nasofaringe para el SARS-CoV-2. A los pacientes con EII asintomáticos que se infecten por el virus, pero no desarrollen COVID-19, se les debe reiniciar el tratamiento a los 14 días. Un resumen de las declaraciones y votaciones del panel sobre las opciones de tratamiento de la EII y diferentes escenarios clínicos de COVID-19 se presenta en la Tabla 1.
Tabla 1 Posición de la IOIBD sobre el uso de medicamentos en EII y COVID-19 26.
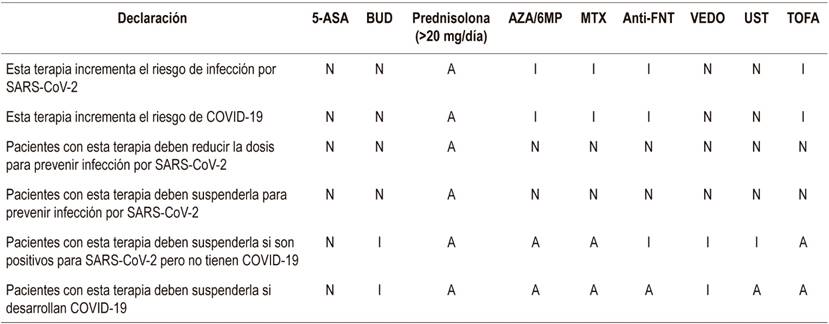
A: apropiado; N: no apropiado; I: incierto; Anti-FNT: antifactor de necrosis tumoral; AZA: Azatioprina; BUD: budesónida; MTX: metotrexato; TOFA: tofacitinib; UST: ustekinumab; VEDO: vedolizumab; 6MP: 6-mercaptopurina. Adaptado de referencia 26.
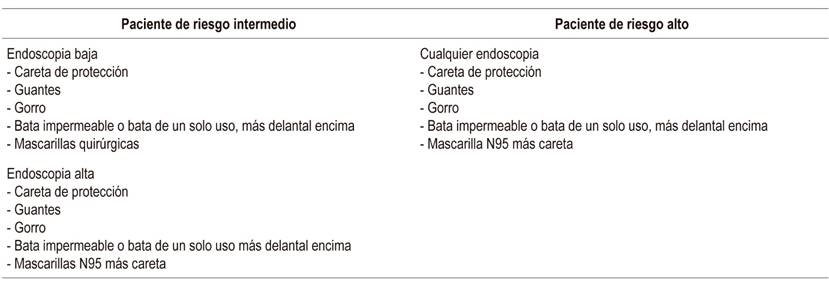
Recomendaciones para los procedimientos endoscópicos en pacientes con enfermedad inflamatoria intestinal durante la pandemia por COVID-19
La transmisión oro-fecal puede ser parte del espectro clínico de la infección por SARS-Cov-2 ante la evidencia disponible 7,30,31. El ARN de este virus se elimina en las heces y puede persistir hasta incluso después de que desaparezcan los síntomas respiratorios 11. No obstante, una publicación reciente muestra que, aunque se pudieron detectar grandes cantidades de ARN viral de SARS-CoV-2 en las heces, no se pudo replicar el virus en dichas muestras de materia fecal 32.
La principal ruta de transmisión de COVID-19 de humano a humano es la vía aérea, y aunque existe la posibilidad de transmisión fecal, esto no se ha demostrado; por lo tanto, ante la corta distancia física que existe entre los pacientes y el personal durante los procedimientos endoscópicos, se considera que tanto las endoscopias superiores como las inferiores pueden conllevar un riesgo de infección por el SARS-CoV-2. Diversas sociedades científicas han publicado recomendaciones sobre procedimientos endoscópicos durante la pandemia por COVID-19, las cuales se pueden aplicar a los pacientes con EII 33-37. La IOIBD considera apropiado aplazar todo procedimiento endoscópico y quirúrgico no urgente en los pacientes con EII 26. Siguiendo las anteriores recomendaciones, en nuestro hospital, el Pablo Tobón Uribe en Medellín (Colombia), limitamos la realización de estudios endoscópicos a pacientes con EII que requieran procedimientos urgentes (hemorragia digestiva con inestabilidad hemodinámica, colangitis aguda, extracción de cuerpo extraño, obstrucción del tubo digestivo y a pacientes con cáncer). Decidimos entonces estratificar el riesgo del procedimiento endoscópico a realizar (Tabla 2), y definimos el riesgo de cada paciente según los síntomas que presente y los antecedentes que tenga (Tabla 3); basados en lo anterior, determinamos el nivel de protección del personal de salud para cada procedimiento endoscópico (Tabla 4).
Conclusiones
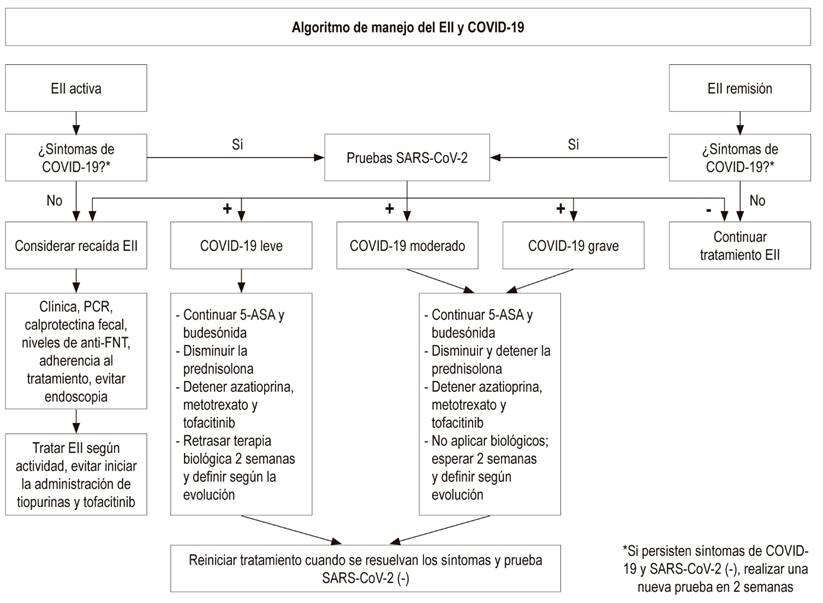
La pandemia por COVID-19 se ha convertido en un gran problema para la humanidad; hasta el momento, no hay recomendaciones basadas en evidencia clínica para pacientes con EII. Existe una interacción de este virus con el tracto gastrointestinal a través de la interacción con el receptor de la ECA tipo 2, y se ha documentado su eliminación fecal, aunque la transmisión por esta vía no se ha demostrado. Existen recomendaciones basadas en la opinión de expertos sobre el cuidado de pacientes con EII durante la pandemia por COVID-19, teniendo en cuenta el riesgo de la infección y su tratamiento 26,38. En la Figura 1 se propone un algoritmo de manejo de pacientes con EII y diferentes escenarios clínicos de la infección por SARS-CoV-2 y el desarrollo de COVID-19.
Dado que la pandemia por COVID-19 es dinámica y el conocimiento está creciendo rápidamente, algunas de estas recomendaciones presentadas en esta revisión pueden actualizarse de acuerdo con la aparición de mejor evidencia clínica. Se esperan resultados definitivos del registro SECURE-IBD.