Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista colombiana de Gastroenterología
versión impresa ISSN 0120-9957versión On-line ISSN 2500-7440
Rev. colomb. Gastroenterol. vol.37 no.1 Bogotá ene./mar. 2022 Epub 24-Mayo-2022
https://doi.org/10.22516/25007440.710
Reporte de caso
Terapia de vacío endoluminal (Endo-Vac) en el manejo de la fístula de anastomosis esofagogástrica
1Gastroenterology and Digestive Endoscopy Specialist. Associate Professor of Medicine at Pontificia Universidad Javeriana, Hospital Universitario San Ignacio. Bogotá, Colombia.
2 Fellow Gastroenterology and Digestive Endoscopy Internist. Pontificia Universidad Javeriana, Hospital Universitario San Ignacio. Bogotá, Colombia.
La terapia de vacío endoluminal (Endo-Vac) es una alternativa promisoria en el manejo endoscópico de las fístulas o perforaciones gastrointestinales, que no responden a procedimientos endoscópicos cuando se utilizan técnicas como clips, stents o incluso refractarias a procedimientos quirúrgicos. En este reporte de caso describimos el cierre endoscópico exitoso de una fístula anastomótica esofagogástrica, utilizando la terapia Endo-Vac, conectada a un sistema de vacío mediante una sonda en la cavidad, que no presentó cierre inicial a manejo con clips, dada la friabilidad y el edema del tejido perilesional. Se concluye que esta es una alternativa exitosa en el cierre de estas complicaciones, que en ocasiones son de difícil resolución.
Palabras clave: Técnica de cierre de heridas; endoscopia; fístula esofágica; anastomosis quirúrgica
Endoluminal vacuum therapy (EVAC) is a promising alternative for the endoscopic management of gastrointestinal fistulas or perforations that do not respond to endoscopic procedures using clips and stents or are even refractory to surgical procedures. In this case report, we describe the successful endoscopic closure of an esophagogastric anastomotic fistula using EVAC, connected to a vacuum system through a probe in the cavity, which did not close with clip management given the friability and edema of the peri-wound tissue. In conclusion, it is a successful alternative to treat these complications, which are sometimes difficult to resolve.
Keywords: Wound closure technique; endoscopy; esophageal fistula; surgical anastomosis
Introducción
Una de las complicaciones más importantes, luego de una esofagectomía, es la fístula anastomótica, con una incidencia entre el 1 % y 30 %1. Entre las alternativas de manejo endoscópico encontramos la terapia de vacío endoluminal (Endo-Vac), que consiste en una esponja conectada a una sonda nasogástrica, que se ubica en el defecto a corregir y se conecta a presión negativa2. Este sistema disminuye la contaminación bacteriana y el edema, además que estimula la granulación del tejido mediante la angiogénesis, lo que disminuye gradualmente el tamaño de la cavidad hasta lograr el cierre3,4. Las fístulas anastomóticas esofágicas son una condición potencialmente mortal, entre el 0,8 % al 11,6 %, debido al desarrollo de mediastinitis, empiema pleural y sepsis5,6. En pacientes oncológicos se han encontrado tasas de mortalidad de hasta 18 %7. Presentamos un caso de fístula anastomótica esofagogástrica manejada con Endo-Vac.
Caso clínico
Hombre de 69 años con antecedente de adenocarcinoma gástrico, con extensión a la unión gastroesofágica, estadificado III b (pT4N0M0), con antecedente de diabetes mellitus. El paciente se llevó a esofagogastrectomía por laparoscopia y toracoscopia con bordes de sección negativos, en manejo con adyuvancia y protocolo Capeox. Presentó disfagia orofaríngea y odinofagia, así como pérdida de peso de 18 kg. En el día 11 posoperatorio presenta signos de respuesta inflamatoria, con esofagograma, que evidenció una fístula a nivel de anastomosis. El estudio endoscópico mostró hallazgo de fístula de 15 mm en la anastomosis a los 30 cm de las arcadas dentarias; bajo visión fluoroscópica presentó extraluminización fuera de la pared esofágica (Figura 1). El manejo inicial consistió en la colocación de 5 clips. Debido a la friabilidad de la mucosa no se logró el cierre total del defecto.
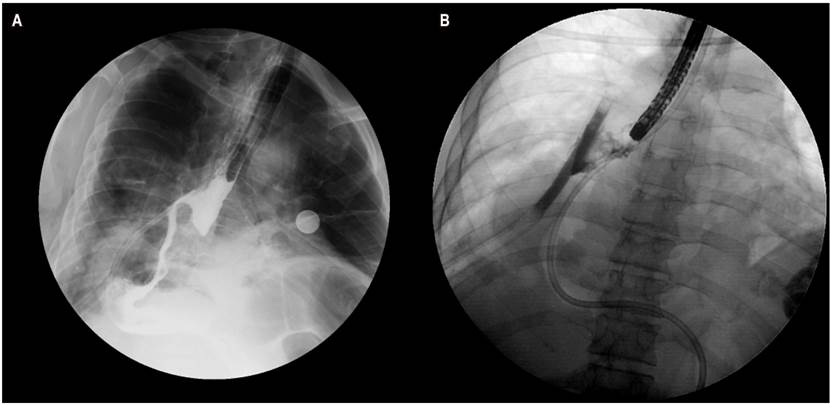
Figura 1 A. Esofagograma: trayecto fistuloso en la anastomosis esofagogástrica. B. Irrigación del medio de contraste, con extraluminización fuera de la pared esofágica.
Dado la persistencia de una fístula de 5 mm sobre anastomosis se realiza terapia Endo-Vac con esponja de GranuFoamTM, conectada a un sistema de drenaje intermitente, con una presión negativa de 100 mm Hg (Figura 2). Conjuntamente se llevó a cabo una yeyunostomía laparoscópica. Se realiza recambio de esponja a los 7 días y se observa una reducción del defecto fistuloso. A las 2 semanas de inicio de la terapia se logra la adecuada cicatrización, sin evidencia de fístula. Se extrae la esponja y la sonda nasogástrica con asa de 30 mm sin complicaciones. Control endoscópico al mes y 3 meses de finalizar la terapia Endo-Vac. Anastomosis con cambios inflamatorios y disminución de la luz en 30 %, por efecto de angulación y no por estenosis, lo que permitió el paso fácil del equipo (Figura 3). Se indicó manejo con inhibidor de bomba de protones, y se logró una mejoría de la disfagia, sin dolor torácico.
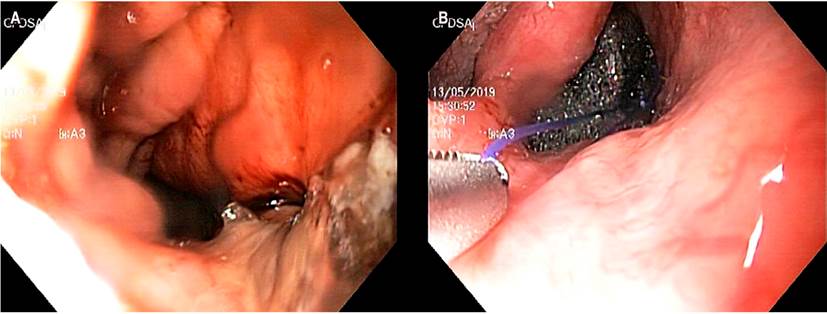
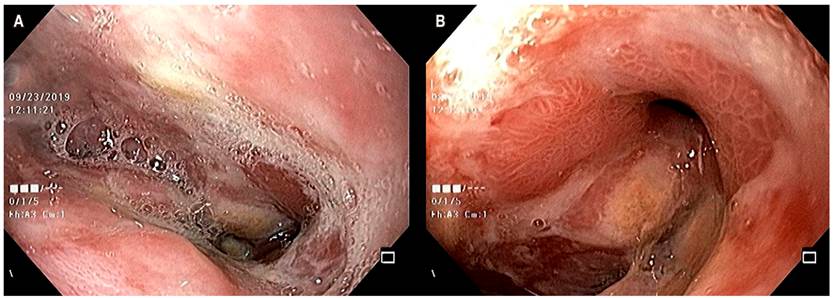
Figura 2 A. Visualización endoscópica de la fístula de la anastomosis esofagogástrica. B. Endo-Vac: inserción endoscópica de la esponja traccionada de material de sutura con pinza.
Discusión
En el presente artículo se describe un caso de cierre de fístula anastomótica esofagogástrica en un paciente con antecedente de esofagogastrectomía por adenocarcinoma gástrico, con extensión a la unión gastroesofágica. Se manejó con colocación de clips endoscópicos, con cierre parcial de la fístula, y ulterior realización de la Endo-Vac mediante dos recambios. Se obtiene un excelente resultado en el manejo de esta fístula compleja, sin presentar complicaciones.
Aunque las perforaciones esofágicas son una entidad clínica poco frecuente, estas tienen una alta mortalidad y morbilidad, lo que representa un paradigma desafiante en su manejo8. El tratamiento de la fístula anastomótica depende de la causa, el tamaño, el tiempo de la solución de continuidad y el estado nutricional del paciente. El plan terapéutico incluye medidas de soporte, terapia antibiótica y, en algunos casos, antifúngicos, drenaje de colección extraluminal y mantenimiento de la nutrición enteral. El manejo endoscópico es menos mórbido que la cirugía9.
El pilar de tratamiento de las fístulas gastrointestinales superiores es la terapia endoscópica con clips o sistema OVESCO, para perforaciones menor de 2 cm, y sutura endoscópica, para perforaciones mayor de 2 cm. La colocación de stents autoexpandibles se reserva en los casos en los que el cierre primario no se logra10, con una tasa de éxito mayor de 68,8 % a 90 % en la fístula anastomótica posoperatoria por causa neoplásica. Sin embargo, el fracaso ocurre en el 15 % de los casos y el desplazamiento en el 40 %; con complicaciones, como la extracción fallida por el tejido de granulación11 y la estenosis en 28,2 %, una tasa mayor comparada con el Endo-Vac, de 9,4 % (p < 0,05)12. Además, se ha descrito un mayor número de días de estancia en unidad de cuidados intensivos en el grupo del stent comparado con el Endo-Vac (mediana 6 frente a 9 días)13.
En el 2008, Wedemeyer y colaboradores14 reportaron el uso endoscópico del Endo-Vac en el tratamiento de la fístula anastomótica en dos pacientes luego de una esofagectomía y gastrectomía. En esta se logró el cierre de la cavidad a los 15 días, sin recurrencia, y se tuvo resultados iguales en el tiempo de cicatrización en el presente caso. La terapia con Endo-Vac es una técnica alternativa, que ha evolucionado el manejo de las fístulas por causas como gastrectomías tipo sleeve, perforación esofágica por ecocardiograma transesofágico, fístulas en anastomosis, perforación intraoperatoria y perforación de Boerhaave. Las indicaciones dependen de las características de la perforación, como un tamaño menor de 5 cm, el contenido de la fístula y la no presencia de cavitaciones15.
En el 2014 se comercializó la primera esponja de vacío endoluminal Eso-SPONGE® por Braun, con una tasa de éxito del 95 %. La técnica inicia con la inserción de un sobretubo, luego de la aplicación de hidrogel a base de glicerol. A continuación, mediante un empujador, se introduce la Eso-SPONGE® hasta el final del sobretubo. Una vez esta se localiza en la marca del sobretubo, se procede a realizar la extracción del sobretubo hasta el mango del empujador, para lograr la liberación de la esponja; se retira el sobretubo y el empujador. Se introduce una sonda nasogástrica No. 16 Fr por la fosa nasal y se extrae por la boca, se corta el extremo distal y se conecta al Eso-SPONGE®. Se realiza control endoscópico y luego se conecta al sistema de vacío, con una presión entre 50 a 125 mm Hg16.
Los mecanismos por los que se logra la curación de la fístula mediante la terapia de presión negativa o subatmosférica son:
El control del exudado por modificaciones locales en el flujo sanguíneo, eliminación de sustancias nocivas.
La macrodeformación mediada por la succión sobre la esponja causa deformación, que se ejerce sobre los bordes del defecto y produce la unión de los mismos.
La microdeformación son los cambios mecánicos que ocurren a nivel microscópico y causan la deformación del citoesqueleto, la liberación de los factores de crecimiento, la proliferación y migración celular, y la expresión de componentes de la matriz extracelular.
Cambios en la perfusión que aumentan la densidad de los microvasos, hipoperfusión de los bordes del defecto, hipoxia localizada, expresión del factor de crecimiento endotelial vascular y aumento de la angiogénesis (estos cambios ocurren entre los 5 y 8 días), y finalmente el aclaramiento bacteriano17.
Descripción del procedimiento
Paso 1: evaluación y caracterización endoscópica de la fístula. Puede utilizarse inyección de medio de contraste, con evidencia de la fuga bajo visión fluoroscópica.
Paso 2: después de evaluar la localización y el tamaño del defecto se recomienda la irrigación y el desbridamiento endoscópico; luego, la esponja de poliuretano con poros abiertos (VAC® GranuFoamTM, tamaño de poro 400-600 μm) se recorta y ajusta al tamaño del defecto. Seguido, en la punta de una sonda nasogástrica (NG) de cloruro de polivinilo de 12-14 Fr se realizan orificios adicionales con unas tijeras (Figura 4).
Paso 3: se lleva a cabo la inserción de la sonda NG por la fosa nasal y, luego se extrae por la boca con pinzas o con el dedo, donde se fija la esponja con una sutura 2/0 en el extremo proximal y distal, quedando la sonda en el centro de la esponja de poliuretano (VAC®GranuFoamTM), y se realiza un asa corto en su extremo distal (Figura 4).
Paso 4: la punta de la sonda con la esponja se agarra del asa con pinzas de cocodrilo y se lleva, vía endoscópica, al sitio del defecto, y se cubre la totalidad de la cavidad. La esponja debe ser más pequeña que la cavidad para promover el colapso y el ulterior cierre.
Paso 5: después de colocar la parte exterior de la sonda NG, esta se fija a la nariz con cinta adhesiva. La punta externa se conecta al sistema de vacío, con una presión negativa continua entre 100-125 mm Hg.

Figura 4 A. Construcción de la esponja de poliuretano con poros abiertos (VAC® GranuFoamTM. Fijación de la esponja al extremo de la sonda NG y asa distal de agarre. B. Inserción de la sonda NG (14 Fr) introducida por la fosa nasal, con ulterior extracción por la boca con pinza.
La duración promedio del tratamiento con Endo-Vac son 23 días (rango entre 9-86 días)12, con un recambio de la esponja cada 3 a 5 días18; sin embargo, en el presente caso se realizó a los 7 días, con un buen resultado. Para el recambio o retiro de la esponja se debe suspender la succión, luego se hace lavado de la sonda con solución salina, para separar el tejido de granulación. Seguido, se procede a la retracción de la esponja y retiro. Se puede realizar vía endoscópica o directamente, con ulterior revisión endoscópica19.
La tasa de éxito global de la Endo-Vac es de 84 % a 100 %, promedio del 90 %4. También se han descrito que las técnicas de inserción del Endo-Vac modificada, con introducción de la esponja a través de un sobretubo, parecen demostrar mayor facilidad para el endoscopista, con una tasa éxito del 100 %, tiempo del procedimiento entre 12 y 30 minutos20.
Pournaras y colaboradores9 realizaron una serie con 21 pacientes llevados a Endo-Vac. Las indicaciones fueron fístula anastomótica ulterior a esofagectomía, fístula en anastomosis gastrogástrica y perforación esofágica iatrogénica. La tasa de curación fue del 95%, y el número de recambios fue entre 3 y 12. El diagnóstico se realizó a los 10 días luego de la intervención, similar al caso descrito, y se realizó yeyunostomía en todos los pacientes.
En un estudio prospectivo de 8 pacientes con fístulas esofágicas posquirúrgicas se les realizó Endo-Vac a los pacientes, con un seguimiento de 193 días. Tuvo un cierre exitoso en el 88 % de los casos, media de tratamiento de 23 +/- 8 días, sin complicaciones a corto y largo plazo. Los recambios fueron 2 veces por semana21. Similar a lo presentado se describe el estudio retrospectivo de Bludau y colaboradores22, que reportó una tasa de éxito en el 86 % de los casos. Kuehn y colaboradores23 informó una tasa de éxito en 9 de 11 pacientes, correspondientes al 82 % de los pacientes con fístula en anastomosis. La distancia promedio de las lesiones fue a los 32 cm de las arcadas dentarias, similar a la descrita en el presente caso. Se indicó el seguimiento con tomografía, si había evidencia de lesión mediastinal o intrapleural o evolución desfavorable en las 24 horas siguientes al procedimiento de Endo-Vac.
Después de la terapia con Endo-Vac fallida se ha descrito el manejo complementario con stents metálicos autoexpandibles parcialmente recubiertos sobre el Endo-Vac, con una tasa de éxito en manejo de primera línea del 71,4 % y en segunda línea en el 80 %, sin eventos adversos graves24. Brangewitz y colaboradores12 compararon el Endo-Vac con la prótesis metálica o plástica en el cierre de las fístulas esofágicas, con una tasa de éxito del 84,4 % comparado con 53,8 % en el grupo de stent; sin diferencias en la estancia hospitalaria, ni en la mortalidad, pero mayor presentación de estenosis en el grupo del stent.
En su estudio, Choi y colaboradores25 incluyeron a 39 pacientes, 11 casos se trataron con Endo-Vac (de los cuales 7 casos fueron cambio de stent a Endo-Vac debido a una no mejoría), y en 28 casos se realizó stent metálico autoexpandible, con una mediana de seguimiento de 19 meses. La tasa de éxito del Endo-Vac fue del 100 % y del stent metálico autoexpandible fue del 74,3 % (26/35), sin diferencias estadísticamente significativas. Un caso presentó muerte relacionada con la fuga por complicación infecciosa en el grupo del stent. Sí hubo diferencias en la duración de la terapia menor en el Endo-Vac comparado con el stent (15 frente a 36 días; p <0,001). Complicaciones como la estenosis se presentaron en 14,3 % en el grupo del stent, una tasa mayor comparada con el Endo-Vac, de 9,1 %. No se han encontrado diferencias en el peso de los pacientes, considerando que en el Endo-Vac se utiliza nutrición parenteral hasta el retiro de la esponja, y en el stent se inicia la nutrición enteral dentro de 1 a 2 días de la inserción.
Las desventajas son la intervención endoscópica periódica, la conexión permanente a la bomba de vacío y el diferir la alimentación oral hasta el cierre de la fístula26. Como complicación se ha descrito la estenosis por granulación excesiva en 5 % a 9,1 %, que responde a dilatación endoscópica13.
Conclusión
La terapia con Endo-Vac es una técnica fácil, segura y efectiva en el tratamiento de las fístulas de anastomosis esofágicas y gástricas, como alternativa al manejo inicial con stents o clips. Esta permite el cierre de las fístulas con una excelente tasa de éxito, baja tasa de complicaciones, como las estenosis susceptibles de manejo endoscópico, y menor estancia hospitalaria.
REFERENCIAS
1. Wu PC, Posner MC. The role of surgery in the management of esophageal cancer. Lancet Oncol. 2003;4(8):481-8. https://doi.org/10.1016/S1470-2045(03)01167-7 [ Links ]
2. Pines G, Bar I, Elami A, Sapojnikov S, Hikri O, Ton D, et al. Modified endoscopic vacuum therapy for nonhealing esophageal anastomotic leak: Technique description and review of literature. J Laparoendosc Adv Surg Tech A. 2018;28(1):33-40. https://doi.org/10.1089/lap.2017.0318 [ Links ]
3. Borejsza-Wysocki M, Szmyt K, Bobkiewicz A, Malinger S, Świrkowicz J, Hermann J, et al. Endoscopic vacuum-assisted closure system (E-VAC): case report and review of the literature. Wideochir Inne Tech Maloinwazyjne. 2015;10(2):299-310. https://doi.org/10.5114/wiitm.2015.52080 [ Links ]
4. Mennigen R, Senninger N, Laukoetter MG. Novel treatment options for perforations of the upper gastrointestinal tract: Endoscopic vacuum therapy and over the scope clips. World J Gastroenterol. 2014;20(24):7767-76. https://doi.org/10.3748/wjg.v20.i24.7767 [ Links ]
5. Barabino G, Filippello A, Brek A, Cuilleron M, Dumas O, Rinaldi L, et al. Management of an esojejunal intrathoracic leak using an endoscopic vacuum-assisted closure technique. Surg Laparosc Endosc Percutan Tech. 2017;27(3):e26-7. https://doi.org/10.1097/SLE.0000000000000393 [ Links ]
6. Heits N, Stapel L, Reichert B, Schafmayer C, Schniewind B, Becker T, et al. Endoscopic endoluminal vacuum therapy in esophageal perforation. Ann Thorac Surg. 2014;97(3):1029-35. https://doi.org/10.1016/j.athoracsur.2013.11.014 [ Links ]
7. Rutegård M, Lagergren P, Rouvelas I, Lagergren J. Intrathoracic anastomotic leakage and mortality after esophageal cancer resection: A population-based study. Ann Surg Oncol 2012;19(1):99-103. https://doi.org/10.1245/s10434-011-1926-6 [ Links ]
8. Smallwood NR, Fleshman JW, Leeds SG, Burdick JS. The use of endoluminal vacuum (E-Vac) therapy in the management of upper gastrointestinal leaks and perforations. Surg Endosc. 2016;30(6):2473-80. https://doi.org/10.1007/s00464-015-4501-6 [ Links ]
9. Pournaras DJ, Hardwick RH, Sujendran V, Bennett J, Macaulay GD, Hindmarsh A. Endoluminal vacuum therapy (E-Vac): A treatment option in oesophagogastric surgery. World J Surg. 2018;42(8):2507-11. https://doi.org/10.1007/s00268-018-4463-7 [ Links ]
10. Lee JH, Kedia P, Stavropoulos SN, Carr-Locke D. AGA clinical practice update on endoscopic management of perforations in gastrointestinal tract: Expert review. Clin Gastroenterol Hepatol. 2021;19(11):2252-61.e2. https://doi.org/10.1016/j.cgh.2021.06.045 [ Links ]
11. van Boeckel PG, Sijbring A, Vleggaar FP, Siersema PD. Systematic review: Temporary stent placement for benign rupture or anastomotic leak of the oesophagus. Aliment Pharmacol Ther. 2011;33(12):1292-301. https://doi.org/10.1111/j.1365-2036.2011.04663.x [ Links ]
12. Brangewitz M, Voigtländer T, Helfritz FA, Lankisch TO, Winkler M, Klempnauer J, et al. Endoscopic closure of esophageal intrathoracic leaks: Stent versus endoscopic vacuum-assisted closure, a retrospective analysis. Endoscopy. 2013;45(6):433-8. https://doi.org/10.1055/s-0032-1326435 [ Links ]
13. Berlth F, Bludau M, Plum PS, Herbold T, Christ H, Alakus H, et al. Self-expanding metal stents versus endoscopic vacuum therapy in anastomotic leak treatment after oncologic gastroesophageal surgery. J Gastrointest Surg. 2019;23(1):67-75. https://doi.org/10.1007/s11605-018-4000-x [ Links ]
14. Wedemeyer J, Scheider A, Manns MP, Jackobs S. Endoscopic vacuum-assisted closure of upper intestinal anastomotic leaks. Gastrointest Endosc. 2008;67(4):708-11. https://doi.org/10.1016/j.gie.2007.10.064 [ Links ]
15. Ooi G, Burton P, Packiyanathan A, Loh D, Chen R, Shaw K, et al. Indications and efficacy of endoscopic vacuum assisted closure therapy for upper gastrointestinal perforatios. ANZ J Surg. 2018;88(4):E257-63. https://doi.org/10.1111/ans.13837 [ Links ]
16. Alakkari A, Sood R, Everett SM, Rembacken BJ, Hayden J, Sarela A, et al. First UK experience of endoscopic vacuum therapy for the management of oesophageal perforations and postoperative leaks. Frontline Gastroenterol. 2019;10(2):200-3. https://doi.org/10.1136/flgastro-2018-101138 [ Links ]
17. Weidenhagen R, Hartl WH, Gruetzner KU, Eichhorn ME, Spelsberg F, Jauch KW. Anastomotic leakage after esophageal resection: New treatment options by endoluminal vacuum therapy. Ann Thorac Surg. 2010;90(5):1674-81. https://doi.org/10.1016/j.athoracsur.2010.07.007 [ Links ]
18. Still S, Mencio M, Ontiveros E, Burdick J, Leeds SG. Primary and rescue endoluminal vacuum therapy in the management of esophageal perforations and leaks. Ann Thorac Cardiovasc Surg. 2018;24(4):173-9. https://doi.org/10.5761/atcs.oa.17-00107 [ Links ]
19. Rubicondo C, Lovece A, Pinelli, D, Indriolo A, Lucianetti A, Colledan M. Endoluminal vacuum-assisted closure (E-Vac) therapy for postoperative esophageal fistula: successful case series and literature review. World J Surg Onc. 2020;18(1):301. https://doi.org/10.1186/s12957-020-02073-6 [ Links ]
20. Kwon H, Kim S, Lee J, Cho B, Choi J, Kim SW, et al. An endoscopic vacuum-assisted closure technique modified for patients with esophageal anastomotic leaks. Amer J Gastroenterol. 2019;114:1009-10. https://doi.org/10.14309/01.ajg.0000596724.81881.1c [ Links ]
21. Wedemeyer J, Brangewitz M, Kubicka S, Jackobs S, Winkler M, Neipp M, et al. Management of major postsurgical gastroesophageal intrathoracic leaks with an endoscopic vacuum-assisted closure system. Gastrointest Endosc. 2010;71(2):382-6. https://doi.org/org/10.1016/j.gie.2009.07.011 [ Links ]
22. Bludau M, Holscher AH, Herbold T, Leers JM, Gutschow C, Fuchs H, et al. Management of upper intestinal leaks using an endoscopic vacuum-assisted closure system (E-VAC). Surg Endosc. 2014;28(3):896-901. https://doi.org/10.1007/s00464-013-3244-5 [ Links ]
23. Kuehn F, Schiffmann L, Janisch F, Schwandner F, Alsfasser G, Gock M, et al. Surgical endoscopic vacuum therapy for defects of the upper gastrointestinal tract. J Gastrointest Surg. 2016;20(2):237-43. https://doi.org/10.1007/s11605-015-3044-4 [ Links ]
24. Valli PV, Mertens JC, Kroger A, Gubler C, Gutschow C, Schneider PM, et al. Stent over sponge (SOS): A novel technique complementing endosponge therapy for foregut leaks and perforations. Endoscopy. 2018;50(2):148-53. https://doi.org/10.1055/s-0043-120442 [ Links ]
25. Choi SI, Park JC, Jung DH, Shin SK, Lee SK, Lee YC. Efficacy of endoscopic vacuum-assisted closure treatment for postoperative anastomotic leak in gastric cancer. Gut Liver. 2020;14(6):746-54. https://doi.org/10.5009/gnl20114 [ Links ]
26. Winder J, Pauli EM. Novel endoscopic modalities for closure of perforations, leaks, and fistula in the gastrointestinal tract. Tech Gastrointest Endosc. 2019;21(2):109-14. https://doi.org/10.1016/j.tgie.2019.04.004 [ Links ]
Citación: Cañadas-Garrido R, Ramírez-Barranco R, Cáceres-Escobar D. Terapia de vacío endoluminal (Endo-Vac) en el manejo de la fístula de anastomosis esofagogástrica. Rev Colomb Gastroenterol. 2022;37(1):83-89. https://doi.org/10.22516/25007440.708
Recibido: 01 de Enero de 2021; Aprobado: 15 de Diciembre de 2021











 texto en
texto en