Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista colombiana de Gastroenterología
versión impresa ISSN 0120-9957versión On-line ISSN 2500-7440
Rev. colomb. Gastroenterol. vol.38 no.2 Bogotá abr./jun. 2023 Epub 05-Sep-2023
https://doi.org/10.22516/25007440.950
Trabajos originales
Experiencia con el uso de balón intragástrico de contenido líquido para el manejo de la obesidad de riesgo bajo y moderado en un centro de referencia colombiano
1Internist, gastroenterologist, and epidemiologist. Gastroenterology and digestive endoscopy, Gastroadvanced IPS, Clínica Palermo, and Clínica Infantil Santa María del Lago. Bogotá, Colombia. Hospital Internacional de Colombia and Fundación Cardiovascular de Colombia. Bucaramanga, Colombia.
2Gastroenterology and digestive endoscopy, Gastroadvanced IPS. Bogotá, Colombia. Gastroenterology and digestive endoscopy, Hospital Internacional de Colombia and Fundación Cardiovascular de Colombia. Bucaramanga, Colombia.
3Internist. Universidad de La Sabana. Chía, Cundinamarca, Colombia.
4Gastroenterology and digestive endoscopy, Gastroadvanced IPS. Bogotá, Colombia.
5Surgeon, gastroenterology, and digestive endoscopy, Gastroadvanced IPS, Clínica Infantil Santa María del Lago. Bogotá, Colombia.
6Surgeon, gastroenterology, and digestive endoscopy, Gastroadvanced IPS, Clínica Palermo. Bogotá, Colombia.
7Gastroenterology and digestive endoscopy, Gastroadvanced IPS, Clínica Palermo. Bogotá, Colombia.
8Gastroenterology and digestive endoscopy, Gastroadvanced IPS. Bogotá, Colombia.
9Surgeon, gastroenterology, and digestive endoscopy, Gastroadvanced IPS. Bogotá, Colombia.
Introducción:
los balones intragástricos (BIG) de llenado líquido han surgido como una opción segura y eficaz para el manejo de sobrepeso y obesidad. En nuestro medio hay poca información acerca de su implementación en obesidad de riesgo bajo y moderado.
Objetivo:
evaluar la implementación del BIG de contenido líquido en individuos con obesidad de riesgo bajo y moderado en términos de pérdida de peso, seguridad y tolerancia a 4, 6 y 12 meses de tratamiento.
Materiales y métodos:
estudio observacional prospectivo y descriptivo, se incluyeron a 109 sujetos con obesidad de riesgo bajo y moderado (índice de masa corporal [IMC] de 30 a 40 kg/m2), a quienes se les implantó por vía endoscópica un BIG de llenado líquido. Se analizaron las variables de sexo, edad, peso inicial y final, porcentaje de pérdida de peso y efectos secundarios.
Resultados:
109 sujetos, 75,22% correspondieron a mujeres, el peso promedio fue de 87,22 kg, con IMC promedio de 31,59 kg/m2. Se usaron tres marcas (Orbera, n: 103; Spatz, 3, n: 3; y Elipse, n: 3). La pérdida de peso promedio presentó diferencias importantes al analizar por meses y marcas: Elipse: 4 meses (-4,6 kg), Spatz 3: 3 meses (-7 kg), Orbera: 6 meses (15,2 kg), Orbera: 12 meses (19,7 kg). Se logró la reducción del IMC promedio a 27,71 kg/m2. La tasa de complicaciones fue del 2,75%, 2 (1,83%) por intolerancia (dolor abdominal) y una por apendicitis aguda (0,91%).
Conclusiones:
El BIG de llenado líquido es un procedimiento seguro y eficaz. Un período de implantación del BIG de al menos 12 meses se considera óptimo para obesidad de riesgo bajo y moderado.
Palabras clave: Balón gástrico; riesgo; obesidad; pérdida de peso; manejo de la obesidad; endoscopia
Introduction:
Liquid-filled intragastric balloons (IGBs) have emerged as a safe and effective option for managing overweight and obesity. However, there is limited information available regarding the implementation of liquid IGBs in individuals with low- and moderate-risk obesity.
Objective:
The objective of this study was to assess the implementation of liquid IGBs in low- and moderate-risk obese individuals in terms of weight loss, safety, and tolerance at four, six, and twelve months of treatment.
Materials and methods:
This prospective, descriptive observational study included 109 subjects with low- and moderate-risk obesity (body mass index [BMI] of 30-40 kg/m2), who underwent endoscopic implantation of liquid-filled IGBs. The variables analyzed included sex, age, initial and final weight, percentage of weight loss, and side effects.
Results:
Out of the 109 subjects, 75.22% were women. The average weight at baseline was 87.22 kg, with an average BMI of 31.59 kg/m2. Three different brands of IGBs were used: Orbera (n=103), Spatz3 (n=3), and Elipse (n=3). The average weight loss showed significant differences when analyzed by months and brands-Ellipse: four months (-4.6 kg), Spatz3: three months (-7 kg), Orbera: six months (15.2 kg), Orbera: twelve months (19.7 kg). The average reduction in BMI achieved was 27.71 kg/m2. The complication rate was 2.75%, with two cases (1.83%) attributed to intolerance (abdominal pain) and one case due to acute appendicitis (0.91%).
Conclusions:
The findings of this study indicate that liquid-filled IGBs are a safe and effective procedure for managing low- and moderate-risk obesity. A minimum duration of twelve months with an IGB implantation is considered optimal for individuals with low- and moderate-risk obesity.
Keywords: Gastric balloon; risk; obesity; weight loss; obesity management; endoscopy
Introducción
La obesidad es un problema de salud pública con alta morbimortalidad. Se ha demostrado que el aumento de 5 kg/m2 en el índice de masa corporal (IMC) por encima de 25 kg/m2 se asocia a un mayor riesgo de mortalidad por todas las causas1. También se considera una enfermedad crónica y de difícil manejo, que condiciona a múltiples complicaciones metabólicas, cardiovasculares, articulares y psicosociales. Se ha descrito que lograr una pérdida de peso sostenida del 5% al 10% puede prevenir y reducir el riesgo cardiovascular y otras complicaciones en personas con obesidad2.
En el manejo inicial se incluyen medidas conservadoras como la restricción calórica, ejercicio y cambios comportamentales. La farmacoterapia se recomienda en pacientes que fracasan en la pérdida de peso y el abordaje quirúrgico se reserva para personas extremadamente obesas3. El balón intragástrico (BIG) se encuentra en un escalón intermedio entre el manejo médico y quirúrgico4,5, es una opción atractiva por considerarse un método temporal (menor a 6 meses), reversible, mínimamente invasivo, seguro y eficaz para la pérdida de peso6-8. Se ha llegado a demostrar una media de pérdida de peso corporal total del 15,5% en adultos con sobrepeso u obesidad 1 año después de su extracción7.
Actualmente hay varios modelos de BIG que incluyen los de contenido líquido o de aire, los más utilizados comprenden los de llenado líquido, debido a su menor tasa de complicaciones9. Al ser colocado, el BIG flota libremente en el estómago, con un mecanismo de acción multifactorial, con cambios fisiológicos y neurohormonales, lo que lleva a un aumento de la saciedad y disminuye la capacidad de reservorio gástrico e ingesta de comida4. Puede mantenerse en el estómago 6 meses, y una nueva generación de BIG permite hasta 12 meses10. Los BIG más comúnmente utilizados en la actualidad incluyen Orbera, Spatz 3, Reshape Duo, Bariatrix, Elipse y Heliosphere. Con respecto a cuál usar, no hay ninguna indicación precisa en la literatura, por lo que según el criterio del médico y la experiencia en cada una de sus técnicas se puede escoger la mejor opción11. Aún más, en Colombia hay poca información acerca de los resultados de la implementación de BIG con llenado líquido en obesidad de riesgo bajo y moderado (IMC de 30 a 40 kg/m2).
El propósito de este estudio es evaluar la implementación del BIG de contenido líquido en individuos con obesidad de riesgo bajo y moderado (IMC de 30 a 40 kg/m2) en términos de pérdida de peso, seguridad y tolerancia a los 4, 6 y 12 meses de tratamiento.
Metodología
Diseño del estudio y extracción de datos
Se realizó un estudio observacional prospectivo y descriptivo mediante un muestreo por conveniencia que tomó como población fuente a los pacientes con obesidad de riesgo bajo y moderado (IMC de 30 a 40 kg/m2), en la Clínica Palermo del 1 de enero de 2019 al 31 de diciembre de 2020. La Clínica Palermo es un hospital de tercer nivel y centro de referencia nacional en gastroenterología. La población del estudio consistió en pacientes ≥ 18 años, refractarios al tratamiento conservador y participantes en un programa de pérdida de peso. Se excluyeron a individuos con IMC > 40 kg/m2 o con contraindicaciones para BIG. Todos los pacientes fueron informados y firmaron el consentimiento informado.
Recolección de datos
Como fuente de información primaria se usaron las historias clínicas y el reporte oficial del procedimiento realizado. Se recogieron variables sociodemográficas y clínicas de ingreso. Se analizaron las variables de sexo, edad, peso inicial y final, porcentaje de pérdida de peso y efectos secundarios. Se consideraron complicaciones como efectos adversos atribuibles al BIG después de dos semanas de inserción, identificados durante el seguimiento ambulatorio. Se utilizaron métodos estándar para cuantificación de la pérdida de peso, como el IMC y el porcentaje de pérdida de peso.
Procedimiento
El protocolo de pérdida de peso preprocedimental consistió en el seguimiento ambulatorio multidisciplinario (con gastroenterólogo y nutricionistas). Al inicio del implante del BIG, se manejó con dieta hipocalórica (1000 cal/día) y actividad física.
Se incluyó a 109 pacientes, a quienes se les implantó por vía endoscópica el BIG Orbera de Apollo Endosurgery, Elipse de Allurion y Spatz 3. Cada paciente requirió de un solo BIG con capacidad de llenado de 500-700 mL de líquido (Figura 1). Estos procedimientos se realizaron bajo sedación por anestesiología, sin requerimiento de intubación endotraqueal.
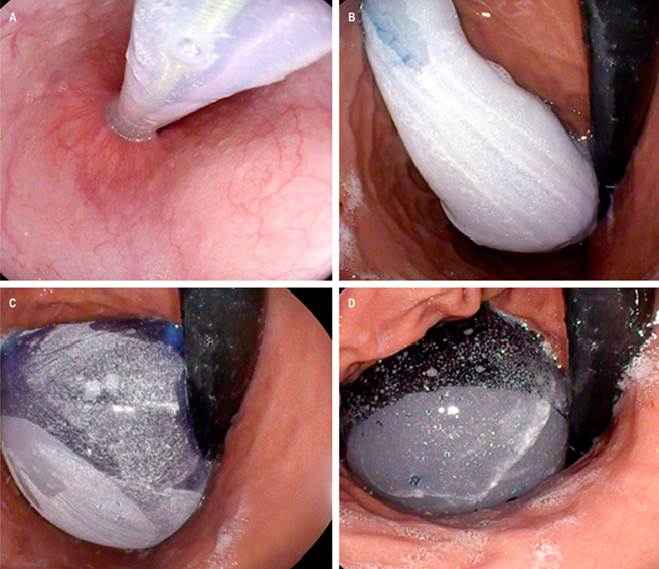
Figura 1 Implante de BIG con llenado líquido. A. Vista endoscópica del posicionamiento del BIG durante el implante. B. Vista endoscópica del BIG que se llena con líquido. C. Vista endoscópica del BIG en una adecuada posición completando el llenado líquido. D. Vista endoscópica del BIG después de haberse completado el llenado, sin fuga de líquido. Imágenes propiedad de los autores.
La extracción también se realizó bajo sedación en 106 pacientes, sin intubación endotraqueal. Se usaron gastroscopios con canal de trabajo de 2,8 mm y accesorios estándar (catéter de aguja, pinzas de cuerpo extraño y asas de polipectomía) (Figura 2). 3 pacientes presentaron expulsión espontánea (elipse de Allurion).
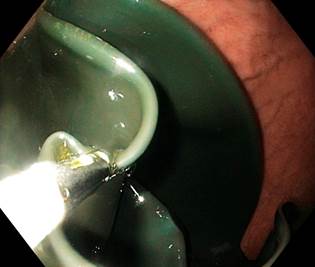
Figura 2 Retiro del BIG por vía endoscópica. Vista endoscópica del globo vacío después de la succión del líquido. Imagen propiedad de los autores.
Además, se realizaron seguimientos periódicos con gastroenterología para evaluar la eficacia y tolerancia. Se prescribieron inhibidores de la bomba de protones (IBP) durante la permanencia del BIG, junto con antieméticos y analgésicos durante las dos primeras semanas. Se realizó el seguimiento del peso en todos los pacientes antes del implante de BIG, en cada control de seguimiento y en la extracción.
Definiciones
Se consideró como peso ideal el correspondiente a 18,7-24,9 kg/m2 para todos los adultos, independientemente de la edad12, y porcentaje de pérdida de peso eficaz de al menos el 10% del peso excesivo13.
Análisis estadístico
Se elaboró la base de datos en Excel versión 2019. Se completaron los datos faltantes con nuevas revisiones de las fuentes de información y al final solo se analizaron datos completos. El procesamiento de datos se realizó en el programa para ciencias sociales SPSS versión 25,0. Para el análisis descriptivo de las variables cuantitativas se utilizó el promedio aritmético, mientras que para las variables cualitativas se utilizaron frecuencias absolutas y relativas.
Consideraciones éticas
Este estudio fue aprobado por el comité de ética e investigación de la Clínica Palermo, Bogotá, Colombia. Las principales fuentes de información incluyeron registros clínicos. En su diseño se tuvieron en cuenta los requerimientos establecidos en la Resolución 8430 de 1993 del Ministerio de Salud de Colombia, de manera que se consideró una investigación de bajo riesgo, y se garantizó confidencialidad y reserva de la información recolectada. Todos los pacientes fueron informados y firmaron el consentimiento informado. Ningún registro contenía información sensible sobre la identidad de los pacientes.
Resultados
De los 109 pacientes intervenidos, 82 correspondieron a mujeres (75,22%), el promedio de peso de los pacientes fue de 87,22 kg, con IMC promedio de 31,59 kg/m2. Las principales comorbilidades al principio del tratamiento fueron hipertensión arterial (HTA; n: 23, 21,1%), diabetes tipo 2 (n: 18, 16,51%), dolores articulares mecánicos en miembros inferiores (n: 15, 13,76%) y síndrome de apnea hipopnea obstructiva del sueño (SAHOS; n: 9, 8,25%) (Tabla 1). Se usaron 3 marcas de balones de llenado líquido, (Orbera, n:103; Spatz 3, n: 3; y Elipse, n: 3).
Tabla 1 Características de los pacientes tratados con BIG al principio del manejo
| Parámetro | Estadística |
|---|---|
| Sexo femenino (n: 82) | 75,22% |
| Edad promedio | 33,44 años |
| Comorbilidades | |
| HTA (n: 23) | 21,10% |
| Diabetes tipo 2 (n: 18) | 16,51% |
| Dolor articular (miembros inferiores) (n: 15) | 13,76% |
| SAHOS (n: 9) | 8,25% |
Tabla elaborada por los autores.
El BIG estuvo implantado por un tiempo promedio de 8,2 meses, y en todos los casos se utilizaron dispositivos con llenado líquido. La media de pérdida de peso varió significativamente entre Elipse y Orbera, aunque fueron muy pocos los casos con esta primera marca. Globalmente se logró una reducción del IMC promedio a 27,71 kg/m2. La pérdida de peso promedio presentó diferencias importantes en los análisis por meses y marcas, respectivamente: Elipse: 4 meses (-4,6 kg), Spatz 3: 3 meses (-7 kg), Orbera: 6 meses (15,2 kg), Orbera 12 meses: (19,7 kg). En la Tabla 2 se muestran las variables antropométricas basales de los pacientes incluidos, y en la Tabla 3, después del implante de BIG.
Tabla 2 Características demográficas y antropométricas basales de los pacientes en el día de la inserción del BIG
| Parámetro | Orbera (n = 103) | Spatz 3 (n = 3) | Elipse (n = 3) |
|---|---|---|---|
| Sexo femenino, n (%) | 80 (77,66) | 2 (66,66) | 2 (66,66) |
| Edad, promedio (DE) | 33,2 (5,2) | 36,4 (3,32) | 38,5 (4,6) |
| Peso inicial, promedio (DE) | 87,36 (8,31) | 85,38 (7,17) | 84,25 (5,92) |
| Peso excesivo, promedio (DE) | 18,27 (3,46) | 19,62 (4,62) | 19,1 (4,03) |
| IMC, promedio (DE) | 31,34 (3,56) | 36,78 (7,23) | 34,98 (5,92) |
BIG: balón intragástrico; DE: desviación estándar; IMC: índice de masa corporal. Tabla elaborada por los autores.
Dado que la muestra poblacional fue pequeña y que se trata de un estudio descriptivo, no fue posible evaluar diferencias estadísticamente significativas entre distintas marcas de BIG. Sin embargo, se observó una tendencia a una mayor pérdida de peso en tiempos de implantación del BIG superiores a 6 meses (Tabla 3).
Tabla 3 Características antropométricas de los pacientes en el día del retiro del BIG
| Parámetro | Orbera, 12 meses (n = 58) | Orbera, 6 meses (n = 45) | Spatz 3 (n = 3) | Elipse (n = 3) |
|---|---|---|---|---|
| Tiempo de implante del BIG, meses, media (DE) | 12 (0,8) | 6 (1,1) | 3 (0,2) | 4 (0,5) |
| Reducción IMC (kg/m2) (media ± DE) | 8,12 ± 3,76 | 7,42 ± 3,34 | 3,3 ± 0,62 | 2,1 ± 0,3 |
| Pérdida de peso (kg), media, (SD) | 19,7 (6,3) | 15,2 (4,32) | 7 (1,83) | 4,6 (0,23) |
| Porcentaje de pérdida de peso excesivo (media ± DE) | 26,2 ± 2,3 | 22,4 ± 1,84 | 10,56 ± 0,92 | 8,5 ± 1,86 |
BIG: balón intragástrico; DE: desviación estándar; IMC: índice de masa corporal. Tabla elaborada por los autores.
Se realizó el retiro del balón antes de los 2 meses en 3 pacientes (2,75%), 2 (1,83%) por intolerancia (dolor abdominal) y una por apendicitis aguda (0,91%). No se documentaron casos de pancreatitis aguda o sangrado digestivo. No se presentaron complicaciones al momento del retiro ni con el procedimiento ni con la sedación.
Discusión
El BIG de llenado líquido es una opción menos invasiva para el manejo de la obesidad de riesgo bajo y moderado, particularmente en casos de IMC mayores de 25 kg/m2 sin resultados óptimos al manejo medico inicial14,15. Más allá de esto, no interfiere de modo permanente con la anatomía gástrica ni con el tamaño del volumen gástrico por intervenciones como suturas, estomas, destrucción térmica de la mucosa, entre otras, utilizadas en otros métodos intervencionistas5,11,16. Las principales complicaciones descritas en la literatura comprenden desinflamiento o migración (hasta 28,9% de los casos), seguido de efectos secundarios menores (0,2%-27%), náuseas y vómitos (18% de los casos)16,17. En el presente estudio se encontró una frecuencia global de complicaciones inferiores al 3%, 2 pacientes (1,83%) por intolerancia (dolor abdominal), y es aproximada a lo descrito en el estudio de Sander y colaboradores18, en el cual hubo un retiro temprano del BIG en el 3% de los casos. La intolerancia se caracteriza por emesis persistente por largos períodos asociada a distensión abdominal, lo que puede llevar a insatisfacción por parte del paciente o falta de motivación19. Esta sintomatología es más atribuible a todos los BIG con llenado gaseoso, y en lo BIG con contenido líquido son menos frecuentes11. En nuestro estudio se requirió el retiro temprano del BIG debido al riesgo particular para desbalance hidroelectrolítico, deshidratación e insuficiencia renal en estos pacientes en particular. El porcentaje de intolerancia encontrado está acorde a lo reportado en la literatura, sin encontrar ninguna característica de base que lo predisponga.
Otras complicaciones menos frecuentes incluyen perforación gástrica, sobrellenado, obstrucción intestinal, dilatación e impactación gástrica20. Ninguna de estas complicaciones se documentó en la población de nuestro estudio, por lo que la incidencia global de estas se considera aceptable. Un paciente (0,91%) en el estudio presentó apendicitis aguda. La presentación de apendicitis es rara en lo descrito en la literatura5, y este evento puede representar una coincidencia más que una causalidad directa relacionada con el BIG o el procedimiento. En el presente estudio se corrobora que la presentación de apendicitis, al igual que las complicaciones relacionadas con el procedimiento, exige la remoción del BIG.
La pérdida de peso es el desenlace principal de interés por excelencia al momento de evaluar los BIG. Los resultados en pérdida de peso son heterogéneos en los diferentes estudios, con resultados variables en relación con múltiples factores11. La mayoría de estudios establecen como criterios de selección a pacientes con IMC mayor o igual a 40 kg/m2, con pérdida de peso variable a los 6 meses de 17 a 21 kg21,22; sin embargo, son pocos los estudios que evalúan específicamente la eficacia del BIG de contenido líquido en pacientes con obesidad de riesgo bajo y moderado en períodos comprendidos de 6 a 12 meses. En un estudio retrospectivo por Fittipaldi-Fernández y colaboradores23 se evaluó la implementación de los BIG en 5874 sujetos con sobrepeso y cualquier grado de obesidad, con una población predominante de mujeres (n = 4081; 74,96%). De acuerdo con los subgrupos, 371 (6,81%) presentaban sobrepeso (IMC: 25-29,99 kg/m2), y 1848 (33,94%), obesidad de grado I (IMC: 30-34,99 kg/m2), y en conjunto correspondieron al 37,7% de la muestra total; de modo global se presentó una pérdida de peso de 19,13 ± 8,86 kg, y de acuerdo con los grupos de obesidad en particular se observó una pérdida de peso de 12,83 ± 4,51 kg y 16,2 ± 6,42 kg en los grupos de sobrepeso y obesidad grado I, respectivamente. En nuestra cohorte encontramos una pérdida de peso mayor a los 12 meses (19,7 kg) y una disminución media del IMC de 3,88 kg/m2, cifra que se aproxima a la descrita por Fittipaldi-Fernández y colaboradores23. Se puede afirmar que los resultados demostrados para pérdida de peso son posiblemente atribuibles a un adecuado seguimiento regular multidisciplinario y a la motivación de los participantes. Es importante mantener un manejo multidisciplinario con nutrición y medidas de ejercicio para evitar la reganancia de peso posterior al retiro del dispositivo.
En nuestro estudio, al hacer el análisis comparativo por sexo se encontró un mayor porcentaje de pérdida de peso en mujeres, estos hallazgos concuerdan con estudios comparativos previos en los que también se ha observado una mayor pérdida de peso excesivo en mujeres23,24; sin embargo , esto se ha atribuido al menor exceso de peso basal en mujeres24. Esto también se puede deber a que en nuestro estudio la mayor parte de la población correspondió a mujeres (75,22% de los casos); previamente, se sabe que las mujeres son más prestas a reportar síntomas gastrointestinales, pedir atención médica oportuna, recibir recomendaciones para pruebas diagnósticas y lograr adherencia a un tratamiento25. En el presente estudio se corrobora el hecho de que las mujeres pueden recibir un tratamiento oportuno para obesidad de riesgo bajo y moderado, así como lograr metas de control de peso en un tiempo óptimo. Se requiere de mayor investigación para aclarar estos hallazgos.
Múltiples estudios han demostrado que del 80% al 90% de la pérdida de peso se logra durante los primeros tres a cuatro meses de la terapia con BIG; después de esto, el estómago se acomoda y se pierde el efecto restrictivo parcialmente, por lo que se requiere un aumento en el volumen del BIG para inducir una mayor pérdida de peso17. En el presente estudio se evaluaron los BIG de última generación, que son ajustables; es decir que a los 3 meses de inserción se pierde el efecto de pérdida de peso, por lo que se necesita agregar volumen al BIG para cambiar el volumen y el peso de este y lograr mejores resultados26.
Estudios recientes han corroborado la eficacia de las marcas de BIG utilizadas en el estudio. A partir de un metaanálisis en 2015, en el que se incluyeron 17 estudios con 1638 pacientes, se demostró un porcentaje de pérdida de peso excesivo del 25,44% (intervalo de confianza [IC] del 95%: 21,47%-29,41%) y 11,27% de pérdida total del peso corporal a los 12 meses con el BIG Orbera, que se considera como una opción de tratamiento apropiado debido a que superaba el umbral de preservación intragástrica y supera el 5% de pérdida total del peso corporal27. Por otro lado, Schwaab y colaboradores en 2020 publicaron un estudio cruzado en el que se incluyeron a 470 sujetos con sobrepeso y obesidad, a 144 de ellos les implantaron un BIG Spatz por hasta 12 meses, y se logró una pérdida de peso corporal total 15,5 ± 9,6%28. En cuanto al BIG Elipse, un metaanálisis por Ramai y colaboradores evaluó 7 estudios con 2152 pacientes, y se demostraron resultados similares, con un porcentaje de pérdida total de peso del 12,2% (IC 95%: 10,1-14,3; índice de inconsistencia [I2]: 94%) y porcentaje de pérdida de peso excesivo del 49,1% (IC 95%: 30,6-67,5; I2 = 97%)29. En nuestro estudio, se evaluaron los BIG de larga duración con capacidad de hasta 12 meses en el estómago, y demostraron mejores resultados y utilidad ya que permite más tiempo para la educación sobre los cambios en el estilo de vida, mientras que los balones de corta duración (menores de 4 meses) no lograron una pérdida significativa de peso. Aunque en más del 90% de los casos se utilizó BIG Orbera, que corroboró la eficacia en objetivos terapéuticos, en los casos en que se utilizaron Spatz y Elipse los resultados en la eficacia fueron similares.
Entre las limitaciones de este estudio se incluye que fue en un solo centro, y en más del 90% de los sujetos se utilizó BIG Orbera, lo que podría limitar su generalización. Sin embargo, se logró mostrar la eficacia y complicaciones del BIG de llenado líquido en población adulta con obesidad de riesgo bajo y moderado, de lo cual hay escasa literatura en Colombia. Se debe mencionar que solo se incluyó a sujetos mayores de 18 años, lo que limita su aplicabilidad en grupos más jóvenes; no obstante, la población adulta incluida en el estudio se considera representativa. La evaluación antropométrica de los pacientes se limitó a una evaluación de bioimpedancia. No se utilizaron otras medidas que podrían haber agregado detalles a la evaluación de los cambios corporales y al impacto del BIG en la composición corporal. Al momento de evaluar la eficacia no se incluyeron otros parámetros metabólicos como niveles de hemoglobina glucosilada, perfil lipídico y desenlaces cardiovasculares, los cuales son de interés para esta población en particular. Al ser un estudio retrospectivo, la calidad de la información puede verse afectada al diligenciamiento de las historias clínicas. La verificación de los datos de los registros clínicos por al menos dos investigadores también pudo disminuir el sesgo de transcripción.
Conclusiones
El BIG de llenado líquido surge como una opción atractiva para el manejo de la obesidad de riesgo bajo y moderado; es un procedimiento seguro y eficaz en el que logran metas óptimas de pérdida de peso.
El seguimiento cuidadoso del paciente es de primordial importancia para evitar complicaciones y respaldar la eficacia del tratamiento, un período de implantación del BIG de al menos 12 meses se considera óptimo para obesidad de riesgo bajo y moderado.
Dado que el BIG representa una alternativa temporal no quirúrgica y no farmacológica para la obesidad, que es totalmente reversible y repetible, debe recomendarse especialmente a pacientes con fracaso terapéutico a alguno de los métodos tradicionales de reducción de peso.
Agradecimientos
Ninguno declarado por los autores.
REFERENCIAS
1. Bhaskaran K, dos-Santos-Silva I, Leon DA, Douglas IJ, Smeeth L. Association of BMI with overall and cause-specific mortality: a population-based cohort study of 3·6 million adults in the UK. Lancet Diabetes Endocrinol. 2018;6(12):944-53. https://doi.org/10.1016/S2213-8587(18)30288-2 [ Links ]
2. Kushner RF, Ryan DH. Assessment and lifestyle management of patients with obesity: Clinical recommendations from systematic reviews. JAMA. 2014;312(9):943-52. https://doi.org/10.1001/jama.2014.10432 [ Links ]
3. Garvey WT, Mechanick JI, Brett EM, Garber AJ, Hurley DL, Jastreboff AM, et al. American association of clinical endocrinologists and American college of endocrinology comprehensive clinical practice guidelines for medical care of patients with obesity. Endocr Pract. 2016;22(Cdc):1-203. https://doi.org/10.4158/EP161365.GL [ Links ]
4. Dayyeh BKA. Intragastric balloons for obesity management. Gastroenterol Hepatol. 2017;13(12):737-9. [ Links ]
5. Kumbhari V, Hill C, Sullivan S. Bariatric endoscopy: State-of-the-art. Curr Opin Gastroenterol. 2017;33(5):358-65. https://doi.org/10.1097/MOG.0000000000000383 [ Links ]
6. Saber AA, Shoar S, Almadani MW, Zundel N, Alkuwari MJ, Bashah MM, et al. Efficacy of First-Time Intragastric Balloon in Weight Loss: a Systematic Review and Meta-analysis of Randomized Controlled Trials. Obes Surg. 2017;27(2):277-87. https://doi.org/10.1007/s11695-016-2296-8 [ Links ]
7. Keren D, Rainis T. Intragastric Balloons for Overweight Populations-1 Year Post Removal. Obes Surg. 2018;28(8):2368-73. https://doi.org/10.1007/s11695-018-3167-2 [ Links ]
8. Yorke E, Switzer NJ, Reso A, Shi X, de Gara C, Birch D, et al. Intragastric Balloon for Management of Severe Obesity: a Systematic Review. Obes Surg. 2016;26(9):2248-54. https://doi.org/10.1007/s11695-016-2307-9 [ Links ]
9. De Castro ML, Morales MJ, Del Campo V, Pineda JR, Pena E, Sierra JM, et al. Efficacy, safety, and tolerance of two types of intragastric balloons placed in obese subjects: A double-blind comparative study. Obes Surg. 2010;20(12):1642-6. https://doi.org/10.1007/s11695-010-0128-9 [ Links ]
10. Silva LB, Neto MG. Intragastric balloon. Minim Invasive Ther Allied Technol. 2021;(Cdc):33571068. https://doi.org/10.1080/13645706.2021.1874420 [ Links ]
11. Stavrou G, Shrewsbury A, Kotzampassi K. Six intragastric balloons: Which to choose? World J Gastrointest Endosc. 2021;13(8):238-59. https://doi.org/10.4253/wjge.v13.i8.238 [ Links ]
12. Donato KA. Executive summary of the clinical guidelines on the identification, evaluation, and treatment of overweight and obesity in adults. Arch Intern Med. 1998;158(17):1855-67. https://doi.org/10.1001/archinte.158.17.1855 [ Links ]
13. Wing RR, Hill JO. Successful weight loss maintenance. Annu Rev Nutr. 2001;21:323-41. https://doi.org/10.1146/annurev.nutr.21.1.323 [ Links ]
14. Ali MR, Moustarah F, Kim JJ. American Society for Metabolic and Bariatric Surgery position statement on intragastric balloon therapy endorsed by the Society of American Gastrointestinal and Endoscopic Surgeons. Surg Obes Relat Dis. 2016;12(3):462-7. https://doi.org/10.1016/j.soard.2015.12.026 [ Links ]
15. Neto MG, Silva LB, Grecco E, de Quadros LG, Teixeira A, Souza T, et al. Brazilian Intragastric Balloon Consensus Statement (BIBC): practical guidelines based on experience of over 40,000 cases. Surg Obes Relat Dis. 2018;14(2):151-9. https://doi.org/10.1016/j.soard.2017.09.528 [ Links ]
16. Olmos MÁM, Cancer E, Bretón I, Álvarez V, Abilés V, Abilés J, et al. Balón intragastrico: Revisión de los dispositivos alternativos a los métodos clásicos (Bioenterics). Nutr Hosp. 2015;31(1):84-91. https://doi.org/10.3305/nh.2015.31.1.8090 [ Links ]
17. Gaur S, Levy S, Mathus-Vliegen L, Chuttani R. Balancing risk and reward: A critical review of the intragastric balloon for weight loss. Gastrointest Endosc. 2015;81(6):1330-6. https://doi.org/10.1016/j.gie.2015.01.054 [ Links ]
18. Sander B, Neto MG, Fittipaldi-Fernandez R, Baretta G, Scarparo J, Diestel C. Intragastric Balloon: A Brazilian Multicentric Study of 3545 Cases. Surg Obes Relat Dis. 2015;11(6):S3. https://doi.org/10.1016/j.soard.2015.10.006 [ Links ]
19. Mitura K, Garnysz K. Tolerance of intragastric balloon and patient’s satisfaction in obesity treatment. Wideochirurgia I Inne Tech Maloinwazyjne. 2015;10(3):445-9. https://doi.org/10.5114/wiitm.2015.54047 [ Links ]
20. Popov VB, Thompson CC, Kumar N, Ciarleglio MM, Deng Y, Laine L. Effect of Intragastric Balloons on Liver Enzymes: A Systematic Review and Meta-Analysis. Dig Dis Sci. 2016;61(9):2477-87. https://doi.org/10.1007/s10620-016-4178-2 [ Links ]
21. Borges AC, Almeida PC, Furlani SMT, Cury MDS, Gaur S. Balões intragástricos em obesos de alto risco em um centro brasileiro: Experiência inicial. Rev Col Bras Cir. 2018;45(1):12-3. https://doi.org/10.1590/0100-6991e-20181448 [ Links ]
22. Mathus-Vliegen EM, Alders PR, Chuttani R, Scherpenisse J. Outcomes of intragastric balloon placements in a private practice setting. Endoscopy. 2015;47(4):302-7. https://doi.org/10.1055/s-0034-1390860 [ Links ]
23. Fittipaldi-Fernández RJ, Zotarelli-Filho IJ, Diestel CF, Klein MRST, de Santana MF, de Lima JHF, et al. Intragastric Balloon: a Retrospective Evaluation of 5874 Patients on Tolerance, Complications, and Efficacy in Different Degrees of Overweight. Obes Surg. 2020;30(12):4892-8. https://doi.org/10.1007/s11695-020-04985-4 [ Links ]
24. Al-Sabah S, Al-Ghareeb F, Ali DAM, Al-Adwani A. Efficacy of intragastric balloon for the management of obesity: experience from Kuwait. Surg Endosc. 2016;30(2):424-9. https://doi.org/10.1007/s00464-015-4212-z [ Links ]
25. Heitkemper M, Jarrett M, Bond EF, Chang L. Impact of sex and gender on irritable bowel syndrome. Biol Res Nurs. 2003;5(1):56-65. https://doi.org/10.1177/1099800403005001006 [ Links ]
26. Fittipaldi-Fernández RJ, Zotarelli-Filho IJ, Diestel CF, Klein MRST, de Santana MF, de Lima JHF, et al. Randomized Prospective Clinical Study of Spatz3® Adjustable Intragastric Balloon Treatment with a Control Group: a Large-Scale Brazilian Experiment. Obes Surg. 2021;31(2):787-96. https://doi.org/10.1007/s11695-020-05014-0 [ Links ]
27. Abu Dayyeh BK, Kumar N, Edmundowicz SA, Jonnalagadda S, Larsen M, Sullivan S, et al. ASGE Bariatric Endoscopy Task Force systematic review and meta-analysis assessing the ASGE PIVI thresholds for adopting endoscopic bariatric therapies Prepared by. Gastrointest Endosc. 2015;82(3):425-438.e5. https://doi.org/10.1016/j.gie.2015.03.1964 [ Links ]
28. Schwaab ML, Usuy EN, de Albuquerque MM, Moreira DM, Derossi VO, Usuy RT. Assessment of weight loss after non-adjustable and adjustable intragastric balloon use. Arq Gastroenterol. 2020;57(1):13-8. https://doi.org/10.1590/s0004-2803.202000000-04 [ Links ]
29. Ramai D, Singh J, Mohan BP, Madedor O, Brooks OW, Barakat M, et al. Influence of the Elipse Intragastric Balloon on Obesity and Metabolic Profile: A Systematic Review and Meta-Analysis. J Clin Gastroenterol. 2021;55(10):836-841. https://doi.org/10.1097/MCG.0000000000001484 [ Links ]
Citación: Flórez-Sarmiento C, Parra-Izquierdo V, Frías-Ordóñez JS, Jaimes-Valderrama E, Castillo JD, Rodríguez CS, Rodríguez V, Piñeros MI, Alvarado J. Experiencia con el uso de balón intragástrico de contenido líquido para el manejo de la obesidad de riesgo bajo y moderado en un centro de referencia colombiano. Revista. colomb. Gastroenterol. 2023;38(2):123-130. https://doi.org/10.22516/25007440.950
Aprobación ética y consentimiento de participación Esta investigación fue revisada y aprobada por el Comité de Ética en Investigación de la institución
Consentimiento para la publicación Se tuvieron en cuenta los requerimientos establecidos en la Resolución 8430 de 1993 del Ministerio de Salud de la República de Colombia, de manera que se consideró una investigación de bajo riesgo, y se garantizó confidencialidad y reserva de la información recolectada. Todos los pacientes fueron informados y firmaron el consentimiento informado. Ningún registro contenía datos sensibles sobre la identidad de los pacientes
Disponibilidad de datos y material Los datos y el material disponibles para la publicación están en el manuscrito y no se omite ninguna información
Recibido: 27 de Julio de 2022; Aprobado: 04 de Octubre de 2022











 texto en
texto en 



