Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista colombiana de Gastroenterología
versão impressa ISSN 0120-9957versão On-line ISSN 2500-7440
Rev. colomb. Gastroenterol. vol.38 no.4 Bogotá out./dez. 2023 Epub 26-Fev-2024
https://doi.org/10.22516/25007440.1060
Trabajos Originales
Eficacia diagnóstica de la calprotectina fecal en enfermedad inflamatoria intestinal: revisión sistemática de la literatura
1 Médica epidemióloga, Universidad de Caldas, Fundación Universitaria Autónoma de las Américas, Clínica Comfamiliar Risaralda. Pereira, Risaralda, Colombia.
2 Médica general, Socimédicos y Clínica San Rafael. Pereira, Colombia.
Introducción:
La enfermedad inflamatoria intestinal es un conjunto de patologías entre las que están incluidas la colitis ulcerativa y la enfermedad de Crohn, las cuales tienen presentación similar. En la actualidad, el diagnóstico y seguimiento de dicha enfermedad se basa principalmente en estudios endoscópicos, pero este método difícilmente puede aplicarse a la monitorización periódica de la enfermedad al ser costoso, invasivo y con disponibilidad limitada. La calprotectina fecal cumple con ser ampliamente disponible, fácil de usar y de precio asequible, y actualmente es el biomarcador mejor caracterizado para el uso en esta patología.
Metodología:
Diseño de investigación tipo revisión sistemática de la literatura de validación de prueba diagnóstica. Se realizó una búsqueda en diferentes bases de datos y para la evaluación de la calidad metodológica se empleó la lista verificación QUADAS-2.
Resultados:
La búsqueda inicial para la selección de los artículos arrojó un total de 352.843 artículos publicados principalmente en PubMed seguido de Scopus y Science Direct. Después de múltiples filtros se logró elegir 221 artículos, los cuales se llevaron a revisión completa. Se valoraron con criterios de inclusión y exclusión, lo que determinó la elección final de 18 artículos.
Conclusiones:
La calprotectina fecal es un marcador sustituto fiable de la actividad endoscópica en la EII. Se evidencia la falta de consenso para delimitar un punto de corte y mejorar la aplicabilidad y la precisión diagnóstica. La colonoscopia sigue siendo en todos los estudios el estándar de oro.
Palabras clave: Enfermedad inflamatoria intestinal; calprotectina fecal; aprobación de pruebas de diagnóstico; biomarcador; eficacia diagnóstica
Introduction:
Inflammatory bowel disease is a group of pathologies that include ulcerative colitis and Crohn’s disease, which have similar manifestations. Currently, the diagnosis and monitoring of this disease rely mainly on endoscopic studies. Still, this method can hardly be applied to periodic disease monitoring as it is expensive, invasive, and not readily available. Fecal calprotectin is widely known, easy to use, and affordable, and it is currently the best-characterized biomarker for this pathology.
Materials and methods:
The research design is a systematic diagnostic test validation literature review. A search was conducted in different databases using the QUADAS-2 checklist to evaluate the methodological quality.
Results:
The initial search yielded 352,843 articles published chiefly in PubMed, followed by Scopus and Science Direct. After multiple filters, 221 papers were selected and wholly reviewed. They were evaluated with inclusion and exclusion criteria, with 18 articles being chosen.
Conclusions:
Fecal calprotectin is a reliable surrogate marker of endoscopic activity in IBD. However, there is a lack of consensus on delimiting a cut-off point and improving applicability and diagnostic accuracy. Colonoscopy remains the gold standard in all studies.
Keywords: Inflammatory bowel disease; fecal calprotectin; approval of diagnostic tests; biomarker; diagnostic efficacy
Introducción
La enfermedad inflamatoria intestinal (EII) es un conjunto de patologías entre las que están incluidas: la colitis ulcerativa (CU) y la enfermedad de Crohn (EC), las cuales tienen patrones de presentación similar, pero sus diferencias son las que permiten la clasificación1,2. La EC se caracteriza por compromiso transmural y fistulizante, que afecta todo el tracto digestivo y la región perineal, mientras que la CU presenta compromiso mucoso, el cual está limitado únicamente al colon1.
Las recientes guías de la Organización Europea de Crohn y Colitis (ECCO) para el diagnóstico de CU y EC describen que no existe un “patrón de oro” establecido sino que este se debe realizar por medio de hallazgos clínicos, de laboratorio, imagenológicos, endoscópicos e histopatológicos2. El uso de pruebas genéticas y serológicas no está recomendado2.
En la actualidad, el diagnóstico y seguimiento de la EII se basa principalmente en la evaluación directa de la mucosa en estudios endoscópicos, estos proporcionan información sobre la extensión y gravedad de las lesiones, así como de posibles complicaciones3,4. Sin embargo, la monitorización periódica de la enfermedad difícilmente puede darse por este método dado su elevado costo, su limitada disponibilidad y su carácter invasivo3,4. La calprotectina fecal (CF) cumple con ser ampliamente disponible, fácil de usar y de precio asequible, y es actualmente el biomarcador mejor caracterizado en el ámbito de la EII.
Múltiples estudios han demostrado que la CF es un marcador fiable el cual evalúa la presencia o ausencia de actividad endoscópica, al igual que la gravedad4, por lo que ha mostrado superioridad en comparación con la proteína C-reactiva (PCR) y otros biomarcadores fecales3. Sin embargo, no existe un consenso sobre la evidencia del uso de la CF y ni sobre su validez diagnóstica.
A lo largo este del trabajo se podrán evidenciar las limitaciones de la estrategia diagnóstica actual, la importancia de definir un método diagnóstico y de seguimiento con mayor accesibilidad. Así mismo, se mostrará la disponibilidad de biomarcadores como la CF, que es una ayuda diagnóstica no invasiva que permitiría distinguir la EII de patologías funcionales y, a su vez, identificar recaídas tanto en EC como en CU. Por esto, para el desarrollo de esta investigación se decidió escoger la revisión sistemática de la literatura ya que permite identificar, sintetizar y evaluar la información actual relacionada con la precisión diagnóstica de la CF en pacientes adultos con EII.
Materiales y métodos
El diseño de investigación es de tipo revisión sistemática de la literatura (RSL) sobre la validación de la prueba diagnóstica con el uso de la estrategia de pregunta PICOT. La RSL se realizó siguiendo las recomendaciones de la lista de verificación PRISMA, cumpliendo a cabalidad con la lista de chequeo.
Se desarrolló una estrategia de búsqueda exhaustiva y sistemática para identificar estudios disponibles y relevantes. Se emplearon términos MeSH y DeCS en las diferentes bases de datos: PubMed, Scopus, Science Direct, OVID, Cochrane Library, Scielo, Web of Science y Biblioteca Virtual en Salud. No se utilizaron restricciones de idiomas.
Se realizaron registros de búsqueda, se exportaron los resultados de las diferentes búsquedas al software Rayyan, en el que se seleccionaron los artículos por título y resumen, y en los desacuerdos se realizó la selección por consenso entre los dos investigadores. Se descartaron duplicados por medio del mismo software y, posteriormente, con los artículos seleccionados se realizó una matriz de Excel para cumplimiento de criterios de inclusión y, además, descartar con criterios de exclusión.
En la investigación se incluyeron todos los estudios disponibles en texto completo, realizados entre 1992 y julio de 2022, que hayan sido publicados en inglés, portugués y español. Asimismo, que evaluaran como método diagnóstico la CF en adultos con diagnóstico establecido de EII reportado por otro método diagnóstico. Por el contrario, se descartaron estudios que incluyeran pacientes con diagnóstico de otra patología que altere la CF o que hayan sido realizados en animales. Además, se excluyeron documentos con datos incompletos y que no contaran con las variables para el análisis de datos.
Ya con el grupo de artículos rigurosamente seleccionados con lectura de título y resúmenes se prosiguió a la lectura del texto completo para evaluar su elegibilidad y así, finalmente, obtener los estudios para realizar la síntesis de la información y definir el nivel de evidencia con ayuda de la herramienta QUADAS-2 (Quality Assessment of Diagnostic Accuracy Studies).
Para la evaluación de la calidad metodológica de los estudios de métodos diagnósticos se empleó la lista verificación QUADAS-2 para estudios de precisión diagnóstica, usando los 4 dominios: selección de pacientes; prueba índice; estándares de referencia, flujo y tiempo, y su correspondiente aplicabilidad5. Esta herramienta está totalmente disponible en el sitio web y fue adaptada para nuestro tipo de estudio y aplicada por ambos investigadores. Esta herramienta está diseñada para evaluar la calidad de los estudios primarios de precisión diagnóstica, pero no para reemplazar el proceso de extracción de datos de la revisión, y debe aplicarse además de la extracción de los datos primarios.
Para medir la eficacia diagnóstica se determinaron medidas como sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo; además, se tomaron en cuenta medidas como punto de corte y área bajo la curva en los estudios que lo permitían6. Después de la verificación de la calidad de la información se procedió a organizar y a documentar mediante características, diseño, población, muestra y condiciones del estudio las investigaciones seleccionadas para realizar la comparación, y así realizar una matriz con la evidencia.
La RSL se trata de un estudio de síntesis de la información; es decir, un estudio de estudios que no tiene como objeto de estudio los individuos (ni seres humanos ni animales). Sin embargo, esta RSL fue evaluada por el comité de ética de la Universidad de Caldas, y se obtuvo el respectivo aval. Además, se trató de disminuir los sesgos y así evitar la manipulación indebida de la información.
Resultados
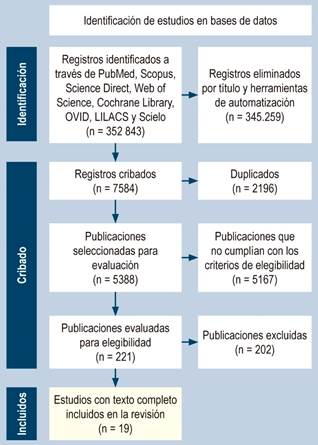
La búsqueda inicial para la selección de los artículos arrojó un total de 352 843 artículos publicados principalmente en PubMed, seguido de Scopus, Science Direct, Cochrane Library, OVID y Web of Science, y en español, LILACS y Scielo. Por la gran cantidad de hallazgos en la búsqueda, se decidió realizar un primer filtro por título y quedó un total de 7584 artículos. Después de esto, por medio del software Rayyan (Intelligent Systematic Review) se detectaron y descartaron 2196 artículos duplicados; después de cribar los duplicados quedó un total de 5388, los cuales fueron revisados por título y resumen con dinámica de doble ciego, descartando principalmente los estudios realizados en animales, en población pediátrica y obstétrica. También se descartó una gran cantidad de estudios cuyo objetivo era evaluar el tratamiento y no la precisión diagnóstica, y otro grupo realizaba los estudios en calprotectina sérica. Además, se seleccionaron únicamente artículos que estuvieran disponibles en inglés, español y portugués. Finalmente, se eligieron 221 artículos, los cuales se llevaron a revisión completa. Lo anterior se encuentra resumido en la Figura 1.
En este punto se revisaron los artículos de manera completa verificando que evaluaran la precisión diagnóstica de la CF, que la población en estudio no tuviera otra patología que pudiera afectar los resultados de CF y que contaran con todos los datos para permitir la evaluación de la precisión diagnóstica, por lo que se incluyeron en la RSL 19 artículos escritos principalmente en idioma inglés.
El resultado final de la RSL, presentado en la Tabla 1, incluyó 18 artículos escritos principalmente en inglés en los períodos comprendidos entre 2004 y 2019, sobre todo en el año 2018 con 5 artículos seleccionados, año en el que se encontró la mayor cantidad de publicaciones. Se logró evidenciar como diseño de estudio más frecuente el tipo de cohorte prospectiva en un 61,1%, cohorte retrospectiva en un 15,8%, al igual que casos y controles, y un 5,5% restante equivalente a 1 estudio observacional de corte transversal.
Tabla 1 Características de los estudios seleccionados
Tabla elaborada por los autores.
La mayoría de estudios se realizaron en población con diagnóstico definitivo o presuntivo de EII; además, en uno de los artículos la población estudiada fue pacientes que acudieron con síntomas gastrointestinales sugestivos de EII y las personas sanas se encontraron como grupo de control en 2 de los artículos.
Los estudios se realizaron en población adulta, como se indicó en los criterios de inclusión; sin embargo, 2 artículos no contaban con la edad de los participantes. De los 18 estudios elegidos, 5 no diferenciaron el sexo de los participantes; mientras que, en 8 estudios (el 44,4%) predominaron los participantes de sexo masculino y en el 26,1% restante predominaron las mujeres.
En todos los artículos se utilizaron como criterios de exclusión que los sujetos del estudio no hubiesen consumido antiinflamatorios no esteroideos o antibióticos durante los tres meses anteriores a su inscripción, no padecer enfermedades graves concomitantes, no estar en embarazo y no tener abuso de alcohol.
Del total de los estudios, 14 de ellos estudiaron la actividad clínica para determinar el riesgo de recaída y 2 de ellos analizaron la CF para distinguir entre EII y trastorno orgánico tipo síndrome de intestino irritable (SII), 1 estudio evaluó ambas problemáticas y otro estudio, por el contrario, usó la CF para evaluar la progresión tanto en CU como en EC.
En el 94,4% de los artículos se realizó el diagnóstico de EII por medio de estudios endoscópicos como la colonoscopia total o la sigmoidoscopia y solo en uno de los artículos se utilizó la exploración de glóbulos blancos radiomarcados (WCS) para este fin.
Para la clasificación de progresión de EII se utilizó la clasificación de Montreal, usada principalmente en CU. Esta escala fue utilizada en 3 de los estudios en los que el fenotipo principal fue el inflamatorio (B1), seguido del estenosante (B2). La puntuación de Mayo, también validada para categorizar la actividad clínica en la CU, se utilizó en 11 de los 18 estudios, en los que concluyó recaída o enfermedad activa con una puntuación mayor de 2, en 1 estudio se estableció a partir de 4 puntos y en 7 estudios se encontró el uso del índice de actividad de enfermedad de Crohn (CDAI) que estableció 150 mg/g como punto de corte para definir actividad clínica o, por el contrario, remisión. También se utilizaron en los artículos la puntuación endoscópica simple de enfermedad de Crohn (SES-CD), el índice de Harvey-Bradshaw, en el que solo se utilizan 5 variables del CDAI, y el índice de Truelove-Witts en CU para definir brotes.
La CF fue empleada como método diagnóstico en la totalidad de los artículos, como se especificó en los criterios de inclusión; 13 de los artículos reportaron que las heces fueron congeladas a -20 ºC para posteriormente ser procesadas, 1 artículo refería entre -2 y -4 ºC y otro en estudio se congelaron las muestras a -80 ºC, mientras que 3 artículos no refirieron su protocolo de toma y manejo de muestras. A su vez, 6 artículos mostraron que el método de procesamiento de la muestra fue ensayo de inmunoabsorción ligado a enzimas, 4 estudios se procesaron con método de ensayo de prueba cualitativa y 3 estudios con inmunoensayo enzimático de fluorescencia.
En la totalidad de los artículos seleccionados, que se encuentran resumidos en la Tabla 2, se utilizó la curva ROC para determinar el mejor valor de corte de la CF; sin embargo, no hay consenso en los puntos de corte, que oscilan desde 48,5 hasta 710 μg/g. Estos valores contaban con una variación en la sensibilidad importante: desde el 70% hasta valores del 100%, mientras que los valores de especificidad encontrados fueron un poco más heterogéneos: desde el 50% con punto de corte de 15 μg/g hasta el 100%. Se calcularon las razones de verosimilitud positiva (LR+) y negativa (LR-) para la totalidad de los artículos y se pudo concluir que, según la LR+, en 4 artículos la CF permite confirmar con certeza altamente relevante la presencia de enfermedad y, en estos mismos artículos, la CF logró tener la LR- tan baja que es altamente relevante para descartar enfermedad; sin embargo, en 3 artículos se refirieron a estos valores con una mala relevancia, tanto para confirmar como para descartar la patología.
Tabla 2 Evaluación de precisión diagnóstica
Tabla elaborada por los autores.
Para la evaluación de la calidad metodológica de los estudios de métodos diagnósticos se utilizó la lista verificación QUADAS-2 para estudios de precisión diagnóstica en forma de cuestionario con preguntas de sí/no que clasificaban los dominios con alto o bajo riesgo(34). Esta herramienta está totalmente disponible en el sitio web, fue adaptada para nuestro tipo de estudio y aplicada por ambos investigadores.
Con los datos organizados en la matriz de Excel, como se muestra en la Tabla 3, se logró evidenciar que, en el dominio 1 enfocado hacia la selección de pacientes, se encuentran 13 estudios con bajo riesgo de sesgo; en el dominio 2, por su parte, se evidencia una frecuencia más alta de preocupación de alto riesgo de sesgo en 6 estudios; mientras que en el dominio 4 (que se enfoca en el sesgo que el flujo y el cronograma de pacientes podría introducir) se encuentran 4 estudios con alto riesgo, y en el dominio 3, la totalidad de los artículos tienen bajo riesgo para sesgo. Lo anterior lleva a concluir que 8 estudios tienen alta preocupación por la introducción de sesgos; sin embargo, la gran mayoría de artículos tienen baja preocupación. La aplicabilidad, por su parte, solo se encuentra con alta preocupación en un estudio con respecto a la prueba índice, y el 94,7% restante se encuentra con baja preocupación.
Tabla 3 Evaluación del riesgo de sesgo de los estudios
| # | Dominio 1 | Dominio 2 | Dominio 3 | Dominio 4 | |||
|---|---|---|---|---|---|---|---|
| Selección de pacientes | Aplicabilidad | Prueba índice | Aplicabilidad | Prueba de referencia | Aplicabilidad | Flujo y cronograma | |
| 1 | Alto | Bajo | Alto | Bajo | Bajo | Bajo | Alto |
| 2 | Bajo | Bajo | Alto | Bajo | Bajo | Bajo | Alto |
| 3 | Alto | Bajo | Alto | Bajo | Bajo | Bajo | Alto |
| 4 | Alto | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 5 | Bajo | Bajo | Alto | Bajo | Bajo | Bajo | Bajo |
| 6 | Alto | Bajo | Alto | Bajo | Bajo | Bajo | Bajo |
| 7 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 8 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 9 | Alto | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 10 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 11 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 12 | Bajo | Bajo | Alto | Alto | Bajo | Bajo | Alto |
| 13 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 14 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 15 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 16 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 17 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| 18 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
Tabla elaborada por los autores.
Se hace la claridad de que esta evaluación no debe usarse para “puntaje de calidad”, ya que es una metodología enfocada en el riesgo de sesgos y de aplicabilidad7. Si un estudio se considera “alto” o “bajo” en uno o más dominios, entonces se puede considerar “en riesgo de sesgo” o con “preocupación con respecto a la aplicabilidad” (8. Por recomendación, no se usó una metodología que arrojara un puntaje resumido de calidad porque la interpretación del puntaje resumido podría ser problemática y potencialmente engañosa9.
Discusión
Esta investigación correspondió a una RSL que evaluó la calidad de la evidencia científica con respecto a la eficacia diagnóstica de la CF en pacientes adultos con EII y su capacidad para distinguir entre trastornos funcionales y orgánicos intestinales, como el SII y la EII, así como su respectiva actividad clínica para definir recaída o remisión.
Estudios previos han señalado la importancia de realizar una búsqueda bibliográfica rigurosa y extensa para garantizar la confiabilidad de la RSL. Se encontró una RSL realizada en 2007 por Gisbert y colaboradores, cuya búsqueda bibliográfica fue realizada solo en Medline10; se estima que aproximadamente solo el 60% de la literatura disponible se encuentra en esta base de datos, en contraste con nuestro estudio, en el que se realizó una búsqueda exhaustiva en múltiples bases de datos (Cochrane Library, PubMed, Scopus, Science Direct, OVID, Scielo, Web of Science y Biblioteca Virtual en Salud), garantizando así la mayor cobertura posible del tema en desarrollo.
Por otro lado, se aprecia que la gran mayoría los artículos incluidos en esta revisión tiene bajo riesgo de sesgos; mientras que en el estudio realizado por Orcajo-Castelán, en el que se utilizaron varias metodologías para la evaluación de precisión diagnóstica, se concluyó que no existen publicaciones científicas que estén libres de sesgos, aunque existen procedimientos para reducirlos11.
En una RSL de precisión de prueba diagnóstica realizada por Hosseini y colaboradores en 2022 también se utilizó QUADAS-2, herramienta exclusiva para estudios de precisión diagnóstica. Tanto en nuestro estudio como en la revisión de Hosseini y colaboradores se utilizó dicho método de forma independiente por los autores, con la diferencia de que en dicha RSL se incluyó un tercer autor, que evaluó las discrepancias de los dos autores principales. Cabe destacar que, además, clasificaron los sesgos como de bajo, moderado y alto riesgo, mientras que en nuestra revisión solo se incluyó alto y bajo riesgo, según los dominios y su aplicabilidad12.
Es importarte resaltar que la mayoría de artículos encontrados fueron desarrollados en el año 2018 y, a pesar de no tener claridad acerca de este fenómeno, se infiere que esto respondió al aumento en la incidencia de la EII y su reconocimiento, puesto que en años anteriores dicha patología continuaba siendo mal clasificada o subdiagnosticada.
En 1992, Roseth y colaboradores desarrollaron el primer método de determinación de CF mediante una técnica de enzimunoanálisis de adsorción (ELISA)13; desde entonces, el método se ha mejorado y validado extensamente y se emplean muestras muy pequeñas de heces14. Sin embargo, solo se encuentra literatura que cumpla con los requisitos de validez de precisión diagnóstica desde 2004, que puede corresponder a los avances tecnológicos del método diagnóstico y a la divulgación de su uso para la práctica clínica habitual.
Resulta claro que el principal diseño epidemiológico utilizado en estudios de precisión diagnóstica es de tipo prospectivo, seguido por el de tipo retrospectivo. En un estudio realizado en 2010 por gastroenterólogos pediatras, se mostró que todos los estudios evaluados tenían un diseño epidemiológico prospectivo e incluyeron pacientes ambulatorios consecutivos con sospecha de EII15. En dicha RSL se analizó una muestra inferior a la presentada en este trabajo, con la diferencia de que incluyeron 6 artículos en adultos y 6 en población pediátrica15.
La CF es un indicador indirecto del estado de la mucosa intestinal. Hasta la fecha, varios metaanálisis han demostrado que es útil para discriminar la EII de otras enfermedades, principalmente orgánicas, y predecir la recaída de los pacientes con EII en remisión evaluando la actividad clínica con los diferentes índices16, lo que también se evidencia en los resultados de esta investigación.
Esta RSL en conjunto con información encontrada en la literatura logra confirmar que el nivel de CF está asociado directamente con los índices de actividad clínica y endoscópica de la EII, con una alta sensibilidad y especificidad. Lo anterior permite concluir que es una herramienta útil en la práctica clínica con beneficios como reducción en procedimientos invasivos, diagnósticos tempranos de recaída y seguimiento en la remisión, debido a que es una prueba fácil de realizar, no invasiva y de relativo bajo costo en comparación con la colonoscopia. Sin embargo, no se ha realizado un consenso para establecer un punto de corte óptimo para la identificación de enfermedad orgánica frente a la funcional, ni para identificar recaída15,17,18. Los datos actuales aún no son concluyentes respecto a un nivel de corte de CF como predictor de actividad clínica o remisión, pues se encontraron valores de corte que varían de 48,5 a 710 μg/g18,19.
Una RSL realizada en 2013 mostró que la mayoría de los estudios que evalúan la CF utilizaron mecanismos de ELISA y gran parte de los fabricantes recomendaron como punto de corte 50 μg/g17, al igual que en el presente estudio. Además, continúa siendo la principal prueba de referencia la colonoscopia18, que se considera el estándar de oro para la evaluación de la inflamación de la mucosa intestinal, aunque es un procedimiento costoso e invasivo; de allí el interés en biomarcadores como la CF, que pueden tener un rendimiento comparable a la colonoscopia.
Conclusión
La CF es un marcador sustituto fiable de la actividad endoscópica en la EII, y es especialmente útil en la predicción de la actividad endoscópica para ayudar a la diferenciación de la enfermedad funcional de la orgánica; por tanto, tiene el potencial de ser usado como biomarcador de diagnóstico y seguimiento en pacientes con EII, sin desconocer que falta consenso para delimitar un punto de corte y mejorar la aplicabilidad y la precisión diagnóstica. La colonoscopia sigue siendo en todos los estudios el estándar de oro.
La evidencia que hay hasta el momento parte de estudios de diseño prospectivo que en su gran mayoría tienen bajo riesgo de sesgo con baja preocupación de su aplicabilidad; sin embargo, son necesarios más estudios para desarrollar consensos para la toma de decisiones en el ámbito clínico.
REFERENCIAS
1. Aguirre D, Archila PE, Carrera J, Castaño R, Escobar CM, García Duperly R, et al. Consenso Colombiano de Enfermedad Inflamatoria Intestinal. Rev Col Gastroenterol. 2012;27(3 supl):s1-s44. [ Links ]
2. Juliao-Baños F, Puentes F, López R, Saffon MA, Reyes G, Parra V, et al. Caracterización de la enfermedad inflamatoria intestinal en Colombia: resultados de un registro nacional. Rev Gastroenterol Méx. 2021;86(2):153-62. https://doi.org/10.1016/j.rgmx.2020.05.005 [ Links ]
3. Guardiola J, Lobatón T, Cerrillo E, Ferreiro-Iglesias R, Gisbert JP, Domènech E, et al. Recomendaciones del Grupo Español de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa (GETECCU) sobre la utilidad de la determinación de calprotectina fecal en la enfermedad inflamatoria intestinal. Gastroenterol Hepatol. 2018;41(8):514-29. https://doi.org/10.1016/j.gastrohep.2018.05.029 [ Links ]
4. Spiceland CM, Lodhia N. Endoscopy in inflammatory bowel disease: Role in diagnosis, management, and treatment. World J Gastroenterol. 2018;24(35):4014-20. https://doi.org/10.3748/wjg.v24.i35.4014 [ Links ]
5. Juliao-Baños F, Arrubla M, Osorio L, Camargo J, Londoño J, Cáceres C, et al. Caracterización y prevalencia de manifestaciones extraintestinales en una cohorte de pacientes con enfermedad inflamatoria intestinal en Medellín (Colombia). Gastroenterol Hepatol. 2021;44(6):398-404. https://doi.org/10.1016/j.gastrohep.2020.07.012 [ Links ]
6. Seyedian SS, Nokhostin F, Malamir MD. A review of the diagnosis, prevention, and treatment methods of inflammatory bowel disease. J Med Life. 2019;12(2):113-22. https://doi.org/10.25122/jml-2018-0075 [ Links ]
7. Frolkis A, Dieleman LA, Barkema HW, Panaccione R, Ghosh S, Fedorak RN, et al. Environment and the inflammatory bowel diseases. Can J Gastroenterol. 2013;27(3):e18-24. https://doi.org/10.1155/2013/102859 [ Links ]
8. Bernstein CN, Blanchard JF, Rawsthorne P, Wajda A. Epidemiology of Crohn’s Disease and Ulcerative Colitis in a Central Canadian Province: A Population-based Study. Am J Epidemiol. 1999;149(10):916-24. https://doi.org/10.1093/oxfordjournals.aje.a009735 [ Links ]
9. Ng SC, Shi HY, Hamidi N, Underwood FE, Tang W, Benchimol EI, et al. Worldwide incidence and prevalence of inflammatory bowel disease in the 21st century: a systematic review of population-based studies. Lancet. 2017;390(10114):2769-78. https://doi.org/10.1016/S0140-6736(17)32448-0 [ Links ]
10. Kotze PG, Underwood FE, Damião AOMC, Ferraz JGP, Saad-Hossne R, Toro M, et al. Progression of Inflammatory Bowel Diseases Throughout Latin America and the Caribbean: A Systematic Review. Clin Gastroenterol Hepatol. 2020;18(2):304-12. https://doi.org/10.1016/j.cgh.2019.06.030 [ Links ]
11. Orcajo-Castelán R, Sidonio-Aguayo B, Alcacio-Mendoza JA, López-Díaz GL. Análisis comparativo de pruebas de tamiz para la detección de problemas en el desarrollo diseñadas y validadas en México. Boletín Médico del Hospital Infantil de México. 2015;72(6):364-75. https://doi.org/10.1016/j.bmhimx.2015.11.004 [ Links ]
12. Hosseini P, Whincup R, Devan K, Ghanem DA, Fanshawe JB, Saini A, et al. The role of the electroencephalogram (EEG) in determining the aetiology of catatonia: a systematic review and meta-analysis of diagnostic test accuracy. EClinicalMedicine. 2023;56:101808. https://doi.org/10.1016/j.eclinm.2022.101808 [ Links ]
13. Røseth AG, Fagerhol MK, Aadland E, Schjønsby H. Assessment of the neutrophil dominating protein calprotectin in feces. A methodologic study. Scand J Gastroenterol. 1992;27(9):793-8. https://doi.org/10.3109/00365529209011186 [ Links ]
14. Rodrigo L. Calprotectina fecal. Rev Esp Enferm Dig. 2007;99(12):683-8. https://doi.org/10.4321/S1130-01082007001200001 [ Links ]
15. van Rheenen PF, Van de Vijver E, Fidler V. Faecal calprotectin for screening of patients with suspected inflammatory bowel disease: diagnostic meta-analysis. BMJ. 2010;341:c3369. https://doi.org/10.1136/bmj.c3369 [ Links ]
16. Lin J-F, Chen J-M, Zuo J-H, Yu A, Xiao Z-J, Deng F-H, et al. Meta-analysis: Fecal Calprotectin for Assessment of Inflammatory Bowel Disease Activity. Inflamm Bowel Dis. 2014;20(8):1407-15. https://doi.org/10.1097/MIB.0000000000000057 [ Links ]
17. Waugh N, Cummins E, Royle P, Kandala NB, Shyangdan D, Arasaradnam R, et al. Faecal calprotectin testing for differentiating amongst inflammatory and non-inflammatory bowel diseases: systematic review and economic evaluation. Health Technol Assess. 2013;17(55):xv-xix, 1-211. https://doi.org/10.3310/hta17550 [ Links ]
18. Rokkas T, Portincasa P, Koutroubakis IE. Fecal calprotectin in assessing inflammatory bowel disease endoscopic activity: a diagnostic accuracy meta-analysis. J Gastrointestin Liver Dis. 2018;27(3):299-306. https://doi.org/10.15403/jgld.2014.1121.273.pti [ Links ]
19. Boube M, Laharie D, Nancey S, Hebuterne X, Fumery M, Pariente B, et al. Variation of faecal calprotectin level within the first three months after bowel resection is predictive of endoscopic postoperative recurrence in Crohn’s disease. Dig Liver Dis. 2020;52(7):740-4. https://doi.org/10.1016/j.dld.2020.03.020 [ Links ]
Citación: Gómez-Raigosa J, Valencia-Sánchez N. Eficacia diagnóstica de la calprotectina fecal en enfermedad inflamatoria intestinal: revisión sistemática de la literatura. Revista. colomb. Gastroenterol. 2023;38(4):430-438. https://doi.org/10.22516/25007440.1060
Recibido: 27 de Marzo de 2023; Aprobado: 30 de Junio de 2023











 texto em
texto em