Introducción
La colitis ulcerativa pediátrica (CUP), la enfermedad de Crohn pediátrica (ECP) y la enfermedad inflamatoria intestinal pediátrica no clasificable (EIIPNC) tienen particularidades clínicas y psicosociales que las diferencian de las del adulto y que pueden condicionar enfoques terapéuticos distintos, especialmente por las posibles repercusiones nutricionales y sobre el crecimiento y el desarrollo, lo que representa un desafío tanto para el pediatra como para el gastroenterólogo. Por esta razón, este consenso tiene como objetivo principal generar recomendaciones para el diagnóstico y el tratamiento oportunos y seguros de la enfermedad inflamatoria intestinal (EII) en menores de 18 años, tanto para los profesionales de la salud que atienden estos pacientes como para los pagadores del gasto en salud.
Epidemiología
La enfermedad inflamatoria intestinal pediátrica (EIIP) ha ido aumentado en las últimas décadas, especialmente en la población urbana de los países desarrollados. La incidencia de la EII alcanza su punto máximo durante la adolescencia y/o en el adulto joven hasta en un 30% de los casos diagnosticados antes de los 20 años1,2. En Europa se reportó recientemente una incidencia de ECP y CUP de 0,3-10 y de 0-9,5 por 100.000, respectivamente, y una prevalencia de ECP y CUP entre 8,2-60 y entre 8,3-30 por 100.000, respectivamente, con una mayor incidencia de norte a sur que de este a oeste. En Estados Unidos de Norteamérica (EE. UU.) se reporta una prevalencia para ECP y CUP de 2 y de 4,5 por 100.000, respectivamente, y se encuentra que solo un 4% ocurren antes de los 4 años y un 20% antes de los 10; esto sugiriere que 10.000 casos nuevos son diagnosticados anualmente en menores de 18 años2. En Latinoamérica, los estudios epidemiológicos de EIIP son escasos, sin embargo, en un reciente estudio multicéntrico se reportaron 607 pacientes: 475 (78,3%) con CUP, 104 (17,1%) con ECP y 28 (4,6%) con EIINCP, lo que se traduce en un incremento lineal de la CUP anual, la mayoría con pancolitis3. En Colombia, el primer registro de EIIP se presentó en 2013 con un reporte de 66 pacientes: 50% de sexo femenino, de 10,1 (± 4,3) años; 36 (54,5%) con CUP, 27 (41%) con ECP y 3 (4,5%) con EIIPNC (datos no publicados). En 2021 se inició el segundo registro nacional, en el cual participaron 21 instituciones distribuidas en ocho ciudades del país y se identificaron 209 pacientes con EII; de estos, 54,55% de sexo masculino, 104 (53,06%) con CUP típica, 52 (26,53%) con ECP, 18 (9,18%) con EII no clasificable, 11 (5,61%) con CUP atípica y 11 (5,61%) con ECP colónica (Registro Nacional de EIIP).
Metodología
Primera etapa
Se seleccionó un panel de 32 expertos en EIIP del Colegio Colombiano de Gastroenterología, Hepatología y Nutrición Pediátrica (COLGAHNP), un grupo multidisciplinario, incluyendo un revisor experto internacional (Javier Martín de Carpi), y dos epidemiólogos. Cada uno de los miembros del panel de expertos declaró sus conflictos de intereses antes de iniciar la redacción del consenso, y solo uno de los expertos tenía un conflicto de interés por trabajar con la industria; sin embargo, no tenía conflicto con los temas asignados del consenso. El equipo coordinador realizó una búsqueda sistemática de la literatura con especial énfasis en las principales guías de práctica clínica (GPC), estudios clínicos aleatorizados (ECA) y revisiones sistemáticas de la literatura mediante las bases de datos Medline, Embase, Cochrane Central, artículos de la base de datos LILACS y SciELO en el contexto latinoamericano, y referencias de revisiones en idioma inglés y español de los últimos diez años (2010-2020). Para la búsqueda se emplearon términos MeSH tanto en español como en inglés (inflammatory bowel disease, Crohn’s disease, ulcerative colitis, practice guideline, child, pediatrics) y se escogieron como base las 12 guías más importantes en español e inglés4-15. Las preguntas de interés en relación con el cuadro clínico, el diagnóstico y el tratamiento de la EIIP, que debían ser abordadas en este consenso, se formularon de manera consensuada y siguiendo el formato PICO (Population, Intervention, Comparator, Outcomes).
Posteriormente, se formaron 16 grupos de trabajo. Cada uno de los panelistas se incluyeron en uno de los grupos de trabajo, y les fue asignada una sección de acuerdo con su especialidad. Cada grupo de expertos realizó un análisis crítico de la literatura con especial énfasis en las 12 guías clínicas de base y la bibliografía que consideraron de utilidad para la sección asignada, así redactaron recomendaciones y puntos prácticos y clasificaron la evidencia y el grado de recomendación para cada pregunta asignada.
El equipo coordinador se reunió virtualmente con cada uno de los grupos de panel de expertos, revisaron cada una de las secciones del consenso y evaluaron cada una de las recomendaciones, los puntos prácticos, la clasificación de la evidencia y el grado de la recomendación. Se compiló el documento final, el cual fue enviado al revisor externo, experto internacional en EIIP, quien revisó cada una de las recomendaciones y puntos prácticos para tener el documento definitivo que sería sometido a votación.
Niveles de evidencia y grados de recomendación
La calidad de la evidencia se realizó en forma descriptiva, fundamentándose en el tipo de diseño de los estudios, según las recomendaciones realizadas por la U.S. Preventive Services Task Force (Tabla 1)16,17. Para contestar cada pregunta se recomendó analizar solo los estudios más relevantes de acuerdo con el diseño y los resultados, idealmente con los niveles de confianza y/o el valor de p. Las respuestas se fundamentaron en la mejor evidencia disponible y fueron resumidas con una recomendación breve y concisa, asignándose el grado de recomendación respectivo de acuerdo con la Tabla 2 16,17.
Tabla 1 Niveles de evidencia16,17
*Se entiende como estudio controlado aquel en el que la intervención es manejada por el investigador.
**Se entiende como estudio observacional a aquel en el que la intervención no es controlada por el investigador.
Tabla 2 Grados de recomendación16,17
| Recomendación | Lenguaje |
|---|---|
| A | El consenso recomienda fuertemente la intervención o el servicio indicado. Esta recomendación se sustenta en evidencia de alta calidad, con beneficio categórico que supera los riesgos. |
| B | El consenso recomienda el uso clínico rutinario de la intervención o el servicio indicado. La recomendación se sustenta en evidencia de calidad moderada, con beneficio que supera los riesgos. |
| C | El consenso no recomienda ni a favor ni en contra de la intervención o el servicio. No se realiza una recomendación categórica dado que la evidencia, de calidad al menos moderada, no muestra una relación riesgo/beneficio satisfactoria. Se debe decidir caso a caso. |
| D | El consenso recomienda en contra de la intervención o el servicio. La recomendación se sustenta en evidencia de calidad al menos moderada que no muestra beneficio o que el riesgo o daño supera los beneficios de la intervención. |
| I | El consenso concluye que la evidencia es insuficiente, ya sea por estudios de baja calidad, resultados heterogéneos o el balance riesgo/beneficio no puede ser determinado. |
Segunda etapa
Se realizó una primera ronda de votación en la que, de acuerdo con la técnica Delphi de consenso18,19, los coordinadores, junto con los responsables de cada pregunta, una vez recibida la información y generado un documento centralizado y emitida la recomendación, sometieron a votación electrónica en modalidad mixta (presencial y virtual) a todo el grupo desarrollador para dar el grado de acuerdo en porcentaje (%). Todas las recomendaciones fueron votadas y aceptadas, en todas las recomendaciones más del 80% de acuerdo fue logrado en la primera ronda de votación, por lo que no se requirió realizar una segunda ronda (a pesar de que se había diseñado así). Dos epidemiólogos revisaron cada una de las recomendaciones y, con base en la evidencia revisada, se otorgó el nivel de evidencia y grado de recomendación correspondiente (Tablas 1 y 2).
Revisión consenso
Se sugiere que cada dos años se realice una revisión de bibliografía que pueda modificar las recomendaciones formuladas en este consenso, al igual que revisar cualquier nueva tecnología, fármaco o legislación que modifique las recomendaciones. En este sentido, sugerimos que este consenso se actualice completamente al cabo de cinco años.
Generalidades de la enfermedad inflamatoria intestinal pediátrica (EIIP)4-6,20,21
Pregunta 1. ¿Cuáles son las diferencias clínicas de la EIIP con la del adulto?
Afirmación 1la EIIP tiene mayor compromiso en extensión (pancolitis), severidad y evolución hacia la estenosis y la penetración, enfermedad perianal y manifestaciones extraintestinales y retraso en el crecimiento, especialmente en las formas tempranas, que en adultos, por lo que su manejo debe ser realizado por grupos multidisciplinarios liderados por gastroenterólogos pediatras.
Nivel de evidencia: II-2.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
La EIIP tiene una mayor extensión, actividad severa (con mayor riesgo de recaídas graves corticorrefractarias en 30%-40% de los casos), con una evolución más rápida de la ECP hacia la estenosis y el grado de penetración20,21.
Un análisis multivariado demostró en la presentación de EIIP una mayor frecuencia en la enfermedad perianal (12,8%) (p <0,0001) y manifestaciones extraintestinales (14,3%) (p = 0,043) que en la edad adulta, y durante el seguimiento, la presencia de manifestaciones extraintestinales (50,4%) (p = 0,005) y enfermedad perianal (44,8%) (p = 0,006) progresaron más rápidamente20.
En la colitis ulcerativa se encontró que la pancolitis fue más frecuente en la población pediátrica (73,1% vs. 30,2%; p <0,00001), y que los agentes 5-ASA (96,9% vs. 79,9%; p = 0,0034) y el uso de anti-TNF (factor de necrosis tumoral) (25% vs. 9,2%; p =0,054) fueron usados con mayor frecuencia en el subgrupo de ECP en comparación con el subgrupo de adultos21.
Pregunta 2. ¿Debemos usar los criterios de Porto de EIIP de ESPGHAN para clasificar los fenotipos de EIIP en Colombia?
Afirmación 2: se recomienda usar los criterios de Porto de EIIP de ESPGHAN para clasificar los fenotipos de EIIP. Los criterios de Porto revisados nos permiten clasificar de una manera práctica la CUP típica y los cinco fenotipos de la CUP atípica, ECP e EIIPNC y también descartar la EIIP. Por medio de un algoritmo práctico basado en las recomendaciones y con base en los puntos de práctica, se pueden escoger los exámenes diagnósticos que nos permitan clasificar correctamente los síntomas intestinales o extraintestinales sugestivos de EIIP, que constituyen un desafío para el clínico.
Nivel de evidencia: II-2.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
Recientemente, un estudio retrospectivo multicéntrico de 23 centros de ESPGHAN, que incluyó 749 niños con EII: 236 (32%) con colitis de Crohn, 272 (36%) con CU y 241 (32%) con EIIPNC, encontró que, con base en los criterios de Porto revisados, diferenciaba CUP de ECP y EIIPNC con 80% de sensibilidad y especificidad del 84%, y EC de EIIPNC y CU con 78% de sensibilidad y 94% de especificidad; se concluyó que el algoritmo puede clasificar adecuadamente a los niños con EII en EC de intestino delgado, EC de colon, EIIPNC, CU atípica y CU5.
Enfermedad de crohn pediátrica (ECP)
Pregunta 3. ¿Cuáles son las manifestaciones clínicas y extraintestinales para sospechar ECP?
Afirmación 3: la ECP abarca desde la boca hasta el ano. Es más frecuente la forma ileocolónica y puede comprometer solo el colon (colitis de Crohn). El 50% tiene compromiso superior (estómago, duodeno). El compromiso es transmural, por lo que se pueden desarrollar fístulas y/o estenosis. Es característica la enfermedad perianal y se asocia con una mayor frecuencia a manifestaciones extraintestinales.
Nivel de evidencia: II.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
La presentación típica inicial es dolor abdominal crónico con retraso en el crecimiento21.
En la ECP, los síntomas digestivos dependen de la zona comprometida. Los síntomas más frecuentes son dolor abdominal y diarrea crónica. Si hay compromiso colónico, la diarrea puede ser disentérica. Puede haber disfagia o dolor retroesternal si hay afectación esofágica, y náuseas, vómito o dolor epigástrico si hay afectación gástrica4.
En el momento del diagnóstico, hay una mayor localización en el tracto digestivo superior e ileocolónica vs. adultos (41% vs. 15%; p = 0,001 y 74% vs. 26%; p < 0,001, respectivamente)20.
Las diferencias clínicas en comparación con los adultos son: retardo en crecimiento lineal y retardo puberal. En el primer caso, en un 25% este retardo puede preceder a la aparición de los otros síntomas y el diagnóstico4. En la ECP hay un mayor patrón inflamatorio que en los adultos, donde es más el fenotipo estenosante y penetrante20.
La desnutrición crónica se asocia con el retardo de crecimiento y su origen es multifactorial (anorexia, inflamación, miedo al comer por empeoramiento de los síntomas, malabsorción intestinal, etc.) e incluso se puede presentar mucho antes del inicio de los síntomas digestivos4.
Las manifestaciones extraintestinales (20% vs. 13%, p = 0,05) y la enfermedad perianal (17% vs. 8%, p < 0,0001) se presentan más frecuentemente en los niños que en los adultos20; y en la edad pediátrica, estas manifestaciones son más frecuentes en la población escolar vs. los adolescentes (58% vs. 32%; p = 0,002)20.
Los síntomas extraintestinales son menos frecuentes frente a los adultos (13,5% vs. 36%; p = 0,0006)21 y se pueden presentar en diferentes regiones o sistemas: osteoarticulares (artralgias, artritis, sacroileitis), mucosa oral (aftas orales), piel (eritema nodoso, pioderma gangrenoso), oculares (epiescleritis, uveítis) genitourinaria (amenorrea y enfermedad metastásica vulvar), vasculares (vasculitis, trombosis), etc. (Tabla 3).
Tabla 3 Manifestaciones extraintestinales en EIIP (n=1649)
| Manifestaciones extraintestinales | CU | EC |
|---|---|---|
| Manifestaciones musculoesqueléticas | ||
| - Osteoporosis/osteopenia (%) | 25 | 41 |
| - Falla en el crecimiento (%) | 6-10 | 40 |
| - Artritis periférica (%) | 2-50 | 4-49 |
| - Artralgia (%) | 15 | 17 |
| - Espondilitis anquilosante | Rara | 0,5 |
| Manifestaciones mucocutáneas | ||
| - Estomatitis aftosa (%) | 3-42 | 10-46 |
| - Eritema nodoso (%) | 1-13 | 4-56 |
| - Pioderma gangrenoso (%) | 8 | 0,4-3 |
| Manifestaciones oculares (%) | 0,4 | 0,8-13 |
| Colangitis esclerosante primaria (%) | 2 | 1 |
| Pancreatitis (%) | 1-5 | 0,7-5 |
| Anemia (%) | 5 | 70 |
Adaptado de: Yu YR, et al. Semin Pediatr Surg. 2017;26(6):349-5522.
Pregunta 4. ¿Debemos usar la clasificación de París de la ECP?
Afirmación 4: se recomienda usar la clasificación de París de la ECP. Debemos usar la clasificación de París, que es un documento de consenso de expertos que proporciona una modificación específica de la clasificación de Montreal de la EII para la edad pediátrica, la cual resalta características fenotípicas que son más comunes o exclusivas de la EIIP a diferencia del adulto.
Nivel de evidencia: III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
La clasificación de Montreal solo permitía incluir tres categorías de edad, y es el punto de corte para pediatría 16 años con base en la necesidad de incluir a la población pediátrica, sin considerar aspectos tales como la ubicación o la extensión de la enfermedad, ni la edad13,23.
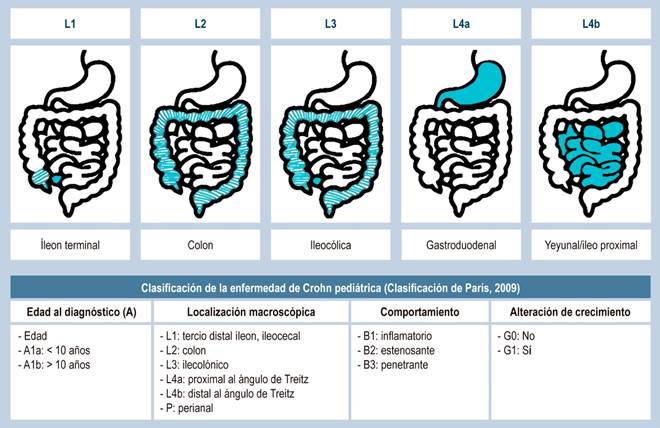
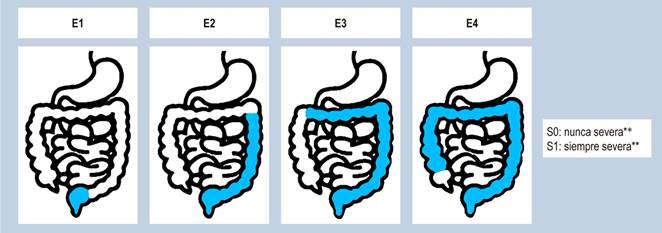
Las modificaciones importantes de la clasificación de Paris incluyen: edad al diagnóstico, como A1a (0 a < 10 años), A1b (10 a < 17 años), distinguiendo la enfermedad como L4a (proximal al ligamento de Treitz) y L4b (distal al ligamento de Treitz), lo que permite clasificar tanto la enfermedad inflamatoria, estenosante y penetrante en el mismo paciente (B1, B2, B3), teniendo en cuenta la falla de crecimiento (G1)13,23.
La localización de la enfermedad es importante, ya que, en el compromiso del intestino delgado, el pronóstico es más sombrío asociado con falla para crecer, pérdida de peso y enfermedad estenosante. Es por ello que en la clasificación de París se modificó la clasificación L1 y se confinó el compromiso al último tercio del íleon distal con enfermedad limitada al ciego, y L4 subdividiendo el compromiso del tracto digestivo superior proximal al ligamento de Treitz y distal al mismo13,23 (Figura 1).
Pregunta 5. ¿Cuál es la utilidad de la endoscopia en el diagnóstico de EC en niños con sospecha de EII?
Afirmación 5:
Se recomienda la realización de una ileocolonoscopia más una esofagogastroduodenoscopia para el diagnóstico de todos los pacientes pediátricos con sospecha inicial de EII. (Nivel de evidencia II-2) (Figura 2).
Los estudios endoscópicos deben ser utilizados en el seguimiento para garantizar la curación mucosa en pacientes asintomáticos con enfermedad de Crohn colónica cuando la calprotectina esté elevada, en pacientes con enfermedad de Crohn de intestino delgado y cuando se vayan a realizar escalamientos terapéuticos. (Nivel de evidencia III).
Después de la resección ileocecal, los pacientes deben ser monitorizados con endoscopia entre los 6-12 meses posoperatorios, aunque estén asintomáticos. (Nivel de evidencia I).
La dilatación endoscópica con balón puede ser utilizada como tratamiento transitorio en estenosis únicas alcanzables, menores de 4 cm de longitud, idealmente de las anastomosis; sin embargo, es una medida transitoria que puede requerir reintervención o cirugía con mayor frecuencia que la resección quirúrgica. (Nivel de evidencia I).
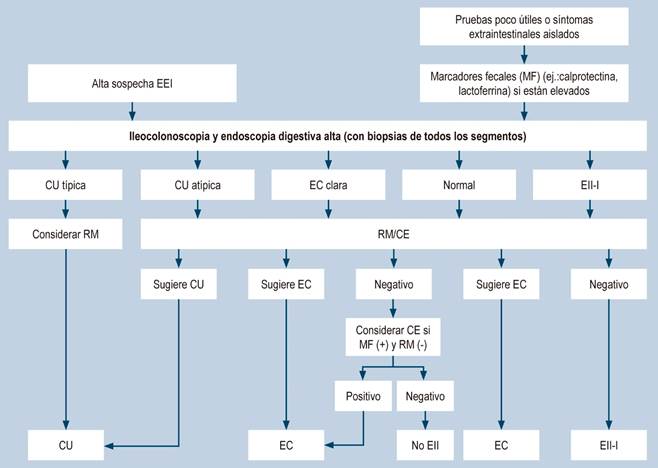
Figura 2 Evaluación de niños y adolescentes con síntomas intestinales o extraintestinales sugestivos de EII. CU: colitis ulcerativa; CEI: cápsula endoscópica inalámbrica; EC: enfermedad de Crohn; EII: enfermedad inflamatoria intestinal; EII-I: EII indeterminada o no clasificada; ERM: enterografía por resonancia magnética. Adaptada de: Levine A, et al. J Pediatr Gastroenterol Nutr. 2014;58(6):795-8066.
Puntos prácticos
El diagnóstico de enfermedad inflamatoria incluye la realización de endoscopia alta e ileocolonoscopia, excepto en situaciones de urgencia. Debe ser llevado a estudio endoscópico para estudiar enfermedad inflamatoria en todo paciente con signos de alarma (diarrea con sangre, pérdida de peso, fallo de medro, dolor abdominal, etc); en aquel sin signos de alarma, pero con elevación de reactantes de fase aguda (velocidad de sedimentación globular [VSG], proteína C-reactiva [PCR]) o pacientes con calprotectina elevada24,25.
En el registro EUROKIDS de enfermedad inflamatoria pediátrica entre 428 niños, el diagnóstico de enfermedad de Crohn se realizó por los hallazgos en la endoscopia alta en el 7,5% de los pacientes26.
La inflamación ileal aislada puede ocurrir en presencia de un colon normal hasta el 6%-17% de los niños con ECP, por lo que siempre se debe intentar la intubación ileal27.
Se recomienda tomar dos biopsias del duodeno, el estómago y el esófago durante la endoscopia alta y de íleon terminal, ciego, colon transverso, sigmoide y recto durante la ileocolonoscopia24.
Se recomienda la evaluación de la mucosa intestinal en las siguientes circunstancias:
antes de cambios mayores en el tratamiento;
en pacientes sintomáticos en quien no es claro si tienen inflamación activa o se sospecha un trastorno funcional;
para comprobar la curación mucosa24.
Debe realizarse una endoscopia cuando se sospecha pouchitis.
En estenosis únicas, mayores de 4 cm o múltiples, no se recomienda el uso de dilatación con balón por el mayor riesgo de complicaciones y menor tasa de éxito28.
Antes de realizar la dilatación endoscópica se recomienda caracterizar el número de estenosis, la naturaleza de las mismas (inflamatorias o fibróticas) y la longitud utilizando enteroresonancia28.
Si hay presencia de fístulas o abscesos cerca del sitio de estenosis, se recomienda no realizar dilatación por el riesgo de perforación28.
La cápsula endoscópica es complementaria a la enterografía por resonancia magnética para evaluar la inflamación, las erosiones, las úlceras, el sitio de sangrado, etc., en el intestino medio. Sin embargo, dado el riesgo de retención de la cápsula en zonas estenóticas inflamatorias o por fibrosis, se recomienda realizarla después de la enterorresonancia (ERM).
Nivel de evidencia: I-III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Pregunta 6. ¿Qué índice endoscópico se debería usar en la ECP?
Afirmación 6: se recomienda que el informe endoscópico siempre incluya el puntaje de actividad endoscópica, el cual permite disminuir la variabilidad interobservador y hacer un seguimiento objetivo del paciente. En la ECP sugerimos usar el Simple Endoscopic Score for CD (SES-CD) (Nivel de evidencia I) (Tabla 4), para lo cual se pueden utilizar herramientas digitales como el IG-IBD SCORES CALCULATORS IN GASTROENTEROLOGY: https://www.igibdscores.it/en/score-sescd.html.
Nivel de evidencia: I.
Nivel de recomendación: A.
Grado de acuerdo: 96,6%.
Puntos prácticos
Todas las endoscopias diagnósticas y de seguimiento en pacientes con sospecha o diagnóstico de ECP deberán incluir en su reporte un índice de actividad, el cual debe ser siempre el mismo para poder realizar comparaciones y evaluar resultados terapéuticos de la siguiente forma:
la curación mucosa significa la ausencia de inflamación con SES-CD = 0;
la remisión endoscópica es considerada con SES-CD ≤ 2;
la respuesta endoscópica está definida como una disminución del SES-CD ≥ 2 o la disminución del 50% del SES-CD de su línea de base29.
Tabla 4 SES-CD (https://www.igibdscores.it/en/score-sescd.html)
| Variable | 0 | 1 | 2 | 3 |
|---|---|---|---|---|
| Tamaño de la úlcera (cm) | Ninguno | Úlcera aftoide (0,1-0,5 cm) | Úlceras grandes (0,5-2 cm) | Úlceras muy grandes (diámetro > 2 cm) |
| Superficie ulcerada (%) | Ninguna | < 10 | 10-30 | > 30 |
| Superficie afectada (%) | Sin afectación | < 50 | 50-75 | > 75 |
| Presencia de estenosis | No | Única, puede ser pasada | Múltiples, pueden ser pasadas | No pueden ser pasadas |
El valor total del SES-CD: se suma el valor de las cuatro variables en los cinco segmentos examinados (íleon, colon derecho, colon transverso, colon izquierdo y sigma, y recto). Los valores deben ser dados por cada variable y cada segmento examinado. Adaptada de: Walsh A, et al. Gastrointest Endosc Clin N Am. 2014;24(3):367-7830.
Pregunta 7. ¿Cuál es la utilidad de las biopsias para confirmar el diagnóstico de EII
Afirmación 7: se recomienda la realización de una ileocolonoscopia con múltiples biopsias para el diagnóstico inicial de los pacientes pediátricos con sospecha de EII.
Nivel de evidencia: II-III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
Se considera indispensable el estudio histopatológico para el diagnóstico inicial de la EII31,32.
El examen histológico de las biopsias endoscópicas o de las muestras de resección sigue siendo un paso clave en la EII y puede utilizarse para el diagnóstico y el diagnóstico diferencial, en particular para diferenciar la CU de la EC y otras colitis no relacionadas con la EII33.
La afectación del tracto gastrointestinal superior de la EIIP se observa más frecuentemente en pacientes pediátricos34.
Adicionalmente, se debe incluir rutinariamente la endoscopia digestiva superior de los niños con sospecha de EII para mejorar el diagnóstico y el tratamiento31,34.
Para el estudio histopatológico se deben realizar múltiples biopsias escalonadas de todas las secciones del tracto gastrointestinal, incluidas las zonas que son endoscópicamente normales para la evaluación histopatológica. Este estudio es esencial para diferenciar la ECP de la CUP e identificar la localización y la extensión de la enfermedad35-37.
Deben obtenerse múltiples biopsias (> 2, idealmente 4), fijadas adecuadamente en formol tamponado neutro, representativas de cada segmento evaluado, incluyendo el esófago, el estómago y el duodeno; el íleon, el ciego, el colon ascendente, el colon transverso, el colon descendente, el colon sigmoide y el recto9,33,38.
Las muestras de biopsia deben ir acompañadas de información clínica, incluidos los hallazgos endoscópicos, así como la edad del paciente, la duración de la enfermedad, la duración y el tipo de tratamiento, las comorbilidades y los antecedentes completos33.
La ausencia de síntomas gastrointestinales superiores específicos no excluye la presencia de una inflamación gastrointestinal superior como compromiso de EII especialmente en EC, por lo cual el estudio histopatológico es fundamental y puede ayudar a establecer el diagnóstico final en el 10% de los niños con EII37.
Pregunta 8. ¿Cuáles son los hallazgos morfológicos necesarios para confirmar la EII? ¿Existen diferencias entre la CU y la EC?
Afirmación 8:
Los hallazgos de las biopsias tomadas durante la endoscopia y la colonoscopia, aunque no son totalmente específicas, siguen siendo en conjunto con el cuadro clínico el método definitivo para confirmar la EII12,31.
Es importante establecer la presencia de cronicidad en el estudio histopatológico de las biopsias (Tabla 5)39.
En el estudio histopatológico se debe determinar la actividad, su severidad y la extensión (Tabla 6)39.
En la CU es característico el compromiso distal, especialmente rectal. La inflamación se limita a la mucosa y los hallazgos habituales son la inflamación de la mucosa, el infiltrado predominante de células plasmáticas, criptitis y abscesos crípticos y cambios arquitecturales leves6,32,35,40 (Tabla 7).
En la EC es característico el compromiso inflamatorio del intestino delgado, en especial íleon distal. Los hallazgos histológicos clásicos son la inflamación transmural y la formación de granulomas no caseificantes6,32,35,40 (Tabla 7).
En fases iniciales, los pacientes pediátricos tienen poca o ninguna alteración arquitectural; el tiempo de progresión a la clásica “colitis crónica” histológica puede ser más largo en la población pediátrica que en los adultos41.
Nivel de evidencia: II-III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Tabla 5 Hallazgos morfológicos que indican cronicidad
| Infiltrado inflamatorio de la lámina propia linfoplasmocitario con plasmocitosis basal |
| Acúmulos linfoides o folículos linfoides, más de 2 por mm de mucosa |
| Granulomas epitelioides |
| Distorsión arquitectural |
| Metaplasia sudopilórica o de células de Paneth |
| Depleción de mucina |
| Duplicación de la muscular de la mucosa |
| Hialinizacion de la lámina propia y/o fibrosis de la submucosa |
Adaptada de: Battat R, et al. Aliment Pharmacol Ther. 2020;52(10):1574-8238.
Tabla 6 Hallazgos histológicos que indican actividad
| Infiltrado de neutrófilos en la lámina propia |
| Criptitis aguda |
| Abscesos crípticos |
| Erosión del epitelio superficial |
| Ulceración |
| Úlceras aftosas |
| Seudomembranas |
| Trayectos fistulosos |
| Fisuras |
Adaptada de: Battat R, et al. Aliment Pharmacol Ther. 2020;52(10):1574-8238.
Tabla 7 Cambios morfológicos que ayudan a diferenciar entre CU y EC
| Características macro y microscópicas | CU | EC |
|---|---|---|
| Segmentos comprometidos |
|
Íleon principalmente y cualquier sitio del tracto gastrointestinal |
| Patrón de inflamación crónica | Difuso y superficial, limitado a la mucosa | En parches y transmural |
| Presencia de úlceras | Superficiales | Aftosas Profundas, lineales o serpiginosas |
| Inflamación de neutrófilos | Más frecuente y continua | Es focal y en parches |
| Abscesos crípticos | Son típicos | Menos frecuentes |
| Fístulas y fisuras | No son usuales | Típicas |
| Estrecheces | No son usuales | Típicas |
| Pseudopólipos | Usualmente presentes | Muy ocasionales |
| Atrofia mucosa | Marcada | Mínima |
| Distorsión críptica | A menudo marcada | Presente, pero menos marcada |
| Agregados linfoides | Basales | Transmurales |
| Granulomas | Solo pericrípticos | Típicos |
| Depleción de mucina | Prominente | Menos frecuente |
| Metaplasia pilórica | Inusual | Típica |
| Metaplasia de Paneth | En colon izquierdo | Menos frecuente |
| Hiperplasia neuronal e hipertrofia de la muscular | Inusual | Típica |
| Engrosamiento de la pared/fibrosis | No existe | Usualmente engrosada |
| Serositis | Presente en la colitis fulminante | Usualmente presente |
Adaptada de: Levine A, et al. J Pediatr Gastroenterol Nutr. 2014;58(6):795-8066; Fuller MK, et al. Surg Clin North Am. 2019;99(6):1177-8331; Abuquteish D, et al. World J Gastroenterol. 2019;25(16):1928-3534; Langner C, et al. Virchows Arch. 2014;464(5):511-2739.
Puntos prácticos
El informe patológico en todas las colitis e ileítis crónicas debe dar una indicación de la actividad de la enfermedad.
Se consideran hallazgos clásicos o típicos de CU: colitis crónica activa con inflamación difusa de la mucosa, con linfoplasmocitosis basal especialmente en etapas tempranas de la enfermedad y en niños pequeños, distorsión de la arquitectura de las criptas (incluidas alteraciones en la forma o el tamaño y orientación irregular de las criptas, con ramificación, atrofia o el cambio villiforme de la superficie), metaplasia de células de Paneth en las biopsias del colon izquierdo. Es inusual la afectación extracolónica35,41.
En la EC son hallazgos considerados patognomónicos: el compromiso inflamatorio segmentario, la inflamación discontinua con zonas de mucosa normal y la presencia ileítis crónica activa, las úlceras aftosas caracterizadas por la inflamación adyacente a folículos linfoides, los granulomas no caseificantes (no relacionados con las criptas), la inflamación crónica transmural y la inflamación mucosa con metaplasia pilórica, criptitis y abscesos crípticos en parches. Además, úlceras, fisuras, estrecheces y fístulas35,41.
Una mayor proporción de niños con CU presenta inicialmente una colitis subtotal o una colitis extensa, por lo que la presencia de ileítis backwash no excluye el diagnóstico de CU, al igual que la inflamación periapendicular, sin inflamación cecal observada con frecuencia en la CU en niños; y la preservación rectal es más frecuentemente observada en niños menores de 10 años e indica una mayor severidad de la enfermedad33,42.
En los niños pequeños con una presentación inusual de la enfermedad, la colitis ulcerosa debe considerarse siempre en el diagnóstico diferencial, aunque la histología no sea típica33,41.
En la primera década de la vida, la EC se asocia con más colitis y menos ileítis33.
La frecuencia de los granulomas es mayor en niños que en los adultos. La inflamación focal en el tracto gastrointestinal superior ayuda a diferenciar la EC de la CU33,41.
Cuando los niños se acercan a la edad adulta, las características histológicas son similares a las de los adultos33.
Pregunta 9. ¿Cuál es la utilidad de las imágenes en el diagnóstico de EC en niños con sospecha de EII?
Afirmación 9: se recomienda la realización de imágenes diagnósticas, que incluyen (ERM), ultrasonido intestinal (UIS) realizado por un profesional experto y enterotomografía (ETC), las cuales son muy útiles para el diagnóstico, para determinar la actividad de la enfermedad, el grado de severidad, las complicaciones, la recurrencia y la respuesta al tratamiento de los pacientes con EII. La ERM es el estándar de referencia y la modalidad de elección para evaluar el compromiso de la actividad de la ECP. Es una técnica útil, no invasiva y libre de radiación. En la población pediátrica se debe evitar la exposición a radiación ionizante, pues estos pacientes requerirán múltiples estudios de seguimiento a lo largo de su vida. En el metaanálisis y la revisión sistemática realizada por Choi y colaboradores en el 2016 acerca de la evaluación de la actividad de la enfermedad por ERM, se tuvieron en cuenta 12 estudios con 1515 segmentos de intestino. Se encontró que la sensibilidad y la especificidad de la ERM fue de 92,9% (intervalo de confianza [IC] del 95%, 86%-97%) y de 91% (IC del 95%, 80%-96%), respectivamente.
Nivel de evidencia: I.
Nivel de recomendación: A.
Grado de acuerdo: 93,1%.
Puntos prácticos
Se recomienda una estrecha colaboración entre los clínicos y los radiólogos con el fin de escoger la modalidad diagnóstica más apropiada y evitar la exposición innecesaria del paciente a la radiación ionizante43.
La ERM es el estándar actual para la evaluación del intestino delgado y sus complicaciones en la EC y se ha propuesto como un procedimiento alternativo a la colonoscopia en la evaluación de la EC ileocolónica45.
El protocolo de ERM debe incluir imágenes de contraste, de difusión y de saturación grasa antes y después de la administración del medio de contraste. Se considera opcional la aplicación de imágenes de cine46. La resonancia magnética de pelvis contrastada es la modalidad de elección para valorar la presencia de fístulas y/o abscesos perianales47.
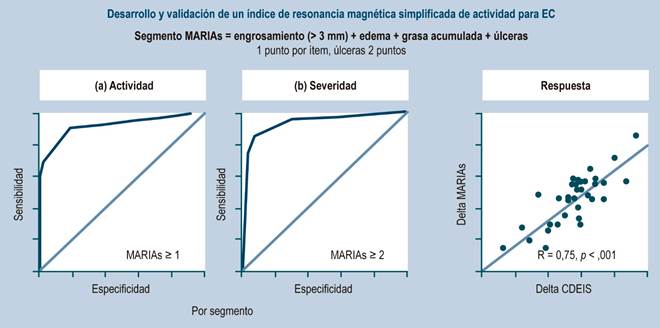
Existen varias escalas para evaluar la actividad de la EII en ERM (Nancy y MaRIA simplificado) (Anexos 1 y 2), las cuales se encuentran en proceso de validación en la edad pediátrica y son utilizadas principalmente en ensayos clínicos y en el futuro pueden ser de utilidad en la práctica clínica48,49.
La ERM tiene una alta sensibilidad (78%-94%) y especificidad (82%-85%) para el diagnóstico de estenosis, fístulas perianales y recurrencia posoperatoria45,50,51.
Se ha propuesto que la resonancia con difusión podría ser una alternativa a la ERM convencional porque es más rápida y podría no requerir administración de contraste endovenoso, preparación del intestino, ni ayuno. Sin embargo, su elección está sujeta al grado de experticia del grupo de radiólogos que interpreta estos estudios y es una opción en quienes no es posible la administración de medios de contraste. Esta no tiene utilidad en la evaluación de fístulas por su baja resolución anatómica44.
Afirmación 10:
Se recomienda el uso de contraste oral intraluminal, como soluciones tipo polietilenglicol (PEG) y manitol en ERM, por lo que mejora la certeza en el diagnóstico de EII. La valoración de la actividad de la enfermedad se realiza con la administración de contraste intravenoso.
Se recomienda el uso de gadolinio intravenoso de composición macrocíclica, pues se ha demostrado que los agentes macrocíclicos producen menos depósitos de contraste cerebrales, en dosis de 0,1 mL/kg intravenoso.
Se recomienda la administración intravenosa lenta de n-butil-bromuro de hioscina en dosis de 0,3 mg/kg en pacientes con peso menor a 50 kg o 20 mg en pacientes con más de 50 kg, en el momento del examen.
Nivel de evidencia: I.
Nivel de recomendación: A.
Grado de acuerdo: 100%.
Puntos prácticos
Manitol: presentación de 250 mL. Llevar con solución salina al 0,9% a 2000 mL.
PEG: presentación de 105 g. Agregar agua o solución azucarada hasta llevar la solución a 1 litro.
º Preparación: aquellos pacientes con peso < 50 kg deben tomar 10 mL/kg de la solución una hora antes del estudio, luego 5 mL/kg 30 minutos antes y posteriormente 5 mL/kg justo antes del examen. Si pesan más de 50 kg deben tomar 500 mL de la solución una hora antes del estudio, luego 500 mL 30 minutos antes y finalmente 300-500 mL justo antes del examen, si lo tolera52.
Afirmación 11: la evaluación inicial con ERM del paciente pediátrico, con sospecha de EII, debe tener en cuenta la edad. En menores de 7 años se recomienda un protocolo completo (ayuno de 6 horas y preparación), idealmente bajo anestesia o sedación, especialmente en pacientes con déficit cognitivo, con dificultad para colaborar o con claustrofobia. En mayores de 7 años se recomienda la ingesta de contraste oral y considerar el uso de anestesia o sedación en pacientes que lo requieran.
Nivel de evidencia: III.
Nivel de recomendación: A.
Grado de acuerdo: 96,6%.
Puntos prácticos
Aquellos que no pueden tolerar definitivamente la ERM deben ser propuestos para otras técnicas alternativas como ETC o UIS54.
Ultrasonido intestinal (UIS)
Afirmación 12: se recomienda el uso del UIS como una alternativa válida a la ERM, ya que es económico, bien tolerado, no invasivo, ampliamente disponible, no necesita preparación ni medio de contraste y, realizado por un profesional entrenado, permite visualizar el intestino en tiempo real.
Nivel de evidencia: I.
Nivel de recomendación: A.
Grado de acuerdo: 89,7%.
Puntos prácticos
Su precisión diagnóstica es baja para las patologías proximales al íleon distal y es un examen altamente operador dependiente55.
10 estudios incluyeron un total de 925 pacientes con diagnóstico de EC. Solo un estudio se realizó en población pediátrica. Se consideró adicionalmente una revisión sistemática. La sensibilidad del ultrasonido para identificar anatómicamente la lesión fue de 55,6% para lesiones yeyunales, 92,7% para lesiones ileales y 81,8% para lesiones colónicas56. La experiencia está limitada a centros en Europa y Norteamérica47.
La sensibilidad y la especificidad del ultrasonido es comparable a la de la ERM en algunos centros de Europa con mucha experiencia. Un metaanálisis de 68 estudios mostró para el ultrasonido una sensibilidad global por pacientes del 85% y una especificidad del 98%, en comparación con 78% y 85% para la ERM8,11,44.
El ultrasonido debe evaluar los siguientes parámetros: grosor de la pared, patrón de la pared (normal, multicapa, disrupción focal, pérdida), presencia o ausencia de fístulas y abscesos, y el flujo de la pared mediante evaluación Doppler. La escala semicuantitativa más usada con este fin es el Limberg score (Anexo 3)44.
El ultrasonido en modo Doppler aumenta la sensibilidad y la especificidad del ultrasonido convencional y tiene buena precisión diagnóstica para determinar la actividad de la EII a través de marcadores como el aumento del flujo sanguíneo en el segmento de intestino y en el mesenterio adyacente56, disponible en Colombia.
Afirmación 13: el UIS con preparación oral tiene una precisión del 86% para predecir la curación de la mucosa intestinal, lo que implica que puede ser utilizado para monitorizar el seguimiento al tratamiento y la extensión quirúrgica por profesional entrenado. El uso de medios de contraste intraluminales orales, tales como soluciones isoosmolares tipo PEG o manitol, aumenta la precisión diagnóstica para la EII, al permitir la distensión de las asas intestinales.
Nivel de evidencia: I.
Nivel de recomendación: A.
Grado de acuerdo: 93,1%.
Puntos prácticos
La precisión para evaluar lesiones en el intestino delgado proximal y para evaluar la extensión en la pared del íleon puede aumentarse con el uso del ultrasonido con medio de contraste oral. El uso de preparación oral no altera en gran medida el procedimiento, se adicionan de 375 a 800 mL de contraste oral; sin embargo, el tiempo aumentó a 25-60 minutos en total. Cuatro estudios, incluyendo un total de 217 pacientes, arrojaron una sensibilidad de 97,1% (IC del 95%, 95,2%-99%) y una especificidad del 100%56.
El ultrasonido intestinal con preparación oral es muy sensible y específico en la detección de recurrencia posoperatoria y tiene buena correlación con la ileocolonoscopia56.
El uso de medio de contraste oral aumenta la precisión para identificar lesiones pequeñas del intestino delgado y su correlación con la extensión radiológica y quirúrgica, la precisión de la identificación de complicaciones estructurales y penetrantes, así como la recurrencia posoperatoria58.
A la fecha no se dispone de contraste intravenoso para el ultrasonido en nuestro país.
El engrosamiento de la pared intestinal es la variable que mejor predice la curación de la mucosa59.
Enterotomografía (ETC)
Afirmación 14: la ETC se considera la primera línea en casos de sospecha de complicaciones agudas/severas de la EII: dolor abdominal severo, fiebre, leucocitosis y desviación a la izquierda. La preparación del paciente es similar a la ERM y su tiempo de disponibilidad y rapidez de adquisición es mucho más rápido.
Nivel de evidencia: II-2.
Nivel de recomendación: B.
Grado de acuerdo: 89,7%.
Puntos prácticos
La ETC permite muchas veces realizar el diagnóstico inicial en pacientes con un cuadro clínico ambiguo o sospechoso de EII. Se recomiendan seguimientos posteriores con ERM o UIS para disminuir la exposición a la radiación ionizante60.
La ETC suele ser útil para evaluar la EII debido a su mayor disponibilidad y rapidez de adquisición (tiempo de ERM 45 minutos vs. 2 minutos o menos de tiempo de ETC), mejor resolución espacial, menos artificios de movimiento, menor costo y mayor disponibilidad47.
La exposición a la radiación de la ETC hace que esta no sea apropiada para el seguimiento de la EII, en donde es necesario realizar exámenes repetidos43,61.
Se recomienda realizar la ETC con protocolo de bajas dosis (control automático de exposición y reconstrucción iterativa) de 2 a 5 mSv de acuerdo con el tamaño del niño60.
Limitar la cobertura de escaneo, reducir el potencial, usar corriente de tubo modulada/control automático de exposición y utilizar la reconstrucción iterativa y los algoritmos de eliminación de ruido son componentes vitales en optimizar la calidad de la imagen de la ETC con la menor exposición posible a la radiación, aplicando el principio “ALARA” (tan bajo como sea razonablemente posible)60.
El contraste oral de densidad neutra distiende el intestino delgado y permite una mejor visualización y evaluación del realce de la pared del intestino delgado47.
La sedación puede ser necesaria en pacientes menores si no pueden permanecer quietos durante la exploración47.
La preparación del examen es similar a la usada en ERM60.
En el futuro se propone el uso de tomografía por emisión de positrones/tomografía computarizada (PET/CT) y tomografía por emisión de positrones/resonancia magnética (PET/RM) dado su buena sensibilidad y especificidad. Este método permite localizar áreas de inflamación y alteraciones estructurales de la EII. Un metaanálisis en pacientes con EII reportó una sensibilidad y una especificidad por segmentos de 85% y 87%, respectivamente, con una área bajo la curva (AUC) de 0,93344,62. La PET/MR se ha utilizado para detectar fibrosis en la EC44,62. Dentro de las desventajas de este método están el costo, la exposición del paciente a radiación ionizante de la PET/CT y la falta de disponibilidad de la PET/RM en el país44,62.
Afirmación 15: se recomienda la ERM como el examen de elección para evaluar pacientes con EII; la ETC es útil para establecer la progresión o la regresión de la EII solo cuando no se disponga de ERM.
Nivel de evidencia: II-2.
Nivel de recomendación: B.
Grado de acuerdo: 89,7%.
Puntos prácticos
Se encontró buena correlación entre la ETC y los hallazgos histológicos y endoscópicos63.
La ERM y la ETC son herramientas útiles para monitorizar la respuesta a la terapia biológica, y los estudios muestran una correlación con la respuesta clínica y endoscópica47.
La ETC tiene una sensibilidad del 86%-100% y una especificidad del 62%-100%. Un estudio reciente comparó la precisión de la ETC y la ERM en pacientes pediátricos con EII y concluyó que no existe una diferencia estadísticamente significativa en la precisión diagnóstica en la detección de la actividad de la enfermedad entre los dos métodos de imagen47.
Tránsito intestinal
Afirmación 16: los estudios de fluoroscopia tales como vías digestivas altas y colon por enema no se recomiendan como herramienta diagnóstica primaria. Puede ser un examen alternativo en casos en los que no se pueda realizar ERM, ETC ni UIS para el seguimiento o para valorar las complicaciones de la EII.
Nivel de evidencia: III.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Pregunta 10. ¿Cuál es la exactitud del PCDAI para determinar la inflamación y/o la actividad en la ECP en el diagnóstico y el seguimiento?
Afirmación 17: los índices clínicos de actividad de la ECP (Pediatric Crohn’s Disease Activity Index [PCDAI], weighted Paediatric Crohn’s disease activity index [wPCDAI], short Pediatric Crohn’s Disease Activity Index [shPCDAI], abbreviated Pediatric Crohn’s Disease Activity Index [abbrPCDAI]) deben ser una herramienta, que, en conjunto con la calprotectina y la PCR, pueden ofrecer una mejor precisión diagnóstica para la evaluación de la curación mucosa. Sin embargo, los índices o puntajes de la actividad de la enfermedad clínica por sí solos no son precisos, ya que casi la mitad de los pacientes en remisión clínica pueden tener lesiones mucosas. Se recomienda el uso del índice no invasivo de inflamación de la mucosa validado en ECP como el miniIndex.
Puntos prácticos
Valores mayores o iguales a 30 proporcionan una definición aceptable para la actividad de la enfermedad en rango moderado.
Valores menores o iguales a 10 de PCDAI indican remisión; sin embargo, ante puntajes más bajos la especificidad es mayor, pero la sensibilidad es menor para la detección de la enfermedad inactiva vs. leve.
Puntaje del miniIndex < 8 tiene una buena sensibilidad y especificidad para la curación mucosa.
La disminución del PCDAI de 12,5 puntos o más refleja una mejora significativa en la condición del paciente. Mayores disminuciones en PCDAI tienen una mayor especificidad con una pequeña caída en la sensibilidad64-69.
Nivel de evidencia: II.
Nivel de recomendación: B.
Grado de acuerdo: 96,6%.
Pregunta 11. ¿Cuál es la utilidad diagnóstica de los laboratorios iniciales en los pacientes con sospecha de EIIP?
Afirmación 18: se recomienda que, en niños con sospecha de EIIP, los laboratorios iniciales incluyan: cuadro hemático, albúmina, perfil hepático y marcadores de inflamación como VSG, PCR y calprotectina fecal (CF). (Nivel de evidencia II).
Nivel de evidencia: I-II.
Nivel de recomendación: A.
Grado de acuerdo: 96,6%.
Puntos prácticos
No existe una prueba de laboratorio específica de EII; por tanto, resultados de laboratorio normales no excluyen el diagnóstico de ECP o CUP. Laboratorios normales se encontraron en el 21% de casos de EC leve y 54% de CU leve. En contraste, solo un 3,8% de los casos de EC moderado a severo y 4,3% de CU moderada a severa tenían laboratorios normales. (Nivel de evidencia II-2)70.
La sensibilidad y la especificidad de anemia y aumento de la VSG como predictoras de EII fue de 83% y 94%, respectivamente. (Nivel de evidencia II-3)71.
En niños con sospecha de EC y CU con compromiso nutricional, la presencia de anemia y trombocitosis tuvo una sensibilidad de 90,8% y una especificidad de 80% para diagnosticar CU y EC. (Nivel de evidencia II-3)35.
Una albúmina sérica baja puede estar en relación con una enteropatía perdedora de proteínas y usualmente estar asociada con actividad y severidad de la EII y no solo el reflejo del estado nutricional. (Nivel de evidencia II-2)6.
Un metaanálisis, que incluyó 19 estudios con total de 2806 pacientes, concluyó que la albúmina, la PCR y la CF tenían un potencial valor clínico para seleccionar los niños en bajo riesgo de EII (resultados negativos) o alto riesgo para EII (PCR y CF positivas y albúmina baja). (Nivel de evidencia I)72.
Se deben realizar pruebas de función hepática y considerar otras pruebas adicionales en la búsqueda de enfermedades extraintestinales asociadas a EC. (Nivel de evidencia II-2)6.
Afirmación 19: en niños con sospecha de EII se recomienda excluir las infecciones gastrointestinales como causa de sus síntomas, antes de realizar estudios endoscópicos. La investigación microbiológica debe descartar infecciones bacterianas, incluyendo Clostridiodes difficile. (Nivel de evidencia II-2).
Nivel de evidencia: II.
Nivel de recomendación: A.
Grado de acuerdo: 96,6%.
Puntos prácticos
Se debe realizar coprocultivo y/o panel gastrointestinal (FilmArray™) para descartar infección por Salmonella, Shiguella, Yersinia, Campylobacter y Clostridiodes difficile en todos los niños con sospecha de EII. (Nivel de evidencia II-2)6.
Se debe realizar una investigación más extensa para parásitos, incluyendo Giardia lamblia y agentes infecciosos inusuales en áreas endémicas como Colombia o en poblaciones de alto riesgo. (Nivel de evidencia II-2)6.
El hallazgo de un patógeno no necesariamente excluye el diagnóstico de EII considerando que una infección intercurrente puede ser el disparador de un primer episodio o recaída de la enfermedad. (Nivel de evidencia II-2)6.
Pregunta 12. ¿Cuál es la utilidad diagnóstica de los marcadores serológicos en la EIIP?
Afirmación 20: en niños con EII, los marcadores serológicos P-ANCA (anticuerpos anticitoplasma perinuclear neutrófilo) y ASCA (anticuerpos anti-Saccharomyces cerevisae) no se recomiendan de rutina considerando que a menudo el resultado es negativo; sin embargo, pueden ser de utilidad en casos atípicos si su resultado es positivo, lo que ayuda a diferenciar la ECP de la CUP en los casos de EII no clasificada. (Nivel de evidencia II-2). Por otro lado, no se ha determinado la utilidad en pediatría de otros marcadores como anti-OmpC (anticuerpos contra porina de membrana externa de la E. coli), anti-I2 (anticuerpos contra la secuencia asociada a Pseudomonas fluorescens), anti-OmpW (anticuerpos contra porina de membrana externa de Bacteroides caccae), anti-CBirl (anticuerpos anti-flagelina). Estos pueden ser positivos en niños con EII con serología negativa, pero son inespecíficos y pueden detectarse en niños con otras patologías. (Nivel de evidencia II-3).
Nivel de evidencia: II.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Puntos prácticos
Una revisión sistemática, que incluyó población adulta y pediátrica, concluyó que los anticuerpos séricos individuales o en combinación tienen una utilidad limitada en el proceso diagnóstico de los pacientes con EII dada su moderada sensibilidad y valor predictivo negativo; sin embargo, su alta especificidad y valor predictivo positivo (VPP) pueden hacerlos útiles en casos seleccionados. La combinación ASCA+/P-ANCA- es la combinación más precisa para diferenciar EC y Crohn colónico (CC) de CU. (especificidad de 91% a 94% y VPP de 77%-95%); sin embargo, la sensibilidad es baja en CC (30%-38%). La combinación PANCA+/ASCA- predice la CU en 64% de los casos. (Nivel de evidencia I)73.
En niños, la presencia de ASCA+/P-ANCA- no necesariamente precluye el diagnóstico de CU, pero sí reduce esta posibilidad. ASCA es más frecuentemente encontrado en EC (50%-70%) que en CU (10%-15%) o en sanos (< 5%). P-ANCA es más frecuente en CU (60%-70%) que en EC (20%-25%). (Nivel de evidencia II-2)6.
En una cohorte prospectiva de niños con EII no clasificada, Joossens y colaboradores encontraron que de 26 pacientes con ASCA+/P-ANCA- al inicio, ocho pacientes fueron posteriormente diagnosticados con EC y dos con CU. (Nivel de evidencia II-2)74.
Un gran estudio longitudinal multicéntrico, publicado por el grupo de Porto de la ESPGHAN, concluyó que los marcadores serológicos no eran de utilidad para diferenciar EC de CU en EII no clasificada de expresión colónica y sugieren no realizarlos de rutina con este propósito. (Nivel de evidencia II-2)75.
La presencia de ASCA en el momento del diagnóstico de EC pediátrica se relaciona con la presencia de complicaciones tempranas y mayor necesidad de cirugía. (Nivel de evidencia II-2)76.
Aunque se considera que la adición al panel de anticuerpos de otros marcadores serológicos para EII, como anti-OmpC, anti-I2 y anti-CBirl, puede mejorar la sensibilidad diagnóstica, en un trabajo retrospectivo en 394 niños se encontró un bajo valor predictivo en la búsqueda de EII comparado con las pruebas usuales. (Nivel de evidencia II-3)35.
Pregunta 13. ¿Cuál es la utilidad diagnóstica de las diferentes pruebas de laboratorio para establecer un diagnóstico diferencial, confirmarlo y establecer el seguimiento o el pronóstico de la EIIP?
Analizamos los siguientes escenarios de las pruebas de laboratorio: a) en el diagnóstico inicial; b) como control del tratamiento, y c) como agente predictor de recaída.
Pregunta 14. ¿Qué tan eficaz es la CF como ayuda diagnóstica inicial en la EIIP?
Afirmación 21: la CF como marcador de inflamación se considera altamente sensible en la detección de inflamación mucosa sin ser específica de EII. Dentro de los marcadores fecales existentes, se recomienda la CF por ser la más sensible para el diagnóstico de la EII de nueva aparición comparado con marcadores inflamatorios séricos como PCR y VSG. No existe un valor de corte ideal de CF para reflejar el grado de inflamación mucosa. Los valores difieren sustancialmente en los diferentes estudios utilizando diferentes cortes.
Nivel de evidencia: III.
Nivel de recomendación: B.
Grado de acuerdo: 96,6%.
Puntos prácticos
La CF es una proteína inflamatoria de 36 kilodalton que se encuentra en el citosol de los neutrófilos, macrófagos y monocitos77.
La presencia de CF es directamente proporcional al flujo de neutrófilos en el tracto gastrointestinal durante los procesos de inflamación. Es un marcador estable, resistente a la degradación y estable a temperaturas habituales hasta por siete días, aunque los productores de la prueba tipo ELISA recomiendan tomar la primera muestra de la mañana y refrigerar, especialmente si la muestra va a ser procesada después de cuatro días78.
Su principal utilización hoy en día es como marcador de actividad inflamatoria en CU y en EC6.
Los niveles elevados de CF no pueden distinguir entre las diferentes causas de inflamación intestinal (p. ej., EII frente a infección), el tipo de EII (EC frente a CU) o la ubicación de la enfermedad (intestino delgado vs. grueso). Los niveles de CF en menores de un año de edad sanos están normalmente aumentados comparados con los niveles de CF en niños y adultos6,79.
A pesar de múltiples estudios, su uso en pediatría no ha podido dilucidarse certeramente, en principio, por su variabilidad en los valores normales ya que se encuentra aumentado en niños, especialmente en menores de un año y también en menores de 6 meses comparados con los adultos.
El valor de referencia estándar en pediatría se ha estipulado en 50 µg/g de heces.
Pregunta 15. ¿La CF es un método útil para predecir la curación endoscópica en ECP?
Afirmación 22: el valor de corte de la CF < 250 µg/g indica remisión endoscópica, mientras que su aumento (> 250 µg/g) precede a la recurrencia clínica en dos a tres meses. En los pacientes con EC luminal, el descenso de la CF en un contexto de mejoría clínica, tras el tratamiento de inducción, se puede utilizar como marcador de respuesta al tratamiento.
Nivel de evidencia: II-III.
Nivel de recomendación: B.
Grado de acuerdo: 93,1%.
Puntos prácticos
No existe una correlación lineal entre niveles de CF y la gravedad o la extensión de la inflamación.
En niños menores de cinco años se han postulado niveles más elevados de CF.
Se debe tener en cuenta que existen diferentes kits, y se ha documentado la pérdida de estabilidad a temperatura ambiente.
Se acepta la medición de CF una vez se haya logrado remisión clínica sostenida para verificar la cicatrización de la mucosa y seleccionar aquellos pacientes que requieren evaluación endoscópica9,76,80.
Pregunta 16. ¿Es la CF un buen indicador o predictor de recaída?
Afirmación 23: en pacientes con EC luminal en remisión clínica, un aumento significativo de la CF seriada (> 250 µg/g) identifica de forma precoz la recaída y debe desencadenar más investigaciones para considerar la intensificación o el escalamiento del tratamiento, especialmente cuando los valores aumentan en el tiempo.
Nivel de evidencia: II-1.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Tratamiento de la ECP
Pregunta 17. ¿Cuáles son los objetivos de tratamiento de la EII? ¿La estrategia Treat to Target (tratamiento por objetivos) aplicada a la población pediátrica?
Afirmación 24: la iniciativa Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE II) de la Organización Internacional para el Estudio de las Enfermedades Inflamatorias Intestinales (IOIBD) ha propuesto objetivos de tratamiento en la EII tanto en adultos como en niños. El grupo desarrollador de la guía resume las recomendaciones de este consenso aplicadas a la población pediátrica de vital importancia para dirigir las decisiones terapéuticas.
Nivel de evidencia: III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Aspectos clínicos
1. La respuesta clínica es un objetivo de tratamiento inmediato. Considere cambiar el tratamiento si no se ha logrado este objetivo.
2. La respuesta clínica debe definirse como:
EC: en niños, la disminución de PCDAI de al menos 12,5 puntos y de wPCDAI de al menos 17,5 puntos.
CU: en niños, la disminución de PUCAI de al menos 20 puntos.
3. La remisión clínica es un objetivo de tratamiento intermedio (es decir, a mediano plazo). Considere cambiar el tratamiento si no se ha logrado este objetivo.
4. La remisión clínica debe definirse como:
EC: en niños por PCDAI (< 10 puntos o < 7,5, excluyendo el ítem de altura) o wPCDAI (< 12,5 puntos).
UC: en niños, un PUCAI < 10 puntos.
5. La respuesta clínica o la remisión son insuficientes para ser utilizados como objetivos de tratamiento a largo plazo.
6. En los niños, la restauración del crecimiento normal es un objetivo de tratamiento a largo plazo. Considere cambiar el tratamiento si no se ha logrado este objetivo.
Evaluación endoscópica y transmural
1. La cicatrización endoscópica es un objetivo a largo plazo. Considere cambiar el tratamiento si no se ha logrado este objetivo.
2. La evaluación de la cicatrización endoscópica se puede lograr mediante sigmoidoscopia o colonoscopia. Cuando no es factible, las alternativas en EC pueden ser la cápsula endoscópica o la enteroscopia con balón.
3. La cicatrización endoscópica debe medirse por:
CD: SES-CD < 3 puntos o ausencia de ulceraciones (p. ej., subpuntuaciones de ulceración de SES-CD = 0)
UC: subpuntuación endoscópica de Mayo = 0 puntos, o un Ulcerative Colitis Endoscopic Index of Severity (UCEIS) ≤ 1 punto.
4. La remisión histológica no es un objetivo de tratamiento ni en la EC ni en la CU. No obstante, en la CU se podría utilizar como complemento de la remisión endoscópica para representar un nivel más profundo de curación.
5. La curación transmural (evaluada por entero-TAC, enterografía por resonancia o ecografía intestinal) no es un objetivo de tratamiento ni en la EC ni en la CU. No obstante, en la EC debe utilizarse como complemento de la remisión endoscópica para representar un nivel más profundo de curación.
Biomarcadores
1. La normalización de la PCR (a valores por debajo del límite superior de lo normal) y de CF (a 100-250 μg/g) es un objetivo de tratamiento intermedio en CU y EC. Considere cambiar el tratamiento si no se ha logrado este objetivo.
Calidad de vida y discapacidad
1. La ausencia de discapacidad y la normalización de la calidad de vida relacionada con la salud son objetivos de tratamiento a largo plazo. Considere cambiar el tratamiento si no se ha logrado este objetivo.
Finalmente, presentamos el algoritmo modificado, traducido y adaptado a la población pediátrica objeto de la presente guía y una tabla de semanas aproximadas de respuesta a los diferentes tratamientos (Figura 3).
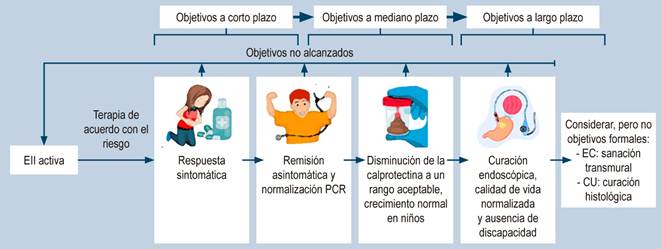
Figura 3 Algoritmo de tratamiento por objetivos. Adaptado de: Turner D, et al. Gastroenterology. 2021;160(5):1570-8380.
A continuación, se presenta el tiempo (número medio de semanas) requerido para lograr la meta después de iniciar el tratamiento para EC (n = 39) y CU (n =36), basado en el proceso similar a Delphi y la revisión sistemática de la evidencia. Nota: dada la escasez de datos clínicos de alta calidad, esta tabla debe considerarse simplemente como una estimación aproximada de la opinión de los expertos (Tabla 8).
Tabla 8 Determinando los objetivos terapéuticos para la estrategia treat to target (tratamiento por objetivos) en EIIP en semanas
Nivel de evidencia III, recomendación B. Adaptado de: Turner D, et al. Gastroenterology. 2021;160(5):1570-8380.
Pregunta 18. ¿Cuáles de las siguientes intervenciones son más eficientes y seguras para inducir remisión y mantenimiento de la ECP inflamatoria, estenosante y penetrante?
Afirmación 25: se recomienda que el tratamiento de la ECP sea individualizado para lograr un rápido control de la inflamación y reducir el daño intestinal a largo plazo considerando la edad, la localización, el comportamiento, el retraso del crecimiento, los efectos secundarios y la calidad de vida, con una identificación de factores de alto riesgo y de curso complicado (cirugía precoz, progresión a daño intestinal permanente) (Tabla 9, Figura 4):
Fenotipo estenosante (B2).
Fenotipo fistulizante (B3).
Enfermedad perianal.
Sin respuesta a la terapia de inducción.
Nivel de evidencia: III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Tabla 9 Estratificación de riesgo de peor desenlace en ECP y terapia sugerida
1Perforación intestinal, fístula, masa y/o abscesos antes de cirugía; 2NEE: nutrición enteral exclusiva; 3TNF: factor de necrosis tumoral; 4POP: posoperatorio; 5Clasificación de París. Adaptada de: van Rheenen PF, et al. J Crohns Colitis. 2021;15(2):171-9468.
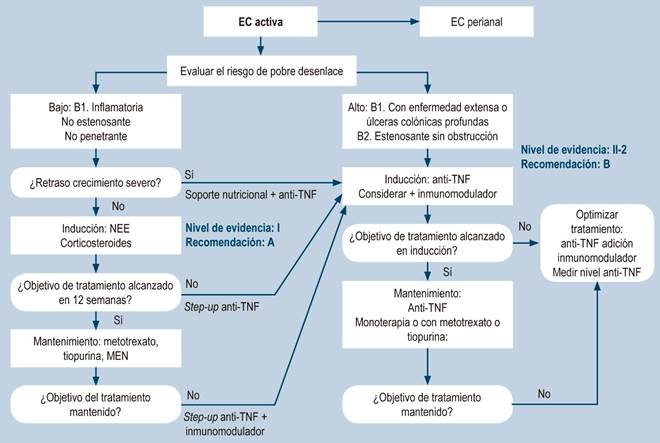
Figura 4 Mantenimiento de la enfermedad de Crohn pediátrica luminal. Adaptada de: van Rheenen PF, et al. J Crohns Colitis. 2021;15(2):171-9468.
Inducción de la remisión
Afirmación 26: los objetivos de la inducción son:
Lograr la remisión clínica: wPCDAI < 12,5.
Lograr una respuesta endoscópica: disminución del SES-CD o del CDEIS al menos un 50% del basal.
Lograr la remisión endoscópica (curación mucosa): ausencia de lesiones inflamatorias macroscópicas o SES-CD < 3 puntos.
Si es posible, lograr una remisión histológica: histología normal (controvertido).
Nivel de evidencia: III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Inducción de la remisión
¿En la inducción de la remisión en ECP debemos usar nutrición enteral exclusiva (NEE), nutrición enteral parcial (NEP), o nutrición parenteral (NP)?
Afirmación 27: en niños con EC luminal activa, el tratamiento con NEE se recomienda como primera línea para la inducción de la remisión.
Nivel de evidencia: I y II-1.
Nivel de recomendación: A.
Grado de acuerdo: 96,6%.
Puntos prácticos
La NEE tiene la misma eficacia que los corticoides orales en la inducción de remisión de niños con EC activa luminal, por lo que debe ser considerada la terapia de primera línea para inducir remisión en EC activa luminal64,75,81. Los pacientes con enfermedad puramente inflamatoria (B1) y riesgo bajo a medio en el momento del diagnóstico son elegibles para NEE. Esta elección puede ser independiente de la ubicación de la enfermedad68,82,83.
No hay diferencia en la eficacia entre las fórmulas elementales y no elementales, entre dietas de composición proteica similar con diferente composición de grasas, entre alimentación oral, en bolos y alimentación enteral continua. Teniendo en cuenta la palatabilidad reducida, el riesgo de abstinencia temprana y los altos costos asociados con dietas elementales, la elección principal de una fórmula es la polimérica a menos de que existan otras comorbilidades como la alergia a las proteínas de leche de vaca (APLV)81-83.
Se puede considerar el uso de una sonda de alimentación nasogástrica para superar la aversión a la fórmula o en caso de no lograr el consumo diario requerido por vía oral68. Las dietas basadas en alimentos pueden ser alternativas para los pacientes que no pueden tolerar la NEE80-82,84.
La NEE puede ser reusada durante el curso de la enfermedad en caso de recaída81.
Duración: se recomienda una duración de NEE al menos de ocho semanas81.
No hay evidencia suficiente para recomendar un esquema de reintroducción de alimentos. Se sugiere reintroducción gradual de alimentos con la concomitante reducción de la fórmula en períodos de 2-3 semanas85.
Existe evidencia suficiente para recomendar la NEE en enfermedad oral o perianal aislada o cuando hay manifestaciones extragastrointestinales86.
Efectos adversos: se debe prestar atención al síndrome de realimentación (SR) en pacientes desnutridos severos. Otros son: náuseas, vómito, diarrea, dolor abdominal y distensión87,88.
Duración de la remisión: no está bien determinada81.
La NEE promueve la curación mucosa y la curación transmural en algunos pacientes83,89,90.
Afirmación 28: la NEP podría inducir remisión clínica e histológica en pacientes con EC activa si se acompaña de una dieta especial (dieta antiinflamatoria o dieta de exclusión para EC: CDED).
Nivel de evidencia: I.
Nivel de recomendación: A.
Grado de acuerdo: 82,8%.
¿Uso de corticoides en la inducción de remisión de la ECP?
Afirmación 30:
En ECP luminal activa, cuando la NEE no es una opción (NEE pobremente tolerada o inefectiva después de dos a cuatro semanas de un cumplimiento adecuado), los corticosteroides pueden ser considerados para inducir la remisión. (Nivel de evidencia: 3. Grado de recomendación: B).
La dosis inicial de prednisolona es de acuerdo al peso y debe reducirse una vez se alcance la remisión clínica, pero no más tarde de 4 semanas después de su inicio. (Nivel de evidencia: 3) (Tabla 10).
En el caso de enfermedad ileocecal leve (L1), si la NEE no es eficaz, es preferible el tratamiento con budesonida de liberación ileal que prednisolona. (Nivel de evidencia: 2).
Los corticosteroides no deben utilizarse como terapia de mantenimiento de la remisión; las estrategias de ahorro de esteroides deben ser aplicadas. (Nivel de evidencia: 4).
Es necesario implementar estrategias ahorradoras de esteroides, con inicio de inmunomoduladores, realizando un destete planificado y evitando la estrategia de montaña rusa.
Nivel de evidencia: II-III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Tabla 10 Esquema de reducción gradual de prednisona o prednisolona (administración una vez al día)
Adaptada de: van Rheenen PF, et al. J Crohns Colitis. 2021;15(2):171-9468.
Puntos prácticos
Diferentes estudios muestran que no hay diferencias significativas entre el uso de la NEE y los corticosteroides en cuanto a la eficacia para inducir la remisión de la ECP; sin embargo, la NEE es superior a los corticosteroides en la mejora de la inflamación de la mucosa a corto plazo y la reducción del índice PCDAI95-97. Además, se han evidenciado cambios en la composición de la microbiota intestinal89,98) y evita el uso de esteroides a largo plazo sin aumentar el uso de agentes biológicos ni la necesidad de cirugía99. Los niños que reciben NEE tienen tendencia a un mejor crecimiento, pero tienen tasas similares de recaídas y complicaciones en la ECP100. La NEE como tratamiento para inducir la remisión de la ECP debe ofrecerse como primera línea101.
La dosis recomendada de prednisona/prednisolona oral (o equivalente) para la ECP activa es de 1 mg/kg (máximo de 40 mg/día) una vez al día. Puede considerarse un aumento de la dosis a 1,5 mg/kg hasta un máximo de 60 mg/día si la respuesta es insatisfactoria8.
Los esquemas de reducción gradual usualmente utilizan un tiempo de reducción de ocho a 12 semanas. En la práctica clínica, la introducción y el descenso de corticosteroides no están estandarizados y se basan en recomendaciones empíricas más que en ensayos clínicos, y existe gran variabilidad entre los clínicos. El acortamiento de cada etapa de siete a cinco días o cualquier otra modificación de reducción debe individualizarse102,103.
Los efectos adversos de los corticosteroides están relacionados con la dosis y la duración del tratamiento, sin embargo, la sensibilidad entre los individuos es muy variable104. Se han asociado con un mayor riesgo de infecciones y un riesgo elevado de abscesos intraabdominales o pélvicos105; no obstante, los efectos secundarios de mayor importancia percibidos por los usuarios son el aumento de peso, el insomnio y las facies cushingoides106,107.
La dosis inicial de la budesonida para pacientes > 40 kg es de 9 mg una vez al día durante seis semanas, seguido de un descenso así: 6 mg una vez al día durante dos semanas y 3 mg una vez al día durante dos semanas. Se han utilizado dosis de hasta 12 mg durante las primeras cuatro semanas que han mostrado una leve mejoría en las tasas de remisión y respuesta108. Las dosis de budesonida deben adaptarse en función de la edad y el peso en los niños pequeños108.
No hay evidencia de beneficio de la budesonida en el compromiso de colon más distal. Para la inducción de la remisión clínica, la budesonida fue más eficaz que el placebo, pero menos eficaz que los esteroides convencionales. La probabilidad de eventos adversos con el uso de budesonida es menor que con los corticosteroides convencionales. La budesonida no es eficaz para el mantenimiento de la remisión109,110.
Los pacientes que deban someterse a una intervención quirúrgica mayor mientras estén recibiendo dosis suprafisiológicas (> 50% de la dosis inicial de prednisolona) durante tres semanas o más, debe asumirse que padecen insuficiencia suprarrenal y necesitarán una dosis perioperatoria adicional de hidrocortisona. Los pacientes con supresión suprarrenal poco clara (están en las últimas semanas de su esquema de reducción o los que terminaron la terapia con corticosteroides en los últimos tres meses) deben ser considerados para el asesoramiento del endocrinólogo y la realización de pruebas preoperatorias del eje hipotálamo-hipófisis-suprarrenal)111,112.
Cuando los corticosteroides orales han fracasado, los endovenosos pueden resultar eficaces en algunos pacientes. La administración de corticosteroides endovenosos se limita a la enfermedad grave y activa8.
En la enfermedad colónica distal pueden utilizarse corticosteroides en presentación de enema, como en los pacientes adultos113.
¿Uso de antibióticos en la inducción de la remisión en ECP?
Afirmación 31: no se recomienda el uso de antimicrobianos en ECP, su uso es incierto debido a que la evidencia sobre los efectos de los antibióticos en la inducción de remisión y mantenimiento de ECP es insuficiente.
Nivel de evidencia: II.
Nivel de recomendación: C.
Grado de acuerdo: 86,2%.
Puntos prácticos
Basado en el único estudio clínico controlado en pediatría, la combinación de azitromicina y metronidazol es más efectivo que metronidazol solo, para inducción de remisión clínica a ocho semanas en EC leve a moderada (PCDAI > 10 y < 40)68,114. Sin embargo, el desenlace primario, definido como una disminución en PCDAI > 12,5 puntos, no fue estadísticamente significativo.
Una combinación de antibióticos puede ser considerada para inducción de remisión en Crohn pediátrico leve a moderado, donde la terapia nutricional no es una opción68,114.
El esquema antibiótico sugerido es: azitromicina de 7,5 mg/kg (cinco días por semana, por cuatro semanas, seguido de tres días por semana por otras cuatro semanas) y metronidazol de 20 mg/kg/día por ocho semanas68,114.
Para infecciones bacterianas que complican la EC, los antibióticos también tienen gran utilidad al igual que para el sobrecrecimiento bacteriano y en sospecha de enfermedad perianal68,115.
Terapia de mantenimiento
¿Uso de aminosalicilatos en la terapia de mantenimiento en ECP?
Afirmación 32: los aminosalicilatos no están indicados para inducir la remisión en la EC ileal/ileocolónica/intestino delgado proximal. (Nivel de evidencia: I).
Nivel de evidencia: III.
Nivel de recomendación: C.
Grado de acuerdo: 93,1%.
Puntos prácticos
El uso de aminosalicilatos se puede considerar en pacientes seleccionados para la inducción de remisión en pacientes con ECP con actividad muy leve. (Nivel de evidencia II)8.
Los aminosalicilatos son poco beneficiosos para la inducción de remisión de la EC activa. No hay datos basados en la evidencia que indiquen las ventajas de su uso113,116-118.
La sulfasalazina parece ser superior en comparación con otros aminosalicilatos para inducir la remisión en pacientes adultos con afectación colónica, pero no en aquellos con enfermedad limitada al intestino delgado119,120.
No hay ningún papel de los aminosalicilatos en el mantenimiento de la remisión en la mayoría de los pacientes con EC119.
La dosis de aminosalicilatos oral para la ECP pediátrica es similar a la de la de CUP, 50-80 mg/kg/día hasta 4 g diarios8.
No hay evidencia de que los aminosalicilatos induzcan la curación mucosa, por lo que debe considerarse como una terapia adyuvante. Si se utilizan como tratamiento en monoterapia debe verificarse la cicatrización de la mucosa121. El seguimiento estrecho de la PCR, la VSG y la calprotectina fecal debe garantizar la remisión completa y debe establecerse un umbral bajo para la intensificación del tratamiento8.
En caso de EC limitada a colón con actividad leve, que se encuentre en remisión con mesalazina, esta se debe intentar retirar progresivamente, evaluando la necesidad de reiniciarla o eventualmente iniciar terapia inmunomoduladora como estrategia de mantenimiento a corto plazo122.
Crohn luminal
¿Uso de inmunomoduladores en el mantenimiento de ECP luminal, estenosante y penetrante?
Afirmación 33: cuando se ha conseguido la remisión en pacientes con EC luminal, se pueden utilizar los inmunomoduladores azatioprina (AZA) y 6-mercaptopurina (6-MCP) para mantenerla. Los tiopurínicos en monoterapia nunca deberían usarse para la inducción a la remisión. (Nivel de evidencia I-II).
Nivel de evidencia: I-II.
Nivel de recomendación: B.
Grado de acuerdo: 96,6%.
Puntos prácticos
Los inmunomoduladores se han utilizado ampliamente y han demostrado su eficacia para mantener la remisión tanto en EC como en CU en estudios en adultos, pero la evidencia en pediatría es limitada, excepto un ensayo clínico aleatorizado con limitaciones metodológicas123, por lo que la decisión de utilizarlos debe ser cuidadosa tomando en cuenta los riesgos de mielosupresión y linfoma, que son muy bajos124, y de linfoma de células T de hígado, así sea mucho menor125. A su favor están su relativo bajo costo, y la desaparición de los riesgos al suspenderlos, independientemente del tiempo de utilización126. Hasta hace unos años cuando se hablaba de corticodependencia/resistencia se recomendaban como una opción para el mantenimiento libre de corticoides8, pero, con el conocimiento actual, los corticoides solo se deben utilizar para inducir la remisión y no para mantenimiento68,123-126.
La dosis recomendada para AZA es de 2-2,5 mg/kg/día y de 1-1,5 mg/kg/día; para mercaptopurina (MP), una vez al día, iniciándola dosis completa y obteniendo su máximo efecto entre ocho a 16 semanas68.
Afirmación 34: se recomienda el uso de AZA y 6-MCP para mantener la remisión, pero en su administración deberían tenerse en cuenta los efectos secundarios.
Nivel de evidencia: I-II.
Nivel de recomendación: C.
Grado de acuerdo: 89,7%.
Puntos prácticos
Dentro de los efectos secundarios del uso de AZA y 6-MCP se encuentran: toxicidad hematológica (2%-14%), hepatotoxicidad, pancreatitis (7%), náuseas, vómitos, especialmente el linfoma, más frecuente en el sexo masculino, cáncer de piel no melanoma (medidas de protección solar) y primoinfección por virus de Epstein-Barr (VEB), por el riesgo de síndrome hemofagocítico/linfoma68,127. Se ha documentado que el linfoma hepatoesplénico de células T (HSTCL) ocurre entre 1-3/10.000 pacientes expuestos, y este riesgo está probablemente asociado con la duración del tratamiento por tiopurinas por más de dos años y el riesgo no aumenta al suspenderlos125.
La evidencia ha demostrado que la aparición de HSTCL, cuando se presenta, es mucho mayor en varones, por lo que la recomendación es utilizarlos en niños con EII, con precaución68,124,125.
Los pacientes con baja o ausente actividad de la tiopurina metiltransferasa (TPMT) tienen mayor riesgo de mielotoxicidad grave, por lo que se recomienda una disminución de dosis en heterocigotos por TPMT o actividad enzimática intermedia y la monitorización hematológica mensual los primeros tres meses y, posteriormente, cada tres meses68,124,125.
Se debe considerar el estudio de metabolitos (6-tioguanina [6-TGN] y 6-metilmercaptopurina [6-MMP]) en respuesta subóptima, citopenia, aumento de enzimas hepáticas, adherencia, optimización de tratamiento, considerando niveles terapéuticos de 6-TGN = 230-450 pmol/8x108 RBC67,124,125.
Crohn estenosante y penetrante
Afirmación 35: se recomienda contemplar el uso de los inmunomoduladores AZA y 6-MCP para prevenir recurrencias poscirugía cuando el paciente no las ha tomado previamente y cuando la enfermedad tiene bajo riesgo de recaída.
Nivel de evidencia: III.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Puntos prácticos
La evidencia existente viene de estudios en adultos, por lo que esta recomendación en niños se ha extrapolado, ya que se ha demostrado que las tiopurinas son superiores a las 5-ASA. No se menciona una comparación con MTX, o con biológicos.
Afirmación 36: si las tiopurinas han fallado para evitar la cirugía, se recomienda que su uso posterior sea evaluado cuidadosamente contrastando el riesgo/beneficio.
Nivel de evidencia: III.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Puntos prácticos
AZA o 6-MCP se pueden considerar para mantener remisión en el posoperatorio cuando el paciente no las había recibido previamente, sin importar los factores de riesgo de recaída o la extensión de la enfermedad; pero si se utilizaban adecuadamente y no impidieron la cirugía, no se deberían recomendar127.
En general, AZA o 6-MCP solo demostraron superioridad comparadas contra placebo o mesalazina, pero el MTX podría ser una mejor opción. En estas condiciones de baja evidencia, los inmunomoduladores AZA y 6-MCP solo tendrían indicación para optimizar el rendimiento de los anti-TNF.
¿Uso de MTX para el mantenimiento de ECP?
Afirmación 37: se recomienda el MTX para mantener la remisión clínica como inmunomodulador de primera elección, o después del fracaso o la intolerancia a las tiopurinas.
Nivel de evidencia: II-III.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Puntos prácticos
La evidencia del uso de MTX en ECP es escasa y posterior al uso de tiopurinas. Dos revisiones sistemáticas del uso de MTX en ECP de estudios retrospectivos mostraron una tasa de remisión clínica de mantenimiento combinada entre 25%-53% a los 12 meses, con una duración de remisión hasta de 24 meses68,128,129.
Se recomiendan dosis de 15mg/m2 (superficie corporal) (máximo: 25 mg) a la semana subcutánea (SC) o intramuscular (IM) y luego de conseguir la remisión clínica y curación de la mucosa administrar: 10 mg/m2 a la semana SC o IM. Se deben usar como coadyuvantes el ácido fólico oral de 5 mg; 24-72 horas posteriores al MTX una vez a la semana o 1 mg diario durante cinco días a la semana para reducir hepatotoxicidad, y/o ondansetrón 1 hora antes y el día después del MTX para evitar náuseas y vómito68.
Se han descrito desórdenes linfoproliferativos por el uso de MTX en otras patologías, lo que nos puede dar una falsa sensación de seguridad, con menos estudios de eficacia que las tiopurinas130.
Nutrición enteral exclusiva (NEE)
Nutrición enteral parcial (NEP)
Afirmación 39: se recomienda la NEP como una opción de tratamiento para mantener la remisión en algunos pacientes seleccionados.
Nivel de evidencia: I y II-1.
Nivel de recomendación: A.
Grado de acuerdo: 93,1%.
Puntos prácticos
La nutrición enteral parcial (NEP) y la nutrición enteral de mantenimiento (NEM) son términos que se usan con frecuencia de manera intercambiable en la literatura68,84.
La NEP se usa en mantenimiento de pacientes con enfermedad leve y bajo riesgo de recaída. La cantidad diaria y duración de NEP efectiva es desconocida68,112,131.
En niños con EC de bajo riesgo que lograron la remisión clínica, la monoterapia de mantenimiento con nutrición enteral (en al menos el 50% de las necesidades energéticas diarias) puede prolongar la remisión132.
La adherencia con NEP a mediano plazo es deficiente; de ahí la falta de eficacia. El efecto puede deberse en parte a una mala adherencia más que a la falta de eficacia per se68.
La NEP puede funcionar bien como un puente a corto plazo entre tratamientos, por ejemplo, después de NEE mientras se espera que la inmunosupresión sea completamente eficaz, o como un complemento para mejorar el efecto de otras terapias68.
La fórmula polimérica se prefiere sobre la elemental68.
El uso de NEM, de manera concomitante con una dieta baja en grasa, se ha asociado con una disminución en el riesgo de recurrencia de enfermedad en pacientes sometidos a resección quirúrgica133.
Existen diferentes estrategias alimentarias para el mantenimiento de la remisión en EC, sin embargo, se necesitan más estudios multicéntricos, controlados y aleatorizados que evalúen su eficacia y confirmen objetivamente la disminución de la inflamación intestinal134.
Nutrición enteral suplementaria (NES)
Afirmación 40: se recomienda el uso de la NES (alimentos con propósitos médicos especiales-suplementación oral) en EIIP como complemento de la terapia.
Nivel de evidencia: I.
Nivel de recomendación: A.
Grado de acuerdo: 100%.
Puntos prácticos
La suplementación vía oral o la nutrición enteral se puede recomendar en pacientes con EC en remisión, en caso de que la desnutrición no se pueda tratar mediante asesoramiento dietético15,135.
Si la alimentación oral no cubre la demanda nutricional, se debe considerar la NES como terapia de apoyo. El uso de fórmulas debe tener siempre preferencia sobre la NP, a menos que esté completamente contraindicado.
La NE con fórmula polimérica se puede emplear para tratamientos primarios y de apoyo en la terapia nutricional en EII activa136.
La terapia nutricional enteral suplementaria se puede administrar por sonda nasogástrica (SNG) durante la noche y en el día dieta normal vía oral. También es válido implementar períodos cortos de alimentación enteral por SNG con cierta frecuencia, así como suplementos nutricionales vía oral como complemento de la dieta normal. Ninguno ha demostrado ser superior a otro. No hay estudios que comparen NEP con tratamiento médico estándar8.
Intervenciones dietarias como prevención de la ECP
Afirmación 41: se recomiendan las intervenciones dietarias porque pueden contribuir a la prevención de la EII.
Nivel de evidencia: II-2.
Nivel de recomendación: B.
Grado de acuerdo: 89,7%.
Puntos prácticos
La lactancia materna es recomendada por su efecto protector en la EII137.
Una dieta rica en frutas y verduras, rica en ácidos grasos ω-3 y baja en ácidos grasos ω-6 se asocia con un menor riesgo de desarrollar EC o CU y, por lo tanto, está recomendado15.
No se debe recomendar una dieta de eliminación o restrictiva en niños/adolescentes con EII a menos que los beneficios potenciales superen los riesgos potenciales de la dieta138,139.
En la EII se deben evitar los alimentos “occidentalizados” (ricos en grasas, proteínas, azúcares, bajos en frutas y verduras), ya que el consumo de estos alimentos se ha identificado como factor de riesgo para el desarrollo de la EII140.
En la EII se debe evitar una dieta alta en grasas (incluidas las grasas de la leche), al igual que los alimentos o bebidas que contengan grandes cantidades de emulsionantes (salsas, comidas rápidas, margarinas, helados)140.
Papel de los micronutrientes
Afirmación 42: en niños con EII se recomienda la suplementación de hierro, vitamina D, zinc y calcio en función de los déficits.
Nivel de evidencia: II-2.
Nivel de recomendación: B.
Grado de acuerdo: 82,8%.
Puntos prácticos
Se recomienda suplementar con hierro oral a todos los pacientes con EIIP que cursen con anemia por deficiencia de hierro141.
Las pruebas de detección iniciales para deficiencia de hierro deben realizarse en el momento del diagnóstico y deben repetirse en cada intervalo de tres meses para los pacientes con enfermedad activa y cada seis a 12 meses con enfermedad inactiva142.
Se recomienda monitorizar el magnesio sérico en niños con diarrea superior a cuatro semanas o con riesgo de síndrome de realimentación (SR). En tal caso, suplementar de dos a cuatro semanas magnesio oral cuando se encuentre deficiencia6,8,68,81.
En caso de deficiencia de calcio, la EFSA recomienda usar dosis de: 450 mg/día de uno a tres años, 800 mg/día de cuatro a ocho años y 1150 mg/día de nueve a 18 años143.
Se recomienda monitorear de rutina los niveles de vitamina D81.
Suplementar vitamina D cuando los valores séricos estén por debajo de 20 ng/mL o 50 nmol/L144.
Todos los pacientes deben monitorizarse una vez al año para ácido fólico141.
Pacientes con resección intestinal, bolsa ileal, sobrecrecimiento bacteriano extenso y enfermedad ileal deben monitorizarse para deficiencia de B12 cada tres a seis meses113,142.
Uso de probióticos en ECP
Afirmación 43: se recomienda en pacientes con EC, no usar los probióticos para inducir o mantener la remisión.
Nivel de evidencia: II.
Nivel de recomendación: D.
Grado de acuerdo: 96,6%.
Puntos prácticos
En el único estudio aleatorizado controlado en pediatría, el uso de la cepa de Lactobacillus rhamnosus (LGG) administrada además de la terapia de mantenimiento estándar tuvo tasas de recaída numéricamente más altas en comparación con el placebo, pero no fueron estadísticamente significativas145.
En una revisión de Cochrane acerca del uso de probióticos en EC, al igual que en una revisión sistemática, no demostró ningún efecto benéfico de los probióticos en la EC146,147.
No hay evidencia de los efectos benéficos del uso probióticos en el tratamiento de la ECP. Esta conclusión ha sido reiterada recientemente por el documento de consenso de la Sociedad Europea de Gastroenterología Pediátrica, Hepatología y Nutrición (ESPGHAN), para no recomendar probióticos en la inducción o el mantenimiento de la remisión de la ECP. Es necesario tener en cuenta el número limitado de ECA realizados, especialmente en niños, y los diversos genotipos y fenotipos, que probablemente requieran un enfoque terapéutico más personalizado68.
Trasplante de microbiota fecal (TMF)
Afirmación 44: no se recomienda en pacientes con EC, usar el TMF para inducir o mantener la remisión.
Nivel de evidencia: II.
Nivel de recomendación: D.
Grado de acuerdo: 96,6%.
Tratamiento con talidomida en ECP
Afirmación 45: se recomienda la talidomida como una alternativa eficaz para la inducción de la remisión y el mantenimiento en la ECP en casos seleccionados, como aquellos intolerantes a las terapias con biológicos o aquellos refractarios a varios productos biológicos, especialmente por sus efectos colaterales. Se requieren más estudios.
Nivel de evidencia: II.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Puntos prácticos
Un ensayo clínico randomizado controlado demostró la remisión clínica en el 60% a las ocho semanas; 54% a las 52 semanas; curación mucosa: 26% a las 12 semanas; y 41% a las 52 semanas.
La dosis oral recomendada para inducción es: para < 30 kg 50 mg/día; de 30-60 kg dar 100 mg/día; > 60 kg dar 150 mg/día, la dosis de mantenimiento se debe reducir en un 25% durante los siguientes 6 meses.
Se han descrito efectos adversos importantes como teratogenicidad, neuropatía periférica y sedación68,150,151.
Uso de biológicos en ECP
Afirmación 46:
En pacientes que debutan con ECP, con alto riesgo de curso complicado, la terapia anti-TNF es recomendada para inducir remisión. (Nivel de evidencia III)68,152-156.
Los pacientes que fallan en alcanzar o mantener la remisión clínica con agentes anti-TNF, a pesar de la optimización de la dosis y el uso de inmunomodulador, ustekinumab o vedolizumab deben ser considerados (Nivel de evidencia IV) (Tabla 11).
Nivel de evidencia: II-III.
Nivel de recomendación: B.
Grado de acuerdo: 96,6%.
Tabla 11 Medicamentos, dosis, monitorización de niveles
| Medicación | Recomendación dosis de inducción | Recomendación dosis de mantenimiento | Niveles biológicos, remisión (ug/mL) | Niveles recomendados de curación mucosa (ug/mL) |
|---|---|---|---|---|
| Infliximab | 5 mg/kg en semanas 0-2 y 6. | 5 mg/kg cada 8 semanas. | 3-7 | > 5 |
| Adalimumab |
|
|
> 5,9 | > 7,5 |
| Golimumab |
|
|
> 1,4 | NA |
| Vedolizumab | 6 mg/kg en semanas 0, 2 y 6, máximo 300 mg. | 6 mg/kg cada 8 semanas, máximo 300 mg. | > 13,6 | NA |
| Ustekinumab |
|
|
> 0,8 | > 4,5 |
Adaptado de: Chavannes M, et al. J Crohns Colitis. 2019;13(5):578-84155; Colombel JF, et al. N Engl J Med. 2010;362(15):1383-95201; Schneider AM, et al. BMC Gastroenterol. 2018;18(1):140202; Jossen J, et al. J Pediatr Gastroenterol Nutr. 2020;70(3):304-9203; Singh N, et al. Inflamm Bowel Dis. 2014;20(10):1708-13208; Papamichael K, et al. Clin Gastroenterol Hepatol. 2019;17(9):1655-1668.e3209; Feuerstein JD, et al. Gastroenterology. 2017;153(3):827-34210.
Puntos prácticos
En pacientes con ECP activa con fallas en el mantenimiento de la remisión con un inmunomodulador, se recomiendan los agentes anti-TNF para inducción y mantenimiento de la remisión. (Nivel de evidencia II).
En pacientes con enfermedad perianal fistulizante, la terapia anti-TNF es recomendada como inducción primaria y mantenimiento, en combinación con manejo antibiótico, quirúrgico o ambas. (Nivel de evidencia III).
En pacientes que inician infliximab, se recomienda la combinación de la terapia con un inmunomodulador. (Nivel de evidencia II).
En pacientes que nunca han recibido adalimumab, este en monoterapia es una alternativa a la terapia combinada con adalimumab (Nivel de evidencia III).
En pacientes en manejo con anti-TNF, una monitorización terapéutica proactiva temprana, seguida de la optimización, es recomendada. (Nivel de evidencia II).
En pacientes con ECP activa, quienes son tratados con anti-TNF, se recomienda usar medición de niveles para guiar los cambios en el tratamiento sobre el escalonamiento empírico de la dosis o cambio de terapia. (Nivel de evidencia III).
Se sugiere pasar a monoterapia anti-TNF después de seis a 12 meses de terapia combinada, dosis estándar de biológicos, niveles adecuados del fármaco y remisión clínica, endoscópica y transmural68,152-156.
Existen unos predictores de respuesta inadecuada que están estratificados en la Tabla 9, que sugieren cuál es el manejo de inducción más recomendado según el compromiso.
Infliximab debe administrarse inicialmente a 5 mg/kg por dosis (en las semanas 0, 2 y 6 seguidas de 5 mg/kg cada ocho semanas para el mantenimiento). Se debe considerar una dosis inicial más alta en niños con bajo peso corporal (< 30 kg), con enfermedad extensa e hipoalbuminemia, pueden requerir dosis de inducción más alta (10 mg/kg), intervalos más frecuentes para alcanzar niveles objetivos.
El adalimumab debe iniciarse con 160 mg, seguido de 80 mg después de dos semanas y luego 40 mg cada dos semanas en adolescentes con peso > 40 kg. En menores de 40 kg las dosis recomendadas son 80 mg, seguido de 40 mg después de dos semanas y luego 20 mg cada dos semanas. Inyecciones semanales son consideradas en la respuesta o en niveles bajos.
El uso de adalimumab en monoterapia tiene iguales tasas de remisión que con el uso de terapia combinada con inmunomoduladores.
La medición proactiva de los niveles de los anti-TNF debe ser: adalimumab justo antes de la tercera inyección (cuatro semanas luego de la primera dosis), infliximab antes de la cuarta infusión (14 semanas luego de la primera dosis).
Los niveles de mantenimiento mínima de infliximab es 5 ug/mL y adalimumab 7,5 ug/mL. Fenotipos específicos, como fisura perianal, requieren niveles de infliximab > 12,7 ug/mL para cicatrización de la lesión.
Pacientes con títulos de anticuerpos contra el medicamento: si son bajos títulos, se puede ajustar la dosis y/o adicionar un inmunomodulador, pero si hay altos títulos, se debe cambiar de biológico.
Ustekinumab, anticuerpo dirigido contra la IL-12 y 23, es efectivo para remisión y mantenimiento, con poca evidencia en niños, pero demuestra una remisión importante en pacientes que nunca han recibido anti-TNF vs. los que fallaron con anti-TNF. La dosis es intravenosa y se administra 6 mg/kg (redondeando 130 mg, máximo 520 mg). La dosis SC se inicia a la semana 8 a 90 mg/m2 cada ocho semanas. Tiene baja inmunogenicidad y no requiere uso de inmunomodulador concomitante. No se han establecido unos niveles específicos para monitorización.
Vedolizumab es un anticuerpo monoclonal dirigido a la a4B7 integrina. Es efectivo en EC y CU (más en esta última). Tiene mejores tasas de cicatrización cuando se da como primera línea que como rescate ante la no respuesta de anti-TNF. En > 40 kg se administran 300 mg intravenosos (en las semanas 0, 2 y 6), seguidos de un mantenimiento de 300 mg intravenosos cada ocho semanas. En < 40 kg se administra 6 mg/kg hasta máximo 300 mg, en el mismo esquema que > 40 kg. La respuesta a este medicamento toma 16 semanas. La intensificación del esquema a cuatro semanas puede usarse cuando hay una falta de respuesta secundaria68,152-156.
Uso de biosimilares en EIIP
Afirmación 47:
La Agencia Europea de Medicamentos (EMA) aprobó el uso de biosimilares para infliximab para todas las indicaciones, incluida la EII en adultos y niños. El grupo de Porto de la EII pediátrica de la ESPGHAN aboga por dar alta prioridad a la realización de ensayos pediátricos con seguimiento a largo plazo para respaldar esta decisión.
El tratamiento de un niño con remisión sostenida con un biológico específico no debe cambiarse a un biosimilar hasta que los ensayos clínicos en EII estén disponibles para respaldar la seguridad y eficacia de dicho cambio.
Los programas de vigilancia poscomercialización de eficacia, seguridad e inmunogenicidad en niños con EII deben ser un requisito obligatorio para la comercialización de biológicos y biosimilares con las respectivas indicaciones.
Nivel de evidencia: II-III.
Nivel de recomendación: B .
Grado de acuerdo: 100%.
Puntos prácticos
La Organización Mundial de la Salud (OMS) los ha definido como “un producto bioterapéutico que es similar en términos de calidad, seguridad y eficacia a un producto bioterapéutico de referencia ya autorizado”.
Agencias como la Administración de Alimentos y Medicamentos de los EE.UU. (FDA) y la EMA decidieron que, para los biosimilares, no se necesita documentación de eficacia para todas las indicaciones de la molécula original. La extrapolación puede ser aceptable siempre que se hayan demostrado las propiedades farmacocinéticas (PK) y farmacodinámicas en estudios de todos los niveles.
Los biofarmacéuticos de referencia se caracterizan por una marcada heterogeneidad molecular debido a una variedad de factores que conducen a una magnitud de formas químicas.
Debido a que los productos biofarmacéuticos se fabrican en líneas de células vivas, son sensibles a los cambios en el proceso de fabricación, como las condiciones de crecimiento, los procesos de purificación, la formulación o las condiciones de almacenamiento.
Se requieren evaluaciones clínicas para evaluar la farmacodinamia, la farmacodinamia, la eficacia y la seguridad.
Las herramientas analíticas actualmente disponibles siguen siendo limitadas en la capacidad de caracterizar todas las posibles variantes químicas de los productos biológicos. Por tanto, la ausencia de diferencias detectables no implica necesariamente biosimilitud.
Debido a que el proceso de fabricación del producto original sigue siendo un secreto comercial incluso después de la expiración de la patente, no hay información sobre los pasos del proceso (es decir, vector, sistema de expresión de la célula huésped, procedimiento de expansión celular, mecanismo de recuperación de proteínas, proceso de purificación o formulación de la proteína terapéutica en un fármaco).
Deben tenerse en cuenta los cambios en la fabricación a lo largo de los años de producción con las consiguientes diferencias incrementales entre varios medicamentos biológicos, ya sean productos originales autorizados o biosimilares.
Incluso después de la demostración de biosimilitud en el momento de la aprobación, un medicamento biosimilar y uno de referencia podrían divergir con el tiempo. Por lo tanto, también es necesaria la demostración de la comparabilidad entre los productos biosimilares posteriores y el biosimilar inicial157.
Pregunta 19. ¿Cuál es la terapia médica en caso de ECP refractaria o en recaída?
Afirmación 48: en pacientes con EC moderada y severa en quienes ha fallado la inducción de la remisión clínica con corticoides se recomiendan los anti-TNF, tanto para inducirla como para mantenerla. Cuando no se ha logrado mantener la remisión clínica con AZA o 6-MCP en pacientes con EC moderada a severa, se recomiendan los anti-TNF para inducirla y mantenerla.
Nivel de evidencia: III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
Un paciente es refractario al tratamiento cuando después de haber excluido la no adherencia o la presencia de otra enfermedad causante de los signos y síntomas, se presenta más de una recaída en el curso de un año, a pesar de un manejo de mantenimiento adecuado con inmunomoduladores, anti-TNF u otros biológicos, o no responde a la terapia de inducción con corticoides o con NEE68,127,158.
En un reciente estudio de cohorte restrospectivo, de recaída de ECP luminal, se encontró que las siguientes variables se asociaron con la recaída clínica: sexo femenino, exposición a 5-ASA oral, uso de agentes inmunomoduladores y aumento de eosinófilos en biopsias intestinales, niveles altos de PCR y CF y niveles bajos de infliximab sérico158.
En niños se han documentado iguales resultados de los anti-TNF que en adultos, pero en ensayos clínicos no enmascarados.
Los inmunomoduladores AZA o 6-MCP no se deben utilizar en EC cuando se presentan recaídas o su comportamiento es refractario.
A pesar de la escasa evidencia de calidad, es necesario considerar que la EC que se inicia en la niñez tiene varias secuelas que no se ven en adultos, para las cuales se debe proceder de forma contundente. El impacto nutricional y el potencial riesgo de baja talla final es uno de los puntos a considerar. Otro es la progresión a formas incapacitantes, la mayor frecuencia de manejos quirúrgicos y los mayores índices de hospitalización, que nos deben mover a utilizar medicamentos de segunda línea, biológicos o inhibidores de la calcineurina, ciclosporina y tacrolimus para tratamientos más agresivos.
Pregunta 20. ¿Cuándo descontinuar el tratamiento en EIIP?
Afirmación 49: a la fecha se desconoce el momento apropiado para suspender el tratamiento cuando se ha logrado la remisión profunda sostenida de la EII. No existe evidencia que la soporte.
Nivel de evidencia: II.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Puntos prácticos
A pesar del riesgo de los efectos secundarios de las diferentes medicaciones, se ha intentado buscar el momento apropiado para dar por concluida su administración con resultados desalentadores. Las dificultades de diseño y el tiempo de observación de los pocos estudios en adultos dan porcentaje inaceptables de recaídas, que en promedio son del 30% al año y del 50% a los dos años. Incluso, en la mayoría de los estudios, recomiendan diferir la suspensión159,160.
Para pediatría la situación es más compleja. A la respuesta de cuándo retirar el tratamiento en EIIP, solo se encontraron dos trabajos. El primero de 2015, con 84 pacientes, contempla solamente EC con baja calidad del diseño. No es aleatorizado ni enmascarado y los desenlaces utilizados fueron muy débiles: disminución “significativa” del PCDAI, un puntaje endoscópico SES-CD, Simplified Endoscopic Activity Score for Crohn’s Disease y un año de seguimiento. Concluyó que probablemente se puede retirar el inmunomodulador a los seis meses de tratamiento cuando se da terapia combinada con infliximab. El segundo estudio, de marzo de 2021, contempla EC y CU, está en proceso con datos preliminares generales y anuncia una próxima publicación con resultados definitivos.
Pregunta 21. ¿Cuál es la seguridad y la efectividad del abordaje quirúrgico para el tratamiento de los pacientes pediátricos con EC?
Afirmación 50: se recomienda que la resección quirúrgica en niños con EC se reserve para aquellos que son refractarios a la terapia anti-TNF, para los que tienen enfermedad estenosante (B2) con dilatación preestenótica o enfermedad penetrante (B3). Para la mayoría de pacientes, la cirugía no es curativa.
Nivel de evidencia: I y II-1.
Nivel de recomendación: A.
Grado de acuerdo: 100%.
Puntos prácticos
La intervención quirúrgica en pacientes pediátricos con EC suele reservarse en el escenario de urgencias para pacientes con enfermedad activa con perforación con peritonitis o con sangrado no controlable68.
En el escenario electivo se reserva para pacientes con enfermedad estenosante asociada con obstrucción sin respuesta a manejo médico óptimo, enfermedad fistulizante que no responda a manejo médico.
Enfermedad intestinal de segmento corto sin respuesta total a manejo médico y pacientes prepuberales con segmento corto sin adecuada ganancia de peso y talla7,161.
Se debe considerar el abordaje inicial por laparoscopia siempre y cuando sea posible161.
Después de la resección ileocecal, los pacientes deben ser monitorizados por endoscopia seis a 12 meses después de la resección. El Rutgeerts Score se usa para valorar la severidad de la inflamación en el segmento “nuevo de íleon terminal”, predice la recurrencia endoscópica, pero no está validado en niños161.
Se deben evitar resecciones intestinales amplias en el intestino delgado y, en caso de estenosis múltiples, se prefiere la estricturoplastia161.
Se debe evitar la reconstrucción con bolsa (pouch) ileal en pacientes con EC conocida7.
En escenario electivo se debe optimizar el estado nutricional de los pacientes previo a ser llevados a procedimiento quirúrgico161.
En pacientes con alto riesgo de recurrencia, se recomienda el uso postoperatorio de agentes anti-TNF162.
Colitis ulcerativa pediátrica (CUP)
Pregunta 22. ¿Cuáles son las manifestaciones clínicas y extraintestinales para sospechar CUP?
Afirmación 51: la principal manifestación clínica para sospechar CUP es la diarrea con sangre, con presencia o no de dolor abdominal y síntomas rectoanales como pujo, tenesmo y urgencia defecatoria (Tabla 3).
Nivel de evidencia: II-2.
Recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
Además de lo descrito, los síntomas dependen de la extensión de la enfermedad, el fenotipo más frecuente al diagnóstico es la pancolitis. Con proctitis leve, el sangrado es leve e intermitente. Puede haber pérdida de peso e incluso perforación del colon en enfermedad severa más extensa4,20.
La presentación típica inicial es la diarrea sanguinolenta21.
La diarrea con sangre es más común en niños preescolares y escolares que en adolescentes (92% y 64%, respectivamente, OR 1,7; IC 0,83-3,4; p = 0,146)20.
El dolor abdominal es más severo, hay mayor compromiso del estado general, mayor presencia de fiebre en los escolares y adolescentes frente a preescolares.
En el momento del diagnóstico, la pancolitis es más frecuente en niños frente a adultos (81% vs. 34%; p <0,001). La proporción de proctitis es menor en niños vs. adultos (1,7% vs. 24%; p <0,001)20.
Las manifestaciones extraintestinales son menos frecuentes que en la EC (14% vs. 5%, p = 0,05)20) y también pueden afectar diferentes sistemas o regiones del cuerpo.
No existe compromiso perianal en la CU como sí lo hay en la EC (17% vs. 0%, p <0,0001)20.
Pregunta 23. ¿Debemos usar la clasificación de París de la CUP?
Afirmación 52: se recomienda utilizar la clasificación de París en la CUP, ya que puede contribuir a definir distintos subgrupos de pacientes con diferente pronóstico y con diferente enfoque terapéutico.
Nivel de evidencia: III.
Recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
La extensión de la enfermedad en pediatría es generalizada comprometiendo la totalidad del colon o casi su totalidad, por lo que la clasificación de París incluye una categoría adicional (E4) definiendo el compromiso de la enfermedad que se extiende desde el recto hasta proximal al ángulo hepático (Figura 5).
En la clasificación de París para CU se divide en dos categorías: S0 nunca severa y S1, que denota la presencia de enfermedad grave en cualquier momento en la historia del paciente (definida por una puntuación PUCAI ≥ 65).
Por otro lado, se ha definido EII de inicio muy temprano (< 6 años de edad en el momento del diagnóstico) y EII infantil (< 2 años de edad)163.
Pregunta 24. ¿Cuál es la utilidad de la endoscopia en el diagnóstico de CUP en niños con sospecha de EII?
Afirmación 53:
Se recomienda la realización de una ileocolonoscopia más una esofagogastroduodenoscopia para el diagnóstico de todos los pacientes pediátricos con sospecha inicial de EII. (Nivel de evidencia II-2; Grado de recomendación: B) (Figura 2).
La endoscopia debe ser utilizada en el seguimiento de los pacientes para garantizar la curación mucosa en CU asintomática; cuando la CF esté elevada, cuando se vayan a realizar cambios importantes en el manejo (estrategias de tratamiento de escalada y disminución), para diagnosticar complicaciones (por ejemplo, estenosis, displasia), para excluir otros diagnósticos como isquemia, infección (por ejemplo, citomegalovirus [CMV]) y para vigilancia de cáncer de colon. (Nivel de evidencia III).
Nivel de evidencia: II-III.
Recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
La esofagogastroduodenoscopia debe formar parte de la investigación de primera línea en todos los casos de sospecha de EII. La ausencia de síntomas gastrointestinales superiores específicos no excluye la presencia de inflamación gastrointestinal superior. (Nivel de evidencia III)164,165.
El diagnóstico incluye, excepto en situaciones de urgencia, la realización de endoscopia de vías digestivas altas y colonoscopia. Todo paciente con signos de alarma (diarrea con sangre, pérdida de peso, fallo de medro, dolor abdominal, etc), o sin signos de alarma pero con elevación de reactantes de fase aguda (VSG, PCR) o CF elevada debe ser llevado al estudio endoscópico para descartar enfermedad inflamatoria24,166.
La colonoscopia que incluye la intubación del íleon terminal y múltiples biopsias para histología obtenidas de todos los segmentos del tracto intestinal inferior, es esencial para diferenciar la EC de la CU e identificar la localización y extensión de la enfermedad27,37.
Deben obtenerse múltiples biopsias (> 2) representativas de cada segmento evaluado: de la endoscopia digestiva alta: esófago, estómago y duodeno; de la colonoscopia: íleon, ciego, colon ascendente, colon transverso, colon descendente, colon sigmoide y recto9.
El estudio endoscópico debe ser realizado por un gastroenterólogo pediatra con experiencia siempre bajo anestesia general o sedación profunda. Idealmente el niño debe recibir previamente una preparación de limpieza colónica adecuada para la edad167.
En colitis aguda severa, la colonoscopia total debe ser reservada para expertos; de lo contrario, la realización de sigmoidoscopia es suficiente y más segura para confirmar el diagnóstico167. Cuando hay una enfermedad activa grave, el valor de la colonoscopia completa se ve contrarrestado por un mayor riesgo de perforación intestinal. La enfermedad grave, el uso de esteroides, el sexo femenino y las dilataciones endoscópicas están asociados con un mayor riesgo de perforación (0,3% a 1%). En estos casos puntuales, la sigmoidoscopia flexible es más segura y la ileocolonoscopia debe posponerse hasta que las condiciones clínicas del paciente mejoren168.
En colitis aguda severa sin respuesta adecuada a tratamiento de inducción a las 72 horas se recomienda la realización de sigmoidoscopia con toma de muestras para estudio de Clostridioides y citomegalovirus, ya que los hallazgos típicos de pseudomembranas pueden no estar presentes11,24.
Las características macroscópicas típicas de la CU incluyen eritema, granularidad, friabilidad, exudados purulentos y úlceras que suelen aparecer pequeñas y superficiales. La inflamación puede terminar en una zona de transición en cualquier parte del colon o afectar a todo el colon de forma continua. La parte más distal del íleon terminal puede mostrar eritema o edema no erosivo si hay compromiso cecal y hay afectación de la válvula ileocecal, pero debe ser normal en todas las demás circunstancias. Típicamente la inflamación es más severa distalmente, excepto en los casos de preservación rectal macroscópica que ocasionalmente se observa en la CU10,11,169,170.
En el momento de la presentación, a diferencia de los adultos, del 10% al 34% de los niños con CU de nueva aparición carecen de las características histológicas de la colitis crónica11.
La CU de inicio pediátrico puede presentarse con fenotipos atípicos como preservación rectal macroscópica, úlceras gástricas aisladas no serpiginosas, arquitectura normal de las criptas, ausencia de cronicidad en las biopsias o parche cecal. Los pacientes con colitis aguda grave pueden tener inflamación transmural11.
Los estudios endoscópicos deben estar enfocados a completar los criterios de Porto para el diagnóstico y la clasificación adecuada de la enfermedad inflamatoria. Cuando un paciente haya iniciado tratamiento y este sea exitoso, no está indicado repetir los estudios endoscópicos para completar los criterios. Si existen diferencias entre el comportamiento clínico, los hallazgos endoscópicos y la histología los estudios endoscópicos deben repetirse para una adecuada caracterización de la enfermedad11.
La curación mucosa, que actualmente se considera el blanco de tratamiento en CU, debe comprobarse por endoscopia solo en pacientes con CU con discrepancia entre el PUCAI y los niveles de CF24.
En pacientes poscolectomía, la sospecha de pouchitis debe ser confirmada por evaluación endoscópica e histológica, ya que un síndrome de pouch irritable puede incrementar la frecuencia de las evacuaciones y producir dolor a pesar de pouch histológico y endoscópicamente normales24.
La endoscopia es actualmente el estándar para el diagnóstico y la evaluación de la actividad de la mucosa, la vigilancia de la displasia y la evaluación de la respuesta al tratamiento10,171.
Todos los pacientes con EII deben someterse a una colonoscopia de detección y vigilancia del cáncer colorrectal (CCR), la cual debe ser realizada por un endoscopista pediatra entrenado y debe incluir biopsias de reestadificación junto con la colonoscopia de detección a los ocho años después del inicio de los síntomas. Se deben evaluar factores de riesgo como la extensión de la enfermedad, la gravedad de esta durante el curso de la misma y los antecedentes familiares172.
Se recomienda utilizar cromoendoscopia de alta definición con biopsias dirigidas; con dos biopsias cada 10 cm en frascos separados más cualquier lesión sospechosa por separado. Si se utiliza la endoscopia de luz blanca, la recomendación es tomar cuatro biopsias por cada 10 cm de todo el colon, así como biopsias dirigidas de cualquier lesión visible173.
La vigilancia endoscópica es ampliamente recomendada por las sociedades gastrointestinales internacionales para la detección temprana y resección de displasia o CCR. Múltiples estudios de casos, controles y estudios de cohortes poblacionales han demostrado que la vigilancia endoscópica mejora la supervivencia relacionada con el CCR en pacientes con EII y con mayor riesgo de cáncer de colon174,175.
Aunque el intervalo de vigilancia óptimo no está bien definido y varía de uno a tres años, la presencia de factores de riesgo como inflamación activa, anomalías anatómicas como estenosis y múltiples pseudopólipos, antecedentes de displasia, antecedentes familiares de CCR en familiares de primer grado y la colangitis esclerosante primaria (CEP) merecen una vigilancia anual174.
Pregunta 25. ¿Qué índice endoscópico usaríamos en CUP?
Afirmación 54: el índice endoscópico de gravedad de la colitis ulcerosa (UCEIS) es un índice práctico, conveniente y validado que recomendamos usar de forma sistemática en todas las valoraciones endoscópicas de pacientes con CU.
Nivel de evidencia: II.
Recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
Un índice de calificación endoscópica mide la actividad de la enfermedad de acuerdo con los hallazgos evidenciados endoscópicamente. Los índices endoscópicos habitualmente utilizados incluyen el Baron Score, el Rachmilewitz Index, el Ulcerative Colitis Endoscopic Index of Severity, la Mayo Clinic Endoscopic Subscore y el Ulcerative Colitis Colonoscopic Index of Severity176.
El UCEIS fue desarrollado por Travis y colaboradores en 2012 como una herramienta para predecir con precisión la evaluación global de la gravedad endoscópica de la CU. Se encontró que la puntuación UCEIS se ve mínimamente afectada por la información clínica de la actividad de la enfermedad y está fuertemente correlacionada con los síntomas informados por el paciente10. Este índice consta de tres descriptores: patrón vascular (puntuado 0-2), sangrado (puntuado 0-3) con erosiones y úlceras (puntuado 0-3); para un puntaje máximo de 8 (Tabla 12)177.
El índice de Mayo tiene como ventaja que es ampliamente usado, sin embargo, no cuenta con una validación formal, no permite diferenciar entre úlceras superficiales y profundas, ni extensión de la enfermedad, además de contener índices subjetivos como la friabilidad24.
Es importante usar siempre un índice de calificación endoscópica en el diagnóstico y seguimiento endoscópico de los pacientes con CU. Aunque recomendamos el UCEIS por la menor variabilidad interobservador, es importante que el endoscopista escoja el índice que encuentre más fácilmente aplicable para garantizar su uso continuo.
La interpretación de los índices puede realizarse de la siguiente forma: curación mucosa significa la pérdida completa de la inflamación en la evaluación endoscópica referida como: UCEIS/Mayo=0. La remisión endoscópica se define como UCEIS/MAYO= ≤ 1. La respuesta endoscópica se refiere a un cambio en el puntaje de Mayo ≥ 1 y en UCEIS ≥ 224.
Tabla 12 Descriptores y definiciones del UCEIS (índice endoscópico de gravedad de la colitis ulcerosa)
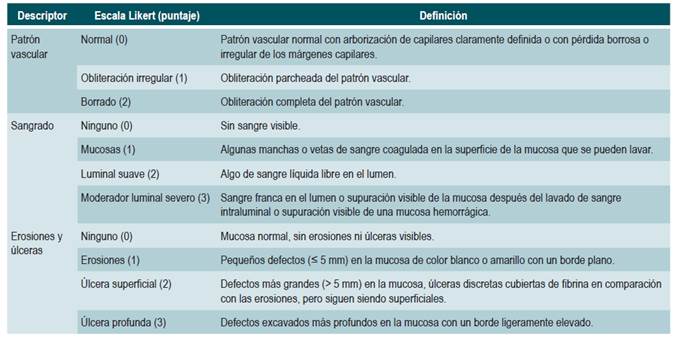
Adaptado de: Xie T, et al. Gastroenterol Rep. 2018;6(1):38-44(177) (https://www.mdapp.co/ulcerative-colitis-endoscopic-index-of-severity-uceis-score-calculator-608/).
Pregunta 26, ¿Cuál es la utilidad diagnóstica de los hallazgos histológicos para confirmar la presencia de CUP en pacientes con signos y síntomas sugestivos de EII?
Ver la sección de enfermedad de Crohn.
Pregunta 27. ¿Cuál es la utilidad de las imágenes en el diagnóstico de CUP en niños con sospecha de EII?
Ver la sección de enfermedad de Crohn.
Pregunta 28. ¿Cuál es la exactitud del PUCAI para determinar la actividad de la CUP en el diagnóstico y seguimiento?
Afirmación 55: el PUCAI de la historia de las últimas 48 horas ha demostrado ser válido y tiene una buena correlación con los puntaje endoscópicos, por lo que se recomienda que la actividad de la CUP se monitorice en cada control utilizando el PUCAI y el tratamiento debe revisarse cuando el PUCAI sea ≥ 10 puntos10,178.
Nivel de evidencia: I-II.
Recomendación: A.
Grado de acuerdo: 93,1%.
Puntos clave
La remisión clínica se define como PUCAI < 10 puntos, enfermedad leve de 10-34 puntos, enfermedad moderada de 35-64 puntos y enfermedad grave ³ 65 puntos. La respuesta clínicamente significativa se define por un cambio de PUCAI de al menos 20 puntos o al entrar en remisión (http://pucai.s3-website-us-west-2.amazonaws.com/).
La puntuación PUCAI < 10 diferenció muy bien a los pacientes con enfermedad activa frente a inactiva, con un área bajo la curva ROC (Receiver Operating Characteristic) de 0,99 (IC del 95%, 0,98 -1), sensibilidad del 97% y especificidad del 95%.
Puntajes en remisión por al menos tres meses después del diagnóstico predicen una remisión sostenida sin esteroides de un año y sin colectomía a los dos años.
Se recomienda medir la calprotectina durante la remisión clínica sostenida para verificar la cicatrización de la mucosa y seleccionar a aquellos que requieren evaluación endoscópica, ya que hasta el 20% de pacientes con PUCAI < 10 pueden tener lesiones.
Pacientes que requirieron esteroides endovenosos en el inicio de la enfermedad que no logren remisión (PUCAI < 10) cuatro semanas posteriores al egreso, podrían necesitar terapia adicional a la semana 1210,178.
Pregunta 29. ¿Cuál es la utilidad diagnóstica de las diferentes pruebas de laboratorio para establecer un diagnóstico diferencial, confirmarlo y establecer el seguimiento o el pronóstico de la CUP?
Ver la sección de enfermedad de Crohn.
Pregunta 30. ¿Cuáles son las intervenciones más efectivas y seguras para inducir la remisión y mantenimiento de la CUP leve, moderada o severa?
Uso de antibióticos
Afirmación 56: se recomienda que los antibióticos no se usen de forma rutinaria para la inducción o el mantenimiento de la remisión de la CUP.
Nivel de evidencia: III.
Recomendación: D.
Grado de acuerdo: 100%.
Puntos prácticos
Los antibióticos se han evaluado como terapia en CU, tanto en la inducción de la remisión y para prevenir las recaídas de la enfermedad. Así lo muestran así dos revisiones y metaanálisis, ambos incluyeron 9 estudios clínicos controlados y concluyeron que los antibióticos pueden mejorar los resultados en CU, pero que se requieren más estudios para confirmar este beneficio, ya que los ensayos clínicos incluidos fueron muy heterogéneos en su metodología y en el tipo de intervención metodológica10.
Los antibióticos pueden ser considerados cuando el Clostridiodes difficile u otras infecciones bacterianas son sospechadas, hasta tener confirmación por paraclínicos11.
¿Papel de la nutrición en la CUP?
Afirmación 57: las dietas de exclusión no deben usarse para inducir o mantener la remisión en la CUP y podrían conducir a deficiencias nutricionales. Se recomienda para promover la cicatrización de la mucosa, promover una nutrición adecuada y balanceada, ejercicio regular y evitar fumar.
Nivel de evidencia: III.
Nivel de recomendación: D.
Grado de acuerdo: 100%.
¿Papel de la nutrición y osteopenia en la CUP?
Afirmación 58: La osteopenia puede estar presente hasta en el 22% de pacientes con CUP, además de evitar los esteroides, se debe proporcionar un tratamiento eficaz que este dirigido a la cicatrización mucosa y control de la enfermedad. Se recomienda tratar a los pacientes cuya osteopenia esté asociada a deficiencia de vitamina D, ya que indica una enfermedad más activa.
Nivel de evidencia: II
Nivel de recomendación: B
Grado de acuerdo: 100%
Puntos prácticos
En pacientes con CUP dependientes de corticoides, desnutrición crónica, retraso puberal, amenorrea y enfermedad severa, se debe realizar un DEXA (dual energy x-ray absorptiometry), corregidos por edad, talla y sexo, para el diagnóstico de osteopenia.
Cumplir los requerimientos de calcio para la edad, el ejercicio con pesas, evitar el cigarrillo y en deficiencia de vitamina D, las suplementación diaria de 2000 UI de vitamina D o el uso de dosis de carga son estrategias suficientes en la mayoría10,180,181.
¿Cuál es la evidencia del papel de la nutrición enteral en el mantenimiento en CUP?
Afirmación 59: la evidencia disponible hasta el momento no soporta el uso de la NEE en el mantenimiento de pacientes con colitis ulcerativa. La NE parece segura y puede recomendarse como terapia de apoyo de acuerdo con la práctica nutricional estándar en pacientes con CU grave.
Nivel de evidencia: III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
En caso de intolerancia a la vía oral, iniciar soporte NE. La nutrición parenteral está indicada en caso de intolerancia a la NE, en presencia de dilatación colónica o en caso de cirugía inminente15,82.
El soporte nutricional parenteral se recomienda como primera línea en casos de megacolon con cirugía inminente y dilatación prolongada del intestino11,81.
¿Aminosalicilatos y enemas?
Afirmación 60:
Los salicilatos orales se recomiendan como terapia de inducción y mantenimiento de primera línea para la CUP leve a moderada. (Nivel de evidencia: II).
El tratamiento combinado de aminosalicilatos por vía oral y rectal es más eficaz que la monoterapia por vía oral. (Nivel de evidencia: II).
La monoterapia rectal debe reservarse para la proctitis ulcerativa con actividad leve a moderada. (Nivel de evidencia: II).
Ante un episodio de colitis aguda severa todas las preparaciones de mesalazina (orales y rectales) deben suspenderse para excluir la intolerancia, especialmente cuando su uso corresponde a semanas anteriores; la reintroducción debe considerarse después de una mejoría significativa. (Nivel de evidencia: III).
Nivel de evidencia: II.
Nivel de recomendación: B.
Nivel Grado de acuerdo: 100%.
Puntos prácticos
Ningún compuesto específico de 5-ASA fue superior para inducir la remisión, aunque la sulfasalazina fue estadísticamente superior a otros compuestos de 5-ASA para el mantenimiento de la remisión10.
Los supositorios de mesalazina son útiles para la proctitis limitada, mientras que los enemas de espuma y líquidos también son adecuados en colitis más extensas10. La terapia rectal (supositorios) está indicada para la proctitis ulcerativa182.
Al utilizar terapia rectal, se prefiere el 5-ASA a los esteroides10.
La dosis sugerida es: mesalazina oral de 60 a 80 mg/kg/día (1 a 4,8 g día); mesalazina rectal 25 mg/kg hasta 1 g diario; sulfasalazina 40 a 70 mg/kg/día (1 a 4 g día). Dosis rectales más altas, de hasta 4 g, no son más eficaces10,11,183,184.
La dosis de 5-ASA una vez al día puede considerarse para la inducción de la remisión y para el mantenimiento10) con tasas de respuesta clínica y remisión adecuadas185.
El aumento gradual de la dosis de sulfasalazina durante siete a 14 días puede mitigar los efectos secundarios dependientes de la dosis10,11,183,184.
La dosis de inducción efectiva debe continuarse también como dosis de mantenimiento. La reducción de la dosis, dentro del rango de dosis sugerido, puede considerarse después de varios meses de remisión sostenida10.
La mayoría de los niños con CUP leve a moderada no alcanzarán la remisión con la monoterapia de mesalamina oral sola. Se debe considerar la modificación del tratamiento en aquellos que no muestren una respuesta inicial significativa en dos o tres semanas10.
La intolerancia aguda a la mesalazina puede presentarse como una exacerbación de la CUP, usualmente en el primer mes de tratamiento. Los síntomas se resuelven a los pocos días de suspender el tratamiento. La recurrencia en la reexposición es diagnóstica y excluye su uso futuro, los síntomas suelen aparecer también tras la administración rectal10,11,183,184.
El control regular de recuentos sanguíneos, función renal y uroanálisis, aunque no está respaldado por la evidencia, continúa realizándose en la práctica médica186.
Los efectos adversos con el uso de 5-ASA son infrecuentes, como efectos leves se describen reacción alérgica, cefalea y síntomas gastrointestinales; dentro de los efectos graves se incluyen complicaciones renales, pancreáticas, pulmonares y cardíacas183.
Se requiere de un período de dos semanas de manejo con 5-ASA antes de considerar a un paciente como no respondedor184.
¿Uso de corticoides en CUP?
Afirmación 61:
Se recomiendan los corticosteroides orales como tratamiento de segunda línea para la CUP leve a moderada que no responde a 5-ASA (oral y/o rectal) y pueden considerarse como la primera línea en el extremo superior del rango de enfermedad moderada. (Nivel de evidencia: III).
La CUP grave debe tratarse con corticosteroides endovenosos. (Nivel de evidencia: II).
Los corticosteroides orales de segunda generación con efecto sistémico menor, como el dipropionato de beclometasona (Nivel de evidencia: II) y la budesonida-MMX (la evidencia de budesonida-MMX es de apoyo solo para colitis izquierda; Nivel de evidencia: III), puede considerarse en pacientes con enfermedad leve refractaria a 5-ASA previo a prednisolona oral.
No se recomiendan los esteroides para mantenimiento de la remisión; las estrategias de ahorro de esteroides deben ser aplicadas. (Nivel de evidencia: III).
Nivel de evidencia: II-III.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
La dosis diaria recomendada de prednisolona/prednisona es de 1 mg/kg (máximo de 40 mg/día) una vez al día durante dos a tres semanas, seguida de un período de disminución gradual de hasta ocho a diez semanas (Tabla 13). La administración de corticosteroides una vez al día por la mañana es tan eficaz como la misma dosis administrada en múltiples dosis divididas. El riesgo de exacerbación es menor con dosis de prednisolona superiores a 20 mg, pero el riesgo de reacciones adversas es mayor. Se recomienda una reducción más rápida hasta los 20 mg. Acortar cada etapa de siete a cinco días o cualquier otra modificación de la reducción debe individualizarse. La meta es descontinuar los corticosteroides en la semana 1010.
Después de las primeras dos a tres semanas si el PUCAI está entre 15 a 30 se debe considerar la posibilidad de mantener la dosis estable; si el PUCAI es > 35 se debe aumentar el corticosteroide hasta la dosis de los pasos uno o dos anteriores durante una semana y luego reiniciar el destete lentamente; si el PUCAI es > 60 o hay un aumento del PUCAI en 20 puntos en cualquier momento se debe escalar el tratamiento, después de excluir otras causas de enfermedad refractaria a los corticosteroides10. Los estudios sobre corticosteroides orales para el tratamiento de niños con CU activa informan de tasas de remisión a corto plazo (uno a tres meses) del 50% al 64%187 y al año del 49% al 61%188,189.
La dosis de metilprednisolona endovenosa es de 1 mg/kg (hasta 40 mg/día) una vez al día por la mañana como tratamiento inicial; una dosis mayor de 1,5 mg/kg (hasta 60 mg/día) en una o dos dosis diarias divididas debería reservarse para los casos más graves o para los niños a los que les hayan fallado los corticosteroides orales previo al ingreso. No hay pruebas contundentes de que la dosis más alta sea superior a la dosis más baja, por lo que debe realizarse un descenso rápido de la metilprednisolona a 1 mg/kg (40 mg/día) una vez que se haya observado la respuesta. La infusión continua de este no tiene ninguna ventaja sobre la administración en bolo190,191. La metilprednisolona, por su menor efecto mineralocorticoide, es preferible que la hidrocortisona11.
Los corticosteroides endovenosos conducen a una mejoría clínica en el 70% de los pacientes con CUP aguda severa y reducen la tasa de mortalidad165-167.
Se puede considerar el uso de corticosteroides orales en CUP grave (PUCAI 65) en pacientes que se encuentren hemodinámicamente estables y con valores de laboratorio normales o casi normales10.
Las recomendaciones del uso de los corticosteroides de segunda generación (dipropionato de beclometasona y budesónida-MMX) se extrapolan de estudios en adultos. Proporcionan una mejor tasa de inducción a la remisión en la CU192. La budesónida-MMX se utiliza principalmente en CU leve a moderada en quienes el tratamiento de inducción con 5-ASA fue fallido o pobremente tolerado para evitar el tratamiento con corticosteroides sistémicos193,194. Tienen un perfil de seguridad y tolerabilidad más favorable que los corticosteroides sistémicos192. La budesónida-MMX se asoció a concentraciones medias de cortisol normales y a una menor incidencia de efectos adversos195.
La budesónida-MMX en la CUP es eficaz y bien tolerada, puede considerarse como la alternativa a los corticosteroides convencionales para inducción de remisión y como segunda línea después del 5-ASA en la exacerbación leve a moderada, incluso con antecedentes de reagudización grave y tratamiento con inhibidores de la calcineurina y/o agentes biológicos193.
El término dependencia de corticosteroides se aplica a pacientes que no pueden dejar de tomar corticosteroides dentro de los tres meses sin enfermedad activa recurrente, o que tienen una recaída que requiere corticosteroides dentro de los tres meses posteriores a la interrupción de estos10. Se debe evitar la dependencia de los esteroides aumentando oportunamente el tratamiento de mantenimiento cuando sea necesario10. La dependencia de los corticosteroides resulta ser mayor en los niños que en los adultos (45% frente al 8%). Las estrategias para evitar la dependencia de los esteroides incluyen la optimización del 5-ASA, la terapia adyuvante con enemas y el escalonamiento a tiopurinas o biológicos196.
Las dosis altas de corticosteroides y la duración prolongada del tratamiento (> 3 meses) se han asociado con la aparición de supresión suprarrenal en el 20% de los niños con EII10. Si se presentan síntomas de supresión suprarrenal (debilidad/fatiga, malestar, náuseas, vómitos, diarrea, dolor de cabeza, artralgia y dolor abdominal) durante el retiro de los corticosteroides, la insuficiencia suprarrenal debe excluirse mediante la medición de niveles séricos de cortisol a las 08:00 a. m. y debe tener acompañamiento del endocrinólogo. Se debe considerar la posibilidad de insuficiencia suprarrenal incluso muchos meses después de la reducción de los esteroides10.
Tabla 13 Esquema de reducción gradual de esteroides (dosis mg/día equivalente de prednisolona/prednisona)
| Semanas | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 60 | 50 | 40 | 35 | 30 | 25 | 20 | 15 | 10 | 5 |
| 50 | 45 | 40 | 35 | 30 | 25 | 20 | 15 | 10 | 5 |
| 45 | 40 | 40 | 35 | 30 | 25 | 20 | 15 | 10 | 5 |
| 40 | 40 | 40 | 35 | 30 | 25 | 20 | 15 | 10 | 5 |
| 35 | 35 | 35 | 30 | 25 | 20 | 15 | 15 | 10 | 5 |
| 30 | 30 | 30 | 25 | 20 | 15 | 15 | 10 | 10 | 5 |
| 25 | 25 | 25 | 20 | 20 | 15 | 15 | 10 | 5 | 5 |
| 20 | 20 | 20 | 15 | 15 | 12,5 | 10 | 7,5 | 5 | 2,5 |
| 15 | 15 | 15 | 12,5 | 10 | 10 | 7,5 | 7,5 | 5 | 2,5 |
Iniciar prednisona a 1 mg/kg hasta 40 mg al día (después de hospitalización por colitis aguda grave, la dosis puede ser de hasta 60 mg/día). Adaptada de: Turner D, et al. J Pediatr Gastroenterol Nutr. 2018;67(2):257-9110.
¿Uso de inmunomoduladores en el mantenimiento de CUP?
Afirmación 62: no se recomienda la AZA y su metabolito, la 6-MCP, para inducir la remisión.
Nivel de evidencia: II.
Nivel de recomendación: B.
Grado de acuerdo: 96,6%.
Puntos prácticos
AZA y 6-MCP, por su farmacocinética que garantiza niveles adecuados del medicamento en sangre solo hasta las ocho a diez semanas, no tiene ninguna utilidad en la inducción de la remisión. Se debe dar en una sola dosis en la mañana, pero se puede mejorar la tolerancia y disminuir la hepatotoxicidad dándolas cada 12 horas. En caso de efectos adversos, se puede cambiar de AZA a 6-MTP o viceversa. Se recomienda la cuantificación de metabolitos de AZA y 6-MTP en pacientes con leucopenia, o con respuesta inadecuada y elevación de enzimas hepáticas. Para identificar mielosupresión es útil la determinación del genotipo-fenotipo de la tiopurina metiltransferasa (TPMT). En heterocigotos, se debe bajar la dosis de AZA a 6-MTP y suspenderla en homocigotos o en pacientes con muy baja actividad. Si no hay posibilidad de tipificar el feno/genotipo de la TPMT, ni los niveles de 6-TGN se deben cuantificar enzimas hepáticas y conteo de glóbulos rojos cada dos semanas en el primer mes, cada mes en los siguientes dos meses y en adelante cada tres meses. Se recomienda protección solar.
Mantenimiento en CUP
Afirmación 63: cuando el paciente se encuentra con un adecuado tratamiento con 5-ASA y presenta por lo menos dos recaídas al año, o ha hecho intolerancia, se recomienda el uso de AZA o su metabolito 6-MCP para mantener la remisión.
Nivel de evidencia: II.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
La eficacia de las tiopurinas para mantener la remisión en CUP es evidente con muchos estudios retrospectivos en adultos, pero es limitada en niños con solo dos estudios prospectivos. En el primero se demuestra que una vez iniciadas las tiopurinas, el paciente se mantiene en remisión en el curso del primero y segundo año, en promedio en un 50%, y progresivamente baja a 37%, 27% y 13% al tercer, cuarto y quinto año, respectivamente68. El segundo estudio, que compara la administración temprana y tardía con un número menor de pacientes, demuestra una remisión del 72% y 73% a los dos años de seguimiento, respectivamente, pero es llamativo que este porcentaje se mantuvo prácticamente igual durante los dos años de observación, contrario al primero que disminuyó progresivamente74. En lo que sí coinciden los dos estudios es que estos resultados fueron independientes de género, extensión y severidad endoscópicas, uso previo o concomitante de 5-ASA o duración de los corticoides. Igualmente concluyeron que el uso de tiopurinas disminuía la probabilidad de terapia de rescate con inhibidores de la calcineurina, biológicos o la realización de colectomía, por lo menos en los cinco y dos años de observación, respectivamente.
Como los corticoides en niños no se tienen en cuenta en esta guía para mantenimiento en ningún caso de CUP, no se evalúan tiopurinas contra corticodependencia/corticorresistencia. El uso de corticoides en niños, distinto a los adultos, se debe limitar a la inducción de la remisión solo en aquellos casos severos con PUCAI ≥ 6510. Los corticoides, como se sabe, son excelentes como antiinflamatorios y han demostrado su utilidad para inducir una rápida remisión de los síntomas agudos en EII, pero los efectos secundarios y las secuelas en niños, osteoporosis, retardo del crecimiento, cataratas, glaucoma, riesgo aumentado de trombosis, hipertensión arterial, síndrome de Cushing, enfermedad ulcerosa y supresión adrenal, entre otros, inhabilitan su uso en menores de 18 años. Adicionalmente los pobres resultados en EII y la corticodependencia/corticorresistencia hacen que su uso no tenga indicación en el mantenimiento de la remisión10,11,68,78.
Afirmación 64: AZA y 6-MTP son más efectivas que las 5-ASA para mantener la remisión, pero deberían reservarse como medicación posterior si llegan a fallar las 5-ASA.
Nivel de evidencia: II.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
Las tiopurinas son más efectivas que las 5-ASA. En adultos es notable la evidencia con metaanálisis y ensayos aleatorizados y controlados a favor de las tiopurinas comparadas con las 5-ASA68. Estudios similares no existen en pediatría, pero se deben tener en cuenta los de adultos, hasta que la experimentación se haga en población pediátrica.
En casos de CU leve y aún en moderada, se debe iniciar el tratamiento con 5-ASA y escalar el manejo a tiopurinas en el momento en que se compruebe la falla de las 5-ASA, con la finalidad de no agotar sus ventajas. A pesar de no pasar de observaciones aisladas, parece que la combinación de estas dos clases de medicamentos tiene efectos sumatorios. Los 5-ASA, al inhibir la tiopurina metiltransferasa, incrementa los niveles de 6-tioguanina nucleótido mejorando los efectos de la tiopurinas159. A esta característica debe sumarse la acción antineoplásica comprobada de los 5-ASA, que en numerosos estudios experimentales y metaanálisis ha demostrado disminuir el riesgo de carcinoma colorectal asociado a CU10.
Mantenimiento en CU severa
Afirmación 65: AZA y 6-MTP se podrían considerar al egreso luego de un episodio de colitis aguda severa cuando la respuesta a corticoides intravenosos fue efectiva.
Nivel de evidencia: III.
Nivel de recomendación: B .
Grado de acuerdo: 100%.
Puntos prácticos
Luego de un episodio de colitis aguda severa, la efectiva y rápida acción de los corticoides intravenosos en los primeros siete días marcarán la probabilidad de usar AZ o 6-MP para mantener la remisión. En varios estudios en adultos y uno solo en niños con muy pocos pacientes se ha demostrado la eficacia de las tiopurinas sobre los salicilatos para mantener la remisión en el primer año. El estudio de pediatría con 16 pacientes no es suficiente para afirmar la superioridad de las tiopurinas, y es necesario hacer observaciones con un número suficiente de niños68. Los porcentajes de remisión mejoran y se extienden a los primeros dos años, disminuyendo la probabilidad de terapias de rescate y la frecuencia de colectomía cuando se mejora la efectividad de la tiopurinas dando, simultáneamente, salicilatos.
¿Uso de biológicos en CUP?
¿Es eficaz el infliximab en la inducción de la remisión del paciente con brote moderado de CU en paciente que ha fallado a otras terapias convencionales?
Afirmación 66:
Se recomienda el uso del infliximab en CU crónicamente activa dependiente de esteroides, no controlada por 5-ASA y tiopurinas, tanto para la inducción como para el mantenimiento de la remisión.
El infliximab debe considerarse en CU crónica con actividad o dependiente de esteroides, no controlada por 5-ASA y tiopurinas, tanto para la inducción como para el mantenimiento de la remisión.
Se recomienda utilizar infliximab preferiblemente en combinación con un inmunomodulador (IMM) (siendo la mayor evidencia en CU las tiopurinas) para reducir la probabilidad de desarrollar anticuerpos contra infliximab (ATI) y en pacientes sin tiopurina para mejorar la eficacia. Se puede considerar la interrupción de la IMM después de seis meses, especialmente en niños, preferiblemente después de asegurar un nivel mínimo de infliximab > 5 mcg/mL, ya que los niveles pueden disminuir después de suspender la IMM.
Nivel de evidencia: I.
Nivel de recomendación: A.
Grado de acuerdo: 96,6%.
La evidencia pediátrica sobre adalimumab en la CU sigue siendo escasa y se limita a dos pequeños estudios retrospectivos en pacientes que experimentaron una pérdida de respuesta secundaria a infliximab. En estos dos estudios, la respuesta a la terapia anti-TNFα se recuperó en el 55% al 80% de los pacientes, con una remisión clínica mantenida durante una mediana de seguimiento de dos años197-200.
Terapia combinada frente a monoterapia
El beneficio potencial de la terapia combinada se demostró por primera vez en el histórico ensayo SONIC, que mostró tasas más altas de remisión clínica y endoscópica con el uso de infliximab en combinación con una tiopurina (57% frente a 44%; p = 0,02).
Un análisis post hoc del ensayo SONIC encontró que entre los pacientes con concentraciones séricas mínimas similares de infliximab, la terapia combinada no fue significativamente más efectiva que el infliximab solo. Aunque el uso de la terapia combinada se asoció con un menor riesgo de inmunogenicidad, no se demostró una diferencia significativa en las tasas de remisión clínica entre la terapia combinada y la monoterapia. Los beneficios del uso de la terapia combinada deben sopesarse con la posibilidad de tasas más altas de eventos adversos como infección, malignidad y toxicidad. En la EIIP, el uso de la terapia combinada puede ser apropiado en niños que presenten un mayor riesgo de complicaciones de la enfermedad, niños con pérdida de respuesta inmunogénica a la terapia anti-TNFα previa o niños que pueden beneficiarse del efecto sinérgico entre los dos agentes. Finalmente, la suspensión de los inmunomoduladores después de seis meses en pacientes que alcanzan niveles terapéuticos del fármaco se ha recomendado como el momento óptimo para lograr beneficios a largo plazo201.
Nivel de evidencia: II-2.
Nivel de recomendación: B.
Grado de acuerdo: 96,6%.
Vedolizumab
Vedolizumab es una molécula de receptor de integrina anti-α4β7 humanizado, que inhibe el tráfico de linfocitos hacia el intestino al interferir con la capacidad de los linfocitos para unirse a la molécula de adhesión celular de direccionamiento de la mucosa-1 (MAdCAM-1).
La evidencia pediátrica se limita a estudios pequeños, prospectivos, observacionales y retrospectivos, así como informes de datos de seguimiento abiertos a largo plazo. Usando una dosificación adaptada de 5 mg/kg hasta 300 mg, estos estudios pediátricos combinados informaron tasas de remisión clínica en las semanas 14 y 22 de 37% a 76% y 34% a 71%, respectivamente, en una población heterogénea de pacientes. De manera similar a lo que se observa en las cohortes de adultos, las tasas de remisión han sido numéricamente más altas en la CU en comparación con la EC y en los niños sin experiencia previa con anti-TNFα en comparación con los pacientes con exposición previa. En una cohorte retrospectiva publicada recientemente, vedolizumab también demostró inducir la cicatrización de la mucosa (puntuación compuesta de remisión endoscópica e histológica) a una tasa del 38%.
Los datos de seguridad sobre el uso de vedolizumab en niños son limitados. En la serie de casos multicéntrica más grande de 64 niños, el Grupo de Oporto de EIIP de ESPGHAN no informó eventos adversos graves en una mediana de seguimiento de 24 semanas157,202-204.
Nivel de evidencia: II-3.
Nivel de recomendación: C.
Grado de acuerdo: 96,6%.
Ustekinumab
Ustekinumab es un anticuerpo monoclonal humano dirigido a la subunidad p40 común de la interleucina (IL) 12 e IL-23; han surgido nuevos datos sobre el uso de anti-IL-12/23 para la CU del ensayo UNIFI de fase 3. El uso no autorizado de ustekinumab en la población pediátrica está en aumento. Sin embargo, la evidencia de su eficacia y seguridad en este grupo de edad se limita a tres estudios de cohortes observacionales en niños con EC refractarios a las terapias anti-TNFα. Recientemente, Dayan y sus colegas destacaron una mayor eficacia entre los pacientes sin tratamiento previo con productos biológicos en comparación con los pacientes expuestos a productos biológicos (90% frente a 50%; p = 0,03) en un estudio observacional que incluyó a 52 niños y adultos jóvenes. Fusillo y colegas, en un análisis preliminar de una cohorte prospectiva de 20 pacientes pediátricos expuestos a productos biológicos, incluidos 16 con EC, describieron una respuesta clínica en el 52% de los pacientes en la semana 6 y en el 45% en una mediana de seguimiento de 26 semanas. Se informaron resultados similares a largo plazo a los 12 meses en una cohorte retrospectiva separada de 44 pacientes pediátricos. En general, estos resultados sugieren que ustekinumab es eficaz en pacientes pediátricos con EII, pero se requerirán estudios de cohortes más grandes para validar la eficacia, el perfil de seguridad y el régimen de dosificación optimizado en esta población205-207.
Puntos prácticos
Considerar adalimumab o golimumab en aquellos que inicialmente responden, pero luego pierden la respuesta o son intolerantes a infliximab, basados en los niveles séricos y los anticuerpos. Adalimumab y el golimumab no tienen ninguna función en los pacientes con falta de respuesta primaria a infliximab.
Vedolizumab debe considerarse en pacientes crónicamente activos o dependientes de esteroides como terapia biológica de segunda línea después de la falla del anti-TNF.
En pacientes ambulatorios con CU, el infliximab debe administrarse inicialmente a 5 mg/kg por dosis (en las semanas 0, 2 y 6 seguidas de 5 mg/kg cada ocho semanas para el mantenimiento). Se debe considerar una dosis inicial más alta en niños con bajo peso corporal (< 30 kg) o IMC alto, y en presencia de mayor carga inflamatoria e hipoalbuminemia. Los niveles mínimos objetivo después de la inducción (semana 14) y las dosis posteriores se informan en diferentes estudios como > 4 a 5 mcg/mL. La infusión rápida (1 hora) parece tan segura y eficaz como las infusiones más lentas tradicionales, si las dosis de inducción se toleraron bien y la dosis es estable.
La utilidad de la combinación de adalimumab, golimumab y vedolizumab con tiopurinas es más controvertida y se prescribe con mayor frecuencia como monoterapia en niños.
Las dosis recomendadas de golimumab para la inducción son 200 mg en la semana 0, seguidas de 100 mg en la semana 2 para los que pesan > 45 kg. Los niños con menor peso deben recibir la dosis en función de la superficie corporal (115 y 60 mg/m2 en las semanas 0 y 2). Las dosis de mantenimiento cada cuatro semanas son de 60 mg/m2 si el peso es < 45 kg y de 100 mg si el peso es de 45 kg. Los niveles mínimos objetivo durante el mantenimiento son > 2 mg/mL. En Colombia no está autorizado
Extrapolando de la ECP, el adalimumab debe iniciarse con 160 mg, seguido de 80 mg después de dos semanas y luego 40 mg cada dos semanas en adolescentes con peso > 40 kg. No se ha definido bien la dosificación óptima en niños más pequeños, pero se podría considerar la dosificación basada en área de superficie corporal (BSA) con 92 mg/m2, seguido de 46 mg/m2 y 23 mg/m2 cada dos semanas para el mantenimiento). Los niveles objetivo de adalimumab durante el mantenimiento se informan en diferentes estudios como > 5 a 8 mcg/mL.
La medición de los niveles de fármaco y de anticuerpos antidroga después de la inducción (es decir, en la semana 14 de infusión para infliximab y entre ocho y 10 semanas para adalimumab) puede ayudar a optimizar el tratamiento. La medición de los niveles del fármaco también es útil en la evaluación de la respuesta insatisfactoria al anti-TNF para guiar el aumento de la dosis, acortando el intervalo o el cambio a otro biológico.
La dosificación estándar de vedolizumab en adultos se ha adaptado en estudios pediátricos (5 mg/kg hasta 300 mg por dosis en las semanas 0, 2, 6 y posteriormente cada ocho semanas). Para aquellos que pesan < 30 kg, se requiere una dosis más alta por kilogramo, pero se puede preferir el cálculo basado en BSA (es decir, 177 mg/m2). Se ha descrito que el efecto de vedolizumab en la CU se produce en la semana 6 de tratamiento, pero la respuesta completa puede no ser aparente hasta la semana 14. Puede ser necesario acortar el intervalo entre infusiones a cuatro semanas durante el mantenimiento en pacientes con respuesta parcial. En Colombia no está autorizado.
Nivel de evidencia: II-III.
Nivel de recomendación: C .
Grado de acuerdo: 96,6%.
Uso de tacrolimus en CUP
Afirmación 67: se recomienda que el tacrolimus oral (FK-506) sea considerado en pacientes ambulatorios como otra opción a los esteroides para pasar a las tiopurinas o vedolizumab (dado el mayor tiempo de inicio de acción). En pacientes con proctitis ulcerosa refractarios o intolerantes a las terapias tópicas de mesalamina y esteroides, se puede usar tacrolimus rectal (0,07 mg/kg/día; dosis máxima en adultos de 3 mg/día).
Nivel de evidencia: III.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Puntos prácticos
Debe lograrse inicialmente un nivel alto en suero (10 a 15 ng/mL), con una disminución progresiva y titulación gradual a niveles mínimos más bajos (5 a 10 y posteriormente de 2 a 5 ng/mL) para evitar eventos adversos graves. Pacientes seleccionados pueden beneficiarse de un tratamiento a largo plazo con dosis más bajas (objetivo: 2 ng/mL), considerando la posible toxicidad y la limitada evidencia en niños, ya que muchos terminan en colectomía10,211,212.
Otros: trasplante de microbiota, probióticos, cúrcuma, aféresis
Aféresis
Afirmación 68: se recomienda que la aféresis de granulocitos/monocitos no sea usada de forma rutinaria en pacientes con CUP.
Puntos prácticos
La aféresis actúa mediante la eliminación extracorpórea de leucocitos y otras células del sistema inmunológico (granulocitos, granulocitos/monocitos) a través de un sistema de adsorción de perlas de acetato de celulosa o una fibra filtro de poliéster.
En población pediátrica se sugiere una posible eficacia en niños con CU corticodependiente como corticorresistente. Las tasas de respuesta reportadas se encuentran entre el 60% y el 85%, siendo estudios de casos o cohortes pequeños213-216. Las preocupaciones sobre una calidad metodológica de los estudios identificados impiden un metaanálisis riguroso y conclusiones definitivas217. En consecuencia, se requieren ensayos controlados aleatorios de alta calidad para explorar el valor clínico genuino de la aféresis en el tratamiento de pacientes con EII10,191.
Nivel de evidencia: III.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Probióticos
Afirmación 69: se recomienda que los probióticos: VSL#3, Escherichia coli Nissle 917 sean considerados como tratamiento complementario en la CUP leve.
Puntos prácticos
Se ha evaluado el uso de probióticos para la inducción y el mantenimiento de la remisión en pacientes con CU. En un ensayo pediátrico se encontró que la cepa E. coli Nissle 1917 puede ser tan eficaz como la mesalazina en el mantenimiento de remisión10,218,219. La dosis utilizada fue de 200 mg/día (100 mg contienen 25 x 109 bacterias E. coli viables) administradas como cápsulas.
Una revisión sistemática y un metaanálisis sugieren que E. coli Nissle 1917 es equivalente a la mesalazina en cuanto a prevención de recaídas, mientras que su eficacia es comparable al placebo en la inducción de la remisión220.
VSL#3
Esta multicepa probiótica contiene ocho cepas bacterianas (Lactobacillus paracasei DSM 24733, Lactobacillus plantarum DSM 24730, Lactobacillus acidophilus DSM 24735, Lactobacillus delbrueckii subespecie bulgaricus DSM 24734, Bifidobacterium longum DSM 24736, Bifidobacterium infantis DSM 24737, Bifidobacterium breve DSM 24732 y Streptococcus thermophilus DSM 24731). Un pequeño ensayo aleatorio controlado con placebo de 29 niños tratados con 5-ASA y la combinación de VSL#3 fue superior al placebo en la inducción y el mantenimiento de la remisión a un año10,221. Un pequeño estudio abierto en 18 niños con CU leve a moderada evaluó la eficacia de VSL#3 añadido a la terapia estándar, observándose una tasa de remisión del 56%222.
En la Tabla 14, la dosificación de VSL#3 se recomienda de la siguiente manera:
Tabla 14 Dosificación de VSL#3
| Edad (años) | Peso (kg) | Dosis diaria |
|---|---|---|
| 4-6 | 17-23 | 1 sachet (450 billones UFC) |
| 7-9 | 24-33 | 2 sachets (900 billones UFC) |
| 11-14 | 34-53 | 3 sachets (1350 billones UFC) |
| 15-17 | 54-66 | 4 sachets (1800 billones UFC) |
UFC: unidades formadoras de colonias. Adaptado de: Turner D, et al. J Pediatr Gastroenterol Nutr. 2018;67(2):257-9110.
Una revisión realizada recientemente por Cochrane concluye que existe una certeza de evidencia baja respecto al uso de probióticos y la inducción de remisión clínica en CU activa en comparación con el placebo e igualmente comparado con el uso de 5-ASA. Tampoco existe evidencia de si los probióticos son efectivos en personas con enfermedad grave y más extensa, o si las preparaciones específicas son superiores a otras. Se necesitan más ECA dirigidos y diseñados adecuadamente, en particular, se necesita una potencia adecuada de los estudios, tamaños de muestra más grandes y la necesidad de minimizar el riesgo de sesgo223.
Nivel de evidencia: II-2 y II-3.
Nivel de recomendación: C.
Grado de acuerdo: 96,6%.
Probióticos y pouchitis
Afirmación 70: se recomienda el uso de cepas probióticas como el VSL#3 en la prevención y el mantenimiento de la remisión de la pouchitis.
Nivel de evidencia: II.
Nivel de recomendación: B.
Grado de acuerdo: 96,6%.
Puntos prácticos
La pouchitis, o inflamación dentro del reservorio ileal, puede ocurrir hasta en el 60% de los pacientes con CU después de una anastomosis anal de la bolsa ileal. La pouchitis puede provocar síntomas de urgencia, aumento de la frecuencia de las deposiciones y dolor.
Los datos más sólidos para respaldar el uso de los probióticos en EII se encuentran en la pouchitis y, en particular, para el uso de VSL#3, tanto en la prevención primaria de la pouchitis después de la anastomosis anal de la bolsa ileal como en el mantenimiento de la remisión después del tratamiento antibiótico exitoso de la pouchitis aguda224.
Se encontró que VSL#3 era superior al placebo para mantener la remisión en pacientes con pouchitis aguda tratados con éxito con antibióticos. Además se observó una remisión sostenida de un 85% de los pacientes tratados con VSL#3 en comparación con el 0% al 6% del placebo en dos EAC225,226. La administración de VSL#3 se ha asociado con una reducción de mediadores proinflamatorios, aumento en las células T reguladoras de la mucosa entérica227, mejora de la función de barrera y aumento de la diversidad bacteriana intestinal228.
Cúrcuma
Afirmación 71: la cúrcuma se podría considerar como una terapia complementaria para mantener la remisión clínica de los pacientes con CU leve a moderada.
Nivel de evidencia: II.
Nivel de recomendación: C.
Grado de acuerdo: 96,6%.
Puntos prácticos
Las acciones de la curcumina se logran mediante varios mecanismos, como la reducción de la expresión de interleucina IL-1, IL-6, IL-12 y el TNFα. Además, reduce los niveles de especies reactivas de oxígeno, como aniones superóxido y malondialdehído229,230. Dos ensayos controlados con placebo realizados en adultos sugirieron la posible eficacia de la curcumina para lograr y mantener una remisión clínica sostenida231,232. A nivel endoscópico, se observó una remisión en el 38% (8/22) de los pacientes tratados con curcumina, en comparación con el 0% (0/16) en el grupo de placebo232. Los resultados del uso de curcumina en pacientes con EC y CU son difíciles de evaluar porque los ECA son variables en cuanto a la dosis, el momento del tratamiento y la vía de administración. El número de pacientes de las muestras también ha sido muy pequeño229.
Tanto la formulación como la dosificación de cúrcumina (ingrediente activo de la cúrcuma) no están establecidos para niños. Sin embargo, la evidencia sugiere que puede ser utilizado de forma segura hasta 4 g/día para la fase inducción y hasta 2 g/día durante la terapia de mantenimiento.
En un estudio pediátrico realizado la dosificación en fase inducción de un ensayo pediátrico en curso es la siguiente: dosis diarias, divididas en 2 tomas10.
Nivel de evidencia: II.
Nivel de recomendación: C.
Grado de acuerdo: 96,6%.
Trasplante de microbiota fecal (TMF)
Afirmación 72: se recomienda que el TMF no sea utilizado de forma rutinaria en pacientes con CU pediátrica.
Nivel de evidencia: III.
Nivel de recomendación: D.
Grado de acuerdo: 100%.
Puntos prácticos
Para CUP se han publicado algunos estudios, pero no son concluyentes10. En un estudio de 9 niños con CU se evidenció una remisión clínica del 33% (PUCAI < 10) con enemas seriados233. Otro estudio pediátrico de TMF realizado a través de sonda nasogástrica no demostró mejoría clínica230.
Además de lo anterior, se debe considerar que puede haber un riesgo teórico relacionado con la transferencia de un microbioma adulto a un niño, especialmente en los muy pequeños que se encuentran con un microbioma en desarrollo, y esto puede desarrollar consecuencias relacionadas con el sistema inmunológico234.
Afirmación 73:
Se recomienda el uso de metilprednisolona endovenosa una vez al día como tratamiento inicial. (Nivel de evidencia: II).
La perforación intestinal o el megacolon tóxico deben considerarse en caso de dolor abdominal severo o en aumento. Estos pacientes deben ser evaluados rápidamente por cirugía pediátrica y el tratamiento conservador solo debe considerarse ante estabilidad hemodinámica y en centros altamente especializados bajo estrecha vigilancia; se recomienda la colectomía urgente si no se observa mejoría en 24 a 72 horas. (Nivel de evidencia: III).
El infliximab se recomienda como segunda línea de manejo para los pacientes que no responden al tratamiento con corticoide endovenoso, aquellos que no lo han recibido antes235,236. (Nivel de evidencia: III).
Los inhibidores de la calcineurina (tacrolimus y ciclosporina) pueden considerarse como un manejo alternativo de segunda línea235. (Nivel de evidencia: III).
Nivel de evidencia: II-III.
Nivel de recomendación: C.
Grado de acuerdo: 96,6%.
Puntos prácticos
La CU aguda severa es definida por un PUCAI ≥ 65 puntos11,237. (Nivel de evidencia: II).
Es necesario realizar una búsqueda de posibles desencadenantes de CU aguda severa como infecciones bacterianas por medio de un coprocultivo, que incluya toxinas A y B de Clostridioides difficile11,238. Además, la búsqueda de infecciones virales y parasitarias en casos de fiebre, diarrea no sanguinolenta, noción de contagio positiva o estudios dirigidos a zonas endémicas. Asimismo, en caso de no respuesta a los esteroides en tres días, debe excluirse colitis por CMV11,239. (Nivel de evidencia: III).
La mesalazina (oral y rectal) debe suspenderse en CU aguda severa para excluir la intolerancia a esta, especialmente cuando se ha iniciado el tratamiento con mesalazina en las semanas previas; la reintroducción debe considerarse después de una mejoría clínica significativa11,183. (Nivel de evidencia: III).
La radiografía de abdomen debe realizarse al ingreso, especialmente en niños con sensibilidad o distensión abdominal, dolor significativo y toxicidad sistémica11. (Nivel de evidencia: III).
La monitorización y el seguimiento de la actividad de la enfermedad debe realizarse diariamente para confirmar la respuesta gradual antes de tomar decisiones acerca de terapias de segunda y tercera línea. Un PUCAI > 45 puntos en el tercer día de tratamiento con corticoides endovenosos debería llevar a la planificación de la terapia de segunda línea entre los días 3 y 5. (Nivel de evidencia: 2). Un PUCAI > 65 puntos al quinto día de tratamiento con corticoides endovenosos tiene indicación de inicio de terapia de segunda línea. (Nivel de evidencia: 2). El manejo con un corticoide endovenoso debe continuar durante dos a cinco días adicionales en niños con un PUCAI de 35 a 65 puntos en el quinto día11,235,236. (Nivel de evidencia: II).
El alta hospitalaria debe ser como máximo en actividad de la enfermedad leve (PUCAI < 35 puntos), preferiblemente más cerca de la remisión (PUCAI < 10 puntos)11. (Nivel de evidencia: III).
El mantenimiento con tiopurinas se recomienda después de que la CU aguda severa responda a los corticoides endovenosos; podría considerarse la terapia de mantenimiento con mesalazina exclusiva si la respuesta a los esteroides ha sido rápida y el paciente era nuevo en el uso de mesalazina previo al ingreso11. (Nivel de evidencia: III).
Los pacientes que responden al infliximab iniciado durante la CU aguda severa deben continuar con este fármaco como terapia de mantenimiento posterior al alta hospitalaria11. (Nivel de evidencia: II).
Un PUCAI de 65 se asocia con un curso de la enfermedad más refractario tanto al inicio de la enfermedad como posteriormente235,236,240, y a un mayor riesgo de colectomía241.
Es importante tomar muestras de toxina para Clostridium difficile A y B a través de inmunoensayos enzimáticos rápidos (se deben tomar dos muestras)242. Si se dispone de una prueba de amplificación de ácidos nucleicos, dirigida a los genes de las toxinas A y B principalmente por PCR debido a su alta sensibilidad y especificidad, solo se requiere una muestra de heces243.
La infección por CMV se puede identificar mediante la obtención de biopsias de mucosa a través de una rectosigmoidoscopia flexible. Las biopsias deben teñirse con hematoxilina y eosina e inmunohistoquímica para detectar el CMV. Una PCR positiva en ausencia de cuerpos de inclusión o tinción positiva es insuficiente para diagnosticar el CMV, ya que la PCR carece de especificidad11,244.
Los antibióticos no se recomiendan de forma rutinaria en niños con CU aguda severa al ingreso. Se puede considerar el tratamiento antibiótico específico empírico cuando se sospeche infección por C. difficile u otra bacteria. Se podría considerar un ciclo corto de antibióticos orales en casos refractarios graves seleccionados, mientras se prepara la colectomía; estos deben suspenderse si no se observa una respuesta significativa en cuatro a siete días11,245.
La vancomicina oral debe considerarse el tratamiento de primera línea para la infección por C. difficile en la CU aguda severa. Debe prescribirse por 10 a 14 días en dosis de 10 mg/kg cuatro veces al día (hasta una dosis para adultos de 125 a 250 mg, que se incrementa si es necesario hasta un máximo de 500 mg cuatro veces al día). El metronidazol oral puede utilizarse en ausencia de vancomicina oral en una dosis de 7,5 a 10 mg/kg tres veces al día (máximo de 2 g/24 horas) durante 10 a 14 días11,246.
Para la infección por CMV, el ganciclovir debe utilizarse a dosis de 5 mg/kg dos veces al día durante 21 días. Si no hay respuesta, debe considerarse la valoración por infectología pediátrica. El cambio a valganciclovir oral puede considerarse después de varios días de tratamiento endovenoso exitoso11,239.
Para el manejo del dolor, los antiinflamatorios no esteroideos (AINE) deben evitarse en la CU aguda severa por riesgo de exacerbación de la enfermedad247,248. Los opiáceos deben utilizarse excepcionalmente con precaución y estrecha vigilancia en dosis equivalentes a 0,1 mg/kg de morfina, dado el riesgo de facilitar el megacolon (disminución de la peristalsis intestinal)11,249. Se pueden utilizar medidas no farmacológicas como el uso de compresas calientes y paracetamol para el tratamiento del dolor11.
La dieta normal se puede continuar en la mayoría de los casos de CU aguda severa. La nutrición enteral o parenteral también pueden utilizarse en caso de existir no tolerancia de vía oral o en caso de desnutrición, proporcionando la ingesta calórica, proteica y de micronutrientes estándar para la edad. El peso corporal, la ingesta calórica y el estado de hidratación deben controlarse diariamente, incluyendo el acompañamiento por nutrición11,236,239.
La alimentación oral o enteral está contraindicada en casos de megacolon, o cuando la cirugía es inminente. Debe monitorizarse el desequilibrio electrolítico (hipopotasemia e hipomagnesemia), pues puede favorecer la dilatación del colon, control cada uno a tres días11.
Se recomienda el uso de metilprednisolona endovenosa a dosis de 1 mg/k/día (hasta 40 mg/día) una vez al día como tratamiento inicial. (Nivel de evidencia: II); una dosis mayor de 1,5 mg/kg/día (hasta 60 mg/día) dividida en una o dos dosis debería reservarse para casos graves o previa falla de los esteroides orales11.
Se recomienda el uso de anticoagulación para la prevención del evento tromboembólico venoso o cuando están presentes más factores de riesgo en adolescentes: tabaquismo, uso de anticonceptivos orales, inmovilización completa, catéteres venosos centrales (incluido catéter de inserción periférica [PICC]), obesidad, infección significativa recurrente (respiratoria, urinaria, cutánea e intraabdominal), desorden protrombótico conocido, evento tromboembólico previo o historia familiar de este. En prepúberes se requiere una mayor evaluación de la seguridad y la eficacia de la tromboprofilaxis antes de su uso, puede considerarse en aquellos con al menos dos factores de riesgo. La duración del tratamiento debe ser individualizada; consultar con hematología11,250,251.
La heparina de bajo peso molecular (HBPM) más común es la enoxaparina subcutánea a dosis de 1 mg/k/día (100 UI/kg/día). La monitorización con el nivel de actividad anti-Xa no suele ser necesaria, excepto en deterioro renal significativo. Además, fomentar la movilización, la hidratación adecuada y la retirada precoz de catéteres venosos centrales y arteriales11,252.
La metilprednisolona es el medicamento de elección por menor efecto mineralocorticoide. Realizar un descenso rápido de la metilprednisolona a 1 mg/k/día (40 mg/día) una vez que se haya obtenido una adecuada respuesta. La infusión continua no tiene ninguna ventaja sobre la administración en bolo11,188,253,254.
En los pacientes sin megacolon en la radiografía, pero con signos de peritonitis o deterioro inexplicable, puede estar indicada una tomografía abdominal o una resonancia nuclear magnética para excluir una perforación11,255.
El diagnóstico de megacolon tóxico en pediatría se realiza con la evidencia de un diámetro del colon transverso > 56 mm (o > 40 mm en niños menores de 10 años) con signos de toxicidad sistémica: fiebre, taquicardia, deshidratación, alteración electrolítica, alteración del nivel de conciencia e hipotensión o choque. Se debe tener en cuenta que los esteroides pueden enmascarar los signos peritoneales11,256.
Los factores de riesgo para el megacolon tóxico incluyen la infección por CMV o C. difficile, la hipopotasemia, la hipomagnesemia y el uso de anticolinérgicos, antidepresivos, loperamida y opioides11.
El tratamiento inicial del megacolon tóxico incluye reanimación hídrica, antibióticos intravenosos (cubrimiento para bacterias gramnegativas y anaerobias, ampicilina, gentamicina y metronidazol), reposo intestinal, corticoide endovenoso y preparación para cirugía. Se puede considerar la vancomicina oral hasta que se conozca el estado de C. difficile. La infección por CMV se asocia más comúnmente con el megacolon tóxico, no hay suficientes pruebas para apoyar el tratamiento empírico con ganciclovir sin la confirmación de la infección por CMV11,256.
La ciclosporina, el tacrolimus y los anti-TNF no se recomiendan en el tratamiento rutinario del megacolon tóxico11,236.
La planificación recomendada para el tratamiento de segunda línea entre los días 3 y 5 en los pacientes que no responden incluye la rectosigmoidoscopia (para detectar colitis infecciosa [CMV], granulomas y grado de inflamación), la valoración por cirugía pediátrica, la exclusión de la tuberculosis latente, la serología para el virus de la hepatitis B (VHB) y el virus de la hepatitis C (VHC) y/o los laboratorios necesarios antes del tratamiento con inhibidores de la calcineurina (creatinina, perfil lipídico y magnesio)11,236 (Figura 6).
Se aconseja un control frecuente de laboratorios (hemograma, PCR, VSG, albúmina y electrolitos) según sea necesario, pero al menos en el momento del diagnóstico y en los días 3 y 5 posteriores. La PCR, la albúmina y la VSG tienen cierto valor para predecir el fracaso de los corticoides endovenosos y deben controlarse también con ese propósito11.
Los marcadores inflamatorios fecales no se encuentran en el diagnóstico ni en el tratamiento de la CU aguda severa11.
Cuando se introduce una terapia de segunda línea, siempre debe discutirse la posibilidad de no respuesta y plantear la necesidad de colectomía11.
El papel de la ciclosporina o el tacrolimus como terapia de rescate es solo un puente hacia la terapia de mantenimiento a largo plazo. Entre los pacientes refractarios a los esteroides que han fracasado en la terapia de mantenimiento con tiopurina; infliximab es de segunda línea de manejo preferida, a menos que se considere la posibilidad de hacer un puente a vedolizumab11.
La dosis de infliximab es de 5-10 mg/kg/día semanas 0, 2 y 6 y luego para el mantenimiento cada cuatro a ocho semanas, con niveles objetivo de 5-10 ug/Ml; ciclosporina 2 mg/kg/día en infusión continua, con niveles objetivo iniciales de 150-300 ng/mL y mantenimiento de 100-200 ng/mL; y tacrolimus 0,1 mg/kg/dosis dos veces al día, con niveles objetivo iniciales de 10-15 ng/mL y mantenimiento de 5-7 ng/mL11.
Considerar la intensificación del régimen de inducción para proporcionar una exposición al fármaco equivalente a la que se consigue con la dosificación estándar fuera del entorno de CU aguda severa. La farmacocinética del infliximab puede verse influida por múltiples factores (IMC, albúmina sérica, carga de inflamación y uso concomitante de medicamentos inmunosupresores). La dosis de infliximab hasta 10 mg/kg/dosis y/o con mayor frecuencia de lo habitual (semanas 0, 1 y 4-5). Los niveles del fármaco obtenidos durante la inducción pueden guiar la maximización de la eficacia11,257,258.
La respuesta al infliximab o a los inhibidores de la calcineurina debe vigilarse diariamente mediante el PUCAI y marcadores como la PCR y la albúmina séricas. Se prevé una respuesta significativa (descenso del PUCAI de al menos 20 puntos) en un lapso de cuatro a siete días11,259.
Para reducir la inmunosupresión innecesaria, los corticosteroides (ineficaces) deben retirarse tras la introducción de la terapia de segunda línea o la decisión de proceder a colectomía. La estrategia de reducción debe ser individualizada en función de la exposición previa a los corticoides y el estado clínico11.
Los pacientes con adecuada respuesta a la inducción intensificada, las dosis subsiguientes de infliximab durante la fase de mantenimiento pueden reducirse gradualmente y ajustarse a la dosis estándar, idealmente guiadas por la monitorización de niveles séricos197,259.
Los niños que presentan CU aguda severa refractaria a los esteroides tienen un riesgo más elevado de colectomía en el lapso de un año. Se recomienda añadir un inmunomodulador a los pacientes que respondan a infliximab durante al menos seis meses, se prefiere la terapia con tiopurina sobre el metotrexato en CUP por su mayor efecto en el tratamiento de la colitis. Sin embargo, el metotrexato se asocia con un menor riesgo de linfoma, por lo que debe evaluarse el riesgo-beneficio260,261.
Los pacientes deben asistir a control con gastroenterología pediátrica dentro de las dos a tres semanas posteriores al egreso hospitalario de CU aguda severa y luego según sea necesario11.
La metilprednisolona debe convertirse antes del alta en la dosis equivalente de prednisona. Un miligramo de metilprednisolona equivale a 1,25 mg de prednisona.
La profilaxis de la neumonía por Pneumocystis jirovecii (PJP) con trimetoprim-sulfametoxazol (450 mg/m2 dos veces al día durante tres días a la semana) debe considerarse para la inmunosupresión triple, que incluye un anti-TNF o un inhibidor de la calcineurina más otros dos inmunosupresores, principalmente esteroides. 450 mg/m2 dos veces al día durante tres días a la semana11,246.
Los suplementos de hierro por vía oral deben iniciarse tras el alta en los casos de anemia con hemoglobina de 10 g/dL y enfermedad quiescente. El hierro intravenoso debe considerarse en caso de anemia grave (< 10 g/dL), enfermedad activa o si no se toleran los suplementos orales11,262.
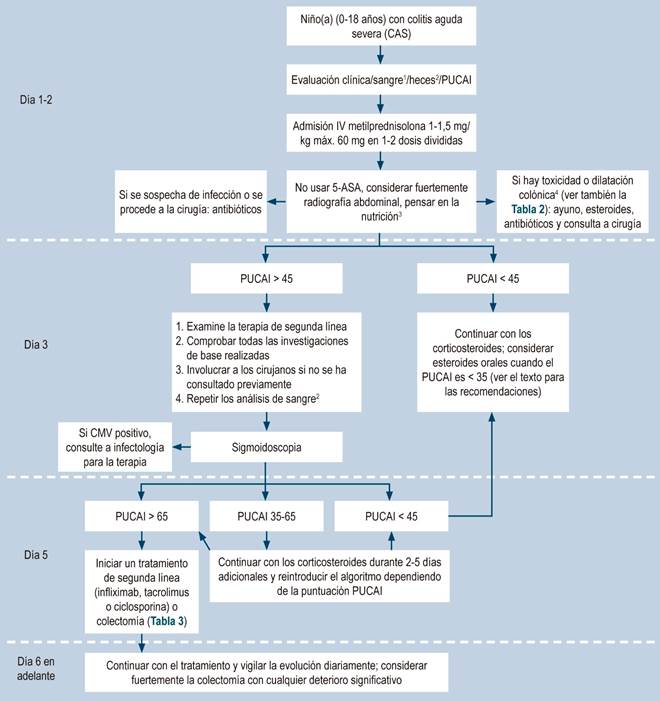
Figura 6 Algoritmo para el manejo de la CUP aguda severa. Apoyarse en paraclínicos: hemograma, electrolitos, enzimas hepáticas, albúmina, PCR, VSG, hemocultivo (si está febril). Cultivo de heces, virus y toxina de C. difficile. Continuar con la dieta normal si es posible; si no, apoyar con alimentación por sonda enteral. Si no se tolera la alimentación por sonda enteral o en presencia de dilatación colónica o cirugía inminente, puede ser necesaria la nutrición parenteral. La dilatación en la radiografía simple de abdomen es sugerida por una anchura colónica de > 56 mm en niños mayores de 10 años y > 40 mm en niños más pequeños. Adaptada de: Turner D, et al. J Pediatr Gastroenterol Nutr. 2018;67(2):292-31011.
Pregunta 32. ¿Cuál es la seguridad y la efectividad del abordaje quirúrgico para el tratamiento de los pacientes pediátricos con CUP?
Afirmación 74: se recomienda considerar la colectomía electiva en niños con CU activa o dependiente de esteroides a pesar de la optimización en la terapia médica, y en aquellos con diagnóstico de displasia del colon10.
Nivel de evidencia: II.
Nivel de recomendación: B.
Grado de acuerdo: 96,6%.
Puntos prácticos
Proctocolectomía restauradora con anastomosis con reservorio ileoanal (IPAA; bolsa J) y una loopileostomía es la cirugía electiva recomendada para CUP10.
La cirugía para CUP puede requerir procedimientos de hasta tres etapas: primera etapa, colectomía subtotal con ileostomía terminal; segunda etapa, proctocolectomía restauradora con anastomosis ileoanal-bolsa o anastomosis ileorrectal (con o sin ileostomía de cobertura); tercera etapa, cierre de la ileostomía de cobertura10.
En lo posible, el abordaje laparoscópico mínimamente invasivo es el indicado en la población pediátrica10.
La EC debe excluirse antes del momento de la cirugía a través de un estudio de diagnóstico que incluya ileocolonoscopia, gastroscopia e imágenes del intestino delgado antes de la colectomía10.
Recomendaciones especiales
Pregunta 33. ¿Cuál debe ser el esquema de vacunación de un paciente con EIIP?
Los pacientes con EII van a requerir en algún momento, para control de su enfermedad de base, esquemas basados en terapias inmunosupresoras, incluyendo esteroides a dosis altas, para manejo a corto plazo y fármacos inmunomoduladores o modificadores de la respuesta biológica para terapia de mantenimiento, lo que aumenta el riesgo de enfermedades infecciosas, oportunistas e inmunoprevenibles. La vacunación adecuada y oportuna continúa siendo una de las estrategias de mayor costo-efectividad para prevenir dicho riesgo, muchas veces subutilizada por los médicos tratantes ante el desconocimiento de los esquemas recomendados en estos pacientes. Es por esto que con el grupo revisor de la guía se hace a continuación un sumario de los consensos y guías recientes sobre inmunizaciones y prevención de infecciones en el paciente con EII con y sin terapia inmunosupresora.
¿Cuáles son las inmunizaciones recomendadas en los pacientes con EII con y sin terapia inmunosupresora? (Tablas 15-20)
Afirmación 75: las guías y consensos recientes recomiendan que el paciente con EII debe tener el mismo esquema de vacunación con vacunas inactivadas que la población general, independientemente de su estado de inmunosupresión, lo que demuestra seguridad y eficacia. Las vacunas vivas o atenuadas no deben aplicarse en pacientes considerados inmunosuprimidos, por lo cual, cuando se hace diagnóstico de EII, es fundamental conocer el estado previo de inmunización para, en caso de requerirlo, ajustarlo antes de definir el inicio de terapia inmunosupresora.
Los pacientes con EII y el uso de aminosalicilatos en monoterapia no se consideran inmunosuprimidos, y su esquema de vacunación debe ser el mismo recomendado que en la población general. Con las vacunas inactivadas no hay un intervalo mínimo entre el inicio del tratamiento y la vacunación, pero en varios consensos se recomienda contar con un intervalo mínimo de dos semanas entre el inicio del tratamiento inmunosupresor y la vacunación, para asegurar la respuesta eficaz a las vacunas.
Nivel de evidencia: III.
Nivel de recomendación: C.
Grado de acuerdo: 100%.
Puntos prácticos
Los pacientes con EII que se consideran inmunosuprimidos son aquellos que reciben 6-MCP, AZA, metotrexato, biológicos, tacrolimus, ciclosporina o altas dosis de corticoesteroides (más de 20 mg día o más de 2 mg/kg/día en menores de 10 kg de prednisona o su equivalente, usado por tiempo mayor a 14 días). Los pacientes con desnutrición severa también se consideran inmunosuprimidos.
Se recomienda que la terapia inmunosupresora se descontinúe al menos tres meses antes de la administración de vacunas vivas, con excepción de la terapia con corticoesteroides, que se debe suspender al menos un mes antes. Si es necesaria la aplicación de vacunas vivas, se recomienda esperar al menos cuatro semanas después de la vacunación con varicela, y al menos seis semanas después de la vacunación con vacuna triple viral (rubéola/sarampión/paperas) para el inicio del tratamiento inmunosupresor.
En caso del uso de biológicos como anti-CD20 (rituximab) y anti-CD25 (alemtuzumab), se recomienda que la terapia inmunosupresora se descontinúe al menos 12 meses antes de la aplicación de vacunas vivas. Los siguientes esquemas muestran escenarios clínicos para la vacunación al momento de diagnóstico y en el seguimiento y los intervalos para vacunación de los pacientes con diagnóstico de EII e inmunosupresión y su núcleo familiar.
Tabla 15 Resumen de enfermedades prevenibles en EIIP
| Enfermedad prevenible | Marcador(es) | Resultado | Conducta |
|---|---|---|---|
| Sarampión | IgG | Positiva | Ninguna |
| Negativa | Administrar una dosis de triple viral al menos cuatro semanas antes de comenzar el tratamiento (o dos dosis separadas de cuatro semanas, si se cuenta con el tiempo suficiente). | ||
| Varicela | IgG | Positiva | Ninguna |
| Negativa | Administrar una dosis de VVZ al menos cuatro semanas antes de comenzar el tratamiento (o dos dosis separadas de cuatro semanas, si se cuenta con el tiempo suficiente). | ||
| Hepatitis B | AgHBs, anti-HBs, anti-HBC | Negativos | Se administrarán tres dosis de hepatitis B (0, 1 y 6 meses) o dosis de refuerzo a partir de los dos años. |
IgG: inmunoglobulina G; VVZ: virus de la varicela zóster.
Tabla 16 Recomendación de vacunación de pacientes con EIIP en terapia con inmunosupresores
Modificado de: R Ferreiro-Iglesias, M Piqueras, E Ricart, et al., Recomendaciones del Grupo Español de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa sobre la importancia, el cribado y la vacunación en pacientes con enfermedad inflamatoria intestinal, Gastroenterología y Hepatología, https://doi.org/10.1016/j.gastrohep.2022.03.012
Tabla 17 Recomendaciones de vacunas para niños con EII
| Curso de la enfermedad | Recomendación | Acción |
|---|---|---|
| En el diagnóstico | Evaluación del estado de vacunación | Evaluación de títulos de anticuerpos Acs HA, contra VHB (AgHBS, Anti-HBs-AntiHBc). Si son negativos: 3 dosis HB 0, 1 y 6 meses o dosis de refuerzo; MMR IgG sarampión-rubéola negativa: 1 dosis MMR 6 semanas antes de iniciar el tratamiento o 2 dosis separadas por 4 semanas; y VVZ IgG negativa: 1 dosis de VVZ al menos 4 semanas antes del tratamiento o 2 dosis separadas por 4 semanas si se dispone de más tiempo. |
| Administración de todas las vacunas recomendadas para la edad según el calendario nacional, así como vacunación con vacunas MMR y VVZ. | ||
| Durante el seguimiento | Administración de dosis de refuerzo periódicas | Vacunas de refuerzo contra neumococo, meningococo y DTP. |
| Vacunación antigripal anual | Administración anual de la vacuna antigripal tetravalente. | |
| Vacuna para COVID-19 | Administración de la vacuna COVID-19, independientemente del tipo de terapia para la EII. | |
| Vacunación de los cuidadores | Estado de vacunación adecuado. | |
| Vacunación antigripal anual. | ||
| Administración de la vacuna contra COVID-19. |
DTP: difteria, tétanos, tos ferina; MMR: sarampión, paperas, rubéola. Adaptado de: Esposito S, et al. Vaccines. 2021;9(5):487263.
Tabla 18 Recomendaciones de vacunas para niños con EII
| Tratamiento | Desde la interrupción del tratamiento a la vacunación | Desde la vacunación al reinicio de tratamiento |
|---|---|---|
| Glucocorticoide oral ≥ 20 mg | 4 semanas | 4 semanas |
| Glucocorticoide en bolo | 3 meses | 4 semanas |
| Metotrexato, AZA, 6-MCP | 0* a 3 meses | 4 semanas |
| Sulfasalazina y mesalazina | 4 semanas | 2 semanas |
| Tacrolimus, ciclosporina | 3 meses | 4 semanas |
| ADA-IFX-GOLI-CERTO | 12 semanas | 4 semanas |
| Ustekinumab | 15 semanas | 4 semanas |
*Se considera que las personas que reciben metotrexato < 0,4 mg/kg/semana 9, AZA < 3 mg/kg/día y 6-MCP < 1,5 mg/kg/día tienen inmunosupresión de bajo nivel, por lo que no sería necesario aplicar estos intervalos. ADA: adalimumab; CERTO: certolizumab pegol; GOLI: golimumab; IFX: infliximab. Adaptado de: Esposito S, et al. Vaccines. 2021;9(5):487263.
Tabla 19 Susceptibilidad según el medicamento usado en EII
IBS: Infección bacteriana severa; IO: infección oportunista; MAC: Mycobacterium avium complex; VHS: virus del herpes simple. Adaptado de: Maus MV, et al. Curr Opin Infect Dis. 2020;33(4):281-9264.
Tabla 20 Tamizaje y profilaxis para pacientes con EII antes del inicio de la terapia inmunosupresora
*Esposito S, et al. Vaccines in Children with Inflammatory Bowel Disease: Brief Review. Vaccines. 11 de mayo de 2021;9(5):487.
**Maus MV,et al. Infections associated with the new ‘nibs and mabs’ and cellular therapies. Curr Opin Infect Dis. agosto de 2020;33(4):28
Vacunas vivas
Hepatitis A
Administrar dos dosis, con intervalo de seis a 18 meses.
Primera dosis: recomendada a los 12 meses de vida, esquema del programa ampliado de inmunizaciones (PAI) actual.
Excelente inmunogenicidad en EII. No se han reportado casos de exacerbación de la enfermedad. Puede ser menor la inmunogenicidad con inhibidores de TNF y terapia combinada.
Hepatitis B
Se debe evaluar el estado previo por riesgo de exacerbación de hepatitis B, incluida en el esquema PAI a los 0, 2, 4 y 6 meses de vida.
Esquema 0, 1, 6 o 0, 1, 4 meses. Evaluar la respuesta de anticuerpos al mes de última dosis. Si los anticuerpos antiantígeno de superficie de hepatitis B (AcHBsAg) son menores de 10 UI/L se recomienda revacunar con dosis con intervalo de dos meses. Con los inhibidores de TNF hay una menor respuesta, pero con tiopurinas y metotrexato, en cambio, hay una buena respuesta.
Neumococo
Esquema PAI: 2, 4 y 12 meses de vida. Los pacientes nacidos antes de febrero de 2022 recibieron la vacuna conjugada 10 valencias. Actualmente, desde abril 2022, igual esquema 2, 4 y 12 meses con PCV 13 valencias.
Recomendado: esquema con vacuna conjugada de 13 serotipos en esquema de 2, 4, 6 y 12 meses.
Refuerzo o paciente no vacunado en la adolescencia: una dosis de conjugada de 13 serotipos seguida a las ocho semanas de la vacuna polisácarida de 23 serotipos.
El paciente que será llevado a estado de inmunosupresión mayor de dos años, que cuenta vacunación con vacuna conjugada, debe recibir una dosis de neumococo polisacárida 23 valencias.
Influenza
Esquema PAI: trivalente, inactivada: seis meses; refuerzo a los siete meses, anual hasta los cinco años.
En pacientes con diagnóstico de EIIP: tetravalente o trivalente: buena inmunogenicidad, no exacerbación de la enfermedad.
En primovacunación: dos dosis con cuatro semanas de diferencia.
Refuerzo anual durante el tiempo que requiera manejo.
Menor inmunogenicidad para influenza B, y con uso de inhibidores de TNF.
Vacuna SARS-CoV-2
En los pacientes de 12 a 18 años la recomendación es que deben recibir el esquema de dos dosis de vacunas ARNm (Pfizer) o vacunas de virus inactivado (Sinovac) con un intervalo de 21 a 84 días, según la plataforma utilizada.
Vacunación en niños de 3 a 11 años: se encuentra disponible la vacunación con Sinovac (virus inactivado) dos dosis en intervalos de 28 días.
No debe retardarse su vacunación independiente de tratamiento instaurado y actividad de la enfermedad, excepto en aquellos que reciban medicamentos inmunosupresores, como se menciona a continuación.
En Colombia, se debe recomendar la tercera dosis para los mayores de 12 años en estado de inmunosupresión. Se consideran como medicamentos inmunosupresores: alemtuzumab, abatecept, belatecept, obinutizumab, rituximab, fingolimod, ocrelizumab, antimetabólicos e inhibidores de la calcineurina, que hayan sido administrados en el último año. Si ha recibido medicamentos biológicos que producen depleción de células B (por ejemplo, globulina antitimocito, rituximab, obinituzumab), la vacunación se debe posponer de tres a seis meses. La recomendación de la tercera dosis en los pacientes mayores de 12 años en estado de inmunosupresión es usar un homólogo (cuando el esquema inicial usado fue un virus inactivado o ARNm) o con un biológico heterólogo con plataforma ARNm (cuando el esquema inicial fue vector viral) 30 días después de completar su esquema de vacunación. Resoluciones vigentes de vacunación (sujetas a cambio) para COVID-19: 1151/21, 092/22, 419/22 para uso de refuerzo en pacientes en condiciones de inmunosupresión y 762/22 para el uso de cuarta dosis.
El Centro para el Control y Prevención de Enfermedades (CDC) recomienda en pacientes de 5 a 11 años con inmunosupresión moderada a grave un total de cuatro dosis para la vacuna de COVID-19 con vacuna ARNm (Pfizer-BioNTech), en un esquema de tres dosis y un refuerzo, y para adolescentes y adultos cinco dosis de vacuna de plataforma ARNm (Pfizer o Moderna) en esquema de tres dosis y dos refuerzos. En Colombia aún no hay autorización gubernamental, hasta la última revisión del consenso, del uso de la vacuna ARNm Pfizer-BioNTech para menores de 12 años.
Pregunta 34. ¿Cuándo sospechar inmunodeficiencia en el paciente con EIIP?
Afirmación 76: la EIIP asociada a errores innatos de la inmunidad (incluidas las formas monogénicas) debuta principalmente antes de los 10 años de vida; sin embargo, las asociadas a defectos de inmunidad humoral presentan un pico más tardío entre la segunda y la tercera década de la vida. Las características clínicas más frecuentes en estos casos son: infecciones, anomalías de piel/cabello/uñas, enfermedad perianal, autoinmunidad, úlceras orales y hepatoesplenomegalia. Por estas razones, todo paciente que cuente con estas características requiere valoración por inmunología y genética. Todo paciente con EIIP requiere una tamización inmune con: dosificación de inmunoglobulinas (G, A, M, E y D), conteos de linfocitos (T/B/NK) y prueba de dihidrorodamina.
Nivel de evidencia: I.
Nivel de recomendación: A.
Grado de acuerdo: 100%.
Puntos prácticos
Aproximadamente, el 11,5% de los pacientes con EIIP presentan una etiología monogénica265; de estos, más del 80% de los pacientes debutan antes de los 10 años266. Sin embargo, los pacientes con XIAP, enfermedad granulomatosa crónica (EGC) y haploinsuficiencia de A20 desarrollan EII desde la infancia hasta la tercera década de la vida266. Por otro lado, los casos de EIIP asociados a inmunodeficiencia común variable debutan principalmente en la segunda década de la vida267.
La mayoría de los pacientes con EIIP de inicio antes de los dos años no presentan manifestaciones extraintestinales previas al inicio de síntomas gastrointestinales, en tanto que más de la mitad de los pacientes con formas monogénicas diagnosticadas después de esta edad las presentan266. Las manifestaciones extraintestinales más frecuentes en estos casos son: infecciones (recurrentes, severas, atípicas), anomalías de piel/cabello/uñas, enfermedad perianal, autoinmunidad, úlceras orales y hepatoesplenomegalia.
Las etiologías más frecuentes son los defectos relacionados con la vía de señalización de IL-10, la enfermedad granulomatosa crónica (en todas sus variantes) y la deficiencia de XIAP266. Sin embargo, en condiciones como la inmunodeficiencia común variable, alrededor del 11% de los pacientes presentan EIIP al momento del diagnóstico267.
Al momento del diagnóstico de EIIP, se deben realizar pruebas inmunológicas básicas que incluyen: dosificación de inmunoglobulinas (G, A, M, E y D), conteos de linfocitos (T/B/NK) y prueba de dihidrorodamina266,268,269. Esta evaluación adquiere mayor importancia ante la necesidad de manejo inmunomodulador en estos pacientes y servirá también como evaluación basal para el seguimiento inmunológico en los casos que lo requieran270.
Se sugiere realizar un estudio genético a todos los pacientes en quienes la EIIP debuta antes de los 6 años y presenta las características previamente relacionadas. Respecto a la metodología de estudio genético a realizar, los paneles de secuenciación de siguiente generación garantizan alta profundidad y cobertura de las regiones génicas a secuenciar frente a la secuenciación del exoma clínico o completo271. La secuenciación del genoma completo no se recomienda como estudio inicial, lo anterior es crucial para aumentar la eficiencia de detección de variantes patogénicas o probablemente patogénicas y reducir errores en un entorno de diagnóstico271; por este motivo, se plantea como primera línea el uso de estos paneles272, incluyendo en estos el análisis de los genes propuestos por el Grupo de Porto de EII272.
Pregunta 35. ¿Condiciones para la transición del paciente con EIIP al grupo de EII de adultos?
Afirmación 77: se recomienda que los adolescentes con diagnóstico de EII sean incluidos en un programa de transición a adultos.
Nivel de evidencia: II.
Nivel de recomendación: B.
Grado de acuerdo: 100%.
Puntos prácticos
Los centros especializados en el manejo de la EII deben ofrecer atención integral a los pacientes adolescentes que pronto serán trasladados al cuidado médico de adultos273.
La adherencia al tratamiento debe ser frecuentemente evaluada por un equipo multidisciplinario (entrevistas, monitorización de niveles de medicamento)273.
Transición se define como el movimiento planeado de un paciente con una condición crónica, del cuidado pediátrico al cuidado de adultos. El período de transición usualmente inicia alrededor de los 12-14 años y puede ir hasta después de los 18, proceso que debe ser individualizado con cada paciente porque depende de características como madurez del paciente, conocimiento de la enfermedad, apoyo de los cuidadores, condiciones del equipo de adultos, entre otras. El adolescente debe ser motivado para que aumente su responsabilidad sobre el conocimiento de la enfermedad, adherencia al tratamiento farmacológico-nutricional y actitud en la consulta.
Una transición exitosa redunda en una mejor adherencia al tratamiento y, por ende, en menores complicaciones médicas y menores costos; además, permite al grupo de salud desarrollar un proceso más satisfactorio de sus labores al poder controlar los progresos logrados, basados en un plan preestablecido10.