Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Agronomía Colombiana
versão impressa ISSN 0120-9965
Agron. colomb. v.24 n.1 Bogotá jan./jun. 2006
Cambios físicos, químicos y sensoriales durante el almacenamiento congelado de la pulpa de arazá (Eugenia stipitata Mc Vaugh)
Physical, chemical and organoleptic changes during frozen storage of araza (Eugenia stipitata Mc Vaugh) pulp
Liliana Josefina Mejía1, Carlos Eduardo Narváez2 y Luz Patricia Restrepo3
1 Química, Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia, Bogotá. e-mail: ljmejiah@unal.edu.co
2 Profesor asistente, Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia, Bogotá. e-mail: cenarvaezc@unal.edu.co
3 Profesor asociado, Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia, Bogotá. e-mail: lprestrepos@unal.edu.co
Resumen:
Se evaluaronlosefectosdelacongelación lenta a -20 °C en pulpa de arazá (Eugenia stipitata Mc Vaugh). La pulpa fue almacenada durante 4 meses y cada 15 d se evaluó: pH; acidez total titulable; grados Brix; contenido de algunos compuestos antioxidantes: ácidoascórbico, carotenoides,fenólicos;actividad antioxidante por el método del blanqueamiento del ß-caroteno y características sensoriales de aroma, sabor, textura, apariencia y color. El estudio mostró que el tratamiento de congelación conservó la pulpa con buenas características sensoriales durante el primer mes de almacenamiento. Si bien la textura instrumental y el ácido ascórbico se vieron seriamente afectados durante este periodo, los compuestos fenólicos totales, los carotenoides y la actividad antioxidante se mantuvieron invariables. Si se considera que esta fruta es una buena fuente de sustancias con poder antioxidante y que su capacidad antioxidante es buena, de acuerdo a la técnica del ß-caroteno, se debe continuar trabajando en técnicas que prolonguen su calidad durante tiempos aún más largos.
Palabras claves adicionales: actividad antioxidante, ácido ascórbico, compuestos fenólicos.
Abstract:
The effects of slow -20 °C freezing on araza fruit (Eugenia stipitata Mc Vaugh) pulp were evaluated. Pulp was stored for 4 months and aroma, flavour, texture, appearance and colour (sensory characteristics) and pH, acidity, soluble solids, ascorbic acid, carotenoids, phenol compounds and antioxidant activity (physicochemical properties) were evaluated by the ß-carotene blanching method each fortnight. Organoleptic evaluation led to the conclusion that freezing the pulp conserved it well during the first 30 days’ storage, retaining good sensory characteristics. Although texture and ascorbic acid became depleted during this period, phenol compounds, carotenoids and antioxidant activity remained constant. It should be taken into account that araza fruit has high levels of substances having good antioxidant activity; it is thereforedesirableto continueworkingontechniques for prolonging its quality for longer periods of time.
Additional key words: antioxidant activity, ascorbic acid, phenol compounds.
Introducción
EL ARAZÁ (EUGENIA STIPITATA MC VAUGH) se considera como un fruto promisorio de la región amazónica colombiana, con producciones anuales del orden de 15 t·ha-1. Se destaca por su adaptación a los suelos pobres y ácidos propios de esta región, por sus propiedades organolépticas, como sabor y aroma, y por su contenido nutricional. Este fruto se emplea en diversas industrias en la elaboración de mermeladas, néctares, dulces y perfumes (Delgado, 2004; Quevedo, 1995; Vargas et al., 2005).
Ya que el fruto tiende a sufrir daños acelerados durante su poscosecha, se han adelantado trabajos para establecer las condiciones para una vida en anaquel adecuada, con el fin de mejorar la integración del fruto al mercado interno y proporcionar herramientas para llevarlo al mercado internacional (Hernández, 2001; Narváez, 2003). La refrigeración, en combinación con choque térmico o con choques intermitentesyelusodeatmósferasmodificadas,son algunos de los métodos de almacenamiento empleados para la conservación del fruto de arazá en fresco. En general, tras el uso de estas técnicas se ha logrado mantener la vida útil del fruto durante 15 d, pues se consigue disminuir la pérdida de peso, el ablandamiento, el pardeamiento y la susceptibilidad a las pudriciones, manteniendo, por lo tanto,suscaracterísticasorganolépticasdurante unmayor tiempo (Hernández, 2001; Narváez, 2003).
Dada la alta perecibilidad del fruto, el almacenamiento congelado de la pulpa puede constituirse en una alternativa adecuada para aumentar el tiempo de vida de la fracción comestible. En la congelación, al pasar el agua de estado líquido a sólido, se disminuyen en gran medida las reacciones que conllevan el deterioro de la pulpa, lográndose extender el período de uso del producto. El almacenamiento congelado debe garantizar la calidad del producto a través del tiempo; en este sentido se deben tener en cuenta criterios tales como: calidad sensorial, microbiológica, física y química, con el fin de mantener su aceptación por parte de los consumidores (Lisiewska y Kmieecik, 2000; Redmond et al., 2003).
La calidad de un alimento está definida, en buena medida, por la percepción que tenga el consumidor de él. En este punto, las características sensoriales son de gran importancia, pues juegan un papel fundamental en la determinación de las condiciones adecuadas de almacenamiento del alimento (Hough y Fiszman, 2005). La calidad sensorial es el reflejo de las características microbiológicas, físicas y químicas, por lo que se constituye en una herramienta valiosa e integral para el diagnóstico de la calidad del producto.
De otro lado, en años recientes ha surgido un gran interés por los compuestos antioxidantes naturales, presentes principalmente en frutas y verduras que hacen parte de la dieta diaria. El arazá es una fruta que ha mostrado tener una buena capacidad antioxidante, medida por el método de la decoloración del ß-caroteno, y un buen contenido de antioxidantes, como ácido ascórbico (30 mg· 100 g-1 pulpa base húmeda [BH]) y compuestos fenólicos totales (64 mg de ácido gálico·100 g-1 de pulpa BH) (Vargas et al., 2005). En general, este tipo de compuestos tienen acciones antitumorales, antialérgicas, antiinflamatorias y disminuyen el riesgo de padecer enfermedades degenerativas y coronarias, pues actúan como antioxidantes al atrapar radicales libres y como agentes sinérgicos, como es el caso del ácido ascórbico con fenoles y carotenoides, regenerando o restaurando sus propiedades antioxidantes (Jan et al., 2001).
La técnica de medida de la actividad antioxidante por el método de la decoloración del ß-caroteno consiste en generar radicales libres por oxidación del ácido linoleico; estas especies, a su vez, degradan el ß-caroteno. Si existe un antioxidante en el medio de reacción, la degradación del ß-caroteno deberá ser menor. La medida de la degradación del ß-caroteno se puede efectuar en la región visible del espectro electromagnético (Gadow et al., 1997; Velioglu et al., 1998).
Teniendo en cuenta que la pulpa de arazá suele ser congelada en el hogar o en microempresas en congeladores convencionales, el objetivo de este trabajo fue evaluar algunas características sensoriales, físicas y químicas deestapulpaenalmacenamiento congeladolento a -20 °C durante 4 meses, para proporcionar información sobre la efectividad de esta técnica de conservación en la calidad de la pulpa.
Materiales y métodos
Frutos de arazá
Se utilizaron muestras comerciales adquiridas en Bogotá. Se seleccionaron los frutos en condiciones óptimas de maduración (corteza 100% amarilla) y se limpiaron para eliminarles partículas extrañas y polvo de la superficie. Se efectuó una desinfección en hipoclorito de sodio al 2% por 20 min.
Procesamiento
Las frutas se sometieron a pelado y separación de semillas de forma manual. La pulpa se homogenizó y almacenó en bolsas de polietileno de baja densidad (aproximadamente 100 g por bolsa). Por último, las muestras se colocaron durante 4 meses en un congelador convencional a -20 °C. El proceso de congelación se hizo a baja velocidad (menor a 1 °C· min-1). Cada 15 d se retiró una muestra de pulpa del almacenamiento congelado y se le efectuaron diversos análisis sensoriales, físicos y químicos. Para los análisis instrumentales de la textura y la evaluación sensorial se efectuó una descongelación rápida con microondas durante 2 min. Para los demás análisis no se hizo descongelación. Los análisis para el día 0 se realizaron con la pulpa fresca, antes de congelarla.
Análisis sensorial
Un grupo de seis panelistas entrenados, con habilidad para percibir las diferencias entre la pulpa de arazá fresca y congelada, evaluó aroma, sabor, textura, apa riencia y color. Para la evaluación se tomó una escala previamente diseñada (Delgado, 2004). La escala y los descriptores aparecen en la tabla 1.

Sólidos solubles, pH y acidez titulable
Estos análisis se realizaron de acuerdo a los procedimientos propuestos por Bernal (1992).Los sólidos solubles se midieron con un refractómetro manual Atago®. Los resultados se reportaron como grados Brix a 18° C. El pH se midió, sin diluciones, con un potenciómetro Inolab pH level 1®. Para determinar la acidez titulable se tomaron 2,0 g de pulpa y se homogenizaron con 10 mL de H2O mediante agitación magnética por 5 min. Al final, se determinó la acidez por titulación con NaOH 0,1 M y fenoftaleína como indicador. Los resultados se expresaron como gramos de ácido málico en 100 g de pulpa BH.
Determinación de los cambios de textura
Se midieron la pérdida de agua por centrifugación, la consistencia y el índice de viscosidad. La capacidad de retención de agua en la pulpa fue evaluada por centrifugación de 10 g de pulpa a 3.000 rpm durante 5 min.
Posteriormente, se midió el volumen de agua liberada por la pulpa. Los resultados se expresaron como porcentaje de peso/volumen (Redmond et al., 2003). Para evaluar la consistencia y el índice de viscosidad se usó un texturómetro Plus Texture Analyser, modelo TA-XT2®, equipado con una celda de 50 mm de diámetro, un cilindro metálico y una sonda redonda de 45 mm de diámetro (A/BE-45). La distancia de recorrido fue de 30 mm a una velocidad de 1 mm· s-1 y una compresión de 1 mm· s-1.
Compuestos que contribuyen a la actividad antioxidante
Ácido ascórbico. Se homogenizó 1,0 g de pulpa con 4 mL de ácido oxálico al 0,15% durante 2 min en mortero, se centrifugó a 3.000 rpm durante 5 min y en el sobrenadante se efectuó la cuantificación del ácido ascórbico de acuerdo con el método de la 2-nitroanilina por lectura espectrofotométrica a 540 nm. Se realizó una curva de calibración con soluciones de ácido ascórbico entre 0,02 y 0,12 mg· mL-1, preparado en ácido oxálico al 0,15%. Los resultados se expresaron como miligramos de ácido ascórbico por 100 g de pulpa BH (Bernal, 1992).
Carotenoides. Se homogenizaron2,0 g de pulpa con 8 mL de acetona en mortero, se centrifugaron a 3.000 rpm durante 5 min y se reservó el sobrenadante. Al residuo se le adicionaron otros 8 mL de acetona, repitiendo el procedimiento una vez más. Ambos sobrenadantes se reunieron. Posteriormente, se efectuó una extracción líquido-líquido en un embudo de separación con 10 mL de éter etílico, efectuando 4 lavados con porciones pequeñas de solución acuosa de NaCl al 10%. Las fases acuosas se descartaron y la fase orgánica se filtró sobre un lecho de Na2SO4 anhidro. Finalmente, se midió el volumen obtenido de la fase orgánica y se leyó su absorbancia a 450 nm. El resultado se expresó en miligramos de carotenoides por 100 g de pulpa BH; para ello se hizo una curva de calibración con soluciones patrones de ß-caroteno en un intervalo de concentración entre 0,01 y 0,07 mg· mL-1 (Dámaso y Míngues, 2000).
Compuestos fenólicos libres y totales. Se pesó1g de pulpa. Para la extracción de los compuestos fenólicos libres se hizo una extracción por molturación con 2 mL de metanol acuoso al 80% y para los compuestos fenólicos totales (compuestos fenólicos libres y ligados) con 2 mL de metanol acidulado (80:19:1, metanol:H2O:HCl). Las muestras se colocaron en un agitador recíproco a 200 rpm durante 2 h. Se centrifugaron a 3.000 rpm durante 5 min, y se reservó el sobrenadante. Al residuo se le adicionó otros 2 mL de la solución extractora y se repitió el procedimiento una vez más. Los dos sobrenadantes se reunieron para la cuantificación.
La cuantificación se realizó por el método de Folin- Ciocalteu (Velioglu et al., 1998), con lectura espectrofotométrica a 765 nm. Los compuestos fenólicos se expresaron como miligramos de ácido gálico en 100 g de pulpa BH. Para cada tipo de extractante se efectuó una curva de calibración con solución patrón de ácido gálico en un intervalo de concentración entre 0,01 y 0,30 mg· mL-1 (Narváez, 2003; Vargas et al., 2005).
Medida de la actividad antioxidante
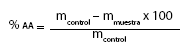
Se determinó por el método de blanqueamiento de ß-caroteno (Gadow et al., 1997), para lo cual se prepararon dos soluciones: solución A (2 mL de solución de ß-caroteno en cloroformo, de 1 mg· mL-1 , 400 µL de Tween 20 y 40 µL de ácido linoléico en frascos de 100 mL) y solución B (2 mL de cloroformo, 400 µL de Tween 20 y 40 µL de ácido linoleico, también en frascos de 100 mL). Después de la evaporación en una estufa al vacío a temperatura ambiente durante 15 min, se adicionaron 100 mL de H2O destilada previamente saturada con oxígeno. Los frascos se taparon y sometieron a ultrasonido (Ultrasonic LC 60H®) durante 5 min. Para efectuar las medidas de actividad antioxidante se prepararon cuatro tipos de soluciones en tubos de ensayo con tapa: 1) 7,5 mL de la solución B y 400 µL de metanol acidulado, usada para ajustar el cero en el espectrofotómetro; 2) un control, para evaluar el comportamiento del sistema sin antioxidante, con 7,5 mL de la solución A y 400 µL de metanol acidulado; 3) 7,5 mL de la solución A y 400 µL de cada una de las muestras (extractos en metanol acidulado) y 4) 7,5 mL de la solución A y 400 µL de butilhidroxitolueno (BHT) (0,32 mg· mL-1 en metanol acidulado), como estándar antioxidante. Las muestras se incubaron a 50 °C y, durante 2 h, cada 10 min se les hizo la lectura espectrofotométrica a 470 nm. Para calcular la actividad antioxidante (AA), se evaluó la pendiente (m) de la recta obtenida para el control y para cada muestra al graficar la absorbancia en función del tiempo de reacción, expresándola de la siguiente forma (Gadow et al., 1997):
Análisis de datos
Para definir el tiempo que las características sensoriales de la pulpa se mantuvieron adecuadas para el consumo, se evaluaron los resultados del análisis sensorial (n = 6) con la prueba no paramétrica de Friedman y se calculó la diferencia mínima significativa (dms) entre tratamientos (días de congelación). Para las demás variables (n = 4), se llevaron a cabo los Anova y se compararon las diferencias entre tratamientos por la prueba de Tuckey (α = 0,05) (Conover, 1980).
Resultados y discusión
Análisis sensorial
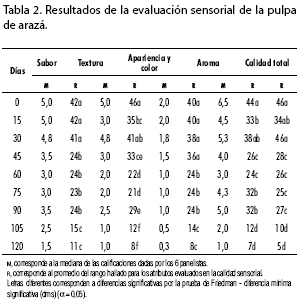
En la tabla 2 se muestra cómo la calidad sensorial se va deteriorando a través del tiempo de almacenamiento. En general, las características sensoriales se mantuvieron relativamente estables –similares a las de la calidad inicial– durante el primer mes de almacenamiento. Los panelistas detectaron cambios en el sabor y el aroma de la pulpa, lo que puede suceder por la formación de productos tales como ácidos carboxílicos, formaldehído y otros, a causa de la degradación del ácido ascórbico por vía enzimática, además de la degradación de azúcares por reacciones de fermentación y la autooxidación de los lípidos. Este tipo de reacciones contribuye también con cambios en la apariencia y el color (Fennema, 2000). Luego de la descongelación de la pulpa los panelistas reportaron pérdida de homogeneidad de la pulpa, caracterizada por la formación de dos fases: una acuosa y otra rica en fibras. Esta pérdida de homogeneidad es un efecto indeseable, pues la textura juega un papel importante en la aceptación del producto por los consumidores. El cambio en la textura puede ser debido a procesos tales como la homogenización, la congelación lenta (donde hay formación de cristales de hielo de tamaño grande) y la descongelación de la pulpa (que afectan la integridad de la célula y produce pérdida los compartimentos celulares). Como resultado final, se disminuye la capacidad de retención de agua de los componentes celulares. Es importante resaltar que, aunque la congelación disminuye la velocidad de reacción enzimática, no la detiene; en este sentido, es probable que la pérdida de la homogeneidad se deba también a que enzimas del grupo de las hidrolasas, entre las que se encuentran la pectinesterasa, la poligalacturonasa, la celulasa y la xilanasa, produzcan la degradación de los componentes de la pared celular, que contribuyen a la estabilidad de la textura (Bartley y Knee, 1982). Esta falta de estabilidad puede ser un inconveniente al momento de emplear la pulpa en la elaboración de productos, lo cual podría solucionarse con el empleo de una técnica de congelación rápida, con tratamientos previos de escaldado y la inclusión de estabilizantes de textura (Fennema, 2000).
Sólidos solubles, pH y acidez titulable
En la figura 1 se observa que el tiempo de almacenamiento congelado tiene un efecto negativo sobre estas variables. Los Anova mostraron que no existe evidencia estadística significativa que permita concluir que las variables objetodeestudiosemantienenatravésdeltiempo. Durante el primer mes de almacenamiento, tiempo en el que la calidad sensorial se mantiene, los sólidos solubles disminuyen, el pH aumenta, ambos de manera significativa, en tanto que la acidez permanece invariable.
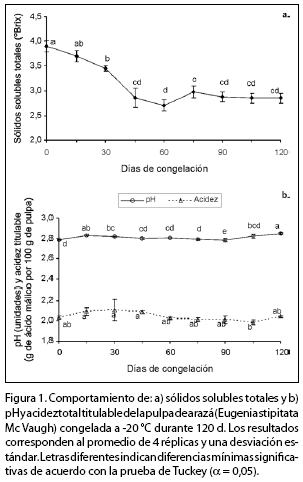
En la pulpa fresca (día 0), el valor de los sólidos solubles fue 3,9%; el pH, 2,79 y la acidez titulable, 2,04 mg de ácido málico por 100 g de pulpa. Estos valores son cercanos a los reportados en un trabajo previo (Hernández, 2001) y permiten clasificar el arazá como un fruto bajo en azúcares y de alta acidez. La disminución en los sólidos solubles durante el almacenamiento congelado puede deberse a la fermentación de los carbohidratos por procesos anaerobios. Aunque los sólidos solubles disminuyeron de manera significativa en el día 30, los panelistas detectaron el sabor residual y aroma a fermentado desde el día 45.
Determinación de los cambios de textura
En la figura 2 se observa que la capacidad de retención de agua de la pulpa disminuye progresivamente durante los primeros 45 d de almacenamiento, para luego volverse constante. La consistencia y el índice de viscosidad cambian también con el tiempo de almacenamiento, pero de manera importante durante los primeros 15 d. Para las tres variables en estudio, el Anova mostró un efecto significativo a través del tiempo. Los resultados demuestran que la congelación tiene una consecuencia negativa, no sólo sobre la textura estimada de manera instrumental, si no también sobre la pérdida de capacidad de retención de agua de la pulpa.
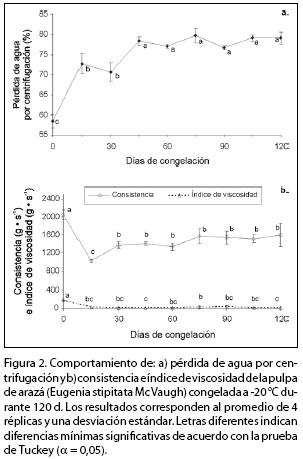
Es importante señalar que la medida instrumental de la textura mostró resultados negativos en los primeros 15 d de almacenamiento; sin embargo, el panel de evaluación sensorial no reportó un punto de corte claro para la pérdi da de textura respecto a este atributo en la pulpa fresca sin congelar. La pérdida de la capacidad de retención de agua en la pulpa congelada indica que si la pulpa es empleada para elaborar un néctar, en éste habrá una mayor tendencia a la separación de fases y además, la consistencia y la viscosidadseránmenoresqueenunnéctarpreparadocon fruta fresca sin congelar, por lo que es común que en la industria de los zumos se incorporen estabilizantes de textura, que incluyen compuestos como carboximetilcelulosa y gomas, entre otros. Si bien, según la normatividad colombiana, estos estabilizantes están permitidos en zumos, están prohibidos en pulpas. Sin embargo, en pulpas azucaradas se permite la incorporación de sacarosa que podría estabilizar la pectina de la pulpa y, por lo tanto, mejorar su textura una vez ésta sea descongelada.
Compuestos que contribuyen a la actividad antioxidante
En la figura 3 se observa que el tiempo de almacenamiento influye de manera negativa en la concentración de ácido ascórbico, carotenoides y compuestos fenólicos libres. El Anova mostró un efecto significativo del tiempo sobre estas variables. Al evaluar los compuestos fenólicos totales se encontró que su concentración no variaba en el tiempo: de acuerdo al Anova, se mostró que estos compuestos no variaban de manera significativa durante el almacenamiento congelado.
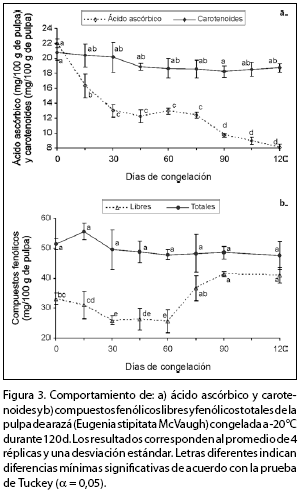
En la pulpa fresca, el contenido de ácido ascórbico (22 mg por 100 g) es menor al reportado en trabajos anteriores (30 mg por 100 g), ambos en base húmeda (Hernández, 2001; Vargas et al., 2005). Los compuestos fenólicos totales expresados como ácido gálico (51 mg por 100 g-1) son menores a los reportados previamente (64 mg por 100 g-1), también en base húmeda (Vargas et al., 2005). Este comportamiento puede ser debido a las diferencias en las muestras objeto de análisis, pues se debe tener en cuenta que las frutas varían su composi ción de acuerdo con la precosecha, el estado de maduración, la temperatura de almacenamiento, entre otros (Hernández, 2001).
Luego de 30 d en congelación, el ácido ascórbico representa tan sólo 59% de su valor inicial (diferencia significativa), los carotenoides mantienen 97% de la concentración inicial (diferencia no significativa), los compuestos fenólicos libres representan 78% (diferencia significativa), mientras que los compuestos fenólicos totales representan 96% de su concentración inicial (diferencia no significativa). Es posible que este comportamiento se vea reflejado en la evaluación sensorial, pues, como se mencionó anteriormente, productos de degradación del ácido ascórbico pueden producir sabores y olores desagradables; además, la degradación de carotenoides producen disminución del color de la pulpa a través del tiempo.
Una tendencia similar a la observada en el comportamiento del ácido ascórbico y de los carotenoides se reporta en trabajos anteriores (Lisiewska y Kmieecik, 2000; Bahceci et al., 2005; Vural et al., 2005). Estos estudios han demostrado que el tratamiento de escaldado contribuye en gran medida a la inactivación de las enzimas peroxidasa y lipooxigenasa, por lo que la degradación de esos compuestos es menor (Vural et al., 2005; Bahceci et al., 2005). Estas dos enzimas se emplean como indicadores de la efectividad de los tratamientos térmicos por su estabilidad térmica relativamente alta, por lo que se asume que si estas enzimas están inactivas, las otras también lo estarán. Además, el interés de inactivarlas radica en que la peroxidasa está vinculada con cambios en la coloración de los vegetales, la degradación de compuestos fenólicos con importante valor antioxidante y la pérdida del aroma. De otro lado, la lipoxigenasa es responsable de la oxigenación y peroxidación de compuestos insaturados, como los ácidos grasos libres, produciendo características sensoriales inadecuadas (sabores y olores desagradables). Ambas enzimas pueden catalizar las reacciones mencionadas, incluso en productos congelados (Bahceci et al., 2005).
Ya que la medida de ácido ascórbico se toma como un parámetro clave para medir la calidad nutricional de los frutos y las hortalizas, se han desarrollado modelos cinéticos para evaluar el efecto de la temperatura de congelación y del tiempo de almacenamiento (Giannakourou y Taoukis, 2003). La cinética de degradación de este compuesto puede describirse por una reacción de primer orden, de acuerdo a la siguiente ecuación:
C = C0e-kt
ó,
Ln(C/C0) = -kt
En donde, C y C0 son las concentraciones de ácido ascórbico a un tiempo t y en el momento cero, respectivamente; k es la constante de reacción aparente que describe la velocidad de desaparición del ácido ascórbico. Esta constante se calcula al graficar Ln(C/C0) contra el tiempo. Al aplicar este modelo a los resultados obtenidos para la degradación del ácido ascórbico en la pulpa de arazá, se encontró la ecuación:
Ln(C/C0) = -0,0063t - 0,1888, con R2 = 0,8937
Al calcular de esta ecuación el tiempo de vida media –tiempo necesario para que la concentración de ácido ascórbico disminuya en un 50%–, se obtiene un valor de 80 d. Este tiempo es menor al reportado para arvejas (Pisum sativum), espinacas (Spinacia oleracea) y fríjoles (Phaseolus vulgaris L.) almacenados también a -20 °C, en los que se obtienen tiempos de vida media de 325, 253 y 311 d, respectivamente (Giannakourou y Taoukis, 2003). Al revisar este experimento, se encuentra que los vegetales fueron escaldados previamente y se congelaron enteros. Si bien para la pulpa de arazá se obtuvo un tiempo de vida media de 80 d, valor relacionado con la calidad química, con la calidad sensorial evaluada a través de un panel entrenado se obtuvo un tiempo de vida media de 30 d, por lo que esta calidad sería la que limitaría el tiempo de vida útil de la pulpa.
En el presente trabajo, los compuestos fenólicos libres aumentaron a partir del día 60. Esto puede deberse a la acción de enzimas del tipo glicosidasas que hidrolizan los enlaces glicosídicos y, como consecuencia, generan las agliconas (compuestos fenólicos libres) y los respectivos carbohidratos (Fennema, 2000), sin conducir a la pérdida de compuestos fenólicos totales.
Medida de la actividad antioxidante
En la figura 4 se muestra que la actividad antioxidante disminuye significativamente en el periodo de almacenamiento ya que pasa de ser buen antioxidante, con 56% de AA, a convertirse en prooxidante, con -14% de AA. De otro lado, en estas medidas se obtuvo 77% de AA para el estándar de BHT. En trabajos anteriores (Vargas et al., 2005), a pesar de haberse usado la misma técnica que la utilizada en esta investigación, las relaciones entre los reactivos cambiaron; por tanto, no se puede pen sar en una comparación coherente sobre los resultados de la actividad antioxidante en pulpa fresca.
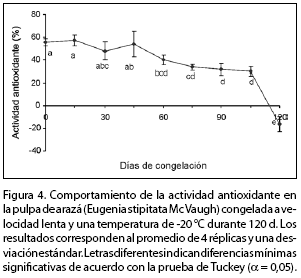
Vale la pena resaltar que durante los primeros 45 d de almacenamiento este atributo no disminuye de manera significativa, por lo que el potencial antioxidante de este fruto congelado sigue siendo equivalente al de la fruta fresca. Luego de 60 d, la actividad antioxidante tiene un descenso significativo: en este momento la actividad representa 72% de la inicial. Al finalizar el almacenamiento, los contenidos de ácido ascórbico, de compuestos fenólicos totales y de carotenoides representan 37%, 85,5% y 92% de su valor inicial, respectivamente. Si bien estos grupos de antioxidantes disminuyeron en diferente proporción durante la congelación, no permiten explicar el porqué la pulpa pasó de ser anti- a prooxidante, ya que durante su congelación la cantidad de compuestos prooxidantes debió aumentar considerablemente, lo que no se pudo comprobar. Dentro del grupo de prooxidantes pueden existir productos de la degradación de los compuestos lipídicos, entre los que se pueden encontrar radicales libres. Este tipo de compuestos puede generarse en el tratamiento de congelación y por causa del almacenamiento prolongado (Jan et al., 2001).
Conclusiones
Los análisis hechos a la pulpa de arazá muestran que la congelación lenta a -20 °C mantiene las características organolépticas en condiciones óptimas durante el primer mes de almacenamiento. En este tiempo la actividad antioxidante permaneció significativamente invariable, al igual que los compuestos fenólicos totales, los carotenoides y la acidez; sin embargo, el ácido ascórbicosedegradósignificativamente,disminuyendo considerablemente el aporte que puede hacer la pulpa de arazá de esta vitamina.
Si la utilización de la pulpa va a hacerse antes de un mes, se puede utilizar la técnica de congelación lenta sin previo escaldado, pues disminuye los costos de producción. Sin embargo, si el empleo de la pulpa se va a hacer luego de periodos más largos de almacenamiento bajo congelación, podría ensayarse técnicas que incluyan el escaldado y la congelación rápida. Por lo tanto, es importante evaluar en el futuro el efecto, tanto del tratamiento de congelación a alta velocidad –los cristales de hielo que se forman son de menor tamaño–, como de la inactivación de enzimas por medio de un escaldado previo y llevar a cabo: análisis de la actividad de las enzimas relacionadas con el deterioro de los componentes que contribuyen a la actividad antioxidante y a la estabilidad de la textura, análisis microbiológicos para complementar el diagnóstico de la calidad de la pulpa y la evaluación sensorial, tanto con panelistas como con consumidores, para definir de mejor manera la vida sensorial útil de la pulpa.
Literatura citada
Bahceci, K.S., A. Serpen, V. Gôkmen y J. Acar. 2005. Study of lipoxygenase and peroxidase as indicator enzymes in green beans: change of enzymes activity ascorbic acid and chorophylls during frozen storage. J. Food Eng. 66, 187-192. [ Links ]
Bartley, I.M. y M. Knee. 1982. The chemistry of textural changes in fruit during store. J. Food Chem. 9, 47-58. [ Links ]
Bernal, D.R. 1992. Análisis de alimentos. Tercera edición. Editorial Guadalupe, Bogotá. pp. 99-100, 114-117. [ Links ]
Conover, W.J. 1980. Practical nonparametric stadistics. 2nd edition. Jhon Wiley & Sons, New York. pp. 299-304, 483. [ Links ]
Dámaso, H.M. y I. Mínguez. 2000. Xanthophyll esterification accompanying carotenoid overaccumulation in chromoplast of Capsicum annuum ripening fruits is a constitutive process and useful for ripeness index. J. Agric. Food Chem. 48, 1617-1622. [ Links ]
Delgado, J.L. 2004. Efecto del procesamiento de crio-concentración sobre el ‘flavor’ de pulpas de arazá. Tesis de maestría. Facultad de Ciencias, Universidad Nacional de Colombia, Bogotá. pp. 9 -16. [ Links ]
Fennema, O. 2000. Química de alimentos. Segunda edición. Editorial Acribia, Zaragoza (España). pp. 593, 669, 805, 1191. [ Links ]
Gadow, A., E. Jobert y C.F. Hansmann. 1997. Comparison of the antioxidant activity of aspalathin whit that of other plant phenols of rootbos tea (Aspalathus linearis) ?? -tocopherol, BHT, and BHA. J. Agric. Food Chem. 45, 632-638. [ Links ]
Giannakourou, M.C. y P.S. Taoukis 2003. Kinetic modeling of vitamin C in frozen green vegetables under variable storage conditions. Food Chem. 83, 33-41. [ Links ]
Hernández, M.S. 2001. Conservación del fruto de arazá (Eugenia stipitata) durante la poscosecha mediante la aplicación de diferentes técnicas. Tesis doctoral. Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. [ Links ]
Hough, G. y S. Fiszman. 2005. Estimación de la vida útil sensorial de los alimentos. Primera edición. Editorial Programa CYTED, España. pp. 13-23 [ Links ]
Jan, P., N. Yanishlieva y M. Gordon. 2001. Antioxidantes de los alimentos. Primera edición. Editorial Acribia, España. pp. 1, 37-39, 319-324 [ Links ]
Quevedo, E. 1995. Aspectos agronómicos sobre el cultivo de arazá. Agronomía Colombiana 12, 27-65. [ Links ]
Narváez, C.E. 2003. Efecto del choque térmico de arazá (Eugenia stipitata Mc Vaugh) sobre la tolerancia al frío. Rev. Col. Quím. 32, 93-102. [ Links ]
Lisiewska, Z. y W. Kmieecik. 2000. Effect of storage period and temperature on the chemical composition and organoleptic quality of frozen tomato cubes. J. Food Chem. 70, 167-173. [ Links ]
Redmond, G.A., T.R. Gormley. y F. Butler. 2003. The effect of short and long-term freeze-chilling on the quality of mashed potato. Innov. Food Sci. Emerging Technol. 4, 85-97. [ Links ]
Vargas, A.M., C.A.P. Rivera y C.E. Narváez. 2005. Capacidad antioxidante durante la maduración del arazá (Eugenia stipitata Mc Vaugh). Rev. Col. Quím. 34, 7-65. [ Links ]
Velioglu, Y.S., G Mazza., L. Gao y B.D. Oomah. 1998. Antioxidant and total phenolics in selected fruits, vegetables, and grain products. J. Agric. Food Chem. 46, 4113-4117. [ Links ]
Vural, G., K.S. Bahceci, A. Serpen y J. Acar. 2005. Study of lipoxygenase and peroxidase as blanching indicator of enzymes in peas: change of enzymes activity ascorbic acid and chorophylls during frozen storage. Food Sci. Technol. 38, 903-908. [ Links ]