Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Agronomía Colombiana
versão impressa ISSN 0120-9965
Agron. colomb. v.25 n.2 Bogotá jul./dez. 2007
Mario Lobo1, Óscar Delgado2, José Régulo Cartagena3, Elizabeth Fernández4 y Clara Inés Medina5
1 Investigador titular, Corpoica, Centro de Investigación La Selva, Rionegro, Antioquia y Profesor asociado, Facultad de Ciencias Agropecuarias, Universidad Nacional de Colombia, Medellín. mlobo@corpoica.org.co
2 Investigador Corpoica, Centro de Investigación La Selva, Rionegro, Antioquia. odelgado@corpoica.org.co
3 Profesor asociado, Universidad Nacional de Colombia, Facultad de Ciencias Agropecuarias, Medellín. jrcartag@unalmed.edu.co
4 Ingeniera agrónoma, Universidad Nacional de Colombia, Medellín. eservi@hotmail.com
5 Investigadora Corpoica, Centro de Investigación La Selva, Rionegro, Antioquia. cmedina@corpoica.org.co
Fecha de recepción: agosto 9 de 2007. Aceptado para publicación: octubre 1 de 2007
RESUMEN
Se estudió la latencia y germinación de semillas de guanábana y chirimoya con el fin de categorizar la latencia de las simientes y desarrollar un protocolo de rompimiento de ésta; conocimiento básico para el establecimiento y monitoreo de un duplicado de seguridad en las colecciones de campo, por la vía de almacenamiento a largo plazo de las unidades de propagación sexuales. No se detectó latencia exógena, a través de la imbibición obtenida por las semillas. Se encontró, a través de pruebas de viabilidad, con tetrazolio, que en cada uno de los taxa existe alrededor de un 20% de unidades no viables en el conjunto de semillas aparentemente normales. La estratificación caliente húmeda, por espacio de 90 días, produjo rompimiento de la latencia, al igual que la imbibición con AG3, con obtención del mejor resultado al imbibir la simiente en 800 ppm de la hormona. En chirimoya se obtuvo efectos sinérgicos al combinar el tratamiento de 800 ppm de AG3 y estratificación caliente húmeda durante 90 días, lo cual no fue evidente en el caso de la guanábana. A partir de los resultados se clasificó el bloqueo de la germinación de las semillas de las dos especies, como latencia morfofisiológica simple, no profunda. La caracterización definida, junto con el protocolo de remoción, apoyan el establecimiento de un duplicado de seguridad de la colección de campo, por la vía de semilla, con un concepto dinámico que se esboza en este escrito.
Palabras clave: recursos genéticos, latencia morfofisiológica, conservación de germoplasma.
ABSTRACT
Cherimoya (Annona cherimola) and soursop (Annona muricata) seed germination and dormancy were studied in order to characterize a dormancy type for both taxa, develop dormancy breaking procedures, and obtain a basic knowledge required for seed viability monitoring for the establishment of long-term seed conservation duplicate of field germplasm collection and utilization of stored germplasm. The presence of exogenic dormancy in seeds was not detected during the imbibition of seeds. About 20% of the apparently normal seeds in both species were non viable based on the results of tetrazolium test. Seed dormancy release was obtained after warm stratification under humid conditions, as well as seed imbibition with GA3, demonstrating the best results for 90 days stratification and 800 ppm of the hormone. In cherimoya, the combination of warm stratification with 800 ppm GA3 produced the highest seed germination, which did not happen with the soursup seeds. Based on the results, the seed dormancy for both species was classified as simple, non-deep morphophysiological dormancy. A dynamic concept described in the current paper for seed behaviour in terms of dormancy and germination provides a support to establish a security duplicate of seed field collection for both species.
Key words: genetic resources, morphophysiological dormancy, germplasm conservation.
Introducción
En Colombia, la chirimoya y la guanábana: Annonaceae, son frutales con potencial, de desarrollo el primero, y con importancia actual el segundo, tanto para consumo en fresco como para procesamiento. El desarrollo de estas especies debe cimentarse en una base genética amplia, con indicación de que en muchos taxa, la cantidad de variabilidad disponible para procesos selectivos es limitada (Cooper et al., 2001) y por tanto, es necesario establecer una colección representativa de la riqueza genética de estos taxa en el país, el cual es parte de la zona de diversidad primaria de las dos entidades biológicas. El conjunto de accesiones obtenidas debe privilegiar materiales locales de agricultor, las cuales poseen amplia diversidad (Lobo, 1992), aspecto que debe categorizarse en sus atributos, para promover su utilización sostenible.
Lo anterior implica el establecimiento de huertos de campo con las poblaciones colectadas y la necesidad de conformar un duplicado de seguridad de éstas. La semilla de la chirimoya y la guanábana es ortodoxa (Ferreira y Pinto, 2005; Hong et al., 1996), esto es que soporta desecación, lo cual permite bajar el contenido de humedad y almacenarla a baja temperatura por períodos considerables (Engelmans y Engels, 2002). Lo precedente señala que la preservación por esta vía puede utilizarse como respaldo a la colección de campo. Por este medio, se puede almacenar una mayor variabilidad de los demes de la metapoblación colectada, con alelos provenientes de un conjunto más representativo de los individuos de cada subpoblación. Por el contrario, los materiales de campo se establecen con un número reducido de árboles por material. Adicionalmente, las accesiones sembradas pueden estar sujetas a condiciones bióticas y abióticas desfavorables (Pinto y Andrade, 2005), lo que indica que el duplicado de semillas es importante, como respaldo a las pérdidas de colectas que pueden ocurrir en los huertos ex situ. Los frutales perennes son especies con un proceso incipiente de domesticación, aspecto derivado del hecho de que muchos de éstos han pasado de ser plantas silvestres a cultivadas, con un síndrome de la domesticación incompleto (Gepts, 2002).
Esto conduce a pensar que las semillas exhiben latencia, la que se ha definido como un bloqueo al proceso para completar la germinación de unidades de propagación intactas y viables, bajo condiciones favorables (Finch-Savage y Leubner-Metzger, 2006). El proceso ha evolucionado en forma diferente en las especies a través de la adaptación a las condiciones prevalentes del ambiente en el que se encuentran éstas, de forma que la germinación toma lugar cuando las condiciones para el establecimiento de una nueva generación de plantas son apropiadas para la supervivencia (Finch-Savage y Leubner-Metzger, 2006; Fenner y Thompson, 2005; Baskin y Baskin, 2004). Al respecto, se ha indicado que la latencia no está asociada únicamente con la ausencia de germinación y que más bien está relacionada con los atributos de la semilla que determinan las condiciones requeridas para que proceda la emergencia del embrión (Fenner y Thompson, 2005; Thompson, 2000). En línea con lo anterior Koornneef et al. (2002) afirmaron que la latencia y la germinación son determinadas por una interacción entre el potencial de crecimiento del embrión y las restricciones impuestas por los tejidos que rodean éste. En diversos géneros y especies de la familia Annonaceae, se ha reportado la presencia de latencia morfológica y morfofisiológica (Baskin y Baskin, 2001).
La primera ocurre en semillas con embriones rudimentarios y laminares, en las cuales la mayoría de la simiente está ocupada por el endosperma y el embrión corresponde aproximadamente a un 1% del volumen de la unidad de propagación sexual (Nikolaeva, 1969); estos presentan diferenciación, sin estar latentes y simplemente necesitan tiempo para crecer y germinar (Finch-Savage y Leubner-Metzger, 2006). En la segunda, adicionalmente al embrión rudimentario, un mecanismo fisiológico inhibe la germinación de la semilla (Baskin y Baskin, 2001; Baskin y Baskin, 2004), por lo cual hay que emplear protocolos de estratificación, los que, en algunos casos, pueden remplazarse por aplicación de ácido giberélico, AG3, (Finch-Savage y Leubner-Metzger, 2006). En el contexto anterior, se ha reportado latencia morfológica en Annonaceae de los géneros Cyathocalix, Rollinia y Annona (Annona squamosa y Annona cracifolia) y morfisiológica en taxa de los géneros Goniothalamus, Mitrephora, Monocarpia, Paeaunthus, Polyanthia, Xylopia, Unonopsis y Annona, específicamente en Annona coriaceae y Annona spraguei (diversos autores, citados por Baskin y Baskin, 2001).
Igualmente, se ha encontrado latencia fisiológica y embriones inmaduros en Annona crasiflora (Da Silva et al., 2007). Con relación a los taxa cultivados de Annona, se ha señalado que las semillas presentan generalmente una germinación irregular, lo que dificulta la propagación sexual (Pinto, 2005b; Padilla y Encina, 2003). Igualmente, se ha afirmado que este tipo de comportamiento es debido a diferentes niveles de latencia (Ferreira et al., 1999; Moreno et al., 1999; Pinto, 1975), con reportes no concordantes sobre la presencia o ausencia de ésta, lo cual ha sido atribuido, por Pinto (2005a), al grado de madurez de la semilla en los diversos trabajos y que ésta puede ser inducida por factores climáticos, en lugar de ser innata. Tomando como referente el establecimiento de un duplicado de la colección de campo de las Annona, por medio de semillas, se hace necesario establecer protocolos que permitan medir la viabilidad de la semilla a través de pruebas de germinación y la necesidad de multiplicar materiales para actividades de investigación y transferencia, con estas especies, se planteó la investigación actual. Esta buscó categorizar latencias en las simientes de chirimoya y guanábana y obtener protocolos de remoción de los bloqueos a la germinación.
Materiales y métodos
Localización
Los trabajos se llevaron a cabo en el Laboratorio de Semillas del Centro de Investigación La Selva, de la Corporación Colombiana de Investigación Agropecuaria Corpoica), localizado en Rionegro, Antioquia a 2.120 msnm, con una temperatura promedio de 17 °C. El sitio, donde se encuentra el Centro, presenta una humedad relativa del 78% y pertenece a la formación ecológica bosque húmedo montano bajo (Espinal, 1977).
Material biológico
Las semillas de ambas especies se extrajeron de frutos obtenidos en la Central Mayorista de Antioquia que presentaban un estado fisiológico uniforme, bajo la hipótesis de que las poblaciones objeto de conservación corresponden a mezclas de árboles de una zona dada y, por tanto, a una muestra de los genes presentes en cada accesión (Fernández, 2004).
Extracción de la semilla
Esta se obtuvo a partir de frutos en completa madurez y blandos al tacto. Para ello se separó la semilla de la pulpa y el arilo; las unidades de propagación sexual se lavaron y luego se colocaron en toallas de papel absorbentes con el fin de secarlas. Antes de realizar los estudios, se eliminaron aquellas en apariencia vanas y las que exhibían daños mecánicos. Lo último es concordante con los procesos de selección de simientes para su conservación en los bancos de germoplasma.
Obtención de una curva de secado de las semillas
Con el fin de simular las condiciones de contenido de humedad de las semillas, en conservación en los cuartos fríos (alrededor del 7%), se estandarizó un protocolo de secado, para obtener una curva de pérdida del agua contenida en éstas. Para lo anterior, se utilizaron cámaras herméticamente selladas, con sílica gel en el fondo en proporción 1:1 (peso de semilla a peso del desecante). Enéstas se colocaron grupos de 100 simientes, a las cuales se les determinó el contenido inicial de humedad. La curva obtenida se utilizó para calcular el tiempo de secado, hasta el 7% de contenido de agua, para cada uno de los lotes incluidos en los estudios de la presente investigación. Adicionalmente, se monitoreó el contenido de humedad, mediante secado en estufa a 80 °C, hasta que las semillas alcanzaron peso constante y gravimetría a grupos de muestras aleatorias de las unidades de propagación, colocadas en las cámaras de extracción de humedad. El curso de la pérdida de humedad se determinó en lotes de 100 semillas, con cuatro repeticiones, a través de muestras periódicas, en principio cada hora y luego a intervalos mayores.
Protocolo de tinción con tetrazolio
Para medir la viabilidad de los embriones, se empleó, en ambas especies, la metodología de tinción con tetrazolio, propuesta por la Asociación Internacional de Chequeo de las Semillas (ISTA,1995) con evaluación de diversos cortes antes de la aplicación del protocolo. Estos incluyeron: corte longitudinal dorsal, corte longitudinal ventral, corte transversal ventral y eliminación de la testa. Para ello, se emplearon 15 semillas por tratamiento, con dos repeticiones. Las unidades de propagación se incubaron, bajo condiciones de oscuridad, en la solución de tetrazolio al 1,0% durante 24 h, a 30 ºC y luego se hizo la evaluación de la tinción obtenida en el embrión. El tetrazolio interactúa con los procesos de reducción y oxidación de las células vivas en la semilla, por lo cual, las formas hidrogenadas cambian de color, lo que hace posible distinguir las partes vivas (coloreadas) de aquellas muertas (incoloras) (Poulsen et al., 2006).
Determinación de imbibición de las semillas por agua
Los ensayos se llevaron a cabo para determinar si las semillas son impermeables al agua, indicativo de latencia exógena física, tópico que debe evaluarse en forma previa a las pruebas de germinación (Baskin y Baskin, 2001). Para ello, se colocaron simientes, con un 7% de contenido de humedad, a imbibir en toallas de papel humedecidas, en el interior de recipientes plásticos con tapa hermética. El estudio se realizó en las condiciones de temperatura ambiente, se pesaron en el tiempo cero y a intervalos de una hora, en principio hasta las 12 horas, con una determinación final a las 24 horas. En cada uno de estos períodos se removieron las semillas, se secaron externamente con papel absorbente y se obtuvo su masa. El incremento en peso indica que las semillas son permeables, en tanto que el no incremento señala que estas poseen testas impermeables (Bansal et al., 1980). La categorización anterior, la cual está relacionada con latencia exógena física, se realizó con cuatro repeticiones de 50 semillas, en cada una de las dos especies.
Categorización de la germinación
Esta se realizó, para ambas especies, en cámaras de germinación, con termostato, a una temperatura de 27±1 oC, seleccionada teniendo en cuenta el intervalo utilizado en diferentes Annona (Colauto et al., 2003; Padilla y Encina, 2003; Vilar et al., 2005). Cada unidad experimental constó de 50 semillas, con cuatro repeticiones por tratamiento a evaluar, lo cual está de acuerdo con lo señalado por Baskin y Baskin (2001). Las unidades de propagación se colocaron en hojas simples de papel filtro, en cajas de Petri que se humedecieron periódicamente. Los ensayos se condujeron durante 30 días, aspecto recomendado por Baskin y Baskin (2001), cuando se obtiene incremento en los porcentajes de germinación luego de dos semanas de iniciada la prueba. Las simientes no germinadas en este período se consideraron como latentes o no viables, con diferenciación de las dos categorías a través de la aplicación del protocolo de tetrazolio.
Evaluación de protocolos de rompimiento de latencia
A partir de los reportes sobre latencias morfológica y morfofisiológica, en semillas de diversas especies de la familia Annonaceae (Baskin y Baskin, 2001), se evaluaron métodos reportados para su rompimiento, los cuales correspondieron a estratificación caliente y fría, para la primera categoría y aplicación de ácido giberélico para la segunda. Para la estratificación caliente se incubaron semillas, de los dos taxa, en cámaras con y sin suministro de humedad, a 25 °C, durante diferentes intervalos: 30, 60 y 90 días, con extracción de 25 unidades de propagación en cada repetición y para los diferentes tiempos. La estratificación fría se condujo a 8 °C, colocando las semillas en un refrigerador, en cámaras plásticas, herméticamente selladas, con suministro de humedad. Al igual la estratificación caliente, la incubación se realizó durante 30, 60 y 90 días.Una vez finalizadas las estratificaciones caliente y fría, se realizaron pruebas de germinación, con unidades experimentales de 25 semillas por tratamiento y cuatro repeticiones. Estas se condujeron durante 30 días, en cámaras de germinación, con control de la temperatura a 28 °C. Para lo anterior, se empleó un diseño completamente al azar y, adicionalmente, se incluyó un testigo absoluto, sin tratamiento alguno para la remoción de latencia. A partir de los resultados se evaluó el efecto de la imbibición previa con AG3 sobre la germinación en dosis de 200, 400, 600, 800 y 1.000 ppm, en comparación con estratificaciones húmedas, caliente y fría por espacio de 90 días y una combinación de las dosis de AG3 y las dos estratificaciones, con testigos absolutos, sin tratamiento de remoción de latencia alguno en las dos especies. La evaluación de germinación se llevó a cabo en la misma forma descrita para las estratificaciones caliente y fría.
A medida que se aplicaron los diferentes métodos de rompimiento de latencia endógena para cada uno de los tratamientos utilizados (estratificación caliente o fría, y ácido giberélico), fue necesario desinfestar las semillas semanalmente con una solución de hipoclorito de sodio al 2,6%, ya que se encontraron hongos de los géneros Fusarium y Rhizopus como patógenos contaminantes. Las variables registradas en cada ensayo fueron: porcentaje de germinación obtenido a los 30 días de establecidas las pruebas de germinación, con base en el numero de semillas viables de cada una de las unidades experimentales y porcentaje de latencia, el cual corresponde a semillas no germinadas teñidas con la solución de tetrazolio. Adicionalmente, se determinó el porcentaje de semillas no viables por especie, en los lotes empleados en los dos estudios de germinación. Esto se hizo mediante la tinción con tetrazolio de las semillas no germinadas, lo cual permitió distinguir entre las semillas latentes y las no viables. Con cada una de las variables registradas: porcentaje de germinación total y de semillas latentes, se llevó a cabo un análisis de varianza en forma individual para cada especie. Para efectos del análisis estadístico, los porcentajes se transformaron a arcoseno, lo cual es recomendable cuando se tiene una amplitud en los porcentajes superior a 40 (Little y Hills, 1976). Los análisis de varianza tuvieron como fuente de variación: tratamientos, correspondientes a los diferentes procedimientos evaluados para rompimiento de latencia, por ensayo y error experimental. De acuerdo con la significación obtenida para los tratamientos, se aplicó la prueba de Student, con una probabilidad de error P≤0,05.
Resultados y discusión
Curva de secado de las semillas
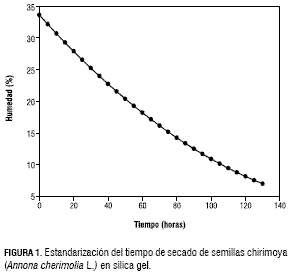
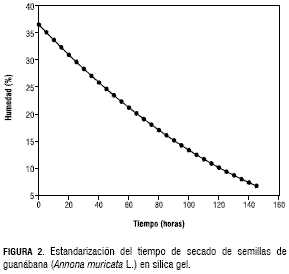
La figura 1 presenta la curva de secado obtenida con las semillas de chirimoya y en la figura 2, la lograda con las unidades de propagación de guanábana, al ser introducidas en cámaras herméticamente selladas con sílica gel en el fondo y mantenidas a una temperatura entre 25 y 30 °C. En ambos casos el curso de la pérdida de humedad se ajustó a modelos cuadráticos altamente significativos (P<0,01). Las expresiones matemáticas fueron: y = 29,302 - 0,5299x + 0,0021x2, en el caso de chirimoya y y = 33,65 - 0,302x + 0,000747x2 en el de guanábana. Las curvas obtenidas son útiles para predecir el tiempo requerido para la obtención de una humedad determinada, a partir del contenido de inicial de ésta, de acuerdo con el procedimiento indicado por Rao et al. (2006). En el caso actual, se obtuvo un contenido de humedad del 7% en las unidades de propagación de chirimoya luego de 128 horas en las cámaras en chirimoya y de 145 horas en guanábana, a partir de contenidos iniciales de humedad de 33,6 y 36,5%, respectivamente.
Protocolo de tinción con tetrazolio
La mejor tinción con tetrazolio, evaluada visualmente, se obtuvo con los cortes longitudinales: dorsal (figura 3a) y ventral (figura 3b), en comparación con las semillas a las cuales se les eliminó la testa (figura 3c) y aquellas a las que se les practicó un corte transversal (figura 3d). En los dos primeros procedimientos se apreció penetración del producto hasta el embrión, con presencia de color rojo intenso de éste en las semillas viables. En consecuencia, se decidió evaluar la viabilidad de las semillas mediante la aplicación del químico al primer tipo de corte.El cloruro de tetrazolio, como se indicó previamente, interactúa con los procesos de oxidación y reducción de las células vivas de la semilla, con cambio en el color de la forma hidrogenada; lo anterior permite distinguir las partes vivas, con coloración roja en la semilla, de las muertas, que no exhiben tinción (Poulsen et al., 2006). El procedimiento es útil para distinguir entre semillas vivas y latentes ya que en las Annonaceae hay problemas de polinización que pueden conducir a la presencia de simientes sin embrión.
Al respecto, Pinto y Andrade (2005) indicaron, en el caso de la chirimoya, que la polinización es baja debido a la ocurrencia de poblaciones pequeñas de insectos polinizadores y a la antesis lenta, lo que reduce las visitas de éstos, aparte de que las flores exhiben protoginia y dicogamia. Al respecto, Guirado et al. (2001) indicaron que es común un bajo cuajamiento de los frutos de esta especie, y que aun en los casos en que la polinización natural es suficiente, los insectos no cubren todos los estigmas con polen. Con información por parte de Rubí (1994) y Martínez y Vidal (1993) (citados por Franco et al., 2001), que normalmente el cuajamiento de frutos en las plantaciones de chirimoya y guanábana es reducido, con valores del 8 y 25% respectivamente para las dos frutas, por lo cual los autores recomendaron polinización manual. También González et al. (2006), reportaron un mayor índice de semillas, medido como el número de éstas por 100 g de peso fresco de fruto, como resultado de polinización manual en chirimoya. Rosell et al. (2006) reportaron que el polen de esta especie tiene un período de viabilidad y germinación reducido. Pinto (2005) señaló como factores que inciden en forma importante en la polinización de las Annona, aparte de la protoginia, la dicogamia y la ausencia de polinizadores, las condiciones ambientales y la viabilidad del polen.
Categorización de la germinación
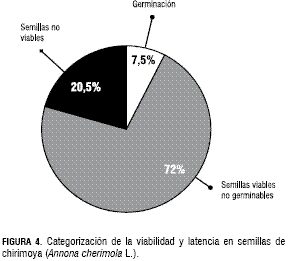
En la figura 4 se incluye la categorización de viabilidad (germinación y latencia) y no viabilidad obtenida con las semillas de chirimoya (falta de tinción con tetrazolio), y en la figura 5, los mismos parámetros para las unidades de propagación de guanábana. Como se observa en la figura 4, las semillas de chirimoya exhibieron un 80% de viabilidad y un 20% de no viabilidad, con 8% de germinación y 72% de semillas latentes, monitoreada a través de la prueba de tetrazolio, a los 30 días de incubación de éstas. Por su parte, las simientes de guanábana presentaron 69% de viabilidad, sin evidencias de germinación a los 30 días y 31% de individuos no viables (figura 5). Los resultados permiten inferir la presencia de latencia en las dos especies; la cual, en el caso actual, fue más notoria en las simientes de guanábana, taxón que no exhibió germinación durante los 30 días de duración de la prueba. Se ha indicado que en condiciones espontáneas, las plantas tienen que responder a condiciones variables en tiempo y espacio, constituyendo la latencia una estrategia paradispersar la germinación en tiempo (Snyder, 2006).
La germinación reducida de las Annona, constituye un común denominador en la literatura. Así, Colauto et al. (2003) reportaron germinaciones en atemoya (Annona cherimola Mill. x Annona squamosa L.), sin tratamientos de remoción de latencia, del orden del 1 hasta el 5% de emergencia y del 3,8% con simientes de Annona squamosa L., en un período de 63 días. En el mismo contexto, Infante y Moreno-Casasola (2005) encontraron germinaciones inferiores al 20%, luego de 120 días, en Annona glabra. Vilar et al. (2005), por su lado, obtuvieron un valor máximo de germinación, con el taxón Annona montana de 55% a 30°C y de 25% a 25 °C, luego de 56 días. También Da Silva et al. (2007) notificaron que la germinación de las simientes de Annona crassiflora ocurría después de 150 días de la siembra e incluyeron una información de Rizzini (1973), quien indicó que ésta tomaba entre 230 y 300 días, a nivel de campo. En consonancia, Padilla y Encina (2003) señalaron que uno de los problemas relacionados con la multiplicación de la chirimoya, a través de semilla sexual, es su germinación pobre e impredecible. Los autores añadieron que la brotación de simientes, recién cosechadas, puede ser ampliamente variable, con presentación de datos obtenidos a lo largo del año, los cuales fluctuaron entre 13,5 y 52,55%, con una media de 33,3±15,9, al incubar las simientes durante 45 días. Padilla y Encina (2003) incluyeron datos obtenidos con este taxón, por parte de George y Nissen (1987), e Ibar (1979), quienes informaron que la emergencia de los embriones ocurría en el intervalo entre 30 y 80%, sin indicación del número de días relacionados con las cifras anteriores.
Sobre lo anterior, Pinto (2005) escribió que la germinación de la Annona ocurre en un período prolongado, lo cual fue atribuido a diferentes niveles y tipos de latencia. Al respecto, Hayat (1963) informó que la germinación de las semillas de Annona squamosa demora entre 1 y 3 meses, lo cual atribuyó a una tasa de crecimiento lenta por parte de los embriones. Baskin y Baskin (2001) recomiendan, para la evaluación del porcentaje de semillas germinables, un tiempo máximo de 30 días. Las semillas que germinan después de este período pueden considerarse latentes. Sobre esto, Finch-Savage y Leubner-Metzger (2006) puntualizaron que la definición de la latencia se basa en la ausencia de germinación. Este es un mecanismo de dispersión de la germinación en tiempo, para asegurar la preservación de las especies (Foley, 2001), el cual es notorio en las Annona, dada su domesticación incipiente; este aspecto fue indicado por Gepts (2002), en forma generalizada, para los frutales perennes. También fue evidente, en ambos frutales, la existencia de semillas no viables, lo cual podría estar relacionado con problemas de polinización, como ya se indicó. Esto señala, en el caso del manejo de colecciones de semilla de las dos especies, la necesidad del desarrollo de procedimientos que permitan diferenciar este tipo de unidades, para asegurar el almacenamiento de un número mínimo de individuos viables.
Categorización de la latencia
Latencia física (exógena)
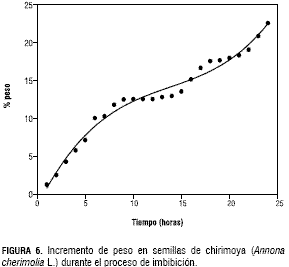
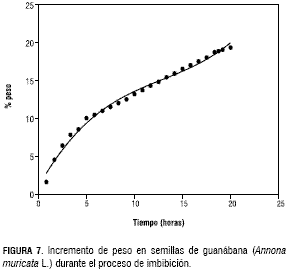
Como se puede observar en las figuras 6 y 7, durante las 24 horas de incubación en agua de las simientes de chirimoya y guanábana, éstas imbibieron, lo que se tradujo en un aumento de peso de alrededor del 20%. Lo anterior señala la ausencia de impermeabilidad en la testa de las semillas de las dos especies y consecuentemente de latencia exógena o física, Baskin y Baskin (2001, 2004). Finch-Savage y Leubner-Metzger (2006) señalan que la impermeabilidad es causada por capas de células de empalizada en la semilla que controlan el movimiento del agua. Los resultados difieren de los presentados por otros investigadores, con diversas especies de Annona. Así, Ledo y Cabanelas (1997) indicaron que la aplicación de procedimientos de escarificación a las semillas de guanábana produjo incremento en la germinación; también Lemos et al. (1987) señalaron efectos positivos de la escarificación en simientes de Annona squamosa, con información por parte de la FAO (1988), de que Annona senegalensis responde al tratamiento anterior. En sentido contrario, Ferreira et al. (1997) verificaron que las semillas de Annona squamosa y las del híbrido interepecífico Atemoya, Annona cherimola Mill. X Annona squamosa L., no presentaban impedimentos físicos a la entrada del agua, lo cual los condujo a descartar la presencia de impermeabilidad en la testa de las unidades de propagación. Resultados similares fueron notificados por Esquinca et al. (1997) con el taxón Annona diversifolia. Por su parte, Castillo el al. (1997) y De Smett et al. (1999) indicaron un efecto muy leve en la germinación, en chirimoya, como secuela de la escarificación.
Latencia morfológica
En la tabla 1 se incluyen los resultados a partir de procedimientos de estratificación caliente y fría aplicados a las semillas de chirimoya y guanábana, referidos a las semillas viables; luego del estudio se encontró 20,3% y 24,8% de semillas no viables en la chirimoya y la guanábana respectivamente. Como puede apreciarse, la estratificación caliente en ambiente húmedo, a los 30, 60 y 90 días, causó un incremento sensible en la germinación de la chirimoya, en comparación con el testigo. Con esta especie, los mayores valores se obtuvieron en el tratamiento de 90 días. En el caso de la guanábana, la estratificación caliente húmeda produjo germinación en las simientes sometidas a ésta por espacios de 60 y 90 días, con un valor, significativamente superior a los 90 días, sin que se obtuviera emergencia alguna de los embriones, en las unidades de propagación sexual no tratadas, durante los 30 días de duración de la prueba. Con las dos especies no se apreció germinación alguna, con las estratificaciones caliente sin cámara de humedad y fría húmeda.
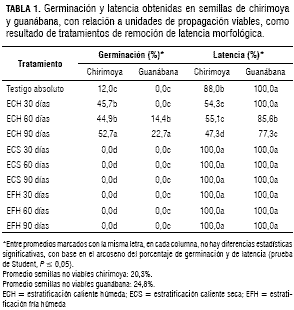
En ambas especies, el efecto positivo de la estratificación caliente húmeda, apunta a la presencia de latencia morfológica que se caracteriza por la presencia de embriones pequeños que tienen que crecer para que las semillas puedan germinar, lo cual ocurre después de la dispersión de estas a partir de la planta madre (Baskin y Baskin, 2001). La posmaduración de las semillas se ha considerado que no es un cambio abrupto de un estado de latencia a uno de germinación (Foley, 2001), al contrario, las simientes adquieren la capacidad de responder a un conjunto de condiciones que restringen la germinación (Bewley y Black, 1994; Baskin y Baskin, 2001). Durante el estudio, se evaluó el crecimiento de los embriones, en los tratamientos de estratificación caliente, y se encontró como promedio de las dos especies, que éstos pasaron de 3,6 a 9,9 mm, hecho que corrobora la presencia de latencia morfológica, referida a embriones poco desarrollados. Scheldeman (2002) indicó que el embrión de las semillas de chirimoya es rudimentario y muy pequeño, entre 3 y 4 mm. En línea con lo anterior, Da Silva et al. (2007) reportaron en Annona crasiflora, especie con latencia morfológica, un crecimiento de los embriones desde un tamaño inicial de 1,6 hasta 6,0 mm, en forma previa a la germinación. Cabe señalar que Hayat y Canright (1965), en un estudio anatómico de las Annonaceae, el cual incluyó algunas Annona, entre ellas la guanábana, indicaron que en los embriones, cuando tienen alrededor de 3 mm, presentan un patrón de organización definido sin que se aprecie un tejido meristemático visible entre los dos cotiledones en el ápice; éste es evidente en la parte terminal del epicótilo al lograr el embrión 7 mm, pero aún las células son inactivas en cuanto a elongación y división. Lo anterior apoya la necesidad del crecimiento de los embriones, hasta alcanzar un tamaño en el que puede proceder la germinación; esto implica que las células meristemáticas estén activas. En el caso de los dos taxa del estudio, se apreció el mayor tamaño de éstos alrededor de los 9 mm.
La respuesta diferencial entre la chirimoya y la guanábana del tiempo requerido para la obtención de mayor germinación, con relación al testigo, en la primera especie y al logro de ésta en la segunda, podría estar relacionada con la temperatura del proceso, 25 °C. En ese sentido, mientras la chirimoya se encuentra en la zona altoandina, la guanábana proviene de zonas tropicales bajas, por lo cual podría requerir una temperatura más elevada en el período de estratificación. Al respecto, diversos autores, citados por Baskin y Baskin (2001), señalaron que la temperatura óptima para el crecimiento de los embriones, de un número importante de especies, está en el intervalo de 15 a 30 °C. El comportamiento obtenido, con los taxa objeto del estudio, está en relación directa con lo que ocurre en sus hábitats espontáneos. En estos la semilla es dispersada en la época seca, la cual coincide con temperaturas más elevadas. De germinar la simiente, al entrar en contacto con humedades transitorias en el suelo, podría morir fácilmente. Por ello, en este período, con el estímulo de la temperatura, maduran los embriones y la simiente queda lista para germinar en el período lluvioso.
Latencia morfofisiológica
Como puede percibirse en la tabla 2, lo obtenido con las dos especies apunta a la presencia de latencia morfofisiológica, la cual corresponde a la categoría de latencia simple no profunda, de acuerdo con el criterio de clasificación presentado por Nikolaeva (1977) y Baskin y Baskin (1991). Esta se rompió con estratificación caliente, como puede observarse en el incremento en germinación entre las semillas del testigo y las sometidas a estratificación caliente durante 90 días en el caso de la chirimoya, y en el de la guanábana donde se pasó de no germinación a la obtención de esta a través de la aplicación del protocolo. Adicionalmente, se cumplió el segundo criterio para este tipo de latencia, el cual corresponde a la remoción del bloqueo de la germinación con la sola aplicación de ácido giberélico AG3, con obtención de la mejor respuesta mediante la aplicación de 800 ppm de la hormona. Bassin et al. (1995) señalan que en este tipo de latencia, además de la presencia de embriones pequeños, existe latencia fisiológica, la cual debe ser removida para la obtención de la germinación. En consonancia con la respuesta obtenida con el AG3, Colauto et al. (2003) consiguieron incrementos sensibles en la germinación de semillas de atemoya (Annona cherimola Mill. X Annona squamosa) al aplicar la fitohormona AG3, en dosis entre 50 a 100 ppm. Adicionalmente, los investigadores lograron incrementos significativos en la emergencia de los embriones de Anona squamosa, con 50 ppm de AG3.
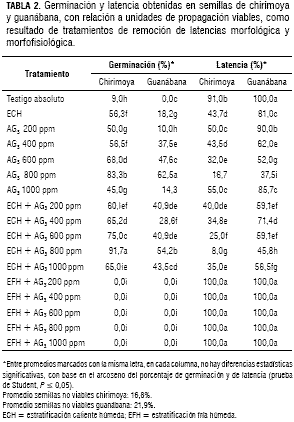
La latencia morfofisiológica ha sido reportada en diversas especies del género Annona. Así, Baskin y Baskin (2001) incluyeron informes sobre taxa con este tipo de bloqueo de la germinación en Annona coriaceae y Annona spraguei; igualmente, Da Silva et al. (2007) presentaron evidencias de embriones inmaduros y latencia fisiológica en Annona crassiflora. Pinto (1976) obtuvo incrementos en la germinación de semillas de guanábana con aplicación de 300 mg·L-1 de AG, y Hernández (1993) notificó aumentos sensibles en la germinación de chirimoya a través de la imbibición con AG, 100 mg·L-1. Adicionalmente, Ferreira et al. (2002) obtuvieron incrementos estadísticamente significativos en cuanto a emergencia de los embriones de Annona squamosa, con aplicaciones de AG, y Da Silva et al. (2007) describieron un efecto promotor del AG, que provocó germinación en semillas de Annona crassiflora. La combinación de la estratificación caliente húmeda y aplicación de ácido giberélico, tuvo un efecto sinérgico en la chirimoya, con obtención de la mayor acción positiva en la imbibición de la semilla con 800 ppm de AG3, e incubación posterior, durante 90 días en la cámara húmeda. Con el tratamiento anterior, se logró una germinación del 91,7%, y una no remoción de latencia del 8,3% de las simientes viables, como se observa en la tabla 2.
En contraste, la mayor emergencia de embriones en guanábana se obtuvo mediante la imbibición con 800 ppm de AG3, una germinación del 62,5% y una latencia del 37,55, exhibiendo diferencias significativas con los demás tratamientos. Con el último taxón no fue evidente la complementación entre la aplicación de la fitohormona y la estratificación caliente húmeda (tabla 2). Como se indicó previamente, es posible que la semilla de guanábana requiera una mayor temperatura para la estratificación caliente, dado su origen tropical bajo. Vilar et al. (2005) encontraron con la especie relacionada tropical Annona montana, que su germinación era considerablemente superior a 30 °C que a los 25 °C, 55% contra 25%, sin germinación alguna a los 20 °C. Lo anterior señala la importancia de la temperatura en el proceso germinativo, aspecto que es dependiente de la especie y aun del genotipo dentro de cada taxón y del conjunto de condiciones en las cuales se incuba la semilla. En este contexto, se ha indicado que la guanábana es la Annona más tropical (Popenoe, 1939; Nakasone y Paull, 1998), con origen probable en Centroamérica, las Antillas o el norte de Suramérica (Pinto, 2005a), la cual se cultiva desde el nivel del mar hasta los 1.200 msnm (Pinto y Silva, 1994).
Mata y Moreno-Casola (2005) informaron que las especies Annona crassiflora y Annona glabra difieren en el tipo de ambiente al cual responden para germinar, con adición de que el rompimiento de la latencia se produce bajo las condiciones ambientales a las cuales están adaptados cada uno de estos taxa. En la investigación no se obtuvo germinación alguna, con las dos especies en la estratificación fría húmeda, aun en los casos de imbibición previa con AG3 (tablas 1 y 2). Esto es un indicativo de posible inducción de una latencia secundaria por las bajas temperaturas. Este aspecto debe tomarse en consideración durante el almacenamiento de la semilla, aun cuando la diferencia es que el almacenamiento se realiza con bajo contenido de humedad, en empaques que no tienen intercambio de agua con el medio ambiente de conservación. Al respecto, se ha indicado que las semillas de chirimoya toleran desecación hasta 4,8% de humedad y las de guanábana hasta 5%, lo cual es un eferente para su mantenimiento a bajas temperaturas (Ferreira y Pinto, 2005). Se ha señalado que la latencia secundaria ocurre al ser sometidas las semillas maduras, después de su dispersión, a condiciones ambientales que inducen este estado (Bewley y Black, 1994), con información de que esta puede presentarse luego de la maduración de las semillas o aún en semillas con embriones no completamente desarrollados (Foley, 2001), como es el caso las dos Annona objeto del estudio actual.
Consideraciones generales
La presencia de semillas latentes fue descrita por Teofrastohace 2.300 años y se cree que fue detectada desde el principio de la agricultura (Jurado y Flores, 2005). Tweddle et al. (2003), postularon que la latencia de las semillas, en conjunción con el hecho de que éstas sean ortodoxas, tiene gran importancia en la ecología de la regeneración poblacional, atributos que se presentan en las semillas de chirimoya y guanábana. Estas fueron categorizadas como ortodoxas por parte de Ferreira y Pinto (2005) y Hong et al. (1996); en esta investigación se pudo definir la presencia de latencia morfofisiológica simple no profunda. Lo anterior indica, de acuerdo con Liu et al. (2005), que en condiciones naturales, luego de la dispersión de las unidades de propagación, estas pueden soportar períodos de sequía, bajas temperaturas y esparcir su germinación en espacio y tiempo. Se ha indicado que una de las dificultades al comparar la germinación y la latencia entre taxa es la variación intraespecífica (Pezzani y Montaña, 2006). Esta puede depender de diversidad genética, condiciones ambientales locales durante el crecimiento de las plantas madres y la maduración de la semilla, posición de esta en el vegetal, calidad del suelo y otros factores naturales (Karlsson y Milberg, 2007).
Lo anterior indica la dificultad para comparar los datos obtenidos con las simientes de chirimoya con los de guanábana, por ello, se consideraron en forma independiente. Así mismo, la información obtenida, además de permitir categorizar el tipo de latencia, debe validarse y extenderse a otros tópicos como son: exploración de las temperaturas y tiempo de estratificación y evaluación de dosis de AG3, en especial para la especie guanábana. Otro tópico relevante es la evaluación de la germinación en diversas accesiones de las colecciones de chirimoya y guanábana Colombia, con repetición a lo largo del tiempo, de forma que se cubran diversas épocas climáticas y con registro de los factores ambientales prevalentes durante el desarrollo de las semillas. Diferencias en la germinación a nivel intraespecífico han sido reportados en diversas especies; por ejemplo, Pérez- García et al. (2006) señalaron variación entre genotipos de Hypericum perforatum, sometidos a condiciones similares para su germinación. Los autores indicaron emergencias entre el 6 y 98%, en 68 poblaciones silvestres del taxón. De acuerdo con Ferreira (2001), la mayoría de colecciones de Annona, se conservan como bancos de campo, llamados también repositorios clonales o colecciones de plantas vivas.
Estos tienen una serie de limitantes, como son: altos costos de mantenimiento; representación de cada población por un número reducido de plantas, con estrechamiento genético de la variabilidad de las accesiones; riesgos de pérdida por enfermedades, incendios y otros fenómenos naturales, y la necesidad de disponer de un duplicado de seguridad en otra localidad, lo cual es oneroso. Dado que las dos especies de la referencia poseen semilla ortodoxa, con latencia morfológica simple, no profunda, se facilita la conservación de un duplicado de campo por la vía de la simiente. En los bancos de campo se han establecido frutales tropicales que se almacenan preferiblemente como material clonal (Tao, 2001), los cuales representan combinaciones deseadas de genes y no la variabilidad de las especies. El duplicado de seguridad por semilla permite colectar una muestra más amplia de los genes de cada deme, con la obtención de unidades de propagación sexual del mayor número de árboles posibles. Esta ingresa a conservación a largo plazo y además permite el establecimiento en campo de individuos multiplicados por la vía sexual, como complemento a los clones previamente existentes.
Con el almacenamiento en cuartos fríos y el mantenimiento en campo, es posible establecer un modelo de conservación dinámico del germoplasma, el cual se basa en conservación a largo plazo de la semilla colectada, incluyendo la de los materiales presentes previamente en la colección y conformación de colecciones activas, logradas a partir de semillas de polinización abierta, lo que permite enriquecimiento genético de las plantas madres. Esta semilla se monitorea y renueva cuando sea necesario a partir de una nueva cosecha de simientes producida por librepolinización, en la colección de campo, lo que permite disponer de una base genética más amplia para procesos de selección, clonación e hibridación, con los dos frutales de la referencia. La conservación anterior se considera dinámica ya que permite conservar semilla sexual obtenida a partir de cada una de las poblaciones colectadas y favorece la recombinación de todas las poblaciones establecidas en el huerto de campo, en contraste con la llamada “conservación estática”, en la cual se mantiene cada subpoblación con cambios genéticos mínimos. El apoyo al modelo de conservación anterior parte del conocimiento logrado en la investigación actual, la cual dio luces sobre el tipo de latencia presente en las simientes de chirimoya y guanábana, con identificación de los protocolos a utilizar para lograr germinación, en procesos de monitoreo y utilización del germoplasma. Estos, como se indicó, deben perfeccionarse, con estudio de aspectos como: efectos de la variabilidad intraespecífica, del ambiente prevalente durante la cosecha y la interacción entre los dos componentes anteriores de la función fenotípica.
Conclusiones
• La mejor metodología para la evaluación de la viabilidad de los embriones, mediante la prueba de tetrazolio, fue la imbibición de la semilla, con el químico, en condiciones de oscuridad, por un lapso de 24 h, con cortes posteriores longitudinales ventrales o dorsales.
• A través de la evaluación de viabilidad con tetrazolio, se pudo detectar que en los dos taxa, objeto de la investigación, se presentaron semillas no viables, con valores de alrededor del 20% de las semillas, aparentemente normales.
• Las semillas de chirimoya y guanábana no exhiben latencia exógena, por testa impermeable; esto se comprobó por medio de la ganancia de peso obtenida al imbibir estas con agua, por espacio de 24 h.
• Estas poseen embriones poco desarrollados en tamaño, en el momento de la madurez de los frutos, y requieren de la posmaduración para germinar.
• La posmaduración de la semilla se logró con estratificación caliente húmeda, a 25 °C, durante 90 días, lo que condujo a germinación posterior de la semilla, al ser incubada para tal fin.
• En las dos especies también existe latencia fisiológica, la cual fue removida, en ambos taxa, a través de la imbibición de las semillas en AG3.
• La imbibición con 800 ppm de AG3, causó la mayor germinación, en ambas especies, al incubar las semillas, luego de la aplicación de la hormona.
• Se categorizó el bloqueo de germinación como “latencia morfofisiológica simple, no profunda”.
• La combinación del AG3 y la estratificación caliente húmeda incrementaron la germinación en chirimoya; en guanábana esto no fue evidente.
• Ya que las dos frutas estudiadas presentan semilla ortodoxa, se puede conservar por esta vía un duplicado de las colecciones de campo.
• Los datos obtenidos brindan una primera aproximación para procesos de monitoreo y germinación, lo cual permite la utilización del material conservado como semilla.
• También proporcionan soporte para la implementación de un modelo dinámico de conservación del germoplasma de chirimoya y guanábana, cuyos componentes son: la colección de campo, semilla de las colectas originales conservada a largo plazo y semilla de polinización abierta, colectada periódicamente en cada subpoblación de campo, para procesos de selección y clonación, con miras al uso del recurso genético de estas especies.
• Es conveniente estudiar el efecto de la variabilidad intraespecífica sobre la latencia, al igual que el del ambiente de producción de la simiente y la interacción genotipo por ambiente al respecto. Así se podrán ajustar protocolos de remoción de latencia y germinación de los dos taxa.
Literatura citada
Bansal, R.P., P.R.Bathi y D.N. Sen. 1980. Differential specificity in water imbibition of Indian arid zone seeds. Biol. Plant. 22, 327-331. [ Links ]
Baskin, C.C. y J.M. Baskin. 2001. Seeds. Ecology, biogeography, and evolution of dormancy and germination. Academic Press, San Diego, California. 666 p. [ Links ]
Baskin, C.C., S.E. Meyer y J.M. Baskin. 1995. Two types of morphophysiological dormancy in seeds of two genera (Osmorhiza and Eeythronium) with an arcto-tertiary distributium pattern. Amer. Bot. 82(3), 293-298. [ Links ]
Baskin, J.M. y C.C. Baskin. 1991. Non deep complex morphophysiological complex dormancy in seeds of Osmorhiza claytonii (Apiaceae). Amer. Bot. 78, 588-593. [ Links ]
Baskin, J.M. y C.C. Baskin. 2004. A classification system for seed dormancy. Seed Sci. Res. 14, 1-16. [ Links ]
Bewley, J.D. y M. Black. 1994. Seeds - Physiology of development and germination. Plenum Press, Nueva York. 445 p. [ Links ]
Castillo, P., R.B. Muno, M. Rubi y J.G. Cruz. 1997. Métodos de propagación del chirimoyo (Annona cherimola Mill.), en Catapec, Harinas, México. pp. 195-203. En: Memorias Congreso Internacional de Anonáceas. Universidad Autónoma de Chapingo, Chapingo. [ Links ]
Colauto, N.M., I. Massanori y C.S. Vieira. 2003. Superação da dormência em sementes de atemóia e fruta-do-conde. Revista Brasileira de Fruticultura 25(2), 305-308. [ Links ]
Cooper, H.D., C. Spillane y T. Hodgkin. 2001. Broadening the genetic base of crops: an overview. pp. 1-23. En: Cooper H.D. , C. Spillaney T. Hodgkin (eds.). Broadening the genetic base of crop production. IPGRI, FAO, CABI Publishing, Wallingford. [ Links ]
Da Silva E.A.A., D.L.B. De Melo, A.C. Davide, N. De Bode, G.B. Abreu, J.M.R. Faria y H.W.M. Hilhorst. 2007. Germination ecophysiology of Annona crassiflora seeds. Ann. Bot. 99, 823-830. [ Links ]
De Smett, S., P. Van Damme, X. Scheldeman y J. Romero. 1999. Seed structure and germination of cherimoya (Annona cherimola Mill.). Acta Hort. 497, 269-278. [ Links ]
Engelman, F. y J.M.M. Engels. 2002. Technologiess and strategies for ex situ conservation. pp. 89-104. En: Engels, J.M.M.; V. Ramanta, P. Brown y M.T. Jackson (eds.). Managing plant genetic diversity. CABI Publishing, Wallingford. [ Links ]
Espinal, S. 1977. Zonas de vida: formaciones vegetales del departamento de Antioquia. Universidad Nacional de Colombia, Medellín. [ Links ]
Esquinca, A.R.G., J.G.A. Moctezuma y G.M.P. Pérez. 1997. Duración de la latencia e importancia de la cubierta dura y la inmadurez anatómica, en la imbibición de la germinación de papausa blanca (Annona diversifolia Saff, Magnoliade, Annonaceae). Investigación, Ciencias y Artes en Chipias, México. pp. 37-44. [ Links ]
FAO. 1988. Traditional food plants- A resource book for promoting the exploitation and consumption of food plants in arid, semiarid and sub-humid lands of Eastern Africa. FAO Forestry Paper 4(1), 11-14. [ Links ]
Fenner, M. y K. Thompson. 2005. The ecology of seeds. Cambridge University Press, Cambridge. [ Links ]
Fernández, E. 2004. Estudios de viabilidad y latencia de semillas de guanábana (Annona muricata L.) y chirimoya (Annona cherimola M.). Trabajo de grado. Universidad Nacional de Colombia, Medellín. 35 p. [ Links ]
Ferreira, F.R. 2001. Conservação de germoplasma de espécies frutiferas no campo. pp. 38-40. En: III SIRGEALC Simposio de Recursos Genéticos para America Latina e o Caribe. IAPAR, Londrina. [ Links ]
Ferreira, F.R. y A.C. Pinto. 2005. Chapter: 8: Genetic Resources En: Williams, J.T., R.W. Smith, A. Hughes, N. Haq y C.R. Clements. (eds.). Annona species. International Centre for Underutilized Crops, University of Southhampton. 284 p. [ Links ]
Ferreira, G.Z., L.A. Fogaça y M.M. Malavasi. 1999. Germinación de semillas de Annona squamosa L., sometidas a diferentes tiempos y concentraciones de ácido giberélico. En: Memorias del II Congreso Internacional de Anonáceas. Universidad de Ciencias y Artes del Estado de Chiapas. Tuxtla Gutiérrez, Chiapas, México. pp. 79. [ Links ]
Ferreira, G., C.P. Silva, E. Cereda y J.F. Pedras. 1998. Efeito do ácido giberélico na germinação de sementes de fruta-do-conde. pp. 186-187. En: Anais Congreso Nacional de Botânica 49. Sociedade de Botânica do Brasil, Salvador. [ Links ]
Ferreira, G., P.R. Erig y E. Moro. 2002. Uso de ácido giberélico em sementes de fruta-do-conde (Annona squamosa L.) visando á produção de mudas em diferentes embalagens. Revista Brasileira de Fruticultura 24(1), 178-182. [ Links ]
Ferreira, G., E. Cereda, C.P. Silva, R.J.P. Cunha y A. Cataneo. 1997. Imbibition study of sugar apple (Annona squamosa L.) and atemoya (Annona squamosa L. X A. cherimola Mill) seeds. pp. 210-224. En: Memorias Primer Congreso Internacional de Anonáceas. Universidad Autónoma de Chapingo, Chapingo. [ Links ]
Finch-Savage, W.E. y G. Leubner-Metzger. 2006. Seed dormancy and the control of germination. New Phytologist 171, 501-523. [ Links ]
Foley, M.E. 2001. Seed dormancy: an update on terminology, physiological genetics, and quantitative trait loci regulating germinability. Weed Sci. 49, 305-317. [ Links ]
Franco, O., J. Jasso, E. García y C. Saucedo. 2001. Crecimiento y calidad de frutos de Annona muricata L., con diferentes niveles de polinización. Revista Fitotecnia Mexicana 24(2), 139-144. [ Links ]
George, A.P. y R.J. Niessen. 1987. Propagation of Annona species: a review. Scientia Hort. 33, 75-85. [ Links ]
Gepts, P. 2002. A comparison between crop domestication, classical plant breeding and genetic engineering. Crop Sci. 42, 1780-1790. [ Links ]
González, M., B. Baeza, J.L. Lao y J. Cuevas. 2006. Pollen load affects fruit size and shape in chirimoya. Scientia Hort. 110, 51-56. [ Links ]
Guirado, E., J.M. Hermoso, M.A. Pérez, J. García y J.M. Farré. 2001. Polinización del chirimoyo. Estación Experimental La Nacla. CSIC, Junta de Andalucia, Caja Rural de Granada. 52 p. [ Links ]
Hayat, M.A. 1963. Morphology of seed germination in Annona squamosa. Bot. Gazette 124(5), 360-362. [ Links ]
Hayat, M.A. y J.E. Canright. 1965. The developmental anatomy of the Annonaceae. I. Embryo and Early Seedling. Amer. Bot. 53(3), 228-237. [ Links ]
Hernández, L.V. 1993. La reproducción sexual y reproducción vegetativa de las annonaceas. Universidad Veracruzana, Xalapa. 35 p. [ Links ]
Hong, T.D., S. Linington y R.H. Ellis, 1996. Seed storage behaviour: a compendium. Handbooks for genebanks No. 4. International Plant Genetic Resources Institute, Roma. 62 p. [ Links ]
Ibar, L. 1979. Cultivo del aguacate, chirimoyo, mango y papaya. Aedos, Barcelona. [ Links ]
Infante, D. y P. Moreno-Casasola. 2005. Effect of in situ storage, light, and moisture on the germination of two wetland tropical tree. Aquatic Bot. 83, 206-218. [ Links ]
ISTA 1995. Conductivity test. pp. 22-34. En: Hampton, J.G. y D.M. Tekrony. (eds.). Handbook of vigour test methods. 3rd edition. International Seed Testing Association, Zürich, Switzerland. [ Links ]
Jurado, E. y J. Flores. 2005. Is seed dormancy under environmental control or bound to plant traits? Vegetation Sci. 16, 559-564. [ Links ]
Karlsson, L.M. y P. Milberg. 2007. A comparative study of germination ecology of four Papaver taxa. Ann. Bot. 99, 935-946. [ Links ]
Koornneef, M., L. Bentsink y H. Hilhorst. 2002. Seed dormancy and germination. Current Opinion. Plant Biol. 5, 33-36. [ Links ]
Ledo, A.S. y C.I.L. Cabanelas. 1997. Superação de dormência de sementes de graviola (Annona muricata L.). Revista Brasileira de Fruticultura 19(3), 397-400. [ Links ]
Lemos, E.E.P., R.L.R.R. Cavalcanti, A.A. Carrazoni y T.M. Lobo. 1987. Germinação de sementes de pinha submetidas a tratamentos para quebra de dormência. Anais Congreso Brasileiro de Fruticultura 2(9), 675-678. [ Links ]
Little, T.M. y F.J. Hills. 1976. Métodos estadísticos para la investigación en la agricultura. Editorial Trillas, México. 270 p. [ Links ]
Liu, Y., Y-P. Qui, L. Zhang y J. Chen. 2005. Dormancy breaking and storage behavior of Garcinia cowa Roxb. (Guttiferae) Seeds: Implications for ecological function and germplasm conservation. Integrative Plant Biol. 47(1), 37-49. [ Links ]
Lobo, M. 1992. Los recursos fitogenéticos: evolución, tipos y utilización. En: Memorias Curso Internacional sobre Recursos Fitogenéticos. Vol 1. 9 de noviembre- 4 de diciembre de 1992. Universidad Nacional de Colombia, Icetex, IBPGRI, OEA, Universidad del Valle, Palmira. [ Links ]
Mata, D.I. y P. Moreno-Casola. 2005. Effect of in situ storage, light and moisture on the germination of two wetland trees. Aquatic Bot. 83, 206-218. [ Links ]
Moreno, R., l. Luna y R. Gonzalez. 1999. Estudios sobre la germinación de Annona lutescens. En: Memorias del II Congreso Internacional de Anonáceas. Universidad de Ciencias y Artes del Estado de Chiapas. Tuxtla Gutiérrez, Chiapas, México. pp. 82. [ Links ]
Nakasone, H.Y. y R.E. Paull. 1998. Annonas. pp. 45-75. En: Nakasone, H.Y. y R.E. Paull (eds.). Tropical fruits. CAB International, Londres. [ Links ]
Nikolaeva, M.G. 1969. Physiology of deep dormancy in seeds. Izdatelsvo Nauka Lenningrad. National Science Foundation, Washington D.C. [ Links ]
Nikolaeva, M.G. 1977. Factors controlling the seed dormancy pattern in the physiology and biochemistry of seed dormancy and germination. Nort Holland, Amsterdam. pp. 51-74. [ Links ]
Padilla, I.M.G. y C.L. Encina. 2003. In vitro germination of chirimoya (Annona cherimola) seeds. Scientia Hort. 97, 219-227. [ Links ]
Pérez-García, F., M. Huertas, E.Mora, B. Peña, F. Varela y M.E. González. 2006. Hypericum perforatum L. seed germination: interpopulation variation and effect of light, temperatura, presowing treatments and seed dessication. Genet. Resources Crop Evolution 53, 1187-1198. [ Links ]
Pezzani, F. y C. Montaña. 2006. Inter- and intraspecific variation in the germination response to light quality and scarification in grasses in two-phase mosaics of the Chihuahuan desert. Ann. Bot. 97, 1063-1071. [ Links ]
Pinto, A.C. 1975. Influencia do hormonio sobre o poder germinativo de sementes de graviola (Annona muricata L.) pp. 1-18. En: Anais do III Congreso Brasileiro de Fruticultura. Sociedade Brasileira de Fruticultura, Rio de Janeiro. [ Links ]
Pinto, A.C. 1976. Influência do hormônio sobre o poder germinativo de sementes de graviola. pp. 415-420. En: Anais Congreso Brasileiro de Fruticultura, Rio de Janeiro. [ Links ]
Pinto, A.C. 2005a. Chapter 3: Origin and distribution. pp. 17-20. En: Williams, J.T., R.W. Smith, A. Hughes, N. Haq, C.R. Clements. (eds.). Annona species. International Centre for Underutilized Crops, University of Southampton. [ Links ]
Pinto, A.C. 2005b. Chapter 10. Agronomy. pp. 70-123. En: Williams, J.T., R.W. Smith, A. Hughes, N. Haq y C.R. Clements. (eds.). Annona species. International Centre for Underutilized Crops, University of Southampton, Southampton. [ Links ]
Pinto, A.C., S.R.M. Andrade. 2005. Chapter 9. Genetic improvement. pp. 53-69. En: Williams, J.T., R.W. Smith, A. Hughes, N. Haq y C.R. Clements (eds.). Annona Species. International Centre for Underutilised Crops. University of Southampton, Southampton. [ Links ]
Pinto, A.C. y E.M. Silva, 1994. Graviola para exportação. Aspectos técnicos da produção. FRUPEX. Minagricultura do Abastecimento e da Reforma Agrária. Sec. De Desenvolvimento Rural SDR, Prog. de Apoio a Prod. e Export. de Frutas, Hortaliças, Flores e Plantas Ornamentais. 49 p. [ Links ]
Popenoe, W. 1939. Importantes frutas tropicais. União Panamericana. Departamento de Cooperação Agrícola. Washington D.C. 29 p. [ Links ]
Poulsen, G., C. Holten y R. Von Bohmer, 2006. Identification and revival of low viability seed simples. Genet Resources Crop Evolution 53, 675-678. [ Links ]
Rao, N.K., J. Janson, M.E. Duloo, K. Ghosh, D. Nowell y M. Larinde. 2006. Manual of seed handling in genebanks. Handbook for genebanks 8, 163 p. [ Links ]
Rosell, P., V. Galán y M. Herrero, 2006. Pollen germination as affected by pollen age in cherimoya. Scientia Hort. 109, 97-100. [ Links ]
Scheldeman, X. 2002. Distribution and potential of cherimoya (Annona cherimola Mill) and highland papayas (Vasconcellea spp.) in Ecuador. Ph.D. thesis Universiteit Gent, Bélgica. 176 p. [ Links ]
Snyder, R.E. 2006. Multiple risk reduction mechanisms: can dormancy substitute for dispersal? Ecology Letters 9, 1106-1114. [ Links ]
Tao, K.L. 2001. Complementary conservation strategy for plant genetic resources. Chapter 5. pp. 46-53. En: Saad, M.S. y V.R. Rao. (eds.). Establishment and management of field genebanks. A training manual. IPGRI, APO. Roma. [ Links ]
Thompson, K. 2000. The functional ecology of soil seed banks. pp. 215-235. En: Fenner, M. (ed.). Seeds: the ecology of regeneration in plant communities. CAB International, Wallingford. [ Links ]
Tweddle, J.C., J.B. Dickie, C.C. Baskin y J.M. Baskin. 2003. Ecological aspects of seed dissication sensitivity. Ecol. 91, 294-304. [ Links ]
Vilar, I., R.A. De Andrade y A. Baldo. 2005. Influência da temperatura na germinação de sementes de Annona montana. Revista Brasileira de Fruticultura 27(2), 344-345. [ Links ]














