Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Agronomía Colombiana
Print version ISSN 0120-9965
Agron. colomb. vol.26 no.1 Bogotá Jan./June 2008
Alejandra Hilarión1, Angie Niño1, Fernando Cantor2, Daniel Rodríguez2 y José Ricardo Cure2
1 Biólogas, Facultad de Ciencias, Universidad Militar Nueva Granada, Bogotá. alekus47@gmail.com; alejandra_2601@hotmail.com
2 Docentes, Programa de Biología Aplicada, Facultad de Ciencias, Universidad Militar Nueva Granada, Bogotá.ecologia@umng.edu.co
Fecha de recepción: febrero 15 de 2008. Aceptado para publicación: abril 9 de 2008
RESUMEN
Phytoseiulus persimilis ha sido utilizado en programas de manejo integrado de plagas como alternativa al uso de acaricidas para el manejo de Tetranychus urticae. Los daños ocasionados por generan un costo de manejo cercano a los 4.500 dólares por hectárea, esta cifra corresponde aproximadamente al 30% del costo de los plaguicidas (Ceniflores, 2008). La implementación de esta estrategia de manejo debe considerar criterios de liberación basados en los niveles de población de T. urticae del cultivo, estimados a partir de una metodología de muestreo apropiada. En el presente trabajo, se propuso una metodología para estimar el nivel de infestación de T. urticae, para conocer la cantidad de P. persimilis a liberar en el cultivo de rosa y se evaluó la efectividad del control ejercido por P. persimilis. En el área experimental se tomaron 81 cuadros, en cada uno de ellos se muestrearon al azar tres plantas de rosa y se contó el número de individuos en tres hojas de cada tercio de la planta. Así mismo, se determinó el número óptimo de muestras para un muestreo bietápico. Se tuvo en cuenta la respuesta funcional como criterio de liberación de P. persimilis. La población de T. urticae estimada después de la liberación se dividió entre la población previa a la liberación para obtener un índice de control, el cual se comparó entre las estrategias de manejo. Con el control biológico se obtuvo una mayor reducción de la población de la plaga y una menor fluctuación de esta a través del tiempo.
Palabras clave: ácaros, control biológico, muestreo.
ABSTRACT
Phytoseiulus persimilis has been used in IPM programs as alternative to the use of acaricides in order to control the phytophagous mite Tetranychus urticae. The damages caused by T. urticae generate the cost of management about 4,500 dollars per hectare, which corresponds approximately to 30% of pesticide cost (Ceniflores, 2008). The implementation of this management strategy must consider the release criteria based upon the population levels of T. urticae in the crop estimated by means of appropriate sampling methods. In this research, a methodology for estimating the population density of T. urticae is proposed, in order to assess the quantity of P. persimilis to be released in the rose crop, and the effectiveness of control exerted by P. persimilis was evaluated. In the experimental area, 81 squares were taken, at each of them three rose plants were randomly selected and the number of individuals were counted were counted taken three leaves on the stratum on the plant. The optimum number of sampling units for a bietapic sampling was assessed. The functional response was assumed as a criterion to set the release of P. persimilis. The population density of T. urticae after each release was divided by the population prior to the release, in order to obtain an index control, which was compared between the management strategies. By means of the biological control a greater reduction in the population density and its lesser variation in time were obtained.
Key words: mites, biological control, sampling.
Introducción
Colombia es el segundo país exportador de flores de corte a nivel mundial (Flórez et al., 2000). Hoy, uno de los requisitos de exportación es la disminución del uso de productos químicos en busca de un desarrollo ambientalmente amigable y de bajo costo tanto para el hombre como para el medio ambiente (Gómez et al., 2004).
Entre las principales plagas que atacan los cultivos de rosas están los ácaros del género Tetranychus. Estos causan pérdida de calidad, disminución en el crecimiento de las plantas y reducción en la producción de botones (Acosta et al., 2001). Aunque se desconoce el porcentaje de pérdidas de flores a causa de T. urticae, el costo de acaricidas para el control es cercano al 30% del costo de plaguicidas (F. Acosta, comunicación personal, 14 de diciembre de 2007). Por lo general, el control de dicha plaga se ha realizado mediante el uso de plaguicidas. Sin embargo, se han desarrollado diferentes estrategias de control que permiten mantener infestaciones por Tetranychus sp. a niveles tales que no representen pérdidas económicas ni problemas ecológicos, como es el caso del control biológico (Mendoza et al., 2001).
Uno de los controladores más efectivos de T. urticae es el ácaro depredador P. persimilis, el cual presenta una alta capacidad de búsqueda y voracidad (Acosta, 2000), un ciclo de desarrollo menor que el de su presa y, junto con la proporción de sexos (4 hembras/1 macho), el desarrollo de las poblaciones es más rápido (Barreto, 2004).
Para la implementación de P. persimilis en un programa MIP, que permita reducir la aplicación de acaricidas, es necesario realizar ensayos previos para determinar la distribución de T. urticae dentro del área de muestreo y posteriormente, tomar decisiones de manejo. Además es necesario tener en cuenta que P. persimilis, después de varias semanas de liberación, puede llegar a establecerse dentro del cultivo (Casey et al., 2007).
En función de conocer la densidad de T. urticae y la metodología de liberación de P. persimilis, el presente trabajo tuvo como objetivos determinar algunos criterios para la liberación de P. persimilis como controlador biológico de T. urticae en cultivo de rosa, variedad Versilia bajo invernadero, mediante el establecimiento de una metodología de muestreo directo.
Este muestreo permitirá estimar la población de T. urticae susceptible de ser consumida y, a partir de esa información, aplicar el concepto de respuesta funcional de P. persimilis como criterio de liberación. Así mismo, evaluar la efectividad de esta metodología mediante la comparación con la eficacia del control convencional utilizado en los cultivos de rosa e identificar el tipo de sustrato que facilita la dispersión de P. persimilis en campo y aumentar la sobrevivencia en el empaque de transporte del ácaro depredador al lugar de liberación en el cultivo y, por último, cuantificar el costo de liberaciones de P. persimilis como un sistema alternativo al convencional para el manejo de poblaciones de T. urticae en rosa.
Materiales y métodos
Área de estudio
El trabajo se realizó en un cultivo comercial de rosa, bajo condiciones de invernadero, ubicado en el municipio de Tenjo (Cundinamarca), durante los meses de marzo a diciembre de 2006. Se seleccionaron plantas de rosa de variedad Versilia de aproximadamente 2,5 años, sembradas en 162 camas de 32 m de longitud y 0,80 m de ancho, localizadas en 32 naves de 476 m2 cada una en un invernadero de 15.232 m2, cuyas temperaturas alcanzaron los 4 ºC y 30 ºC. Las plantas sembradas en cada cama están dispuestas en dobles surcos, con una distancia de 15 cm entre ellos y de 15 cm entre plantas. El cultivo presenta una producción continua y un sistema de formación de plantas tipo agobio. El control químico consistió en aplicar esporádicamente Diafentiurion, con una concentración de 1,5 g·L-1, el cual fue aplicado cuatro veces durante el ensayo, y Bifenazate, con una concentración de 0,25 g·L-1, el cual fue aplicado una vez a lo largo del ensayo.
Determinación de la distribución espacial de T. urticae en cultivo comercial de rosa
Cada cama de 32 m de longitud se dividió en ocho cuadros, los cuales se tomaron como unidad de evaluación. Cada cuadro estaba conformado por un total de 54 plantas y en cada muestreo se evaluó un promedio de 81 cuadros, cada uno de los cuales se escogió al azar de cada tercera cama del invernadero, con el fin de que no se presentara interferencia entre los tratamientos: control biológico y control químico. En cada cuadro se contaba el número de individuos de todos los estados de desarrollo de T. urticae presentes en tres hojas de cada tercio de la planta. Para determinar la distribución espacial del ácaro fitófago se calculó la relación varianza-media (ID), a partir de la cual se puede establecer si la distribución es agregada (S2/x > 1), uniforme (S2/x < 1) o al azar (S2/x = 1) (Pedigo y Buntin, 1994). Este ensayo se realizó durante los meses de marzo y abril de 2006, tiempo durante el que se realizaron cinco repeticiones del muestreo.
Determinación de la distribución espacial de T. urticae en plantas y hojas de rosa
De cada cuadro se tomaron tres plantas al azar y cada planta se dividió en tres tercios: el primer tercio conformado por el agobio; el segundo, del agobio al punto de corte y el tercero, del punto de corte al botón floral. Se muestrearon tres hojas de cada tercio para determinar la distribución de los individuos en la planta y el porcentaje de estos en cada tercio.
Para establecer la distribución de la plaga en las hojas, se tuvo en cuenta la cantidad de individuos presentes en cada foliolo, se hicieron cinco muestreos durante el periodo de evaluación. En cada muestra se contó el total de huevos y de individuos móviles. A través del software estadístico R se realizó un análisis de varianza, en el que se tomaron como factores los tercios, con el fin de determinar si existían o no diferencias en el número de individuos y la proporción de estos en cada tercio. La diferencia en el número de individuos se determinó comparando el número de estos, ya que el promedio de individuos por hoja varía, al igual que el promedio de estos por tercio.
Además, se realizó otro análisis de varianza y una prueba de Tukey con foliolos como tratamiento para establecer la distribución de los individuos en la hoja. El Anova se realizó con el número de individuos y, al encontrar diferencias, se sacaron las proporciones. Los datos fueron transformados por medio Box Cox (Gómez, 1999), para mejorar la aproximación de los conteos a una distribución normal. Para cada proporción se calculó un intervalo de confianza, con el propósito de comparar las proporciones de los individuos en los tres tercios de la planta.
Determinación del tamaño de muestra para las diferentes unidades de muestreo
Se propone utilizar la distribución binomial negativa, que se usa para estimar el tamaño de muestra cuando la población presenta una distribución agregada. En este modelo se incluye el parámetro k (factor de agregación). Sin embargo, el valor de k generalmente varía con la densidad media, de forma que el tamaño de la unidad de muestra estimado cambiaría a través del tiempo conforme a la densidad de la población (Pedigo y Buntin, 1994).
Como consecuencia se han utilizado índices para desarrollar planes secuenciales de clasificación o estimación basados en la relación entre la varianza y la media, como es el caso de la Ley de Poder de Taylor (LPT) (ecuaciones 34 y 35 que se encuentran en Pedigo y Buntin, 1994). Las fórmulas para adaptar o aplicar el muestreo trietápico para la Ley de Taylor sugiere que el intercepto (a) no tiene una significancia biológica y varía con la técnica de muestreo empleada; mientras que la pendiente (b) es una constante que depende del comportamiento de la especie o el ambiente. Este parámetro puede ser utilizado para determinar el patrón de distribución (Shelton y Trumble, 1986; Pedigo y Buntin, 1994). La metodología para el muestreo en etapas se basó en lo propuesto por Gómez (1999) (tabla 1) y la estimación de tamaños de muestra se realizó mediante la aplicación de la Ley de Poder de Taylor al muestreo en etapas como lo plantean Shelton y Trumble (1986).
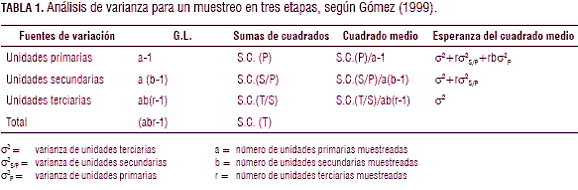
Con el fin de establecer las unidades de muestreo que se deben seleccionar, se tomaron como unidades primarias los cuadros (a), como unidades secundarias las plantas dentro del cuadro (b) y como unidades terciarias las hojas dentro de la planta (r). A dichas muestras se les realizó un análisis de varianza para un muestreo en etapas. Una vez se obtuvieron los componentes de varianza para cada etapa, se estimó la proporción de cada varianza sobre el total, para determinar si era necesario considerar las tres unidades de muestreo (hojas, plantas y cuadros). Posteriormente, se estimaron los parámetros de pendiente e intercepto necesarios para aplicar la Ley de Poder de Taylor (LPT) mediante una regresión lineal. A través de la LPT se estimó el tamaño de muestra para aquellas unidades donde la varianza cambia en función de la densidad. Mientras que, para las unidades donde no hay una relación entre la varianza y la media el tamaño de muestra se estimó mediante el muestreo por etapas propuesto por Gómez (1999).
Comparación de la efectividad de P. persimilis para el control de poblaciones de T. urticae, en función de la respuesta funcional como criterio de liberación, y del control convencional
Para comparar la efectividad de dos métodos de control para el manejo de T. urticae en rosa, se definieron dos tratamientos: (1) liberación semanal de P. persimilis en relación a la respuesta funcional y (2) aplicaciones semanales por aspersión de acaricidas.
Para esta evaluación se seleccionaron dos naves del invernadero, cada una con un tamaño de 476 m2 y en las que se tomaron cuatro camas a las cuales se les aplicó un determinado tratamiento. Los tratamientos se implementaron en campo, bajo un diseño completamente al azar con cuatro repeticiones. Para el caso del control biológico la densidad a liberar variaba semanalmente, pero se mantenía constante la proporción predador-presa, la cual dependía del número de individuos-plaga presentes para cada muestreo. En el caso del control químico se tuvo en cuenta el plan de aplicaciones que llevaba la finca durante el tiempo del ensayo, el cual consistió en aplicar los productos Diafentiurion y Bifenazate. El primero se aplicó cuatro veces y el segundo una vez, durante la evaluación de los diferentes tratamientos de control.
Se realizaron liberaciones P. persimilis de acuerdo con la densidad de la población de T. urticae y a la respuesta funcional de P. persimilis (Fernando y Hassell, 1980). La densidad del depredador se ajustó multiplicando la densidad a liberar, la cual es la relación predador-presa determinada mediante la tasa máxima de consumo de la respuesta funcional, por el porcentaje de mortalidad (7%), de forma que se compensó la cantidad de depredadores que posiblemente murieran por causa del sustrato y el transporte.
Los ácaros eran adultos con una edad promedio de siete días, se liberaron en el primer tercio de las camas a las 3:00 p.m., luego de la cosecha. Después de 24 h de la liberación se realizaba un muestreo en los mismos cuadros que fueron evaluados previamente a la liberación. Este muestreo consistió en tomar dos cuadros por cama, de cada cuadro se muestreaban dos hojas del tercio inferior y se contaban los cuatro primeros foliolos de la misma que van desde el foliolo apical hacia abajo y se contaban tanto huevos como estados móviles de T. urticae de P. persimilis, para evaluar la presencia de P. persimilis y el nivel de control obtenido. El análisis de datos contempló únicamente los estados de huevo y larva de T. urticae, considerados como los estados preferidos por P. persimilis (Fernando y Hassell, 1980). A pesar de que solo se tienen en cuenta estos estados para la liberación de P. persimilis y los adultos son los que causan el principal daño en la planta, lo que se busca es causar un rompimiento en la dinámica poblacional.
El control químico o convencional se realizó mediante la aplicación de los productos Diafentiurion con una concentración de 1,5 g·L-1, el cual fue aplicado cuatro veces durante el ensayo, y Bifenazate con una concentración de 0,25 g·L-1 aplicado una vez a lo largo del ensayo.
Registro de variables en campo y análisis
Se registraron cambios en el número de huevos e individuos móviles durante el muestreo previo y posterior a la liberación o aplicación del control convencional y con estos datos se evaluó el nivel de control. Se realizó un análisis de varianza a los índices de efectividad, para establecer si, en ese sentido, había diferencias entre los tratamientos de control. Adicionalmente, se determinó el efecto de ambos tratamientos sobre la proporción de individuos de cada estado.
Cuantificación del costo de liberaciones de P. persimilis como un sistema alternativo al convencional para el manejo de poblaciones de T. urticae en cultivo comercial de rosa
Se realizó una comparación del costo (en pesos por área de evaluación (4 camas)) de muestreo y liberación de individuos del ácaro depredador para el control biológico con el costo de la implementación del control convencional. Por lo anterior, fue necesario registrar el número de ácaros depredadores liberados, así como la frecuencia de aplicación de ambos métodos de control. Para estos dos tratamientos se realizó el mismo tipo de muestreo y, al final, una comparación de costos entre ambos.
Resultados y discusión
Distribución espacial de T. urticae en cultivo comercial de rosa
El índice de relación varianza-media (ID) para la población de T. urticae presenta valores mayores a uno. Por lo anterior se puede afirmar que la población de T. urticae presenta una distribución de tipo agregado. Esta clase de distribución caracteriza las poblaciones de T. urticae, las cuales tienden a alcanzar altas densidades poblacionales al formar focos. Este resultado concuerda con trabajos realizados por Nachman (1981), Zhang y Sanderson (1995), entre otros.
Distribución de T. urticae en plantas de rosa variedad Versilia
Se puede establecer que la mayor población se encuentra en la hoja del tercio inferior (alrededor del 72%), mientras que en las hojas del tercio medio y superior se encuentra alrededor del 22% y 6% de la población, respectivamente (figura 1).
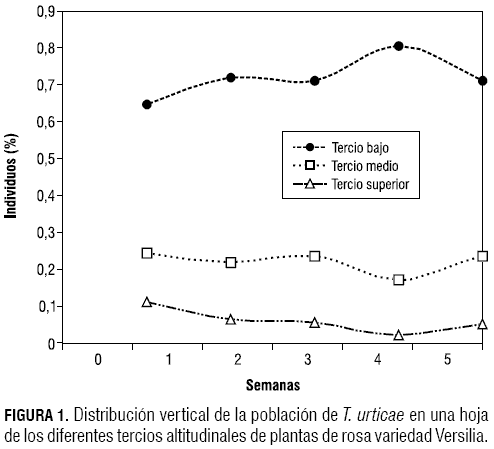
La preferencia de los ácaros por el tercio inferior en rosa puede estar atribuido a que en esta zona se atenúan los cambios de temperatura fuertes (Salas, 2001; Cifuentes y Vanegas, 1987). Adicional a esto, la plaga puede encontrar hojas frescas de rosa debido al sistema de formación tipo agobio, el cual permite un aumento en el número de hojas, de manera que obtiene los recursos preferidos para la oviposición (Santamaría et al., 2002).
Distribución de T. urticae en hojas de rosa variedad Versilia
Se presentaba una distribución heterogénea de T. urticae en los diferentes foliolos de la hoja (P = 2,2e-16) (figura 2). Se encuentra la mayor proporción de ácaros en el foliolo apical y la densidad disminuye a medida que los foliolos se alejan del mismo. Sin embargo, no se presentaron diferencias significativas entre los foliolos opuestos (2-3, 4-5 y 6-7) (P = 0,629). Esta tendencia también fue registrada por Cifuentes y Vanegas (1987) y Acosta (2003) en cultivo de rosa con T. urticae.
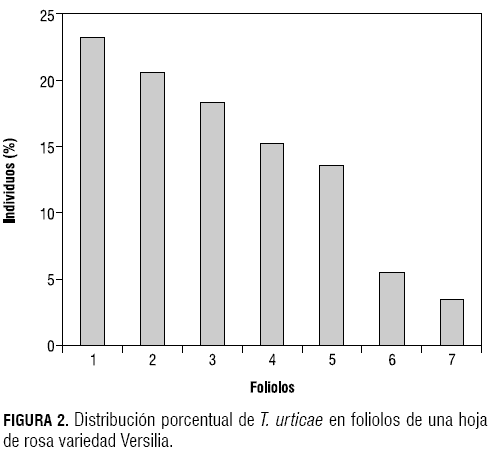
La preferencia por dicho foliolo se puede atribuir a que este presenta una mayor área, tiene mejores condiciones de iluminación por estar más alejado del tallo y además tiene un mayor contacto con las corrientes de aire (Cifuentes y Vanegas, 1987).
Al determinar la distribución de los individuos en la hoja se puede reducir el tiempo de evaluación de la unidad, de manera que no se evalúe toda la hoja, sino una parte de la misma. Se recomienda contar el total de individuos presentes en los primeros cuatro foliolos de la hoja, ya que en estos se ve representado aproximadamente el 75% del total de individuos de la hoja, por lo cual se requiere estimar solo el 25% de la población de la misma, en cambio, si se cuentan dos o tres foliolos, el error estándar es aproximadamente el 13% mayor que si se cuentan los cuatro sugeridos y, en el caso de contar cinco o seis foliolos, el error estándar es menor, pero no existiría un ahorro en el tiempo que es lo que se busca con este muestreo.
Tamaño de muestra para las diferentes unidades de muestreo
Los porcentajes fluctuaban debido a que los porcentajes de varianza para cada una de las etapas fueron altos, lo que indica que no se puede omitir ninguna de las etapas, ya que cada una tiene un efecto importante sobre la varianza total (tabla 3).
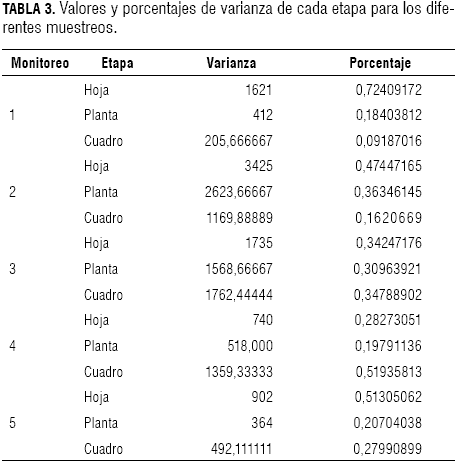
Se encontró que la distribución espacial en las hojas no cambia en función de la densidad de individuos, por lo que no es necesario emplear la LPT para estimar el tamaño de muestra para dicha etapa (tabla 2). El tamaño de muestra para hojas se estimó mediante el muestreo en etapas propuesto por Gómez (1999) y se obtuvo que la unidad mínima de muestreo es una hoja/planta.

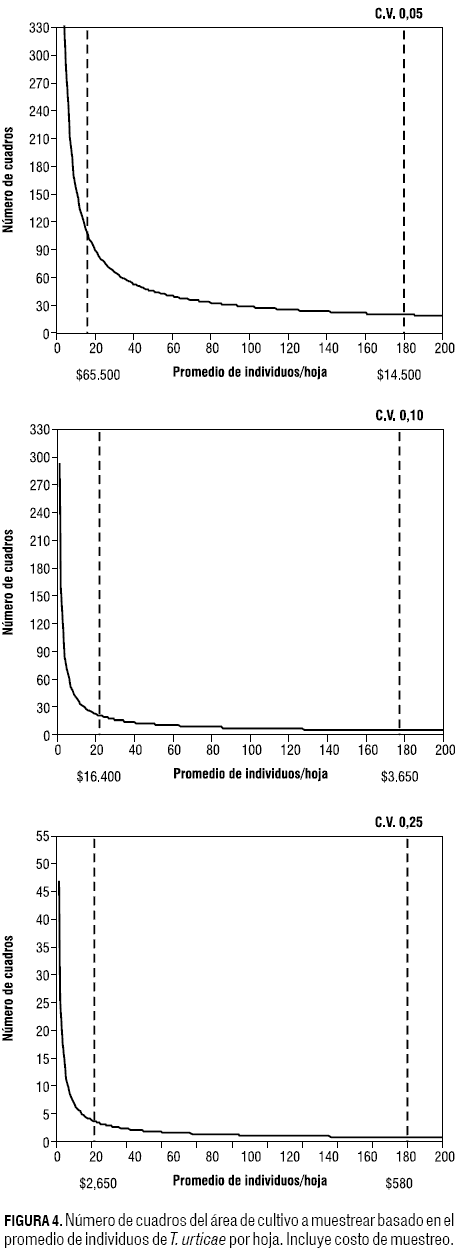
Por otro lado, se observó una relación entre la varianza y la media para las unidades de cuadros y plantas, de forma que la cantidad de unidades a muestrear dependerá del promedio de individuos encontrados en una hoja (figuras 3 y 4), como lo establece la LPT.
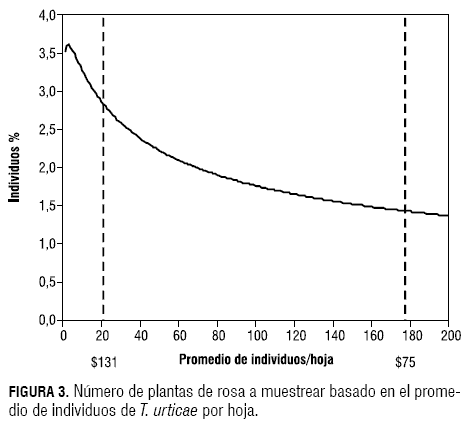
El tamaño de muestras para plantas estará comprendido entre una y cuatro plantas por cuadro, mientras que para cuadros no solo variará de acuerdo al promedio de individuos por hoja, sino que además dependerá del coeficiente de variación que se desee manejar (figura 4).
Para estimar la densidad de huevos y larvas de T. urticae con el fin de utilizar dicha información junto con la respuesta funcional como criterio de liberación de P. persimilis, se propone el siguiente protocolo:
1.Realizar un muestreo piloto, en el cual se escogen cinco plantas al azar, tomar una hoja por planta y contar el total de individuos en la hoja.
2. Estimar el promedio de individuos por hoja. Sumar el total de individuos de todas las hojas y dividirlo en el número de hojas muestreadas (5).
3. A partir del promedio de individuos obtenido, determinar el tamaño de muestra para cuadros por área de muestreo (figura 4). El total de cuadros por área varía según el coeficiente de variación (CV) con el que se desee trabajar (5%, 10%, 25%): entre más alto sea el porcentaje de variación que se tome, disminuye el costo, ya que para un CV del 25% se va a muestrear un menor número de cuadros en comparación si se toma un CV del 5%.
Los cuadros a muestrear se escogen de forma aleatoria en toda el área de muestreo.
4. El número de plantas por cuadro a muestrear también se determinará según el promedio de individuos por hoja (figura 3). Las plantas se escogen al azar dentro de los cuadros.
5. El tamaño de muestra para hojas es constante (una hoja por planta). Escoger al azar una hoja del tercio inferior.
6. Contar el total de individuos en estado de huevo y larva presentes en los primeros cuatro foliolos de la hoja.
7. Contar el total de hojas por tercio de las plantas que se muestrearán por cuadro, según el promedio de individuos por hoja A partir de esta información, sacar el promedio del número de hojas presentes por cada tercio.
8. Sumar para cada hoja el total de huevos y larvas presentes en los cuatro foliolos muestreados. Calcular el promedio de individuos para las diferentes hojas muestreadas en el cuadro (el número de hojas por cuadro dependerá del tamaño de muestra para plantas).
9. El valor promedio obtenido anteriormente se debe multiplicar por 1,35 para estimar el número de huevos o larvas presentes en una hoja del primer tercio.
10. El número de huevos o larvas presentes en una hoja del tercio inferior es multiplicado por 0,4 para estimar el total de individuos que se encuentran en una hoja, tanto del tercio medio como del superior.
11. Multiplicar el promedio de hojas del tercio inferior calculado en el numeral cinco, por el número de huevos o larvas presentes en una hoja del tercio inferior, estimado en el numeral nueve. Esto permitirá calcular el número de individuos que se encuentran en el tercio inferior.
12. Para estimar el número de individuos presentes en el tercio medio y superior, multiplicar el promedio de hojas del tercio medio y superior calculado en el punto siete por el número de huevos o larvas presentes en una hoja del tercio medio y superior estimado en el punto diez.
13. Al sumar los valores obtenidos para cada tercio de la planta (puntos 11 y 12) se obtendrá el número total de individuos de la plaga por planta.
14. Este resultado se debe multiplicar por el total de plantas presentes en el área de muestreo.
15. Finalmente, a partir del resultado obtenido en el punto 14 y al tener en cuenta la respuesta funcional de P. persimilis, se podrá determinar el número de ácaros depredadores a liberar.
Comparación de la efectividad de los diferentes métodos de control con base en el índice de efectividad
En la figura 5 se puede observar la comparación de los índices de efectividad que se alcanzaron con los métodos de control utilizados para el manejo de las poblaciones de T. urticae. Las liberaciones se realizaron teniendo en cuenta la relación predador-presa, las cuales variaban en cada uno de los muestreos.
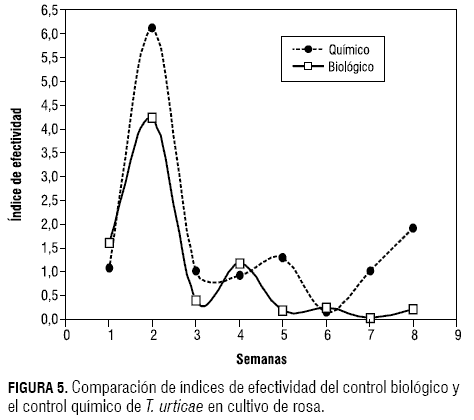
Aunque no se presentaron diferencias significativas entre los tratamientos para huevos (P = 0,07), para larvas (P = 0,38) y para ninfas (P = 0,09), se observa que en el tratamiento con control biológico no se logró un control efectivo al iniciar las liberaciones, pero en los monitoreos posteriores la tendencia general del índice es a disminuir, ya que, a medida que se acerca a cero, se está indicando que el control se hace más efectivo en el caso del control biológico. Es decir que el control biológico al principio resulta poco efectivo, pero a medida que el tiempo transcurre, la efectividad se incrementa, posiblemente como resultado del establecimiento de los ácaros depredadores. Según Andrews et al. (1989) y Barreto (2004), el control biológico puede ser mejor que el químico pero la diferencia solo es evidente en un plazo prolongado.
Por otro lado, con el control químico se obtuvieron valores superiores o iguales a uno, lo que indicaría que en la mayoría de casos no hubo efecto sobre la densidad de población o, por el contrario, la población aumentó después de la aplicación. Este comportamiento frente al control químico puede ser atribuido a la resistencia previa que presentaban los T. urticae, ya que esta se puede presentar en algunas especies debido a la selección de poblaciones genéticamente resistentes (Malais y Ravensber, 1991); resistencia que, en muchos casos, es favorecida por uso de acaricidas con composición química similar y la alta frecuencia de aplicación (Criollo y Duarte, 2004; Marín, 2002). Esta última aumenta debido a que no todas las fases del ciclo requieren del mismo tipo de acaricida, lo que favorece el desarrollo de numerosas y superpuestas poblaciones en corto tiempo (Marín, 2002), de forma que productos que antes eran efectivos para controlar ciertas plagas pierden efectividad (Andrews et al., 1989).
Efecto de los métodos de control sobre la proporción de individuos de cada estado
Para el control biológico, como se observa en la figura 6, se obtuvo una disminución en la densidad de huevos y larvas después de la liberación. La depredación sobre los estados más jóvenes de la plaga puede ser atribuida a la preferencia de P. persimilis sobre huevos y larvas (Fernando y Hassell, 1980). Sin embargo, se esperaba un control total de dichos estados porque la densidad de depredadores liberados se estimó a partir de la respuesta funcional, de forma que la cantidad liberada sería suficiente para consumir el total de individuos de T. urticae pertenecientes a los estados susceptibles a la depredación.
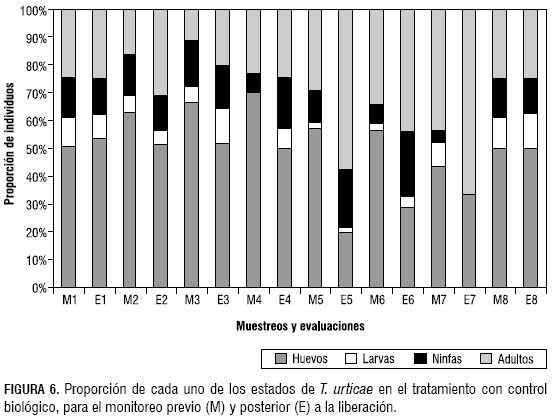
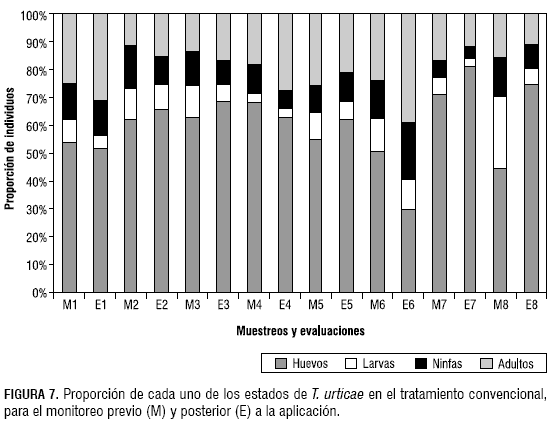
Para el caso del control convencional, en la mayoría de los casos no se ve un efecto en la proporción de los diferentes estados (figura 7). Esto puede explicarse mediante las características de los productos aplicados, los cuales afectan todos los estados de la plaga (Diccionario HC Agropecuario, 2005).
Costo de liberación de P. persimilis como sistema alternativo al convencional para el manejo de poblaciones de T. urticae en un cultivo comercial de rosa
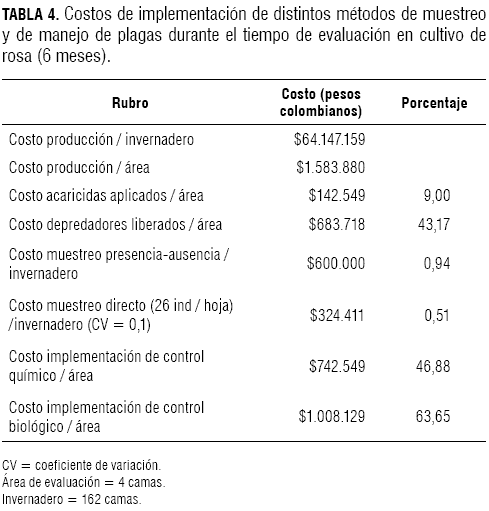
Al comparar los dos métodos de monitoreo, se observa que el directo propuesto, aunque no permite una reducción de los costos, aporta una información más precisa sobre la población de la plaga comparado con el monitoreo presenciaausencia (tabla 4). La información sobre variabilidad y costo de la técnica es esencial para seleccionar la mejor técnica, ya que una técnica de muestreo aceptable debe maximizar la precisión mientras minimiza costos (Pedigo y Buntin, 1994).
Por otro lado, aunque el control biológico involucra un mayor costo de implementación, provee otros beneficios comparados con el control químico. Este método de control tiene un carácter duradero, porque permite una estabilidad entre el enemigo natural y la plaga, no tiene efectos colaterales sobre el ambiente, puesto que no causa daños al medio por su selectividad y seguridad y aumenta la complejidad faunística del ecosistema (Andrews et al., 1989; Barreto, 2004).
Conclusiones
• Para el manejo de cualquier plaga agrícola con liberaciones de enemigos naturales es necesario establecer los criterios de liberación, con el fin de generar las condiciones más favorables que permitan obtener máximos índices de control.
• Para el caso del control biológico de T. urticae con liberaciones de P. persimilis en cultivo de rosa variedad Versilia, estos criterios fueron definidos así:
(1) Realización de un muestreo de área vegetal afectada por T. urticae, teniendo en cuenta un muestreo por etapas en hojas por plantas, plantas por cuadros y cuadros por área de muestreo. El número de muestras a tomar dependerá del promedio de individuos encontrados por hoja, que se encuentren en la edad susceptible de ser consumidos por P. persimilis. Con el fin de reducir tiempo en el muestreo y obtener una estimación más precisa de la población de la plaga, el muestreo de hojas debe estar dirigido hacia el tercio inferior de la planta y se debe contar el total de individuos de cada estadio presentes en los primeros cuatro foliolos de la hoja.
(2) Aplicación de la relación predador-presa, que es el máximo número de individuos que puede consumir un individuo de P. persimilis por unidad de tiempo determinada en 24 h para estimar el número de depredadores que se debe liberar según la población de T. urticae susceptible de ser consumida que se estimó en el muestro anterior.
Agradecimientos
A la Universidad Militar Nueva Granada por el apoyo financiero del proyecto identificado con el código CIAS- 2003-007, y a la empresa Flores de Tenjo por el apoyo logístico para el mismo.
Literatura citada
Acosta, A. 2000. Escrito sobre lo que seguramente usted ya ha oído de los famosos ácaros Tetranychus spp. Conocimientos generales y manejo integrado de Tetranychus spp. (Acariformes: Tetranychidae) en cultivos de flores. Facultad de Agronomía, Universidad Nacional de Colombia, Novartis. 47 p. [ Links ]
Acosta, A. 2003. Bases útiles para el manejo integrado de ácaros Tetranychidae en cultivos de flores (MIP de Tetranychidae). Facultad de Agronomía, Universidad Nacional de Colombia. 109 p. [ Links ]
Acosta, O., M. Yépez, A. Acosta, y L. Díaz. 2001. Ciclo biológico de Tetranychus cinnabarinus Boisduval y Tetranychus urticae Koch en rosa, clavel y alstroemeria bajo siete ambientes. Asocolflores 60, 25-39. [ Links ]
Andrews, K., M. Barnes y H. Hoffman. 1989. Utilización del control químico. En: Andrews, K. (ed.). 1989. Manejo integrado de plagas insectiles en la agricultura. Estado actual y futuro. Departamento de Protección Vegetal, Escuela Agrícola Panamericana, Honduras. 623 p. [ Links ]
Barreto, C. 2004. Introducción del depredador Phytoseiulus persimilis Athias Henriot dentro de un programa de manejo integrado de plagas para el control del ácaro Tetranychus urticae Koch en un cultivo comercial de rosa en la Sabana de Bogotá. Trabajo de grado. Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. 167 p. [ Links ]
Casey, C., J. Newman, K. Robb, S. Tjosvold, J. MacDonald y P. Parrella. 2007. IPM program successful in California greenhouse cut roses. California Agr. 61(2), 71-78. [ Links ]
Ceniflores. 2008. Manejo integrado de los ácaros de ornamentales. Litocamargo Ltda., Bogotá. 83 p. [ Links ]
Cifuentes, A. y M. Vanegas. 1987. Distribución de poblaciones de arañita verde inmaculada (Tetranychus urticae Koch) y efecto de cuatro acaricidas en cultivo de rosa (Rosa sp.) variedad Visa. Trabajo de grado. Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. 73 p. [ Links ]
Cloyd, R. 2003. Managing insects and mites. En: Hamrick, D. (ed.). Ball redbook: Crop protection. Ball Publishing, Illinois. 724 p. [ Links ]
Criollo, Y. y G. Duarte. 2004. Evaluación de la fluctuación de los estado biológicos de Tetranychus urticae Koch, sobre dos variedades de fresa en tres fincas del municipio de Sibaté Cundinamarca. Trabajo de grado. Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. [ Links ]
Fernando, M.H.J.P. y M. P. Hassell. 1980. Predator-prey responses in acarine system. Res. Popul. Ecol. 22, 301-322. [ Links ]
Flórez, V.J., A Leyba, G. Reyes y G. Fischer, G. 2000. Diagnóstico y evaluación en procedimientos en la poscosecha de rosas. Asocolflores 59, 48-52. [ Links ]
Forero, L.G. 2006. Determinación de algunos criterios para el control de Tetranychus urticae Koch (Acari: Tetranychidae) con el ácaro depredador Amblyseius sp. (Acari: Phytoseiidae) en rosas. Tesis de grado. Facultad de Ciencias, Universidad Militar Nueva Granada, Bogotá. 53 p. [ Links ]
Gómez, H. 1999. Algunos métodos estadísticos para el estudio de poblaciones de organismos. Facultad de Ciencias Agropecuarias, Universidad Nacional de Colombia, Medellín. 216 p. [ Links ]
Gómez, S., M. Pérez, C. Barreto, M. García, J. Cure y E. Torrado. 2004. Introducción del depredador Phytoseiulus persimilis como componente del manejo integrado de la arañita roja Tetranychus urticae. Asocolflores 65, 43-58. [ Links ]
Diccionario HC Agropecuario. 2005. Vademécum de productos agropecuarios. Edición 15. HC Ediciones, Bogotá. [ Links ]
Jiménez, L. 1997. Evaluación de ciclos de vida y comportamiento de Phytoseiulus persimilis Athias-Henriot y Tetranychus urticae Koch en follaje de Rosa (Rosa sp.) variedad visa. Tesis de grado. Facultad de Ciencias, Universidad Nacional de Colombia, Bogotá. 59 p. [ Links ]
Malais, M. y W. Ravensberg. 1991. Conocer y reconocer la biología de las plagas de invernadero y sus enemigos naturales. Editorial Koppert Bilogical Systems, Holanda. 109 p. [ Links ]
Marín, A. R. 2002. Estudio y propuesta de un modelo de manejo integrado para el control de ácaros Tetranychus urticae Koch en un cultivo de rosa para exportación de la Sabana de Bogotá. Tesis de grado. Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. [ Links ]
Mendoza, L., A. Acosta, J. Ospina y L. Díaz. 2001. Evaluación de diferentes estados de ácaros del género Tetranychus en cultivos de flores de la Sabana de Bogotá. Asocolflores 60, 11-24. [ Links ]
Nachman, G. 1981. Temporal and spatial dynamics of an acarine predator-prey system. Animal Ecol. 50 (2), 435-451. [ Links ]
Pedigo, L.P. y G. Buntin (eds.). 1994. Handbook of sampling methods for arthropods in agriculture. CRC Press, Boca Ratón, Florida. 714 p. [ Links ]
Praktijkonderzoek, P. y K. Omgeving. 2001. Cultivo moderno de la rosa bajo invernadero. Ediciones Hortitecnia, Bogotá. 203 p. [ Links ]
Salas, C. 2001. Disposición espacial del ácaro Tetranychus urticae (Koch) en un cultivo de rosas y de Tetranychus cinnabarinus (Boisduva) en un cultivo de claves en el municipio de Subachoque, Cundinamarca. Tesis de grado. Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. 142 p. [ Links ]
Santamaría, G., C. Salas, A. Acosta y J. Amador. 2002. Estudio de la disposición vertical y horizontal de Tetranychus spp. en plantas de rosa, clavel y alstroemeria. Asocolflores 63, 44-60. [ Links ]
Shelton, A. y J. Trumble. 1986. Monitoring insect populations en handbook of pest management in agriculture. Volumen II. CRC Press. [ Links ]
Van Lenteren, J. C. y M.G. Tommasin. 2003. Mass production, storage, shipment and release of natural enemies. En: Van Lenteren, J.C. (ed.). Quality control and production of biological control agents- Theory and testing procedures. Cabi Publishing, Londres. 327 p. [ Links ]
Vélez, R. 1997. Plagas agrícolas de impacto económico en Colombia: bionomía y manejo integrado. Editorial Universidad de Antioquia, Medellín. 482 p. [ Links ]
Zhang, Z.y J. Sanderson. 1995. Twospotted spider mite (Acari: Tetranychidae) and Phytoseiulus persimilis (Acari: Phytoseiidae) on greenhouse roses: Spatial distribution and predator efficacy. Economic Entomol. 88 (2), 352-357. [ Links ]














