Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Medicas UIS
versão impressa ISSN 0121-0319
Medicas UIS vol.29 no.2 Bucaramanga maio/ago. 2016
https://doi.org/10.18273/revmed.v29n2-2016001
DOI: http://dx.doi.org/10.18273/revmed.v29n2-2016001
Evaluación de la gestión del suministro de
medicamentos antirretrovirales en una institución
prestadora de salud Medellín-Colombia 2013
Flor Ángela Tobón-Marulanda*
Jessica Loaiza-Ocampo**
Yesenia Andrea Rojas-Durango***
* Química Farmacéutica. Magíster en Farmacología. Especialista en Atención Farmacéutica. Docente Titular Investigadora de la Universidad de Antioquia. Integrante de los Grupos de Investigación en Tecnología en Regencia de Farmacia de la Facultad de Ciencias Farmacéuticas y Alimentarias y del grupo UNI-PLURI/VERSIDAD de la Facultad de Educación. Universidad de Antioquia. Medellín. Antioquia. Colombia.
** Estudiante de Tecnología en Regencia de Farmacia. VI Nivel. Facultad de Ciencias Farmacéuticas y Alimentarias. Universidad de Antioquia. Medellín. Antioquia. Colombia.
*** Licenciada en Ciencias Naturales. Magíster en Educación. Docente Investigadora. Facultad de Educación. Universidad de Antioquia. Medellín. Antioquia. Colombia.
Correspondencia: Profesora Flor Ángela Tobón Marulanda. Dirección: Calle 67 #53-108, bloque 1-of.413. Universidad de Antioquia, Medellín. Teléfono: (4)2198452. Correo electrónico: flor.tobon@udea.edu.co
Artículo recibido el 20 de Abril de 2015 y aceptado para publicación el 13 de Febrero de 2016.
RESUMEN
Introducción: existe la necesidad de impulsar el suministro racional de medicamentos, según la necesidad del paciente, desde la gestión integral de un seguimiento fármaco-terapéutico con calidad y un enfoque de riesgo al usar un fármaco. Objetivo: analizar antecedentes en perspectiva de la gestión integral del suministro de los medicamentos antirretrovirales, con el fin de contribuir a mejorar la calidad de vida del paciente. Materiales y Métodos: estudio cualitativo retrospectivo con enfoque hermenéutico, en una institución prestadora de salud de la ciudad de Medellín en el año 2013. Se realizó una revisión y análisis de los protocolos del sistema de gestión de la calidad de la institución en estudio, conforme a la normatividad vigente. A su vez, se hizo un diario de campo junto con observación no participante a los procesos que se ejecutan en las categorías de Inspección, Vigilancia y Control. Principalmente, se llevó a cabo un análisis estadístico del seguimiento fármaco-terapéutico mediante el coeficiente de Spearman. Resultados: se encontró que la gestión del suministro de los antirretrovirales en general se cumple conforme a las normas. No obstante, se halló que el seguimiento fármaco-terapéutico a cada uno de los pacientes que asisten a la institución es deficiente. Se evidenció que en el primer trimestre del año 2013 97,5% de los pacientes tratados con antirretrovirales, no le hicieron seguimiento fármaco-terapéutico en conformidad a la normatividad vigente y a lo establecido por los protocolos. Conclusión: se requiere mejorar y fortalecer el servicio de atención farmacéutico, liderado por profesionales suficientes y capacitados, que implementen otro seguimiento fármaco-terapéutico holístico, sistemático y permanente. MÉD.UIS. 2016;29(2):11-20.
Palabras clave: Servicios Farmacéuticos. Antirretrovirales. Control de Calidad.
Antiretrovirals drug supply management evaluation at a health care institution in
Medellín-Colombia 2013
ABSTRACT
Introduction: there is the need to promote rational drug supply, according to the patient's need, from the comprehensive management of drug-therapeutic monitoring quality and a perspective of risk by the use a drug. Objective: to analyze antecedents in perspective to the integrated management supply of antiretroviral drug system s in order to contribute to improving the quality of life for patients. Materials and Methods: a retrospective qualitative study was performed with hermeneutical approach, the methodological process was the review and the analysis of the protocols of the institution under the study, according to the regulations; field diary and non-participant observation processes running on the categories of Inspection, Monitoring and Control. Especially, the pharmaceutical care, this statistical analysis was performed using Spearman coefficient. Results: it was found that protocols from integrated management supply of antiretroviral drugs system are comply. Nevertheless, the pharmaceutical care to each of the patients attending the institution is poor. They showed that in the first quarter of 2013, 97.5% of the patients with antiretroviral regimens were not under pharmaceutical care in accordance with the current regulations and the provisions of the protocols. Conclusion: it is necessary to improve and strengthen the pharmaceutical care service led by a trained professional that implements other permanent, systematic, holistic and pharmaceutical care. MÉD.UIS. 2016;29(2):11-20.
Keywords: Pharmaceutical Services. Anti-Retroviral Agents. Quality Control.
¿Cómo citar este artículo?: Tobón-Marulanda FA, Loaiza-Ocampo J, Rojas-Durango YA. Evaluación de la gestión del suministro de medicamentos antirretrovirales en una institución prestadora de salud Medellín-Colombia 2013. MÉD.UIS. 2016;29(2):11-20.
INTRODUCCIÓN
La terapia con Medicamentos Antirretrovirales (MARV) contribuye a reducir la mortalidad y a mejorar la calidad de vida de las personas infectadas con el Virus de la Inmunodeficiencia Humana (VIH), pero a la vez puede inducir complicaciones al cuadro clínico, el cual en algunos casos puede ser más complejo por los efectos tóxicos e interacciones de los MARV con otro medicamento o algún alimento1. Por ello, surge el reto de impulsar un Sistema de Gestión Integral de Calidad (SGIC) en el suministro de MARV, una responsabilidad social de todos los involucrados en el Servicio de Atención en Salud2 (SAS), articulado al Servicio Integral de Atención y Cuidados Farmacéutica (SIACF), a fin de que se ejecuten actividades de promoción de la salud y de prevención de factores de riesgo (FR) en la cadena del suministro de los MARV por la seguridad del paciente desde la atención primaria en salud (APS) y una política farmacéutica beneficosa1-5.
En Colombia, hoy se mercadea alrededor de 20 MARV, de los cuales cerca de 16 están incluidos en el Plan Obligatorio de Salud (POS) del sistema General de Seguridad Social en Salud (SGSSS), como Lamivudina, Zidovudina, Ritonavir, entre otros, los cuales requieren de un SGIC a través del SIACF, desde la APS y de la política farmacéutica beneficiosa. Se señala en algunos estudios consultados en el ámbito global, que cerca del 96% de los pacientes con terapia antirretroviral presentan como mínimo un evento clínico, es decir una Reacción Adversa Medicamentosa (RAM) que podría alterar el efecto farmacológico y el estado clínico, dando como resultado la inefectividad de la terapia o complicación del paciente que amerita la utilización de un medicamento adicional5-7.
En este sentido, si bien el uso óptimo de los MARV contribuye a reducir la morbimortalidad por infección del VIH-SIDA y a mejorar la calidad de vida del paciente, en otros casos puede representar una RAM de diferente grado de severidad. Por ejemplo, la Zidovudina produce granulocitopenia, acidosis láctica, cardiomiopatía, rabdomiolisis, entre otras. De igual modo, el Ritonavir induce el metabolismo del sistema enzimático P450 del Diclofenaco o Fenitoina, Amitriptilina, Omeprazol, Fluoxetina, Warfarina o Glibenclamida, disminuyendo la concentración plasmática de estos fármacos, paralela a la disminución del efecto terapéutico. Por ejemplo, la interacción entre el Ritonarir con el omeprazol, reduciría el efecto antisecretor gástrico y con la fenitoina; disminuye el efecto anticonvulsivante de esta8-12.
En general las RAM e interacciones de los medicamentos, se asocian a la variabilidad biológica (disposición genética) de cada ser humano único o algún problema en la cadena del suministro. No obstante, algunos factores de riesgo son prevenibles, como errores relacionados con la disponibilidad, la prescripción, la dispensación, la calidad del MARV y el uso adecuado de este. Aspectos que se pueden ayudar a prevenir a través de un SGIC en el SIACF integrado al SAS en cada contexto en particular10-13.
Por estas razones, hoy desde una visión holística sistemática de las IPS y las EPS, es una necesidad la estructuración de la Gestión Integral del Suministro de los Medicamentos Antirretrovirales (GISMARV) desde el SIACF, para una prevención oportuna de los FR asociados al suministro de MARV. Donde, los profesionales sanitarios tienen una responsabilidad y función social de proporcionar al paciente los MARV con cierta garantía de seguridad, eficacia, costo y oportunidad de acceso al tratamiento terapéutico y asistencial de carácter técnico y científico, en coherencia con la Lex Artis o Ley del Arte14,15 desde la APS2-5,13.
El presente trabajo tiene como objetivo analizar los antecedentes en perspectiva de la GISMARV, respetando principios éticos, mediante la indagación retrospectiva de acciones y procedimientos que se realizan coordinados por el sistema integral de atención y cuidados farmacéutica y la gestión del servicio de atención en salud en una IPS de la ciudad de Medellín 2013, unidos al Seguimiento Farmacoterapéutico (SFT) desde la APS16-18.
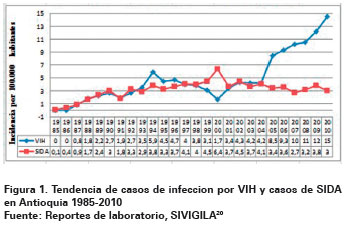
Teniendo en cuenta los datos epidemiológicos, la prevalencia de VIH/SIDA en Medellín entre 2006 a 2012 fue 1,8%19, lo que indica que puede favorecer un aumento en la incidencia de esta enfermedad; en algunos casos influyen errores en la prescripción, conductas de vida, entre otros factores de riesgo que constituyen un problema de salud pública en la región (Ver Figura 1).
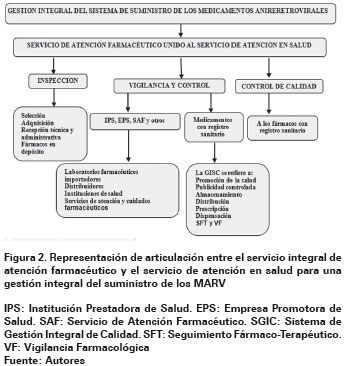
Por tanto, este estudio se enfocó en el análisis de lo que debe ser una estructura organizacional del SIACF, articulado al SAS, en la búsqueda de la transformación de la GISMARV actual en las IPS y en las EPS, por otra GISMARV renovada11-12 (Ver Figura 2).
En este ideal, se pretende promover una GISMARV de impacto positivo en el marco de la salud pública, para que se ayude al paciente a la prevención de algún FR probable, como un aporte a la disminución de los errores en la medicación, para lo que se debería construir indicadores que evalúen el riesgo/beneficio y costo/utilidad. Los cuales impactan las dimensiones de lo humano, social, clínico, político y lo económico, atribuible a la posible complicación del estado de salud del paciente.
Una GISMARV que promueva la dignidad y una mejor calidad de vida del ser humano; según referentes de reglamentación y de regulación colombiana, tales como la Norma ISO 9000:2000; artículos 176 y 245 de la Ley 100 de 1993; resoluciones del Ministerio de Protección Social (MPS), 1403 de 2007; 4316 de 2010 y resolución 458 de febrero de 2013 que deroga la resolución 4377 de 2010 y la Ley 1438 de 201. De obligatorio cumplimiento aplicable en todos los procesos de la IVC eficiente del SAS, relacionados a la calidad de la cadena de los MARV.
MATERIALES Y MÉTODOS
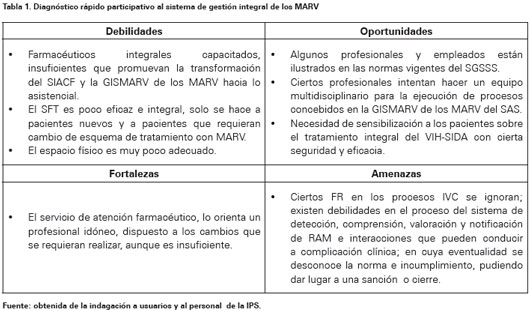
Se trata de un estudio cuali-cuantitativo retrospectivo de carácter hermenéutico21-22. El proceso metodológico se realizó mediante un diagnóstico rápido y participativo de la GISMARV a la IPS en estudio mediante la matriz de debilidades, oportunidades, fortalezas y amenazas. La revisión documental que proporcionó la IPS sobre las acciones y procedimientos que realiza en las categorías de la IVC, relacionadas con la gestión del suministro de MARV.
Como criterios de inclusión, se seleccionaron los documentos que se ajustaban a las normas vigentes ya mencionadas y se tuvo en cuenta las acciones y procedimientos que se estuvieran ejecutando periódicamente en cada uno de los procesos de la IVC de la GISMARV. El análisis cualitativo de la información obtenida, se confrontó con la documentación legal disponible en Colombia ya señalada y con las observaciones consignadas en un diario de campo, utilizado como una herramienta práctica en la formación investigativa temprana, donde se registró procesos sobre la IVC en el marco de la legislación colombiana, durante el año 2013. El proceso de este análisis fue la transcripción textual, la organización y la triangulación de la información obtenida, relacionada con las acciones y procedimientos que realizaba la IPS en los procesos de la IVC, mediante el programa de cómputo Atlas-ti, Versión 6.0. 7.
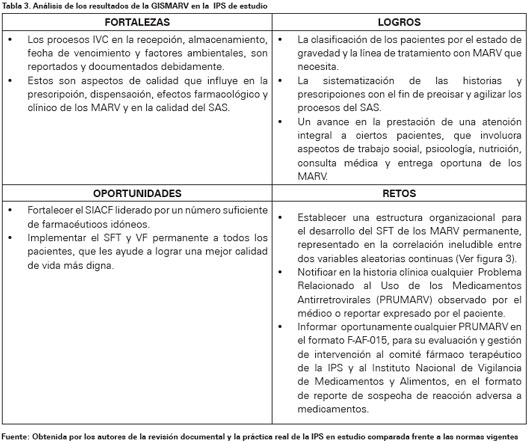
A partir de la triangulación de la información, esta se clasificó en documentos primarios y se creó las unidades hermenéuticas, denominadas las categorías de análisis en la IVC. El análisis de los hallazgos se realizó conforme a la directriz del SGSSS y se empleó la matriz FLOR (Fortalezas, Logros, Oportunidades y Reto) en cada una de ellas. Esta técnica perfecciona la matriz tradicional DOFA (Debilidades, Oportunidades, Fortalezas y Amenazas), convirtiendo los aspectos negativos en positivos, sin dejar de lado los inconvenientes u obstáculos. Las categorías de IVC, se analizaron como retos de la situación actual, en perspectiva de avances en el futuro de las características internas y externas de la IVC en contexto. Los hallazgos del SFT, se analizaron mediante el coeficiente estadístico de correlación de Spearman.
RESULTADOS
Al analizar por categoría de la IVC en la cadena del suministro de los MARV durante la GISMARV, se encontró la necesidad de talento humano farmacéutico capacitado en un SIACF para sensibilizar y motivar al paciente con VIH-SIDA en la importancia del tratamiento integral (Ver Tabla 1), cabe aclarar que este proceso está regulado por el artículo 245 de la Ley 100 de 1993 y el Decreto 1280 de 2002 y debe ser evaluado por organismos de vigilancia en salud a través de la seccional de salud, hospital, IPS o EPS.
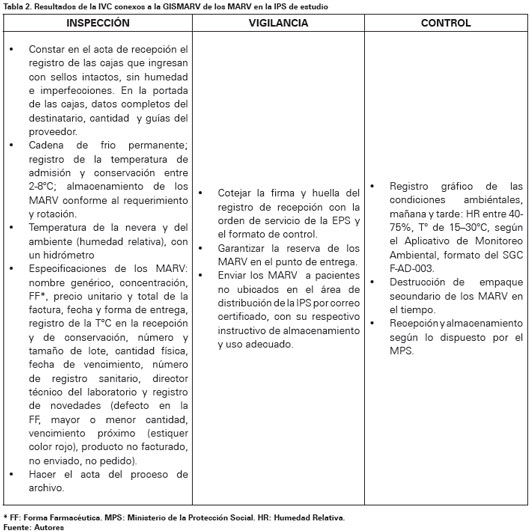
Entre los hallazgos ejecutados por la IPS durante las etapas de recepción y almacenamiento se resaltan los encontrados en los procesos de IVC, como las condiciones más importantes de registro, empaque y almacenamiento en la etapa transitoria de la recepción de los MARV (Ver Tabla 2). Además se encontró un plan de contingencia de mantenimiento de la nevera y calibración del termo-higrómetro en los procesos de recepción y almacenamiento transitorios, con el fin de garantizar una temperatura óptima, que brinde estabilidad a los MARV almacenados en cadena de frío mientras son distribuidos a su sitio final. Los MARV fotosensibles son almacenados sobre estibas o estantes, separados de las paredes y del techo; allí son ubicados por orden alfabético y no tienen iluminación directa o indirecta. La reposición de los MARV, se hace una o dos veces por semana, según la demanda de usuarios.
En la dispensación de los MARV a los usuarios por el SAF, los registros de entrada y salida son controlados por médicos de esta IPS según el formato de verificación mensual de la prescripción, con fecha del mismo mes de dispensación, firma y registro del médico, cantidad, fotocopia de la cédula, firma y huella del paciente junto con la orden de solicitud de la EPS. Cuando el paciente se hospitaliza, el caso lo reporta la EPS o el paciente a la IPS y se solicita su dispensación. Si el paciente no puede asistir a la dispensación de los ARV, autoriza a una persona mediante un poder firmado, número de cédula y copia de esta.
El análisis de los resultados aplicando el modelo de la matriz FLOR, muestra los avances más importantes en algunos aspectos de calidad en la GISMARV, como los relacionados a la prescripción, dispensación, efectos farmacológicos y clínicos, prestación y calidad del SAS. No obstante, existen oportunidades y retos por alcanzar, como una articulación mejor del SAS con un SIACF para la estructuración del seguimiento farmacoterapéutico con vigilancia farmacológica adecuada (Ver Tabla 3).
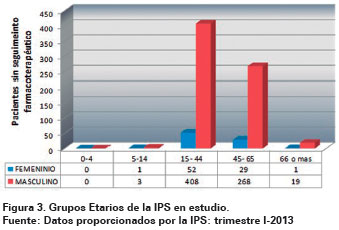
Al correlacionar los grupos etarios de usuarios, según el sexo, se encontró que de 781 pacientes diagnosticados con VIH en el primer trimestre del año 2013, 97,5% no recibió seguimiento farmacoterapéutico (Ver Figura 3).
DISCUSIÓN
La IPS estudiada sigue un manual de condiciones y de procedimientos esenciales coherentes con los requisitos de los procesos técnico-científicos relacionados a lo administrativo y sanitario. Sin embargo, si bien estos son referentes del cumplimiento o no de la reglamentación y de las condiciones para habilitar el SAS en los procesos de la IVC en la etapas de recepción y almacenamiento de la cadena de los MARV, sin embargo, el proceso de SFT a los pacientes con VIH-SIDA que consultan a la institución; no se cumple con la celeridad y equidad suficiente.
Se observa que la IVC en la fase de las recepción y almacenamiento transitorio, se realiza conforme a lo establecido en los instructivos de la guía de buenas prácticas I-AD-002, F-AD-002, I-AD-011 y I-AD-010, cumple el monitoreo de la T0 y de la HR, al menos dos veces al día en puntos críticos del área de la bodega, durante los siete días de la semana. El área permite la manipulación ordenada de los MARV seleccionados, técnicas higiénicas adecuadas y el flujo del personal con materiales y productos. La selección de los laboratorios farmacéuticos para la compra de los MARV, no aplica rigurosamente la Norma ISO 9000:200023. Al respecto, se requiere de la búsqueda y estructuración de alternativas que mejoren la gestión y aseguramiento de la calidad de los medicamentos y afines en general.
Aunque la compra se hace por orden médica, en el 100% de los casos, llama la atención que se hallaron almacenados pocos MARV incluidos en el POS y predominaban los MARV no POS, lo que admite plantear que este punto es contrario a lo que estipula el SGSSS y surge la inquietud: ¿Cuál es la razón para que no se tenga disponibles los MARV incluidos en el POS, para una dispensación oportuna a los pacientes?
Aunque la IPS en estudio cumple los procesos de la IVC durante la dispensación de estos fármacos, debería acompañarse del valor agregado de la información educativa necesaria al paciente y a familiares sobre el uso y almacenamiento adecuado del MARV, junto con el seguimiento farmacoterapéutico y la vigilancia farmacológica de forma individualizada, según la necesidad clínica de cada paciente. En esta perspectiva, la IVC de la dispensación debería ejecutarse junto con la información sobre cualquier PRUMARV e interacción con otro fármaco, alimento o prueba de laboratorio.
Este análisis según el coeficiente de correlación de Spearman, evidencia que en oposición a lo que debería ser las acciones y procedimientos de un SFT, al 97,5% de los pacientes tratados con MARV, no se les realizó SFT en esta IPS. En conjunto, este estudio revela la necesidad del acompañamiento del farmacéutico idóneo en conocimiento integral de lo humano, psicoafectivo, sociocultural y político-económico, en la práctica asistencial para que lidere el SFT en equipo con los demás profesionales de salud, a todos los pacientes con tratamiento antirretroviral e investigue PRUMARV.
Esta exploración a partir de la visión de la gestión integral de calidad en el suministro de MARV, indica que es contraria al trabajo de otros países, como España, Australia, entre otros, donde los procesos de IVC del SFT son más integrados y documentados de forma holista sistemática y permanente, incluida la colaboración del paciente, hacia la identificación de los errores de medicación, RAM y de los PRUMARV24-29. Esto último se hace mediante el método Dáder29-30, un procedimiento activo global del SIACF, que permite registrar en la historia clínica, monitorear, identificar y evaluar la información asociada a los PRUMARV.
Además de intervenir y evaluar el impacto clínico y económico del evento, hay la necesidad de hacer más investigaciones fármaco-epidemiológicas, con el fin de mejorar la calidad de vida de los usuarios y reducir costos en el área de salud. Un ejemplo, es el estudio realizado en el año 2007 por Amariles et al, atribuible al SFT1,7,11 en el ámbito colombiano a 498 pacientes, donde se detectó 508 PRUMARV, de los cuales 443 (87,2%) fueron resueltos a través de intervenciones farmacéuticas, significando para la institución un ahorro de 9000 dólares en cinco meses aproximadamente. En contraste, 65 casos no fueron resueltos y el 23% terminaron en RAM. Otro ejemplo, es un estudio de vigilancia farmacológica, sobre interacciones medicamentosas en pacientes afiliados al sistema de salud en Colombia17 realizado por Amariles en el año 2002, este indicó que hasta un 41% de los pacientes que usan juntos dos o más MARV pueden presentar algún tipo de RAM. De estos pacientes, el 0,3% al 23,0%, pueden requerir hospitalización con costo representativo humano, clínico, social y económico para el SGSSS Colombiano, las cuales podrían ser prevenibles o evitables, entre el 59 al 81,0%.
Se requiere transferencia de conocimiento que eduque, forme y forje integralmente a los estudiantes, prescriptores y a los pacientes en otras actitudes y alternativas prácticas saludables que mejore y fortalezca la rectoría de la gestión integral de calidad en el suministro de MARV, en el saber-hacer en equipo durante el acompañamiento en el uso adecuado cuando sean realmente necesarios, considerando que todos somos corresponsables, esencialmente las autoridades responsables directas de educación (universidades) y salud (regional, hospitales, EPS y las IPS).
Esto se puede lograr a través de planes, programas y proyectos que desarrollen la IVC en el SFT de los MARV, que impulsen la expansión de la creatividad y de la formación investigativa temprana de forma transversal, hacia la evolución de los FR relacionados con el uso incorrecto de los MARV (errores en la prescripción, dispensación; disponibilidad deficiente; información poco transparente; el gasto, la oferta y en el suministro insuficiente de MARV). Mediante estudios enfocados hacia:
1. La responsabilidad social del farmacéutico en la identificación y clasificación de las causas probables atribuibles a los PRUMARV, dentro de la rectoría del sistema de calidad del INVIMA en todos los procesos de la GISC. Considerando a los profesionales sanitarios parte de este sistema de salud colombiano complejo, en el cual, el objetivo común es prevenir, controlar o resolver un problema de salud de ciertos pacientes, asociados con el uso de los MARV. Esto implica que aún con la ejecución adecuada de los procesos que componen la gestión integral de calidad en el suministro de MARV, existe incertidumbre latente de PRUMARV que impide lograr el efecto específico fármaco-terapéutico deseado, persiste el dilema que se debe convertir en oportunidad para el despliegue de factores protectores para la salud integral3, 24-27.
2. El aumento de consciencia humana, social y ética en los actos clínicos y farmacéuticos, a partir de una comprensión más profunda de la aplicación racional de las ciencias de la farmacología, farmacoepidemiología y de la clínica. Es preciso entender lo que representa un porcentaje alto de ingreso y prórroga hospitalaria por la falta de un SFT, lo que aumenta el costo humano, clínico y social para el paciente, la IPS y el SGSSS. Teniendo en cuenta que el SGSSS requiere de la disponibilidad, acceso y calidad de los medicamentos que sean seguros, efectivos y a precio justo; los cuales el sistema pueda soportar en esta crisis económica de la salud colombiana y global, en el marco del modelo político-económico neoliberal.
Por tanto, es un reto fundamental de las instituciones educativas y de salud, la educación en un conocimiento más amplio de las RAM e interacciones medicamentosas de los MARV. Lo que requiere del avance en diálogo de saberes entre las ciencias biomédicas con las ciencias farmacéutica, humana y social; estas aplicadas a la comunicación clara, precisa y completa entre el médico-paciente, el farmacéutico-paciente y el médico con la industria farmacéutica. Así se podría disminuir, evitar e intervenir los FR probables evitables, de la creciente aparición de RAM tóxicos e interacciones medicamentosas.
Desde esta mirada amplia, se resalta que un SAS poco articulado al servicio integral de atención y cuidados farmacéuticos, se relaciona con una calidad holística deficiente y puede constituirse en un factor de riesgo que afecta la salud integral del paciente, en perspectiva de derecho superior a la salud física, mental, social y ambiental. Considerando que varios casos de estos se convierten en un problema de salud pública, sumado a una visión de servicio farmacéutico con tendencia al negocio nacional y global, se induce el consumismo y acceso inequitativo de la población a los medicamentos esenciales, entre ellos algunos MARV.
La esencia de la GISMARV en las IPS y de las EPS debe estructurarse en un servicio de atención y cuidados farmacéuticos basados en principios psicoafectivos, socioculturales, político-económicos, tecnológicos, ambientales y metas de desarrollo, partiendo de la APS y la política farmacéutica beneficiosa en pro de la seguridad del paciente, reflejada por la satisfacción principalmente de las partes involucradas. Todo lo anterior debe realizarse con el fin común de lograr el mejor efecto terapéutico y clínico posible, evitando los PRUMARC y contribuyendo a la calidad de vida del ser humano, a la transformación y al progreso de la sociedad13-16,28-34.
CONCLUSIONES
Este estudio revela la oportunidad y el desafío principal de la institución de lograr una estructuración organizacional del SFT eficaz, oportuno y continuo, que fortalezca la cultura institucional y garantice la seguridad y la adherencia del paciente al tratamiento. Para lo cual se requiere de la vinculación de talento humano idóneo suficiente para lo cual se debe asignar el recurso económico suficiente para el desarrollo del SIACF conexo al SAS, donde se practique la Ley del Arte; una herramienta estratégica que ayuda a disminuir la probabilidad de falla terapéutica, PRUMARV, inestabilidad o vencimiento del MARV, entre otros aspectos que otorgan beneficios al paciente, al SGSSS y a los colectivos.
Asimismo, desde una visión holística sistemática, a manera de recomendación relevante para una mayor aproximación al lema de esta IPS: "El bienestar del paciente, es la esencia de nuestra filosofía empresarial", se propone el desarrollo del SIACF unido al SAS, donde se ejecute estrategias sencillas, efectivas y posibles que contribuyan al mejoramiento continuo del SFT y la VF de los MARV. Mediante la indagación, identificación, evaluación del impacto social y de la prevención de PRUMARV evitables; asociados con la seguridad y eficacia de la prescripción, en cada uno de los pacientes de la institución.
Además, la dispensación de estos fármacos debería acompañarse del valor agregado de la información educativa necesaria al paciente y familiares sobre el uso y almacenamiento adecuado del MARV.
Una alternativa que podría aportar al reto de evitar y reducir los PRUMARV específicos, relacionados a los procesos en la cadena de la gestión integral de calidad en el suministro de MARV, es plantear metas mediante la implementación de ciertos indicadores que evalúen la causalidad en el marco de la seguridad/beneficio, utilidad/eficacia, entre otros. Por ejemplo, establecer la relación entre el número de PRUMARV por el número de problemas relacionados con el medicamento en un periodo de tiempo. La estimación del daño por un PRUMARV es diversa, compleja y específica en toda la cadena del medicamento y determinada por la variabilidad biológica característica de cada ser humano. En este sentido, los indicadores deben ser construidos por el investigador en cada contexto específico, según niveles de apreciación del PRUMARV de leve, moderado, grave, hasta letal.
CONFLICTO DE INTERESES
Los autores declaran no tener conflicto de intereses.
FINANCIAMIENTO
Estudio financiado por la Facultad de Ciencias Farmacéuticas y Alimentarias, dentro de las prácticas profesionales de Tecnología en Regencia de Farmacia, con el enfoque de investigación formativa temprana.
CONSIDERACIONES ÉTICAS
El estudio tuvo en cuenta el respeto a la confidencialidad de la información proporcionada por la IPS estudiada.
AGRADECIMIENTOS
Al estudiante en formación investigativa temprana, Juan G. Gutiérrez por apoyar el proceso de esta investigación, a la comunidad de la IPS estudiada y a la Facultad de Ciencias Farmacéuticas y Alimentarias de la Universidad de Antioquia.
REFERENCIAS BIBLIOGRÁFICAS
1. Highleyman L. Interacciones Medicamentosas y Terapia Antirretroviral. [en linea]2005. Disponible en: http://publicaciones.ops.org.ar/publicaciones/piezas%20comunicacionales/cdTallerServiciosFarmaceuticos/publicaciones/Guia_%20SF-APS_4a_version_%2006%2003%2011.pdf [con acceso el 5 de noviembre de 2014] [ Links ]
2. República de Colombia. Ministerio de la Protección Social. Lineamientos para la implementación de la política de seguridad del paciente. [en linea] . 2008. Disponible en:http://www.minsalud.gov.co/Documentos%20y%20Publicaciones/Lineamientos_para_Implementaci%C3%B3n_de_Pol%C3%ADtica_de_Seguridad_del_Paciente.pdf [con acceso el 17 de abril de 2012] [ Links ]
3. Franco A. Fundamentos en seguridad al paciente. Para la disminución de los errores médicos. [en linea] Cali: Universidad del Valle. 2006. Disponible en:https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/DE/CA/LINEAMIENTOS_IMPLEMENTACION_POLITICA_SEGURIDAD_DEL_PACIENTE.pdf [con acceso el 22 de abril de 2014] [ Links ]
4. Tobón F, Gómez M, Salamanca R. Responsabilidades en los acto farmacéuticos. Perspectiva del Sistema de Garantía de Calidad- Atención Farmacéutica. [en linea] Disponible en: http://aprendeenlinea.udea.edu.co/revistas/index.php/vitae/article/viewFile/389/320 [con acceso el 22 de abril de 2014] [ Links ]
5. Organización panamericana de la salud. Guía Servicios Farmacéuticos en la Atención Primaria de Salud (Internet). Washington: Organización Panamericana de la Salud; 2011 [Citado 05 Nov 2015]. Disponible en: http://publicaciones.ops.org.ar/publicaciones/piezas%20comunicacionales/cdTallerServiciosFarmaceuticos/publicaciones/Guia_%20SFAPS_4a_version_%2006%2003%2011. [ Links ]pdf.
6. República de Colombia. Consejo Nacional de Política Económica y Social -CONPES-. Bogotá: Departamento Nacional de Planeación. [en linea] 2012. Disponible en: http://www.minsalud.gov.co/Politicas%20Farmaceuticas/Pol%C3%ADtica%20farmac%C3%A9utica/Documentos%20soporte/23042012%20CONPES%20POLIITCA%20FARMACEUTICA%20PROYECTO.pdf [con acceso el 17 de abril de 2012] [ Links ]
7. Amariles P, Giraldo N. A, Faus M. J. Interacciones medicamentosas en pacientes infectados con el VIH: aproximación para establecer y evaluar su relevancia clínica. Farm Hosp. 2007; 31(5):283-302. [ Links ]
8. Uso racional de los medicamentos: progresos realizados en la aplicación de la estrategia farmacéutica de la OMS. Consenso Ejecutivo. EB11B/6 11Ba, reunión 11 de mayo de 2006. Punto 5.3 del orden del día provisional. [ Links ]
9. República de Colombia. MPS. Boletín de Fármaco vigilancia, número 1. [en linea] 2011. Disponible en: http://web.invima.gov.co/portal/faces/index.jsp?id=4540 [con acceso el 25 de octubre de 2011] [ Links ]
10. Tobón F. Interacción farmacocinética entre un medicamento y un nutriente. Nuevos Tiempos. 2010;18:73-84. [ Links ]
11. Amariles P, Giraldo N, Gómez A. Gestión y aseguramiento de la calidad de la farmacoterapia. En: Aproximación para el contexto del sistema de salud en Colombia. Grupo de Promoción y Prevención Farmacéutica 2007; 64. [ Links ]
12. Fernández F, Faus M, Caelles N, Espejo J, Gastelurrrutia M, Ibañez J, et al. Seguimiento fármaco-terapéutico y dispensación activa: Diferencias y similitudes. Pharm Care Esp. 2002;4:179-185. [ Links ]
13. Machado-Alba J, Morales-Plaza C. Prevalencia de interacciones potenciales evitables entre antidepresivos y otros medicamentos en pacientes colombianos. Colomb Psiquiat. 2013; 42(2):162-166. [ Links ]
14. Le Tourneau P, López M, Bello D, Carrillo R, Cesano J, Santos J. Tratado de responsabilidad médica: responsabilidad civil, penal y hospitalaria. 1st ed. Buenos Aires: Legis Editores; 2007. [ Links ]
15. Valencia G. La Lex Artis. Rev Médico-Legal. 2001; 7(3):21-35. [ Links ]
16. Segura O. El Plan Nacional de Salud Pública: tesis, antítesis, síntesis. Biomédica. 2008; 28(2):177-80. [ Links ]
17. Amariles P. Seguimiento farmacéutico de pacientes en el contexto del sistema de salud de Colombia. Nuevos tiempos. 2002; 10(2): 15-25. [ Links ]
18. Faus M, Amariles P, Martínez F. Atención Farmacéutica conceptos, procesos y casos prácticos. Ergon. 2008;62. [ Links ]
19. Cardona J, Álvarez C, Ruiz G. Prevalencia de VIH/Sida en Medellín y evaluación del desempeño de la prueba presuntiva, 2006-2012. Rev. Salud pública. 2013; 15(6):929-942. [ Links ]
20. Servicio Seccional de Salud de Antioquia. Estructura de la Morbilidad en el Departamento de Antioquia. Tendencia de la infección por VIH-SIDA. [en linea]2010. Disponible en: https://www.dssa.gov.co/index.php/descargas/250-capituloestructura/file [con acceso el 25 de octubre de 2015] [ Links ]
21. Bonilla E, Rodríguez P. El proceso de investigación cualitativa. En: Más allá del dilema de los métodos. Bogotá: Editorial Norma; 1997. [ Links ]
22. Hammersley, M, Atkinson P. Etnografía: métodos de investigación. 2 ed. Barcelona: Editorial Paidós; 2000. [ Links ]
23. Instituto Colombiano de Normas Técnicas y Certificación - ICONTEC- Norma Técnica Colombiana-ISO9000. Sistemas de gestión de la calidad. Fundamentos y vocabulario. [en linea] 2005. Disponible en:: http://www.ceicmo.com/resources/documents/NTC_ISO_9000-2005.pdf [con acceso el 30 de abril de 2016] [ Links ]
24. Medication Errors Fact Sheet. American Society of Health-System Pharmacists. [en linea]1993. Disponible en: https://www.ssspr.com/NR/rdonlyres/B3E77786-1813-443C-9917-C57810E0888/0/PharmaNewsVol8Issue5.pdf [con acceso el 25 de octubre de 2014] [ Links ]
25. Anurag J, Bhatia M, Srivastava S. Medication Errors in Clinical Practice. Delhi Psychiatry Journal. [en linea] 2011. Disponible en: http://medind.nic.in/daa/t11/i2/daat11i2p205.pdf [con acceso el 25 de octubre de 2014] [ Links ]
26. Medical Errors: The Scope of the Problem. Fact sheet, Publication No. AHRQ 00-P037. Agency for Healthcare Research and Quality, Rockville, MD. [en linea]1999. Disponible en: http://www.ahcpr.gov/qual/errback.htm [con acceso el 25 de octubre de 2014] [ Links ]
27. Llor C. Medicamentos que matan y crimen organizado. ElServier Aten Primaria. [en linea]2014. Disponible en: http://apps.elsevier.es/watermark/ctl_servlet?_f=10&pident_articulo=90298172&pident_usuario=0&pcontactid=&pident_revista=27&ty=83&accion=L&origen=zonadelectura&web=www.elsevier.es&lan=es&fichero=27v46n04a90298172pdf001.pdf [con acceso el 22 de abril de 2014] [ Links ]
28. Aguas Y, De Miguel E, Fernández F. El seguimiento fármaco-terapéutico como innovación en las farmacias comunitarias de Badajoz (España). [en linea] 2005. Disponible en: http://www.cipf-es.org/sft/vol-03/010-016.pdf [con acceso el 22 de abril de 2014] [ Links ]
29. Amariles P, Giraldo N, Faus M. Clinical Relevance of Drug Inteactions in HIV-Infected Patients Receiving Antiretroviral Therapy. 1st ed. United States; 2011. [ Links ]
30. Fajardo P, Baena M, Alcaide J, Martínez J, Faus M, Martínez F. Adaptación del Método Dáder de seguimiento fármaco-terapéutico al nivel asistencial de atención primaria. [en linea] 2005. Disponible en: http://www.cipf-es.org/sft/vol-03/158-164.pdf [con acceso el 22 de abril de 2014] [ Links ]
31. Flores L, Segura C, Quesada M, Hall V. Seguimiento Fármacoterapéutico con el Método Dáder en un grupo de pacientes con hipertensión arterial. [en linea]2005. Disponible en: http://www.cipf-es.org/sft/vol-03/154-157.pdf [con acceso el 22 de abril de 2014] [ Links ]
32. Tobón F, Gómez M. Análisis sobre la implementación de consultorios farmacéuticos, un servicio de apoyo de los servicios farmacéuticos. Rev Vitae. 2000; 7(1-2): 63-82. [ Links ]
33. Amariles P, Alzate G, Faus M. Management and Care-Pandemic Approaches in the 21st Century. 1st ed. United States: 2011. [ Links ]
34. República de Colombia. Ministerio de salud y protección social. Lista de chequeo para las buenas prácticas de seguridad de pacientes obligatorias. [en linea] 2008. Disponible en: https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/DE/CA/Guia-buenas-practicas-seguridad-paciente.pdf [con acceso el 17 de abril de 2012] [ Links ]