Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Medicas UIS
versión impresa ISSN 0121-0319
Medicas UIS vol.29 no.2 Bucaramanga may./ago. 2016
https://doi.org/10.18273/revmed.v29n2-2016004
DOI: http://dx.doi.org/10.18273/revmed.v29n2-2016004
Plasmaféresis en rechazo agudo del injerto renal
mediado por anticuerpos. Estudio realizado en el
Hospital Pablo Tobón Uribe, Medellín, Colombia.
Año 2005-2015
Catalina Ocampo-Kohn*
John Fredy Nieto-Ríos*
Arbey Aristizabal-Alzate*
Gustavo Adolfo Zuluaga-Valencia*
Juan Pablo Villa**
Lina María Serna-Higuita***
Catalina Vélez-Echeverri***
Juan José Vanegas-Ruiz***
John Jairo Zuleta-Tobón****
* Nefrólogo Clínico y de Trasplantes. Docente Universidad de Antioquia. Hospital Pablo Tobón Uribe. Medellín. Antioquia. Colombia.
** Médico Internista. Hospital Pablo Tobón Uribe. Medellín. Antioquia. Colombia.
*** Médico Pediatra Nefrólogo. Docente Universidad de Antioquia. Hospital Pablo Tobón Uribe. Medellín. Antioquia. Colombia.
**** Epidemiólogo Clínico. Hospital Pablo Tobón Uribe. Medellín. Antioquia. Colombia.
Correspondencia: Dra. Lina María Serna Higuita. Hospital Pablo Tobón Uribe. Dirección: Calle 78b # 69-240. Medellín. Antioquia. Colombia. Teléfono: +57 4 4459902. Correo electrónico: lm.serna@hotmail.com
Artículo recibido el 30 de Diciembre de 2015 y aceptado para publicación el 04 de Abril de 2016.
RESUMEN
Introducción: el rechazo agudo mediado por anticuerpos es una complicación que se presenta luego del trasplante renal y es una causa importante de pérdida del injerto. La plasmaféresis es una de las terapias utilizadas para su tratamiento, algunos estudios sugieren mejor supervivencia del injerto renal con el uso de plasmaféresis; sin embargo su evidencia es débil. Objetivo: este estudio tiene como objetivo describir la experiencia del uso de plasmaféresis en el rechazo agudo mediado por anticuerpos. Materiales y Métodos: estudio descriptivo retrospectivo realizado en el Hospital Pablo Tobón Uribe entre agosto de 2005 y junio de 2015 en pacientes con diagnóstico de rechazo agudo mediado por anticuerpos, quienes recibieron entre tres y nueve sesiones de plasmaféresis. Resultados: se realizaron un total de 769 trasplantes renales; de los cuales 26 pacientes presentaron rechazo agudo mediado por anticuerpos y recibieron plasmaféresis como parte del tratamiento. Todos los pacientes recibieron terapia de inducción al momento del trasplante y en el 80,8% la terapia de mantenimiento utilizada fue tacrolimus-micofenolato-prednisolona. El rechazo mediado por anticuerpos se presentó en forma temprana en el 61,5% de los pacientes. A seis y doce meses el 44% y 53,8% de los pacientes respectivamente presentaron pérdida del injerto renal; las complicaciones se presentaron en el 53,8% de los pacientes, las cuales fueron hipocalcemia, hipotensión y anafilaxia. Conclusión: en esta cohorte el uso de plasmaféresis en el rechazo agudo mediado por anticuerpos no logró evitar la pérdida del injerto renal en el 50% de los pacientes; se sugiere adicionar a esta terapia otras alternativas de tratamiento entre ellas, la inmunoglobulinas intravenosas, rituximab, eculizumab y bortezomib. MÉD.UIS. 2016;29(2):41-8.
Palabras clave: Plasmaféresis. Rechazo de Injerto. Supervivencia de Injerto. Trasplante de riñón.
Plasmapheresis in antibody-mediated renal allograft rejection. Experience of Pablo Tobon
Uribe, Medellin, Colombia. Year 2005-2015
ABSTRACT
Background: antibody-mediated renal allograft rejection is a complication after kidney transplantation, and it has poor prognosis for graft survival. Plasmapheresis has been used with controversial results; few trials indicate a trend towards superior graft survival in patients receiving this treatment; however, the evidence remains weak. Objetive: the aim of this study was to describe the experience in treating Antibody-mediated renal allograft rejection with plasmapheresis in kidney transplant recipients. Methods: retrospective and descriptive study of the patients that underwent three to nine session of plasmapheresis as a treatment of severe Antibody-mediated renal allograft rejection in Pablo Tobón Uribe Hospital. Results: between August 2005 and June 2015, 769 patients underwent kidney transplantation at our institution; 26 patients received plasmapheresis as part of the treatment for Antibody-mediated renal allograft rejection. All patients received induction therapy. Maintenance therapy used was tacrolimus, mycophenolic acid and steroids in 80,8% of the patients and cyclosporine, micophenolic acid and steroids in 19,2%. Antibody mediated rejection had an early onset in 61,5% of the cases. At six and 12 months after therapy, 44% and 53,8% patients respectively were back on dialysis. Complications were reported in 53,8% of the patients (hypocalcaemia, hypotension and anaphylaxis). Conclusion: in this cohort, 50% of patients who received Plasmapheresis as therapy for severe Antibody-mediated renal allograft rejection presented loss graft after one year of follow up. It is necessary adding to this therapy new treatment alternatives, among them intravenous immunoglobulin, rituximab, eculizumab and bortezomib. MÉD.UIS. 2016;29(2):41-8.
Keywords: Plasmapheresis. Graft rejection. Graft Survival. Kidney transplantation.
¿Cómo citar este artículo?: Ocampo-Kohn C, Nieto-Ríos JF, Aristizabal-Alzate A, Zuluaga-Valencia GA , Villa JP, Serna-Higuita LM, et al. Plasmaféresis en rechazo agudo del injerto renal mediado por anticuerpos. Estudio realizado en el Hospital Pablo Tobón Uribe, Medellín, Colombia. Año 2005-2015. MÉD.UIS. 2016;29(2):41-8.
INTRODUCCIÓN
El Rechazo agudo Mediado por Anticuerpos (RMA) es una complicación cada vez más frecuente en el trasplante renal1-5. Se define según la clasificación de Banff por la presencia de hallazgos histológicos compatibles con rechazo humoral como la infiltración de neutrófilos en capilares peritubulares, glomerulitis, vasculitis severa y necrosis tubular aguda6,7, sumado a la presencia de Anticuerpos Donante Específicos (ADE), definidos como anticuerpos circulantes preformados dirigidos contra el HLA del injerto renal y depósitos de C4d en los capilares peritubulares2. Esta complicación se presenta en el 5% al 7% de los pacientes trasplantados renales8, pero puede ser tan alta como del 28% al 40%8. Aproximadamente 30% de todos los episodios de rechazo son secundarios a RMA4. La importancia del RMA radica en que es una de las causas más importantes de disfunción del injerto, limitando la supervivencia a mediano y a largo plazo del injerto renal9-11, 15% al 20% de los pacientes con RMA pierden el injerto con necesidad de terapia de reemplazo renal3,12.
El RMA se presenta principalmente en los primeros tres meses luego del trasplante renal, pero puede observarse en cualquier momento10. Existen algunos factores de riesgo para RMA, como las transfusiones sanguíneas, embarazos y trasplantes previos2,13,14. Todos estos eventos inducen la formación de ADE, que se depositan en el riñón y activan la cascada de complemento, lo que lleva a lesión del endotelio de los capilares peritubulares y de los capilares glomerulares15.
En la actualidad existen pocas guías y con escasa evidencia para el tratamiento del RMA. Las guías Kidney Disease Improving Global Outcomes16 recomiendan el uso de corticosteroides, plasmaféresis, inmunoglobulinas intravenosa (IVIG), anticuerpos antiCD20 y anticuerpos depletores de linfocitos2,16; sin embargo no existe una recomendación definitiva. La plasmaféresis es una técnica de depuración sanguínea extracorpórea que permite remover proteínas plasmáticas de alto peso molecular, complejos inmunes y autoanticuerpos17; esta terapia se ha utilizado en el RMA, sin embargo los resultados existentes sobre su uso son controversiales; algunos estudios han mostrado que la plasmaféresis alcanza excelentes resultados con tasas de supervivencia a un año del 81%18,19, por el contrario otros estudios no han demostrado beneficio2 y la evidencia que existe es muy débil20. El grupo de trasplante renales del Hospital Pablo Tobón Uribe utiliza la plasmaféresis dentro de su protocolo de manejo en los pacientes con RMA grave; este estudio tiene como objetivo describir la experiencia de esta institución en el manejo del RMA durante los años 2005 a 2015.
MATERIALES Y MÉTODOS
Estudio descriptivo retrospectivo realizado en el hospital Pablo Tobón Uribe, hospital de cuarto nivel de complejidad de la ciudad de Medellín, Colombia. Se incluyeron todos los pacientes con diagnóstico de RMA grave que recibieron plasmaféresis como parte de su tratamiento. El RMA grave se definió por los hallazgos en la biopsia renal21,22 más la necesidad de terapia de reemplazo renal o un valor de creatinina sérica mayor de 2 mg/dl al momento del diagnóstico. Se excluyeron aquellos pacientes en los que no se logró un seguimiento mínimo de seis meses, en quienes no se obtuvo datos suficientes para el análisis estadístico, y quienes no recibieron plasmaféresis como parte de la terapia del RMA.
Para la extracción de los datos, se revisaron las historias clínicas electrónicas de los pacientes trasplantados renales del hospital Pablo Tobón Uribe con diagnóstico de RMA grave y que recibieron plasmaféresis como parte del tratamiento, los datos fueron suministrados por el departamento de sistemas de la información. Para la recolección de la información se construyó una base de datos en Excel®; se incluyeron características demográficas como edad, sexo, etiología de la enfermedad renal crónica estadio terminal, número de incompatibilidades HLA, tiempo de isquemia fría y caliente, transfusiones y trasplantes previos, uso de terapia dialítica previa al trasplante, tipo de donante (vivo o fallecido), inmunosupresión utilizada al momento de la inducción y mantenimiento, y el tiempo transcurrido entre el trasplante y el diagnóstico de RMA. Se recolectó además el número de plasmaféresis realizadas, sus complicaciones y respuesta al tratamiento. Se consideró una adecuada respuesta a la plasmaféresis la no necesidad de terapia de reemplazo renal. Estos pacientes fueron seguidos por un período de un año y durante este tiempo se evaluó la función del injerto renal por medio de la creatinina sérica y la necesidad de Terapia de Reemplazo Renal (TRR), para evaluar los valores de creatinina sérica al momento del alta, 6 y 12 meses pos plasmaféresis, solo se incluyeron los pacientes que no estaban en TRR. La pérdida del injerto renal se definió por el reingreso a TRR23.
Para el análisis estadístico se utilizó el programa SPSS versión 18®. Los pacientes fueron agrupados de acuerdo al descenlace pérdida o no del injerto renal, y de acuerdo al momento del rechazo; el RMA temprano se definió como aquel que ocurrió en un período menor a seis meses luego del trasplante y tardío cuando se presentó luego de seis meses4.
Se realizó un análisis descriptivo de los datos, calculando frecuencias y proporciones para las variables cualitativas; las variables cuantitativas se describieron como promedios o medianas con su respectiva desviación estándar o cuartiles, según la distribución de los datos identificados por la prueba de Shapiro Wills. La supervivencia del injerto se evaluó por medio de una curva de Kaplan Meier.
RESULTADOS
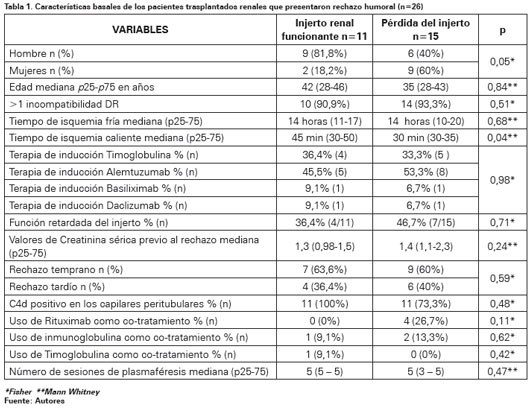
Entre agosto de 2005 y junio de 2015, se realizaron un total de 769 trasplantes renales. De estos 3,4%, presentaron RMA grave quienes recibieron plasmaféresis como parte del tratamiento. El diagnóstico de RMA se confirmó en todos por biopsia renal; la distribución por sexo fue de 58% hombres y 42% mujeres; la edad al momento del diagnóstico de RMA tuvo una mediana de 37,5 años (percentiles (p) 25-75: 28 - 45,3). De los 26 pacientes evaluados, todos recibieron un injerto renal de donante fallecido ABO compatible, el tiempo entre el trasplante y el diagnóstico de RMA temprano tuvo una mediana de 17,5 días (p25-75: 17,5-40,25) y el tiempo entre el trasplante y el diagnóstico de RMA tardío fue de 458 días (p25-75: 313,5-1638). Al agrupar las características basales de acuerdo al descenlace pérdida o no del injerto renal, solo se encontró diferencias con el sexo y el tiempo de isquemia caliente (Ver Tabla 1).
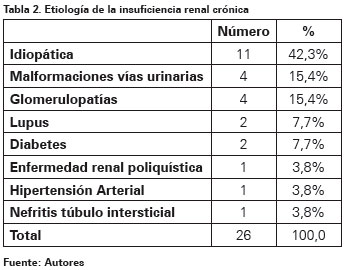
Al momento del trasplante, todos los 26 pacientes recibieron terapia de inducción distribuida de la siguiente manera: 52% alemtuzumab, 34,6% timoglobulina, 7,7% basiliximab y 7,7% daclizumab. La terapia de mantenimiento utilizada fue tacrolimus-micofenolato-prednisolona en el 80,8% de los pacientes y ciclosporina-micofenolato y prednisolona en el 19,2%. En la Tabla 2 se encuentra la etiología de la enfermedad renal crónica.
El rechazo mediado por anticuerpos se presentó en forma temprana en el 61,5% de los pacientes con una mediana de tiempo entre el momento del trasplante y el RMA de 17,5 días (p 25-75:17,5-40,25) y en el 38,5% se presentó en forma tardía (Ver Tabla 1). La mediana de la creatinina sérica al momento del diagnóstico fue de 5,2 mg/dl (p 25-75: 2,2-7,9). El 15,4% de los pacientes requirieron terapia de reemplazo renal al momento del diagnóstico. El RMA se confirmó en todos los pacientes por medio de la biopsia renal; la positividad para C4d se encontró en el 84,6% de los pacientes y en el 15,4% de la biopsias el C4d fue negativo, sin embargo los hallazgos histológicos eran muy sugestivos de rechazo humoral21. Por otro lado más de la mitad de los pacientes presentaron rechazo celular asociado.
Todos los pacientes recibieron como tratamiento tres bolos de metilprednisolona de 500 mg día por tres días, plasmaféresis e intensificación de su inmunosupresión. La plasmaféresis se realizó con una volemia en el 80,8% y con 1,5 volemias en el 19,2% de los casos. El intervalo de tiempo entre cada sesión de plasmaféresis varió de uno a dos días, de los cuales en 12 pacientes se realizó diariamente y en 14 pacientes cada 48 horas. En promedio se realizaron cinco plasmaféresis por paciente mínimo tres, máximo nueve. El tipo de reemplazo utilizado en la plasmaféresis fue albúmina en el 80,8% y plasma fresco congelado en el 19,2% por el hallazgo de microangiopatía trombótica asociada, adicional a la plasmaféresis se administró timoglobulina en un paciente, IVIG en tres y rituximab en cuatro pacientes. Previo a cada sesión de plasmaféresis se evaluaron los valores de hemoglobina, pruebas de coagulación y electrolitos. Todos los pacientes fueron monitorizados durante el procedimiento en la unidad de cuidados especiales.
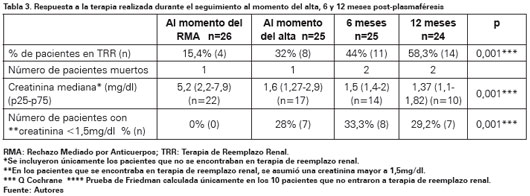
Durante el seguimiento se observó que a los seis y doce meses el 44% y 53,8% de los pacientes respectivamente presentaron pérdida del injerto renal. En los pacientes libres de TRR se observó mejoría de los valores de creatinina sérica (5,1 mg/ dl al diagnóstico de RMA grave vs 1,6 mg/dl al alta, p=0,001) y estos valores de creatinina permanecieron estables a 12 meses de seguimiento (p=0,062) (Ver Tabla 3). Al momento del diagnóstico de RMA, cuatro pacientes necesitaron TRR, todos ellos presentaron pérdida del injerto durante los primeros 12 meses de seguimiento.
Respecto a otros co-tratamientos utilizados al momento de la plasmaféresis, tres pacientes recibieron rituximab, de los cuales todos perdieron el injerto renal, uno al momento del alta, y los otros dos a los tres y seis meses de seguimiento. La IVIG fue utilizada en tres pacientes de los cuales dos perdieron el injerto renal a los dos y seis meses de seguimiento.
El 43,2% de los pacientes presentaron hipocalcemia, sin embargo solo en tres pacientes esta fue severa (valores menores a 7,5 mg/dl); con respecto a otras complicaciones, dos pacientes desarrollaron hipotensión y uno anafilaxia, la solución de reemplazo utilizada en los dos pacientes que presentaron hipotensión fue albúmina, y en el paciente con anafilaxia fue plasma fresco congelado; con respecto a las complicaciones hidroelectrolíticas se presentaron valores de calcio sérico menores de 8,5 mg/dl en el 42,3% de los pacientes. Las infecciones se presentaron en el 38,5% de los pacientes, cuatro pacientes presentaron infección abdominal, tres pacientes bacteriemia y tres neumonía. No se encontró evidencia de infección por citomegalovirus o enfermedad por poliomavirus, infecciones que se presentan con frecuencia en los pacientes trasplantados renales.
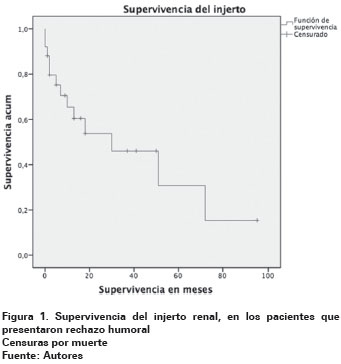
La mortalidad durante el seguimiento fue del 7,7%, la causa de muerte en uno de ellos fue secundaria a infección grave posterior a la plasmaféresis y el segundo por causas no asociadas a la plasmaféresis. La supervivencia del injerto a 6, 12 y 24 meses fue de 91,8%, 77% y 49,3% respectivamente (Ver Figura 1).
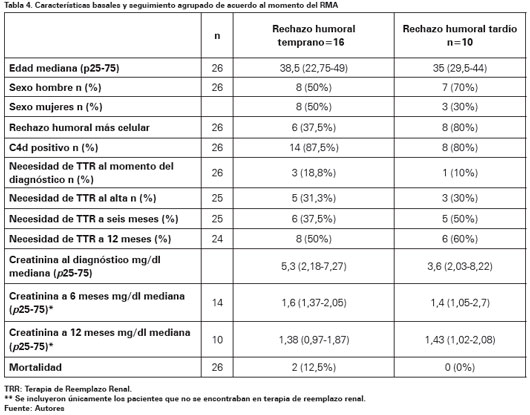
Al agrupar los pacientes de acuerdo al momento del rechazo, un porcentaje mayor de pacientes con diagnóstico de RMA tardío necesito TRR a 6 y 12 meses de seguimiento (Ver Tabla 4).
DISCUSIÓN
El presente estudio describe la experiencia de un único centro de trasplante con el uso de plasmaféresis en los pacientes trasplantados renales con diagnóstico de RMA. Entre los hallazgos más representativos se encuentra que a 6 y 12 meses de seguimiento el 44% y 53,8% de los pacientes respectivamente presentaron pérdida del injerto con necesidad de terapia de reemplazo renal, lo cual es más alto a lo reportado en la literatura, donde la pérdida del injerto en los pacientes con RMA a un año de seguimiento oscila entre 15% al 20%4. Estos hallazgos pueden ser explicados por la gravedad del rechazo en la población estudiada; sin embargo esto puede sugerir que la plasmaféresis, sumado a los bolos de metilprednisolona y ajuste de la medicación inmunosupresora es insuficiente para el control del RMA y por este motivo se requieren otras terapias adicionales3.
En la actualidad existe poca evidencia sobre cual es el tratamiento de elección en el RMA; un gran número de intervenciones terapéuticas se han utilizado con el objetivo de remover los aloanticuerpos responsables del RMA18 y disminuir su producción24-6; la plasmaféresis es la forma más rápida y efectiva de remover ADE3. Uno de los primeros reportes de uso de plasmaféresis en RMA fue publicando en 1998 por Pascual y colaboradores quienes reportaron el tratamiento exitoso en cinco pacientes con RMA que recibieron plasmaféresis más inmunosupresión con tacrolimus y micofenolato, con una supervivencia del injerto a 19,6 meses de 100%13. Böhmig y colaboradores realizaron un estudio en 44 pacientes con RMA y uso de plasmaféresis encontrando una supervivencia del injerto del 80% versus 30% en los que no lo recibieron19. Brown y colaboradores utilizaron plasmaféresis más intensificación de su inmunosupresión en 18 pacientes con RMA, 14 pacientes presentaron mejoría de la función renal y la supervivencia del injerto a un año y cinco años fue de 86% y 78% respectivamente12. No obstante, muchos de estos estudios utilizaron diferentes criterios de inclusión, entre ellos los hallazgos histológicos en la biopsia renal para el diagnóstico de RMA, lo que hace que sus resultados sean conflictivos25. Por el contrario, los estudios aleatorizados no han confirmado el beneficio de la plasmaféresis sola en el RMA2. En el año 2012 se publicó una revisión sistemática que evaluó la eficacia de los diferentes tratamientos utilizados en RMA, de un total de 12 estudios, cuatro fueron estudios controlados aleatorizados que evaluaron el efecto de la plasmaféresis en RMA, de estos solo uno fue benéfico, uno fue peligroso y dos no mostraron efecto2, esta no respuesta se explica posiblemente porque la plasmaféresis no suprime la síntesis de ADE3.
Estudios recientes muestran que la combinación de plasmaféresis, IVIG modificación de la terapia inmunosupresora, sumando bortezomib y rituximab e incluso eculizumab alcanzan excelentes resultados en reversar el RMA con tasa de supervivencia a un año que va del 60% al 81%2,27. Lehrich y colaboradores evaluaron retrospectivamente una cohorte de trasplantados de riñón y páncreas durante los años 1999 a 2003; de un total de 519 trasplantes, 23 pacientes presentaron RMA, 22 pacientes recibieron plasmaféresis e IVIG y un paciente plasmaféresis sola, 11 recibieron pulsos de metilprednisolona y 7 terapia antitimocitica, el 86% de los pacientes respondieron a la terapia y la supervivencia del injerto a dos años fue del 78%1. Gungor y colaboradores evaluaron 39 pacientes trasplantados renales con diagnóstico de RMA en quienes se utilizó plasmaféresis en el 100% de los pacientes, IVIG en once pacientes, timoglobulina en catorce y rituximab en tres pacientes. Se observó mejoría en el 61,5% de los pacientes con valores de creatinina sérica al momento del tratamiento de 2,4mg/dl y a un mes de la plasmaféresis de 1,1mg/dl11, estos hallazgos sugieren que el utilizar otras medidas terapéuticas en el RMA que acompañen el uso de plasmaféresis puede mejorar la supervivencia del injerto renal, entre ellas el rituximab, bortezomib o la IGIV12.
El rituximab es uno de los medicamentos propuestos para el RMA; es un anticuerpo quimérico anti CD20 que inhibe directamente la proliferación de las células B por medio de activación de citotoxicidad dependiente de complemento y apoptosis celular, uno de los inconvenientes con este medicamento es que no remueve las células CD20 negativas que continúan produciendo anticuerpos anti HLA28. En este estudio los tres pacientes que recibieron rituximab perdieron el injerto renal en el primer año de seguimiento, sin embargo es una población muy pequeña para evaluar la respuesta al tratamiento. El Bortezomib es otro de los medicamentos propuestos para el RMA; este es un dipéptido borónico que inhibe el proteosoma 26S, previniendo la activación del factor nuclear Kappa B, esto genera un freno en el ciclo celular e inducción de la apoptosis de las células plasmáticas, destruyendo así la principal fuente de producción de ADE28; por otro lado afecta la presentación antigénica en las moléculas del complejo mayor de histocompatibilidad, posiblemente por inhibición de la síntesis de pequeños péptidos25,28. Everly y colaboradores describieron el uso de bortezomib en una serie de seis pacientes que desarrollaron rechazo mixto y que fueron refractarios a la plasmaféresis, IVIG y rituximab, ellos encontraron mejoría de la función renal y del número de ADE29. Tzvetanov y colaboradores reportan una serie de tres pacientes con RMA temprana y poca respuesta a las terapias convencionales, esto pacientes recibieron bortezomib con mejoría en los valores de creatinina sérica5.
Entre las limitaciones del estudio se destaca su realización en un único centro, lo que puede impedir la aplicabilidad de los resultados incluso en el mismo contexto de nuestro país. Así mismo, el pequeño tamaño de muestra no permite dar conclusiones definitivas sobre la efectividad de la plasmaféresis en el RMA y estimar el efecto de potenciales variables de confusión. Por otro, lado Colombia tiene dificultades para la realización de los ADE y por este motivo este criterio no fue incluido para el diagnóstico de RMA sin embargo en todos se realizó biopsia renal e inmunohistoquímica para C4d, esta última fue negativa en el 15,4% de los pacientes, pero los hallazgos clínicos e histológicos fueron muy sugestivos de RMA. Estos datos concuerdan con el reporte de Banff 2011 y 2013 donde se cuestiona la sensibilidad y especificidad del C4d como un marcador diagnóstico de RMA30,31, ya que hay pacientes con hallazgos y evolución clínica de RMA con disfunción aguda del injerto sin la presencia de C4d15.
CONCLUSIÓN
En la población estudiada la plasmaféresis como terapia única para el tratamiento del RMA no fue suficiente para evitar la pérdida del injerto a un año de seguimiento. Se sugiere adicionar otras opciones terapéuticas, especialmente en el RMA grave, entre ellas iniciar con pulsos de metilprednisolona, plasmaféresis y cambios en el esquema inmunosupresor para continuar con tacrolimus y micofenolato3, acompañado idealmente de otras terapias como timoglobulina, IVIG, rituximab, bortezomib o eculizumab. En Colombia el uso de la de las IVIG, el rituximab y el bortezomib para el tratamiento del RMA no esta aprobado por el Instituto Nacional de Vigilancia de Medicamentos y Alimentos; por este motivo su uso esta sujeto a la aprobación de las aseguradoras; sin embargo se debe tener en cuenta el alto costo de estas terapias en un país con pocos recursos, sumado a que la respuesta con estos tratamientos no han demostrado aún buenos resultados a mediano y largo plazo y los estudios no tienen un numero de pacientes tan grande que pueda justificar completamente el uso de estos medicamentos. Se hace imperativo realizar estudios a largo plazo que puedan dilucidar un tratamiento más costo efectivo, no solo en los centros en los que la industria patrocine estas terapias, sino en países en los que la sobrevida del injerto se relaciona íntimamente con la del paciente, como es el caso de Colombia.
CONSIDERACIONES ÉTICAS
Este estudio fue aprobado por el comité de ética en investigación de la institución y se siguieron las normas sobre aspectos éticos de la investigación en seres humanos contenidas en la Resolución 008430 de 1993 del Ministerio de Salud de Colombia, además se conservó la confidencialidad de los datos personales de los pacientes incluidos en el estudio. Como se trató de un estudio descriptivo no fue necesario consentimiento informado.
CONFLICTO DE INTERESES
Ninguno de los autores tiene conflictos de interés con respecto al contenido de este articulo.
FINANCIACIÓN
Estudio financiado por el Hospital Pablo Tobón Uribe.
REFERENCIAS BIBLIOGRÁFICAS
1. Lehrich RW, Rocha PN, Reinsmoen N, Greenberg A, Butterly DW, Howell DN, et al. Intravenous immunoglobulin and plasmapheresis in acute humoral rejection: experience in renal allograft transplantation. Hum Immunol. 2005;66(4):350-8. [ Links ]
2. Roberts DM, Jiang SH, Chadban SJ. The treatment of acute antibody-mediated rejection in kidney transplant recipients-a systematic review. Transplantation. 2012;94(8):775-83 [ Links ]
3. Lucas JG, Co JP, Nwaogwugwu UT, Dosani I, Sureshkumar KK. Antibody-mediated rejection in kidney transplantation: an update. Expert Opin Pharmacother. 2011;12(4):579-92. [ Links ]
4. Gupta G, Abu Jawdeh BG, Racusen LC, Bhasin B, Arend LJ, Trollinger B, et al. Late antibody-mediated rejection in renal allografts: outcome after conventional and novel therapies. Transplantation. 2014;97(12):1240-6. [ Links ]
5. Tzvetanov I, Spaggiari M, Joseph J, Jeon H, Thielke J, Oberholzer J, et al. The use of bortezomib as a rescue treatment for acute antibody-mediated rejection: Report of three cases and review of literature. Transplant Proc. 2012;44(10):2971-5. [ Links ]
6. Mosquera Reboredo JM, Vázquez Martul E. Diagnostic criteria of antibody-mediated rejection in kidney transplants. Nefrologia. 2011;31(4):382-91. [ Links ]
7. Pascual M, Saidman S, Tolkoff-Rubin N, Williams W, Mauiyyedi S, Duan JM, et al. Plasma exchange and tacrolimus-mycophenolate rescue for acute humoral rejection in kidney transplantation. Transplantation. 1998;66(11):1460-4. [ Links ]
8. Puttarajappa C, Shapiro R, Tan HP. Antibody-mediated rejection in kidney transplantation: a review. J Transplant. 2012;2012:1-9. [ Links ]
9. Mosquera Reboredo JM, Vázquez Martul E. Criterios diagnósticos de rechazo mediado por anticuerpos en el trasplante renal. Nefrologia. 2011;31(4):382-91. [ Links ]
10. Seck SM, Bertrand D, Boucar D. Current indication of plasma exchanges in nephrology: a systematic review. Saudi J Kidney Dis Transpl. 2011;22(2):219-24. [ Links ]
11. Gungor O, Sen S, Kircelli F, Yilmaz M, Sarsik B, Ozkahya M, et al. Plasmapheresis therapy in renal transplant patients: five-year experience. Transplant Proc. 2011;43(3):853-7. [ Links ]
12. Brown CM, Abraham K a, O'Kelly P, Conlon PJ, Walshe JJ. Long-term experience of plasmapheresis in antibody-mediated rejection in renal transplantation. Transplant Proc. 2009;41(9):3690-2. [ Links ]
13. Pascual M, Saidman S, Tolkoff-Rubin N, Williams WW, Mauiyyedi S, Duan JM, et al. Plasma exchange and tacrolimus-mycophenolate rescue for acute humoral rejection in kidney. Transplantation. 1998;66(11):1460-4. [ Links ]
14. Ibernón M, Gil-Vernet S, Carrera M, Serón D, Moreso F, Bestard O, et al. Therapy with plasmapheresis and intravenous immunoglobulin for acute humoral rejection in kidney transplantation. Transplant Proc. 2005;37(9):3743-5. [ Links ]
15. Fehr T, Gaspert A. Antibody-mediated kidney allograft rejection: therapeutic options and their experimental rationale. Transpl Int. 2012;25(6):623-32. [ Links ]
16. Kidney Disease: Improving Global Outcomes (KDIGO) transplant work group. KDIGO clinical practice guideline for the care of kidney transplant recipients. Am J Transplant. 2009;9 Suppl 3:1-155. [ Links ]
17. Seck SM, Bertrand D, Boucar D. Current indication of plasma exchanges in nephrology: a systematic review. Saudi J Kidney Dis Transpl. 2011;22(2):219-24. [ Links ]
18. Lefaucheur C, Nochy D, Andrade J, Verine J, Gautreau C, Charron D, et al. Comparison of combination Plasmapheresis/IVIg/ anti-CD20 versus high-dose IVIg in the treatment of antibody-mediated rejection. Am J Transplant. 2009;9(5):1099-107. [ Links ]
19. Böhmig GA, Wahrmann M, Regele H, Exner M, Robl B, Derfler K, et al. Immunoadsorption in severe C4d-positive acute kidney allograft rejection: a randomized controlled trial. Am J Transplant. 2007;7(1):117-21. [ Links ]
20. Sanchez AP, Ward DM. Therapeutic apheresis for renal disorders. Semin Dial. 2012;25(2):119-31. [ Links ]
21. Mengel M, Sis B, Haas M, Colvin RB, Halloran PF, Racusen LC, et al. Banff 2011 Meeting report: new concepts in antibody-mediated rejection. Am J Transplant. 2012;12(3):563-70. [ Links ]
22. Solez K, Colvin R, Racusen L, Haas M, Sis B, Mengel M, et al. Banff 07 classification of renal allograft pathology: updates and future directions. Am J Transplant. 2008;8(4):753-60. [ Links ]
23. El-Zoghby ZM, Stegall MD, Lager DJ, Kremers WK, Amer H, Gloor JM, et al. Identifying specific causes of kidney allograft loss. Am J Transplant. 2009;9(3):52-35. [ Links ]
24. Venetz J-P, Pascual M. New treatments for acute humoral rejection of kidney allografts. Expert Opin Investig Drugs. 2007;16(5):625-33. [ Links ]
25. Bartel G, Schwaiger E, Böhmig G. Prevention and treatment of alloantibody-mediated kidney transplant rejection. Transpl Int. 2011;24(12):1142-55. [ Links ]
26. Pape L, Becker JU, Immenschuh S, Ahlenstiel T. Acute and chronic antibody-mediated rejection in pediatric kidney transplantation. Pediatr Nephrol. 2015;417-24. [ Links ]
27. Orandi BJ, Zachary AA, Dagher NN, Bagnasco SM, Garonzik- Wang, Van Arendonk K J, et al. Eculizumab and Splenectomy as Salvage Therapy for Severe Antibody-Mediated Rejection After HLA Incompatible Kidney Transplantation. Transplantation. 2014;98(8):857-63. [ Links ]
28. Sin Y-H, Kim Y-J, Oh JS, Lee JH, Kim SM, Kim JK. Treatment of acute antibody-mediated rejection using bortezomib: a case report. Nephrology. 2015;20 Suppl 2:86-9. [ Links ]
29. Everly M, Everly J, Susskind B, Brailey P, Arend L, Alloway R, et al. Bortezomib provides effective therapy for antibody- and cell-mediated acute rejection. Transplantation. 2008;86(12):1754-61. [ Links ]
30. Takeda A, Otsuka Y, Horike K, Inaguma D, Hiramitsu T, Yamamoto T, et al. Significance of C4d deposition in antibody-mediated rejection. Clin Transplant. 2012;26 Suppl 24:43-8. [ Links ]
31. Haas M, Sis B, Racusen LC, Solez K, Glotz D, Colvin RB, et al. Banff 2013 meeting report: Inclusion of C4d-negative antibody-mediated rejection and antibody-associated arterial lesions. Am J Transplant. 2014;14(2):272-83. [ Links ]