Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Iatreia
Print version ISSN 0121-0793
Iatreia vol.15 no.3 Medellín July/Sept. 2002
ARTÍCULO DE REVISIÓN
¿Cómo se transporta la glucosa a través de la membrana celular?
HOW IS GLUCOSE TRANSPORTED THROUGH CELL MEMBRANE?
DIANA P. DÍAZ HERNÁNDEZ*; LUIS CARLOS BURGOS HERRERA**
* MD, MSc Fisiología del ejercicio
** MD, MSc Bioquímica. Profesores del Departamento de Fisiología y Bioquímica, Facultad de Medicina, Universidad de Antioquia
LA GLUCOSA ES EL PRINCIPAL SUSTRATO ENERGÉTICO de la célula y para su ingreso requiere una proteína transportadora en la membrana celular. Se han descrito dos sistemas de transporte de glucosa y de otros monosacáridos: los transportadores de sodio y glucosa llamados SGLT (sodium-glucose transporters) y los transportadores de glucosa llamados GLUT (glucose transporters). En este artículo se presenta una revisión de las principales características moleculares, bioquímicas y funcionales de los transportadores de monosacáridos que se han descrito hasta el momento.
PALABRAS CLAVE
GLUCOSA, MONOSACÁRIDOS, SGLT, GLUT, DIFUSIÓN FACILITADA, TRANSPORTADORES DE MEMBRANA
SUMMARY
GLUCOSE IS THE MAIN ENERGY SUPPLY for the cell and requires a transport protein to enter through cell membranes. Two monosacharid transport systems have been described: SGLT (sodium-glucose transporters) and GLUT (glucose transporters). In this article we review the main molecular, biochemical and functional characteristics of these monosacharid transporters.
INTRODUCCIÓN
PARA LA PRODUCCIÓN DEL ADENOSINTRIFOSFATO (ATP), compuesto indispensable en muchas de las reacciones que se llevan a cabo en la célula, se necesitan varios sustratos energéticos, entre los cuales la glucosa es el de mayor importancia. Debido a que ésta no difunde a través de la bicapa lipídica, debe ser transportada al interior de la célula. Este transporte lo realizan dos grupos de proteínas: los transportadores SGLT (sodiumglucose transporters) y los transportadores GLUT (glucose transporters).
TRANSPORTADORES SGLT
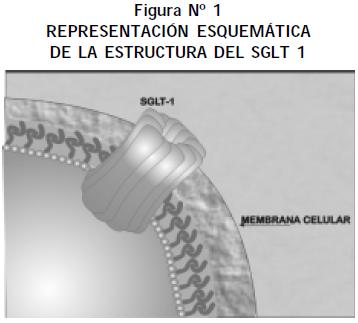
COMO SU NOMBRE LO SUGIERE, son proteínas que efectúan un transporte acoplado, en el que ingresan conjuntamente a la célula sodio y glucosa —o galactosa, en algunos casos—. Se localizan en la membrana luminal de las células epiteliales encargadas de la absorción (intestino delgado) y la reabsorción (túbulo contorneado proximal) de nutrientes. Se aprovecha el ingreso de sodio a favor del gradiente electroquímico, entre el exterior y el interior de la célula, para transportar la glucosa en contra de un gradiente químico. Se han identificado tres transportadores SGLT (SGLT 1, SGLT 2 y SGLT 3) (Tabla 1); que se diferencian en varios aspectos como: 1) la afinidad por la glucosa y el sodio; 2) el grado de inhibición frente a la florizina; 3) la capacidad para transportar glucosa o galactosa, y 4) la ubicación tisular. Todos los SGLT tienen una estructura secundaria similar, con catorce dominios transmembranales en orientación α hélice (Figura 1).
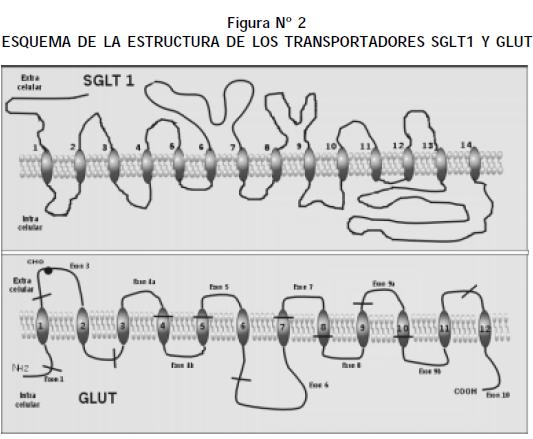
El SGLT 1 es una proteína de 664 aminoácidos codificada por un gen localizado en el cromosoma 22; tiene una alta afinidad por la glucosa, con una constante de Michaelis (Km) de 0,3 mM —la Km corresponde a la concentración de sustrato que semisatura el sistema de transporte—. Transporta dos moléculas de sodio por una de glucosa o galactosa, con una Km, para el sodio, de 32 mM. Se expresa en el intestino delgado y en el segmento S3 de la nefrona proximal; en este último, por sus características cinéticas, se encarga de la reabsorción de la glucosa filtrada que no se reabsorbió en los segmentos S1 y S2. Su conformación proteica presenta catorce dominios transmembranales en orientación α hélice, con los dominios amino (N) y carboxilo (C) terminales localizados en la región extracelular de la membrana (1); presentan un sitio de glicosilación entre los dominios transmembranales seis y siete (Figura 2). Al parecer el transporte del sodio y de la glucosa se realiza a través de dos vías diferentes; el sodio ingresa por una región de la proteína cercana al extremo N-terminal y el monosacárido a través de la región C-terminal. La unión del sodio al SGLT genera un cambio de conformación que permite la unión y el transporte de la glucosa al interior de la célula; de esta manera ingresan dos moléculas de sodio, una de glucosa y 260 moléculas de agua (2,3).
El SGLT 2 es una proteína de 672 aminoácidos con un 59% de homología con el SGLT 1, codificada por un gen localizado en el cromosoma 16. Presenta una Km para la glucosa de 1,6 mM. Transporta una molécula de sodio por una de glucosa; su Km para el sodio es de 200 a 300 mM. Se expresa en el riñón, en los segmentos S1 y S2, pero no en el intestino. Es el encargado de reabsorber el 90% de la glucosa filtrada por el riñón (4).
El SGLT 3 es una proteína de 674 aminoácidos con un 70% de homología con el SGLT 1, codificada por un gen localizado en el cromosoma 22. Presenta una Km para la glucosa de 6 mM. Transporta dos moléculas de sodio por una de glucosa. No hay estudios funcionales del SGLT 3 en humanos, sólo en cerdos (2).
TRANSPORTADORES GLUT
LOS TRANSPORTADORES GLUT están encargados del ingreso de los monosacáridos a todas las células del organismo. Se han identificado trece de ellos, enumerados desde GLUT 1 hasta GLUT 13 (5,6) (Tabla 1).
Los GLUT presentan una conformación proteica similar; son glicoproteínas de 45 a 55 kDa (7), con doce dominios transmembranales en estructura α hélice. Los extremos N y C terminales, al igual que una gran asa central, se localizan en el citoplasma. Además, presentan un sitio de glicosilación en la región externa de la membrana (Figura 2). Cada una de las diferentes isoformas de los GLUT tiene ubicación y características cinéticas propias, adaptadas a las necesidades metabólicas de los distintos tejidos del organismo. Al parecer los segmentos transmembranales 3, 5, 7 y 11 son hidrofílicos en una cara del cilindro α hélice e hidrofóbicos en la otra, por lo que forman un poro y, de esta manera, permiten el paso del monosacárido a favor de un gradiente de concentración (8) (Figura 2). Para que se efectúe el ingreso de la glucosa, se deben formar previamente uniones débiles (tipo puentes de hidrógeno) entre los grupos hidroxilo y carbamino del GLUT y los grupos hidroxilo de la glucosa (9).
La glucosa ingresa a la célula en cuatro etapas: 1) se une al transportador en la cara externa de la membrana; 2) el transportador cambia de conformación y la glucosa y su sitio de unión quedan localizados en la cara interna de la membrana; 3) el transportador libera la glucosa al citoplasma, y 4) el transportador libre cambia nuevamente de conformación, expone el sitio de unión a la glucosa en la cara externa y retorna a su estado inicial (10) (Figura 3).
El GLUT 1 es una proteína de 664 aminoácidos, codificada por un gen que se localiza en el cromosoma 22. Tiene una Km para la glucosa de 1,6 mM y transporta, además, galactosa. Se expresa en los eritrocitos, los astrocitos, las células endoteliales, las células de la retina y las barreras hematoencefálica y placentaria. Durante el desarrollo fetal hay expresión de GLUT 1 en los estadios de oocito y blastocisto y luego en los diferentes tejidos fetales. La expresión en el músculo esquelético depende, al parecer, del estado de desarrollo; su mayor expresión se encuentra durante la gestación y disminuye luego del nacimiento. Se expresa en muy poca cantidad en el músculo del adulto (11). En el riñón se ha encontrado en prácticamente todos los segmentos de la nefrona. En la membrana basolateral de las células ubicadas en la porción contorneada y recta de la nefrona proximal, se asocia con el proceso de reabsorción de la glucosa; en el resto de la nefrona se asocia con el aporte nutritivo a la célula (4).
El GLUT 2 es una proteína de 522 aminoácidos, codificada por un gen ubicado en el cromosoma 3. A diferencia de los otros GLUT su afinidad por la glucosa es baja (Km:17 mM). Transporta además galactosa y fructosa. Se expresa en células B pancreáticas, en hepatocitos, en enterocitos y en células tubulares renales. En células B pancreáticas y en hepatocitos facilita el ingreso de la glucosa como respuesta al incremento de la glicemia (8). Debido a su elevado valor de Km, funciona en condiciones cinéticas de primer orden; esto quiere decir que es muy sensible a los cambios de glicemia e incrementa su actividad cuando se aumenta la glucosa en la sangre. Las características mencionadas permiten que la entrada de glucosa sea el primer paso en el estímulo para la secreción de insulina en las células B del páncreas y en el proceso de glucogenogénesis en el hígado. En el enterocito se localiza tanto en la membrana luminal como en la basolateral; en la membrana luminal es el responsable de la absorción intestinal de glucosa por difusión facilitada (12); en la membrana basolateral permite el paso de glucosa al espacio extracelular. En el riñón se localiza en la membrana basolateral del túbulo proximal, donde también permite el paso de glucosa al espacio extracelular.
El GLUT 3 es una proteína de 596 aminoácidos, codificada por un gen localizado en el cromosoma 12, con una Km para la glucosa de 2 mM; transporta además galactosa. Su mayor expresión, en los humanos, se da en neuronas del sistema nervioso central; también está presente en la placenta, el hígado, el riñón y el corazón (8,13). En el tejido muscular humano su expresión comienza a las 18 semanas de gestación y desaparece luego del nacimiento (11). En el tejido cerebral funciona en secuencia con el GLUT 1 (ubicado en la barrera hematoencefálica), lo que permite un transporte de glucosa en forma vectorial desde la sangre hasta la neurona (8).
El GLUT 4 es una proteína de 509 aminoácidos, codificada por un gen ubicado en el cromosoma 17. Tiene una Km para la glucosa de 5 mM. Se expresa en los tejidos donde el transporte de glucosa es dependiente de insulina: el músculo (cardíaco y esquelético) y el tejido adiposo.
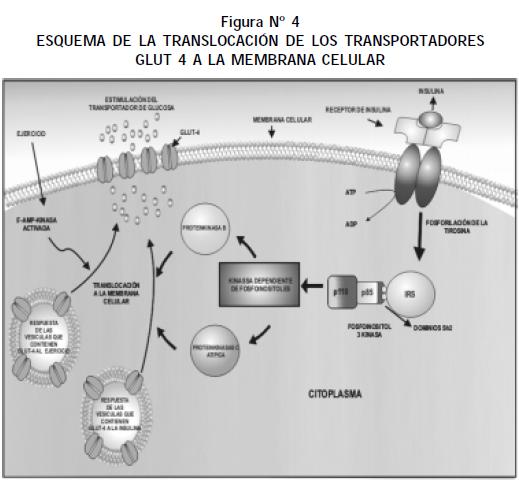
En ausencia de un estímulo apropiado, la mayor parte del GLUT 4 (aproximadamente el 90%) permanece almacenado en vesículas intracelulares, localizadas en el citoplasma. Estas vesículas, en donde reside el transportador, constituyen un compartimiento altamente especializado, cuyo tráfico y contenido sólo se conocen parcialmente; se sabe que en las vesículas, junto al GLUT 4, se localizan otras proteínas, que translocan juntamente con el transportador a la membrana citoplasmática, con la que finalmente se funden (14); uno de los mayores componentes de las vesículas es una aminopeptidasa de función desconocida, también se ha descrito la sinaptobrevina (proteína asociada a vesículas) y una proteína ligadora de GTP (rav 4). Las vesículas están sometidas a un ciclo continuo de exocitosis-endocitosis. La presencia de insulina, la contracción muscular, la estimulación eléctrica y la hipoxia son estímulos que activan la exocitosis (Figura 4) (15).
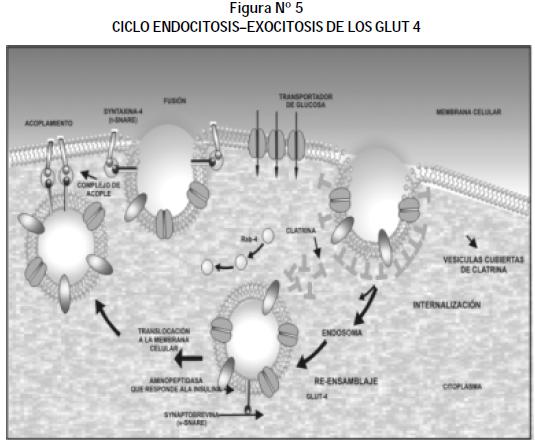
El mecanismo molecular que media entre el estímulo y la movilización de la vesícula a la membrana celular se conoce parcialmente y es objeto de múltiples investigaciones. El efecto de la insulina es el que se ha estudiado con mayor profundidad; el receptor de la insulina actúa como una quinasa que fosforila residuos de tirosina, del propio receptor y de otras proteínas. En ausencia de la insulina la actividad tirosina-quinasa permanece desconectada. Cuando la insulina se une al receptor se induce un cambio conformacional en éste, que estimula la actividad tirosina-quinasa. El receptor activado se autofosforila y, a su vez, fosforila varias proteínas en secuencia, las cuales inducen todos los efectos celulares de la insulina. Las principales proteínas fosforiladas por el receptor son las IRS (Insuline receptor substrate), de las cuales se han descrito cuatro, con diferente distribución tisular. Estas IRS, a su vez, activan otras proteínas entre las cuales se incluyen una que es homóloga del colágeno (SHC) y el Gab 1 (proteína asociada al receptor del factor de crecimiento Grb2) (16), que desencadenan una cascada de eventos moleculares, incluyendo, entre otros, la translocación de las vesículas. Esta exocitosis de las vesículas incrementa momentáneamente el número de GLUT 4 en la membrana del miocito o del adipocito (16,17) y por consiguiente la entrada de glucosa a estas células. Cuando el estímulo cesa se desencadena la endocitosis, la cual involucra la formación de trisqueliones de clatrina y la participación del citoesqueleto celular (Figura 5).
Múltiples investigaciones han demostrado que, independientemente del efecto de la insulina, el ejercicio también incrementa el número de GLUT 4 en la membrana plasmática y en los túbulos transversos (18,19). Los valores basales de GLUT 4, en la membrana celular, se recuperan luego de dos horas de reposo. Algunos autores postulan que también hay translocación de los GLUT 4 luego del ejercicio, al parecer dependiente de la insulina, y este efecto persiste por varias horas (20).
Se ha observado un incremento de la expresión de RNAm para el GLUT 4 luego de la realización de diferentes protocolos de entrenamiento de ejercicio de resistencia (21,22). El estímulo que aumenta la transcripción del gen del GLUT 4, durante el ejercicio, no está claro aún. Al parecer es necesaria la contracción muscular para la expresión de este gen (18), por lo que algunos investigadores sugieren que las moléculas que cambian de concentración durante la contracción muscular, como el calcio, el ATP, el ADP y la fosfocreatina, pueden estar involucradas en este evento (22). Otros postulan que la bradicinina, liberada localmente durante la contracción muscular, puede ser uno de los factores responsables de la translocación de las vesículas con GLUT 4 (23). Algunos autores han implicado, además, a la proteinquinasa activada por 5'AMP y a las especies reactivas del oxígeno y del nitrógeno, como estímulos para la translocación de GLUT 4 (24-26).
El GLUT 5 es una proteína de 501 aminoácidos, codificada por un gen localizado en el cromosoma 1; prácticamente es un transportador de fructosa, ya que su afinidad por otros monosacáridos, incluyendo la glucosa, es mínima. Se localiza en el yeyuno —membrana luminal— (12), los espermatozoides, las células tubulares renales y las células de la microglia (8).
El GLUT 6 era el nombre que se le daba previamente a un supuesto producto que se encontró por análisis de secuencias; posteriormente se demostró que correspondía a un pseudogén. El que antes se llamaba GLUT 9 se llama actualmente GLUT 6; es una proteína de 507 aminoácidos que se expresa en cerebro, bazo y leucocitos (7)
El GLUT 7 originalmente fue descrito como un transportador del retículo endoplásmico de tejidos gluconeogénicos (27), pero posteriormente se demostró que éste era un artefacto de laboratorio y por lo tanto no existía (28)
El GLUT 8 es una proteína de 477 aminoácidos que posee un 30% de homología con el GLUT 1 y se expresa en testículos y placenta (29).
El actual GLUT 9 es una proteína de 540 aminoácidos cuyo gen está ubicado en el cromosoma 4, tiene una homología del 44% con el GLUT 5 y del 38% con el GLUT 1. Se expresa principalmente en riñón e hígado y en menor concentración en bazo, leucocitos, cerebro y corazón (30).
EL GLUT 10 tiene 541 aminoácidos, es codificado por un gen ubicado en el cromosoma 20, con un 35% de homología con los GLUT 3 y 8. El gen del GLUT 10 se ha relacionado con susceptibilidad para presentar diabetes mellitus no insulino dependiente. El GLUT 10 se expresa principalmente en hígado y páncreas (31).
El GLUT 11 es una proteína de 496 aminoácidos, codificada por un gen ubicado en el cromosoma 22; tiene una homología de 41% con el transportador de fructosa GLUT 5. Se expresa en corazón y músculo esquelético (32).
El GLUT 12 es una proteína de 617 aminoácidos. Se expresa en músculo esquelético, tejido adiposo e intestino delgado. Se considera un segundo sistema de transporte de glucosa dependiente de insulina. Se ha demostrado que el transportador tiene una localización perinuclear en ausencia de insulina (5).
El GLUT descrito más recientemente es el GLUT 13 que es el mismo transportador de mioinositol; tiene 629 aminoácidos; presenta una homología de secuencia de 36% con el GLUT 8. Se expresa principalmente en el cerebro (6).
BIBLIOGRAFÍA
1. TURK E, Wright EM. Membrane topology motifs in the SGLT cotransporter family. J Membr Biol 1997; 159: 1- 20. [ Links ]
2. WRIGHT EM. Renal Na+- glucose cotransporter. Am J Physiol 2001; 280: F10-F18 [ Links ]
3. LOO DDF, ZEUTHEN T, CHANDY G, WRIGHT EM. Cotransport of water by the Na+/glucose cotransporter. Proc Natl Acad Sci 1996; 93: 13.367- 13.370. [ Links ]
4. MOE OW, BERRY CA, RECTOR FC. Renal transport of glucose, amino acids, sodium, chloride, and water. In: Brener; BM, ed. The Kidney, 6ª ed. Philadelphia: Saunders. [ Links ]
5. ROGERS S, MACHEDA ML, DOCHERTY SE, CARTY MD, Henderson MA, Soeller WC, et al. Identification of a novel glucose transporter-like protein-GLUT-12. Am J Physiol 2002; 282: E733-738. [ Links ]
6. ULDRY N, IBBERSON M, HORISBERGER JD, CHATTON, JY, RIEDERER BM, THORENS B. Identification of a mammalian H+- myo-inositol symporter expressed predominantly in the brain. EMBO J 2001; 20: 4.467-4.477. [ Links ]
7. DOEGE H, BOCIANSKI A, JOOSTI HG, SCHÜRMANN A. Activity and genomic organization of human glucose transporter 9 (GLUT 9), a novel member of the family of sugar-transport facilitators predominantly expressed in brain and leucocytes. Biochem J 2000; 250: 771-776. [ Links ]
8. GUERRE-MILLO M. Les transporteurs d'hexoses. Medicine/Sciences 1995; 11: 1.111-1.119. [ Links ]
9. LIENHARD GE, SLOT JW, JAMES DE, MUECKLER M. How cells absorb glucose. Sci Am 1992; 266: 86-91. [ Links ]
10. CARRUTHERS A. Facilitated diffusion of glucose. Physiol Rev 1990; 70: 1.135-1.176. [ Links ]
11. GASTER M, HANDBERG A, BECK-NIELSEN H, SCHRODER HD. Glucose transporter expression in human muscle fibers. J Appl Physiol 2000; 279: E529-E538. [ Links ]
12. KELLETT GL, HELLIWELL PA. The diffusive component of intestinal glucose absorption is mediated by the glucose-induced recruitment of GLUT 2 to the brush-border membrane. Biochem J 2000; 350:155-162. [ Links ]
13. SHIN BC, FUJIKURA K, SUZUKI T, TANAKA S. Glucose transporter GLUT3 in the rat placental barrier: a possible machinery for the transplacental transfer of glucose. Endocrinology 1997; 138: 3.997-4.004. [ Links ]
14. MASTICK CC, AEBERSOLD R, LIENHARD GE. Characterization of a major protein in GLUT 4 vesicles. J Biol Chem 1994; 269: 6.089-6.092. [ Links ]
15. ZHONG ZHANG J, BEHROOZ A, ISMAIL-BEIGI F. Regulation of glucose transport by hypoxia. Am J Kidney Dis 1999; 34: 189-202. [ Links ]
16. SHEPHERD PR, KAHN BB. Glucose transporters and insulin action. N Engl J Med 1998; 341: 248-257. [ Links ]
17. TANTI JF, GRÉMEAUX T, GRILLO S, CALLEJA V, KLIPPEL A, WILLIAMS L, et al. Overexpression of a constitutively active form of phosphatidylinositol 3- kinase is sufficient to promote Glut 4 translocation in adipocytes. J Biol Chem 1996; 271: 25.227- 25.232. [ Links ]
18. LUND S, HOLMAN GD, SCHMITZ O, PEDERSEN O. Contraction stimulates translocation of glucose transporters GLUT 4 in skeletal muscle through a mechanism distinct from that of insulin. Proc Natl Acad Sci 1995; 92: 5.817-5.821. [ Links ]
19. GOODYEAR LJ, CHANG PY, SHERWOOD DJ, DUFRESNE SD, MOLLER DE. Effects of exercise and insulin on mitogen-activated protein kinase signalling pathways in rat skeletal muscle. Am J Physiol 1996; 271: E403-E408. [ Links ]
20. BORGHOUTS LB, KEIZER HA. Exercise and insuline sensitivity: a review. Int J Sport Med 2000; 21:1-12 [ Links ]
21. GULVE EA, SPINA RJ. Effect of 7-10 days of cycle ergometer exercise on skeletal muscle GLUT 4 protein content. J Appl Physiol 1995; 79: 1.562-1.566. [ Links ]
22. MACLEAN PS, ZHENG D, DOHM GL. Muscle glucose transporter (GLUT 4) gene expression during exercise. Exerc Sport Sci Rev 2000; 28: 148-152. [ Links ]
23. KISHI K, MUROMOTO N, NAKAYA Y, HAGI A, HAYASHI H, EBINA Y. Bradykinin directly triggers GLUT 4 translocation via an insulin – independent pathway. Diabetes 1998; 47: 550-558. [ Links ]
24. HAYASHI T, HIRSHMAN MF, KURTH EJ, WINDER WW, GOODYEAR LJ. Evidence for 5'AMP- activated protein kinase mediation of the effect of muscle contraction on glucose transport. Diabetes 1998; 47: 1.369-1.373. [ Links ]
25. HOLMES BF, KURTH-KRACZEK EJ, WINDER WW. Chronic activation of 5'AMP- activated protein kinase increases GLUT 4, hexokinase, and glycogen in muscle. J Appl Physiol 1999; 87: 1990-1995. [ Links ]
26. BALON TW, YERNENI KKV. Redox regulation of skeletal muscle glucose transport. Med Sci Sports Exerc 2001; 33: 382-385. [ Links ]
27. WADDELL ID, ZOMERSCHOE AG, VOICE M W, BURCHELL A. Cloning and expression of a hepatic microsomal glucose transport protein. Comparison with liver plasma-membrane glucose-transport protein GLUT 2. Biochem J 1992; 286: 173-177. [ Links ]
28. BURCHELL A. A re-evaluation of GLUT 7. Biochem J 1998; 331: 973. [ Links ]
29. IBBERSON M, ULDRY M, THORENS B. GLUTX1, a novel mammalian glucose transporter expressed in the central nervous system and insulin-sensitive tissues. J Biol Chem 2000; 275: 4.607-4.612. [ Links ]
30. PHAY JE, HUSSAIN HB, MOLEY JF. Cloning and expression analysis of a novel member of the facilitative glucose transporter family, SLC2A9 (GLUT9). Genomics 2000; 66: 217-220. [ Links ]
31. MCVIE-WYLIE AJ, LAMSON DR, CHEN YT. Molecular cloning of a novel member of the GLUT family of transporters, SLC2a10 (GLUT10), localized on chromosome 20q13.1: a candidate gene for NIDDM susceptibility. Genomics 2001; 72: 113-117. [ Links ]
32. DOEGE H, BOCIANSKI A, SCHEEPERS A, AXER H, ECKEL J, JOOST HG, et al. Characterization of human glucose transporter (GLUT) 11 (encoded by SLC2A11), a novel sugar-transport facilitator specifically expressed in heart and skeletal muscle. Biochem J 2001; 359: 443-449. [ Links ]