Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Iatreia
Print version ISSN 0121-0793
Iatreia vol.19 no.4 Medellín Oct./Dec. 2006
ACTUALIZACIÓN CRÍTICA
Ronda clínica y epidemiológica
OSCAR OSÍO URIBE1, JOHN JAIRO ZULETA TOBÓN2
- Especialista en Medicina Interna, MgSc en Epidemiología Clínica. Director de la Corporación Académica de Patologías Tropicales, Universidad de Antioquia. Dirección electrónica: cpt_udea@yahoo.com
- Profesor de Ginecología y Obstetricia, MgSc en Epidemiología Clínica. Universidad de Antioquia, Medellín, Colombia. Dirección electrónica: jjzuleta@epm.net.co
JERARQUÍA DE LA INFORMACIÓN CIENTÍFICA Y LAS RECOMENDACIONES PARA LA PRÁCTICA CLÍNICA
Las guías de práctica clínica han mejorado en calidad durante los últimos 10 años gracias al cumplimiento de algunos principios básicos, como por ejemplo, la revisión sistemática que se hace de la información importante, la valoración de la calidad de los estudios en los cuales están basadas las recomendaciones y el establecimiento de una jerarquía en las recomendaciones clínicas que se emiten.
El GRADE (Grading of Recommendations Assessment, Development and Evaluation) es un grupo de trabajo internacional recientemente constituido y que cuenta con la participación de la Agencia Norteamericana para la Investigación en Salud y Calidad, el Instituto Inglés para la Excelencia Clínica (NICE) y la Organización Mundial de la Salud (OMS); el grupo tiene como misión ayudar a resolver la confusión existente entre los diferentes sistemas para jerarquizar la evidencia investigativa y las recomendaciones clínicas que de ella nazcan. Se anticipa que el desarrollo de un sistema nuevo y uniforme de calificación de la jerarquía de las investigaciones clínicas y de las recomendaciones que de ellas se desprenden no será fácil, y se piensa que tendrá muchas limitaciones, ya que la mayoría de las sociedades científicas han invertido mucho tiempo y dinero en el desarrollo de sus propios sistemas de calificación y serán renuentes a la adopción del nuevo sistema. La calificación propuesta por el grupo GRADE fue publicada hace dos años en la revista BMJ,1 en un artículo que aseguraba que el sistema calificador era simple de usar y era aplicable a una gama amplia de recomendaciones que eran válidas para diferentes especialistas de la práctica clínica. La clasificación del grupo GRADE estableció que existen cuatro calidades posibles en la evidencia suministrada por las investigaciones clínicas sobre una intervención, además de valorar las recomendaciones en fuertes y débiles. La calidad de la evidencia se gradúa así:
Calidad alta: cuando se considera que es poco probable que futuras investigaciones cambien la confianza que tenemos en la estimación del efecto de una terapia.
Calidad moderada: cuando es probable que futuras investigaciones tengan un impacto importante en la confianza que tenemos en la estimación de un efecto y lo cambien.
Calidad baja: cuando es muy probable que futuras investigaciones tengan un impacto importante en la estimación del efecto que tiene una intervención.
Calidad muy baja: cuando existe una estimación incierta de los efectos de una intervención.
El grupo GRADE también estableció unos criterios para asignar los grados de evidencia según el tipo de ensayo clínico en los cuales se basa la estimación del efecto de una intervención y una serie de factores que inciden en la confianza de la estimación de los beneficios, riesgos, carga de enfermedad y costos que entrañan los tratamientos. Los niveles propuestos son: alto (ensayos con conformación aleatoria de los grupos), bajo (estudios de observación) y muy bajo (estudios de cualquier otro tipo).
Los factores que determinan un descenso en el nivel de la evidencia en la revisión sistemática que precede a unas recomendaciones son aquellos en los cuales se detectan fallas en la calidad de los estudios (afectando su metodología y ejecución), cuando existen inconsistencias importantes (por diferencias entre los estudios en cuanto a la estimación del efecto), cuando están basadas en evidencias indirectas, cuando las estimaciones de la asociación muestran intervalos de confianza amplios y cuando los estudios tienen una alta probabilidad de la ocurrencia de sesgos. Los estudios se consideran indirectos si la comparación entre las alternativas terapéuticas no es directa y se basa en la medición de los efectos entre un producto y un placebo y no directamente entre los productos que se están comparando (por ejemplo, para decidir entre irbesartan y losartan en una guía se usan estudios que compararon cada uno de los productos con placebo y no directamente entre sí), o cuando los grupos comparados son diferentes(por ejemplo se quiere valorar el beneficio de la anticoagulación en la fibrilación auricular asociada con valvulopatías y los estudios disponibles solo muestran los efectos de la warfarina en arritmias auriculares de origen no valvular) o cuando existen diferencias en la evaluación de los resultados(por ejemplo, se desea valorar el efecto de un medicamento en el largo plazo y solo se disponen de evaluaciones a las cuatro semanas). Por el contrario, aumenta el nivel de la calificación de la revisión sistemática que da origen a las recomendaciones, si la asociación es fuerte (con un RR mayor de 2 o menor de 0,5) y se origina en evidencias de asociación similares obtenidas a partir de dos o mas estudios de observación, sin variables plausibles de confusión, o cuando existe una muy fuerte asociación (RR mayor de 5 o menor de 0,2), o si hay un gradiente de dosis–respuesta y cuando todos los posibles factores de confusión que hubiesen podido reducir el efecto se han tenido en cuenta. El grupo GRADE continúa debatiendo temas no resueltos en la evaluación de las evidencias, como por ejemplo, cuando se considera un tamaño de la muestra lo suficientemente pequeño para disminuir la fortaleza de la evidencia o cuando los intervalos de confianza se consideran amplios e imprecisos.
En cuanto a las recomendaciones, el grupo GRADE establece que ellas deben nacer de una comparación lo más explícita posible de los beneficios y los daños que puede producir la intervención, sugiriendo que primero se haga su balance clínico antes de considerar sus factores económicos y de costos. Las recomendaciones deben ser lo más específicas posibles, si hay subgrupos o escenarios particulares de intervención. Las recomendaciones que se dan para una intervención podrán catalogarse como fuertes o como débiles. Cuando los beneficios de una intervención claramente excedan de sus riesgos o claramente no los superen, se pueden emitir recomendaciones de peso; si la comparación de los beneficios y los riesgos terapéuticos es compleja o es incierta, bien sea porque la información científica es de pobre calidad o porque las investigaciones hayan demostrado de manera fehaciente que los beneficios y los daños están equilibrados, se impone la prudencia en las recomendaciones que se emiten y los pacientes tendrán la opción de dar su consentimiento informado antes de hacer el tratamiento. La Colaboración Cochrane posiblemente adoptará en un futuro el sistema GRADE y sociedades científicas norteamericanas como las de los endocrinólogos ya lo han adoptado, lo que hace pensar que en un futuro cercano todas las guías terapéuticas tendrán un sistema de calificación uniforme y adoptado por consenso.2
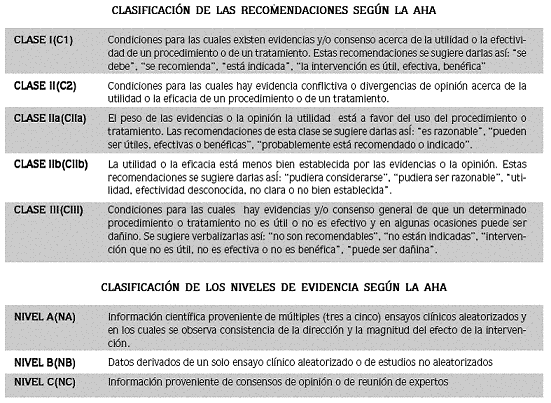
A modo de ejemplo de la calificación de la jerarquía de una información científica y de la postulación de unas recomendaciones graduadas, aunque no sigue el sistema GRADE, se muestra un resumen de la Guía Para La Prevención Primaria del Accidente Cerebro–vascular Isquémico. 3 Los escritores de esta guía hicieron una revisión sistemática de la literatura que cubrió el período de 2001 a Enero de 2005, además de consultar las guías previamente publicadas, sus archivos personales y buscar la opinión de expertos, todo con el fin de resumir las evidencias posibles, identificar vacíos en el conocimiento actual y emitir, cuando fuera posible hacerlo, recomendaciones basadas en los estándares de los criterios de la Asociación Americana del Corazón.
Prevención primaria de la enfermedad cerebro–vascular isquémica (ECEREBI)
Todo adulto debería tener por parte de su médico una evaluación del riesgo de presentar un accidente cerebro–vascular isquémico (C I, NA). Recomendaciones para hacer intervenciones específicas de los principales factores de riesgo de la ECEREBI:
Causas genéticas: remitir el paciente a consejería genética cuando se sospechan causas raras de ECEREBI, tales como la enfermedad de Cadasil, Marfan o Fabry (C IIb, NC).
Hipertensión arterial (HTA): la HTA no tratada condiciona un riesgo relativo (RR) de 4 para ECEREBI en mayores de 50 años, y el tratamiento antihipertensivo puede reducir el riesgo hasta en 38%. Se recomiendan (CI, NA) las tomas regulares de presión arterial y su búsqueda por lo menos cada dos años en los adultos y con mayor frecuencia en grupos minoritarios y en ancianos, con un tratamiento de la HTA como lo establece la guía del séptimo comité.
Tabaquismo: eleva el RR en 80%. Dejar de fumardisminuye el riesgo 50% al año, con regreso alos niveles basales de riesgo a los 5 años.
Las campañas para no comenzar a fumar y la suspensión del hábito son recomendadas
(CI,NB). También se recomienda evitar ambientes contaminados con humo de cigarrillo
(C IIa, NC). La consejería, productos substitutos de la nicotina y los medicamentos para dejar de fumar han mostrado efectividad y deben ser empleados (C IIa, NB).
Diabetes mellitus: proporciona un RR de 1.8 a 6. Se recomienda que la HTA se controle estrictamente en los pacientes con DM tipo 1 y 2 (garantizando cifras menores de 130/80 mm Hg.), como parte de un programa integral de reducción de riesgos (CI,NA). Se recomienda el tratamiento de los diabéticos, especialmente los que tienen otros factores de riesgo con una estatina (C I,NA).
Fibrilación atrial (FA): se recomienda la anticoagulación en pacientes con FA que tienen una enfermedad valvular, especialmente con válvulas mecánicas (CI,NA). Cuando se tiene FA de origen no valvular en pacientes de 50 a 59 años, el RR se cuadruplica. La terapia antitrombótica con warfarina o con ASA para prevenir el ACV en pacientes con FA no valvular puede disminuir el riesgo 22 a 62%, pero la decisión del tratamiento se debe basar en la valoración de los diferentes riesgos, las preferencias del paciente y la disponibilidad de un laboratorio de alta calidad para el control de la anticoagulación (C I,NA). La warfarina se recomienda para los pacientes de alto riesgo (más de 4% de riesgo anual para ACV) y para la mayoría de los pacientes con riesgo moderado que tienen FA, aceptan el tratamiento y no tienen contraindicaciones importantes para la anticoagulación oral, buscando alcanzar un INR entre 2.0 y 3.0 (C I, NA).
Dislipidemias: los niveles altos de colesterol en los menores de 55 años duplican el RR de ECEREBI; el riesgo disminuye 27 a 32% cuando se bajan los niveles lipídicos en enfermos coronarios, hipertensos o diabéticos. Dosis altas de estatinas reducen el riesgo 25% más que las dosis bajas. Niveles reducidos de colesterol HDL en hombres duplican el riesgo. Cuando no se ha tenido ECEREBI y se tiene elevación del colesterol total, del colesterol no HDL y de los triglicéridos, se deben seguir las guías del ATP III. Se recomienda que pacientes con enfermedad coronaria y HTA de alto riesgo, aun con niveles normales de colesterol LDL, deben tratarse con cambios en su estilo de vida y una estatina (C I, NA). los tratamientos sugeridos para pacientes coronarios con Col. HDL bajo incluyen la pérdida de peso, el incremento de la actividad física, dejar de fumar y el uso de niacina o gemfibrozil (C IIa, N B).
Otras condiciones cardiacas: es razonable prescribir warfarina en pacientes con infarto del miocardio con elevación persistente del segmento ST y disfunción del ventrículo izquierdo (VI) y que tienen extensas anormalidades de la motilidad de la pared (CIIa, NA). La warfarina puede ser considerada en pacientes con disfunción severa del VI, con o sin falla cardiaca (C IIb, NC).
Estenosis carotídea asintomática: se deben buscar otras causas tratables de ACV e intervenirlas agresivamente (C I, NC). Es recomendable el ASA, salvo que exista contraindicación para su uso. (CI, NB). Se recomienda endarterectomía carotídea (profiláctica del ACV) en pacientes seleccionados que tengan un alto grado de estenosis, y cuando estén a cargo de cirujanos que muestren porcentajes de morbimortalidad menores del 3% (C1, NA). La selección de los pacientes debe basarse en una cuidadosa valoración de sus diferentes condiciones, riesgos y beneficios. La angioplastia carotidea y la colocación de stents pueden ser una alternativa razonable a la endarterectomia, en pacientes asintomáticos que tengan un alto riesgo para el procedimiento quirúrgico (C IIb, NB).
Enfermedad de células Falciformes (ECFALC): a los niños con ECFALC se les debe hacer ultrasonido transcraneano desde los dos años de edad (CI, NB), con transfusiones sanguíneas cuando se demuestre un alto riesgo de ACV (C I, NB). No están bien definidos los intervalos de los exámenes, de las transfusiones ni los criterios de uso de la resonancia nuclear ni de la angioresonancia. A los adultos con ECFALC hay que buscarles los otros factores de riesgo de ECEREBI conocidos e intervenirlos (C I, NA).
Terapia hormonal posmenopáusica (TRH): aumenta el riesgo de ECEREBI un 40% y por ello no se recomienda (C III, NA). No hay suficiente información todavía para recomendar el uso de los moduladores selectivos de los receptores de estrógeno.
Dieta y nutrición: el RR para ECEREBI asociado con dietas hipersódicas o bajas en potasio se desconoce. La reducción del consumo de sodio y el aumento del potasio se recomienda para disminuir la PA en las personas hipertensas (CI, NA), con lo cual se reduce el riesgo del ACV. El consumo de sodio debe ser menor de 2,3 g/día y el de potasio mayor de 4,7 g/día. También se recomienda la dieta DASH (C I, NA) que disminuye la presión arterial, y que invita al consumo de frutas, vegetales y productos bajos en grasas.
Inactividad física: proporciona un RR de 2.7. El incremento de la actividad física está recomendado (C I, NB). Es válido recomendar una actividad diaria de 30 minutos, de intensidad moderada, como parte de un estilo de vida saludable (C IIa, NB).
Obesidad y distribución central de grasa corporal: RR de 1.75 a 2.37. Estudios epidemiológicos indican que el incremento de la grasa corporal, y especialmente la abdominal, están directamente asociados con el riesgo de ACV. La reducción de peso está recomendada porque disminuye la presión sanguínea (C I, NA) y puede por lo tanto reducir el riesgo del ACV.
Síndrome metabólico: está indicado el manejo individual de los componentes del SM, tal como se recomienda en las guías respectivas; son útiles el ejercicio, la pérdida de peso, dietas apropiadas y medicamentos para disminuir la PA y los lípidos, controlar la glicemia, tratar la microalbuminuria o la proteinuria y el uso de antiagregantes plaquetarios.
Abuso del alcohol: cinco o más tragos diarios de licor representan 60% a 80% de incremento del riesgo. La reducción del consumo de alcohol a 2 tragos por día en los hombres y a uno por día en las mujeres no embarazadas es adecuada (C IIb, NB).
Abuso de drogas: los adictos se deben remitir a manejo especializado (C IIb, N C).
Anticonceptivos orales (ACO): RR de 2.8. El riesgo de ACV asociado con dosis bajas de ACO, con ausencia de otros factores de riesgo, parece ser bajo o inexistente (C III, NB). Se sugiere que los ACO deben evitarse en mujeres con otros factores de riesgo, fumadoras o con antecedentes de tromboembolias (C III, NC). Para quienes eligen asumir el incremento del riesgo es útil la terapia agresiva de sus otros factores (C IIb NC).
Síndrome de apneas del sueño: RR de 1,2%/año. Se debe preguntar por los patrones del dormir en el caso de personas con obesidad abdominal e hipertensión, cuando hay resistencia al tratamiento. Si se sospecha el síndrome, referir el paciente a consulta especializada (C IIb, NC)
Migraña: RR de 2.1. Hay información insuficiente para recomendar un tratamiento específico que reduzca el riesgo de un primer ACV en mujeres con migraña, incluyendo la migraña con aura.
Hiperhomocisteinemia (HCYST): RR de 1.3 a 2.3. Se recomiendan vegetales, frutas, legumbres, carnes, pescado, granos fortificados y cereales (C IIb, NC). Existe poca información para recomendar un tratamiento específico que reduzca el riesgo de un primer ACV cuando hay HCYST. Se recomienda el uso de ácido fólico y vitaminas B en presencia de HCYST elevada, dada su seguridad y bajo costo (C IIB, NC).
Lipoproteina(a) elevada: RRS de 2.92. No hay recomendaciones definitivas acerca de su manejo; el tratamiento con niacina (de liberación inmediata o extendida) puede ser útil, ya que reduce los niveles de Lp(a) en un 25% (C IIb, NC). Se desconoce la utilidad del uso conjunto de niacina y estatinas.
Fosfolipasa A2 Asociada Con lipoproteína elevada: No hay recomendaciones.
Hipercoagulación: los anticuerpos anticardiolipina en hombres confieren un riesgo relativo no significativo de 1.3 y en mujeres de 1.9. El anticoagulante lúpico en mujeres representa un RR significativo de 1.8. Hay insuficiente información para dar recomendaciones de prevención de un primer ACV cuando hay trombofilias hereditarias o adquiridas.
Inflamación: una proteína C reactiva de alta sensibilidad (PCRas) mayor de 3 mg/l condiciona un RR entre 2 y 3. Actualmente no hay evidencias que apoyen el uso amplio de la PCRas en la población adulta como un marcador general de riesgo vascular. La PCRas puede ser útil en la determinación de las metas a alcanzar en aquellos pacientes que tienen un riesgo cardiovascular moderado de acuerdo con los factores de riesgo tradicionales (C IIa, NB).
Infecciones: la información al respecto es insuficiente para recomendar una terapia con antibióticos para prevenir el ACV con base en la seropositividad de uno o varios organismos patógenos.
Ácido Acetilsalicílico: el ASA no se recomienda en la prevención de un primer ACV en hombres (C III, NA). Puede ser útil para la profilaxis de problemas cardiovasculares en general, cuando el riesgo es lo suficientemente alto para que los beneficios pesen más que los riesgos asociados con su prescripción (CI, NA). El ASA puede ser usado para prevenir el primer ACV en mujeres cuyo riesgo cardiovascular sea lo suficientemente alto para que los beneficios pesen más que los riesgos asociados con el tratamiento. (C IIa, NB).
Terapia de Sustitución Hormonal en la menopausia
La divergencia de más impacto en el mundo entre las conclusiones de los estudios de observación y los estudios experimentales posiblemente sea la que se encontró en las investigaciones del empleo de la Terapia de Sustitución Hormonal (TSH) para la mujer menopáusica. Hasta el año 2002 se aceptaban las bondades de la TSH en la prevención de algunas de las condiciones crónicas más importantes para la mujer en esta época de la vida. La investigación clínica disponible era prolífica e incluso se había condensado en varios metanálisis 4,5 que proponían una disminución en el riesgo de enfermedad cardiovascular entre las usuarias de la terapia. Alvan Feinstein, padre de la epidemiología clínica, ya había advertido de las dificultades de los metanálisis de estudios de observación, cuando en un encuentro de expertos en esta metodología de investigación, en su ponencia “Meta–análisis: alquimia estadística para el siglo 21”, había afirmado irónicamente, tal como era su estilo, que “Yo admiro el coraje del grupo que asume esta tarea ( realizar metanálisis con estudios observacionales sin asignación aleatoria ), la cual se parece a un intento de una persona cuadripléjica tratando de escalar el monte Everest sin ayuda” 6 Y de dónde se genera una aseveración tan radical como esta? La explicación está en la esencia de la investigación clínica y las marcadas diferencias entre los ensayos clínicos, considerados a la luz del conocimiento actual como los únicos estudios capaces de confirmar un nexo de causalidad entre un factor y un desenlace, y los estudios de observación analíticos.
Adicional a permitir realizar unas pruebas estadísticas válidas, la asignación aleatoria disminuye notablemente la probabilidad de los sesgos de selección y de confusión que pueden tener los estudios de observación. El enmascaramiento tanto de la secuencia de asignación aleatoria como de la evaluación de la evolución y la medición de los desenlaces minimiza la posibilidad de los sesgos de medición.
Las ramas de tratamiento hormonal del estudio Womens Health Initiative (WHI) 7,8 son ensayos clínicos controlados en los cuales, mediante un mecanismo aleatorio, se asignaron mujeres a recibir tratamiento hormonal o placebo. Esta estrategia de asignación de tratamientos garantiza que el ingreso del individuo a alguno de los grupos de estudio no esté definida por alguna de sus características previas, por lo tanto se obtienen dos grupos de comparación con condiciones clínicas y sociales muy similares lo que lleva a que las diferencias que se presenten en los resultados al final del seguimiento son explicadas por el tratamiento recibido y no por las otras características. Los estudios observacionales previos mostraban que las mujeres usuarias de terapia de sustitución tenían a la vez un mayor nivel educativo, menor índice de masa corporal, mayor consumo de alcohol, dedicaban mayor tiempo al ejercicio, tenían menor peso que a la vez explicaba que tuvieran menores niveles de insulina en sangre en ayunas y un perfil lipídico más favorable, tenían menores niveles de presión arterial, empleaban mayor tiempo libre en ejercicio y era más frecuente que ingirieran dosis bajas de alcohol. 9
El enmascaramiento de la asignación de la secuencia de distribución al azar es tanto o más importante que la misma asignación aleatoria. Su objetivo es que el investigador no sepa a cual grupo pertenece el individuo que va a ingresar a la investigación y con ello se evita que se seleccionen o se excluyan los individuos según el interés del investigador. Esta estrategia metodológica se respetó en los ensayos clínicos y obviamente no hace parte de ningún estudio observacional. El efecto de no cumplir con este requisito es el mismo que tiene la falta de asignación aleatoria. En los ensayos clínicos del WHI la única forma de identificar el medicamento recibido por las mujeres era mediante la lectura de un código de barras en el frasco que contenía los tratamientos, y esto solo se podía realizar en la oficina central. El hecho de conocer a cual grupo pertenecen los individuos facilita que el investigador implemente cointervenciones que favorezcan a un grupo o realice seguimientos diferenciales entre los grupos que en últimas serían los que inducirían los resultados. En los estudios observacionales del tema se puede apreciar que el grupo de usuarias de la TSH tienen una tendencia significativa a realizar más ejercicio, consultar más frecuentemente al médico, realizarse exámenes de control como medición de lípidos, citologías, mamografías, sangre oculta en heces y examen rectal y a implementar otras medidas preventivas de salud. 9 En el WHI todas las mujeres siguieron un mismo protocolo de control y seguimiento. En el estudio de estrógeno más progestina, el ginecólogo tratante, pero nunca los investigadores, supo el grupo de asignación en un 24% y en el de solo estrógeno un 1,7%.
Un aspecto que disminuye validez en los estudios son las pérdidas del seguimiento. En la rama de terapia combinada del WHI se tiene información del 96,5% de las mujeres y en el de solo estrógeno del 94,8%, cifras de seguimiento por debajo de las pérdidas aceptadas que son del 10 a 20%. En los estudios observacionales de casos y controles, fuente importante de información sobre la TSH, no se parte de una población, por lo tanto no se puede conocer la incidencia real de los eventos; adicionalmente, es posible que los individuos seleccionados no sean representativos totalmente de las mujeres que han recibido TSH sino que sean una subpoblación de mejor pronóstico.
Las diferencias de los resultados entre los estudios observacionales y sus respectivos metanálisis con respecto a la enfermedad cardiovascular son diametralmente opuestos a los obtenidos en el WHI. Debido a la diferencia de metodología, a la reconocida superioridad de los ensayos clínicos y a que el WHI se considera un estudio válido, la mayoría de organizaciones y autoridades en el mundo desecharon la propuesta que se tenía de administrar TSH a las mujeres menopáusicas con la intención de disminuir la mortalidad por enfermedad coronaria y hoy se acepta que por el contrario aumentan el riesgo de padecerla.
BIBLIOGRAFÍA
1. GRADE Working Group. Grading quality of evidence and strength of recommendations. BMJ 2004; 328:1490–1497. [ Links ]
2. Guyatt,G.y col. Editorial: An emerging consensus on grading recommendations? ACP Journal Club 2006; 144: A–9. [ Links ]
3. Goldstein LB, Adams R, Alberts MJ, Appel LJ, Brass LM, Bushnell CD, et al. Primary prevention of ischemic stroke: a guideline from the American Heart Association/American Stroke Association Stroke Council: cosponsored by the Atherosclerotic Peripheral Vascular Disease Interdisciplinary Working Group; Cardiovascular Nursing Council; Clinical Cardiology Council; Nutrition, Physical Activity, and Metabolism Council; and the Quality of Care and Outcomes Research Interdisciplinary. Stroke 2006; 37: 1583–1633. [ Links ]
4. Grady D, Rubin S, Petiti D, Fox C, Black D, Ettinger B y cols. Hormone Therapy To Prevent Disease and Prolong Life in Postmenopausal Women. Ann Inter Med 1992; 117: 1038–1041 [ Links ]
5. Stampfer MJ, Colditz GA. Estrogen replacement therapy and coronary heart disease: A cuantitative assessment of the epidemiologic evidence. Prev Med 1991; 20: 47–63 [ Links ]
6. Feinstein A. Meta–aanlysis: statistical alqchemy for the 21st century. J Clin Epidemiol 1995: 71–79. [ Links ]
7. Writing Group for the Womens Health Initiative Investigators. Risk and Benefits of Estrogen plus Progestin in Healthy Posmenopausal Women. JAMA 2002; 288: 321–333. [ Links ]
8. The Womens Health Initiative Steering Commitee. Effecsts of Conjugated Equine Estrogen in Posmenopausal Women With Histerectomy. JAMA 2004; 291:1701–1712. [ Links ]
9. Zuleta J. Terapia de reemplazo hormonal y enfermedad coronaria. Rev Col Obst Ginecol 2003; 54:113–120. [ Links ]














