Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Iatreia
Print version ISSN 0121-0793
Iatreia vol.25 no.1 Medellín Jan./Mar. 2012
ARTÍCULO DE REVISIÓN
Sustitutos cutáneos desarrollados por ingeniería de tejidos
Skin substitutes developed by tissue engineering
Claudia Marcela Arenas Gómez1; Gabriel Jaime Merizalde Soto2; Luz Marina Restrepo Múnera3
1 Microbióloga y Bioanalista, Auxiliar de investigación, Grupo Ingeniería de Tejidos y Terapias Celulares, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
2 Biólogo, Investigador asociado, Grupo Ingeniería de Tejidos y Terapias Celulares, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
3 Bióloga, PhD en Ciencias, Coordinadora del Grupo Ingeniería de Tejidos y Terapias Celulares, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia. grupoittc@yahoo.es
Recibido: noviembre 11 de 2010
Aceptado: marzo 08 de 2011
RESUMEN
La piel es un tejido complejo vulnerable a procesos que alteran su estructura, integridad y funcionalidad como, por ejemplo, quemaduras, heridas crónicas y diversas enfermedades congénitas. Los avances tecnológicos en la fabricación de biomateriales y en el cultivo de células han permitido la producción de sustitutos cutáneos que han sido una alternativa terapéutica para algunas de estas complicaciones. Esta revisión pretende actualizar los aspectos generales, composición, perspectivas futuras y de aplicación de los principales sustitutos cutáneos que se ofrecen actualmente en el mercado internacional. Igualmente, presentará algunas experiencias del Grupo de Ingeniería de Tejidos y Terapias Celulares (GITTC) de la Facultad de Medicina de la Universidad de Antioquia.
PALABRAS CLAVE
Biomateriales, Células Alogénicas, Células Autólogas, Células Xenogénicas, Ingeniería deTejidos, Sustitutos Cutáneos.
SUMMARY
The skin is a complex tissue vulnerable to different processes that may alter its structure, integrity and functionality, among them: burns, chronic wounds and various congenital diseases. Technological advances in biomaterials manufacture and cell culture have allowed the production of skin substitutes thus providing an alternative therapy for some of these complications. This review aims to update the general aspects, composition, future prospects and implementation of the most common skin substitutes currently available in the international market. Some experiences of the Tissue Engineering and Cellular Therapy Group (GITTC), at the University of Antioquia, Faculty of Medicine, in Medellín, Colombia, are also presented.
KEY WORDS
Allogeneic Cells, Autologous Cells, Biomaterials, Skin Substitutes, Tissue Engineering, Xenogeneic Cells.
INTRODUCCIÓN
La piel es un sistema complejo en el cual interaccionan sinérgicamente diferentes tipos de células. La epidermis está compuesta principalmente por queratinocitos, que forman un epitelio estratificado con células basales que proliferan en la capa más profunda y una capa queratinizada relativamente impermeable en la superficie (estrato córneo). La dermis provee integridad estructural, elasticidad y una red vascular para nutrir la piel. Sus principales componentes celulares son los fibroblastos (1). La membrana basal (MB) es una estructura especializada que comprende un complejo multiproteico que establece la unión de la epidermis y la dermis (2). Se ha considerado que la interacción de los fibroblastos y los queratinocitos es esencial para el establecimiento de una membrana basal funcional (3).
La piel protege al organismo de fuerzas físicas, agentes químicos, rayos UV y microorganismos patógenos. Previene la pérdida de fluidos corporales y desempeña un papel importante en la termorregulación y en la respuesta inmune a factores que afecten su integridad (4). Las quemaduras, algunas enfermedades genéticas o autoinmunes (epidermolisis ampollosa, pénfigo vulgar, hiperqueratosis epidermolítica) y las úlceras cutáneas en los miembros inferiores, producto de enfermedades de base (diabetes, hipertensión arterial o insuficiencia venosa), son ejemplos de algunos de estos procesos.
En los últimos 30 años, la ingeniería de tejidos ha venido desarrollando diferentes sustitutos o equivalentes cutáneos que constituyen un avance significativo en el tratamiento de estos problemas de la piel.
EVENTOS IMPORTANTES EN EL DESARROLLO DE LOS SUSTITUTOS CUTÁNEOS
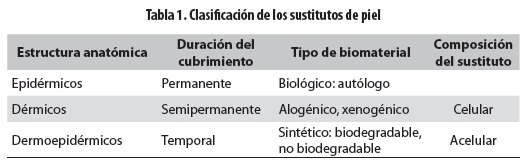
Los cultivos de piel in vitro se iniciaron a partir de la estandarización de la separación enzimática de la epidermis y la dermis (5) y posteriormente con el cultivo de queratinocitos (6). Más adelante, se hicieron nuevos procedimientos que permitieron avanzar en este campo. Uno de ellos fue propuesto por Rheinwald y Green (7), que optimizaron el crecimiento y la expansión de células epidérmicas humanas, utilizando fibroblastos de origen murino que proporcionan principalmente factores de crecimiento a los queratinocitos. Más adelante, Bell y colaboradores (8) crearon un sustituto dermoepidérmico que fue evaluado en un modelo animal. Esta técnica se transformó posteriormente en el producto Apligraf® (8). En la misma época se produce Integra® (9), el primer equivalente dérmico aceptado y comercializado en Estados Unidos a partir de 1996 (9). La obtención y aplicación de este último producto generó un nuevo campo de investigación con el objetivo de proveer una dermis ''sintética'' a los pacientes, eliminando la necesidad de autoinjertos (4). Además, significó un gran avance para la ingeniería de tejidos, al generar una amplia gama de sustitutos y biopolímeros que suministran un soporte mecánico adecuado para la migración y proliferación celulares. Debido a la gran variedad de sustitutos, se han propuesto diferentes clasificaciones (tabla 1).
SUSTITUTOS CUTÁNEOS COMERCIALES
A. Sustitutos epidérmicos
Epicel® y Epidex® se construyen usando queratinocitos autólogos, que se cultivan hasta obtener confluencia y conformar un autoinjerto epitelial cultivado (CEA, por la sigla en inglés de cultured epithelial autografts). Epicel® está compuesto de células autólogas (del propio paciente), derivadas de una pequeña biopsia de piel de la zona retroauricular o la inguinal (10) y es el único sustituto epidérmico autólogo producido comercialmente en Estados Unidos. Para su aplicación se utilizan gasas estériles vaselinadas. Epidex® está compuesto de queratinocitos obtenidos del folículo piloso con una membrana de silicona como soporte (11). La fragilidad mecánica de los autoinjertos epiteliales cultivados es una de sus principales desventajas al momento de aplicarlos y es el resultado de la ausencia de un componente dérmico (1).
MySkin® utiliza queratinocitos autólogos en presencia de fibroblastos murinos irradiados, incluidos en soportes de silicona que contienen elementos especiales (12). Una de las ventajas con respecto a los anteriores es que necesita menor tiempo de cultivo. Este sustituto está indicado para el tratamiento de neuropatías, pie diabético y quemaduras superficiales (13), pero no puede ser utilizado para quemaduras profundas (14).
ReCell® es un sustituto que utiliza queratinocitos autólogos en suspensión que permiten su aspersión directa en la herida. Se lo ha evaluado para tratar pacientes con vitiligo, logrando una repigmentación del 25% al 75% de las áreas afectadas; se lo ha presentado como un sustituto epidérmico de fácil producción y aplicación (15).
Epifast® se comercializa en Latinoamérica y está compuesto por queratinocitos criopreservados obtenidos de prepucio de neonatos. Se utiliza una gasa vaselinada como soporte (16)
Otros sustitutos epidérmicos que aún no cuentan con ensayos clínicos suficientes y que posiblemente puedan aplicarse para el tratamiento de quemaduras son: Laserskin® o Vivoderm® y Bioseed-S®. Laserskin® contiene ácido hialurónico, considerado como una buena matriz extracelular al promover migración y proliferación de fibroblastos y queratinocitos. En el caso de Bioseed-S®, los queratinocitos autólogos están suspendidos en un gel de fibrina (14).
B. Sustitutos dérmicos
Integra® se compone de una matriz de colágeno bovino tipo I y glicosaminoglicanos de tiburón recubiertos con una silicona temporal que protege de la contaminación (14). Se lo ha considerado como el modelo estándar para el tratamiento de quemaduras completas (17) y de úlceras crónicas (18). Entre sus ventajas están su fácil manejo, su baja inmunogenicidad y el bajo riesgo de transmisión de enfermedades (14). Logra buenos resultados cosméticos al reducir las tasas de contracción y formación de cicatrices (19). Como desventajas tiene su largo período de vascularización (10-14 días) (14) y su temporalidad, que implica hacer una nueva cirugía para un injerto definitivo. Además, se ha demostrado que los cultivos epidérmicos autólogos no se integran muy bien sobre la neodermis producida por Integra® (20).
Alloderm® está constituido por dermis alogénica de origen humano que se liofiliza para remover todo el material celular (no produce rechazo inmunológico), preservando la membrana basal (14). Se lo ha utilizado en sitios o heridas donde es menos importante la revascularización inmediata, como en la cirugía periodontal y en la reconstrucción rectovaginal o rectouretral (21); también se ha recurrido a él, con resultados promisorios, en heridas térmicas agudas (14).
Matriderm® es un producto similar al anterior pero de origen bovino (xenogénico). Está conformado por una matriz de colágeno bovino estructuralmente intacta, de un milímetro de espesor, recubierta con un hidrolizado de alfa elastina. Se ha reportado que utilizándolo con autoinjerto ofrece una buena alternativa para tratar quemaduras graves en el dorso de la mano y para úlceras diabéticas (22,23).
Dermagraft® es un material criopreservado que utiliza fibroblastos obtenidos de prepucios de neonatos sembrados sobre un material sintético bioabsorbible de ácido poliglicólico/ácido poliláctico. El soporte se degrada por hidrólisis a los 20 o 30 días, mientras los fibroblastos producen factores de crecimiento y elementos de la matriz extracelular (vitronectina, tenascín, colágenos y gligosaminoglicanos) que ayudan a regenerar la dermis perdida. Se utiliza principalmente para tratar personas con pie diabético y úlceras venosas (24). Una de sus desventajas es el incremento del costo porque se requieren aplicaciones múltiples (14).
EZ Derm® contiene colágeno reconstituido de origen porcino que incluye aldehído para aumentar su resistencia a la tensión. El producto no se incorpora a la herida y debe ser removido (25). Sin embargo, se comercializa como un revestimiento bioactivo para heridas (14).
Terudermis® es una esponja de colágeno bovino desnaturalizado por calor y entrecruzado por tratamiento dehidrotérmico. Se reconstituye y se liofiliza. Es un material diseñado para el tratamiento de heridas profundas, en las que hay exposición de hueso, músculo o ligamento (26).
Biobrane®, Biobrane-L® y TransCyte® son cubiertas semipermeables temporales muy similares que contienen una silicona seudoepidérmica, unida a nailon y colágeno porcino. TranCyte® contiene además fibroblastos de prepucio de neonato. Este tipo de sustitutos ha sido evaluado para tratar quemaduras de grosor parcial (segundo grado). Sin embargo, deben ser retirados después de siete a 14 días puesto que se fabrican con material sintético no biodegradable (14).
Hyalomatrix PA® y Hyalograft 3D® se consideran seguros pues no contienen componentes derivados de animales o de otros seres humanos. Se sintetizan a partir de derivados del ácido hialurónico, uno de los principales polisacáridos que hacen parte de la matriz extracelular de la dermis. Promueven la migración y proliferación de fibroblastos y queratinocitos. Con Hyalomatrix PA® se han llevado a cabo algunos ensayos preclínicos en modelos porcinos con resultados favorables en el tratamiento de heridas complejas (27). Se ha utilizado Hyalograft 3D®, combinado con un sustituto epidérmico autólogo como Laserskin®, para tratar úlceras en los pies (28). Contribuye a una rápida formación de la membrana basal (29).
C. Sustitutos dermo-epidérmicos
Comparados con los sustitutos dérmicos o epidérmicos, los dermo-epidérmicos son los sustitutos biológicos más avanzados, sofisticados y costosos para la reparación de tejidos (30). La mayoría de los sustitutos dermo-epidérmicos utilizan células alogénicas de piel incorporadas en un soporte dérmico. Este enfoque permite la producción de grandes ''lotes'' uniformes del producto y una mayor disponibilidad comercial. Sin embargo, estos biomateriales actúan de preferencia como cubiertas temporales biológicamente activas, que suministran factores de crecimiento, citocinas y matriz extracelular a las células del huésped mientras se inicia la regeneración de la herida (1). Se ha reportado que los fibroblastos alogénicos sobreviven cerca de tres semanas en la herida del paciente mientras que los queratinocitos son rechazados en menor tiempo (31). En consecuencia, para producir sustitutos dermoepidérmicos de piel es posible utilizar fibroblastos autólogos o alogénicos, pero para lograr un cierre permanente del defecto en la piel solo es posible utilizar queratinocitos autólogos (14).
Estos sustitutos en dos o tres dimensiones simulan la estructura histológica y funcional de la piel normal. Los cultivos ''organotípicos'', en interfase aire-líquido, proveen el contacto del sustituto dérmico con el medio nutritivo y el del sustituto epidérmico, con el aire. En este tipo de cultivo in vitro se evidencian la formación de membrana basal y la madurez de la unión dermoepidérmica, que contribuye a la estabilidad mecánica del sustituto al aplicarlo al paciente (32).
Apligraf® está compuesto por fibroblastos y queratinocitos alogénicos de prepucio de neonato, incluidos en una matriz de colágeno bovino tipo I. Este producto no genera rechazo inmunológico, porque después de dos meses las células no sobreviven in vivo (33). Este sustituto tiene licencia para ser aplicado en pacientes con úlceras venosas y pie diabético (tabla 2) pero solo se puede considerar como una cubierta bioactiva temporal. Sus principales desventajas son: su corta viabilidad después de la producción (cinco días), la necesidad de una aplicación delicada y el riesgo de transferir enfermedades por sus constituyentes alogénicos (14).
OrCell®, conformado por fibroblastos y queratinocitos obtenidos de un mismo prepucio de neonato cultivados en una esponja de colágeno bovino tipo I, tiene licencia de aplicación para el tratamiento de pacientes con epidermólisis ampollosa distrófica recesiva y sitios donantes de autoinjertos en quemados (14).
TissueTech Autograft System® combina dos biomateriales aplicados consecutivamente a la herida: Hyalograft 3D® y Laserskin®. Utiliza fibroblastos y queratinocitos autólogos incluidos en membranas microperforadas de ácido hialurónico. Este sistema permite tratamientos exitosos de úlceras en pies diabéticos, pero requiere el implante de dos productos, lo que dificulta su aplicación clínica (34).
PermaDerm (Cincinnati Shriners Skin Substitute) ® es uno de los sustitutos de piel más prometedores, que han alcanzado uso clínico. Está conformado en tres dimensiones (organotípico), sobre una esponja de colágeno que contiene queratinocitos y fibroblastos autólogos. Puede considerarse un sustituto cutáneo ''verdadero'' y permanente que restaura completamente las heridas (35). En la tabla 2 se puede ver un listado de los sustitutos cutáneos disponibles comercialmente.
PolyActive®: queratinocitos y fibroblastos autólogos sembrados en una matriz porosa que contiene una mezcla de compuestos químicos (óxido de polietileno tereftalato/polibutileno tereftalato). Este polímero se usa comúnmente para la reconstrucción ósea, pero podría ser utilizado como un soporte biológico para el tratamiento de heridas en piel (14).
Karoskin®: piel glicerolada o liofilizada de cadáver humano que se incorpora en las heridas profundas. Alivia el dolor y brinda una cubierta temporal a los pacientes con quemaduras extensas durante las primeras semanas en las que la respuesta inmune está suprimida (14).
Biomateriales utilizados en los sustitutos cutáneos
Tanto en décadas anteriores como en la actualidad, muchos sustitutos de piel se han fabricado a partir de colágeno como material de soporte. La popularidad del colágeno se atribuye a su abundancia en la piel, su reconocimiento por receptores de la superficie celular y su propiedad de formar entrecruzamientos para conferir propiedades mecánicas al tejido. Sin embargo, el colágeno aparece durante las últimas etapas del cierre de las heridas, después de que los fibroblastos han invadido y llenado el espacio de la herida (55). Por lo tanto, un soporte construido principalmente con colágeno puede no ser el óptimo para la migración de células al tejido que se quiere reparar (31).
La fibrina es otro soporte utilizado con mucha frecuencia. Este biomaterial ha permitido el cultivo y la proliferación de queratinocitos para la reepitelización de heridas parciales, profundas y completas tanto en modelos animales como en seres humanos (56), con buen rendimiento incluso en sitios donde la movilidad es inevitable (57). Reduce el tiempo de activación de los queratinocitos, promoviendo una reepitelización completa (58). Algunas de las desventajas que se le han atribuido son sus características físicas: baja resistencia mecánica y tasa alta de degradación química (57). Para tratar de solucionar esto se han adicionado membranas de policaprolactona a los geles de fibrina. Estas membranas poseen una cinética de degradación baja, altas fuerzas de tensión, son biocompatibles y biodegradables (59).
La Unidad de Ingeniería de Tejidos del Centro Comunitario de Sangre y Tejidos del Principado de Asturias (CCST) y el Grupo de Biomedicina Epitelial del Centro de Investigaciones Energéticas, Medioambientales y Tecnológicas de Madrid (CIEMAT) han venido desarrollando desde hace varios años un modelo de piel completa (dermis y epidermis), permanente y autóloga. Utilizan un soporte de fibrina/fibronectina con fibroblastos y queratinocitos autólogos. Este sustituto de piel se ha utilizado en el tratamiento de heridas epiteliales graves con diferentes porcentajes de epitelización completa, dependiente de la lesión (60). Esta tecnología ha sido adaptada, implementada y aplicada en nuestro país por el Grupo Ingeniería de Tejidos y Terapias Celulares (GITTC), de la Facultad de Medicina de la Universidad de Antioquia, con la asesoría del Director de la Unidad de Ingeniería de Tejidos del CCST.
Nuevas tendencias en la ingeniería de tejidos para sustitutos cutáneos
Existen muchos retos que se deben enfrentar en la producción de los sustitutos cutáneos con el fin de lograr trasplantes exitosos. El principal objetivo es conseguir que el sistema inmune del paciente no rechace las células cultivadas, y que estas se adhieran con seguridad sobre las áreas difíciles en las heridas o quemaduras. Además, se requieren medios que aceleren la formación de membrana basal y la posterior vascularización. Por otro lado, se debe contar con estrategias que eviten la contracción, pérdida de pigmentación y mala cicatrización, como sucede con los injertos tradicionales (61).
Los productos de la ingeniería de tejidos disponibles en el comercio para una sustitución permanente de la piel pueden reemplazar parcialmente la función de barrera protectora, pero no restauran otras funciones tales como: sensación táctil, temperatura, excreción, respiración, termorregulación, protección contra rayos ultravioleta y funciones sintéticas y estéticas.
Se han obtenido avances importantes en la adición de otras células de la piel que puedan ayudar a mejorar la funcionalidad de los sustitutos: melanocitos y células endoteliales (62), o de apéndices de la piel, como folículos pilosos y glándulas sebáceas (63). Incluso se ha planteado la posibilidad de incluir células derivadas de la médula ósea como recurso para la construcción de los equivalentes (64), y factores que faciliten una vascularización más rápida con el fin de evitar procesos necróticos o el desprendimiento de los sustitutos (65). Además, se está evaluando la posibilidad de hacerles modificaciones genéticas a los fibroblastos y queratinocitos con el propósito de generar más factores de crecimiento y facilitar su proliferación (66). Otra de las alternativas para optimizar la funcionalidad de los sustitutos es la adición de moléculas de señalización para regular las interacciones célula-célula y célula-matriz que aceleren el proceso de biointegración, o para ajustarlo de acuerdo con las fases del proceso de reparación de las heridas (67,68). Estos materiales híbridos biomiméticos ''inteligentes'' están diseñados con el propósito de producir una restauración más natural de la piel (69).
Sustitutos cutáneos: una alternativa de tratamiento en Colombia
Algunos estudios han reportado la problemática de las heridas de piel en Colombia. La Dirección Seccional de Salud de Antioquia, en el período de 1986-2005, reportó un total de 7.158 personas con heridas de piel por la manipulación inadecuada de pólvora (70). Un estudio hecho por la Unidad de Quemados del Hospital San Vicente de Paúl, de Medellín, con 2.319 pacientes en un período de 10 años, halló que la causa más frecuente de quemaduras eran los líquidos calientes (51,4%), seguidos por las llamas (33,7%) y la electricidad (10,6%); se demostró que los incendios y los accidentes domésticos ocasionan el 70,2% de las quemaduras de segundo y tercer grados y que varias de estas heridas afectan hasta el 27% del área corporal total y causan una mortalidad del 7,4% (71). El factor limitante para el tratamiento de las quemaduras que excedan el 50% a 60% de la superficie corporal total es la disponibilidad de piel autóloga. Las ventajas de disponer de sustitutos cutáneos autólogos para pacientes con heridas de piel son las siguientes: evitar el riesgo de rechazo del injerto y la transmisión de infecciones; disminuir el número de intervenciones y la morbilidad de los sitios donantes cuando se realizan autoinjertos (72).
Otro de los problemas de salud pública que se presentan en la población colombiana es la diabetes (73). Una de sus complicaciones más comunes es el pie diabético, con formación de úlceras crónicas, consideradas como la causa principal de amputación no traumática de miembros inferiores, y que está asociado a un alto costo humano, social y económico (74). Los sustitutos cutáneos se han utilizado como una alternativa de tratamiento para este tipo de úlceras (75), con un buen porcentaje de recuperación en el mundo (76), evitando su progreso (77) y la amputación de la extremidad (78). Estas nuevas terapias, aunque consideradas costosas, tienen un impacto positivo en la calidad de vida de las personas que padecen estas enfermedades y es necesario revisar y revaluar el costo-beneficio para este tipo de pacientes (75).
Experiencia del Grupo Ingeniería de Tejidos y Terapias Celulares
Para la construcción de los sustitutos cutáneos de piel humana in vitro, el GITTC utiliza queratinocitos y fibroblastos autólogos, empleando un gel de fibrina como soporte tridimensional biocompatible para la adherencia y proliferación de dichas células (figura 1). El Grupo ha evaluado las características histológicas de este modelo de equivalente cutáneo y ha demostrado que los queratinocitos y fibroblastos presentan características funcionales, estructurales y morfológicas semejantes a las de la piel normal. La presencia de fibroblastos humanos en el sustituto cutáneo permite la diferenciación, expansión y rápido crecimiento clonal de los queratinocitos. Se evidenció el desarrollo de un epitelio con un grado de estratificación similar al normal. Además, presenta ventajas en términos de costos y estabilidad frente a otros productos similares importados (79). También se ha avanzado en estrategias para la recuperación de defectos generados por traumas y enfermedades sistémicas o degenerativas, utilizando estos equivalentes cutáneos para la recuperación de úlceras en las extremidades inferiores (80) (figura 2).
Otro de los campos que se han abordado es la modificación genética de queratinocitos. Se logró evaluar la transducción de queratinocitos humanos cultivados in vitro con el vector retroviral FOCH29- NeoR (81). Lo anterior posibilitaría la modificación genética de los queratinocitos utilizados en sustitutos cutáneos, para aumentar, por ejemplo, la expresión de genes que codifican para factores de crecimiento importantes como el derivado de las plaquetas (PDGF, por la sigla en inglés de platelet-derived growth factor) y el factor de crecimiento del endotelio vascular (VEGF, por la sigla en inglés de vascular endothelial growth factor).
Actualmente se están desarrollando un biosustituto para epitelio corneal (82) y un equivalente autólogo de mucosa oral, para tratar alteraciones en la cavidad oral, como el labio y paladar hendidos y los defectos periodontales ocasionados por trauma, con el fin de solucionar el problema de escasez de tejido donante y evitar las reintervenciones quirúrgicas. Desde 2008 se ha enfatizado en el desarrollo de un empaque que conserve adecuadamente la calidad de las células y los sustitutos cutáneos durante el transporte a otras ciudades del país.
CONCLUSIONES
El avance tecnológico en la fabricación de biomateriales y en el cultivo de células ha permitido la producción de sustitutos de piel que han contribuido al tratamiento de quemaduras, heridas crónicas y enfermedades congénitas de la piel. Sin embargo, es importante continuar investigando la forma de mejorarlos para optimizar su aplicación y lograr mejores resultados, con menores costos, ya que en la actualidad no se dispone comercialmente de un sustituto ''ideal'' de piel para el cierre de heridas complejas.
El rápido progreso en la ingeniería de tejidos y los diferentes enfoques en el diseño de biomateriales para sustitutos de piel, que incluye la utilización de células madre, brinda la posibilidad de obtener en un futuro cercano un producto para regenerar la piel en pacientes con las enfermedades mencionadas y con otras como las heridas producidas por minas antipersonal, que en Colombia desafortunadamente cada vez son más frecuentes.
REFERENCIAS BIBLIOGRÁFICAS
1. Supp DM, Boyce ST. Engineered skin substitutes: practices and potentials. Clin Dermatol. 2005;23(4):403-12. [ Links ]
2. El Ghalbzouri A, Jonkman MF, Dijkman R, Ponec M. Basement membrane reconstruction in human skin equivalents is regulated by fibroblasts and/or exogenously activated keratinocytes. J Invest Dermatol. 2005 Jan;124(1):79-86. [ Links ]
3. König A, Bruckner-Tuderman L. Epithelial-mesenchymal interactions enhance expression of collagen VII in vitro. J Invest Dermatol. 1991 Jun;96(6):803-8. [ Links ]
4. Böttcher-Haberzeth S, Biedermann T, Reichmann E. Tissue engineering of skin. Burns. 2010 Jun;36(4):450-60. [ Links ]
5. Billingham R, Medawa RP. Technique of free skin grafting in mammals. J Exp Biol. 1950;28:385-402. [ Links ]
6. Karasek MA. In vitro culture of human skin epithelial cells. J Invest Dermatol. 1966 Dec;47(6):533-40. [ Links ]
7. Rheinwald JG, Green H. Serial cultivation of strains of human epidermal keratinocytes: the formation of keratinizing colonies from single cells. Cell. 1975 Nov;6(3):331-43. [ Links ]
8. Bell E, Ehrlich HP, Buttle DJ, Nakatsuji T. Living tissue formed in vitro and accepted as skin-equivalent tissue of full thickness. Science. 1981 Mar 6;211(4486):1052-4. [ Links ]
9. Burke JF, Yannas IV, Quinby WC, Bondoc CC, Jung WK. Successful use of a physiologically acceptable artificial skin in the treatment of extensive burn injury. Ann Surg. 1981 Oct;194(4):413-28. [ Links ]
10. Carsin H, Ainaud P, Le Bever H, Rives J, Lakhel A, Stephanazzi J, et al. Cultured epithelial autografts in extensive burn coverage of severely traumatized patients: a five year single-center experience with 30 patients. Burns. 2000 Jun;26(4):379-87. [ Links ]
11. Tausche A-K, Skaria M, Böhlen L, Liebold K, Hafner J, Friedlein H, et al. An autologous epidermal equivalent tissue-engineered from follicular outer root sheath keratinocytes is as effective as split-thickness skin autograft in recalcitrant vascular leg ulcers. Wound Repair Regen. 2003;11(4):248-52. [ Links ]
12. Moustafa M, Simpson C, Glover M, Dawson RA, Tesfaye S, Creagh FM, et al. A new autologous keratinocyte dressing treatment for non-healing diabetic neuropathic foot ulcers. Diabet Med. 2004 Jul;21(7):786-9. [ Links ]
13. Moustafa M, Bullock AJ, Creagh FM, Heller S, Jeffcoate W, Game F, et al. Randomized, controlled, singleblind study on use of autologous keratinocytes on a transfer dressing to treat nonhealing diabetic ulcers. Regen Med. 2007 Nov;2(6):887-902. [ Links ]
14. Shevchenko RV, James SL, James SE. A review of tissue-engineered skin bioconstructs available for skin reconstruction. J R Soc Interface. 2010 Feb 6;7(43):229-58. [ Links ]
15. Cervelli V, De Angelis B, Balzani A, Colicchia G, Spallone D, Grimaldi M. Treatment of stable vitiligo by ReCell system. Acta Dermatovenerol Croat. 2009 Jan;17(4):273-8. [ Links ]
16. Gutiérrez E, González M, Fernández G, Valle V. Vaginoplastia con queratinocitos cultivados: caso clínico. Cir Plast. 2006;16(3):126-30. [ Links ]
17. Heitland A, Piatkowski A, Noah EM, Pallua N. Update on the use of collagen/glycosaminoglycate skin substitute-six years of experiences with artificial skin in 15 German burn centers. Burns. 2004 Aug;30(5):471-5. [ Links ]
18. Silverstein G. Dermal regeneration template in the surgical management of diabetic foot ulcers: a series of five cases. J Foot Ankle Surg. 2006;45(1):28-33. [ Links ]
19. Anthony ET, Syed M, Myers S, Moir G, Navsaria H. The development of novel dermal matrices for cutaneous wound repair. Drug Discovery Today. 2006;3(1):81-6. [ Links ]
20. Sheridan RL, Tompkins RG. Skin substitutes in burns. Burns. 1999 Mar;25(2):97-103. [ Links ]
21. Lesser T, Aboseif S, Abbas MA. Combined endorectal advancement flap with Alloderm graft repair of radiation and cryoablation-induced rectourethral fistula. Am Surg. 2008 Apr;74(4):341-5. [ Links ]
22. Ryssel H, Germann G, Kloeters O, Gazyakan E, Radu CA. Dermal substitution with Matriderm(®) in burns on the dorsum of the hand. Burns. 2010 Dec;36(8):1248-53. [ Links ]
23. Cervelli V, Lucarini L, Cerretani C, Spallone D, Palla L, Brinci L, et al. The use of Matriderm and autologous skin grafting in the treatment of diabetic ulcers: a case report. Int Wound J. 2010 Aug;7(4):291-6. [ Links ]
24. Omar AA, Mavor AID, Jones AM, Homer-Vanniasinkam S. Treatment of venous leg ulcers with Dermagraft. Eur J Vasc Endovasc Surg. 2004 Jun;27(6):666-72. [ Links ]
25. Bello YM, Falabella AF, Eaglstein WH. Tissue-engineered skin. Current status in wound healing. Am J Clin Dermatol. 2001 Jan;2(5):305-13. [ Links ]
26. Choi M, Yi S, Hwang J, Yang W, Lee K. Treatment of bone and tendon-exposed wounds using Terudermis. J. Kor. Soc. Plast. Reconstr. Surg. 1999;26(3):491-7. [ Links ]
27. Myers SR, Partha VN, Soranzo C, Price RD, Navsaria HA. Hyalomatrix: a temporary epidermal barrier, hyaluronan delivery, and neodermis induction system for keratinocyte stem cell therapy. Tissue Eng. 2007 Nov;13(11):2733-41. [ Links ]
28. Caravaggi C, De Giglio R, Pritelli C, Sommaria M, Dalla-Noce S, Faglia E, et al. HYAFF 11-based autologous dermal and epidermal grafts in the treatment of noninfected diabetic plantar and dorsal foot ulcers: a prospective, multicenter, controlled, randomized clinical trial. Diabetes Care. 2003 Oct;26(10):2853-9. [ Links ]
29. Stark H-J, Willhauck MJ, Mirancea N, Boehnke K, Nord I, Breitkreutz D, et al. Authentic fibroblast matrix in dermal equivalents normalises epidermal histogenesis and dermoepidermal junction in organotypic co-culture. Eur J Cell Biol. 2004 Dec;83(11-12):631-45. [ Links ]
30. Jones I, Currie L, Martin R. A guide to biological skin substitutes. Br J Plast Surg. 2002 Apr;55(3):185-93. [ Links ]
31. Clark RAF, Ghosh K, Tonnesen MG. Tissue engineering for cutaneous wounds. J Invest Dermatol. 2007 May;127(5):1018-29. [ Links ]
32. Supp AP, Wickett RR, Swope VB, Harriger MD, Hoath SB, Boyce ST. Incubation of cultured skin substitutes in reduced humidity promotes cornification in vitro and stable engraftment in athymic mice. Wound Repair Regen. 1999;7(4):226-37. [ Links ]
33. Griffiths M, Ojeh N, Livingstone R, Price R, Navsaria H. Survival of Apligraf in acute human wounds. Tissue Eng. 2004;10(7-8):1180-95. [ Links ]
34. Uccioli L. A clinical investigation on the characteristics and outcomes of treating chronic lower extremity wounds using the tissuetech autograft system. Int J Low Extrem Wounds. 2003 Sep;2(3):140-51. [ Links ]
35. Boyce ST, Kagan RJ, Greenhalgh DG, Warner P, Yakuboff KP, Palmieri T, et al. Cultured skin substitutes reduce requirements for harvesting of skin autograft for closure of excised, full-thickness burns. J Trauma. 2006 Apr;60(4):821-9. [ Links ]
36. Renner R, Harth W, Simon JC. Transplantation of chronic wounds with epidermal sheets derived from autologous hair follicles--the Leipzig experience. Int Wound J. 2009 Jun;6(3):226-32. [ Links ]
37. Mulekar SV, Ghwish B, Al Issa A, Al Eisa A. Treatment of vitiligo lesions by ReCell vs. conventional melanocyte- keratinocyte transplantation: a pilot study. Br J Dermatol. 2008 Jan;158(1):45-9. [ Links ]
38. Price RD, Das-Gupta V, Leigh IM, Navsaria HA. A comparison of tissue-engineered hyaluronic acid dermal matrices in a human wound model. Tissue Eng. 2006 Oct;12(10):2985-95. [ Links ]
39. Vanscheidt W, Ukat A, Horak V, Brüning H, Hunyadi J, Pavlicek R, et al. Treatment of recalcitrant venous leg ulcers with autologous keratinocytes in fibrin sealant: a multinational randomized controlled clinical trial. Wound Repair Regen. 2007;15(3):308-15. [ Links ]
40. Gordley K, Cole P, Hicks J, Hollier L. A comparative, long term assessment of soft tissue substitutes: Allo- Derm, Enduragen, and Dermamatrix. J Plast Reconstr Aesthet Surg. 2009 Jun;62(6):849-50. [ Links ]
41. Marston WA, Hanft J, Norwood P, Pollak R. The efficacy and safety of Dermagraft in improving the healing of chronic diabetic foot ulcers: results of a prospective randomized trial. Diabetes Care. 2003 Jun;26(6):1701-5. [ Links ]
42. Stiefel D, Schiestl C, Meuli M. Integra Artificial Skin for burn scar revision in adolescents and children. Burns. 2010 Feb;36(1):114-20. [ Links ]
43. Schneider J, Biedermann T, Widmer D, Montano I, Meuli M, Reichmann E, et al. Matriderm versus Integra: a comparative experimental study. Burns. 2009 Feb;35(1):51-7. [ Links ]
44. Kokkalis ZT, Zanaros G, Sotereanos DG. Ligament reconstruction with tendon interposition using an acellular dermal allograft for thumb carpometacarpal arthritis. Tech Hand Up Extrem Surg. 2009 Mar;13(1):41-6. [ Links ]
45. Lee KC, Lee NH, Ban JH, Jin SM. Surgical treatment using an allograft dermal matrix for nasal septal perforation. Yonsei Med J. 2008 Apr 30;49(2):244-8. [ Links ]
46. Chiu T, Burd A. ''Xenograft'' dressing in the treatment of burns. Clin Dermatol. 2005;23(4):419-23. [ Links ]
47. Ohno S, Hirano S, Tateya I, Kanemaru S-ichi, Umeda H, Suehiro A, et al. Atelocollagen sponge as a stem cell implantation scaffold for the treatment of scarred vocal folds. The Annals of otology, rhinology, and laryngology. 2009 Nov;118(11):805-10. [ Links ]
48. Akita S, Tanaka K, Hirano A. Lower extremity reconstruction after necrotising fasciitis and necrotic skin lesions using a porcine-derived skin substitute. J Plast Reconstr Aesthet Surg. 2006 Jan;59(7):759-63. [ Links ]
49. Kumar RJ, Kimble RM, Boots R, Pegg SP. Treatment of partial-thickness burns: a prospective, randomized trial using Transcyte. ANZ J Surg. 2004 Aug;74(8):622-6. [ Links ]
50. Greenwood JE, Clausen J, Kavanagh S. Experience with biobrane: uses and caveats for success. Eplasty. 2009 Jan;9:e25. [ Links ]
51. Gravante G, Sorge R, Merone A, Tamisani AM, Di Lonardo A, Scalise A, et al. Hyalomatrix PA in burn care practice: results from a national retrospective survey, 2005 to 2006. Ann Plast Surg. 2010 Jan;64(1):69-79. [ Links ]
52. Edmonds M. Apligraf in the treatment of neuropathic diabetic foot ulcers. Int J Low Extrem Wounds. 2009 Mar;8(1):11-8. [ Links ]
53. Windsor ML, Eisenberg M, Gordon-Thomson C, Moore GPM. A novel model of wound healing in the SCID mouse using a cultured human skin substitute. Australas J Dermatol. 2009 Feb;50(1):29-35. [ Links ]
54. Xiao YL, Riesle J, Van Blitterswijk CA. Static and dynamic fibroblast seeding and cultivation in porous PEO/PBT scaffolds. J Mater Sci Mater Med. 1999 Dec;10(12):773-7. [ Links ]
55. Welch MP, Odland GF, Clark RA. Temporal relationships of F-actin bundle formation, collagen and fibronectin matrix assembly, and fibronectin receptor expression to wound contraction. J Cell Biol. 1990 Jan;110(1):133-45. [ Links ]
56. Kaiser HW, Stark GB, Kopp J, Balcerkiewicz A, Spilker G, Kreysel HW. Cultured autologous keratinocytes in fibrin glue suspension, exclusively and combined with STS-allograft (preliminary clinical and histological report of a new technique). Burns. 1994 Feb;20(1):23-9. [ Links ]
57. Ahmed TAE, Dare EV, Hincke M. Fibrin: a versatile scaffold for tissue engineering applications. Tissue Eng Part B Rev. 2008 Jun;14(2):199-215. [ Links ]
58. Geer DJ, Swartz DD, Andreadis ST. Fibrin promotes migration in a three-dimensional in vitro model of wound regeneration. Tissue Eng. 2002 Oct;8(5):787-98. [ Links ]
59. Khor HL, Ng KW, Htay AS, Schantz J-T, Teoh SH, Hutmacher DW. Preliminary study of a polycaprolactone membrane utilized as epidermal substrate. J Mater Sci Mater Med. 2003 Feb;14(2):113-20. [ Links ]
60. Llames S, García E, García V, del Río M, Larcher F, Jorcano JL, et al. Clinical results of an autologous engineered skin. Cell Tissue Bank. 2006 Jan;7(1):47-53. [ Links ]
61. MacNeil S. Progress and opportunities for tissue-engineered skin. Nature. 2007 Feb 22;445(7130):874-80. [ Links ]
62. Ponec M, El Ghalbzouri A, Dijkman R, Kempenaar J, Van der Pluijm G, Koolwijk P. Endothelial network formed with human dermal microvascular endothelial cells in autologous multicellular skin substitutes. Angiogenesis. 2004 Jan;7(4):295-305. [ Links ]
63. Blanpain C, Lowry WE, Geoghegan A, Polak L, Fuchs E. Self-renewal, multipotency, and the existence of two cell populations within an epithelial stem cell niche. Cell. 2004 Sep 3;118(5):635-48. [ Links ]
64. Yoshikawa T, Mitsuno H, Nonaka I, Sen Y, Kawanishi K, Inada Y, et al. Wound therapy by marrow mesenchymal cell transplantation. Plast Reconstr Surg. 2008 Mar;121(3):860-77. [ Links ]
65. Brewster L, Brey EM, Addis M, Xue L, Husak V, Ellinger J, et al. Improving endothelial healing with novel chimeric mitogens. Am J Surg. 2006 Nov;192(5):589-93. [ Links ]
66. Auger FA, Lacroix D, Germain L. Skin substitutes and wound healing. Skin Pharmacol Physiol. 2009 Jan;22(2):94-102. [ Links ]
67. Garcia Y, Wilkins B, Collighan RJ, Griffin M, Pandit A. Towards development of a dermal rudiment for enhanced wound healing response. Biomaterials. 2008 Mar;29(7):857-68. [ Links ]
68. Ma PX. Biomimetic materials for tissue engineering. Adv Drug Deliv Rev. 2008 Jan 14;60(2):184-98. [ Links ]
69. Metcalfe AD, Ferguson MWJ. Tissue engineering of replacement skin: the crossroads of biomaterials, wound healing, embryonic development, stem cells and regeneration. J R Soc Interface. 2007 Jun 22;4(14):413-37. [ Links ]
70. Vélez-L LM, Moreno JA. Balance de la campaña de prevención de accidentes por pólvora en Antioquia 1986- 2005: aún son muchas las personas quemadas. BIA. 2005 Nov;1-5. [ Links ]
71. Franco MAH, Gonzáles NCJ, Díaz MEM, Pardo SV, Ospina S. Epidemiological and clinical profile of burn victims Hospital Universitario San Vicente de Paúl, Medellín, 1994-2004. Burns : journal of the International Society for Burn Injuries. 2006 Dec;32(8):1044-51. [ Links ]
72. Arvelo F. Ingeniería de tejidos y producción de piel humana in vitro. Invest. clín. 2007;48(3):367-75. [ Links ]
73. Secretaría Seccional de Salud y Protección Social de Antioquia. Indicadores básicos 2008 [Internet]. 2011 (cited 2010 May 19);:2. Available from: http://www.dssa.gov.co/index.php/estadisticas/indicadores-basicos-antioquia [ Links ]
74. Gordois A, Scuffham P, Shearer A, Oglesby A, Tobian JA. The health care costs of diabetic peripheral neuropathy in the US. Diabetes Care. 2003 Jun;26(6):1790-5. [ Links ]
75. Langer A, Rogowski W. Systematic review of economic evaluations of human cell-derived wound care products for the treatment of venous leg and diabetic foot ulcers. BMC Health Serv Res. 2009 Jan;9:115. [ Links ]
76. Meaume S, Gemmen E. Cost-effectiveness of wound management in France: pressure ulcers and venous leg ulcers. J Wound Care. 2002 Jun;11(6):219-24. [ Links ]
77. Sibbald RG, Torrance G, Hux M, Attard C, Milkovich N. Cost-effectiveness of becaplermin for nonhealing neuropathic diabetic foot ulcers. Ostomy Wound Manage. 2003 Nov;49(11):76-84. [ Links ]
78. Secretaría Seccional de Salud y Protección Social de Antioquia. Indicadores básicos 2008 [Internet]. Secretaría Seccional de Salud y Protección Social de Antioquia. 2009 (cited 2010 May 19);:1. Available from: http://www.dssa.gov.co/index.php/estadisticas/indicadores-basicos-antioquia [ Links ]
79. Arango-Rodríguez ML, Chamorro CI, Restrepo LM, Correa LA, Henao J. Características histológicas de piel cultivada in vitro. Rev Argent Dermatol. 2009;90:190-200. [ Links ]
80. Escobar-Franco M, Henao Pérez J, Wolff M, Estrada Mira S, Restrepo-Múnera LM. Tratamiento de las úlceras crónicas en los miembros inferiores con un equivalente cutáneo autólogo y desbridación con larvas de Lucilia sp. (Diptera: Calliphoridae). Reporte de un caso. Iatreia. 2007;20(4):397-406. [ Links ]
81. Arango M, Chamorro C, Cohen-Haguenauer O, Rojas M, Restrepo LM. Human skin keratinocytes modified by a Friend-derived retroviral vector: a functional approach. Dermatol Online J. 2005 Jan;11(2):2. [ Links ]
82. Becerra N, Restrepo LM, López BL. Synthesis and characterization of a biocompatible copolymer to be used as cell culture support. Macromolecular Symposia. 2007 Nov;258(1):30-7. [ Links ]