Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Iatreia
Print version ISSN 0121-0793
Iatreia vol.27 no.2 Medellín Apr./June 2014
PRESENTACIÓN DE CASOS
Síndrome de Marfan, mutaciones nuevas y modificadoras del gen FBN1
Marfan syndrome: new mutations of the FBN1 gene
Juan Muñoz Sandoval1; Wilmar Saldarriaga-Gil, M.D, M.Sc.2; Carolina Isaza de Lourido, M.D., M.Sc3
1 Médico Interno, Grupo de Malformaciones Congénitas Perinatales y Dismorfología (MACOS), Escuela de Medicina, Facultad de Salud, Universidad del Valle, Cali, Colombia.
2 Ginecoobstetra. Ciencias Básicas Médicas, énfasis en Embriología y Genética. Grupo de Malformaciones Congénitas Perinatales y Dismorfología (MACOS), Universidad del Valle. Profesor Asociado, departamentos de Morfología y Ginecología y Obstetricia, Facultad de Salud, Universidad del Valle. Ginecólogo, Hospital Universitario del Valle. Director, Programa de Medicina y Cirugía, Universidad del Valle, Cali, Colombia.
3 Profesora Titular, Departamento de Morfología, Facultad de Salud, Universidad del Valle. Vicerrectora de Investigaciones, Universidad del Valle. Grupo de Malformaciones Congénitas Perinatales y Dismorfología (MACOS), Universidad del Valle, Cali, Colombia. wilmar.saldarriaga@correounivalle.edu.co
Recibido: julio 02 de 2013
Aceptado: 04 octubre de 2013
RESUMEN
El síndrome de Marfan (SM) es un trastorno sistémico causado por mutaciones en la proteína de la matriz extracelular fibrilina 1 (FBN1). Con un patrón de herencia autosómico dominante, los pacientes se caracterizan por presentar compromiso ocular, cardiovascular y esquelético dentro de un espectro clínico variable. Se ha sugerido que la variabilidad fenotípica intrafamiliar e interfamiliar característica del síndrome ocurre por la asociación de otras mutaciones denominadas modificadoras (driver mutations). Si bien hay claridad acerca de la causalidad genética clásica de la enfermedad, las mutaciones modificadoras descritas recientemente aún no están bien dilucidadas. Se presenta un caso de SM con una mutación no descrita previamente en el gen de la fibrilina 1; se aplica la nosología de Ghent revisada y se analiza el papel de esta mutación nueva y de las mutaciones modificadoras en la génesis de la enfermedad.
PALABRAS CLAVE
Codón sin Sentido, Fibrilina, Mutaciones Modificadoras, Nosología de Ghent, Síndrome de Marfan
SUMMARY
Marfan syndrome (MS) is a systemic disorder caused by mutations in the extracellular matrix protein fibrillin 1 (FBN1). With a dominant autosomal pattern, MS patients are characterized by ocular, cardiovascular and skeletal involvement, all within a variable clinical spectrum. It has been suggested that the intrafamilial and interfamilial phenotypic variability, characteristic of the syndrome, occurs by the association of other mutations called driver mutations. Even though there is a clear genetic causation, the recently described driver mutations are not yet fully elucidated. We present a MS case with a mutation not previously described in the fibrilin 1 gene, applying the revised Ghent nosology and analyzing the role of this new mutation and of the driver mutations in the genesis of the disease.
KEY WORDS
Codon Nonsense, Driver Mutations, FBN1, Ghent Nosology, Marfan Syndrome
INTRODUCCIÓN
El síndrome de Marfan (SM) es un trastorno sistémico del tejido conectivo causado por mutaciones en la proteína de la matriz extracelular fibrilina 1 (FBN1), con un patrón de herencia autosómico dominante y una penetrancia cercana al 100%. Alrededor del 90% de las mutaciones documentadas son de tipo único y afectan a un individuo o familia; el 20% de los individuos no heredan las mutaciones, por lo que estas se interpretan como nuevas (1). Se ha sugerido que la variabilidad fenotípica intrafamiliar e interfamiliar típica del síndrome ocurre por la asociación de otras mutaciones denominadas modificadoras (driver mutations) (2).
La incidencia calculada del SM es de 2 a 3 casos por cada 10.000 individuos; por los hallazgos fenotípicos notorios es uno de los síndromes genéticos que se sospechan con mayor frecuencia; usualmente existe compromiso ocular, cardiovascular y esquelético (3). El diagnóstico de SM se basa en una serie de criterios clínicos y genéticos denominados nosología de Ghent (tabla 1), que fue actualizada en el 2009 (4).
En el presente artículo se reporta un caso de SM con una mutación nueva no descrita previamente en la literatura y se hace un análisis sustentado en conceptos recientes sobre las mutaciones modificadoras y los criterios revisados de la nosología de Ghent. Estos conceptos son importantes para el enfoque diagnóstico y de consejería genética que se propone en la actualidad a los pacientes con síndrome de Marfan, además de la relevancia en el conocimiento y el aporte de nuevas variantes génicas en el fortalecimiento de las bases de datos genéticos del SM.
DESCRIPCIÓN DEL CASO
Paciente de sexo masculino, edad 29 años, talla 199 cm, con los antecedentes de valvulopatía mitral que requirió corrección quirúrgica, miopía y corrección de pie equinovaro bilateral. Se aplicaron los criterios de Ghent revisados siguiendo el protocolo de evaluación diagnóstica que se describe en la tabla 1. Se encontraron:
- Antecedente familiar sugestivo de SM; muerte materna temprana (42 años) secundaria a disección aórtica con fenotipo similar al del probando (figura 1).
- Al evaluar el puntaje propuesto para el compromiso sistémico (tabla 2) se obtuvieron 8 puntos con los siguientes resultados al examen fisico:
- Signos del pulgar (Steinberg) y de la muñeca (Walker-Murdoch) positivos: 3 puntos (figura 2).
- Pectum excavatum: 1 punto
- Retropié en valgo: aunque había pie plano bilateral, el hallazgo de retropié en valgo no era evaluable por el antecedente de cirugía correctiva de pie equinovaro (figura 3).
- Segmento superior/segmento inferior (SS/SI) (blancos <0,85-negros <0,78) y envergadura del radio >1,05: negativos (0,85 cm y 1,01cm, respectivamente).
- Hallazgos faciales positivos: dolicocefalia (índice cefálico 2,65 cm), enoftalmos, retrognatia e hipoplasia malar presentes: 1 punto.
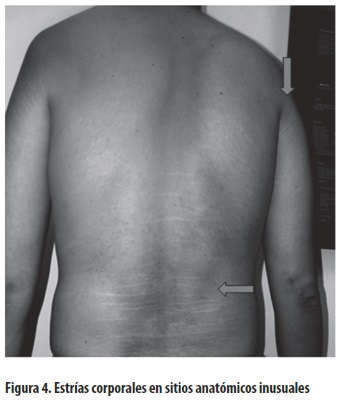
- Estrías presentes: 1 punto (figura 4).
- Miopía mayor de 3 dioptrías positiva: 1 punto.
- Antecedente de prolapso de válvula mitral positivo: 1 punto.
- Se usó ADN genómico del paciente para amplificación por PCR de los 65 exones contenidos en la región codificante del gen FBN1. Los productos se analizaron para mutaciones mediante secuenciación bidireccional usando métodos automatizados con dideoxinucleótidos fluorescentes. Se identificó un cambio heterocigoto en el nucleótido 6684T>A en el gen FBN1. Este cambio nucleotídico produce a su vez el cambio de una tirosina por un codón de parada prematura en la posición 2228 (Y2228X), mutación catalogada como sin sentido (nonsense mutation).
Se catalogó al paciente dentro de la franja diagnóstica de SM número 6 (historia familiar de SM más compromiso sistémico) (tabla 2). El paciente no cumple con el fenotipo clásico de los síndromes Shprintzen Goldberg (SSG), Loeys-Dietz (SLD), Ehrles-Danlos IV, ni de otras entidades menos comunes que hacen parte de los diagnósticos diferenciales para tener en cuenta para SM (tabla 3).
No se planteó la necesidad de hacer pruebas moleculares adicionales para otros genes (TGFBR1/2, COL3A1) ni biopsia de colágeno, como lo sugiere la nosología, pues los hallazgos clínicos del paciente, sugestivos de SM, son compatibles con la mutación patológica presentada (correlación genotipo/fenotipo para SM).
DISCUSIÓN
El síndrome de Marfan (SM; OMIM 154700) es un trastorno sistémico del tejido conectivo, de tipo autosómico dominante, causado por mutaciones en la proteína de la matriz extracelular fibrilina 1 (FBN1). Esta enfermedad afecta principalmente los sistemas cardiovascular, ocular y esquelético. Con una frecuencia estimada de 2 a 3 casos por cada 10.000 individuos y sin diferenciación de sexo, cerca del 90% de las mutaciones documentadas son de tipo único y afectan a un individuo o familia; el 20% de los pacientes no heredan las mutaciones, por lo que estas se interpretan como nuevas.
La fibrilina 1 es una glicoproteína que pesa 350 kilodalton, predominante en la matriz extracelular, codificada solo por un gen (FBN1) constituido por 65 exones, localizado en el cromosoma 15q21.1. Es un componente importante de los tejidos conectivos elásticos y no elásticos, y es la principal proteína de un grupo de microfibrillas del tejido conectivo que son esenciales para una normal fibrilogénesis elástica (ejemplo: tejido aórtico). El riesgo aumentado de dilatación, disección y ruptura aórticas es el responsable de la mortalidad aumentada. Al igual que las demás características clínicas (prolapso de válvula mitral, miopía, etc.) el fenotipo aparece y se desarrolla con la edad, pues usualmente es la consecuencia de una resistencia alterada de los tejidos (1).
El diagnóstico de SM se basa en una serie de criterios clínicos y genéticos denominados nosología de Ghent (tabla 1), que fue actualizada en el 2009 (4) y en la que se otorga mayor peso a tres componentes: 1) hallazgos clínicos de aneurisma/disección aórtica y ectopia del lente ocular; 2) pruebas genéticas del FBN1 y otros genes como TGFBR1 y 2; 3) un énfasis diagnóstico del SM hacia una diferenciación en la que se incluyen entidades como el SLD, SSG, el síndrome de aneurisma y disección aórtica torácica familiar, entre otros. Se ha observado una relación entre el tipo de mutación del gen de la fibrilina 1 y el mecanismo de enfermedad (haplo-insuficiencia frente a dominancia negativa), así como una gama de correlaciones genotipo/ fenotipo. Recientemente se han propuesto como preponderantes en la progresión de la enfermedad aórtica en modelos murinos otros factores como el de crecimiento transformante beta (TGF-β) y algunas proteasas (1). Sin embargo, a pesar de estos avances en la patogénesis del SM, la notable variabilidad fenotípica intrafamiliar e interfamiliar continúa siendo uno de los retos principales de esta entidad (16). Se considera que las mutaciones en el gen FBN1 están asociadas con un continuum fenotípico; en algunos casos se pueden observar recién nacidos con rasgos leves del síndrome que pueden pasar inadvertidos al examen físico, mientras que en otros se presentan formas neonatales graves y de rápida progresión multiorgánica (17).
Dado el impacto del pronóstico y del manejo, se ha sugerido la importancia del reconocimiento de ciertas mutaciones modificadoras que posiblemente expliquen la variabilidad clínica observada incluso en individuos que presentan una mutación en común del gen FBN1. Estas variantes definidas como mutaciones adicionales del FBN1 translocadas parecen acompañar a las mutaciones causales clásicas del SM; se ha sugerido que las mutaciones modificadoras, dentro de un modelo de cosegregación familiar, cambian la gravedad del fenotipo de los individuos con SM en relación con sus parientes afectados no portadores de las mismas. También existen casos en que las mutaciones modificadoras atenúan la expresión fenotípica a tal grado que estos pacientes no cumplirían los criterios clínicos. Lo anterior ha sido reportado por Van Dyjk y colaboradores (2) quienes demostraron en dos familias de casos índices distintos la presencia asociada de estas mutaciones, y las propusieron como posible mecanismo de variabilidad del SM; por otra parte, los hallazgos de Díaz de Bustamante y colaboradores (16) han reforzado la hipótesis propuesta al evidenciar en parientes ''sanos'' (individuos asintomáticos) de pacientes con SM variantes que se asocian a un fenotipo más grave cuando acompañan una mutación del síndrome.
Se han detectado más de 1.700 mutaciones en el gen FBN1 relacionadas con la enfermedad (18) Actualmente se consideran varias mutaciones particulares del FBN1 como de potencial patogénico para SM según los parámetros propuestos en la nosología (tabla 4). Sin embargo, existen mutaciones que no tienen representación fenotípica (variantes de significancia incierta).
El análisis del caso de este paciente con diagnóstico de SM, en el que se encontró una mutación sin sentido (nonsense) no reportada previamente (bases de datos NCBI polimorfismo nucleótido único y John Welsh Cardiovascular Diagnostic Laboratory, Houston, Texas) que implica un codón de parada prematura en la posición 2228, sugeriría dos posibilidades para esta mutación nueva del FBN1: 1) mutación privada única del gen FBN1 que podría presentar cosegregación familiar, por el antecedente materno sugestivo de SM, aunque sin confirmación molecular, lo cual indicaría un hallazgo genético causal de SM en el probando; 2) mutación de novo, dado que la descripción de las características de la madre del probando es sugestiva de SM pero no hay confirmación clínica ni molecular, siendo esta mutación de novo patogénica (mutación sin sentido), según la nosología de Ghent.
A pesar de la dificultad para secuenciar el gen FBN1 en familiares del probando como la madre y otros parientes, con el fin de determinar si la mutación fue heredada o de novo, se puede concluir que la mutación identificada en el FBN1 es patogénica y compatible con las características clínicas del SM en el paciente (correlación genotipo/fenotipo).
Teniendo en cuenta lo anterior y dada la creciente importancia que se les viene dando a las mutaciones modificadoras, el análisis de este paciente y de casos similares podría implicar, una vez confirmado el diagnóstico de SM mediante la aplicación sistemática de la nosología, la realización del estudio molecular a los familiares del probando en primer grado de consanguinidad, aunque no tengan las características fenotípicas sugestivas, e independientemente del tipo de mutación encontrada (heredada o de novo, ya reportada en la literatura o nueva como en el caso aquí presentado).
Este enfoque reconocería que las mutaciones clásicas (patológicas) del FBN1 pueden también presentarse en parientes del caso índice que pasarían inadvertidos dado el chance de copresencia o no de algún tipo de mutación modificadora (no enmarcada dentro de los criterios Ghent) que enmascare su cuadro clínico y que de paso catalogue inicialmente de forma errónea un caso índice como de novo ante la no evidencia clínica de familiares afectados.
Esto abre la posibilidad de identificar qué tipo de polimorfismos define la gravedad del fenotipo dentro de un grupo de individuos relacionados genéticamente, ampliando de esta forma la consejería médica a los parientes del probando que sean asintomáticos o subclínicos, pero cuya progenie puede encontrarse en riesgo de heredar la condición con alguna mutación modificadora de mal pronóstico (2,16).
Los profesionales tratantes deben tener en cuenta que una mutación provee información pronóstica incompleta como lo demuestra la variabilidad intrafamiliar. El reto científico debe por lo tanto encaminarse a identificar los modificadores genéticos que lleven a su vez a la identificación de factores pronósticos. Si bien la secuenciación de rutina de toda la región codificante del gen FBN1 puede tener un costo alto, la mayor disponibilidad de los recursos técnicos para análisis genético y la importancia de su aplicación para la consejería genética deben facilitar su uso clínico.
Es posible en el SM la ausencia de una mutación en el gen FBN1 a pesar de un análisis completo. Sin embargo, en los estudios publicados la sensibilidad del análisis genético ha variado entre el 76% y el 93%; el mejor predictor para identificar una mutación es el compromiso de al menos tres sistemas, incluyendo un criterio mayor de la nosología (1).
CONCLUSIÓN
Se presenta un caso de síndrome de Marfan al que se le aplicó la nosología de Ghent revisada. Se documentó además una mutación nueva no reportada previamente en la literatura y se analizó en el contexto del conocimiento actual sobre la enfermedad. En el diagnóstico de pacientes con SM se acepta mundialmente la prueba molecular y es un criterio de inclusión; aunque la causalidad genética del síndrome está bien establecida, aún se debe evaluar ampliamente las mutaciones modificadoras descritas recientemente y determinar su rol en la enfermedad. Sin embargo, los análisis de casos con estas mutaciones parecen sugerir de manera preliminar que familiares en primer grado de pacientes con SM y sin hallazgos fenotípicos relevantes se deberían hacer pruebas moleculares diagnósticas para establecer según el caso una consejería genética.
CONSIDERACIONES ÉTICAS
Los datos de la historia clínica y las fotografías se tomaron y se publican previo consentimiento informado escrito, firmado por el paciente. Los autores declaran que no hay conflicto de intereses en el presente manuscrito.
REFERENCIAS BIBLIOGRÁFICAS
1. Jondeau G, Michel JB, Boileau C. The translational science of Marfan syndrome. Heart. 2011 Aug;97(15):1206–14. [ Links ]
2. Van Dijk FS, Hamel BC, Hilhorst-Hofstee Y, Mulder BJM, Timmermans J, Pals G, et al. Compound-heterozygous Marfan syndrome. Eur J Med Genet. 52(1):1–5. [ Links ]
3. Judge DP, Dietz HC. Marfan's syndrome. Lancet. 2005 Dec 3;366(9501):1965–76. [ Links ]
4. Loeys BL, Dietz HC, Braverman AC, Callewaert BL, De Backer J, Devereux RB, et al. The revised Ghent nosology for the Marfan syndrome. J Med Genet. 2010 Jul;47(7):476–85. [ Links ]
5. Bennett RL, French KS, Resta RG, Doyle DL. Standardized human pedigree nomenclature: update and assessment of the recommendations of the National Society of Genetic Counselors. J Genet Couns. 2008 Oct;17(5):424–33. [ Links ]
6. Olivar Roldán J, Fernández Martínez A, Díaz Guardiola P, Martínez Sancho E, Díaz Gómez J, Gómez Candela C. [Clinical management of homocystinuria: case report and review of the literature]. Nutr Hosp. 27(6):2133–8. [ Links ]
7. Snead MP, Yates JR. Clinical and Molecular genetics of Stickler syndrome. J Med Genet. 1999 May;36(5):353–9. [ Links ]
8. Van Buggenhout G, Fryns J-P. Lujan-Fryns syndrome (mental retardation, X-linked, marfanoid habitus). Orphanet J Rare Dis. 2006 Jan;1:26. [ Links ]
9. Grau JB, Pirelli L, Yu P-J, Galloway AC, Ostrer H. The genetics of mitral valve prolapse. Clin Genet. 2007 Oct;72(4):288–95. [ Links ]
10. Kivitie-Kallio S, Norio R. Cohen syndrome: essential features, natural history, and heterogeneity. Am J Med Genet. 2001 Aug 1;102(2):125–35. [ Links ]
11. Nishi Y, Hamamoto K, Kajiyama M, Kawamura I. The Perrault syndrome: clinical report and review. Am J Med Genet. 1988 Nov;31(3):623–9. [ Links ]
12. Neri G, Gurrieri F, Zanni G, Lin A. Clinical and molecular aspects of the Simpso n-Golabi- Behmel syndrome. Am J Med Genet. 1998 Oct 2;79(4):279–83. [ Links ]
13. Pagon R, Adam M, Bird T, Dolan C, Fong C, Smith R, et al., editors. GeneReviews. Seattle: University of Washington; 2013. [ Links ]
14. Tamminga P, Jennekens FG, Barth PG, Fleury P, van den Berg H, Oorthuys JW. An infant with Marfanoid phenotype and congenital contractures associated with ocular and cardiovascular anomalies, cerebral white matter hypoplasia and spinal axonopathy. Eur J Pediatr. 1985 Jan;143(3):228–31. [ Links ]
15. Agrawal A, Agrawal R. Warkany syndrome: a rare case report. Case Rep Pediatr. 2011 Jan;2011:437101. [ Links ]
16. Díaz de Bustamante A, Ruiz-Casares E, Darnaude MT, Perucho T, Martínez-Quesada G. Phenotypic variability in Marfan syndrome in a family with a novel nonsense FBN1 gene mutation. Rev Esp Cardiol. (Engl. Ed). 2012 Apr;65(4):380–1. [ Links ]
17. Song Y-H, Kim G-H, Yoo H-W, Kim J-B. Novel de novo nonsense mutation of FBN1 gene in a patient with Marfan syndrome. J Genet. 2012 Aug;91(2):233–5. [ Links ]
18. Barriales-Villa R, García-Giustiniani D, Monserrat L. Genética del síndrome de Marfan. Cardiocore. 2011;46(3):101-4. [ Links ]