Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Iatreia
Print version ISSN 0121-0793
Iatreia vol.28 no.2 Medellín Apr./June 2015
https://doi.org/10.17533/udea.iatreia.v28n2a12
ACTUALIZACIÓN CRÍTICA
DOI 10.17533/udea.iatreia.v28n2a12
Ronda clínica y epidemiológica: club de revistas
Clinical and epidemiological round: journals club
Ronda clínica e epidemiológica: clube de revistas
María Fernanda Tibaduiza García1; César Caraballo Cordovez1; Carolina Hincapié Osorno1; Daniela de Jesús Garcés Rodríguez1; Fabián Jaimes Barragán2
1 Estudiante, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
2 Profesor Titular, Grupo Académico de Epidemiología Clínica (GRAEPIC), Departamento de Medicina Interna, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia. Investigador, Unidad de Investigaciones, Hospital Pablo Tobón Uribe, Medellín, Colombia. fabian.jaimes@udea.edu.co
Recibido: enero 23 de 2015
Aceptado: febrero 5 de 2015
RESUMEN
En esta edición de nuestra ronda clínica y epidemiológica analizamos cuatro artículos relevantes para la práctica clínica: Etminan y colaboradores estudian los efectos adversos de algunos antimicrobianos buscando una posible asociación entre el uso de fluoroquinolonas orales y el riesgo de neuropatía periférica (1). Fralick y colaboradores estudian el riesgo de muerte súbita tras el consumo de trimetoprim-sulfametoxazol (2). Bakker y colaboradores hacen una interesante contribución sobre la necesidad de usar sonda nasoyeyunal en pacientes con pancreatitis aguda (3). Por último, Kanegaye y colaboradores buscan la mejor prueba diagnóstica para las infecciones urinarias en menores de 4 años (4).
PALABRAS CLAVE
Enfermedades del Sistema Nervioso Periférico, Fluoroquinolonas, Muerte Súbita, Pancreatitis, Sulfametoxazol, Trimetoprim, Urianálisis
SUMMARY
In this edition of the clinical and epidemiological round, we analyze four articles relevant for clinical practice, namely: the adverse effects of some antimicrobials are studied by Etminan et al., looking for a possible association between the use of oral fluoroquinolones and the risk of peripheral neuropathy (1). Fralick et al., studied the risk of sudden death after the use of trimethoprim-sulfamethoxazole (2). Bakker and collaborators make an interesting contribution about the need of nasoyeyunal catheter in patients suffering from acute pancreatitis (3). Finally, Kanegaye et al., look for the best diagnostic test for urinary infections in infants (4).
KEY WORDS
Fluoroquinolones, Pancreatitis, Peripheral Nervous System Diseases, Sulfamethoxazole, Sudden Death, Trimethoprim, Urinalysis
RESUMO
Nesta edição de nossa ronda clínica e epidemiológica analisamos quatro artigos relevantes para a prática clínica: Etminan e colaboradores estudam os efeitos adversos de alguns antimicrobianos procurando uma possível associação entre o uso de fluoroquinolonas orais e o risco de neuropatia periférica (1). Fralick e colaboradores estudam o risco de morte súbita depois do consumo de trimetoprim-sulfametoxazol (2). Bakker e colaboradores fazem uma interessante contribuição sobre a necessidade de usar sonda nasoyeyunal em pacientes com pancreatites aguda (3). Por último, Kanegaye e colaboradores procuram a melhor prova diagnóstica para as infecções urinárias em menores de 4 anos (4).
PALAVRAS CHAVES
Doenças do Sistema Nervoso Periférico, Fluoroquinolonas, Morte Súbita, Pancreatites, Sulfametoxazol, Trimetoprim, Urianálises
FLUORO QUINOLONAS ASOCIADAS A NEUROPATÍA PERIFÉRICA : UN EFECTO ADVERSO PARA TENER EN CUENTA
Etminan M, Brophy JM, Samii A. Oral fluoroquinolone use and risk of peripheral neuropathy: a pharmacoepidemiologic study. Neurology 2014; 83(14): 1261-3.
Pregunta: ¿el consumo de fluoroquinolonas orales es un factor de riesgo para el desarrollo de neuropatía periférica?
Diseño: estudio de casos y controles anidado en una cohorte de hombres adultos.
Lugar: Estados Unidos.
Participantes: de aproximadamente un millón de hombres entre 40 y 85 años cuya información está en la base de datos de reclamos en salud llamada Life- Link, se escogieron 6.226 casos y 24.904 controles. Los casos se definieron como aquellos con diagnóstico de polineuropatía idiopática, neuropatía periférica o polineuropatía inducida por medicamentos (ICD-9 356.4, 356.8, 357.6, respectivamente). Se excluyeron aquellos con diagnóstico de diabetes mellitus o polineuropatía hereditaria. Los controles se emparejaron por edad (± 1 año), tiempo de seguimiento y fecha de ingreso a la cohorte.
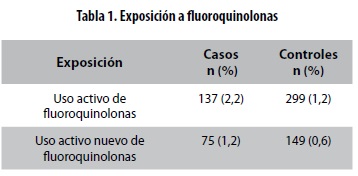
Exposición: consumo de fluoroquinolonas orales en el último año antes de la fecha índice y se consideraron consumidores activos aquellos con prescripción durante los últimos 14 días. (Tabla 1)
Desenlace: diagnóstico de neuropatía periférica no prevalente (de inicio reciente).
Resultados principales: los consumidores activos de fluoroquinolonas tuvieron un riesgo mayor de presentar neuropatía periférica que los controles, incluso después de ajustar por falla renal crónica, falla hepática crónica, neuralgia posherpética, hipotiroidismo y uso de metronidazol o nitrofurantoína (RR = 1,83; IC 95% = 1,49-2,27). Los pacientes con mayor riesgo de presentar neuropatía periférica fueron los consumidores activos nuevos, es decir, quienes no habían consumido fluoroquinolonas anteriormente (RR = 2,07; IC 95% = 1,56-2,74). No hubo diferencias significativas en el riesgo de acuerdo con el tipo de quinolona usada (moxifloxacina, ciprofloxacina o levofloxacina).
Conclusión: los resultados de este estudio demuestran un aumento del riesgo de neuropatía periférica con el consumo de fluoroquinolonas orales.
Comentario: las fluoroquinolonas son un grupo de antibióticos ampliamente usado para tratar infecciones respiratorias, de vías urinarias y gastrointestinales, entre otras. Entre sus efectos adversos más comunes se encuentran alteraciones gastrointestinales como náusea, vómito o diarrea, y del sistema nervioso central como mareo, cefalea o somnolencia. Estos síntomas son transitorios y generalmente no se requiere detener la terapia (5). No obstante, han surgido otras dudas sobre su tolerabilidad y seguridad. En 2013, la FDA (Food and Drug Administration) emitió un comunicado requiriendo incluir como efecto adverso la posibilidad de neuropatía permanente al usar fluoroquinolonas orales o inyectadas. Además, instan a los médicos a explicar detalladamente a los pacientes los síntomas de neuropatía periférica (dolor, parestesia, anestesia, paresia) para detener su uso inmediatamente en caso de presentarlos (6). En 2014, Ali publicó un análisis de los reportes de eventos adversos atribuidos al uso de estos medicamentos en el que se encontró relación con neuropatía periférica en 1% de los casos (7). En este contexto, el estudio actual resalta por su importancia al contribuir a confirmar la asociación entre el uso de fluoroquinolonas y la aparición de neuropatía periférica. El gran número de participantes y la exclusión de aquellos con diagnóstico de diabetes mellitus o neuropatía crónica le da una alta credibilidad a los resultados obtenidos, aunque es necesario reconocer las limitaciones dadas por su naturaleza no experimental y por el hecho de estar circunscrito a hombres. Sin embargo, esta investigación debe confirmar un principio vital de la práctica médica, y es que los médicos deben determinar en cada paciente la verdadera relación riesgo-beneficio de la prescripción de fluoroquinolonas al igual que la de cualquier otro medicamento.
TRIMETOPRIM Y MUERTE SÚBITA : ¿CÓMO Y POR QUÉ?
Fralick M, Macdonald EM, Gomes T, Antoniou T, Hollands S, Mamdani MM, et al. Co-trimoxazole and sudden death in patients receiving inhibitors of renin- angiotensin system: population based study. BMJ 2014;349:g6196.
Pregunta: ¿la prescripción de trimetoprim-sulfametoxazol (TMP-SMX) con inhibidores de la enzima convertidora de angiotensina (IECA) o bloqueadores de los receptores de angiotensina (BRA) está asociada con muerte súbita?
Diseño: estudio de casos y controles anidado en una cohorte de adultos mayores.
Lugar: Ontario, Canadá.
Participantes: se identificó una cohorte de 1.604.542 pacientes mayores de 65 años con prescripción de IECA o BRA entre el 1 de abril de 1994 y el 1 de enero de 2012. Toda la información se obtuvo de las bases de datos de las prescripciones en Ontario, del Instituto Canadiense para la Información de Salud y de los seguros médicos. Se excluyeron aquellos pacientes que recibían simultáneamente medicamentos de las dos familias. En esta cohorte se reportaron 39.879 muertes súbitas, se seleccionaron 1.027 pacientes como casos (muerte súbita y prescripción de antibióticos ambulatorios en la última semana) y se emparejaron con 3.373 controles basados en edad, sexo y presencia o ausencia de diabetes y enfermedad renal.
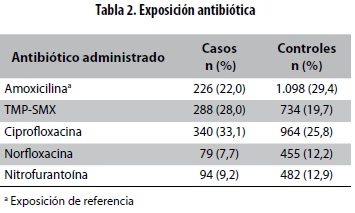
Exposición (factor de riesgo): prescripción de TMPSMX, ciprofloxacina, norfloxacina o nitrofurantoína. La amoxicilina se estableció como exposición de referencia (tabla 2) debido a que no es un factor de riesgo independiente para hiperkalemia y no está asociada con taquicardia ventricular polimorfa. Se excluyeron los pacientes que habían recibido otros antimicrobianos durante los 15 días previos a la fecha índice.
Desenlaces: muerte súbita dentro de los primeros 7 y 15 días posteriores a la prescripción del antimicrobiano.
Resultado: el TMP-SMX, en comparación con la amoxicilina, aumenta el riesgo de muerte súbita en la primera semana de su formulación (OR = 1,83; IC 95% = 1,50-2,24) y esta asociación persiste después de ajustar por el índice de riesgo de muerte (OR = 1,38; IC 95% = 1,09-1,76). La ciprofloxacina mostró un aumento menor en el riesgo ajustado (OR = 1,29; IC 95% = 1,03-1,62) y no se encontró riesgo con la norfloxacina (OR = 0,74, IC 95% = 0,53-1,02) ni con la nitrofurantoína (OR = 0,64; IC 95% = 0,46-0,88). En el análisis secundario para muerte súbita dentro de 14 días, el riesgo ajustado del TMP-SMX en comparación con la amoxicilina también fue mayor (OR = 1,54; IC 95% = 1,29-1,84).
Conclusión: el TMP-SMX se asoció con un aumento del riesgo de muerte súbita en pacientes mayores de 65 años que reciben IECA o BRA.
Comentario: desde la década de los noventa se reconocen casos de hiperkalemia asociada al consumo de TMP, mecanismo investigado por Velásquez y colaboradores quienes describieron que el TMP comparte características estructurales y farmacológicas con la amilorida, al bloquear los canales de sodio epiteliales en la nefrona distal y disminuir la excreción renal de potasio (8). Otros trabajos han ido en la misma dirección: Alappan y asociados describieron en un estudio de casos y controles que la concentración de potasio sérico aumentaba de 4,30 ± 0,36 mmol/L a 4,66 ± 0,45 mmol/L tras 5 días de tratamiento en comparación con el grupo control (9), y el de Marinella quien, además de describir este aumento del riesgo en pacientes ancianos con creatinina sérica normal, documentó la posibilidad de que dicho aumento fuera potenciado por el consumo de IECA (10). Los mismos autores del presente estudio han encontrado que en pacientes hospitalizados y en tratamiento con TMP-SMX más IECA o BRA hay un aumento del riesgo de hiperkalemia, con un OR ajustado de 6,7 (IC 95% = 4,5-10,0) (11), mientras que en pacientes tratados con espironolactona y TMP-SMX la admisión hospitalaria por hiperkalemia aumenta (OR = 11,0; IC 95% = 6,8-17,8), presuntamente por una reducción de la kaliuresis de un 40% (12). Todos los anteriores hallazgos y esta misma investigación, no obstante, surgen de estudios observacionales cuya interpretación requiere cautela por la posibilidad de confusión residual y las limitaciones potenciales en la calidad de los datos. La creciente evidencia sobre la relación del TMPSMX con el riesgo de hiperkalemia y muerte súbita debe ser complementada con estudios que permitan determinar aspectos como el efecto dosis/respuesta del antimicrobiano en distintas infecciones y las posibles interacciones con otros medicamentos diferentes de los estudiados. Igualmente, puede ser válido considerar la necesidad de medir el potasio sérico previo al tratamiento con TMP en pacientes con diabetes, enfermedad renal, disfunción ventricular o edad muy avanzada, quienes tienen mayor riesgo de hiperkalemia asociada con medicamentos que actúan sobre el sistema renina-angiotensina-aldosterona (2).
PANCREATITIS AGUDA : ¿CUÁNDO Y CÓMO REINICIAR LA VÍA ORAL?
Bakker OJ, van Brunschot S, van Santvoort HC, Besselink MG, Bollen TL, Boermeester MA, et al. Early versus on-demand nasoenteric tube feeding in acute pancreatitis. N Engl J Med 2014; 371(21):1983-93.
Pregunta: ¿en pacientes con pancreatitis aguda grave la nutrición por sonda nasoyeyunal en las primeras 24 horas disminuye la mortalidad comparada con la nutrición oral iniciada a las 72 horas?
Diseño: ensayo clínico.
Asignación: aleatoria.
Cegamiento: no se cegó a los médicos tratantes ni a los pacientes, pero los médicos encargados de determinar los desenlaces, un comité de adjudicación compuesto por cuatro cirujanos de páncreas y un gastroenterólogo, no conocían a qué tratamiento había sido asignado el paciente.
Período de seguimiento: 6 meses.
Lugar: 19 centros hospitalarios situados en los Países Bajos.
Pacientes: entre agosto del 2008 y junio del 2012 se incluyeron 205 pacientes mayores de 18 años con diagnóstico de pancreatitis aguda definida con al menos dos de tres criterios: 1) dolor epigástrico, 2) lipasa o amilasa en sangre tres veces mayor que el valor de referencia, 3) hallazgos tomográficos de pancreatitis, y con criterios de gravedad definidos como puntaje Imrie ≥ 3, puntaje APACHE II ≥ 8 o proteína C reactiva por encima de 15 mg/dL dentro de las primeras 24 horas en el hospital. Se excluyeron aquellos con antecedente de pancreatitis aguda o crónica, síntomas por más de 96 horas, pancreatitis aguda asociada con malignidad, diagnóstico de pancreatitis aguda durante cirugía por abdomen agudo, pancreatitis posterior a colangiopancreatografía retrógrada endoscópica (CPRE), nutrición enteral o parenteral previa, o embarazo.
Intervención: a los 101 pacientes del grupo de nutrición nasoenteral temprana se les insertó una sonda nasoyeyunal con asistencia endoscópica o radiográfica en las primeras 24 horas después de la asignación aleatoria. Inmediatamente se les suministró alimentación por la sonda a razón de 20 mL/hora y gradualmente se fue aumentando la dosis hasta la meta de nutrición completa. A los 104 individuos del grupo control únicamente se les dio soporte hídrico con líquidos endovenosos estándar durante las primeras 72 horas y posterior a esto se inició nutrición por vía oral. A los pacientes que no toleraron la vía oral pasadas las 96 horas se les suministró alimentación por sonda nasoenteral.
Desenlace primario: infección mayor, definida como necrosis pancreática infectada, bacteriemia o neumonía; o muerte durante los 6 meses de seguimiento.
Desenlaces secundarios: pancreatitis necrosante diagnosticada sobre la base de la tomografía computarizada hecha 5-7 días después del ingreso y desarrollo de insuficiencia orgánica posterior a la asignación aleatoria.
Resultados: el desenlace primario ocurrió en 30 de 101 pacientes (30%) del grupo de nutrición temprana y en 28 de 104 (27%) del grupo control (RR = 1,07; IC 95% = 0,79-1,44). En este último 72 pacientes (69%) toleraron la dieta oral y no requirieron alimentación por sonda. Con respecto a los desenlaces secundarios, se desarrollaron pancreatitis necrosante en el 63% de los pacientes en el grupo de tratamiento temprano y en el 62% de los del grupo control (RR = 1,06; IC 95% = 0,77-1,47) y falla orgánica múltiple en 10% y 8%, respectivamente (RR = 1,14; IC 95% = 0,67-1,95).
Conclusión: en comparación con una dieta oral a las 72 horas, este ensayo no mostró superioridad del inicio temprano de alimentación por sonda nasoentérica, en la reducción de la tasa de infección o muerte en pacientes con pancreatitis aguda y alto riesgo de complicaciones.
Comentario: en el manejo de la pancreatitis aguda se acepta de manera consistente suspender la vía oral, administrar líquidos endovenosos a necesidad y proporcionar analgesia, pero no ha sido claro cuándo y cómo reiniciar la vía oral. Basados en la aparente diferencia en la ocurrencia de infecciones según la forma en que se restituye la vía oral en pancreatitis aguda, se originó la teoría de que las causas de dichas infecciones eran la translocación bacteriana en el intestino, provocada por la disminución de la motilidad intestinal, el sobrecrecimiento bacteriano y el aumento de la permeabilidad de la mucosa (13). Sun y colaboradores publicaron en 2013 un ensayo clínico con 60 pacientes en el que concluyeron que la nutrición enteral temprana, antes de las 48 horas, podría mejorar el pronóstico, pero sin demostrar disminución de la mortalidad (14). Ese mismo año, Wereszczynska-Siemiatkowska y colaboradores en un estudio de cohorte mostraron una asociación entre la nutrición enteral retrasada y la mortalidad (15). En ambos estudios, contrario a la investigación presentada en esta ronda clínica, la nutrición retrasada se iniciaba al día 8 de evolución de la pancreatitis. Recientemente, Oláh y Romics publicaron una revisión de la evidencia actual de nutrición en pancreatitis aguda comparando diversas intervenciones: nutrición enteral versus parenteral, nutrición enteral temprana versus tardía, nutrición por sonda nasogástrica versus nasoyeyunal, entre otras (16). La única conclusión sustentada fue que la administración de nutrición enteral es beneficiosa para el tratamiento de la pancreatitis aguda grave, y que disminuye la mortalidad, las complicaciones infecciosas y la falla multiorgánica. Con respecto al mejor momento de reiniciar la vía oral, la evidencia actual sugiere que su administración podría ocurrir indistintamente dentro de las primeras 96 horas, condicionada según la evolución clínica de cada paciente, la tolerancia a la ingestión y los aspectos prácticos del uso de sondas o dispositivos enterales.
DIFERENTES OPCIONES PARA EL DIAGNÓSTICO DE INFECCIÓN DEL TRACTO URINARIO EN NIÑOS FEBRILES
Kanegaye JT, Jacob JM, Malicki D. Automated urinalysis and urine dipstick in the emergency evaluation of young febrile children. Pediatrics 2014;134(3):523-9.
Pregunta: ¿cuál es el desempeño del uroanálisis automatizado por citometría de flujo y de la tira reactiva de orina, en el diagnóstico de infección del tracto urinario en niños febriles menores de 4 años que consultan por urgencias?
Diseño: estudio observacional prospectivo.
Lugar: servicio de emergencias de un hospital infantil de tercer nivel en San Diego, California.
Pacientes: se estudiaron 342 niños menores de 48 meses, con temperatura mayor de 38 grados o fiebre documentada en el hogar en las primeras 24 horas y sospecha clínica de ITU, atendidos por urgencias entre mayo 15 del 2009 y mayo 15 del 2010. En todos se obtuvieron muestras por cateterismo uretral para uroanálisis por tira reactiva, uroanálisis automatizado por citometría de flujo y urocultivo. Se excluyeron los pacientes que tenían datos de análisis de orina incompletos, que habían recibido terapia antibiótica en las 24 horas previas, los inmunocomprometidos o en riesgo de neutropenia, o que tuvieran condiciones que predispusieran a una colonización bacteriana asintomática.
Mediciones y desenlaces: el uroanálisis con tira reactiva medía la esterasa leucocitaria que reportaba la presencia de esterasa en la orina como negativa, trazas, 1+ (poca), 2+ (moderada), o 3+ (mucha), y los nitritos, como positivos o negativos. El uroanálisis automatizado por citometría de flujo buscaba hacer los recuentos de células blancas y de bacterias por µL de orina. La prueba de referencia fue el urocultivo, que se reportaba positivo cuando presentaba un crecimiento bacteriano mayor de 50.000 UFC/mL. El crecimiento de organismos de la flora normal, el crecimiento mixto o el recuento inferior a 50.000 UFC/ mL se consideraban negativos.
Resultados principales: 42 de los 342 niños (12,3%) tuvieron urocultivo positivo para al menos un microorganismo uropatógeno. La tira reactiva con esterasa leucocitaria de 1+ o más o con nitritos positivos tuvo sensibilidad de 0,95 y especificidad de 0,98 (LR+ = 57,1; IC 95% = 23,9-136,6), LR- = 0,05: IC 95% = 0,01-0,19). El mejor rendimiento diagnóstico para el recuento de células blancas se obtuvo con un valor por encima de 100 células/µL, con sensibilidad de 0,86 y especificidad de 0,98 (LR+ = 42,9; IC 95% = 19,2- 95,5, LR- = 0,15; IC 95% = 0,07-0,31), y el mejor rendimiento del recuento bacteriano automatizado fue con más de 250 bacterias/µL, con sensibilidad de 0,98 y especificidad de 0,98 (LR+ = 48,8; IC 95 % = 22,1- 107,9, LR- = 0,02; IC 95% = 0-0.17). Ninguna combinación del recuento de glóbulos blancos y el recuento bacteriano en cualquier concentración superó el rendimiento diagnóstico del recuento bacteriano único mayor de 250 bacterias/µL.
Conclusión: el recuento automatizado de bacterias en orina, tomando como punto de corte el valor de 250/µL, tiene un excelente desempeño para confirmar (LR+ > 10) y descartar (LR- < 0.1) el diagnóstico de ITU en niños de 0-48 meses de edad. Sin embargo, la simple tira reactiva de orina con medición de esterasa leucocitaria y nitritos es una alternativa adecuada cuando se necesita una decisión clínica rápida en el escenario común de un servicio de urgencias.
Comentario: en Colombia, la infección urinaria en niños menores de 2 años representa el 0,2%-20% de las consultas en el servicio de urgencias, y su diagnóstico y tratamiento oportunos reducen el riesgo de complicaciones como cicatrices renales, bacteriemia, urosepsis o muerte (17). En nuestro país, en pacientes que llegan al servicio de urgencias con fiebre y clínica sugestiva de ITU se hace un uroanálisis con cintilla reactiva y examen microscópico para tomar decisiones clínicas (18). Este estudio demostró que el recuento bacteriano automatizado con resultado mayor de 250 células/µL tiene la mejor sensibilidad y especificidad en el diagnóstico de ITU en muestras de orina tomadas por sonda uretral. Sin embargo, la tira reactiva de orina con resultados positivos para esterasa leucocitaria o nitritos tiene un rendimiento diagnóstico muy similar al del análisis automatizado por citometría de flujo, por lo que un resultado positivo puede justificar el uso de antibióticos en niños febriles que consultan al servicio de urgencias, en especial cuando la condición clínica sugiere que la intervención se debe iniciar rápidamente y no se cuenta con una equipo de uroanálisis automatizado. En cuanto a la aplicabilidad de los resultados, no obstante, es necesario tener en cuenta que las muestras de orina para todas las pruebas realizadas en esta investigación, incluido el uroanálisis con tirilla, se tomaron por sonda uretral y por tanto los resultados no se deben extrapolar a pacientes cuyas muestras de orina se obtengan de la mitad del chorro miccional.
REFERENCIAS BIBLIOGRÁFICAS
1. Etminan M, Brophy JM, Samii A. Oral fluoroquinolone use and risk of peripheral neuropathy: a pharmacoepidemiologic study. Neurology. 2014 Sep;83(14):1261-3. [ Links ]
2. Fralick M, Macdonald EM, Gomes T, Antoniou T, Hollands S, Mamdani MM, et al. Co-trimoxazole and sudden death in patients receiving inhibitors of renin- angiotensin system: population based study. BMJ. 2014 Oct;349:g6196. [ Links ]
3. Bakker OJ, van Brunschot S, van Santvoort HC, Besselink MG, Bollen TL, Boermeester MA, et al. Early versus on-demand nasoenteric tube feeding in acute pancreatitis. N Engl J Med. 2014 Nov;371(21):1983-93. [ Links ]
4. Kanegaye JT, Jacob JM, Malicki D. Automated urinalysis and urine dipstick in the emergency evaluation of young febrile children. Pediatrics. 2014 Sep;134(3):523-9. [ Links ]
5. Sousa J, Alves G, Fortuna A, Falcão A. Third and fourth generation fluoroquinolone antibacterials: a systematic review of safety and toxicity profiles. Curr Drug Saf. 2014;9(2):89-105. [ Links ]
6. Food and Drug Administration. FDA Drug Safety Communication: FDA requires label changes to warn of risk for possibly permanent nerve damage from antibacterial fluoroquinolone drugs taken by mouth or by injection [Internet]. (cited 2015 Jan 3). Available from: http://www.fda.gov/downloads/Drugs/ DrugSafety/UCM365078.pdf142 [ Links ]
7. Ali AK. Peripheral neuropathy and Guillain-Barré syndrome risks associated with exposure to systemic fluoroquinolones: a pharmacovigilance analysis. Ann Epidemiol. 2014 Apr;24(4):279-85. [ Links ]
8. Velazquez H, Perazella MA, Wright FS, Ellison DH. Renal mechanism of trimethoprim-induced hyperkalemia. Ann Intern Med. 1993 Aug;119(4):296-301. [ Links ]
9. Alappan R, Buller GK, Perazella MA. Trimethoprimsulfamethoxazole therapy in outpatients: is hyperkalemia a significant problem? Am J Nephrol. 1999;19(3):389-94. [ Links ]
10. Marinella MA. Trimethoprim-induced hyperkalemia: An analysis of reported cases. Gerontology. 1999 Jul- Aug;45(4):209-12. [ Links ]
11. Antoniou T, Gomes T, Juurlink DN, Loutfy MR, Glazier RH, Mamdani MM. Trimethoprim-sulfamethoxazoleinduced hyperkalemia in patients receiving inhibitors of the renin-angiotensin system: a population-based study. Arch Intern Med. 2010 Jun;170(12):1045-9. [ Links ]
12. Antoniou T, Gomes T, Mamdani MM, Yao Z, Hellings C, Garg AX, et al. Trimethoprim-sulfamethoxazole induced hyperkalaemia in elderly patients receiving spironolactone: nested case-control study. BMJ. 2011Sep;343:d5228. [ Links ]
13. Besselink MG, van Santvoort HC, Renooij W, de Smet MB, Boermeester MA, Fischer K, et al. Intestinal barrier dysfunction in a randomized trial of a specific probiotic composition in acute pancreatitis. Ann Surg. 2009 Nov;250(5):712-9. [ Links ]
14. Sun JK, Mu XW, Li WQ, Tong ZH, Li J, Zheng SY. Effects of early enteral nutrition on immune function of severe acute pancreatitis patients. World J Gastroenterol. 2013 Feb;19(6):917-22. [ Links ]
15. Wereszczynska-Siemiatkowska U, Swidnicka-Siergiejko A, Siemiatkowski A, Dabrowski A. Early enteral nutrition is superior to delayed enteral nutrition for the prevention of infected necrosis and mortality in acute pancreatitis. Pancreas. 2013 May;42(4):640-6. [ Links ]
16. Oláh A, Romics L Jr. Enteral nutrition in acute pancreatitis: a review of the current evidence. World J Gastroenterol. 2014 Nov;20(43):16123-31. [ Links ]
17. Malo G, Echeverry J, Iragorri S, Gastelbondo R. Infección urinaria en niños menores de dos años: guía de práctica clínica. Sociedad colombiana de urología. Urol Colomb. 2001;36(2) [ Links ].
18. Pemberthy C, Gutierrez J, Arango N, Monsalve M, Giraldo N, Gutierrez F, et al. Aspectos clínicos y farmacoterapéuticos de la infección del tracto urinario. Revision estructurada. CES Med. 2011 Jul-Dic; 25 (2):135-52. [ Links ]