INTRODUCCIÓN
 El espacio epidural es un espacio virtual utilizado ampliamente tanto por anestesiólogos como por especialistas en medicina del dolor. La inyección epidural de esteroides es una de las intervenciones practicadas con mayor frecuencia en Estados Unidos y en el mundo para el tratamiento del dolor lumbar crónico 1. Por otro lado, la aplicación de un parche hemático en el espacio epidural es un procedimiento frecuente llevado a cabo tanto por anestesiólogos como por especialistas en medicina del dolor, por lo que el conocimiento de dicho espacio así como de las posibles complicaciones de las intervenciones que intentan acceder al mismo se deben diagnosticar y tratar precozmente 2. El empleo de la analgesia epidural guiada por fluoroscopia para el control del dolor agudo o para el tratamiento del dolor crónico requiere el conocimiento de la técnica, sus indicaciones, contraindicaciones y posibles complicaciones, así como el de los fármacos que se van a emplear y sus efectos. Es preciso, además, disponer del material adecuado y del personal con formación en el manejo de esta técnica analgésica y en la detección precoz de las posibles complicaciones 3)(4. De estas, una de las menos frecuentes y menos descritas en la literatura, que ocurre al intentar acceder al espacio epidural es la inyección inadvertida de fármacos en el espacio subdural.
El espacio epidural es un espacio virtual utilizado ampliamente tanto por anestesiólogos como por especialistas en medicina del dolor. La inyección epidural de esteroides es una de las intervenciones practicadas con mayor frecuencia en Estados Unidos y en el mundo para el tratamiento del dolor lumbar crónico 1. Por otro lado, la aplicación de un parche hemático en el espacio epidural es un procedimiento frecuente llevado a cabo tanto por anestesiólogos como por especialistas en medicina del dolor, por lo que el conocimiento de dicho espacio así como de las posibles complicaciones de las intervenciones que intentan acceder al mismo se deben diagnosticar y tratar precozmente 2. El empleo de la analgesia epidural guiada por fluoroscopia para el control del dolor agudo o para el tratamiento del dolor crónico requiere el conocimiento de la técnica, sus indicaciones, contraindicaciones y posibles complicaciones, así como el de los fármacos que se van a emplear y sus efectos. Es preciso, además, disponer del material adecuado y del personal con formación en el manejo de esta técnica analgésica y en la detección precoz de las posibles complicaciones 3)(4. De estas, una de las menos frecuentes y menos descritas en la literatura, que ocurre al intentar acceder al espacio epidural es la inyección inadvertida de fármacos en el espacio subdural.
Esta complicación fue descrita por primera vez en 1975 por Boys y Norman 5. Se ha informado una incidencia de bloqueo subdural accidental del 0,1 % al 7 % de las inyecciones epidurales 6)(7)(8.
Con la llegada de la fluoroscopia, que permite la comprobación del espacio epidural con medio de contraste, ha aumentado la eficacia de los bloqueos epidurales analgésicos en pacientes con dolor crónico 9)(10. Así mismo, se puede reconocer la aplicación accidental del medio de contraste ya sea en el espacio subaracnoideo o en el espacio subdural 11; sin embargo, resulta de suma importancia para el clínico poder reconocer los diferentes patrones de medio de contraste producidos en estos espacios.
Desde el punto de vista clínico, es importante tener claro que se debe sospechar esta complicación ante cambios sensitivos o motores que no sigan un patrón habitual, como un bloqueo sensitivo más extenso de lo esperado y asimétrico con latencia prolongada y mínimo bloqueo motor, lo que puede tener consecuencias tales como apnea e inconsciencia por distribución intracraneal del anestésico 12.
INFORME DE LOS PACIENTES
Caso 1
Hombre de 81 años, con diagnóstico de lumbalgia crónica con patrón mixto de dolor irradiado a los miembros inferiores, y antecedentes personales de hipertensión arterial y diabetes mellitus bien controladas con tratamiento. Historia previa de claudicación neurogénica en los miembros inferiores; presenta dolor lumbar que se irradia a la zona glútea y las piernas y que empeora con la marcha, asociado a arreflexia aquiliana bilateral. Peso: 82 kg; talla: 172 cm. Tiene resonancia magnética nuclear (RMN) de columna lumbosacra que muestra canal lumbar estrecho a múltiples niveles. Con esta historia consultó a la Clínica del
Dolor, donde se programó para analgesia epidural interlaminar L5-S1.
Se hicieron evaluación por medicina del dolor, verificación de los consentimientos informados y revisión de los equipos. En la monitorización básica se hallaron los siguientes datos: presión arterial inicial de 150/87 mm Hg, frecuencia cardíaca (FC) de 76 latidos por minuto, frecuencia respiratoria (FR) de 14 respiraciones por minuto y saturación de oxígeno (SaO2) de 96 %. Con el paciente en decúbito prono, se le administró oxígeno con cánula nasal a 2 L/minuto y se le aplicaron midazolam 2 mg más fentanilo 50 µg intravenosos con lo que se alcanzó una sedación consciente, de acuerdo con la escala de Ramsay 3/6.
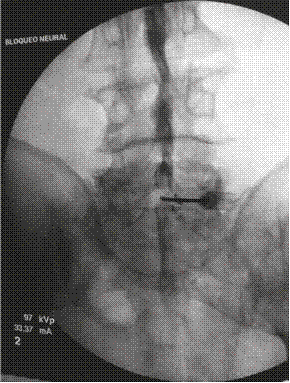
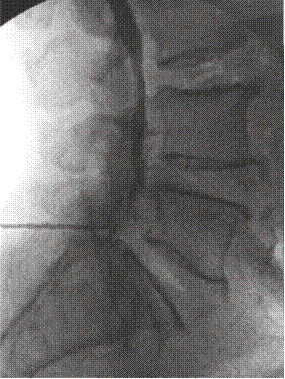
Previas asepsia y antisepsia en la zona lumbar e infiltración de la piel y el tejido celular subcutáneo con 3 mL de lidocaína simple al 2 % al nivel L5-S1, se avanzó una aguja Touhy n.º 17, se obtuvo pérdida de la resistencia al aire y se intentó acceder al espacio epidural L5-S1 (Figura 1). Se inyectó 1 mL de contraste no iónico (Omnipaque™ 300) y se obtuvieron luego imágenes fluoroscópicas del canal espinal lumbar en proyecciones AP y lateral (Figuras 1 y 2), en las que no se detectó anticipadamente un patrón subdural de la inyección por lo que se asumió la inyección epidural interlaminar L5-S1. Se procedió a inyectar en dicho nivel 10 mL de un preparado consistente en 80 mg de metilprednisolona más 10 mg de bupivacaína simple al 0,1 %, se retiró la aguja intacta y se trasladó al paciente a la sala de recuperación, con signos vitales estables, consciente y cooperando al cambio de posición hacia la camilla de transporte.
El paciente permaneció monitorizado en observación y 25 minutos después del procedimiento se tornó pálido y sudoroso, con alteración del sensorio hasta el estupor e imposibilidad para mover las piernas. Se hallaron los siguientes signos vitales: PA 65/50 mm Hg, FC 56 latidos por minuto, FR 18 respiraciones por minuto y SaO2 95 %.
Ante la posibilidad de una inyección subdural del anestésico local, se instaló una cánula nasal con oxígeno a 2 L/minuto y se inició la reposición con líquidos cristaloides (solución salina al 0,9 %) 1000 mL en bolo; se hizo titulación con bolos de etilefrina 2 mg intravenosos cada 3 minutos para mantener la tensión arterial sistólica por encima de 100 mm Hg; la glicemia fue de 90 mg/dL.
Diez minutos después de la aplicación de líquidos y vasopresores, el estado de conciencia y la tensión arterial mejoraron; la tensión sistólica se mantuvo por encima de 100 mm Hg. En ese momento el bloqueo sensitivo en los miembros inferiores estaba en T 10. Una hora más tarde, se encontraba hemodinámicamente estable y no requirió tratamiento farmacológico adicional. Dos horas después del bloqueo analgésico, comenzó a recuperar la fuerza motora en ambos miembros inferiores y cuatro horas más tarde la recuperación era completa.
Seis horas después del bloqueo mantenía un nivel adecuado de conciencia, toleraba la vía oral, no presentaba bloqueo motor y la micción era espontánea. Fue dado de alta con recomendaciones e información sobre los signos de alarma.
Caso 2
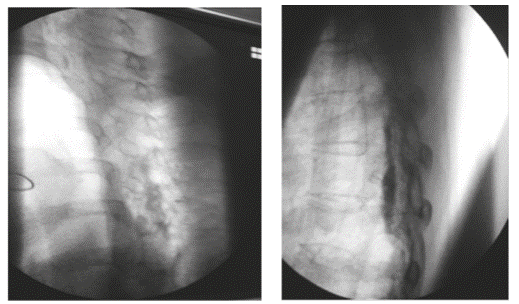
Mujer de 62 años con cuadro de cuatro meses de evolución consistente en cefalea holocraneana constante de predominio occipital que se exacerbaba con la sedestación y la bipedestación, con intensidad máxima referida como 9/10 en la escala verbal análoga (EVA) y que disminuía a 0/10 con la posición supina. Se asociaba a náuseas y vómitos. Se hizo RM cerebral con hallazgos compatibles con hipotensión endocraneana. Como antecedente informó enfermedad coronaria que requirió revascularización miocárdica 12 años antes; en la actualidad no recibe tratamiento farmacológico. El examen físico y el neurológico fueron normales sin signos meníngeos ni de focalización. Se planteó el diagnóstico de síndrome de hipotensión endocraneana probablemente secundario a una fístula espontánea de líquido cefalorraquídeo. Se hizo cisternografía que evidenció extravasación de medio de contraste principalmente a nivel de C7 izquierdo. Con tal diagnóstico se optó, en una junta médica multidisciplinaria, por un abordaje dorsal para aplicar un parche hemático bajo visión directa con fluoroscopia. En el quirófano se hizo un abordaje interlaminar a nivel de T2 mediante la técnica de pérdida de la resistencia con aire y aguja Tuohy n.º 17; sin embargo, en el momento de efectuar el epidurograma se observó migración del medio de contraste al espacio subdural por lo que se suspendió el procedimiento (Figuras 3a y 3b).
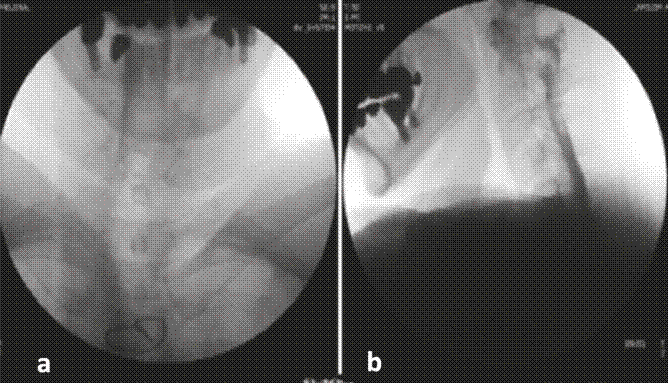
Figura 3a (AP) y 3b (lateral) . Se observa patron de migracion del medio de contraste al espacio subdural
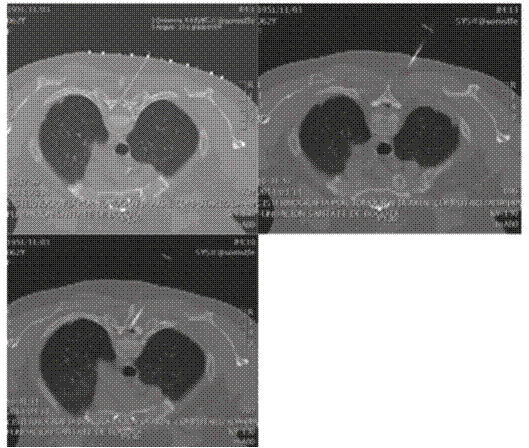
En una nueva junta multidisciplinaria se planteó que la fístula se encontraba en varios niveles por lo que no se consideró a la paciente como candidata para reparación quirúrgica y se procedió a la aplicación guiada por TAC de un parche hemático a nivel de T2; sin embargo, se observó nuevamente paso del medio de contraste al espacio subdural sin encontrar un sitio claro de comunicación de este con el espacio epidural, por lo que se suspendió el procedimiento y se optó por una mielografía dinámica guiada por TAC para detectar el sitio de la fístula; el informe fue de múltiples fístulas de líquido cefalorraquídeo a nivel de C5, C6, C7 y T1 (Figura 4) lo que descartó la posibilidad de tratamiento quirúrgico; por ello se programó nuevamente para el parche hemático.
En el quirófano y bajo guía fluoroscópica, se hizo abordaje interlaminar a nivel de T7 con aguja Tuohy nº 17 y mediante la técnica de pérdida de la resistencia con aire se identificó el espacio epidural. Se avanzó el catéter epidural hasta T2 y mediante epidurograma se confirmó la posición en el espacio epidural con adecuada migración del medio de contraste hasta C5 por lo que se procedió a la infusión de 20 mL de sangre fresca (Figura 5). La paciente tuvo mejoría completa de sus síntomas y fue dada de alta 48 horas después del procedimiento.
DISCUSIÓN
La inyección subdural accidental de fármacos o de sangre como en el segundo caso se puede advertir y prevenir. El espacio subdural, localizado entre la duramadre y la aracnoides, contiene una pequeña cantidad de líquido de tipo linfático. Se extiende desde S2 hasta el interior del cráneo, es decir, igual que el espacio subaracnoideo, este último situado entre la aracnoides y la piamadre y que contiene el líquido cefalorraquídeo (LCR). A su vez, el espacio epidural, que es el espacio virtual entre la duramadre y el ligamento amarillo, va desde el ligamento sacrocoxígeo hasta el agujero occipital y no contiene ningún líquido. Esta diferenciación anatómica es muy importante en el diagnóstico diferencial de la diseminación de un anestésico local en cualquiera de esos tres espacios. Los efectos secundarios que pueden esperarse luego de la administración de un anestésico local en el espacio subudral son: falla del bloqueo epidural o espinal, bloqueos en parche, unilaterales o incluso bloqueo espinal total, con una latencia entre 10 y 15 minutos y progresión durante los siguientes 20 a 40 minutos, con riesgo alto de choque hemodinámico y alteración ventilatoria porque muchas veces no se hace el diagnóstico a tiempo lo que condiciona la diseminación lenta del anestésico local incluso intracranealmente 13)(14)(15)(16)(17)(18)(19.
El diagnóstico de certeza del bloqueo subdural es radiológico 20. En el primer caso, guiado por fluoroscopia, se pudo observar, luego de la aplicación del medio de contraste, la distribución subdural en la proyección AP, como una extensa dispersión a varios niveles por encima y por debajo del sitio de inyección, con patrón homogéneo del contraste (Figura 1). En la proyección lateral (Figura 2) se observó una colección densa de medio de contraste con abombamiento a la porción central del canal espinal, que no salía a las raíces espinales laterales o a la porción inferior del saco tecal.
El medio de contraste en un epidurograma normal da un patrón que se asemeja a un árbol de Navidad; su distribución puede ser asimétrica y se observan burbujas dentro de la mancha de medio de contraste, a diferencia del patrón homogéneo del contraste observado cuando la inyección es subdural, donde se distribuye ampliamente a muchos segmentos de la columna vertebral hacia arriba y hacia abajo en una columna estrecha, por lo que la imagen característica se ha denominado ''rieles de ferrocarril'' patrón visto en la proyección anteroposterior, en la que se observan dos finas columnas laterales, resultado de que el espacio subdural es más ancho lateralmente, lo que permite la acumulación allí del contraste, mientras que en la imagen lateral las columnas de contraste se localizan dorsal y ventralmente. Una opacidad mal definida entre las columnas representa un pequeño volumen de contraste subdural 21, como se pudo detectar a tiempo en el segundo caso (Figura 3a), y, de esta forma, evitar las complicaciones de una inyección en el espacio equivocado.
Se ha descrito que la literatura anestesiológica probablemente sobreestima la capacidad de las técnicas radiológicas para identificar la inyección subdural 22.
Diversos autores sostienen que los signos clínicos de este tipo de bloqueo son lo suficientemente característicos como para hacer el diagnóstico con base en la clínica sin necesidad de confirmación radiológica 16. Lubenow y colaboradores 6, en un trabajo retrospectivo en 2182 pacientes que recibieron bloqueos epidurales lumbares para el tratamiento del dolor crónico de espalda, encontraron una incidencia del 0,8 % de bloqueo subdural; utilizaron para dicho diagnóstico dos niveles de criterios, a saber:
1) Criterios mayores: a) aspiración negativa de LCR; b) aparición de un bloqueo sensitivo inesperadamente extenso. 2) Criterios menores: a) inicio retardado (mayor de 10 minutos) del bloqueo sensitivo o motor; b) algún grado de bloqueo motor (sin importar el uso de dosis bajas de bupivacaína); c) uno o más de los siguientes: hipotensión moderada (descenso de hasta 20 % a 30 % de los valores basales), dificultad respiratoria progresiva e incoordinación y/o recuperación tardía.
Se acepta que existe este tipo de bloqueo ante la presencia de los dos criterios mayores y al menos uno menor 5)(23)(24)(25)(26. Nuestro primer paciente tuvo los dos criterios mayores y más de uno menor, lo que nos orientó hacia dicho diagnóstico.
La inyección de corticosteroides en el espacio epidural para el tratamiento del dolor crónico data de 1930; fue descrita en un artículo de Evans 27, tal como se le aplicó a nuestro paciente en una dilución junto con un anestésico local. En 1983 White 28 observó que hasta un 25 % de las punciones eran por fuera del espacio epidural. En nuestro primer paciente se usó la fluoroscopia para determinar el espacio epidural donde sería aplicado el medicamento 21.
Elliott y colaboradores 24 reportaron que dependiendo de la dosis y el volumen anestésico, los efectos del bloqueo pueden ser clínicamente indistinguibles de un bloqueo epidural y se pueden exacerbar si hay ruptura de la membrana espinal 29)(30.
En vista de que un bloqueo subdural puede ocurrir de manera imprevisible con signos clínicos y tiempo de latencia variables, se recomienda la monitorización y vigilancia periódica y de rutina luego de los procedimientos analgésicos o anestésicos epidurales, incluso cuando la clínica sea aparentemente normal en los minutos posteriores al procedimiento; de ahí la importancia de la formación adecuada del personal que atiende en las unidades de cuidado después de la analgesia y de la anestesia.