INTRODUCCIÓN
La frecuencia de diagnóstico de los quistes del páncreas ha aumentado debido al uso más frecuente de las imágenes diagnósticas y otras nuevas tecnologías1; clásicamente los quistes pancreáticos se han clasificado de acuerdo con su origen en neoplásicos y no neoplásicos. La Organización Mundial de la Salud (OMS) ha clasificado las lesiones quísticas de origen neoplásico en cuatro subtipos histológicos: 1) tumores serosos quísticos, 2) neoplasias quísticas mucinosas, 3) neoplasias papilares intraductales mucinosas y 4) neoplasias sólidas pseudopapilares2, cada uno de ellos con un potencial de malignidad determinado por lo que su tratamiento se define de acuerdo con el subtipo histológico.
Las neoplasias sólidas pseudopapilares (NSP) son infrecuentes y típicamente se presentan en mujeres en la segunda y tercera décadas de la vida. Sus localizaciones más frecuentes son el cuerpo y la cola del páncreas. Se caracterizan en las imágenes diagnósticas por tener componentes sólido y líquido. La mayoría son benignas: menos de 20 % presentan invasión vascular o perineural3. Su tratamiento es esencialmente quirúrgico y el pronóstico es bueno luego de la resección completa. Se presenta el caso de una paciente tratada con resección laparoscópica preservando el bazo.
PRESENTACIÓN DE CASO
Mujer de 15 años, con antecedente de migraña de tratamiento difícil. Tiene una sensación de masa en el hipocondrio izquierdo aproximadamente de 2 meses de evolución con crecimiento estable, asociada a episodios de dolor abdominal.
En el examen físico se la encuentra en buenas condiciones generales, sin adenopatías, con masa blanda palpable en el hipocondrio izquierdo, inmóvil e indolora a la palpación, sin soplos audibles. Hemoglobina 14 g/dL y función renal normal.
Ecografía de abdomen: hígado de tamaño normal, sin lesiones, aorta de calibre normal, bazo normal; en el hipocondrio izquierdo hay una imagen redondeada de componentes sólido y líquido con flujo positivo a la evaluación Doppler; diámetros: 82 x 81 x 90 mm. Se decide caracterizarla mejor con tomografía, en la que se demuestra una lesión mixta en el cuerpo del páncreas (componentes sólido y quístico) de 84 x 84 x 86 mm. El hígado, el bazo y el calibre de los grandes vasos retroperitoneales son normales. No hay adenopatías retroperitoneales; se observa cantidad escasa de líquido en el fondo de saco de Douglas (Figura 1).

Figura 1 Tomografía contrastada de abdomen. Lesión mixta en el cuerpo del páncreas (componentes sólido y quístico) de 84 x 84 x 86 mm. Hígado, bazo y calibre de los grandes vasos retroperitoneales: normales. No se observan adenopatías retroperitoneales
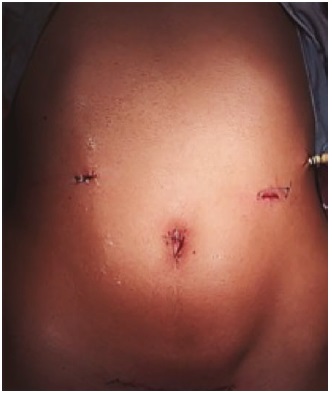
Con base en los hallazgos se decidió hacer pancreatectomía distal laparoscópica (PDL) con preservación del bazo, así: inserción de cuatro puertos laparoscópicos mediante técnica abierta (Figura 2), exploración de la cavidad e ingreso a la transcavidad de los epiplones por sección de la lámina anterior del omento mayor con instrumento de coagulación bipolar avanzado; identificación del tumor y disección circunferencial del mismo, disección de los vasos pancreáticos distales y ligadura térmica con coagulación bipolar avanzada, disección circunferencial del cuello del páncreas, sección y sutura con endograpadora lineal cortante de 60 mm. Inserción de dren retroperitoneal; se observó buena perfusión del bazo. Se hizo incisión de Pfannenstiel para la exéresis de la lesión (Figura 3).
Evolución clínica posoperatoria adecuada. Hemoglobina 11 g/dL. Se la dio de alta al segundo día posoperatorio y siete días después se retiró el dren abdominal, sin evidencia de fístula pancreática. Excelente estado clínico en el seguimiento ambulatorio. En el examen patológico del espécimen quirúrgico se halló un tumor sólido pseudopapilar del páncreas, con márgenes de resección y ganglios linfáticos negativos para malignidad.
DISCUSIÓN
Las lesiones quísticas del páncreas se pueden clasificar como neoplasias o pseudoquistes. Las primeras constituyen el 50 % del total4. Dichas lesiones se clasifican histológicamente de la siguiente manera: 1) tumores serosos quísticos (TSQ); 2) neoplasias quísticas mucinosas (NQM); 3) neoplasias papilares mucinosas intraductales (NPMI) y 4) neoplasias sólidas pseudopapilares (NSP). Difieren en su comportamiento, epidemiología y pronóstico. Los TSQ se presentan en mujeres especialmente en la sexta década de la vida, se consideran lesiones benignas y de lento crecimiento, en las imágenes se pueden identificar quistes (oligo- o macroquistes). Más de 95 % de las NQM ocurren en mujeres de la cuarta y quinta décadas de la vida, usualmente como hallazgo casual; se localizan principalmente en el cuerpo y la cola del páncreas; a diferencia de los TSQ, las lesiones mucinosas tienen un potencial aproximado de malignidad del 18 %, que es mayor en los tumores más grandes. Los NPMI ocurren por igual en ambos sexos entre la quinta y séptima décadas de la vida, con dos variantes principales según que se deriven del ducto principal o de una ramificación de este; los primeros tienen un potencial de malignidad mayor de 65 %, mientras que el de los segundos es de 40 %2.
Lichtenstein5 en 1934 hizo el primer reporte posmortem de este tumor como un cistadenoma papilar de la cola del páncreas con metástasis a peritoneo, omento e hígado. Frantz6 en 1959 informó otros tres casos y describió las características propias de este tumor. Había recibido diferentes nombres hasta que la OMS en 1996 lo definió como “Tumor pseudopapilar sólido”
Macroscópicamente, las lesiones son masas bien definidas con áreas hemorrágicas; al microscopio se caracteriza por células poligonales que no coalescen rodeadas por vasos sanguíneos de pequeño calibre. A menudo hay degeneración y hemorragia intraquísticas7.
Su origen no está claro: según algunos investigadores, se originan de células primordiales pluripotenciales, mientras que otros sugieren un origen extrapancreático8)(9. Constituyen el 5 % de los tumores quísticos del páncreas, el 1 % de las neoplasias pancreáticas exocrinas10 y menos del 4 % de todas las lesiones quísticas resecadas del páncreas3)(11.
Solo 10 % se presentan en hombres, en quienes su comportamiento es más agresivo. Los síntomas más comunes son dolor y distensión abdominales; la ictericia en rara. Con frecuencia son asintomáticos por lo que a menudo son hallazgos casuales en imágenes10.
Hasta 2013 se habían informado 2744 pacientes con TSP11.
El potencial de malignidad de las NSP es bajo, con tasa de supervivencia a los 5 años superior al 95 %; por tanto, su tratamiento debe ser quirúrgico. Las metástasis se producen usualmente a ganglios linfáticos, peritoneo e hígado. Se ha informado afectación peritoneal o hepática en 5 % a 15 %, aproximadamente12.
La tomografía es la prueba diagnóstica de elección, pues permite diferenciar los varios tipos de neoplasias quísticas con base en los siguientes criterios: localización, patrón intralesional (unilocular, oligoquístico, poliquístico), calcificaciones, comunicación con el conducto pancreático principal o los ductos laterales, septos y presencia de nódulos murales13; sin embargo, en años recientes la ecografía endoscópica con o sin aspiración con aguja fina se ha afianzado como estrategia de estudio efectiva y segura en la clasificación de lesiones quísticas y sólidas del páncreas, que da información cuando el diagnóstico no es claro y confirma la presencia o ausencia de características de riesgo o el diagnóstico de malignidad14)(15.
Como en el caso expuesto, los TSP se encuentran más comúnmente en el cuerpo y la cola del páncreas. Se caracterizan en las imágenes por presentar contenido mixto sólido/quístico, bordes regulares y calcificaciones ocasionales. Con frecuencia son de gran tamaño, con diámetro medio de 10 cm. Tienen buen pronóstico si se resecan con criterios oncológicos16.
El tratamiento de estas lesiones es la resección quirúrgica. Antes del advenimiento de la laparoscopia, el procedimiento estándar era la pancreatectomía por laparotomía; sin embargo, con el desarrollo de nuevas técnicas mínimamente invasivas ha aumentado el número de pacientes con tumores pancreáticos quísticos tratados laparoscópicamente. En 1994 se informó la primera pancreatectomía laparoscópica distal17. Una de las opciones quirúrgicas es la enucleación laparoscópica que se considera razonable en el tratamiento de las lesiones pancreáticas benignas pequeñas o malignas de bajo grado, que permite la preservación del parénquima pancreático sin lesión del conducto pancreático principal, pero aun así con tasas altas de fístula pancreática (13 % a 38 %)18.
La pancreatectomía distal laparoscópica (PDL) es el procedimiento quirúrgico más frecuente. Sus principales ventajas sobre la pancreatectomía distal abierta son las siguientes: mejoría de la exposición quirúrgica, la visualización y la recuperación posquirúrgica; disminución del sangrado y de la estancia hospitalaria; sin aumento del tiempo quirúrgico, las complicaciones posquirúrgicas ni el compromiso de los márgenes de resección18)(19)(20.
Debido a la función inmunológica del bazo y al aumento de la morbilidad posquirúrgica temprana y a mediano plazo, principalmente infecciosa, en los pacientes esplenectomizados19)(21)(22 se ha establecido una tendencia quirúrgica marcada a evitar la esplenectomía en estos procedimientos; se considera que la PDL con preservación del bazo es la técnica de elección para el tratamiento quirúrgico de las neoplasias quísticas del páncreas de localización distal y central23.
Se han descrito dos técnicas de preservación del bazo en la pancreatectomía distal: la primera, que se usó en el caso aquí reportado, requiere disección meticulosa y esqueletización de los vasos esplénicos; la segunda, descrita por Warshaw en 198824)(25 divide la arteria y la vena esplénicas y preserva el flujo sanguíneo al bazo a través de los vasos gástricos cortos y la arteria gastroepiploica izquierda; esta última se recomienda para casos de anatomía distorsionada por fibrosis secundaria a pancreatitis crónica o por compromiso vascular no infiltrativo; sin embargo, por el riesgo de necrosis esplénica secundaria a hipoperfusión se pueden presentar tasas altas de abscesos esplénicos18.
La PDL preservadora del bazo tiene complicaciones posquirúrgicas en 18,4 % de los pacientes, fístulas pancreáticas en 13,2 %, mortalidad menor del 1 %26 y tasa de conversión a cirugía abierta de 10 % a 20 %, según la experiencia del cirujano, lo que demuestra que este procedimiento es un enfoque factible, seguro y eficiente para el tratamiento de neoplasias pancreáticas.
En la actualidad existen pocos informes de PDL preservadora del bazo en pacientes con neoplasias quísticas del páncreas con resultados exitosos26)(27)(28)(29)(30)(31.
Debido a su radiosensibilidad, se sugiere la radioterapia en casos de tumores no resecables. La quimioterapia puede ser exitosa en algunos pacientes, especialmente la quimioembolización arterial en pacientes con metástasis hepáticas32.
Se deben tener en cuenta las contraindicaciones para la preservación del bazo: compromiso vascular hiliar, esplenomegalia33 y como contraindicación relativa la inexperiencia del cirujano en la disección vascular esplénica.
Para las lesiones de localización proximal (cabeza) el procedimiento de elección es la pancreatoduodenectomía, mientras que para las localizadas en el cuello es de elección la pancreatectomía central34.
En Colombia se han informado pocos casos y series de casos; una de las más representativas fue la de Sánchez y colaboradores35) con 10 casos todos ellos en mujeres; el tamaño promedio de las lesiones fue 13 x 13 cm, 60 % se presentaron en la cabeza y las restantes en la cola, en contraposición a lo encontrado usualmente en la literatura. Todas las pacientes fueron sometidas a procedimientos de resección quirúrgica, a saber: seis pancreatoduodenectomías y cuatro pancreatectomías distales.
Otra de las series con mayor relevancia clínica fue la de Abad y colaboradores33 con 28 casos entre 1952 y 2006, de los que 87,5 % fueron en mujeres. El promedio de edad de aparición fue de 25 años. Hubo malignidad en dos mujeres de 46 y 29 años (7,1 %), la primera con compromiso duodenal y metástasis hepática, y la segunda solo con lesiones hepáticas. Además, informaron 35,39 meses de seguimiento clínico libre de enfermedad y una tasa de mortalidad de 3,57 %.
En conclusión, presentamos el caso de una mujer de 15 años con un tumor sólido pseudopapilar del páncreas, resecado por PDL con preservación del bazo; la estancia hospitalaria fue corta y no hubo complicaciones; se reafirma que el tratamiento de las lesiones quísticas del páncreas con cirugía mínimamente invasiva es un enfoque con amplios beneficios clínicos, aceptable morbilidad y baja mortalidad, respetando la función inmunológica esplénica.