INTRODUCCIÓN
El tracoma es una enfermedad infecciosa que forma parte del grupo de las 17 Enfermedades Tropicales Desatendidas (ETD); estas se presentan principalmente en el trópico donde predominan la humedad y el calor, junto con las condiciones de pobreza y sus asociaciones como la falta de acceso a agua potable, saneamiento y vivienda adecuada, que son determinantes de su aparición1)(2. Se ha demostrado que la posición socioeconómica tiene una relación importante con la forma activa de la enfermedad, por lo que se la debe tener en cuenta al evaluar las causas del aumento de su prevalencia3.
Las ETD son una gran carga para los enfermos y su entorno porque reducen la productividad, agravan la pobreza, aumentan los costos de salud y generan un menor desarrollo socioeconómico de los países endémicos1)(4. Asimismo, son una causa importante de morbimortalidad, pues afectan a más de mil millones de personas, generan 534 000 muertes y representaron en 2010 el 1 % de la carga mundial de Años de Vida Ajustados por Discapacidad (AVAD), sin contar la malaria5)(6. Se ha demostrado el incremento de la susceptibilidad al tracoma y el empeoramiento de su curso en personas infectadas con VIH, tuberculosis o malaria, lo que evidencia un vínculo notable entre el tracoma y otras enfermedades7. Los principales desafíos que plantea el tracoma son su prevención, tratamiento y erradicación; esta última se ha iniciado con la administración masiva de azitromicina8.
En este artículo se presenta una revisión sobre Chlamydia trachomatis y su papel en el tracoma, abarcando los siguientes aspectos: generalidades, ciclo de vida, mecanismos de transmisión, factores de riesgo para la infección y la progresión, manifestaciones clínicas oculares, diagnóstico, tratamiento, epidemiología y acciones y programas para la prevención, el control y la erradicación.
EPIDEMIOLOGÍA
El tracoma es la principal causa de ceguera prevenible en el mundo; en 2010 representó aproximadamente el 3 % del total de casos (alrededor de 1,3 millones de personas)9)(10; continúa siendo la primera causa de ceguera infecciosa, pero pasó de la segunda o tercera posición a la quinta como causa de ceguera en general11.
Aunque los datos epidemiológicos son insuficientes, se calcula que alrededor de 325 millones de personas viven en 51 países endémicos en África, Asia, Latinoamérica y Oceanía; de ellas, según la Organización Mundial de la Salud (OMS), en 2015, 232 millones estaban en riesgo de contagiarse y 21 millones padecían tracoma activo12)(13. En la actualidad, esta infección es responsable del deterioro visual de 1,8 millones de personas, de las cuales 500 000 tienen ceguera (1,4 % de la ceguera mundial que padecen 39 millones)13.
En áreas endémicas, la tasa de prevalencia de tracoma activo es de 60 % a 90 % en preescolares, pero se vuelve menos frecuente y de menor duración con el aumento de la edad; la familia es la principal unidad de transmisión13. Las mujeres quedan ciegas con una frecuencia dos o tres veces mayor que la de los hombres debido al mayor contacto con niños infectados, aunque los infantes menores de seis meses no son fuente de reinfección13)(14)(15.
Brasil, Guatemala, México y Colombia han sido identificados como los países de América con focos activos de tracoma. Según la Organización Panamericana de la Salud (OPS), alrededor de 50 millones de personas viven en áreas de riesgo16. De los anteriores, México, donde se localiza principalmente en el estado de Chiapas, podría ser el primer país en solicitar la verificación de la eliminación de la enfermedad como causa de ceguera17. Por otro lado, Brasil es la nación con la mayor cantidad de personas en áreas endémicas, algunos de sus estados han iniciado campañas de eliminación y han informado 20 000 personas tratadas y más de 1000 cirugías llevadas a cabo en 201218.
En la zona brasileña que limita con el departamento colombiano del Vaupés, en la región del río Negro, se detectó desde 2001 un foco activo de esta infección en varias comunidades indígenas de la familia Makú; en ella, la prevalencia estimada en niños de 1 a 9 años fue superior al 50 %16. Esta fue la ruta por la que ingresó a Colombia, ubicándose en la región del Orinoco-Amazonas, con las mismas características y determinantes sociales de salud que en Brasil16.
En 2010 se publicó la primera evidencia clínica de la infección en Vaupés (Colombia), donde hay 17 000 personas del área rural en riesgo de desarrollar ceguera por tracoma. Esto llevó a que entre 2012 y 2013 se hiciera un censo en las regiones oriental y occidental del departamento, respectivamente, iniciando la delimitación del foco endémico y demostrando la existencia de diferentes estadios de la enfermedad en más de 70 personas, y tasas de prevalencia superiores al 20 % en niños de 1 a 9 años16)(19. Por último, en el panorama internacional el único país con altos ingresos que tiene áreas endémicas de tracoma es Australia20.
GENERALIDADES
Chlamydia spp
Chlamydia spp., es una bacteria gramnegativa que actúa como patógeno intracelular obligado; su pared posee lipopolisacáridos y proteínas inmunogénicos, pero no tiene peptidoglicano incorporado, pese a contar con los genes necesarios para producirlo, ni ácido murámico21)(22)(23.
El género cuenta con tres especies causantes de enfermedad humana: C. psittaci, C. pneumoniae y C. trachomatis; esta última se divide en 18 serotipos asociados con diferentes manifestaciones clínicas: A, B, Ba y C con el tracoma; D a K con la enfermedad oculogenital que incluye síndromes de transmisión sexual, conjuntivitis de inclusión en adultos y oftalmía neonatal en niños, pero no el tracoma endémico; L1 , L2 y L3 con el linfogranuloma venéreo9)(24)(25.
Las manifestaciones urogenitales causadas por Chlamydia trachomatis ocurren tanto en hombres como en mujeres: en los primeros causa uretritis no gonocócica, epididimitis, prostatitis y proctitis; en las mujeres pueden ocurrir cervicitis mucopurulenta, síndrome disuria-piuria por uretritis, enfermedad inflamatoria pélvica y síndrome de Fitz-Hugh-Curtis o perihepatitis9. Asociadas a la uretritis se pueden presentar manifestaciones articulares como la artritis reactiva; aproximadamente un tercio de los pacientes con esta última cursan con el síndrome de Reiter, cuya tríada clásica consta de artritis, uveítis y uretritis9.
CICLO DE VIDA
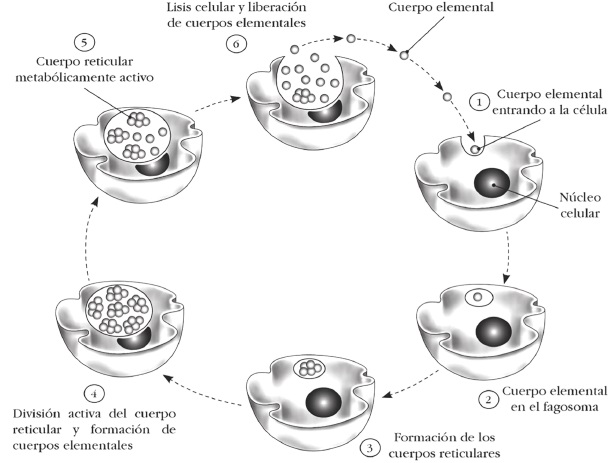
El ciclo replicativo de Chlamydia spp., dura de 2 a 3 días y es único y bifásico, lo que explica la variación del tamaño celular entre 0,25 μm y 1 μm de diámetro9)(21. Incluye dos formas9:
Cuerpo elemental (0,25 μm - 0,35 μm de diámetro): forma de resistencia metabólicamente inactiva, con capacidad de infectar y que se encuentra tanto intracelular como extracelularmente.
Cuerpo reticular (0,5 μm - 1 μm de diámetro): metabólicamente activo e intracelular estricto.
El proceso se inicia cuando el cuerpo elemental se adhiere por las proteínas de la membrana externa al proteoglicano de sulfato de heparina de las células diana26. Después de ello hay una unión irreversible dada por adhesinas bacterianas como OmcB (Outer Membrane Cytochrome B), MOMP (Major Outer Membrane Protein) y MOMP glicosilada26. Una vez interactúan, el cuerpo elemental es endocitado al presentar cambios del citoesqueleto, dados por la proteína TARP (Translocated Actin-Recruiting Protein) y al activar sistemas de secreción tipo III y otros efectores26.
A continuación, se inhibe la fusión lisosomal, dando protección al patógeno en la vacuola, donde se reorganiza formando el cuerpo reticular que comienza a utilizar la maquinaria celular para aumentar de tamaño y dividirse por fisión binaria9. Los cuerpos reticulares se transforman en elementales para perpetuar el ciclo21. Estos salen de la célula por exocitosis, extrusión de inclusiones intactas o apoptosis, esta última con la ayuda de un factor regulador de señales de apoptosis -CPAF- (Chlamydia protease/proteasome-like activity factor), que inhibe la apoptosis durante el ciclo de crecimiento y la acelera cuando el microorganismo está desarrollado (Figura 1)21.
MECANISMOS DE TRANSMISIÓN
La infección se puede propagar de una a otra persona por diferentes mecanismos; probablemente se encuentra una combinación de ellos en la mayoría de los casos, pero su importancia varía según la zona. Entre los medios de transmisión descritos se destacan27:
Diseminación directa por contacto cercano entre el ojo de la persona infectada y el de la persona sana.
Propagación indirecta por fómites.
Transmisión por moscas que buscan los ojos.
Contaminación de los dedos con secreciones oculares o nasales que contengan la bacteria.
Se ha observado que algunas variables climáticas pueden influir indirectamente en la transmisión del agente causal, entre ellas: escasas precipitaciones que disminuyen el acceso al agua o su uso para el lavado de la cara; aumento de la temperatura que puede influir en la actividad del vector Musca sorbens y las condiciones climáticas que favorezcan el secado de las heces dado que es el sitio favorito de reproducción del vector28.
FACTORES DE RIESGO DE INFECCIÓN Y PROGRESIÓN
Los factores de riesgo asociados a la enfermedad por Chlamydia trachomatis son los siguientes29:
Mala higiene facial al no limpiarse las secreciones oculares y nasales.
Hacinamiento.
Vivir en zonas con muchas moscas.
Migración entre comunidades.
Ser niño en áreas endémicas30.
Las mujeres tienen mayor riesgo de sufrir cicatrices conjuntivales y triquiasis, por estar en mayor contacto con niños.
Polimorfismos genéticos en los alelos que codifican para interferón γ (IFN-γ), Factor de Necrosis Tumoral α (TNF-α) y las metaloproteinasas de la matriz. Estos polimorfismos se han asociado con una baja respuesta inmunológica frente a la bacteria y con mayor predisposición a producir cicatrices tracomatosas.
MANIFESTACIONES CLÍNICAS OCULARES
El período de incubación es de 3 a 10 días y los síntomas iniciales son epífora, inyección conjuntival y secreción mucopurulenta; posteriormente pueden presentarse queratitis, triquiasis y entropión31.
Esta enfermedad cursa generalmente con afectación bilateral y consta de dos fases: la primera es activa, se da en niños y puede ser asintomática o manifestarse por prurito, irritación y secreciones oculares asociadas a conjuntivitis folicular25)(32)(33. Se afecta la conjuntiva tarsal, más gravemente la superior; al examen físico se evidencia un engrosamiento folicular y papilar de las glándulas por la acumulación subepitelial de células linfoides y cuerpos elementales32)(34. Estas se observan como pequeños puntos blancos o amarillos, que una vez resueltos dejan depresiones patognomónicas conocidas como pozos de Hebert y, en algunas ocasiones, pannus corneal7)(29)(35. La fase activa más grave genera engrosamiento y edema de la conjuntiva36.
La segunda fase se caracteriza por manifestaciones cicatriciales debidas a la inflamación conjuntival a repetición; inicialmente aparecen como pequeñas cicatrices en forma de estrella, que se van desarrollando a lo largo del tiempo y que, al contraerse, son responsables de la triquiasis y el entropión; este fenómeno genera abrasiones corneales dolorosas, edema, úlceras, cicatrización y por último opacidad corneal7)(25)(33)(34.
Posteriormente se presentan xeroftalmia y ceguera. La sequedad ocular es el resultado de la disminución en la población de células caliciformes y la destrucción de los conductos y glándulas lagrimales lo que lleva a una escasa producción de sustancias mucosas y acuosas lubricantes. Además, la infiltración de células linfoides y la cicatrización pueden afectar las glándulas lagrimales accesorias y sus respectivos conductos9)(34. El tracoma se puede estadificar según los hallazgos físicos de la siguiente manera (Figura 2)37:
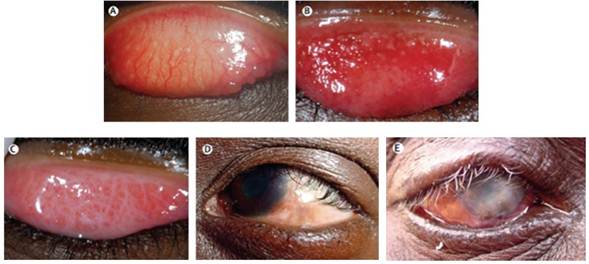
Figura 2 Manifestaciones clínicas y clasificación simplificada del tracoma según la OMS. A. Inflamación tracomatosa folicular. B. Inflamación tracomatosa intensa. C. Cicatrización tracomatosa. D. Triquiasis tracomatosa. E. Opacidad corneal. Imagen cortesía del doctor Hugh R. Taylor, President, the International Council of Ophthalmology, Melbourne, Laureate Professor, and Harold Mitchell Chair of Indigenous Eye Health, Melbourne School of Population and Global Health, University of Melbourne. Disponible en: Taylor HR, Burton MJ, Haddad D, West S, Wright H. Trachoma. Lancet. 2014 Dec 13; 384(9960):2142-52.
Inflamación tracomatosa folicular: cinco folículos o más en la conjuntiva superior.
Inflamación tracomatosa intensa: engrosamiento e inflamación de la conjuntiva, con oscurecimiento de la mitad de los vasos.
Cicatrización tracomatosa: presencia de cicatrices conjuntivales.
Triquiasis tracomatosa: al menos una pestaña está en contacto con la córnea.
Opacidad corneal: opacidad visible con facilidad ubicada sobre el eje óptico.
La afectación visual se manifiesta 15 a 20 años después del comienzo de la enfermedad, como resultado del daño repetitivo de la córnea. Si se llega a la opacidad corneal se produce ceguera irreversible. Las infecciones a repetición aumentan el riesgo de ocasionar cicatrices conjuntivales29)(31. No hay manifestaciones en otras partes del cuerpo31.
DIAGNÓSTICO
El tracoma se diagnostica clínicamente; los exámenes de laboratorio se usan principalmente para propósitos de investigación (8). Al examen ocular, se procede a hacer una eversión palpebral para buscar los signos sugestivos de la enfermedad; se puede hacer un raspado de la conjuntiva tarsal con el fin de buscar las inclusiones citoplasmáticas del microorganismo en un extendido coloreado con Giemsa, procedimiento que no es sensible, pero sí específico27)(31.
No existe un estándar de oro para el diagnóstico de tracoma por laboratorio8. Las pruebas más recomendadas para investigar esta infección son las basadas en ácidos nucleicos, a pesar de su alto costo y complejidad27)(38)(39. La prueba de amplificación de ácidos nucleicos (NAAT, por la sigla en inglés de nucleic acids amplification test) se hace con secreciones oculares o nasales y se hace positiva en 1 a 3 días después de la exposición; puede basarse en ADN o ARN; esta última parece tener más sensibilidad e igual especificidad que la primera8)(38. El diagnóstico clínico es muy sensible, pero los NAAT son más específicos38)(39.
Otros métodos de diagnóstico menos usados son los siguientes:
Cultivo: el microorganismo no es cultivable in vitro, sino que necesita tejidos vivos para crecer; por tanto, se usan cultivos celulares que luego se estudian por microscopía; no obstante, es un procedimiento largo y costoso, que requiere condiciones estrictas; es muy específico (99,9 %), pero poco sensible (50 % - 90 %), por lo que su utilidad es limitada8)(27)(40)(41.
Inmunofluorescencia directa: la presencia de cinco o más cuerpos elementales fluorescentes en el raspado conjuntival hace el diagnóstico.
Esta prueba es una buena opción en las etapas tempranas y asintomáticas de la enfermedad en las que es difícil la diferenciación con otras conjuntivitis, sean bacterianas o virales; su uso está limitado porque se requieren condiciones estrictas de transporte y almacenamiento refrigerados, un microscopio fluorescente y personal adecuadamente entrenado42.
TRATAMIENTO
Incluye la terapia con antibióticos y la cirugía. Epidemiológicamente se calcula que se requiere tratamiento antibiótico para 340 millones de personas y cirugía para 8,2 millones43.
Antibióticos: la azitromicina oral 20 mg/kg hasta 1 g en dosis única, o la tetraciclina tópica al 1 % BID por seis semanas, son igualmente efectivas para disminuir la prevalencia de la infección en las comunidades afectadas y sus manifestaciones clínicas oculares8.
La administración masiva de Zitromax® (azitromicina subvencionada por Pfizer y la Fundación Edna McConnell Clark), que busca una cobertura mínima del 90 % de la población, está indicada cuando la zona tenga una prevalencia de tracoma folicular en niños de 1-9 años mayor del 10 % y se la sugiere si llega a niveles del 5 % al 9 %. Se administra anualmente por 3 años si la prevalencia es de 10 % a 30 % y por 5 años si es mayor del 30 %. Al cumplir este tiempo, se mide nuevamente esta tasa y si es menor del 5 % se suspende la intervención8)(15. Se han reportado los efectos de la administración de azitromicina de alta cobertura en dosis única para el tratamiento de la infección por C. trachomatis en poblaciones como la de Kahe Mpya, en Tanzania. Allí se trató al 97,6 % de los residentes y la prevalencia ocular de la bacteria disminuyó desde 9,5 % a 0,1 % en un período de 24 meses44. Se ha visto que uno o dos ciclos del tratamiento de alta cobertura con azitromicina en la población pueden ser suficientes para eliminar a C. trachomatis en comunidades con niveles moderados de infección; pese a ello, la OMS sigue recomendando ofrecer de 3 a 5 terapias de tratamiento masivo anuales44. No se ha informado resistencia de Chlamydia trachomatis a la azitromicina15)(43.
Cirugía: la OMS recomienda dos técnicas quirúrgicas para el margen de las pestañas: rotación bilamelar tarsal y rotación lamelar tarsal posterior o procedimiento de Trabut; son igualmente eficaces y tienen menor tasa de triquiasis posoperatoria comparadas con la depilación, que es una opción a corto plazo en lugares donde las condiciones sean precarias45. Estas correcciones se hacen en casos de triquiasis tracomatosa y entropión por el riesgo de opacidad corneal y pérdida de la visión8)(15.
La cirugía mejora la agudeza visual, pero no tiene efecto sobre las cicatrices corneales, mientras que la depilación no incide en estos aspectos45. La tasa de recurrencias posquirúrgicas a los 3 años puede variar del 7,4 % al 62 %, por factores como la gravedad preoperatoria de la triquiasis, la variabilidad entre cirujanos, la técnica quirúrgica y la cicatrización posoperatoria de las heridas46. Un estudio en Etiopía47 demostró que la cirugía mejora de manera importante la visión y la calidad de vida independientemente del cambio en la agudeza visual; ello sugiere que el efecto de la cirugía de la triquiasis va más allá de la prevención del riesgo de ceguera y también mejora el bienestar general y la percepción de la salud de los individuos afectados.
Existe poca evidencia sobre desenlaces a largo plazo de los procedimientos quirúrgicos y su tasa de éxito comparados con otros tratamientos correctivos. En uno de los pocos estudios controlados y con asignación aleatoria48, la tasa de fracaso del tratamiento quirúrgico fue 2,2 % frente a 14 % con la depilación, y hubo 17 % de recurrencias a los 2 años después del tratamiento quirúrgico y 49,7 % con la depilación. El fracaso se define como cinco o más pestañas que tocan el globo ocular, y la recurrencia, como una o más pestañas que tocan el globo ocular48. En los pacientes sometidos a cirugía, la incidencia de progresión de la opacificación corneal fue de 4,1 % a los 2 años. Las complicaciones quirúrgicas más comunes son: infección (0,5 %), sangrado (0,5 %), hipocorrección (0,8 %), granulomas (0 a 14 %) y anormalidades o muescas en el borde palpebral (0 a 30 %), que se asocian a lagoftalmos y problemas con la película lagrimal46)(48.
Cabe resaltar el uso de azitromicina antes de los procedimientos quirúrgicos para aminorar la triquiasis posoperatoria; sin embargo, no hay evidencia suficiente que lo respalde; solo un estudio señaló una disminución de la tasa a 1 año y no a tres años45.
ACCIONES Y PROGRAMAS PARA LA PREVENCIÓN, CONTROL Y ERRADICACIÓN
En 1998, la asamblea de la OMS definió esta enfermedad como problema de salud pública y formuló el Programa para la Eliminación Global del Tracoma para 2020 (GET 2020 por su sigla en inglés), cuya primera meta es disminuir la prevalencia de la inflamación tracomatosa folicular en niños de 1 a 9 años a menos del 5 %13)(49. Sus acciones se basan en la implementación de la estrategia SAFE (Surgery, Antibiotics, Facial cleanliness, Environmental improvement) y el fortalecimiento de la capacidad nacional mediante la evaluación epidemiológica, monitoreo, vigilancia, evaluación de proyectos y movilización de recursos13. La estrategia SAFE consiste en lo siguiente26:
Cirugía (Surgery) para evitar complicaciones: aplicada principalmente a los pacientes con estadios avanzados de la enfermedad, con el fin de reposicionar las pestañas para que no estén en contacto con la córnea50. En pacientes con triquiasis menos grave se eliminan las pestañas afectadas y se espera a que haya un compromiso mayor para hacer la cirugía15.
Antibióticos: el de elección es la azitromicina, pero también se utiliza la tetraciclina tópica por 6 semanas para tratar la infección y disminuir la trasmisión en zonas endémicas15)(50.
Higiene facial y corporal (Facial cleanliness): la eliminación y prevención de la enfermedad se inician con este paso, los pacientes deben tener buenas prácticas de higiene personal y estar en un ambiente adecuado. Lo anterior requiere educación en salud y un desarrollo ambiental15.
Mejorar las condiciones ambientales (Environmental improvement): para que los habitantes de áreas endémicas puedan tener acceso de manera constante y oportuna a un sistema de saneamiento adecuado y a fuentes de agua potable15.
Además de la estrategia SAFE, Sightsavers en alianza con The International Coalition for Trachoma Control (ICTC), han desarrollado el proyecto The Global Trachoma Mapping Project (GTMP), cuya finalidad es proveer información al programa GET 2020, mediante encuestas y así saber qué lugares requieren mayor inversión para lograr la meta50)(51.
De esta manera, en 2013 cerca de 234 000 personas recibieron tratamientos quirúrgicos por enfermedad avanzada y en 2015 se entregaron 50 millones de dosis de antibióticos en 30 países para combatir el tracoma13)(52. Hasta la fecha Gambia, Ghana, Irán, Marruecos, Myanmar, Omán y Vietnam son los países que han logrado las metas de eliminación y han progresado hacia la fase de vigilancia13. Es así como los esfuerzos de los diferentes organismos internacionales han tenido un impacto importante en la eliminación de esta enfermedad; se han observado grandes progresos con el paso de las décadas y se está cada vez más cerca de erradicarla, lo que se evidencia en datos como los siguientes:
En 1995, 146 millones de personas padecían tracoma activo y representaban el 15 % de los casos totales de ceguera (6 millones)53.
En 2015, 21 millones de personas padecían tracoma activo y representaban el 1,4 % de los casos totales de ceguera (0,5 millones)13.
CONCLUSIÓN
Pese a los grandes esfuerzos y acciones encaminados a la erradicación del tracoma, este continúa siendo una causa importante de deficiencia visual infecciosa. La estrategia SAFE ha contribuido enormemente a la disminución de la enfermedad (146 millones de afectados en 1995 frente a 21 millones en 2015) y su ceguera consecuente, al pasar de representar el 15 % de los casos de ceguera en 1995 al 1,4 % en 2015. Sin embargo, se debe proseguir de manera efectiva y rápida para lograr los objetivos trazados por la OMS para el año 2020, basados en el desarrollo y la participación tanto del sector salud, mediante una formación continua permanente, como del sector socioeconómico. De esta forma, no solo se intervendrá el tracoma sino también otras enfermedades en las que las condiciones precarias son un factor determinante.