INTRODUCCIÓN
La enfermedad de Parkinson (EP) es una condición neurodegenerativa progresiva que se caracteriza por presentar alteraciones en la función motora como bradicinesia, rigidez, temblor en reposo, alteraciones en la marcha e inestabilidad postural, además de manifestaciones no motoras que pueden preceder a las alteraciones motoras. La terapia farmacológica en la EP logra impactar en los síntomas de la enfermedad durante los primeros años, pero luego se hace más difícil conseguir esta mejoría debido a la aparición de complicaciones como las fluctuaciones motoras y las discinesias y por esta razón se ha venido considerando otras aproximaciones terapéuticas para el paciente con EP avanzada, entre las que se incluye la estimulación cerebral profunda (ECP).
Luego de demostrar sus efectos sobre la mejoría del temblor, la ECP se postuló como una gran alternativa para el manejo de pacientes con EP de difícil control, logrando mejorías iguales o mayores en las complicaciones motoras cuando se la comparaba con la terapia farmacológica sola o con otras intervenciones quirúrgicas1. Actualmente, la ECP es un tratamiento ampliamente extendido para el manejo de la EP avanzada, y es una opción terapéutica en otros trastornos del movimiento y algunas patologías psiquiátricas2.
Esta es una revisión narrativa que describe la importancia de la EP y se hace énfasis en los aspectos clínicos de la ECP, se incluye el mecanismo por el que este último mejora los síntomas de la EP, así como los efectos adversos, costos, selección de pacientes y la evidencia clínica que soporta el uso de esta terapia en quienes padecen esta condición.
Enfermedad de Parkinson
La EP es la segunda causa de enfermedad neurodegenerativa crónica progresiva3 y es el tipo de parkinsonismo más prevalente4. Aproximadamente 10 millones de personas en el mundo se ven afectadas por esta enfermedad, se presenta en casi el 1 % de la población mayor de 65 años y un 4 a 5 % de los mayores de 85 años4-7. La prevalencia global de EP es aproximadamente 213 por cada 100.000 habitantes8 y aumenta considerablemente después de los 70 años, llegando a ser mayor a los 1000 casos por cada 100.000 habitantes9. En Colombia la EP afecta a 4,7 personas por cada mil habitantes10.
Esta enfermedad se caracteriza por presentar signos y síntomas tanto motores como no motores. Los síntomas motores incluyen temblor, bradicinesia-acinesia, rigidez e inestabilidad postural11,12 y el subtipo clínico más frecuente es el temblor con inestabilidad de la marcha13. Estos síntomas suelen ser de inicio y evolución asimétrica, inician en miembros superiores y se hacen bilaterales en un promedio de tres años12,13. En las etapas avanzadas, se presentan manifestaciones refractarias al tratamiento como discinesias, fluctuaciones motoras, trastornos de la postura, marcha, disfagia, y disartria14. Los síntomas no motores pueden preceder a la clínica motora e incluyen trastornos del sueño, síntomas autonómicos, gastrointestinales, cognitivos, dolor y otros5,14. A medida que avanza la enfermedad se hacen evidentes síntomas psiquiátricos como ludopatía, hipersexualidad, compras compulsivas, agresión, celos y fobias, principalmente en aquellos que abusan de fármacos dopaminérgicos14,15.
Se ha estimado que la vida media de supervivencia de los pacientes con EP está entre 11 y 15,8 años16-18. En los últimos años ha habido un aumento progresivo de mortalidad, lo que ha hecho que se ubique entre 0,9 a 3,8 por cada 100.000 habitantes(16, 19-21) y está asociada a comorbilidades como la neumonía, enfermedades cardiovasculares y cáncer17,22,23. La calidad de vida de los afectados por EP y de su familia se deteriora conforme esta progresa, puesto que por un lado aumenta la carga de la enfermedad y por el otro, se hace necesaria la presencia de un cuidador24,25. Para mejorar este panorama se han propuesto diversos tratamientos farmacológicos y quirúrgicos26-28, además de la ECP, que al respecto ha demostrado un impacto positivo29-31.
Principios de la ECP
Este procedimiento ha sido ampliamente usado en pacientes con EP en quienes los síntomas no cesan, la terapia farmacológica ha fallado o no se toleran sus efectos adversos32,33. Esta es una técnica de neuromodulación en la que se implanta uno o más electrodos de cuatro contactos en regiones cerebrales específicas, estos se conectan a un marcapaso subcutáneo implantado en el pecho desde donde se modula eléctricamente los patrones de despolarización, repolarización y conducción del potencial de acción de las neuronas34. Este tipo de intervenciones se viene explorando desde hace ya algunas décadas34,35, pero fue solo en los noventa que se estableció como un abordaje quirúrgico en humanos. Posteriormente se definió con mayor exactitud los sitios, tamaño e intensidad36,37, mejorando así las actividades motoras, las capacidades cognitivas y emocionales, al disminuir los efectos adversos secundarios a la estimulación eléctrica de zonas adyacentes38,39. Actualmente, la FDA (Food and Drug Administration) ha aprobado la modulación por ECP en el núcleo subtalámico (NST), globo pálido interno (GPI) y núcleo ventral intermedio del tálamo (NVIT)40.
En la EP existe una pérdida progresiva de neuronas dopaminérgicas de la sustancia nigra (SN) pars compacta41. Estas forman parte de la vía nigroestriatal que se proyecta hacia los ganglios basales en donde regulan la actividad de neuronas estriatales, cuyas eferencias modulan la actividad del tálamo de forma directa o indirecta42. Debido a la degeneración de estas neuronas dopaminérgicas, existe un predominio de la vía indirecta en donde las eferencias nigroestriatales inhiben las neuronas GABAérgicas del globo pálido externo, llevando a una desinhibición del NST. Éste a su vez envía proyecciones glutamatérgicas hacia la SN pars reticulada y GPI generando la liberación de GABA sobre los núcleos talámicos que se proyectan hacia la corteza cerebral43, lo que en últimas resulta en una disminución de la actividad motora y la consiguiente bradicinesia característica de la EP. La vía directa también juega un papel importante en la enfermedad, la disminución de la liberación de dopamina por las neuronas dopaminérgicas de la SN da lugar a la inhibición de las neuronas estriatales, que a su vez inhiben el GPI y la SN pars reticulata, por lo que el tálamo queda libre de inhibición y puede enviar impulsos excitatorios a la corteza motora que se traducen en aumento de la actividad motora en forma de temblor, (Figura 1)43-45.
La ECP en el NST interrumpe la sincronización neuronal de la vía indirecta que conecta este núcleo con la corteza motora46, esto aumenta el procesamiento de información sensitiva e iniciación del movimiento al incrementar la activación de la corteza premotora y por la modulación del circuito cerebelo-tálamocorteza que está conectado funcionalmente al circuito corteza-ganglios basales, (Tabla 1)47. Asimismo, mejora las capacidades cognitivas, la memoria visual, el reconocimiento de rostros al activar el giro frontal y temporal inferior48. Pese a esto, se han reportado aumentos en la apatía y cambios en el estado de ánimo de los pacientes intervenidos49.
Tabla 1 Efectos generales a nivel funcional y clínico de los núcleos cerebrales involucrados en la estimulación cerebral profunda
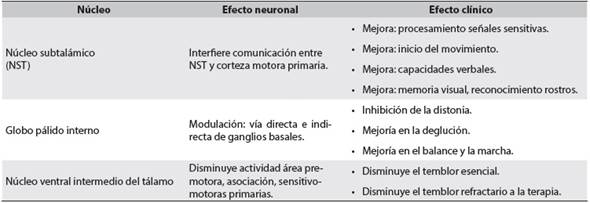

Figura 1 Principales vías de transmisión involucradas en la enfermedad de Parkinson. Se esquematizan las principales conexiones de la vía indirecta y directa que provocan los síntomas de la enfermedad
En el GPI converge la vía inhibitoria directa e indirecta de los ganglios basales, su estimulación con ECP genera una inhibición de la distonía generada por la enfermedad y mejora el balance, la marcha y la deglución50. La neuromodulación que se realiza en el NVIT disminuye la actividad en el área premotora, de asociación, sensitivo-motoras primarias y en el cerebelo contralateral modulando la amplitud, frecuencia y regularidad del temblor esencial y otros tipos de temblores refractarios a la terapia51. El efecto es aún mayor cuando se estimula el mismo sitio bilateralmente, en cuyo caso puede durar hasta 7 años52. Otros sitios explorados son el núcleo pedúnculo pontino, ventrolateral, ventral anterior y centromedial del tálamo40,53.
El efecto a nivel celular lo condiciona la composición y propiedades de las membranas que están en contacto con las frecuencias o por señales eléctricas que dicta el electrodo. En etapas agudas la estimulación produce una respuesta glial e inflamatoria contra el electrodo, las neuronas pueden generar potenciales excitatorios o inhibitorios en sentido ortodrómico o antidrómico, lo que permite la normalización de la frecuencia del potencial de propagación del estímulo en las vías ascendentes y descendentes de los núcleos estimulados54,55. Además, se cambian las frecuencias y el flujo sanguíneo cerebral en las regiones bajo la influencia del estímulo eléctrico33,55. La microglía y los astrocitos promueven la angiogénesis y la reorganización sináptica que se da con el tiempo, haciendo que el efecto crónico de la estimulación genere cambios en la plasticidad sináptica, generación de neuritas, aumento en la densidad sináptica y cambios en la actividad metabólica de las células56.
Después de que se activa la ECP, el curso y los patrones de mejoría en los síntomas varían considerablemente entre los síntomas que pueden ser tratados mediante la neuroestimulación. El temblor y la rigidez suelen responder rápidamente en minutos, mientras que la bradicinesia puede tardar horas, la distonía y el dolor mejoran en meses, los cambios comportamentales y neurocognitivos aparecen también en el transcurso de meses57.
Costos
Se estima que los costos médicos directos por consulta externa, como horas de personal de salud, insumos, medicamentos, entre otros, avalúan un promedio de 485,74 dólares americanos al mes por sujeto58, que podría alcanzar hasta 5.993 euros al año59. Los costos cambian de acuerdo al tipo de tratamiento realizado, se habla de un costo promedio de vida de 126.200 euros en pacientes con tratamiento médico estándar hasta 133.200 euros para pacientes con ECP60, otros reportan un costo promedio a 5 años de 186.244 dólares61, incluso se habla de una reducción de hasta el 40 % promedio de los costos por medicamentos después de la implantación31,61.
En relación al dispositivo, el mayor costo se ve reflejado en el momento de la implantación con cerca de 4.184 dólares hasta alcanzar 29.178 dólares en el primer año y a partir de allí un aumento promedio de 1.490 dólares por año. El mayor costo en el primer año es debido al valor de dispositivo, la intervención quirúrgica y los controles62, pero a partir de ahí muestra ser un tratamiento costo-efectivo y por lo tanto la ECP es una alternativa en el manejo de la EP en estados avanzados60-64.
Efectos adversos
Las infecciones tienen una prevalencia de 0 a 15 %65,66, siendo el Staphylococcus aureus el principal agente etiológico67,68). La hemorragia intracraneal, en especial la hemorragia intraventricular o intracerebral, localizadas a lo largo del trayecto de implantación del dispositivo, pueden ocurrir hasta en el 10 % de los casos66 pero generalmente son asintomáticas y auto limitadas65, aunque se han reportado de forma aislada hemiparesias resueltas con terapia física68.
Los efectos adversos neurológicos son rigidez postoperatoria, convulsiones parciales, confusión y eventos cerebrovasculares66,67. Las discinesias después de encender el dispositivo son un hallazgo normal y de buen pronóstico porque se asocian a un efecto sinérgico entre la medicación y la intervención quirúrgica65. Algunos efectos neuropsicológicos han sido documentados, entre ellos la disminución selectiva de las funciones cognitivas frontales, en la fluidez verbal y en el desarrollo del test de Stroop69-71. Se ha reportado una disminución de la función cognitiva global durante los primeros seis meses después de la implantación, en comparación con los siguientes 6 a 36 meses, debido posiblemente, a la reducción excesiva de levodopa en los primeros meses posquirúrgicos72.
También se han documentado trastornos mentales como comportamientos maníacos, hipomaniacos o depresivos que se manifiestan en los primeros seis meses posquirúrgicos pero muestran una mejoría progresiva65,69,73,74.
Otros efectos posquirúrquicos adversos reportados son la trombosis venosa profunda, aumento del índice de masa corporal, erosión de la piel en la zona del generador de impulsos interno (1-2,5 %), migración del dispositivo (0-19 %), rotura o fractura en la extensión del cable del dispositivo (0-15 %), adherencias alrededor de éste e incluso la muerte65,66,68,74-76.
En su mayoría, tales reacciones adversas no son dependientes del centro donde se realice el procedimiento quirúrgico, ya sea con alto o bajo flujo de pacientes con EP77. El habla, la expresión facial, la bradicinesia, el temblor y los síntomas axiales hacen parte de los signos y síntomas propios de la EP, que mejoran con el encendido del dispositivo, pero que reaparecen una vez este se apaga65,78,79.
Selección de pacientes
Se debe establecer una relación riesgo-beneficio para determinar si un paciente con EP se beneficiará con la terapia quirúrgica80. Centros especializados han establecido los criterios para seleccionar a quienes se podrían beneficiar de la ECP, estos consideran el estado del paciente, las complicaciones asociadas al tratamiento, entre otras, (Tabla 2)33,81,82. Sin embargo, su aplicación reduce sustancialmente el número de inclusión (1,6 %), porcentaje que podría aumentarse con otros más flexibles83 debido a que aún se encuentra en debate algunos aspectos relacionados con el tema82.
Evidencia clínica
A lo largo de los años la ECP ha demostrado beneficios en el tratamiento de los pacientes con EP. La seguridad y eficacia de esta terapia son temas claves y controversiales en las investigaciones, ya que proporcionan argumentos para el médico tratante a la hora de tomar una decisión al respecto. Por eso este apartado busca orientar al lector hacia algunos de los hallazgos clínicos relevantes sobre el tema.
Para comparar la ECP del NST más terapia farmacológica (ECP-F) versus el tratamiento farmacológico solo, se realizó un ensayo aleatorizado donde se incluyeron 156 pacientes con EP avanzada y síntomas motores severos. Se evaluaron los cambios en la calidad de vida según el cuestionario PDQ-39 y la severidad de los síntomas sin medicación, de acuerdo con la escala UPDRS-III. La ECP-F en comparación con la terapia farmacológica sola, causó mejorías desde el inicio hasta seis meses en el PDQ-39 y la UPDRS-III, con una mejoría media de 9,5 y 19,6 puntos, respectivamente. La neuroestimulación resultó en un incremento de 24 % al 38 % en las subescalas para la movilidad (p< 0,001), actividades de la vida diaria (p< 0,001), el bienestar emocional (p< 0,001), el estigma (p< 0,001) y malestar corporal (p= 0,009). Los eventos adversos graves fueron más frecuentes con la neuroestimulación que con la medicación sola (12,8 % frente al 3,8 %, p= 0,04) e incluía una hemorragia intracerebral fatal84.
Un ensayo clínico aleatorizado reunió a un total de 255 pacientes con EP avanzada y comparó el efecto de la ECP contra la terapia farmacológica. A 60 se les realizó ECP bilateral del NST, a 61 ECP del GPI y 134 recibieron tratamiento farmacológico. En relación con el primer grupo, estos últimos presentaron más tiempo libre de discinesias (media de diferencia entre los grupos 4,5 horas/día; IC 95 % 3,7-5,4; p<0,001). Además, comparado con el grupo que recibió el tratamiento farmacológico a los 6 meses (media de diferencia entre los grupos 10,6; IC 95 % 8,1-13,2; p<0,001), se encontró que en el grupo con ECP, mientras no tomaba medicación, tuvo una mejoría en 12,3 puntos en la función motora y se reveló en los exámenes neurocognitivos pequeñas disminuciones en el desempeño en estas pruebas, mientras que el grupo de la terapia farmacológica tuvo leves mejorías31.
En un ensayo clínico aleatorizado pero con una muestra limitada de 30 pacientes se comparó el tratamiento farmacológico solo versus ECP-F y se encontró que en el grupo sometido a ECP-F ocurrieron dos efectos adversos (evento cerebrovascular y hardware infectado) y una disminución en cuanto a la fluidez verbal (p = 0,047), aunque al compararlo con el grupo de solo terapia farmacológica no hay diferencia significativa si se excluyen estos efectos adversos (a los 12 meses de seguimiento: p = 0,066 y a los 24 meses: p = 0,096)85. Otro estudio con el mismo número de pacientes al anterior y con EP temprana, encontró que al comparar la seguridad de la terapia farmacológica con la ECP-F, este segundo grupo requirió menos medicación antiparkinsoniana durante todo el estudio y que a 24 meses no hubo empeoramiento de la función motora86.
En cuanto a los síntomas no motores, se ha encontrado que en un principio la ECP mejora la ansiedad, pero en el seguimiento a tres meses no existieron cambios significativos e incluso continuó empeorando (p<0,05), por lo que se concluye que ni la terapia farmacológica ni la ECP pueden evitar la progresión de la EP87,88.
Las distintas zonas blanco para la neuroestimulación han sido comparadas, es el caso de la estimulación del GPI vs NST en los efectos sobre la postura corporal, que utilizó como grupo control individuos sanos y pacientes que eran candidatos para la cirugía pero decidieron no someterse al procedimiento. Se descubrió que la estimulación tanto del GPI como del NST mejoran la estabilidad postural en el postoperatorio sin medicación (p = 0.002), sin embargo, al comparar aquellos pacientes con adecuado tratamiento farmacológico frente a aquellos con estimulación del NST y medicación, estos últimos presentaron una peor estabilidad postural a los 6 meses (p = 0.012), asociado, probablemente, al mayor número de caídas en pacientes con estimulación del NST89.
Por otro lado, el ensayo clínico NSTAPS demostró que tanto la estimulación del NST y del GBI mejoran los síntomas motores, pero al compararlos, fue mayor la mejoría con estimulación del NST (p = 0.04) y se requirió menor dosis de levodopa en este grupo (p<0.001). Asimismo, se halló que para ambos blancos la mejoría persiste en el tiempo al seguirlos por 3 años90,91.
Al momento no se han encontrado diferencias clínicamente significativas en los resultados neuropsicológicos de la ECP-NST y ECP-GPI (71). Un estudio demostró, en cuanto a la seguridad de la ECP, que los eventos adversos graves se produjeron en el 51 % de ECP-GPI y en el 56 % de las personas sometidas a ECPNST, sin diferencias significativas entre los grupos a los 24 meses (p > 0,05 en todos los reportados)50.
CONCLUSIONES
La ECP es una terapia eléctrica que busca estimular zonas específicas en el cerebro con el fin de disminuir los síntomas de la EP. Los pacientes que pueden beneficiarse son aquellos con complicaciones motoras o discinesias debidas al tratamiento farmacológico o en aquellos que no tienen mejoría en sus síntomas, especialmente en el temblor. En ellos, la ECP ha mostrado ser una alternativa costo-efectiva, con una frecuencia de eventos adversos baja y con mejorías en los síntomas motores y no motores.















