Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de la Universidad Industrial de Santander. Salud
Print version ISSN 0121-0807On-line version ISSN 2145-8464
Rev. Univ. Ind. Santander. Salud vol.43 no.1 Bucaramanga Apr./Aug. 2011
HOS y THP-1
Nanotubos de carbono en células
John Jairo Castillo León1, Leidy Viviana Novoa2, Fernando Martínez Ortega1, Patricia Escobar Rivero2
1. Centro de Investigación en Catálisis, Escuela de Química, Universidad Industrial de Santander, Bucaramanga, Colombia.
2. Centro de Investigación en Enfermedades Tropicales, Departamento de Ciencias Básicas, Escuela de Medicina, Universidad Industrial de Santander, Bucaramanga, Colombia.
Correspondencia: John Jairo Castillo León, Centro de Investigación en Catálisis, Centro de Investigación de Enfermedades Tropicales,
Sede Guatiguará UIS Km 2 vía Refugio, Piedecuesta, Santander, Teléfono: 6550805; E-mail: johnleon76@hotmail.com
Recibido: 1 de mayo de 2010 - Aceptado: 30 de junio de 2010
RESUMEN
Introducción: Los nanotubos de carbono (NTC) son estructuras nanométricas utilizadas en el tratamiento de enfermedades, principalmente en la entrega de fármacos para terapias en cáncer. Objetivos: Estudiar la internalización de NTC acoplado a quitosan (NTC-Q) en células de osteosarcoma humano (HOS) y monocitos humanos de leucemia aguda (THP-1). Materiales y métodos: Los NTC solubilizados con quitosan 30% fueron caracterizados espectroscópicamente por UV-Vis, fluorescencia y Raman. Las células HOS y THP-1 fueron tratadas con NTC-Q y se evaluó la internalización por tinción de Giemsa en microscopio de luz y la citotóxicidad utilizando la prueba fluorométrica de Azul de Alamar. Resultados: Los espectros Raman y de fluorescencia mostraron la funcionalización de los NTC con quitosan. Los NTC fueron internalizados por las líneas celulares después de 24 h mostrando una ubicación citoplasmática sin presentar citotóxicidad en ninguna de las células evaluadas. Discusión: Las características presentadas por los NTC-Q les brinda la posibilidad de ser utilizados como transportadores de fármacos. Salud UIS 2011; 43(1): 21-26
Palabras Claves: Nanotubos de carbono, quitosan, internalización celular
Carbon nanotubes-chitosan in HOS and THP-1 cells
ABSTRACT
Introduction: Carbon nanotubes (CNT) are nanometer-sized structures used in medicine in the treatment of diseases, mainly in drug delivery in therapies against cancer. Objectives: To Study the internalization of carbon nanotubes modified with chitosan (CNT-CH) in human osteosarcom cells (HOS) and human monocytes of acute leukemia (THP1). Materials and methods: The CNTs solubilized in chitosan 30% were characterized spectroscopically by UV-Vis, fluorescence and Raman. HOS cells and THP-1 were treated with CNT-CH, the internalization was evaluated by Giemsa staining with light microscopy, and cytotoxicity was determined using Alamar Blue assay. Results: Raman and fluorescence spectra showed the functionalization of the CNT with chitosan. After 24 h the NTC were internalized in the cell lines showing a cytoplasmic location and were not cytotoxic in any of both cell lines types. Discussion: The properties of CNT-CH on cells allowing it to be potentially used as drug carrier Salud UIS 2011; 43(1): 21-26.
Keywords: Carbon nanotubes, chitosan, cell internalization cells, macrophages
INTRODUCCIÓN
Los nanotubos de carbono (NTC) son estructuras cilíndricas de tamaño nanométrico que gracias a sus propiedades fisicoquímicas, electrónicas y biológicas han permitido ser utilizados en casi todos los campos de las ciencias1. En medicina han encontrado aplicación en el tratamiento y diagnóstico de enfermedades, por ejemplo mediante el transporte y entrega de fármacos en cáncer2.
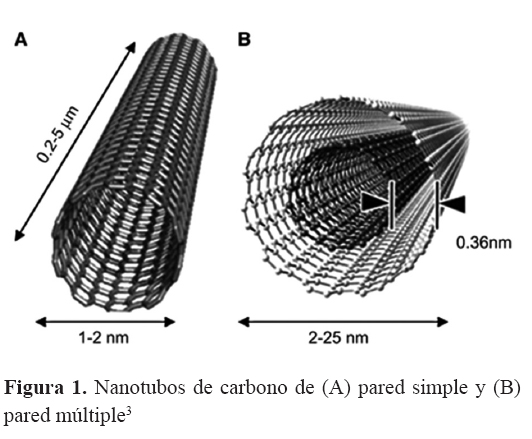
Los NTC se pueden clasificar en dos tipos diferentes según el número de capas: NTC de pared simple (NTCPS) y los NTC (NTCPM) de capa múltiple, formados por capas concéntricas (Figura 1). Los NTCPS están constituidos por átomos de carbono organizados en una red hexagonal cilíndrica. Los extremos pueden estar cerrados por media esfera de fulereno o pueden estar abiertos. Mientras tanto los NTCPM tienen una estructura similar a varios NTC de pared simple concéntrica con diferentes diámetros. En ambos casos la principal característica que da a los NTC sus excelentes propiedades, es que exhiben una relación longitud/diámetro elevada, esto es, su diámetro es del orden de los nanómetros y su longitud puede variar desde unas micras hasta milímetros e incluso algunos centímetros3.
Existen diferentes metodologías para preparar los NTC, entre las cuales se destacan: la vaporización por grafito con pulsos de láser, descarga por arco eléctrico en electrodos de grafito, pirolisis y alta presión de CO3. Sin embargo estas metodologías sufren algunas limitaciones importantes como: producción de mezclas de nanotubos con diferentes longitudes, muchos defectos y variedad de torsiones4. Para superar algunos de estos inconvenientes otras metodologías hacen uso de metales de transición soportados sobre materiales inorgánicos como la sílice y zeolitas4.
El desarrollo de nuevas metodologías para la modificación química de NTC ha estimulado la preparación de nanotubos solubles que pueden ser empleados en varias aplicaciones médicas, entre las cuales el suministro localizado de fármacos para el tratamiento del cáncer es la más promisoria5. La solubilidad y funcionalización de los NTC es un requisito primordial para mejorar las propiedades de biocompatibilidad en aplicaciones biológicas. Los NTC pristinos (puros) son completamente insolubles en todos los solventes, para lo cual es necesaria la funcionalización química de estas nanoestructuras6. Existen varias metodologías para la funcionalización química ya sea covalente o no covalente de los NTC. En la funcionalización covalente los nanotubos primero son oxidados mediante el uso de ácidos fuertes como: acido clorhídrico, sulfúrico y nítrico. Esta oxidación crea defectos en las paredes de los NTC cortándolos, de tal manera que se generan grupos carboxílicos que incrementan la dispersión y solubilidad en soluciones acuosas7. En algunas ocasiones estos defectos superficiales afectan las propiedades estructurales y electrónicas de los NTC7, razón por lo cual se utilizan reacciones no covalentes. La funcionalización no covalente hace uso de biomoléculas y algunos tipos de detergentes, como el SDS y el Triton X-1008. En este caso estas moléculas "envuelven" al NTC mediante interacciones no covalentes como fuerzas de van der Waals e interacciones de apilamiento π-π.
Una vez los NTC han sido funcionalizados con moléculas bicompatibles (ADN, proteínas, enzimas, etc) pueden ingresar por medio de mecanismos como la difusión pasiva o la endocitosis y ser internalizados en el interior de la célula9. El ingreso de los NTC al interior de la célula ha sido aprovechado para utilizarlos como vehículos para entrega y transporte de fármacos. Varios experimentos en células cancerígenas han utilizado a los NTC funcionalizados con fármacos como la anfotericina B6, doxorubicina10, paclitaxel11, etc.
El quitosan es una de las moléculas utilizadas para la funcionalización y solubilización de NTC12 y es un biopolímero (polisacárido) de origen marino, que se encuentra presente en el caparazón de algunos moluscos13. Debido a su origen natural y a su baja toxicidad ha encontrado aplicación en el campo biomédico. Recientemente varios trabajos han utilizado el quitosan para la entrega de fármacos para el tratamiento del cáncer de pulmón12. Las propiedades en la entrega de fármacos del quitosan libre son mejoradas cuando el quitosan es funcionalizado sobre la superficie de NTC13.
Debido a las razones mencionadas anteriormente en este trabajo se utilizó el quitosan funcionalizado no covalentemente a los NTC para estudiar la internalización en dos tipos de líneas celulares: HOS y THP1.
METODOLOGÍA
Solubilización y funcionalización de NTC-Q
Los NTC de pared simple fueron adquiridos comercialmente (Sigma, USA) y funcionalizados con una solución acuosa de quitosan 30% mediante ultrasonido durante 1 hora. La solución NTC-Q fue centrifugada durante 20 minutos a 2800 rpm. El sobrenadante fue retirado cuidadosamente y el sólido fue descartado, debido a que en el sólido están presentes impurezas y conglomerados insolubles de NTC14. Luego los NTC-Q fueron almacenados a 4°C para los ensayos biológicos. Finalmente los NTC-Q fueron caracterizados por espectroscopia UV/Vis, de fluorescencia y de Raman. Los resultados de la caracterización de UV/vis fueron obtenidos y analizados por medio de sus respectivos espectros expresados en unidades de absorbancia contra longitud de onda (nm), en la espectroscopia de fluorescencia los espectros se obtuvieron en unidades arbitrarias de fluorescencia contra longitud de onda (nm) y en el caso de la espectroscopia Raman unidades arbitrarias de intensidad contra desplazamiento químico (cm-1).
Líneas celulares
Las líneas celulares de osteosarcoma humano (HOS, ATCC) y los monocitos humanos de leucemia aguda (THP-1, ATCC), se cultivaron en medio RPMI 1640 con 10% de suero bovino fetal inactivado (SBFi), 0,1% de penicilina-estreptomicina a 37°C, 5% CO2, 95% mezcla-aire.
Prueba de internalización
Las células HOS fueron colocadas en placa de 24 pozos con laminillas circulares en el fondo por 24 h. Las células THP-1 fueron colocadas en las mismas condiciones por 72 h adicionando forbol miristato acetato (PMA) para lograr su transformación al fenotipo adherente. Ambas líneas celulares fueron tratadas con NTC-Q a una concentración de 0,165 mg/mL por un periodo de 4 h a 48 h a 37°C, 5% de CO2, 95% mezcla-aire. Posteriormente, se determinó el porcentaje de células que internalizaban el cual fue calculado por recuento de 300 células en microscopio luz, en células fijadas con metanol y coloreadas con Giemsa. Se consideró como internalización positiva toda célula en la que se observaba claramente la agrupación de NTC-Q intracelularmente.
Prueba de citotoxicidad
Las células HOS y células THP1 transformadas con PMA en placa de 96 pozos fueron tratadas con cinco diferentes concentraciones de NTC-Q (0,33-0,021 mg/mL) durante 24 h a 37°C, 5% CO2, 95% mezcla-aire. Células controles fueron tratadas con miltefosina o dejadas con medio de cultivo sin compuesto. Como blanco se utilizaron pozos que contenían AB sin células. La citotoxicidad fue determinada por el método fluorométrico de Azul de Alamar (AlamarBlue Biosurce, AB). Las células fueron incubadas con AB y se cuantificó la intensidad de fluorescencia (IF) utilizando un fluorométro (Perkin Elmer L5) con lecturas a una longitud de onda de excitación de 560 nm y de emisión de 590 nm. El porcentaje de citotoxicidad se determinó con la formula (1-(IF grupo tratado / IF grupo control) * 100).
RESULTADOS Y DISCUSIÓN
Solubilización y caracterización espectroscópica de NTC-Q
Los NTC de pared simple fueron solubilizados mediante sonicación y centrifugación de una solución acuosa de quitosan 30%. En la (Figura 2) se observan los NTC-Q totalmente homogenizados, lo cual demuestra la solubilización de los NTC. Similares resultados se obtuvieron en otros trabajos realizados con quitosan15,16.
El análisis por espectroscopia UV/Vis mostró una banda de máxima absorbancia a 265 nm característica de los fonones resonantes y de las transiciones electrónicas de los electrones pi presentes en la estructura del grafeno. Esta banda característica ha sido observada en otros trabajos con NTC14.
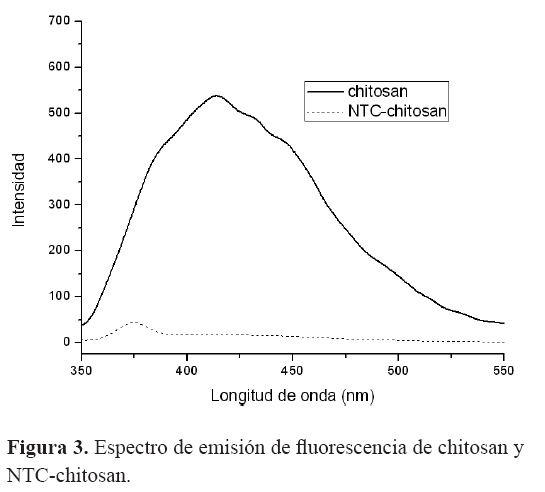
Una de las características de los NTC es el efecto de apagamiento de la fluorescencia (quencher) cuando interacciona con compuestos que tienen fluorescencia17. Este efecto fue observado en este trabajo. En la (Figura 3) se aprecia la emisión del quitosan a una λ= 418 nm, esta emisión desaparece o es apagada casi en su totalidad cuando el quitosan está unido al NTC.
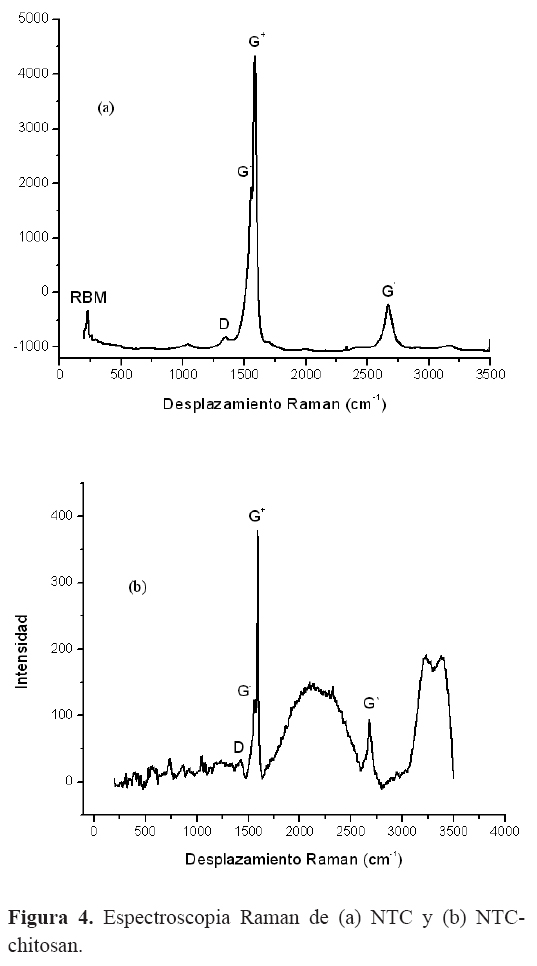
La espectroscopia Raman es una herramienta muy útil en la cual la muestra se excita con una laser de energías entre 2,60 y 1,17 eV (477 y 1064 nm respectivamente), precisamente en el rango de algunas de las transiciones ópticas de los NTC, por lo que se puede esperar que esta espectroscopia aporte información sobre la estructura de los NTC18. Los espectros Raman de los NTC y NTC-Q se pueden observar en la (Figura 4) , se identificaron las bandas características D y G, denominadas, banda de desorden inducido y banda de elongación o vibración tangencial respectivamente. La banda D es indicadora de la presencia de defectos en las paredes, de manera que de la relación de intensidades entre las bandas D y G puede afirmarse que el NTC presenta quitosan en sus alrededores. La relación de intensidades de las bandas G (vibración tangencial) y D (desorden inducido) de NTC y NTC-Q fueron de 0,0637 y 0,096 respectivamente. El aumento en el valor de la relación de las intensidades ID/IG es un indicio de la funcionalización de los NTC con el quitosan. Esta relación de intensidades entre las bandas D y G ha servido también para evaluar cuantitativamente la funcionalización de NTC con agentes dispersantes como dodecil bencenosulfonato de sodio (SDBS)19.
Las células HOS y THP-1 internalizaron los NTC-Q
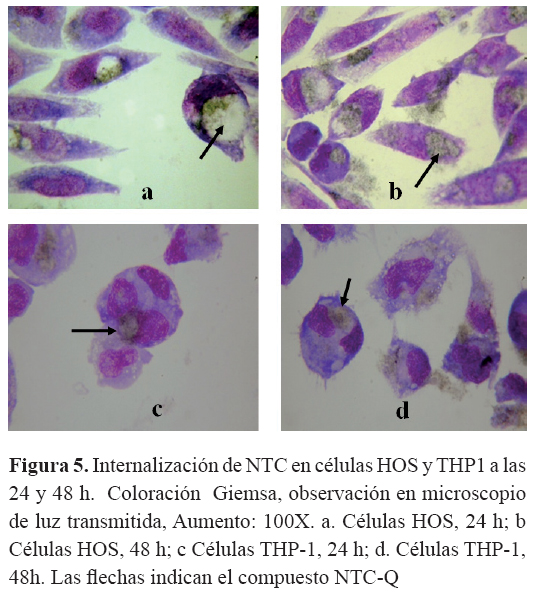
Las células HOS y THP-1 internalizaron los NTC-Q con algunas diferencias. En las células HOS, se observó internalización del NTC-Q a partir de las 4 h de incubación, siendo esta mayor después de 24 y 48 h de incubación con % de internalización de 8,0, 42,3% y 78,0% respectivamente. Las células THP-1 mostraron una agrupación intracelular de NTC-Q a las 24 y 48 h de incubación con % de internalización de 36,3 y 65,7 % respectivamente. La internalización de los NTC-Q por las células HOS se observa en la (Figura 5 a y b) y por las células THP-1 en la (Figura 5 c y d). Ambas líneas celulares presentaron una única ubicación intracelular del compuesto en una posible vacuola, sin observarse dispersión de los NTC en toda la estructura celular.
La internalización de NTC de pared simple funcionalizados con acido fólico, ha sido reportada en varias líneas celulares como en células de carcinoma hepato-celular humano (Hep-G2), donde se registra internalización desde la primera hora completándose a la tercera hora de incubación21. Sin embargo, no se reporta una única agrupación de los NTC en el citoplasma, esta característica en nuestros resultados puede estar dada por la funcionalización de los NTC con el quitosan, el cual como se ha reportado en la literatura forma protuberancias en la superficie de los nanotubos de carbono provocando la formación de paquetes unidos por quitosan22. 0,165 mg/mL
Los NTC-Q no fueron citotóxicos
Los NTC-Q no fueron citotóxicos a la concentración utilizada en los ensayos de internalización (0,165 mg/mL). La máxima concentración evaluada en este trabajo, de 0,33 mg/mL, presentó un bajo porcentaje de toxicidad en las células HOS y THP1 siendo éste de 31,46 y 8,32 % respectivamente. Concentraciones menores no fueron tóxicas para las células. La miltefosina, utilizada como control de muerte, fue tóxica para las células presentando a concentraciones tan bajas como 0,081 mg/mL un porcentaje de muerte celular mayor del 99 % para HOS y THP-1.
Son diversos y discutidos los resultados que se reportan en la literatura sobre la toxicidad de los NTC especialmente aquellos que utilizan el método del bromuro 3-(4,5-dimetiltiazol-2-ilo)-2,5-difeniltetrazol (MTT) como prueba. Se plantea que muchos de los resultados reportados podrían ser erróneos ya que al parecer los NTC podrían interferir con la formación del compuesto coloreado formazan que se produce al reducirse el MTT por acción de enzimas mitocondriales de las células vivas24 Estudios realizados en células embrionarias de riñón humano (HEK293), utilizando como prueba de citotoxicidad el método MTT, reportan una disminución de la viabilidad celular dependiente de la dosis de NTC, pero en concentraciones mucho menores que las reportadas en este trabajo (de 0,78125 μg/mL hasta 200 μg/mL) 23.
CONCLUSIÓN
Una vez preparado y caracterizado los NTC funcionalizados con quitosan, se determinó que estos son internalizados sin presentar toxicidad en algunas células de mamífero. Este resultado abre el camino para la utilización de estos nanocompuestos como vectores de fármacos o de otros tipos de biomoléculas para el tratamiento de cáncer y de diferentes enfermedades que involucren microorganismos intracelulares.
AGRADECIMIENTOS
Los autores agradecen a COLCIENCIAS por la financiación de este trabajo con el proyecto 1102254921468 y por la beca de doctorado de JC.
CONFLICTOS DE INTERÉS
Los autores manifestamos que durante el desarrollo de este trabajo no se presentó conflicto de interés alguno.
REFERENCIAS
1. Fukumori YI. Nanoparticles for cancer therapy and diagnosis. Adv Pow Tech 2006; 17: 1-28. [ Links ]
2. Ji SR, Zhang B, Yang F, Xu J, Long J, Jin C, Fu D, Ni Q, Yu X. Carbon nanotubes in cancer diagnosis and therapy. Biochem et Biophys Acta 2010; 1806: 29-35. [ Links ]
3. Dresselhaus G, Dresselhaus M, Avouris P. Carbon nanotubes: Synthesis, structure, properties and applications. Springer-Verlag 2001, Berlin. [ Links ]
4. Huber JG, Romero JM, Rosolen JG, Luengo CA. Quim Nova 2004; 27: 986-992. [ Links ]
5. Liu Z, Cheng C, Davis S, Sherlock S, Cao Q, Chen X, Dai H. Drug delivery with carbon nanotubes for in vivo cancer treatment. Cancer Res 2008; 68: 6652- 6660. [ Links ]
6. Wu W, Pastorin G, Klumpp C, Benincasa M, Briand JP, Gennaro R, Prato M, Bianco A. Targeted delivery of amphotericin B to cells using functionalised carbon nanotubes. Angewandte Chem Int 2005; 44: 6358-6352. [ Links ]
7. Liu J, Rinzler A, Dai H, Hafner J, Bradley J, Boul K, Lu J, Iverson T, Shelimov K, Huffman C, Rodriguez-Macias C, Shon Y, Lee T, Colbert D, Smalley R. Fullerenes Pipes. Science 1998; 280: 1253-1256. [ Links ]
8. Rastogi R, Kaushal R, Tripathi S, Sharma A, Kaur I, Bharadwaj L. Comparative study of carbon nanotubes dispersion using surfactants. J Colloid Interface Science 2008; 328: 421-428. [ Links ]
9. Kang B, Chang S, Dai Y, Yu D, Chen D. Cell response to CNT: Size-Dependent intracellular uptake mechanism and subcellular fate. Small 2010; 6: 2362-2366. [ Links ]
10. Heister E, Neves V. Triple functionalisation of single-walled carbon nanotubes with doxorubicin, a monoclonal antibody, and a fluorescent marker for targeted cancer therapy. Carbon 2009; 47: 2152-2160. [ Links ]
11. Zhang X, Meng L, Lu Q. Targeted delivery and controlled release of doxorubicin to cancer cells using modified single wall carbon nanotubes. Biomaterials 2009; 30: 6041-6047. [ Links ]
12. Mohapatra S, Kumar A. Method of drug delivery by carbon nanotube-chitosan nanocomplex. US20080214494. [ Links ]
13. Beg S, Rizwan M, Sheikh A, Hasnain S, Anwer K, Kohli K. Advancement in carbon nanotubes: basics, biomedical applications and toxicity. J Pharm Pharmacol 2010. [ Links ]
14. Attal S, Thiruvengadathan R, Regev O. Determination of the concentration of single-walled carbon nanotubes in aqueous dispersion using UV-Visible absorption spectroscopy. Anal Chem 2006; 78, 8098-8104. [ Links ]
15. Zhang M, Smith A, Gorski W. Carbon nanotube-chitosan system for electrochemical sensing based on dehydrogenase enzymes. Anal Chem 2004; 76: 5045-5050. [ Links ]
16. Takahashi T, Luculescu C, Uchida K, Ishii T, Yajima H. Dispersion behaviour and spectroscopic properties of single-walled carbon nanotubes in chitosan acidic aqueous solutions. Chem Lett 2005; 34: 1516-1517. [ Links ]
17. Zhu Z, Tang Z, Philips J, Yang R, Wang H, Tan W. Regulation of Singlet Oxygen generation using single walled carbon nanotubes. J Am Chem Soc 2008; 130: 10856-10857. [ Links ]
18. Domingo C, Santoro G. Raman spectroscopy of carbon nanotubes. Óptica Pura y Aplicada 2007; 40: 175-186. [ Links ]
19. Salzmann Ch, Chu B, Tobias G, Llewellyn S, Green M. Quantitative assessment of carbon nanotubes dispersions Raman spectroscopy. Carbon 2007; 45: 907-912. [ Links ]
20. Ren H, Cheng X, Liu J, Gu N, Huang X. Toxicity of single walled carbon nanotubes: How we were wrong?. Materials Today 2010; 13: 6-8. [ Links ]
21. Kang B, Yu D, Dai Y, Chang S, Chen D, Ding Y. Cancer-cell targeting and photoacoustic therapy using carbon nanotubes as "Bomb" agents. Small. 2009; Doi: 10.1002/smll.200801820. [ Links ]
22. Liu Y, Tang J, Chen X, Xin J.H. Decoration of carbon nanotubes with chitosan. Carbon N.Y. 2005; 43: 3178-3180. [ Links ]
23. Cui D, Tian F, Ozhan C.S, Wang M, Gao H. Effect of single wall carbon nanotubes on human HEK293 cells. Toxicol Lett 2005; 155: 73-75. [ Links ]
24. Worle-Knirsch J.M, Pulskamp K, Krug H.F. Oops They did it again! Carbon nanotubes hoax Scientists in viability assays. Nano Lett 2006; 6(6): 1261-126. [ Links ]