Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de la Universidad Industrial de Santander. Salud
Print version ISSN 0121-0807On-line version ISSN 2145-8464
Rev. Univ. Ind. Santander. Salud vol.43 no.3 Bucaramanga Oct./Dec. 2011
MicroARNs: una visión molecular
Y. Vladimir Pabón-Martínez1
1. Grupo de Investigación de Inmunología y Epidemiología Molecular. Departamento de Ciencias Básicas de la Escuela de
Medicina y Escuela de Bacteriología y Laboratorio Clínico. Grupo "Unit of Molecular Cell Biology and Gene Therapy Science"
del Instituto Karolinska de Estocolmo, Suecia.
Correspondencia: Y. Vladimir Pabón-Martínez. Carrera. 32 No. 29-31. Departamento de Ciencias Básicas. Facultad de Salud.
Universidad Industrial de Santander. Email: yavlapm@yahoo.es por vladimir.pabon@ki.se
Recibido: 22 de Septiembre de 2011- Aceptado: 3 de Octubre de 2011
RESUMEN
Los microARNs son ARN pequeños de aproximadamente 22 nucleótidos de longitud que participan en la regulación de muchos procesos celulares y, su alteración está asociada con el desarrollo de diferentes patologías, especialmente cáncer. Gracias al uso de las herramientas de bioinformática es posible determinar su distribución en el genoma y sus funciones en diferentes tejidos. La mayoría de microARNs son producidos en una vía canónica a partir de un transcripto primario largo, en un proceso secuencial de dos reacciones guiadas principalmente por dos enzimas, Drosha en el núcleo y Dicer en el citoplasma. Sin embargo, actualmente han sido descritas algunas vías no canónicas de generación de microARNs. El objetivo de esta revisión es describir el proceso de generación de microARNs y la maquinaria involucrada en su generación con el propósito de lograr alcanzar un mejor entendimiento de los diferentes procesos en los cuales están involucrados. Salud UIS 2011; 43 (3): 289-297
Palabras Clave: microARNs, ARN de cadena doble, complejo silenciador inducido por ARN, transcripción genética, procesamiento postranscripcional del ARN
MicroRNA (miRNA): A molecular view
ABSTRACT
MicroRNAs are small RNAs of approximately 22 nucleotides in length that participate in the regulation of many cellular processes and it alteration is associated with the development of different pathologies in particular, cancer. Using bioinformatics tools is possible determine their wide distribution in the genome and their functions in different tissues. Mostly of microRNAs are produced in a canonical way from a long primary transcript, in a sequential process of two reactions guided mostly by two enzymes: Drosha in the nucleus and Dicer in the cytoplasm. However, it has been described some pathways non-canonical for the generation of microRNAs. The aim of this review is to describe the generation process of microRNAs and the machinery involved in their generation for the purpose of achieving a better understanding of the different processes they are involved. Salud UIS 2011; 43 (3): 289-297
Keywords: MiRNA, double-stranded RNA, RNA-induced silencing complex, genetic transcription, post-transcriptional RNA processing
INTRODUCCIÓN
Los microARNs regulan el procesamiento postranscripcional del ARN, mediante el apareamiento de bases con su ARN mensajero (ARNm) complementario, conduciendo a la represión de la transcripción o al clivaje del ARNm. Inicialmente, fueron identificados en Caenorhabditis elegans como reguladores de su desarrollo1. Actualmente se conoce que son expresados en forma endógena en la mayoría de eucariotas. Sin embargo, la expresión de microARNs particulares es altamente específica de ciertos estados del desarrollo o de un tejido en particular. Los microARNs inicialmente son procesados como transcriptos primarios en el núcleo por el complejo formado por la proteína de la región crítica del gen 8 del síndrome DiGeorge (DGCR8, del inglés DiGeorge syndrome critical region gene 8 protein)2 y Drosha3, para luego ser exportados al citoplasma por la exportina 54. Finalmente en el citoplasma son procesados por Dicer5 y por el complejo silenciador inducido por ARN (RISC, del inglés RNAInduced Silencing Complex)6, causando la represión de la transcripción del ARNm o el silenciamiento genético por medio del apareamiento con su ARNm blanco7. El conocimiento y entendimiento de la generación de los microARNs es por tanto una necesidad actual, dada la creciente información disponible sobre este tema.
ARN pequeños no codificantes
Existen diversos ARN pequeños eucariotas con capacidad de silenciar genes. Estos ARN tienen una longitud de aproximadamente 20 a 30 nucleótidos y se asocian con miembros de la familia de las proteínas Argonauta para ser guiados a su secuencia blanco o complementaria en el ARNm. Conseguir la reducción de la expresión de estos genes8. Al menos tres ARN pequeños son codificados en nuestro genoma: los microARNs, los ARN interferentes pequeños (siARN, del inglés small interfering RNA) endógenos y los ARN asociados a Piwi (piARN, del inglés Piwi-interacting RNA)8 (Tabla 1).
MicroARNs
Los microARNs son ARN pequeños de aproximadamente 22 nucleótidos de longitud, no codificantes para proteínas y generados de transcriptos endógenos que pueden formar estructuras en forma de horquilla9. Los microARNs conforman una gran familia de genes reguladores postranscripcionales que controlan muchos procesos celulares y del desarrollo en eucariotas, cumpliendo una gran cantidad de funciones. Se estima que el 30% de todos los genes humanos son regulados por mecanismos dependientes de microARNs10 y que un solo microARN puede regular alrededor de 200 diferentes transcriptos que pueden funcionar en diferentes vías en la célula11, así como que un mismo ARNm puede ser regulado por múltiples microARNs12. Muchos genes de microARNs humanos están frecuentemente localizados en sitios frágiles y regiones genómicas asociadas con cáncer, por cuanto su alteración está relacionada con su desarrollo13. Gracias a métodos computacionales y al uso de la bioinformática ha sido posible determinar su amplia distribución en el genoma y sus funciones en diferentes tejidos y en la regulación de la expresión de los genes. Actualmente, existe una gran cantidad de datos e información sobre microARNs, prueba de ello son las 1527 secuencias de microARNs de Homo sapiens que han sido descritas y almacenadas en la base de datos miRBase (revisado noviembre 2011)14.
Importancia biológica de los microARNs
Los microARNs tienen diferentes funciones regulatorias a nivel del desarrollo y proliferación celular en diferentes organismos. De igual forma, los microARNs median diferentes procesos en tumorogénesis, como inflamación, regulación del ciclo celular, respuesta a estrés, diferenciación, apoptosis e invasión. En células madre de tejidos somáticos, los microARNs tienen diferentes funciones incluyendo la regulación de múltiples pasos de la hematopoyesis, modulación de la miogénesis y cardiogénesis, diferenciación osteogénica y de la piel15. Los microARNs también actúan como oncogenes y genes supresores de tumor, estos microARNs son denominados en el idioma inglés como "oncomirs"16 y presentan diferentes patrones en sus funciones, tasa de evolución, expresión, distribución cromosómica, tamaño molecular, factores de transcripción y blancos17. Dada la importancia de los microARNs en los procesos de tumorogénesis y su expresión en enfermedades específicas, tienen un gran potencial como blancos terapéuticos y nuevos biomarcadores para pronóstico y diagnóstico de cáncer18. Por lo que se ha propuesto que la manipulación de la actividad y biogénesis de los microARNs como una estrategia para el desarrollo de terapias eficaces contra el cáncer19.
Enfermedades asociadas a microARNs
Diferentes mecanismos de alteración relacionados con microARNs han sido descritos en enfermedades20, entre ellas alteraciones en el número de copias y localización de microARNs genómicos; muchos microARNs están ubicados en regiones asociadas con cáncer o sitios frágiles, por lo cual son sensibles a sufrir alteraciones debido a amplificaciones, traslocaciones o delecciones de estas regiones cromosómicas. Por ejemplo, el grupo del miARN15a/16-1 está localizado en un locus genómico deleccionado frecuentemente, el cual contiene una región con un gen supresor de tumor en leucemia linfoide de células B crónica, el grupo mir-17- 92 es amplificado en linfoma, lo mismo que el mir-26a en glioblastoma y el mir-17-91 traslocado en leucemia linfoblástica aguda de células T (revisado en 20).
Alteraciones en la regulación transcripcional de los microARNs también resultan en enfermedad; algunos microARNs expresados autónomamente tienen regiones promotoras que permiten una expresión alta de los microARNs en un tipo de células de manera específica, y pueden incluso conducir a la expresión de niveles altos de oncogenes en casos de traslocación cromosomal, ejemplo de este mecanismo de alteración es el mir-142 que se localiza en el cromosoma 17, en el punto de una traslocación t(8;17), el cual está asociado con el desarrollo de leucemia de células B agresiva20.
Así también, muchos microARNs están asociados con la desregulación de ellos mismos y el desarrollo de cáncer; como por ejemplo, la familia del miARN let-7 está asociada con cáncer gástrico, de próstata, de colon, de ovario, melanoma, linfoma; el grupo del miR-15a/16-1 está asociado con linfoma, mieloma múltiple, cáncer de próstata y pancreático; el miR-26a está asociado con linfoma, carcinoma hepatocelular, carcinoma de tiroides y glioblastoma; el miR-155 está asociado con linfoma, cáncer de colon y cáncer de cerebro (revisado en 20).
Localización y estructura de los microARNs en el genoma
Los genes codificadores para microARNs pueden estar localizados en diferentes regiones del genoma8,21. Con base en lo cual son clasificados en: (i) microARNs exónicos localizados en transcriptos no codificantes, (ii) microARNs intrónicos localizados en transcriptos no codificantes, (iii) microARNs intrónicos localizados en transcriptos codificantes para proteínas, (iv) microARNs exónicos localizados en transcriptos codificantes para proteínas22. Adicionalmente, existen también algunos microARNs ubicados en unidades transcripcionales que son expresados en grupo23.
Biogénesis y procesamiento de los microARNs
En una gran proporción los microARNs son generados a partir de un transcripto primario largo, en un proceso secuencial de dos reacciones las cuales son guiadas por Drosha y Dicer, en la llamada vía canónica de generación de microARNs. Sin embargo, actualmente han sido descritos microARNs generados por vías alternas llamadas vías no canónicas9, muchos de los microARNs procesados por estas vías no satisfacen la definición clásica de microARNs.
Vía canónica de biogénesis de microARNs
En la vía canónica los microARNs son inicialmente transcriptos en el núcleo a partir de precursores largos de ARN llamados microARNs primarios o (pri-microARNs, del inglés primary transcritps). La transcripción de los genes de microARNs generalmente es mediada por la ARN polimerasa II24; sin embargo, un grupo menor de microARNs asociados con repeticiones Alu pueden ser transcriptos por la ARN Polimerasa III25. Los (pri-microARNs) generados por la ARN polimerasa II tienen usualmente varias kilobases de longitud y contienen estructuras en forma de horquilla compuesta de un tallo y un bucle3.
En el primer paso de la maduración de los primicroARNs, Drosha cliva el tallo de la estructura larga de ARN en forma de una horquilla pequeña y permite su liberación3. Para ello, Drosha necesita un cofactor, DGCR82; juntos Drosha y DGCR8 forman el complejo microprocesador2. Un pri-miARNs típico en metazoos consiste de un tallo de aproximadamente 33 pares de base, un bucle terminal y segmentos flanqueantes de ARN de cadena sencilla (ssARN, del inglés single strand RNA). La proteína DGCR8 interactúa con los pri-microARNs a través de los segmentos de ssARN y el tallo, permitiendo que Drosha realice el clivaje aproximadamente 11 pares de bases, contadas a partir de la unión ARN de cadena sencilla - ARN de cadena doble (ssARN-dsARN, del inglés single strand – double stranded RNA).
El complejo microprocesador genera una horquilla de 70 nucleótidos, llamado precursor de microARNs (pre-microARNs, del inglés precursor miRNA). Los pre-microARNs poseen dos nucleótidos colgantes en su extremo 3' y un grupo fosfato en el extremo 5', lo cual es característico de los ARN procesadas por la Ribonucleasa III (RNasa, del inglés Ribonuclease III). Finalmente, los pre-microARNs son exportados del núcleo al citoplasma por medio de la exportina 54.
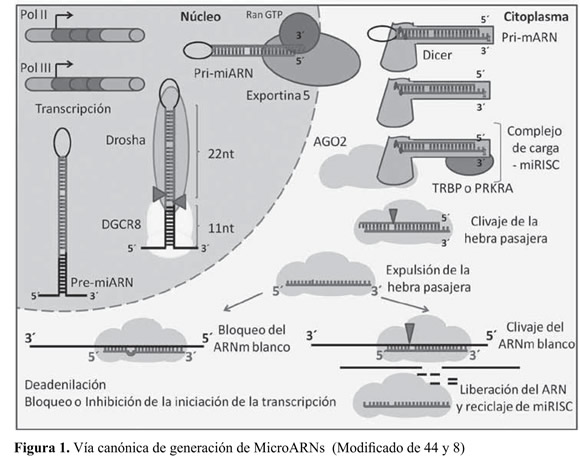
En el citoplasma, los pre-microARNs son reconocidos por el complejo de procesamiento de pre-microARNs formado por Dicer, la proteína de unión a ARN en respuesta a trans-activación (TRBP, del inglés TAR RNA-binding protein) y la proteína quinasa activadora dependiente de ARN de cadena doble inducible por interferón (PRKRA, del inglés protein kinase, interferon-inducible double stranded RNA dependent activator). En el complejo de procesamiento de pre-microARNs Dicer cliva los pre-microARNs cerca del bucle terminal, generando un dúplex de microARN maduro de aproximadamente 22 nucleótidos (microARN:microARN*), este dúplex contiene una cadena madura de microARN y su cadena complementaria, la cadena pasajera (microARN*)6. Posteriormente, este complejo se ensambla con la proteína Argonauta 2, para formar el complejo silenciador inducido por microARNs (miRISC, del inglés miRNA-induced silencing complex), el cual selecciona la cadena madura o guía25. La cadena guía es la responsable de dirigir el silenciamiento. Notablemente, la estabilidad termodinámica del extremo 5' de las cadenas que conforman el dúplex de microARN maduro determina la identidad de la cadena guía y la cadena pasajera26. Sin embargo, dependiendo de la complementariedad perfecta o incompleta de la cadena de microARN a su blanco, el complejo MiRISC puede conducir al clivaje y degradación del ARNm o a la inhibición de la transcripción. En caso de la inhibición de la transcripción, el ARNm reprimido es traslocado a los cuerpos P, donde puede ser destruido o relocalizado en la maquinaria transcripcional bajo la expresión de una señal celular especifica27. La complementariedad perfecta de bases entre la secuencia semilla del microARN (del segundo al octavo nucleótido del extremo 5') y la secuencia complementaria del extremo 3'UTR es lo que permite que los microARNs modulen la expresión génica7. El complejo miRISC puede inhibir la expresión de los ARNm blancos por dos mecanismos: (1) remoción de la poliadenilación del extremo 3' del ARNm, fomentando la actividad de las deadenilasas, seguidas por la degradación del ARNm; y (2) bloqueando el paso de la iniciación o elongación de la traducción, inhibiendo el factor eucariótico de la elongación o causando un estancamiento del ribosoma28 (Figura 1).
Vías no canónicas de generación de MicroARNs
Gracias al avance en las tecnologías de secuenciación ha sido posible generar gran cantidad de información que ha sido analizada, ordenada y procesada obteniéndose datos valiosos sobre subclases de microARNs en diversos tipos de células de diferentes organismos, muchos de los cuales sólo cumplen parcialmente la definición clásica de microARNs. La mayoría de estos análisis, clasifican los microARNs teniendo en cuenta únicamente, dos criterios: la expresión de un ARN de aproximadamente 22 nucleótidos y la presencia de un precursor en forma de horquilla23. Actualmente, se ha descrito que la mayoría de los mamíferos, y la especie H. sapiens, utilizan la vía canónica para la generación de microARNs. Sin embargo, para organismos como Drosophila megaloblaster, Giardia lamblia, Zebrafish y Murine Gamma-herpesvirus 68 se ha descrito la producción de microARNs por vías no canónicas. Por lo cual, es de esperar que las células usen una variedad de transcriptos como fuentes de microARNs y utilicen diferentes mecanismos de generación. Las vías no canónicas son una prueba de la flexibilidad y habilidad de las células para generar estructuras en forma de horquilla como pre-microARNs29-33 (Tabla 2).
Diferencias y similitudes entre la vía canónica y las vías no canónicas de generación de microARNs
Las vías canónicas y no canónicas de generación de microARNs incluyen en su maquinaria dos enzimas: Drosha y Dicer, que realizan su efecto a nivel del núcleo y citoplasma, respectivamente. Sin embargo, la principal diferencia entre la vía canónica y las vías no canónicas, es que tan solo los microARNs de ambas proteínas, Drosha y Dicer; a diferencia de las vías no canónicas, que pueden utilizar tan solo una de estas dos proteínas. De acuerdo a la utilización de la enzima Drosha o Dicer, los microARNs generados por vías no canónicas pueden ser agrupados en dos grandes categorías: (i) microARNs producidos por vías no canónicas independientes de Drosha y (ii) microARNs producidos por vías no canónicas independientes de Dicer (Tabla 2).
Maquinaria involucrada en el procesamiento de los microARNs
Los microARNs necesitan de diferentes proteínas en su generación y procesamiento. Las principales proteínas que participan en la vía de generación de los microARNs son: Drosha, Dicer, Argonauta 234.
Drosha. Es una proteína de la familia RNasa III y es la encargada de catalizar el primer clivaje del primicroARNs para producir el pre-microARN. Posee un dominio rico en Prolina, un dominio rico en Arginina- Serina, dos dominios catalíticos RNasa III y un dominio de unión a ARN de cadena doble (dsRBD, del inglés double-stranded RNA-binding domain)5.
Dicer. Es una proteína de la familia RNasa III como Drosha. Dicer es la encargada de procesar inicialmente los dsARN en pequeños fragmentos de siARNs o microARNs35; así como también de cargar los ARN pequeños en RISC. Dicer posee un dominio DEAD, un dominio helicasa, un dominio DUF283, un dominio PAZ (Piwi–Argonaute–Zwille), dos dominios RNasa III en tándem y un dominio de unión a ARN de cadena doble36. El dominio PAZ se encuentra en Dicer y en las proteínas de la familia Argonauta, y es el sitio de anclaje para el extremo 3' de la cadena guía. La longitud de los microARNs y los siARNs producidos por Dicer es fijada por la distancia entre el dominio PAZ y los dominios RNasa III, la cual es determinada por la longitud de la hélice del dominio conector formado en la estructura tridimensional de la molécula37.
Argonauta 2. Existen cuatro proteínas Argonauta en humanos. Sin embargo, solo la Argonauta 2 tiene la capacidad de clivaje y en el complejo miRISC es la encargada de cortar el miARN*38. Las proteínas Argonautas están compuestas de tres dominios: dominio PAZ, dominio MID y dominio PIWI. El dominio PAZ es el encargado de anclar el extremo 3' de la cadena de ARN tanto en microARNs como en siARNs39. A su vez, el dominio MID ancla el nucleótido terminal del extremo 5'40.
Cuerpos P. Los cuerpos P o cuerpos GW, son gránulos citoplasmáticos que se asocian con Argonauta y pueden ser definidos como sitios de almacenamiento de ARNm; el correcto direccionamiento hacia los cuerpos P de la proteína Argonauta está influenciado críticamente por la proteína del choque térmico 90 (Hsp90, del inglés heat-shock protein 90)41. Estos gránulos son ricos en proteínas implicadas en el catabolismo del ARNm (deadenilación, hidrolisis de la cápsula y degradación del ARNm) y represión de la traducción42.
Algunas proteínas accesorias juegan un papel importante en la acción y biogénesis de los microARNs, entre ellas: DGCR8, Exportina 5, TRBP y PRKRA.
Proteína de la región crítica del gen 8 del síndrome DiGeorge. Es una proteína de unión a dsARN, e inicialmente fue identificada en humanos como una proteína codificada por un gen localizado en el cromosoma 22 que está deleccionado en pacientes con enfermedad congénita del Síndrome de DiGeorge. DGCR8 es la encargada de proveer el anclaje para Drosha durante el procesamiento inicial de clivaje de los pri-microARNs. El Análisis de la estructura cristalina de DGCR8 demostró que la proteína DGCR8 posee un dominio WW y dos dominios de unión a dsARN (dsRBDs, del inglés double-stranded RNAbinding domain); los dsRBDs tienen una estructura en plegamiento αβββα y es la región encargada de interaccionar con el dsARN. DGCR8 tiene su proteína homóloga en plantas, Pasha43.
Exportina 5. Es una proteína miembro de la familia de las carioferinas que son proteínas encargadas de transporte nuclear, tanto de la exportación como de la importación de moléculas hacia y desde el núcleo al citoplasma. La exportina 5 hace parte de las proteínas exportadores y está encargada de transportar a través del poro nuclear los microARNs desde el núcleo hacia el citoplasma en la presencia del cofactor Ran-GTP44. La exportina 5 reconoce los tallos de dsARN mayores de 14 pares de bases junto con un extremo colgante corto 3' (1–8 nucleótidos)4. La exportina 5 se une cooperativamente al microARN y al cofactor Ran-GTP, una vez en el citoplasma, el microARN es liberado y el GTP es hidrolisado4.
Proteína de unión a ARN en respuesta a transactivación
(TRBP, del inglés TAR RNA-binding protein) y la proteína quinasa activadora dependiente de ARN de doble cadena inducible por interferón (PACT o PRKRA, del inglés protein kinase, interferon-inducible double stranded RNA dependent activator). Actúan como cofactores de Dicer, estabilizándolo y contribuyendo a la formación de RISC45, un modelo en el cual las dos proteínas interactúan directamente la una con la otra asociadas a Dicer, sin embargo este modelo no es aceptado totalmente debido a que se ha reportado experimentalmente el procesamiento de los microARNs en la presencia o ausencia de estas dos proteínas46.
Características comunes de las vías de generación de microARNS y siARN
Una característica común del ARN interferente y todas las vías de silenciamiento mediado por ARN pequeños es la asociación de un pequeño ARN silenciador (ARN guía) con una proteína de la familia Argonauta. Posterior a la producción de los pre-microARNs47 y los precursores de siARN, ambos son procesados por Argonauta, el corazón de RISC. En este paso la cadena guía es cargada en Argonauta y la cadena pasajera es disociada y destruida36. RISC utiliza la cadena guía de ARN, como una guía para el apareamiento de bases con la secuencia blanco específica en el ARNm, con el propósito de inhibir la traducción o inducir la degradación del ARN blanco.
La incorporación de los siARN y los microARNs en RISC requiere la presencia de grupos fosfato en el extremo 5' y de dos nucleótidos colgantes en el extremo 3'48. El descubrimiento del dominio PAZ, un dominio de unión a ARN que específicamente reconoce el extremo 3' de ssARN sugirió que este funcionaba como un módulo de anclaje al 3' de la cadena guía de ARN dentro de RISC. El grupo fosfato del 5' de siARNs y microARNs, resultante del mecanismo de biogénesis, es crucial para el ensamble eficiente de estos ARN pequeños en RISC. Además, el grupo fosfato es esencial para la fidelidad de la degradación del ARNm blanco, porque la posición del sitio de clivaje en el ARN blanco es determinada por la distancia del grupo fosfato 5' de la cadena de ARN guía7. Vale la pena destacar que durante los últimos años gracias al conocimiento de los microARNs, ha sido posible diseñar diferentes modelos y estrategias de silenciamiento que combinadas con la tecnología del ARN interferente que permiten mejorar y aumentar el porcentaje de inhibición sin mayores dificultades.
CONCLUSIONES
Desde su descubrimiento y hasta el día de hoy los microARNs se han convertido en uno de los temas más estudiados y abordados; por lo cual, actualmente se encuentra disponible gran cantidad de información que ha llevado a comprender mejor y facilitar el entendimiento de los procesos biológicos en que están involucrados los microARNs, de manera muy especial los relaciones con regulación de la expresión génica. No obstante, y a pesar de toda la información existente, aún quedan muchos mecanismos por comprender y descifrar totalmente, pero el entender la generación de los microARNs es el paso inicial en esta tarea.
CONFLICTO DE INTERÉS
El autor no declara conflicto de interés alguno.
AGRADECIMIENTOS
Fundación "HIV Research Trust" (HIVRT) por la beca (HIVRT10-084), que permitió la pasantía en el grupo "Cell Biology and Gene Therapy Group" del Instituto Karolinska de Estocolmo en Suecia.
Esta revisión constituye un producto del proyecto "RNA interference for the treatment of HIV-1 infection"
financiado por el Departamento Administrativo de Ciencia, Tecnología e Innovación, COLCIENCIAS. Contrato No. ; Código 1102-04-16427
REFERENCIAS
1. Lee RC, Feinbaum RL, Ambros V. The C. elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14. Cell 1993; 75(5): 843-854. [ Links ]
2. Landthaler M, Yalcin A, Tuschl T. The human DiGeorge syndrome critical region gene 8 and Its D. melanogaster homolog are required for miRNA biogenesis. Curr Biol 2004; 14(23): 2162-2167. [ Links ]
3. Lee Y, Ahn C, Han J, et al. The nuclear RNase III Drosha initiates microRNA processing. Nature 2003; 425(6956): 415-419. [ Links ]
4. Yi R, Qin Y, Macara IG, Cullen BR. Exportin-5 mediates the nuclear export of pre-microRNAs and short hairpin RNAs. Genes Dev 2003; 17(24): 3011- 3016. [ Links ]
5. Bernstein E, Caudy AA, Hammond SM, Hannon GJ. Role for a bidentate ribonuclease in the initiation step of RNA interference. Nature 2001; 409(6818): 363-366. [ Links ]
6. Chendrimada TP, Gregory RI, Kumaraswamy E, et al. TRBP recruits the Dicer complex to Ago2 for microRNA processing and gene silencing. Nature 2005; 436(7051): 740-744. [ Links ]
7. Inui M, Martello G, Piccolo S. MicroRNA control of signal transduction. Nat Rev Mol Cell Biol 2010; 11(4): 252-263. [ Links ]
8. Kim VN, Han J, Siomi MC. Biogenesis of small RNAs in animals. Nat Rev Mol Cell Biol 2009; 10(2): 126-139. [ Links ]
9. Lee Y, Kim M, Han J, et al. MicroRNA genes are transcribed by RNA polymerase II. Embo J 2004;23(20):4051-4060. [ Links ]
10. Rajewsky N. microRNA target predictions in animals. Nat Genet 2006;38 Suppl:S8-13. [ Links ]
11. Krek A, Grun D, Poy MN, et al. Combinatorial microRNA target predictions. Nat Genet 2005; 37(5): 495-500. [ Links ]
12. Cai Y, Yu X, Hu S, Yu J. A brief review on the mechanisms of miRNA regulation. Genomics Proteomics Bioinformatics 2009; 7(4): 147-154. [ Links ]
13. Calin GA, Sevignani C, Dumitru CD, et al. Human microRNA genes are frequently located at fragile sites and genomic regions involved in cancers. Proc Natl Acad Sci U S A 2004; 101(9): 2999-3004. [ Links ]
14. Kozomara A, Griffiths-Jones S. miRBase: integrating microRNA annotation and deep-sequencing data. Nucleic Acids Res 2011; 39(Database issue): D152- 157. [ Links ]
15. Gangaraju VK, Lin H. MicroRNAs: key regulators of stem cells. Nat Rev Mol Cell Biol 2009; 10(2): 116-125. [ Links ]
16. Esquela-Kerscher A, Slack FJ. Oncomirs - microRNAs with a role in cancer. Nat Rev Cancer 2006; 6(4): 259-269. [ Links ]
17. Wang D, Qiu C, Zhang H, Wang J, Cui Q, Yin Y. Human microRNA oncogenes and tumor suppressors show significantly different biological patterns: from functions to targets. PLoS One 2010; 5(9). [ Links ]
18. Shah AA, Leidinger P, Blin N, Meese E. miRNA: small molecules as potential novel biomarkers in cancer. Curr Med Chem 2010; 17(36): 4427-4432. [ Links ]
19. Li C, Feng Y, Coukos G, Zhang L. Therapeutic microRNA strategies in human cancer. Aaps J 2009; 11(4): 747-757. [ Links ]
20. Farazi TA, Spitzer JI, Morozov P, Tuschl T. miRNAs in human cancer. J Pathol 2011; 223(2): 102-115. [ Links ]
21. Kim VN, Nam JW. Genomics of microRNA. Trends Genet 2006; 22(3): 165-173. [ Links ]
22. Lee Y, Jeon K, Lee JT, Kim S, Kim VN. MicroRNA maturation: stepwise processing and subcellular localization. Embo J 2002; 21(17): 4663-4670. [ Links ]
23. Miyoshi K, Miyoshi T, Siomi H. Many ways to generate microRNA-like small RNAs: noncanonical pathways for microRNA production. Mol Genet Genomics 2010; 284(2): 95-103. [ Links ]
24. Borchert GM, Lanier W, Davidson BL. RNA polymerase III transcribes human microRNAs. Nat Struct Mol Biol 2006; 13(12): 1097-1101. [ Links ]
25. Han J, Lee Y, Yeom KH, et al. Molecular basis for the recognition of primary microRNAs by the Drosha-DGCR8 complex. Cell 2006; 125(5) :887- 901. [ Links ]
26. Liu J, Rivas FV, Wohlschlegel J, Yates JR, 3rd, Parker R, Hannon GJ. A role for the P-body component GW182 in microRNA function. Nat Cell Biol 2005; 7(12): 1261-1266. [ Links ]
27. Bartel DP. MicroRNAs: target recognition and regulatory functions. Cell 2009; 136(2): 215-233. [ Links ]
28. Berezikov E, van Tetering G, Verheul M, et al. Many novel mammalian microRNA candidates identified by extensive cloning and RAKE analysis. Genome Res 2006; 16(10): 1289-1298. [ Links ]
29. Berezikov E, Chung WJ, Willis J, Cuppen E, Lai EC. Mammalian mirtron genes. Mol Cell 2007; 28(2): 328-336. [ Links ]
30. Ender C, Krek A, Friedlander MR, et al. A human snoRNA with microRNA-like functions. Mol Cell 2008; 32(4): 519-528. [ Links ]
31. Babiarz JE, Ruby JG, Wang Y, Bartel DP, Blelloch R. Mouse ES cells express endogenous shRNAs, siRNAs, and other Microprocessor-independent, Dicer-dependent small RNAs. Genes Dev 2008; 22(20): 2773-2785. [ Links ]
32. Bogerd HP, Karnowski HW, Cai X, Shin J, Pohlers M, Cullen BR. A mammalian herpesvirus uses noncanonical expression and processing mechanisms to generate viral MicroRNAs. Mol Cell 2010; 37(1): 135-142. [ Links ]
33. Miyoshi K, Miyoshi T, Hartig JV, Siomi H, Siomi MC. Molecular mechanisms that funnel RNA precursors into endogenous small-interfering RNA and microRNA biogenesis pathways in Drosophila. Rna 2010; 16(3): 506-515. [ Links ]
34. Mueller GA, Miller MT, Derose EF, Ghosh M, London RE, Hall TM. Solution structure of the Drosha double-stranded RNA-binding domain. Silence 2010; 1(1): 2. [ Links ]
35. Du Z, Lee JK, Tjhen R, Stroud RM, James TL. Structural and biochemical insights into the dicing mechanism of mouse Dicer: a conserved lysine is critical for dsRNA cleavage. Proc Natl Acad Sci U S A 2008; 105(7): 2391-2396. [ Links ]
36. Ma JB, Ye K, Patel DJ. Structural basis for overhangspecific small interfering RNA recognition by the PAZ domain. Nature 2004; 429(6989): 318-322. [ Links ]
37. Meister G, Landthaler M, Patkaniowska A, Dorsett Y, Teng G, Tuschl T. Human Argonaute2 mediates RNA cleavage targeted by miRNAs and siRNAs. Mol Cell 2004; 15(2): 185-197. [ Links ]
38. Song JJ, Joshua-Tor L. Argonaute and RNA--getting into the groove. Curr Opin Struct Biol 2006; 16(1): 5-11. [ Links ]
39. Tolia NH, Joshua-Tor L. Slicer and the argonautes. Nat Chem Biol 2007; 3(1): 36-43. [ Links ]
40. Pare JM, Tahbaz N, Lopez-Orozco J, LaPointe P, Lasko P, Hobman TC. Hsp90 regulates the function of argonaute 2 and its recruitment to stress granules and P-bodies. Mol Biol Cell 2009; 20(14): 3273- 3284. [ Links ]
41. Filipowicz W, Bhattacharyya SN, Sonenberg N. Mechanisms of post-transcriptional regulation by microRNAs: are the answers in sight? Nat Rev Genet 2008; 9(2): 102-114. [ Links ]
42. Perron MP, Provost P. Protein components of the microRNA pathway and human diseases. Methods Mol Biol 2009; 487: 369-385. [ Links ]
43. Sohn SY, Bae WJ, Kim JJ, Yeom KH, Kim VN, Cho Y. Crystal structure of human DGCR8 core. Nat Struct Mol Biol 2007; 14(9): 847-853. [ Links ]
44. Kohler A, Hurt E. Exporting RNA from the nucleus to the cytoplasm. Nat Rev Mol Cell Biol 2007; 8(10): 761-773. [ Links ]
45. Kok KH, Ng MH, Ching YP, Jin DY. Human TRBP and PACT directly interact with each other and associate with dicer to facilitate the production of small interfering RNA. J Biol Chem 2007; 282(24): 17649-17657. [ Links ]
46. Diederichs S, Haber DA. Dual role for argonautes in microRNA processing and posttranscriptional regulation of microRNA expression. Cell 2007; 131(6): 1097-1108. [ Links ]
47. Gregory RI, Chendrimada TP, Cooch N, Shiekhattar R. Human RISC couples microRNA biogenesis and posttranscriptional gene silencing. Cell 2005; 123(4): 631-640. [ Links ]
48. Carthew RW, Sontheimer EJ. Origins and Mechanisms of miRNAs and siRNAs. Cell 2009; 136(4): 642-655. [ Links ]
49. Cifuentes D, Xue H, Taylor DW, et al. A novel miRNA processing pathway independent of Dicer requires Argonaute2 catalytic activity. Science 2010; 328(5986): 1694-1698. [ Links ]
50. Mayer M, Schiffer S, Marchfelder A. tRNA 3' processing in plants: nuclear and mitochondrial activities differ. Biochemistry 2000; 39(8): 2096- 2105. [ Links ]