Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de la Universidad Industrial de Santander. Salud
Print version ISSN 0121-0807
Rev. Univ. Ind. Santander. Salud vol.47 no.2 Bucaramanga May/Aug. 2015
Evaluación de la concentración de
mercurio en arroz (Oryza sativa) crudo
y cocido procedente del municipio
de San Marcos- Sucre y zona aurífera
del municipio de Ayapel - Córdoba
Marcela P. Argumedo G.1, Carlos Vergara R.1, Jhon V. Vidal D.2, Jose L. Marrugo N.3
1. Universidad de Sucre. Colombia.
2. Corporación Universitaria del Caribe CECAR. Colombia.
3. Universidad de Córdoba. Colombia.
Correspondencia: Marcela P. Argumedo. Dirección: Carrera 8D 25G-29 Piso 2, Apto 1 Pioneros. Sincelejo, Sucre.
Correo electrónico: marce404@hotmail.com. Teléfono: 300 527 9665
Recibido: Mayo 8 de 2014 Aprobado: Enero 20 de 2015
Forma de citar: Argumedo MP, Vergara C, Vidal J, Marrugo JL. Evaluación de la concentración de mercurio en arroz (Oryza sativa) crudo y cocido procedente del municipio de San Marcos- Sucre y zona aurífera del municipio de Ayapel - Córdoba. Rev Univ Ind Santander Salud. 2015; 47(2):169-177.
RESUMEN
Introducción: Los metales se encuentran en todos los alimentos, siendo de mayor preocupación la presencia de metales tóxicos como el mercurio, debido a los efectos adversos que causa en la salud del hombre, lo que lo ha convertido en un grave problema de salud pública. Objetivo: Evaluar la concentración de mercurio en arroz (Oryza sativa) crudo y cocido procedente del municipio de San Marcos - Sucre y zona aurífera del municipio de Ayapel - Córdoba. Metodología: El presente estudio es de tipo exploratorio y experimental. La toma de muestras fue realizada en tiempo de recolección del arroz (septiembre) y se tomaron tres repeticiones de cada tipo o variedad de arroz (Fedearroz 2000 - LD 473). La cocción del alimento fue realizada en el laboratorio en condiciones similares a las utilizadas por habitantes de las comunidades donde fueron recolectadas las muestras. Para los análisis de relación estadística entre los tratamientos de cocción y la concentración de mercurio total en muestras, fue realizado un análisis de correlación simple. La determinación de diferencias estadísticamente significativas entre las muestras de arroz crudo y cocido fue realizada mediante un t-test y Anova. Resultados: Se presentaron concentraciones bajas de mercurio total y metilmercurio en las muestras de arroz crudo y cocido. Además, fue detectado que el proceso de cocción del alimento disminuye las concentraciones de HgT, en los diferentes tratamientos de tiempo de cocción. Conclusiones: Los habitantes de los municipios en estudio están expuestos a concentraciones mínimas de mercurio que podrían ser perjudiciales para su salud, debido a la alta ingesta de este cereal en la dieta de las comunidades.
Palabras clave: Minería Aurífera, Mercurio, Arroz, Espectrofotometría de Absorción Atómica por Vapor Frío, Salud Pública.
Evaluation of the concentration of mercury in rice (Oryza
sativa) raw and cooked from the municipality of San Marcos
- Sucre and township gold zone Ayapel - Cordoba
ABSTRACT
Introduction: Metals are found in mostly all kind of food. Presence of toxic metals such as mercury are relevant for public health safety, due to the adverse effects it has on human health. Objective: To evaluate mercury concentrations in raw and cooked rice (Oryza sativa) from San Marcos municipality in Sucre and Ayapel gold zone in Córdoba. Methodology: The present study is exploratory and experimental. Sample collection was conducted in rice harvesting time (September) and three repetitions of each type or variety of rice were taken (Fedearroz 2000 - LD 473). Cooking of rice was made under laboratory standards similar to those used by residents of the communities where the samples were collected. For statistical analysis of the relationship between cooking treatment and the concentration of total mercury in samples, we carried out a simple correlation analysis. Determination of statistically significant differences, between samples of raw and cooked rice, was performed using a t-test and Anova. Results: Low concentrations of total mercury and methylmercury were presented in raw and cooked rice. Furthermore, it was found that food cooking processes decreases HgT concentrations. Conclusion: Inhabitants of the municipalities under study are exposed to minimal concentrations of mercury that could be harmful to their health due to high intake of this cereal in their communities' diet.
Keywords: Gold Mining, Mercury, Rice, Atomic Absorption Spectrophotometry by Cold Vapor, Public Health.
INTRODUCCIÓN
El mercurio (Hg) es uno de los metales pesados con mayor impacto sobre el medio ambiente, por lo que se considera un contaminante global. Su utilización en la minería aurífera ha conllevado a la contaminación de diferentes compartimientos ambientales donde sufre diversas transformaciones, originando en algunos casos, graves intoxicaciones en núcleos importantes de la población1. En ambientes acuáticos y suelos, el Hg se convierte en metilmercurio (MeHg), que es mucho más tóxico que el mercurio cero (Hg°) y debido a la alta afinidad de este contaminante a los grupos sulfhidrilo de las proteínas, es rápidamente incorporado en la cadena alimentaria, bioacumulado en los organismos acuáticos, y bioamagnificado de un nivel trófico a otro2, lo que supone una amenaza potencial para la salud de los seres humanos, generando graves efectos toxicológicos3,4 como neurotoxicidad, nefrotoxicidad, teratogénesis, neumonitis intersticial, entre otros4,5.
Generalmente, las concentraciones de Hg en la mayoría de los productos alimenticios han estado por debajo de 20 ng/g, y están presentes principalmente en formas inorgánicas6. Sin embargo, estudios recientes, han informado niveles altos de MeHg en el arroz de áreas contaminadas por mercurio. Por ejemplo existen reportes de contaminación de arroz por mercurio en zonas contaminadas como Qingzhen y Wanshan en la provincia de Guizhou, China, con niveles elevados de MeHg, hasta 144 ng/g7. Otro estudio determinó las concentraciones de MeHg en 25 muestras de arroz producidas en 15 provincias en China, con valores cercanos a 4,5 ng/g8.
El arroz se ha constituido como fuente primaria de metilmercurio en las zonas donde hay una contaminación considerable de mercurio inorgánico cuyos valores han superado la ingesta diaria tolerable establecida por el Codex alimentarius9, situación que ha contribuido a que el consumo de arroz pueda ser considerado un problema de salud pública, debido a los efectos adversos que se pueden generar10. Esta problemática es evidente debido a que este contaminante muestra su acumulación en los diferentes niveles tróficos, siendo de gran preocupación la biomagnificación en humanos que viven en cercanías a ríos, ciénagas, lagos o algún cuerpo de agua, donde existen explotaciones de oro cercanas11.
En la región de la Mojana en Colombia no existe una explotación masiva de oro, sin embargo, es una zona receptora de mercurio debido a las interconexiones que hay entre las corrientes de agua provenientes de estas zonas altamente contaminadas12. En esta vasta región están localizados los municipios de San Marcos -Sucre y Ayapel- Córdoba, los cuales están interconectados hídricamente a través del río San Jorge, que es una fuente que posee probabilidad de contaminación, por lo que sus habitantes podrían presentar riesgos de exposición al estar expuestos a concentraciones de mercurio perjudiciales para su salud13,14.
No obstante, no se encuentra información sobre estimativos de concentraciones de mercurio total y metilmercurio en las variedades de arroz comercializadas y consumidas por los habitantes de los municipios de San Marcos y Ayapel, así como las posibles variaciones que puedan registrarse en la concentración de este metal pesado debido al proceso de cocción del alimento y las áreas geográficas utilizadas para este cultivo. Por consiguiente, la presente investigación tuvo como objetivo Evaluar la concentración de mercurio en arroz (Oryza sativa) crudo y cocido procedente de los municipios de San Marcos - Sucre y Ayapel - Córdoba.
METODOLOGÍA
Tipo y sitio de estudio
El presente estudio es de tipo exploratorio y experimental. La zona del estudio corresponde a los municipios de San Marcos - Sucre y Ayapel - Córdoba.
Población y muestra
La población corresponde a la totalidad de arroz cultivado en los municipios del estudio. Las muestras de arroz (crudo y cocido) fueron colectadas en los municipios de San Marcos -Sucre y Ayapel-Córdoba, las cuales fueron seleccionadas en forma aleatoria con un nivel de confianza de 95%.
Identificación de la procedencia del arroz (Oryza sativa) y caracterización de las formas de cocción del alimento.
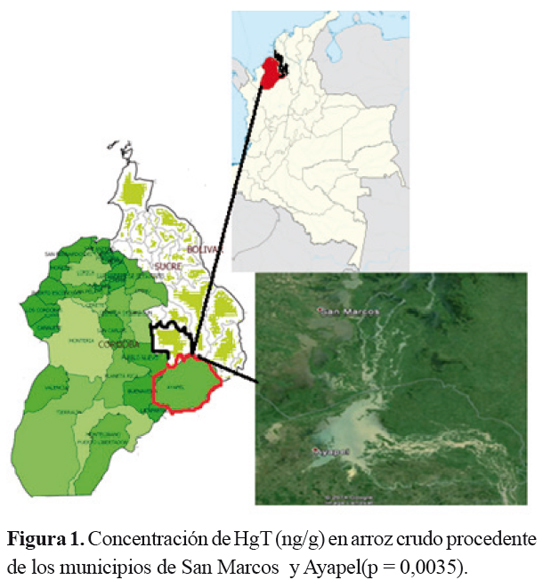
Fue obtenida la información secundaria sobre los sitios geográficos de siembra del arroz, ubicados en los municipios de San Marcos, localizado a 8°39'44''N 75°07'44''O y Ayapel con localización a 8°18'45''N 75°08'42''O. Mediante una encuesta se logró obtener conocimiento sobre las diferentes formas de cocción del alimento, variables como cantidad y clases de ingredientes, temperatura y tiempo utilizado en la cocción.
Selección, toma de muestras y tratamientos de cocción.
La toma de muestras fue realizada en tiempo de cosecha del producto, correspondiente al mes septiembre. En el municipio de San Marcos las muestras fueron tomadas directamente de los cultivos en los sitios de Caño Rabón y Bajo Perano, mientras que en zona aurífera del municipio de Ayapel, fueron colectadas en la vereda Marra Lu, correspondiente a los sitios; lote La Fiebre, La Batea y Taller Nº 1. De cada tipo o variedad de arroz (Fedearroz 2000 - LD 473) se tomaron tres repeticiones.
La fase experimental y de laboratorio fue iniciada con la estandarización de los métodos de cocción para las muestras. Durante este proceso fueron tenidas en cuenta las variables de temperatura y tiempo de cocción. El proceso fue realizado en condiciones similares a las utilizadas por los habitantes de la zona de estudio en cuanto a la relación de cantidades de ingredientes. Para la cocción del alimento en laboratorio, fueron utilizados en cada ensayo 100 gramos de arroz, 120 mililitros de agua, 2.0 gramos de cloruro de sodio y 7 mililitros de aceite. Fue realizada la cocción con dos tipos de tratamiento a diferentes tiempos (36 min y 16 min) de cocción y temperaturas entre 97°C - 120°C.
Determinación de la concentración de Hg en arroz crudo y cocido.
Las muestras de arroz crudo y cocido fueron empacadas en bolsas de polietileno de cierre hermético, almacenadas a 4°C en recipientes de poliestireno expandido y llevadas al laboratorio de Aguas y Química Ambiental de la Universidad de Córdoba.
En laboratorio las muestras fueron digeridas con soda caustica y cloruro de cadmio para la determinación de HgT. Posteriormente, fueron analizadas mediante la técnica de espectrofotometría de absorción atómica por vapor frio adaptado de Sadiq et al.15, y US-EPA16, previamente validado en el laboratorio de Aguas y Química Ambiental de la Universidad de Córdoba. Mediante la diferencia de HgT y Hg inorgánico fue establecida la concentración de Hg orgánico. Las muestras para determinación de mercurio orgánico, específicamente metilmercurio fueron analizadas por cromatografía gaseosa acoplada a masa.
Análisis de datos
Las concentraciones de Hg Total y MeHg halladas en las muestras de arroz crudo y cocido son presentadas como media ± error estándar. La determinación de relaciones estadísticas entre los tratamientos de cocción y la concentración de mercurio total, fueron realizadas mediante un análisis de correlación simple. El análisis de diferencias estadísticamente significativas entre las muestras de arroz crudo y cocido fue realizado mediante t-test y Anova, previa verificación y corrección de la Normalidad y fue utilizado el programa estadístico Statgraphics Centurion XV.
RESULTADOS
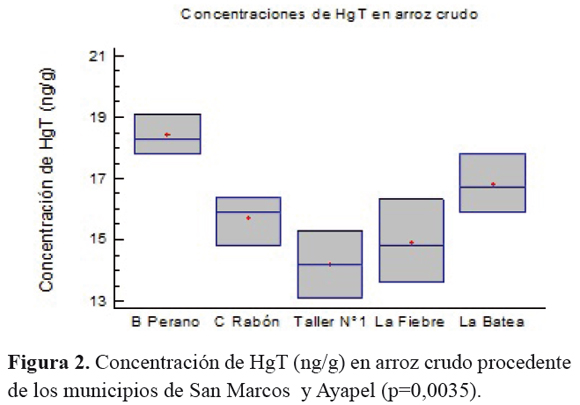
El arroz consumido por los habitantes del municipio de San Marcos procede de cultivos que se extienden en el corregimiento de Bajo Perano y Caño Rabón, mientras que el de zona aurífera de Ayapel proviene de la vereda Marra Lu. Los resultados mostraron que las concentraciones de HgT en arroz crudo y cocido fueron mínimas y las de MeHg estuvieron por debajo del límite de detección del equipo (<14ng/g). Tablas 1 y 2.
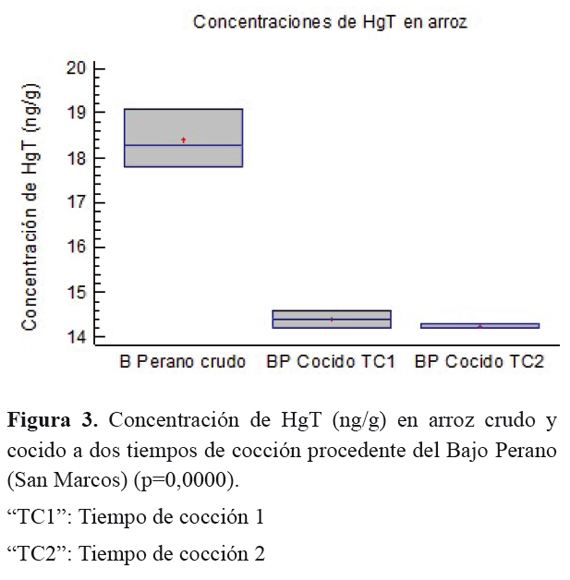
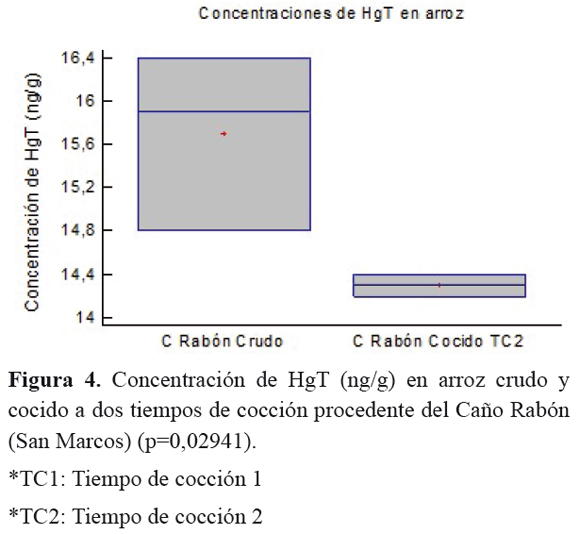
Para comparar las medias de las concentraciones de mercurio total en los diferentes sitios de procedencia del arroz se realizó un t-test y Anova que mostró diferencias estadísticamente significativas entre las muestras de los dos municipios del estudio (p=0,0035), donde hubo diferencias entre los siguientes sitios de procedencia: Bajo Perano - Caño Rabón, Bajo Perano - Lote La Fiebre, Bajo Perano - Lote Taller N° 1, Lote La Batea - Lote La Fiebre y Lote La Batea - Lote Taller N° 1. Figura 2. Con relación al análisis de comparación de los niveles de mercurio de arroz crudo con el sometido a cocción fueron encontradas diferencias estadísticamente significativas con un valor p=0,0000 para las muestras procedentes de Bajo Perano, Figura 3 y un p=0,02941 para las muestras de Caño Rabón. Figura 4.
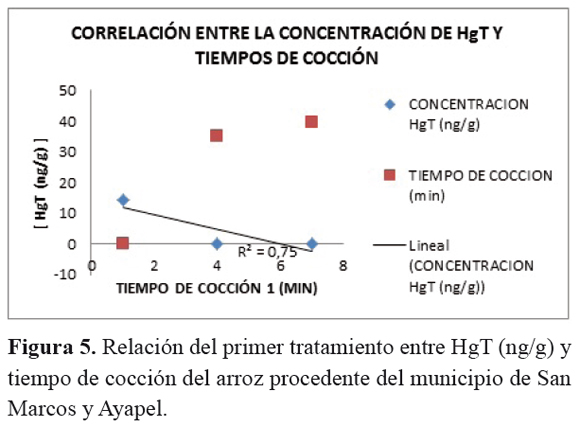
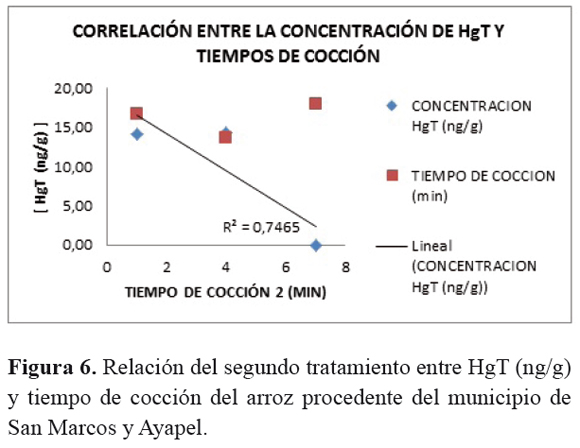
El análisis de correlación de la concentración de HgT del arroz procedente de los municipios San Marcos y Ayapel con los tiempos de cocción en cada tratamiento, presentó valores de p=0,6279 para el tratamiento 1 y p=0,4690 para el tratamiento 2, Figuras 5 y 6, lo cual demuestra que no hay una relación estadísticamente significativa entre la concentración del metal y el tiempo de cocción del alimento, a pesar de que el valor de R2 (R2=0,75 para el tratamiento 1 y R2=0,74 para el tratamiento 2 indica una relación moderadamente fuerte entre las variables.
DISCUSIÓN
El arroz cocido en los dos sistemas de tratamiento o tiempos de cocción mostró una disminución de la concentración de mercurio, lo que indica que el método de cocción puede contribuir a la reducción (muy limitada) de los niveles del metal en este alimento, dependiendo de las condiciones del proceso (tiempo, temperatura y medio de cocción)6. Por tanto, los habitantes del municipio no estarían expuestos a concentraciones perjudiciales para su salud y el consumo de arroz sería un contribuyente en menor concentración a la exposición a mercurio.
En el presente estudio las concentraciones de mercurio en muestras de arroz crudo y cocido no sobrepasaron los límites permisibles establecido por la FAO/OMS17 y el Comité Mixto de Expertos en Aditivos Alimentarios JECFA18, que corresponde a 0,57 μg/kg de peso corporal/día (equivalente a la ingesta semanal tolerable provisional (ISTP) de 4 μg/kg de peso corporal/semana) para HgT y para MeHg 0,23 μg/kg de peso corporal/ día (equivalente al ISTP para MeHg de 1,6 μg/kg de peso corporal/semana)19. Sin embargo, varios estudios han reportado altas concentraciones de mercurio total y metilmercurio en arroz20, demostrando que la exposición humana a MeHg a través del consumo de alimentos no se limita a los peces sino también al consumo de este producto, que es el alimento básico para billones de personas9, tal es el caso de la población de Wuchuan de una zona minera de mercurio, Guizhou, China, donde los niveles del metal fueron de 6,0 hasta 113 ng/g para HgT y de 3,1 hasta 13,4 ng/g para MeHg respectivamente21. Asimismo, Qiu et al.,21 informó que el arroz (Oryza sativa) cultivado en zonas mineras de mercurio contiene niveles de MeHg de 1,61 a 174 ng/g en la porción comestible, lo que resultó ser 10 a 100 veces superior a otras plantas de cultivo. Los resultados demuestran que el arroz es una planta bioacumulativa de MeHg y se constituye en la principal fuente de exposición humana en estas áreas de estudio.
En Colombia no hay registros, siendo un país con altas cosechas y consumo de arroz, pero existen reportes específicamente en el municipio de San Marcos, sitio de estudio de la presente investigación, donde se determinó que los hombres consumen cantidades promedio de 1218.0 gramos de arroz semanalmente, mientras que las mujeres ingieren cantidades promedio de 925.24 gramos de arroz cada semana, demostrando que no hay diferencias entre el grupo de habitantes muestreado y tanto hombres como mujeres están consumiendo cantidades similares de arroz22.
De otra parte, las diferencias en las concentraciones de mercurio en los sitios de procedencia del arroz se deben a que algunos sitios están más cercanos a las fuentes de extracción minera por los flujos de agua procedentes de zonas altamente contaminadas con el metal. Garay y Baleta23 en su investigación determinaron las concentraciones de mercurio total y metilmercurio en agua de los sitios de procedencia de los peces consumidos por los habitantes del municipio de San Marcos, quienes encontraron que el casco urbano del municipio de San Marcos está cercano al río San Jorge, Ciénaga Belén y Ciénaga San Marcos; sitios de donde proviene la mayor cantidad de pescados para su consumo. Sin embargo, se encuentran otros sitios de donde también se extrae en menor proporción este alimento como Caño Viloria, Cuiva, Patillal, vereda Las Pozas, Calle Nueva, Rabón, Caño Cruz, y Caño Carate donde no fueron hallados cantidades detectables de MeHg ni se encontraron proporciones significativas de HgT en dichas muestras, a excepción de la muestra de agua perteneciente a Caño Viloria la cual presentó una concentración de 0,00015 +/- 0,01 ug Hg/ml. Este fenómeno se debe a las interconexiones hídricas, puesto que Caño Viloria conecta la Ciénaga de Ayapel con el río San Jorge a la altura de bocas de San Antonio, cerca al Caño Mojana24, el cual se encuentra comunicado con la ciénaga de Ayapel que está a 25 km de la zona minera con la más alta producción de oro en el país (sur de Bolívar y noreste de Antioquia), donde el mercurio es utilizado para extraer el metal25.
Además, la ciénaga de Ayapel está localizada en la cuenca del río San Jorge, con extensiva minería de níquel aguas arriba, como también importantes explotaciones auríferas en la parte alta del río San Pedro, sobre la misma cuenca. De igual forma, a 15 km aproximadamente de la parte suroriental está el río Cauca, que transporta residuos provenientes de la zona minera, llegando sus aguas hasta la región de la Mojana. La ciénaga recibe aguas del río Cauca a través de los caños y quebradas localizado en el costado oriental y suroriental y algunas veces por corrientes localizadas en el costado norte25.
Cabe resaltar que las bajas concentraciones de Hg en las muestras de arroz después de ser sometidas a cocción pueden deberse a la posible volatilización del metal por acción de la temperatura, dado que los compuestos mercuriales tienden a vaporizarse a temperatura ambiente y generar vapores de mercurio. Además, en este caso, los reportes indican que el aumento de temperatura en el intervalo de 80-140 °C causa un aumento en la eliminación de Hgº 26 y en este estudio en ambos tratamientos, la temperatura alcanzada por la cocción superó los 100°C, lo cual puede posibilitar fenómenos de volatilización del mercurio inorgánico, aumento de humedad del producto y desnaturalización proteica que puede explicar la pérdida de concentración del metal, por tal razón, no hubo ninguna correlación entre la concentración de mercurio y el tiempo de cocción al que fue sometido cada tratamiento.
Sin embargo en estudios de Torres27 se señala que la pérdida media de peso tras el cocinado (crudo/cocinado = 1,3) es igual al incremento de la concentración de Hg tras el cocinado (cocinado/crudo = 1,3), indicando que la pérdida de agua durante el cocinado es la causa principal del incremento en la concentración de Hg observada. En forma contradictoria, en el presente estudio durante el proceso de cocción del arroz a pesar de que no se determinó humedad, hubo ganancia de agua y disminución de la concentración de mercurio, probablemente debido al fenómeno de volatilización. De igual forma, el cambio en la bioaccesibilidad tras el proceso de cocción podría ser atribuible a alteraciones en la conformación estructural de las proteínas presentes en el arroz, debido a la temperatura, lo que podría causar la pérdida de la estructura nativa de las mismas. Estos cambios podrían dificultar el acceso a las moléculas a las que se une el Hg, preferentemente los grupos sulfhidrilo presentes en moléculas como la cisteína28.
A pesar de que en el presente estudio no se registraron concentraciones de metilmercurio en el arroz consumido por los habitantes del municipio de San Marcos y Ayapel, los estudios han revelado que el MeHg en el arroz crudo está presente casi exclusivamente como CH3Hg-L-cisteinato (CH3HgCys)29, un complejo que se cree que es responsable de la transferencia de MeHg través de las barreras hematoencefálica y placentaria30,31. Otros reportes indican que la cocción no cambia la concentración de Hg total y MeHg en arroz, no hay certeza de que CH3HgCys sea medible después de la cocción, lo que sugiere que CH3HgCys se convierte en otras formas de MeHg; no obstante ha sido difícil lograr su identificación y toxicidad32. Asimismo, se ha demostrado la descomposición de MeHgCys durante el proceso de cocción. Sin embargo, aún no se ha deducido el producto de descomposición de CH3HgCys en el arroz después de la cocción, dado que no han sido registrados hay ningún cambio en la concentración de MeHg después de la cocción9; a diferencia de las reportadas en el presente estudio, donde se logra evidenciar que la concentración de HgT disminuyó después del proceso de cocción.
Por otra parte, estudios recientes han demostrado que el nivel elevado de MeHg en el arroz probablemente está relacionado con una alta capacidad de metilación en los suelos donde se cultiva el cereal33. El riego por temporada produce condiciones anaeróbicas en el suelo superficial, lo que favorece la metilación in situ de Hg inorgánico34. Sin embargo, el mecanismo de la absorción de MeHg en el tejido del arroz aún no está claro35. Los hallazgos encontrados en la presente investigación con relación a las bajas concentraciones de mercurio posiblemente estén relacionadas con reportes presentados en un estudio realizado en el municipio de San Marcos donde fueron encontrados concentraciones de MeHg en el suelo de 3,2 ng/g para Bajo Perano y 1,7 ng/g en Caño Rabón, denotando que este último presenta menor estado de contaminación debido a las interconexiones hídricas que posee este sector con zonas menos contaminadas por mercurio24. En este caso, las bajas concentraciones de mercurio determinadas en este estudio han sido a causa de las concentraciones mínimas presentes en el suelo donde se cultiva esta variedad de arroz (Fedearroz 2000 - LD 473).
CONCLUSIONES
Las concentraciones de mercurio total disminuyeron después de los tratamientos de cocción, encontrándose que el tiempo de cocción no afecta los niveles de concentración del metal pesado, por tanto, el método de cocción es un medio de reducción que depende de las condiciones de cocción (tiempo, temperatura y medio de cocción). Asimismo, los sitios de procedencia del arroz presentaron diferencias en las concentraciones de Hg debido a su ubicación geográfica lo que permite que unos estén más cercanos que otros a las fuentes de extracción minera, por los flujos de agua procedentes de zonas altamente contaminadas con el metal. Por tal razón, los habitantes del municipio de San Marcos y Ayapel están expuestos a concentraciones mínimas de mercurio que podrían ser perjudiciales para su salud, debido a que el consumo frecuente de alimentos contaminados podría representar una amenaza potencial para la salud de los consumidores, lo cual hace necesario su permanente monitoreo ambiental.
AGRADECIMIENTOS
Los autores expresan sus agradecimientos a la Universidad de Córdoba y Universidad de Sucre, por su respaldo en el desarrollo de esta investigación y al Departamento Administrativo de Ciencia, Tecnología e Innovación Colciencias por su apoyo mediante la beca - pasantía Joven Investigador. Convocatoria 566 de 2012.
REFERENCIAS
1. Sepúlveda Gallego LE, Agudelo LM, Arengas A. El mercurio, sus implicaciones en la salud y en el ambiente. Revista Científica Luna Azul. Universidad de Caldas. 2007; 1909-2474. [ Links ]
2. Ochoa-Acuna, H, Sepúlveda MS, Gross TS. Mercury in feathers from Chilean birds: influence of location, feeding strategy, and taxonomic affiliation. Mar Pollut Bull. 2002; 44: 340-349. [ Links ]
3. Ozuah PO. Folk use of elemental mercury: a potential hazard for children. J Natl Med Assoc. 2001; 93(9): 320-322. [ Links ]
4. Tirado V, Garcia MA, Moreno J, Galeano LM, Lopera F, Franco A. Pneuropsychological disorders after occupational exposure to mercury vapors in El Bagre (Antioquia, Colombia). Rev Neurol. 2000; 31(8): 712-716. [ Links ]
5. Ye X, Qian V, Xu P, Zhu L, Longnecker M, Fu H. Nephrotoxicity, neurotoxicity and mercury exposure among children with and without dental amalgam fillin. Int J Hyg Environ Health. 2009; 212(4): 378-386. [ Links ]
6. Environmental Health Criteria 118-Inorganic Mercury. World Health Organization; Geneva, Switzerland. 1991. [ Links ]
7. Horvat M, Nolde N, Fajon V, Jereb V, Logar M, Lojen S, et al. Total mercury, methylmercury and selenium in mercury polluted areas in the province Guizhou, China. Sci Total Environ. 2003; 304(1-3): 231-256. [ Links ]
8. Shi JB, Shang L, Jiang G. Simultaneous determination of methylmercury and ethylmercury in rice by capillary gas chromatography coupled on-line with atomic fluorescence spectrometry. J AOAC Int. 2005; 88(2): 665-669. [ Links ]
9. Li L, Wang F, Meng B, Lemes M, Feng X, Jiang G. Speciation of methylmercury in rice grown from a mercury mining area. Environ Pollut. 2010; 158(10): 3103-3107. [ Links ]
10. Mancera N, Álvarez R. Estado del conocimiento de las concentraciones de mercurio y otros metales pesados en peces dulceacuícolas de Colombia. Acta Biol Colomb. 2006; 11(1): 3-23. [ Links ]
11. Barrett JR. Rice is a significant source of methylmercury: research in china assesses exposures. Environ Health Perspect. 2010; 118(9): a398. [ Links ]
12. Olivero J, Mendoza C, Mestre J. Hair mercury levels in different occupational groups in a gold mining zone in the north of Colombia. Rev Saude Publica. 1995; 29(5): 376-379. [ Links ]
13. Díaz-Granados M. Grado de contaminación de los recursos hídricos e ictiológicos en la región de la Mojana [Tesis de grado] Bogotá: departamento de Ingeniería Civil y Ambiental, Centro de investigaciones en Ingeniería Ambiental (CIIA), Universidad de Los Andes.1998. [ Links ]
14. Ramírez-González A. Lineamientos y estadísticas para estudios biológicos para impacto ambiental. INDERENA/INFOTEC Ltda. Bogotá, 1998. Oleoducto Vasconia-Coveñas: Estudio de línea base, componentes biológicos y fisicoquímicos de los ecosistemas acuáticos. ECOPETROL/ICP/ Oleoducto de Colombia S.A./Biología Aplicada/ Ecology Ltda. Bogotá (Colombia). Informe final. 1993. [ Links ]
15. Sadiq M, Zaidi TH, Al-Mohana H. Sample weight and digestion temperature as critical factors in mercury determination in fish. Bull Environ Contam Toxicol. 1991; 47: 335-341. [ Links ]
16. USEPA (US Environment Protection agency) Mercury Study Report to Congress. 1998. [ Links ]
17. FAO (Food and Agriculture Organization of the United Nations). Rice is life: International Rice Commission Meets in Peru. 2006. [ Links ]
18. JECFA (Joint FAO/WHO Expert Committee on Food Additives). Joint FAO/WHO Food Standards Programme, Committee of the Codex Alimentarius Commission, Thirty-third Session 2010. [ Links ]
19. JECFA (Joint FAO/ WHOExpert Committee on Food Additives). Joint FAO/WHO Expert Committee on Food Additives, Sixty-first Meeting, Rome, 10-19 June 2003, Summary and Conclusions. 2003. [ Links ]
20. Barrett JR. Rice is a significant source of methylmercury: research in china assesses exposures. Environ Health Perspect. 2010; 118(9): A398. [ Links ]
21. Qui G, Feng X, Li P, Wang S, Li G, Shang L, et al. Methylmercury accumulation in rice (Oryza sativa L) grown at abandoned mercury mines in Guizhou, China. J Agr Food Chem. 2008; 56: 2465-2468. [ Links ]
22. Argumedo M, Consuegra A, Vidal JV, Marrugo JL. Exposición a mercurio en habitantes del municipio de San Marcos (departamento de Sucre) debida a la ingesta de arroz (Oryza sativa) contaminado. Rev Salud Pública. 2013; 15(6): 903-915 [ Links ]
23. Garay Y, Baleta W. Evaluación de la exposición a metilmercurio (MeHg) en habitantes del municipio de San Marcos - Sucre debido a la ingesta de alimentos contaminados. [Tesis de grado no publicada], Universidad de Sucre; 2013. 58 p. [ Links ]
24. CorAntioquia, Niveles de mercurio en sedimento, agua y tejido vivo "Buchón, arroz, peces y cabello" en los humedales de la Mojana Sucreña, Gaia. 2008. [ Links ]
25. Marrugo J, Lans E, Benítez L. Hallazgo de mercurio en peces de la Ciénaga de Ayapel, Córdoba, Colombia. Rev MVZ Córdoba. 2007; 12(1): 878- 886. [ Links ]
26. Zhao P, Guo X, Zheng C. Removal of elemental mercury by iodine-modified rice husk ash sorbents. J Environ Sci. 2010; 22(10): 1629-1636. [ Links ]
27. Torres S. Bioaccesibilidad de arsénico y mercurio en alimentos con potencial riesgo toxicológico. [Tesis de doctorado] Departamento de Química Analítica. Universidad de Valencia. 2011. [ Links ]
28. Rooney JP. The role of thiols, dithiols, nutritional factors and interacting ligands in the toxicology of mercury. Toxicology. 2007; 234(3): 145-156. [ Links ]
29. Lemes M, Wang F. Methylmercury speciation in fish muscle by HPLCICP- MS following enzymatic hydrolysis. J Anal at Spectrom. 2009; 24: 663-668. [ Links ]
30. Clarkson TW. Molecular and ionic mimicry of toxic metals. Ann Rev Pharmacol Toxicol. 1993; 33: 545- 571. [ Links ]
31. Simmons-Willis TA, Koh AS, Clarkson TW, Ballatori N. Transport of a neurotoxicant by molecular mimicry: the methylmercury-L-cysteine complexis a substrate for human L-type large neutral amino acid transporter (LAT) 1 and LAT2. Biochem J. 2002; 367(Pt 1): 239e246. [ Links ]
32. Harris HH, Pickering IJ. George GN. The chemical form of mercury in fish. Science. 2003; 301(5637) 1203. [ Links ]
33. Gilmour CC, Henry EA. Mercury methylation in aquatic systems affected by acid deposition. Environ Pollut. 1991; 71(2-4): 131-169. [ Links ]
34. Weber JH. Review of possible paths for abiotic methylation of mercury (II) in the aquatic environment. Chemosphere. 1993; 26: 2063-2077. [ Links ]
35. Porvari P, Verta M. Methylmercuryproduction in floodedsoils: a laboratorystudy. Water Air Soil Poll. 1995; 80: 765-773. [ Links ]