I. INTRODUCCIÓN
El sector productivo de curtido y teñido de cueros es reconocido por su considerable consumo de agua y altas cargas contaminantes, representadas en salinidad, materia orgánica, materia inorgánica, solidos disueltos y suspendidos, amoniaco, nitrógeno orgánico y algunos contaminantes específicos tales como sulfuros y cromo [1]. En los municipios de Villapinzón y Chocontá, Cundinamarca – Colombia, existen más de 100 empresas dedicadas al oficio del curtido de pieles [2]. Los vertimientos de las aguas residuales de este sector productivo son realizados al río Bogotá, dando lugar a problemas de contaminación de esta fuente hídrica superficial. Dentro del proceso de curtido y teñido de cueros, se realiza la operación de depilado, acción conocida en el sector curtidor como pelambre, esta etapa es responsable del 60 % al 70 % de la carga contaminante del sector curtidor [3], cabe señalar que el agua residual expelida en el proceso de pelambre contiene alta concentración de sulfuro, Demanda Biológica de Oxígeno (DBO), Demanda Química de Oxígeno (DQO), Sólidos Suspendidos Totales (SST), y Sólidos Disueltos (SD) [1].
El principal problema de los sulfuros en el agua es su fácil reacción para formar sulfuro de hidrogeno, el cual es un compuesto que a exposiciones de menos de 30 minutos a concentraciones entre 1 y 11,6 ppmv causa sensibilidad bronquial en trabajadores sanos, daños en el sistema respiratorio y efectos en el sistema nervioso central de los animales [4]. Igualmente, según lo expuesto por Salas [5], el ion sulfuro, debido a su carácter reductor, disminuye el oxígeno presente en el agua y por lo tanto afecta drásticamente la vida acuática.
Reconocida la problemática que representa los sulfuros en el agua y la apremiante necesidad de aplicar tecnologías para su remoción, se han desarrollado e investigado diferentes alternativas para el tratamiento de aguas residuales contaminadas con sulfuro, siendo las más conocidas la oxidación catalítica con manganeso y aire [5], coagulación/floculación [6], oxidación electroquímica [7], electrocoagulación [8], oxidación con permanganato de potasio [9], las combinaciones entre luz UVC y oxígeno disuelto [10] y tratamiento anaerobio con ozono [11].
La remoción de sulfuros con ozono es una técnica prometedora debido a que es un elemento que no deja residuos secundarios en su reacción, eliminando un amplio tipo de componentes orgánicos presentes en el medio [12]. El ozono (O3) es un compuesto con un potencial de oxidación de 2,07 en V (Voltios) a 25°C, únicamente superado por el potencial de oxidación del flúor (F) 3,03, del radical hidroxilo (HO*) 2,80 y del oxígeno atómico (O) 2,42 [13]. Ramírez et al. (2016) en su estudio sobre el tratamiento de aguas residuales de curtiembre empleando ozono gaseoso, logró remociones de DQO, fenoles totales y color entre el 50% – 95% con un suministro inicial de ozono de 45 mg/L [14]. Investigaciones adicionales, como la de Sivagami et al. (2018) señalan que dosificando ozono a razón de 0,5 mg O3/g de DQO en 500 ml de agua residual de curtiembre y 15 minutos de reacción, se alcanza una remoción entre el 10 – 20% de la DQO presente en el efluente del tanque de sedimentación primario y entre el 40 – 50 % de la DQO presente en el efluente del tanque de sedimentación secundario, así mismo, determinaron que la mayor eficacia del ozono se alcanzaba a pH 11 y que el tratamiento combinado de coagulación + aireación + ozono, alcanzaba una reducción de DQO entre 80 – 90 % [15]. En el presente trabajo se empleó la oxidación de sulfuros con ozono, sin catalizador para la remoción de contaminantes para el tratamiento de aguas residuales de pelambren provenientes de una industria curtidora.
II. METODOLOGÍA
A. Área de estudio
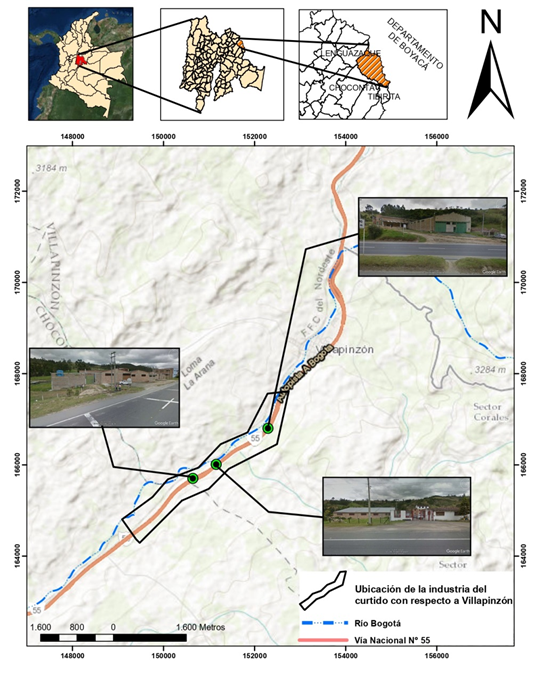
Las empresas curtidoras están situadas a las afueras del municipio de Villapinzón, Cundinamarca. Ubicadas en promedio a los 05º 11’ 34.04’’ N y 73º 36’ 57.49’’ O (151222,454 166108,511 metros en coordenadas planas) al sur occidente del municipio de Villapinzón, cuentan con una altitud media de 2671 m.s.n.m., y se encuentran justo al costado de la vía nacional número 55 y el Río Bogotá. A continuación, se presenta la ubicación de la industria del curtido en Villapinzón, y la ubicación de dicho municipio a nivel departamental y nacional. El mapa se realizó en el software ArcGis 10.3, se usaron mapas base integrados en el software y, Shapefiles de la Infraestructura de Datos Espaciales para el Distrito Capital (IDECA) y ArcGis Online, se utilizó la escala 1:55.000 y el sistema de coordenadas planas Magna Ciudad Bogotá.
Por otro lado, las empresas ubicadas en el área de estudio, pertenecientes al sector industrial del curtido de pieles, en general realizan el mismo proceso para la obtención del cuero; dicho proceso se divide en cuatro etapas:
Ribera: Recepción de las pieles conservadas con cloruro de sodio y eliminación de componentes inservibles para la transformación en cuero. En la Ribera las pieles que llegan presentan la característica de ser de color verdoso debido a la sal o de presentar aún residuos de sangre. Para iniciar el proceso se limpian las pieles extrayendo de ellas el pelo, las proteínas y las grasas que se encuentran en la endodermis. Así mismo, dentro de esta etapa es llevado a cabo el proceso de pelambre o depilado, allí, se realiza un “ataque químico para eliminar el pelo y la epidermis, aumentar la separación entre las fibras de colágeno de la piel, destruir proteínas no estructurales, así como nervios, vasos sanguíneos, etc.” [16].
Curtido: En este proceso se busca obtener una estabilidad química en la materia prima para evitar su descomposición sin importar que presente cambios de temperatura o humedad. Para llevar a cabo este proceso se hace uso de materiales de origen vegetal y sales de cromo. Una vez es finalizado este proceso a la piel se le denomina como cuero azul.
Recurtido: Teñido y Engrase: Las pieles adquieren cualidades físicas pertinentes para la comercialización de las mismas, como lo es el color.
Acabado: El cuero terminado es procesado para que reciba grabados o colores y así cumplir con los requerimientos del comprador, Para ello se implementan lacas o pigmentos.
B. Materiales y reactivos
El ajuste de pH fue realizado con NaOH (6N) y HCl (6N), el pH fue determinado haciendo uso de un potenciómetro Metrohm 781 pH/Ion Meter. Para el análisis de sulfuros en las muestras fueron empleados los reactivos expuestos en los métodos estándar para análisis de agua potable y residual (método Standard Methods 4500-S2-F) [17], todos los reactivos fueron grado analítico, de la marca Merck Millipore.
C. Diseño experimental
El proceso experimental se realizó para determinar el efecto que ejerce el pH sobre la remoción de sulfuros en el tratamiento de aguas, se comparó la remoción del contaminante en aguas de pelambre obtenida en una curtiembre ubicada en el municipio de Villapinzón, Cundinamarca, contra la remoción en un agua residual sintética que solamente contenía sulfuro de sodio y cal.
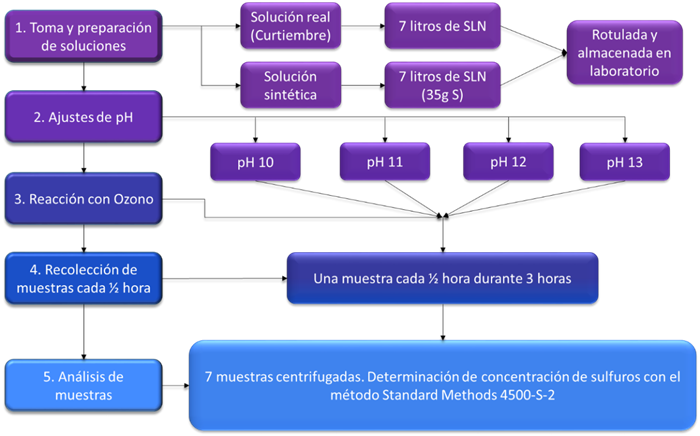
Se evaluó la efectividad de la ozonización a distintos pH para cada una de las aguas, manteniendo constante el caudal de aire (2,6 L min-1), dosis de ozono (0.5 g h-1) y tiempo de reacción (3 horas) de todos los ensayos. La recolección de muestras se hizo cada 30 minutos. El pH inicial de las aguas residuales utilizadas para los ensayos fue variado entre 10, 11, 12 y 13, cada ensayo fue realizado por triplicado, es decir, en total se realizaron 24 experimentos y se recolectaron 7 muestras en cada uno de ellos. Así mismo, se determinó la tendencia cinética de la remoción de sulfuros con ozono para cada solución ideal y real en las distintas condiciones de pH. La figura 2, corresponde al esquema metodológico empleado.
D. Equipo de ozono
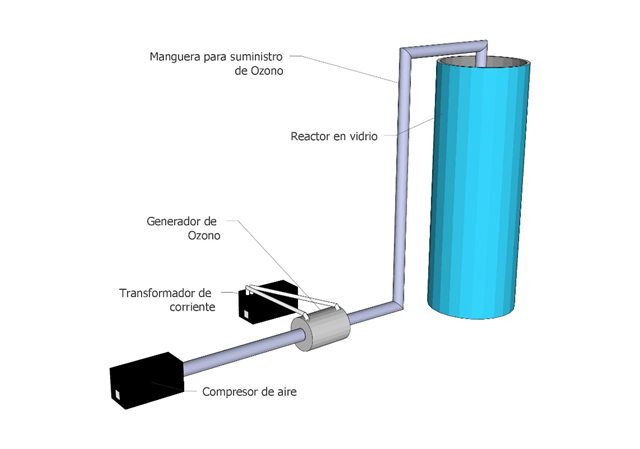
Para el suministro de ozono se empleó un equipo generador de ozono por efecto corona, el cual permito la dosificación de 0,5 g h-1 de ozono, este generador fue alimentado por aire a través de un compresor que entrego un flujo de 2,6 L min-1 de aire. De igual forma, el difusor de piedra porosa generó burbujas de ozono con diámetros entre 2 y 4 mm. A continuación, en la figura 3, presenta las distintas partes del sistema de generación y suministro de ozono para los ensayos realizados.
III. RESULTADOS Y ANÁLISIS
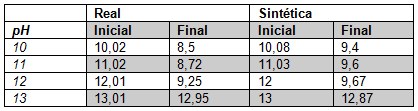
En la Tabla 1 se observa como el pH final del agua vario en todos y cada uno de los ensayos, siendo mayor la diferencia de pH para los ensayos en los cuales se presentó la mayor remoción de sulfuro, es decir, para las muestras reales a pH 11 y 12, lo que confirma que la oxidación de sulfuro procede vía formación de ácido sulfúrico [18], como el único producto final detectable, y que, de acuerdo a la estequiometria de la reacción (1), 2,3 moles de ozono son requeridas para la formación de una mol de ácido sulfúrico.
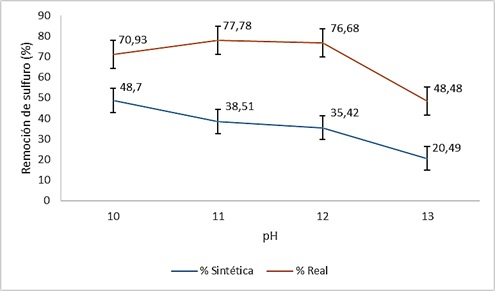
La Figura 4 presenta los porcentajes de remoción del sulfuro obtenidos para los distintos valores de pH inicial del agua, tanto para el agua residual sintética preparada en el laboratorio, como para el agua real tomada de la curtiembre. En el caso del agua residual sintética, se puede observar que el porcentaje de remoción de sulfuros disminuye a medida que se aumenta el pH, lográndose una remoción del 48.7 % para pH inicial de 10, en tres horas de reacción.
De la figura anterior también se observa que el porcentaje de remoción de sulfuros en todos los casos fue mayor para las aguas residuales reales (tomadas en la curtiembre) que para las aguas residuales sintéticas. Con respecto al agua residual real, el máximo porcentaje de remoción (77.78% / 76.68%) fue alcanzado para pH inicial entre 11 y 12 respectivamente, debido a la poca diferencia de los resultados, no se puede concluir cuál de estos dos valores de pH inicial del agua permitió alcanzar la mayor remoción pues no existe una diferencia estadísticamente significativa en la remoción promedio. Finalmente se determina que el pH presenta un efecto significativo sobre el proceso de oxidación de sulfuros con ozono, aumentando la remoción para pH inicial alcalino [15], por otra parte se observó que para pH inicial menor de 11 se presenta disminución de la efectividad del agente oxidante.
Como causa del aumento del porcentaje de remoción en la muestra real puede considerarse la presencia de sólidos en el agua, los cuales intervienen en el flujo del aire dentro del líquido, para favorecer la transferencia de masa de ozono desde la fase gaseosa a la fase liquida de manera que se logre saturar el agua residual con ozono y, por ende, asegurar la presencia y disponibilidad del oxidante en el agua para maximizar la remoción de sulfuros.
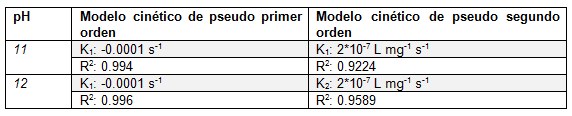
Con base en los resultados de remoción de sulfuro se determinó que la cinética de reacción para la oxidación de sulfuros se ajustó al modelo cinético de pseudo primer orden, se consideraron los modelos de pseudo primer y pseudo segundo orden debido a que el suministro de ozono permite suponer que la concentración de este en el agua fue constante. La Tabla 2 presenta los resultados del ajuste estadístico de los datos para determinar el tipo de modelo cinético que los describe.
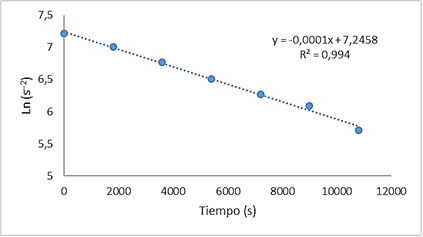
La ecuación del modelo cinético de pseudo primer orden está representada por , en la ecuación anterior K1 es el coeficiente cinético de pseudo primer orden en s-1 y S es la concentración de sulfuros en el agua residual expresada en mg L-1. La tendencia cinética del proceso evaluado fue realizada para agua residual real a pH 11 y 12, teniendo en cuenta que para este valor de pH inicial del agua se alcanzó el mayor porcentaje de remoción de sulfuros. En la figura 5 se presenta el gráfico correspondiente a la linealización de la cinética de pseudo primer orden, para agua residual real a pH inicial de 11, en este se observa claramente que los datos tienen tendencia lineal, lo que confirma el ajuste al modelo cinético analizado.
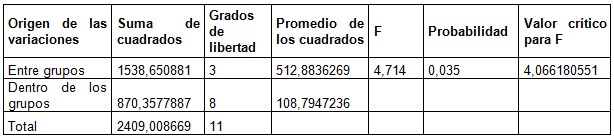
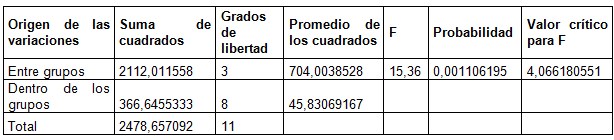
Las muestras tomadas según el diseño experimental fueron analizadas por medio de un ANOVA realzado en Excel Professional Plus 2016, a partir de éste se determinó la incidencia del pH sobre la remoción de sulfuros en el agua residual sintética y en el agua residual real, la hipótesis nula para el ANOVA fue que el porcentaje de remoción no varía con el pH para los ensayos realizados y, se estableció como un grado de confianza del 95%, en la Tablas 3 y 4 se presenta el ANOVA para el análisis de los porcentajes de remoción promedio para los ensayos realizados.
El ANOVA permite concluir que el valor del pH inicial del agua residual afecta la remoción de sulfuros cuando se hace uso de ozono como agente oxidante, lo que se verifica estadísticamente con los valores de probabilidad obtenidos de 0.035 y 0.011 los cual son menores que el valor alfa o grado de certeza seleccionado de 0.05, dando validez a la hipótesis alterna, es decir, que las medias de los resultados si varían con respecto al pH.
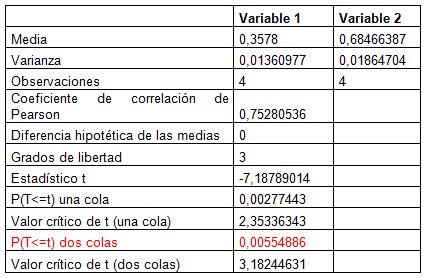
Los valores promedio de porcentaje de remoción fueron analizados para determinar si existen diferencias estadísticamente significativas, entre los resultados para el agua residual sintética y el agua residual real, con el objeto de lograr esto se hizo uso de la prueba de comparación de valores medios por la distribución t-student. La Tabla 5 presenta los resultados de la prueba t-student para la comparación de los valores medios de remoción de sulfuros.
Como punto de partida para la prueba se planteó como hipótesis que el porcentaje de remoción era igual para todos los valores de pH y para los dos tipos de aguas residuales analizadas. El valor obtenido de P(T<=t) para la prueba de dos colas, es menor al alfa establecido de 0.05, indicando que la hipótesis planteada no fue válida, hecho que confirma que los valores obtenidos del porcentaje de remoción son diferentes para cada valor de pH y cada tipo de agua.
IV. CONCLUSIONES
De acuerdo a los resultados se puede concluir que la mayor remoción de sulfuros en el agua se presentó para el agua residual real a pH 11 y alcanzó un valor de 77,78%, además se encontró que el pH inicial óptimo para la remoción de sulfuros con ozono se encuentra entre 11 y 12, pero no se puede establecer con claridad cuál es exactamente el pH óptimo, debido a la baja diferencia estadística de los resultados. Se determinó que la tendencia cinética del proceso evaluado a valores de pH entre 11 y 12 se ajusta al modelo cinético de pseudo primer orden, para el cual el coeficiente cinético (K) alcanzó un valor de -0.0001 s-1. Se puede señalar que la reducción de pH presentada en cada uno de los ensayos se debe a la formación de ácido sulfúrico (H2SO4) como único posible producto de oxidación con ozono. Finalmente, se considera que el aumento en el porcentaje de remoción de sulfuros observado para el agua residual real puede ser por efecto de la presencia de partículas en el agua, que favorecen la dispersión de las burbujas de ozono y por lo tanto maximizan la transferencia de masa aire/agua.