Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Ciencias
Print version ISSN 0121-1935
rev. cienc. vol.18 no.2 Cali July/Dec. 2014
Impacto alimentario de los copépodos calanoideos en el Océano Pacífico colombiano
Grazing Impact of Calanoid Copepods in the Colombian Pacific Ocean
Alan Giraldo
Departamento de Biología. Universidad del Valle, Cali - Colombia
E-mail: alan.giraldo@correounivalle.edu.co
Eliana Velasco
Departamento de Oceanografía, Universidad de Concepción, Concepción - Chile
E-mail: evelasco@udec.cl
Tulia Isabel Martínez
Departamento de Oceanografía Biológica, Instituto de Oceanografía, Universidad de Sao Paulo, São Paulo - Brasil
E-mail: tuismara@usp.br
Received: January 3, 2014
Accepted: December 18, 2014
Abstract
Grazing rate of copepods was evaluated in the oceanic province of the Colombian Pacific during September 2006. Gut pigment content was estimated by spectophotometry considering three size fraction: small (300-500 μm), medium (500-1000 μm) and big (> 1000 μm). In order to estimate the ingestion rate, an experimental gut evacuation rate of 0.702 h-1 was used. Feeding impact was calculated like a proportion of phytoplankton standing stock, projecting the total copepod consumption by size in relation to chlorophyll-a concentration in each station. Small copepods were most abundant than medium or big copepods (Kruskal-Wallis H=21.83; p=0.01). Although the ingestion rate of big copepods was higher than medium or small copepods (Kruskal-Wallis H=6.48; p= 0.04), no significant differences in the consumption rate were detected among sizes (Kruskal-Wallis H=3.07; p=0.21). The chlorophyll-a integrate (0-50m) in the study zone was between 4.4 and 9.5 mg Clo-a m-2, being estimated the grazing impact of the big copepod in 2.57 ± 0.80 %, medium 3.57 ± 1.89 % and small 12.06 ± 5.99%.
Keywords: grazing, ingestion rate, chlorophyll, copepods, Pacific Ocean, Colombia.
Resumen
Se determinó el impacto alimentario de los copépodos en nueve estaciones localizadas en la Cuenca Pacífica Colombiana durante septiembre de 2006. El contenido de pigmentos entéricos, fue medido espectrofotométricamente en tres fracciones de tamaño: pequeño (300-500 μm), mediano (500-1000 μm) y grande (> 1000 μm); y se estimó la tasa de consumo considerando una tasa de evacuación de 0.702 h-1 que fue establecida previamente de manera experimental. Considerando la abundancia de cada fracción y la concentración de clorofila-a en cada estación, se cuantificó el impacto alimentario como un porcentaje de la biomasa fitoplanctónica disponible. Los copépodos de menor tamaño fueron significativamente más abundantes en la zona de estudio (Kruskal-Wallis H=21.83; p=0.01). Aunque la tasa de ingestión de los copépodos grandes fue significativamente mayor (Kruskal-Wallis H=6.48; p= 0.04), no se detectaron diferencias significativas entre las tasas de consumo de las tres fracciones de tamaño evaluadas (Kruskal-Wallis H=3.07; p=0.21). La clorofila-a integrada (0–50m) en la zona de estudio estuvo entre 4.4 a 9.5 mg Clo-a m-2, siendo el impacto alimentario promedio de los copépodos grandes de 2.57 ± 0.80 %, medianos 3.57 ± 1.89 % y pequeños 12.06 ± 5.99%.
Palabras clave: forrajeo, ingestión, clorofila, copépodos, océano Pacífico, Colombia.
1. Introducción
El fitoplancton constituye el productor primario de la materia orgánica y la energía de la columna de agua. A partir de estos organismos, el zooplancton e incluso vertebrados superiores, obtienen la energía necesaria para sobrevivir, estructurando la trama trófica marina tradicional (Cifuentes et al., 2000; Friedland et al., 2012). En este escenario, los consumidores primarios que hacen parte del zooplancton se convierten en el enlace directo entre los productores primarios y los consumidores de la parte alta de la trama trófica, por lo que se convierten en un eslabón crucial para la transferencia de carbono en el ambiente pelágico (Huskin et al., 2001; Mayzaud, 2002; Frederiksen et al., 2006; Benoit-Bird et al., 2012).
En los mares tropicales, los consumidores primarios de la trama trófica pelágica lo conforman esencialmente los copépodos (Cifuentes et al., 2000; Calbet & Saiz, 2005; McKinnnon & Duggan, 2014). Estos organismos consumen diariamente la mitad de su propio peso, es decir cerca de 120000 diatomeas al día (Gifford & Dagg, 1991; Mauchline, 1998; Boling et al., 2012) y se constituyen en el engranaje de la "bomba biológica" en la columna de agua. Es a través de este mecanismo que el carbono atmosférico es asimilado por el fitoplancton, mediado por el proceso fotosintético y es transportado activamente por el zooplancton afuera de la zona fótica de la columna de agua durante el proceso de migración vertical (Small et al., 1983; Ducklow et al., 2001, Passow & Carlson, 2012).
En un contexto amplio, un aspecto esencial en la relación fitoplancton-zooplancton es el pastoreo "grazing" o impacto alimentario. Este impacto es una medida de la presión de consumo que ejerce el zooplancton sobre el fitoplancton, y para su estimación es necesario conocer la abundancia del zooplancton que consume fitoplancton, la cantidad de material fitoplanctónico disponible en el ambiente que se cuantifica con base en la concentración de clorofila-a, y las tasas de ingestiones específicas (Morales et al., 1993; Nejstgaard et al., 2007; Saiz & Calbet, 2011; Symons et al., 2012).
Aunque los copépodos no se alimentan exclusivamente de fitoplancton, junto con las salpas y los eufaúsidos, son considerados los organismos planctónicos que mayor impacto alimentario ejercen sobre el fitoplancton en el ambiente pelágico (Mauchline, 1998). Sin embargo, sus tasas de ingestión generalmente se relacionan con el tamaño del organismos, por lo que los trabajos de impacto alimentario en función del espectro de tamaño presenta ventajas comparativas sobre estudios a nivel de especie (Dam et al., 1993), toda vez que las diferentes fracciones de tamaño se alimentan de tamaños específicos de organismos fitoplanctónicos (Landry & Hassett, 1982; Sprules & Munawar 1986, Landry et al., 1994; Bautista & Harris, 1992; Hernández-Trujillo et al., 2007).
Tradicionalmente, se ha utilizado la fluorescencia intestinal (Mackas & Bohrer, 1976) como método indirecto para realizar la estimación de las tasas de ingestión in situ en diferentes especies de copépodos (Morales et al., 1990; Sautor et al., 2000; Tseng et al., 2008; Li et. al., 2013, Isla et al., 2015). Este método cuantifica la tasa de ingestión, a partir de la tasa de evacuación (k) y el contenido de pigmentos entéricos (G) en los individuos. Si se asume que las tasas de ingestión son similares en los individuos que tienen similar tamaño y se encuentran bajo condiciones ambientales similares(Morales et al.,1990; Bautista & Harris, 1992), entonces a partir de esta información y el estimado de abundancia del zooplancton herbívoro de una localidad se puede establecer el impacto alimentario total (Dagg, 1995; Tan et al., 2004, Hernández-Trujillo et al., 2007; Lee et al., 2012). En el presente trabajo se cuantifica el impacto alimentario que ejercen los copépodos sobre el fitoplancton en el Océano Pacífico colombiano, considerando el aporte proporcional de tres fracciones de tamaño, generándose información novedosa sobre uno de los procesos oceanográficos menos estudiados en esta región.
Materiales y métodos
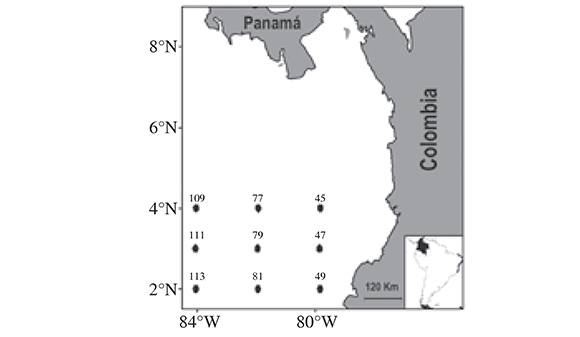
Se seleccionaron nueve estaciones oceánicas durante la campaña oceanográfica Pacífico XLIII, realizada en septiembre de 2006 a bordo de BO ARC Providencia (Figura 1) para realizar el muestreo biológico. En cada estación se cuantificó la concentración de clorofila disponible en la columna de agua, mediante colectas discretas de agua a profundidades estándar (0, 10, 30, 50 y 75 m) utilizando una botella Niskin. De cada profundidad se filtró una submuestra de 1 L de agua a través de filtros GF/F y se congeló en nitrógeno líquido (-70°C) para transportarla al laboratorio, y realizar el procedimiento estándar de extracción en acetona al 90% por 24 h y la correspondiente cuantificación de la concentración de clorofila-a por espectofotometría (Yentsch & Menzel, 1963; Holm-Hansen et al., 1965).
Figura 1. Área de estudio y ubicación de las estaciones en donde se realizaron las capturas de zooplancton durante la campaña oceanográfica Pacífico XLIII-ERFEN XLII en septiembre 2006 a bordo del B.O. ARC Providencia
Adicionalmente, en cada estación se realizaron arrastres oblicuos de zooplancton desde 50m a superficie utilizando una red bongo de 30 cm boca y 300 µm de poro de malla, provista de un flujómetro digital General Oceanic para cuantificar el volumen de agua filtrado. La muestra de uno de los copos de la red fue preservada en formol buferizado al 4% para estimar la abundancia de los copépodos estandarizada por m3 y la muestra del segundo copo fue concentrada por filtración, guardando el material en sobres de papel aluminio y congelada en nitrógeno líquido (-70°C) para realizar la cuantificación de pigmentos entéricos en el laboratorio.
La cuantificación de la concentración de pigmentos entéricos (G) se realizó por espectrofotometría después de 24 h de extracción en acetona al 90%, siguiendo el procedimiento estándar descrito por Mackas & Bohrer (1976) con las modificaciones propuestas por Morales et al., (1990). Los análisis fueron realizados considerando tres fracciones de tamaño: > 1000 µm (grandes), 500-1000 µm (medianos) y 300-500 µm (pequeños). Dependiendo del tamaño se seleccionaron entre 10 a 100 copépodos calanoideos bajo un estereoscopio con luz atenuada. Los organismos seleccionados se colocaron en tubos de ensayo con 10 mL de acetona al 90%. Generalmente los pigmentos son extraídos completamente después de 2 h (Huntley et al., 1987), sin embargo para el desarrollo de este trabajo se siguieron las recomendaciones de Båmstedt et al. (2000) dejando extraer los pigmentos por un período no menor a 12 h, a baja temperatura (4 0C) y en la oscuridad para evitar la fotodegradación. Al finalizar el período de extracción se midieron las concentraciones de clorofila-a (Clo-a) y feopigmentos (Feo), mediante la estimación de la absorbancia del extracto a diferentes longitudes de onda antes y después de la acidificación con HCl (10% v/v) en un espectrofotómetro Génesis 20 como:
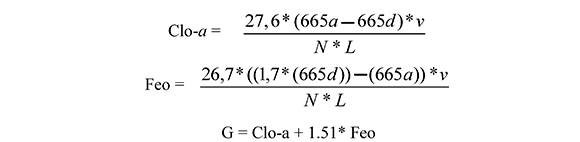
Donde 665a es la absorbancia antes de la acidificación, 665d es la absorbancia después de la acidificación, v es el volumen de acetona utilizado para la extracción en ml, N es el número de individuos utilizados en la extracción y L es el recorrido del camino óptico de la cubeta en cm, expresándose el contenido total de pigmentos entéricos (G) en µg Clo-a ind-1 (Båmstedt et al., 2000).
Para estimar la tasa de ingestión (I) se utilizó la aproximación propuesta por Dagg & Wyman (1983), a partir de la tasa de evacuación y el contenido de pigmentos entéricos previamente estimados como: I = k * G, donde I es la tasa de ingestión en términos de clorofila-a (µg Clo-a ind-1 tiempo-1), G es el contenido total de pigmentos entéricos (µg Clo-a ind-1) y k es la tasa de evacuación (unidades de tiempo-1). Se utilizó una tasa de evacuación de 0.702 h-1, la cual fue estimada experimentalmente a partir del decaimiento temporal del contenido de pigmentos estomacales en copépodos calanoideos del ambiente pelágico de isla Gorgona por Velasco (2009), ya que de acuerdo con Dam & Peterson (1988) la tasa de evacuación es dependiente de las condiciones locales de temperatura.
Para establecer la tasa de consumo por fracción de tamaño se utilizó la tasa de ingestión, y la abundancia estandarizada por volumen de agua filtrada de los copépodos calanoideos presentes en cada una de las fracciones de tamaño, como: C = I * A, donde C es la tasa de consumo (µg Clo-a m-3 tiempo-1), I es la tasa de ingestión (µg Clo-a ind-1 tiempo-1) y A es la abundancia (ind m-3). Considerando que la zona de estudio corresponde a un ambiente ecuatorial, se asumió un tiempo de integración para las tasas de ingestión y de consumo de 12 h, respectivamente. Se definió el pastoreo o impacto alimentario como el porcentaje equivalente de clorofila-a disponible en la columna de agua, que es canalizada a través de los copépodos considerando las tres fracciones de tamaño.
3. Resultados
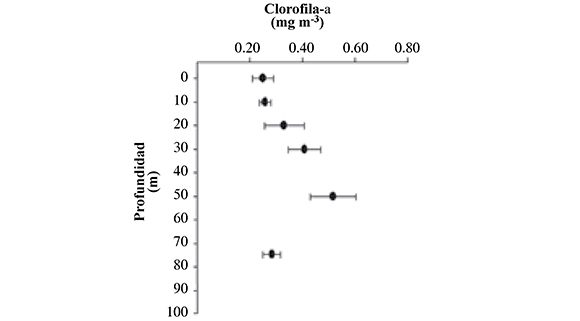
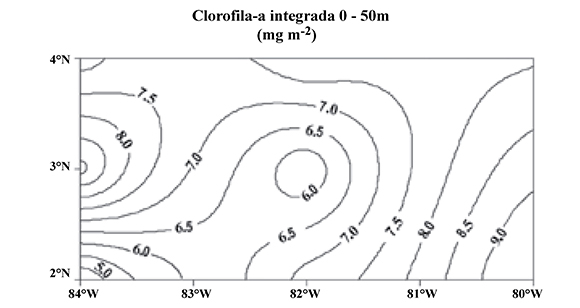
La concentración promedio superficial de la clorofila-a en la zona de estudio fue 0.25 ± 0.04 mg Clo-a m-3, detectándose un máximo subsuperficial (0.52 ± 0.09 mg Clo-a m-3) a 50m de profundidad (Figura 2). Al evaluar la variabilidad espacial en la sección de la columna de agua en donde se realizaron las capturas de zooplancton (0 - 50 m), se detectó la presencia de agua con baja concentración en el sector suroccidental de la zona de estudio (< 5.0 mg Clo-a m-2), registrándose además una tendencia de incremento en dirección al continente (Figura. 3).
Figura 2. Variación vertical de la clorofila-a en el ambiente oceánico del Pacífico colombiano durante septiembre 2006
Figura 3. Variación horizontal de la clorofila-a integrada entre 0 - 50 m de profundidad en el ambiente oceánico del Pacífico Colombiano durante septiembre 2006
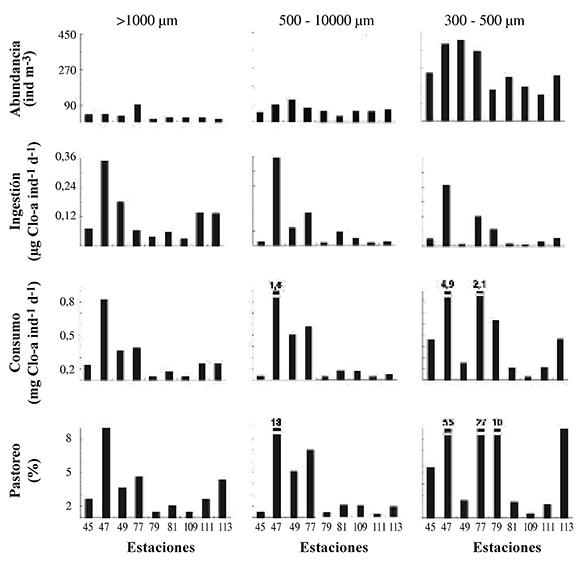
La abundancia total de copépodos calanoideos fue altamente variable en la zona de estudio, con una valor medio de 189.10 ± 49.96 ind m-3 (Figura 4). Al considerar las fracciones de tamaño, se encontró que la abundancia de los copépodos herbívoros fue inversamente proporcional a la clase de tamaño en todas las estaciones de muestreo, de tal manera que la fracción correspondiente a los copépodos pequeños fue significativamente más abundante (Kruskal-Wallis H=21.83; p<0.001).
Figura 4. Abundancia, tasas de ingestión, tasas de consumo y pastoreo de los copépodos en el ambiente oceánico del Pacífico colombiano durante septiembre 2006, considerando 3 fracciones de tamaño
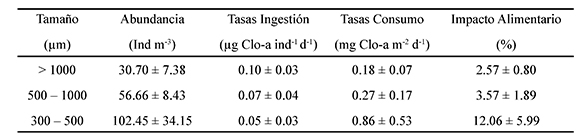
Las tasas de ingestión también fueron altamente variables en la zona de estudio, oscilando entre 0.003 - 0.353 µg Clo-a ind-1 d-1.; sin embargo, la tasa de ingestión fue directamente proporcional al tamaño, siendo significativamente mayor en copépodos grandes (Kruskal-Wallis H = 6.48; p = 0.04) (Tabla 1). No se encontró una asociación significativa entre la tasa de ingestión y la Clo-a integrada en la zona de estudio (Spearman rs = 0.33, p = 0.35, n=9), indicando que no hubo una respuesta funcional de parte de los copépodos asociada con la disponibilidad de alimento en la columna de agua.
Tabla 1. Registro promedio (±ES, n=9) de la abundancia, ingestión, consumo e impacto alimentario de los copépodos en el Pacífico colombiano
Aunque en términos generales la tasa total de consumo, por parte de los copépodos calanoideos, en la zona de estudio fueron homogéneas, se estableció una relación inversa con el tamaño, siendo la fracción más pequeña la que presentó la mayor tasa de consumo (Tabla 1, Figura 4). Esta fracción también fue la que presentó mayor abundancia en la zona de estudio, por lo que también fue la que ejerció una mayor presión de herbivoría (Tabla 1). Sin embargo, no se registraron diferencias significativas para la tasa de consumo (Kruskal- Wallis H = 3.07; p = 0.21) o impacto alimentario (Kruskal- Wallis H = 3.38; p = 0.18) entre las fracciones de tamaño (Tabla 1, Figura 4). Al cuantificar el impacto alimentario conjugado de las tres fracciones de tamaño en cada una de las estaciones de muestreo en la zona de estudio, se encontró que fue altamente variable con registros equivalente entre 2% al 81% de la clorofila-a disponible (Figura.4).
4. Discusión
De acuerdo con Calbet (2001) el impacto alimentario del mesozooplancton (entre los que se incluyen a los copépodos calanoideos) solo tendrá un efecto significativo en ambientes de alta producción, donde la trama trófica clásica parece ser la principal ruta para la transferencia del carbono. En ambientes oligotróficos, como el Océano Pacífico colombiano, los procesos de pastoreo "grazing" estarían principalmente modulados por el accionar de los pequeños consumidores (microzooplancton), quienes se encargan de la transformación del carbono orgánico, direccionándolo a través de la trama trófica pelágica (Tsuda et al., 1989; Morales et al., 1991; Verity et al., 1996, Bradford-Grieve et al., 1998; Turner 2014). Sin embargo, la alta abundancia de los copépodos en el ambiente pelágico y su alta capacidad de producir agregados fecales (Fowler & Knauer, 1986; Small et al., 1989; Altabet & Small, 1990), posicionan a este grupo taxonómico en un lugar clave dentro del proceso de flujo vertical de material biogénico en la columna de agua (Ducklow et al., 2001; Sommer & Stibor. 2002; Christina & Passow, 2007; Beaugrand et al., 2010), condición que aún no ha sido estudiada en el Océano Pacífico colombiano.
Una de las grandes dificultadas conceptuales asociadas con los procesos de estimación de impacto alimentario del zooplancton, en el ambiente pelágico, es la definición trófica funcional de herbívoros y carnívoros entre los diferentes grupos taxonómicos que conforman la comunidad zooplanctónica. En este sentido es relativamente fácil establecer un conjunto de taxa carnívoros como: los quetognatos, medusas, ctenóforos, o heterópodos; sin embargo no es posible definir con claridad el de los herbívoros (Lavaniegos, 2007). Por lo tanto, ha sido sugerido hablar de un hábito herbívoro-omnívoro o de organismos con dieta mixta (Gifford & Dagg, 1991; Dam et al., 1993; Mauchline, 1998) cuando se hace referencia a los consumidores primarios presentes en el mesozooplancton entre los que se destacan los copépodos (Kaehler et al., 2000, Trites, 2003; Martineau et al., 2004).
A pesar de esta limitación conceptual, establecer el impacto del pastoreo de los copépodos es esencial en el propósito de definir las rutas y establecer las tasas de flujo de material, a través de las tramas alimentarias locales (Vidal 1980, Carlotti et al., 2000; Stibor et al., 2004, Forest et al., 2011). En este sentido, una gran transferencia de fitoplancton hacia los copépodos puede estimular la producción de las pesquerías pelágicas, mientras que una baja transferencia favorecería el hundimiento del fitoplancton hacia el fondo de la columna de agua (Dagg, 1995; Ducklow et al., 2001).
Los estimados de consumo e impacto alimentario establecidos durante la presente investigación, fueron consistentes con los reportados para otras localidades y regiones del Pacífico. Por ejemplo Hernández-Trujillo et al. (2007), reportaron para la Bahía de La Paz, Baja California Sur, México, tasas de consumo de copépodos herbívoros entre 5.2 a 18.4 mg clo-a ind-1 y un impacto de pastoreo equivalente a entre 1.0% y 43% de la clorofila-a disponible, valores similares a los reportados para la estación E77 del Pacífico Colombiano (Malpelo). Incluso en zonas de surgencia como la costa del Perú han sido reportados impactos alimentarios equivalentes al 80% de la clorofila-a disponible (Boyd & Smith 1983), valor similar al registrado para E49 durante la presente investigación.
Son muchos los factores que pueden regular el impacto de pastoreo de los copépodos calanoideos sobre el fitoplancton en una localidad o región. Entre estos se destacan el tamaño, sexo y estadio de vida de los organismos, la concentración y el tamaño del alimento, la composición química del alimento, la historia previa de alimentación y las características físicas del medio (Parsons & LeBrasseur, 1970; Atkinson, 1995; Friedman & Strickler, 1975; García-Pámanes et al., 1991; Huntley et al., 2000). El efecto de estos factores provoca una alta variabilidad en las estimaciones de tasas de pastoreo o impacto alimentario, tanto a corta escala como a gran escala espacial y temporal, y en ambientes tropicales, templados y boreales (Dagg et al., 1980; Joiris et al., 1982; Cox et al., 1983; Conover & Cota, 1995; Gifford, 1988; Bautista et al., 1992; Román et al., 1993; García- Panámes et al., 2007), condición similar a la registrada para la zona oceánica del Pacífico colombiano.
A pesar de la reconocida importancia del pastoreo en el flujo del carbono para el ambiente pelágico (Huskin et al., 2001) y que en los ambientes tropicales se genera cerca del 80% de la producción primaria global, que representa el 70% del carbono total exportado en el Océano (Karl et al., 1996), los trabajos sobre pastoreo para la zona tropical y en especial en el Pacífico Oriental han sido escasos y esporádicos (Arinardi et al., 1990; Dam et al., 1995; Fernández-Ãlamo & Färber-Lorda, 2006). En este contexto, los resultados de esta investigación se constituyen en la primera cuantificación de impacto alimentario por parte del mesozooplancton en la provincia oceánica del Pacífico colombiano y es una de las escasas referencias de "grazing" para el Océano Pacífico Oriental Tropical.
Agradecimientos
A los funcionarios del Centro Control Contaminación del Pacífico (CCCP) por su apoyo durante la planificación y ejecución de las campañas de muestreo, en especial al Capitán de Corbeta Javier Ortiz, Dr. Efraín Rodríguez-Rubio y técnicos navales Juan Rueda y Diego Guerrero. Este trabajo fue financiado parcialmente por la Dirección General Marí- tima (DIMAR), el Centro Control Contaminación del Pacífico (CCCP) y la Universidad del Valle, en el marco del proyecto de investigación "Respuesta local de la comunidad zooplanctónica del sistema pelágico del Pacífico Colombiano a forzantes de gran escala, CI7709" a favor de A. Giraldo.
Referecias
Altabet, M.A., & Small, L.F. (1990). Nitrogen isotopic ratios in fecal pellets produced by marine zooplankton. Geochim. Cosmochim. Acta. 54 (1), 155-163. [ Links ]
Arinardi, O.H., Baars, M.A., & Oosterhius, S.S. (1990). Grazing in tropical copepods measured by gut fluorescence, in relation to seasonal upwelling in the Banda Sea (Indonesia). Neth. J. Sea. Res., 25, 545-560. [ Links ]
Atkinson, A. (1995). Omnivory and feeding selectivity in five copepod species during spring in the Bellingshausen Sea, Antarctica. ICES J. Mar. Scien. 52 (3-4), 385-396. [ Links ]
Båmstedt, U., Gifford, D.J., Atkinson, A., Irigioen, X., & Roman, M. (2000). ICES Manual of Zooplankton Methodology. London, UK: Academic Press (pp. 297-339). [ Links ]
Bautista, B., & Harris, R.P. (1992). Copepod gut contents, ingestion rates and grazing impact on phytoplankton in relation to size structure of zooplankton and phytoplankton during a spring bloom. Mar. Ecol. Prog. Ser., 82, 41-50. [ Links ]
Bautista, B., & Harris, R.P. (1992). Copepod gut contents, ingestion rates and grazing impact on phytoplankton in relation to size structure of zooplankton and phytoplankton during a spring bloom. Mar. Ecol. Progr. Ser., 82, 41-50. [ Links ]
Bautista, B., Harris, R. P., Tranter, P.R.G., & Harbour, D. (1992). In situ copepod feeding and grazing rates during a spring bloom dominated by Phaeocystis sp. in the English Channel. J. Plankton Res., 14 (5), 691-703. [ Links ]
Beaugrand, G., Edwards, M., & Legendre, L. (2010). Marine biodiversity, ecosystem functioning, and carbon cycles. Proc. Natl. Acad. Sci., 107 (22), 10120-10124. [ Links ]
Benoit-Bird, K.J., & McManus, M.A. (2012). Bottom-up regulation of a pelagic community through spatial aggregations. Biol. letters, 8(5), 813-816. [ Links ]
Boling, W.B., Sinclair, G.A., & Wawrik, B. (2012). Identification of calanoid copepod prey species via molecular detection of carbon fixation genes. Mar. Biol., 159 (5), 1165-1171. [ Links ]
Boyd, C.M., & Smith, S.L. (1983). Plankton, upwelling, and coastally trapped waves off Peru. Deep-Sea Res., 30, 723-742. [ Links ]
Bradford-Grieve, J., Murdoch, R., James, M., Oliver, M., & McLeod, J. (1998). Mesozooplankton biomass, composition, and potential grazing pressure on phytoplankton during austral winter and spring 1993 in the subtropical convergence region near New Zealand. Deep-Sea Res. Part I., 45 (10), 1709-1737. [ Links ]
Calbet, A. (2001). Mesozooplankton grazing effect on primary production: a global comparative analysis in marine ecosystems. Limnol. Oceanogr., 46 (7), 1824-1830. [ Links ]
Calbet, A., & Saiz, E. (2005). The ciliate-copepod link in marine ecosystems. Aquat. Microbial Ecol., 38 (2), 157-167. [ Links ]
Carlotti, F., Giske, F., & Werner, F. (2000). Modeling zooplankton dynamics. In, R.P. Harris, P. Wiebe, J. Lenz, H.R., Skjodal & M. Huntley (Eds.). ICES zooplankton methodology manual, (pp. 571-667). New York, USA: Academic Press. [ Links ]
Christina, L., & Passow, U. (2007). Factors influencing the sinking of POC and the efficiency of the biological carbon pump. Deep-Sea Res. PT II, 54 (5), 639-658. [ Links ]
Cifuentes, J.L., Torres- García, P., y Frías, M. (2000). El océano y sus recursos: Plancton. (2 ed.). Ciudad de México, México: Fondo de Cultura Económica (p. 161). [ Links ]
Conover, R.J., & Cota, G.F. (1985). Balance experiments with arctic zooplankton. En, J.S. Gray, & M.E. Christiansen (Eds). Marine biology of polar regions and effects of stress on marine organisms, (pp. 217-236). New York, USA: Wiley. [ Links ]
Cox, J.L., Willason, S., & Harding, L. (1983). Consequences of distributional heterogeneity of Calanus pacíficus grazing. Bull. Mar. Sci., 33, 213-226. [ Links ]
Dagg, M., Cowles, T., Whitledge, T., Smith, S., Howe, S., & Judkins, D. (1980). Grazing and excretion by zooplankton in the Peru upwelling system during April 1977. Deep-Sea Res, 27, 43-59. [ Links ]
Dagg, M.J. (1995). Copepod grazing and the fate of phytoplankton in the northern Gulf of Mexico. Cont. Shelf Res., 15, 1303-1317. [ Links ]
Dagg, M.J., & Wyman, K.D. (1983). Natural ingestion rates of the copepods Neocalanus plumchrus and N. cristatus calculated from gut contents. Mar. Ecol. Prog. Ser., 13, 37-46. [ Links ]
Dam, H., & Peterson, W. (1988). The effect of temperature on the gut clearance rate constant of planktonic copepods. J. Exp. Mar. Biol. Ecol., 123, 1-14. [ Links ]
Dam, H., Miller, C., & Jonasdottir, S.H.N. (1993). The trophic role of mesozooplankton at 47°N, 20°W diring the North Atlantic Bloom Experiment. Deep-Sea Res. II., 40 (1), 197-212. [ Links ]
Dam, H.G., Zhang, X., Butler, M., & Roman, M.R. (1995). Mesozooplankton grazing and metabolism at the equator in the central Pacific: implications for carbon and nitrogen fluxes. Deep-Sea Res. II, 42, 735-756. [ Links ]
Ducklow, H.W., Steinberg, D.K., & Buessele, K.O. (2001). Upper Ocean Carbon Export and the Biological Pump. Oceanography, 14(4): 50-58. [ Links ]
Fernández-Álamo, M.A., & Färber-Lorda, J. (2006). Zooplankton and the oceanography of the eastern tropical Pacific: A review. Prog. Oceanogr., 69: 318-359. [ Links ]
Forest, A., Tremblay, J.É., Gratton, Y., Martin, J., Gagnon, J., Darnis, G. et al. (2011). Biogenic carbon flows through the planktonic food web of the Amundsen Gulf (Arctic Ocean): A synthesis of field measurements and inverse modelling analyses. Progr Oceanogr., 91 (4), 410-436. [ Links ]
Fowler, S.W., & Knauer, G.A. (1986). Role of large particles in the transport of elements and organic compounds through oceanic water column. Prog. Oceanogr., 16 (3), 147-194. [ Links ]
Frederiksen, M., Edwards, M., Richardson, A.J., Halliday, N.C., & Wanless, S. (2006). From plankton to top predators: bottom-up control of a marine food web across four trophic levels. J. Anim. Ecol., 75 (6), 1259-1268. [ Links ]
Friedland, K. D., Stock, C., Drinkwater, K.F., Link, J.S., Leaf, R. T.B., Shank, V. et al. (2012). Pathways between primary production and fisheries yields of large marine ecosystems. PLoS One, 7(1), e28945. [ Links ]
Friedman, M.M., & Strickler, J.R. (1975). Chemoreceptors and feeding in calanoid copepod (Arthropoda: Crustacea). Proc. Acad. Nat. Scien., 72, 4185-4188. [ Links ]
García-Pámanes, J., Lara-Lara, J.R., & Gaxiola-Castro, G. (1991). Daily zooplankton filtration rates off Baja California. Estuar. Coast. Shelf Sci., 32, 503-510. [ Links ]
García-Pámanes, J., Lara-Lara, J.R., & Bazán-Guzmán, C. (2007). Pastoreo por el mesozooplancton en la región central del Golfo de California: un estudio estacional. En, B. Hernández de la Torre y G. Glaxiola (Eds). Carbono en ecosistemas acuáticos de México, (pp. 141-155). Ciudad de México, México: Semarnat, Instituto Nacional de Ecología, CICESE. [ Links ]
Gifford, D.J. (1988). Impact of grazing by microzooplankton in the Northwest Arm of Halifax Harbour, Nova Scotia. Mar. Ecol. Prog. Ser., 47, 249-258. [ Links ]
Gifford, D.J., & Dagg, M.J. (1991). The microzooplankton-mesozooplankton link: consumption of planktonic Protozoa by the calanoid copepods Acartia tonsa and Neocalanus plumchrus. Mar. Microbiol. Food Webs., 5, 161-177. [ Links ]
González, A. (1988). Plancton de las aguas continentales. Washington D.C., USA: Secretaria general de la Organización de los Estados Americanos (p. 130). [ Links ]
Hernández-Trujillo, S., Zárate, A., Pacheco, R., Esqueda, G., Reyes, J., & Aceves, G. (2007). Pastoreo del mesozooplancton sobre el fitoplancton en la Bahía de La Paz, B. C. S. México. Hidrobiológica, 17, 225 - 231. [ Links ]
Holm-Hansen, O., Lorenzen, C.J., Holmes, R.W & Strickland, J.D. (1965). Fluorometric determination of chlorophyll. J. Cons. Perm. Int. Explor. Mer., 30, 3-15. [ Links ]
Huntley, M., Gonzalez, A., Zhu, Y., Zho, M., & Irigoien, X. (2000). Zooplankton dynamics in a mesoscale eddy-jet system off California. Mar. Ecol. Prog. Ser., 201, 165-178. [ Links ]
Huntley, M.E., Tande, K., & Eilerstsen, H.C. (1987). On the trophic fate of Phaeocystis pouchetii (Hariot). II. Grazing rates of Calanus hyperoboreus (Kroyer) on diatoms and different size categories of Phaeocystis pouchetii. J. Exp. Mar. Biol. Ecol., 110 (3), 197-212. [ Links ]
Huskin, I., Anadon, R., Medina, G., Head, R.N., & Harris, R.P. (2001). Mesozooplankton distribution and copepod grazing in the Subtropical Atlantic near the Azores: Influence of mesoscale structures. J. Plankton Res., 23 (7), 671-691. [ Links ]
Huskin, I., Anadon, R., Wood-Walker, R.S., & Harris, R.P. (2001). Basin-scale latitudinal patterns of copepods grazing in the Atlantic Ocean. J. Plankton Res., 23 (12), 1361-1371. [ Links ]
Isla, A., Scharek, R., & Latasa, M. (2015). Zooplankton diel vertical migration and contribution to deep active carbon flux in the NW Mediterranean. J Marine Syst. 143, 86-97. [ Links ]
Joiris, C., Billen, G., Lancelot, C., Daro, M.H., Mommaerts, J.P., Bertels, A. et al. (1982). A budget of carbon cycling in the Belgian coast zone: relative roles of zooplankton, bacterioplankton and bentos in the utilization of primary production. Neth. J. Sea Res., 16, 260-275. [ Links ]
Kaehler, S., Pakhomov, E.A., & McQuaid, C.D. (2000). Trophic structure of the marine food web at the Prince Edward Islands (Southern Ocean) determined by d13C and d15N analysis. Mar. Ecol. Prog. Ser., 208, 13-20. [ Links ]
Karl, D.M., Christian, J.R., Dore, J.E., Hedel, D.V., Letelier, R.M., Lupas, L.M. et al. (1996). Seasonal and interannual variability of in primary production and particulate flux at station ALOHA. Deep-Sea Res. II., 43, 259-368. [ Links ]
Landry, M.R., & Hassett, R.P. (1982). Estimating the grazing impact of marine microzooplankton. Mar. Biol., 67, 283-288. [ Links ]
Landry, M.R., Peterson, W.K., & Fagernes, V.L. (1994). Mesozooplankton grazing in the southern California Bight. I. Population abundances and gut pigment contents. Mar. Ecol. Prog. Ser., 115, 55-71. [ Links ]
Lavaniegos, B.E. (2007). El papel del zooplancton en la transferencia del Carbono en el Océano. En, B. Hernández de la Torre y G. Glaxiola (Eds). Carbono en ecosistemas acuáticos de México, (pp. 129-139) Ciudad de México, México: Semarnat, Instituto Nacional de Ecología, CICESE. [ Links ]
Lee, D.B., Song, H.Y., Park, C., & Choi, K.H. (2012). Copepod feeding in a coastal area of active tidal mixing: diel and monthly variations of grazing impacts on phytoplankton biomass. Mar. Ecol., 33 (1), 88-105. [ Links ]
Li, C., Yang, G., Ning, J., Sun, J., Yang, B., & Sun, S. (2013). Response of copepod grazing and reproduction to different taxa of spring bloom phytoplankton in the Southern Yellow Sea. Deep-Sea Res. PT II., 97, 101-108. [ Links ]
Mackas, D., & Bohrer, R. (1976). Fluorescence analysis of zooplankton guts contents and an investigation of the diel feeding patterns. J. Exp. Mar. Biol. Ecol., 25, 77-85. [ Links ]
Martineau, C., Vincent, W.F., Frenette, J.J., & Dodson, J.J. (2004). Primary consumers and particulate organic matter: isotopic evidence of strong selectivity in the estuarine transition zone. Limnol Oceanogr, 49 (5), 1679-1686. [ Links ]
Mauchline, J. (1988). The biology of calanoid copepods. Advances in Marine Biology. 33. San Diego (CA), USA: Academic Press (p. 710). [ Links ]
Mayzaud, P., Tirelli, V., Errhif, A., Labat, J.P., Razouls, S., & Perissinotto, R. (2002). Carbon intake by zooplankton: importance and role of zooplankton grazing in the Indian sector of the Southern Ocean. Deep-Sea Research II, 49, 3169-3187. [ Links ]
McKinnnon, A.D., & Duggan, S. (2014). Community ecology of pelagic copepods in tropical coastal waters. In, L. Seuront (Ed). Copepods: Diversity, Habitat and Behavior, (pp. 25-49). Escocia: Nova Scotia Publishers, Inc. [ Links ]
Morales, C.E., Bautista, B., & Harris, R.P. (1990). Estimates of ingestion in copepod assemblages: gut fluorescence in relation to body size. In, M. Barnes, R.N. Gibson (Eds). Trophic relationships in the marine environment, (pp. 565-577). Univ. Press, Aberdeen, UK: Aberdeen. [ Links ]
Morales, C.E., Bedo, A., Harris, R.P. & Tranter, P.G. (1991). Grazing of copepod assemblages in the north-east Atlantic: the importance of the small size fraction. Plankton, J. Res., 13, 455-472. [ Links ]
Morales, C.E., Harris, R.P., Head, R.N., & Tranter, P.R. (1993). Copepod grazing in the oceanic northeast Atlantic during a 6 week drifting station: the contribution of size classes and vertical migrants. Plankton, J. Res., 15, 185-211. [ Links ]
Nejstgaard, J.C., Tang, K.W., Steinke, M., Dutz, J., Koski, M., Antajan, E., & Long, J.D. (2007). Zooplankton grazing on Phaeocystis: a quantitative review and future challenges. Biogeochemistry, 83 (1-3), 147-172. [ Links ]
Parsons, T.R., & LeBrasseur, R.J. (1970). The availability of food to different trophic levels in marine food chain. In, J.H. Steele (Ed.). Marine food chains, (pp. 325-343) Edinburgh, UK: Oliver Boyd. [ Links ]
Passow, U., & Carlson, C.A. (2012). The biological pump in a high CO2 world. Mar. Ecol. Prog. Ser., 470, 249-271. [ Links ]
Roman, M.R., Dam, H.D., Gauzens, A.L., & Napp, J.M. (1993). Zooplankton biomass and grazing at the JGOFS Sargasso Sea time series station. Deep-Sea Res., 40, 883- 901. [ Links ]
Saiz, E., & Calbet, A. (2001). Copepod feeding in the ocean: scaling patterns, composition of their diet and the bias of estimates due to microzooplankton grazing during incubations. Hydrobiology, 666 (1), 181-196. [ Links ]
Sautour, B., Artigas, L. F., Delmas, D., Herbland, A. & Laborde, P. (2000). Grazing impact of micro-and mesozooplankton during a spring situation in coastal waters off the Gironde estuary. J. Plankton. Res., 22 (3), 531-552. [ Links ]
Small, L.F., Flower, W.S., Moore, S.A., & LaRosa, J. (1983). Dissolved and fecal pellet carbon and nitrogen release by zooplankton in tropical waters. Deep-Sea Res. A, 30, 1199-1220. [ Links ]
Small, L.F., Landry, M.R., Eppley, R.W., Azam, F., & Carlucci, A.F. (1989). Role of plankton in the carbon and nitrogen budgets of Santa Monica Basin, California. Mar. Ecol. Prog. Ser., 56, 57-73. [ Links ]
Sommer, U., & Stibor, H. (2002). Copepoda-Cladocera-Tunicata: the role of three major mesozooplankton groups in pelagic food webs. Ecol. Res., 17 (2), 161-174. [ Links ]
Sprules, W.G., & Munawar, M. (1986). Plankton Size Spectra in Relation to Ecosystem Productivity, Size, and Perturbation. Can, J. Fish. Aquat. Sci., 43, 1789- 1794. [ Links ]
Stibor, H., Vadstein, O., Diehl, S., Gelzleichter, A., Hansen, T., Hantzsche, et al. (2004). Copepods act as a switch between alternative trophic cascades in marine pelagic food webs. Ecol. Lett, 7 (4), 321-328. [ Links ]
Symons, C.C., Arnott, S.E., & Sweetman, J.N. (2012). Grazing rates of crustacean zooplankton communities on intact phytoplankton communities in Canadian Subarctic lakes and ponds. Hydrobiology, 694 (1), 131-141. [ Links ]
Tan, Y., Huang, L., Chen, Q., & Huang, X. (2004). Seasonal variation in zooplankton composition and grazing impact on phytoplankton standing stock in the Pearl River Estuary, China. Cont Shelf Res., 24 (16), 1949-1968. [ Links ]
Trites, A. (2003). Food web in the ocean: who eats whom and how much? In, M. Sinclair & G. Valdimarsson (Eds). Responsible fisheries in marine ecosystem, (pp. 125-141). Rome, Italy: Food and Agriculture Organization of the United Nations, FAO. [ Links ]
Tseng, L.C., Kumar, R., Dahms, H.U., Chen, Q.C., & Hwang, J.S. (2008). Copepod gut contents, ingestion rates and feeding impact in relation to their size structure in the southeastern Taiwan Strait. Zool Stud, 47, 402-416. [ Links ]
Tsuda, A., Furuya, K., & Nemoto, T. (1989). Feeding of micro-and macrozooplankton at the subsurface chlorophyll maximum in the subtropical North Pacific. J. Exp. Mar. Biol. Ecol., 132 (1), 41-52. [ Links ]
Turner, J.T. (2004). The importance of small planktonic copepods and their roles in pelagic marine food webs. Zool. Stud, 43 (2), 255-266. [ Links ]
Velasco, E. (2009). Impacto alimentario de los copépodos herbívoros en la zona de influencia costera del PNN Isla Gorgona, Pacífico colombiano. Trabajo de Grado. Departamento de Biología, Universidad del Valle. Cali, Colombia. [ Links ]
Verity, P.G., Stoecker, D.K., Sieracki, T.M.E., & Nelson, J.R. (1996). Microzooplankton grazing of primary production at 140°W in the equatorial Pacific. Deep-Sea Res. Part II., 43 (4-6), 1227-1255. [ Links ]
Vidal, J. (1980). Physioecology of zooplankton. I. Effects of phytoplankton concentration, temperature, and body size on the growth rate of Calanus pacificus and Pseudocalanus sp. Mar. Biol., 56, 111-134. [ Links ]
Yentsch, C., & Menzel, D. (1963). A method for the determination of phytoplankton chlorophyll and phaeophytin by fluorescence. Deep-Sea Res., 10, 221-231. [ Links ]

Revista de Ciencias por Universidad del Valle se encuentra bajo una licencia Creative Commons Reconocimiento 4.0.