Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Ciencias
Print version ISSN 0121-1935
rev. cienc. vol.20 no.1 Cali Jan./June 2016
Síntesis y caracterización de una perovskita simple del tipo La0.8 Sr0.2 CrO3
Synthesis and Characterization of a Simple La0.8 Sr0.2 CrO3 perovskite
Ariatna Y. Neira Guio
Grupo de Desarrollo y Aplicaciones de Nuevos Materiales (DANUM), Universidad Pedagógica y Tecnológica de Colombia, Tunja - Colombia
E-mail: ariatnaneira@gmail.com
Jairo A. Gómez Cuaspud
Instituto para la Investigación e Innovación en Ciencia y Tecnología de Materiales. Grupo de Integridad y Evaluación de Materiales (GIEM-INCITEMA). Universidad Pedagógica y Tecnológica de Colombia, Tunja - Colombia
E-mail: jairo.gomez01@uptc.edu.co
Enrique Vera López
Instituto para la Investigación e Innovación en Ciencia y Tecnología de Materiales. Grupo de Integridad y Evaluación de Materiales (GIEM-INCITEMA). Universidad Pedagógica y Tecnológica de Colombia, Tunja - Colombia
E-mail: enrique.vera@uptc.edu.co
Received: July 15, 2015
Accepted: April 8, 2016
Resumen
En este trabajo se explora la síntesis y caracterización de un óxido cerámico tipo La0.8 Sr0.2 CrO3, a través de intermediarios tipo citrato que propiciaron la obtención de una fase cristalina pura del material a 900 oC. En la etapa inicial del proceso se partió de disoluciones de nitratos y ácido cítrico, que se trataron a una temperatura de 120 °C, hasta la consolidación de un gel que luego de ser tratado a 250 oC conformó un precursor metal orgánico que sirvió de base para la obtención del óxido cerámico. El precursor se caracterizó por espectroscopia infrarroja (FTIR) y análisis térmico (TGA-DTA), para evaluar la formación de los respectivos citratos e identif car la temperatura ideal de tratamiento térmico para evitar la potencial volatilización de especies de cromo. El material calcinado se caracterizó por difracción de rayos X (XRD) y microscopía electrónica (SEM-TEM), los resultados permitieron identif car la morfología, la textura y las características superf ciales del material, con tamaños promedio de cristalito de 45 nm y distancias interplanares de 0.29 nm para el principal plano de difracción (1 1 2). La composición química del sólido fue determinada mediante f uorescencia de rayos X (XRF), indicando la efectividad del método de síntesis propuesto.
Palabras clave: Perovskitas, precursores de citrato, pilas de combustible de óxido sólido (SOFC).
Abstract
In this work, we explore the synthesis and characterization of a ceramic oxide type La0.8 Sr0.2 CrO3, through citrate intermediaries which made possible to obtain a pure crystalline phase of material at 900 oC. In the initial stage of the process, we started from nitrate solutions and citric acid, which was treated at 120 oC, up to the consolidation of a gel which was treated at 250 oC to obtain a metal-organic precursor which represent the basis of ceramic oxide. The precursor was characterized by infrared spectroscopy (FTIR) and thermal analysis (TGA-DTA), to evaluate the formation of corresponding citrates, identifying the optimal calcination temperature and avoiding the potential volatilization of chromium species. The calcined material was characterized by X-ray diffraction (XRD) and electron microscopy (SEM-TEM), the results allowed to identify the morphology, texture and surface characteristics of the material, with an average crystallite size of 45 nm and d Spacing of 0.29 nm for the main diffraction facet (1 1 2). The chemical composition of solid was determined by X-ray f uorescence (XRF), indicating the effectiveness of the proposed synthesis method.
Keywords: Perovskites, citrate precursors, solid oxide fuel cells (SOFC).
1. Introducción
Durante las últimas décadas ha surgido un creciente interés por el desarrollo de sistemas alternativos para la generación de energía limpia y renovable, que permitan el empleo de combustibles de bajo impacto ambiental, reducir las emisiones de gases de efecto invernadero y una máxima efciencia energética. En este contexto, desde las fuentes eólicas hasta las de tipo fotovoltáico y sistemas híbridos, entre otros, las pilas de combustible son dispositivos que sobresalen como una de las alternativas más prominentes para la producción de energía, toda vez que pueden producir electricidad de forma directa a partir de una fuente de hidrógeno y oxígeno, con efciencias de más de un 70% y rendimientos termodinámicos que no están limitados al ciclo de Carnot (Mahato et al, 20135; Esposito et al., 2015). Si bien en el mercado se comercializan desde hace un tiempo, las pilas de combustible son muy variadas y se clasifcan dependiendo de la naturaleza de sus componentes electrodicos, en pilas de baja, media y alta temperatura de operación. Las pilas de baja y media temperatura fundamentan su desarrollo comercial debido a que posibilitan la fabricación de dispositivos móviles y portables de uso cotidiano en intervalos de temperatura que oscilan entre los 60 y los 200 °C. Esta enome ventaja las ha consolidado como uno de los sistemas más comunes y convencionales a nivel comercial. A pesar de ello, las elevadas cantidades de electrocatalizador de metal noble que emplean en sus ánodos (Pt, Rh, Pd) y su alta tendencia al envenenamiento por monóxido de carbono, las convierten en un blanco fácil del deterioro y, por tanto, de un elevado costo de funcionamiento, sumado al grado de refnamiento que se requiere en los gases de alimentación (Somalu et al., 2015; Gómez-Cuaspud y Valencia-Ríos, 2009).
Por otra parte, las pilas de combustible de alta temperatura de operación con electrodos sólidos cerámicos, denominadas comúnmente como SOFC, son dispositivos relativamente más sencillos, pues no incorporan metales nobles en sus electrodos ni requieren altos niveles de pureza de los gases de alimentación, lo que sumado a su elevada tolerancia a sustancias como el CO, que incluso puede utilizarse como combustible, consolidan este tipo de pilas como uno de los sistemas más apropiados para el diseño de unidades auxiliares de poder y sistemas para el abastecimiento de energía eléctrica en zonas apartadas de la infraestructura convencional (Weil et al., 2007). A pesar de sus amplias ventajas, aspectos negativos como la alta tendencia a la deposición de carbono en el componente anódico y en ocasiones la baja estabilidad térmica y estructural de los electrodos, la ciencia de materiales ha posibilitado la búsqueda de nuevos materiales, más efcientes y con propiedades texturales y morfológicas novedosas, principalmente derivadas de la implementación de nuevas rutas de síntesis, lo que ha permitido focalizar ingentes esfuerzos en el área de la física y la química para el diseño de nuevos sistemas SOFC (Handal & Thangadurai, 2013; Marrony et al., 2015).
En este sentido, una de las estrategias más empleadas, en la actualidad, es la de producir materiales cerámicos con estructura tipo perovskita un óxido con fórmula general ABO3, el cual es capaz de combinar el efecto de un catión con propiedades estructurales en la posición A del óxido (típicamente una tierra rara) y un catión de transición en la posición B, lo que le permite lograr materiales multifuncionales y escalables a nivel industrial, sin la necesidad de emplear costosos metales nobles para promover las reacciones asociadas a este tipo de dispositivos. Si bien es cierto que desde hace mucho se han implementado diversos métodos para la síntesis de esta clase de materiales como el método sol-gel (Cao et al., 2015), el de precipitación (Yang et al. 2012), el de mecano síntesis (Hong et al., 2015) y el hidrotérmico, entre otros (Wang et al., 2013), es el denominado de polimerización-combustión (Shiyi et al. 2015), el que ha proporcionado los mejores resultados debido a que posibilita la conformación de la fase cristalina buscada en los menores tiempos de reacción y permite conservar una serie de propiedades texturales y morfológicas de importancia a nivel electrocatalítico, conformando sólidos de estructura nanométrico (inferiores a los 10 nm) y con áreas superfciales activas que permiten promover el desarrollo de reacciones in situ (reformado de hidrocarburos) para la generación del combustible de hidrógeno a bajos costos. Al respecto y fundamentado en que la efciencia catalítica es uno de los aspectos más relevantes en este tipo de materiales, algunos óxidos tipo perovskita han sido investigados como los materiales más promisorios para eventuales aplicaciones, Gorte et al. (2003) ha reportado una amplia información sobre el comportamiento de diferentes óxidos tipo perovskita para aplicación en componentes anódicos en tecnologías SOFC, mostrando que es necesario que el sólido pueda promover reacciones de reformado interno; aspecto que tras varios años de investigación se concentra en evaluar una zona activa donde el catalizador anódico entra en contacto con la fase de combustible y el electrolito, denominado límite trifásico (abreviadamente TPB), dicho parámetro reviste una especial importancia pues a mayores valores de TPB, mayor desempeño electroquímico, posibilitando un fujo de especies cargadas durante el desarrollo de las reacciones químicas. En este sentido, el uso de diferentes materialess, basados en el sistema La1-x Sr CrO3-δ han representado siempre los más relevantes, permitiendo modifcar la actividad y la selectividad hacia la producción de atmosféricas en hidrógeno (Heidarpouret al., 2013; Oh et al., 2014).
Por lo anterior y con el ánimo de aportar conocimiento alrededor de los procesos de síntesis que rigen la obtención de materiales estructurados tipo perovskita con potenciales aplicaciones en pilas de combustible de óxido sólido (SOFC), la presente investigación se focaliza en la evaluación de una ruta de química húmeda que permita obtener un material basado en la estructura La0.8 Sr0.2 CrO3, para determinar el efecto del proceso de fabricación en términos de la composición, morfología y tamaño de cristalito entre otros. Para este propósito, el material se caracterizará mediante diferentes técnicas físicas y químicas que permitan identifcar y proponer variantes en el proceso y asívalidar la metodología propuesta.
2. Parte experimental
Para la síntesis del óxido de lantano, estroncio y cromo, se utilizaron los correspondientes nitratos de lantano, La (NO3)3.6H2O 99.9%, estroncio Sr(NO3)3 99% y cromo Cr(NO3)3.9H2O 99%, los cuales se disolvieron en agua des-ionizada (Milli-Q system: resistivity 1S.2 MQ cm, TOC < 10 mg L-1), ajustándolos a una concentración fnal de 1.0 M. La concentración de las disoluciones de los cationes se comprobó mediante valoraciones con EDTA en presencia de indicadores metalocrómicos y por valoración gravimétrica de cada uno. Las disoluciones de los iones metálicos se dosifcaron en un reactor de vidrio dotado con agitación magnética (150 rpm), control de temperatura y refujo. El orden de adición de los iones, se estableció de acuerdo a las correspondientes constantes de hidrólisis, asegurando un contenido total de 0.01 moles de iones. El sistema permaneció en calentamiento por 2 horas a S0 oC; al cabo de los cuales se adicionó una disolución de ácido cítrico 2.0 M en una proporción molar 0.5:1 (Hcit: Iones metálicos), con el fn de facilitar la formación de los respectivos compuestos de coordinación como se ha reportado de forma previa (Gómez-Cuaspud & Schmal, 2013).
El pH del medio se ajustó a un valor de 4.0 mediante la adición lenta de una disolución concentrada de amoníaco, con el fn de promover la formación preferente de los compuestos de coordinación tipo citrato y evitar potenciales reacciones de hidrólisis ó precipitados insolubles, de acuerdo con la información derivada del análisis y modelamiento propuesto utilizando el programa Hydra-Medusa (Oh et al., 2014). El sol resultante se calentó a 120 oC durante 24 horas hasta la formación de un gel, que se trató a 250 oC hasta el inicio del proceso de autocombustión y la subsecuente obtención de un conglomerado de polvos cerámicos, los cuales fnalmente se trataron a S00 oC durante 30 min para eliminar algunos residuos carbonosos remanentes de la etapa preliminar. El análisis del precursor mediante espectroscopía infrarroja (FT-IR), se realizó en un equipo Perkin-Elmer FTIR-1000 y los de tipo termo-gravimétrico (TGA-DTA) en un equipo simultáneo TG-STDA Mettler Toledo modelo TGA/SDTAS51e/LF/1600, los cuales permitieron confrmar la presencia de especies tipo citrato y posibilitaron evaluar la temperatura óptima para la consolidación de la fase cristalina buscada.
La formación de la fase, la pureza y la morfología del sólido se determinó por difracción de rayos X (XRD), en un equipo PANalytical X'pert PRO MPD, con detector Ultrafast X' celerator en disposición Bragg-Brentano, usando la radiación Cu Ka (λ = 1.541S6 Å) entre 10 y 90° 2θ con pasos de 0.02o. Los resultados de difracción se analizaron y refnaron utilizando el software X'Pert High Score y Cellref3.0, mientras la determinación del tamaño de cristalito se realizó mediante la ecuación de Debye-Scherrer utilizando la señal de difracción más característica utilizando el programa Scherrer Calculator. El análisis microscópico (SEM-TEM) se realizó en un equipo Leica-Zeiss LEO 440 dotado con cañón de electrones: 1-30kV, LaB6 y W, con imagen digital y analógica EDX y en un equipo JEOL 2100 con cañón termoiónico de LaB6 con un voltaje de aceleración de 200 kV dotado con cámara CCD de adquisición de imágenes de alta resolución. La composición del material ya calcinado se confrmó mediante fuorescencia de rayos X (XRF), en un espectrómetro secuencial de rayos X por dispersión de longitudes de onda S4 Pioneer, Bruker.
3. Análisis y discusión de resultados
3.1 Síntesis en medio acuoso
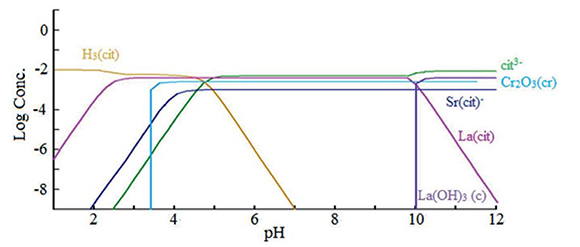
En la parte inicial del proceso de síntesis, la preparación y la naturaleza de los precursores del sistema La0.8 Sr0.2 CrO3 está sujeta a la presencia en el medio de reacción de distintas especies cuya existencia predomina y evoluciona en función del pH, de la concentración de ligandos y de la fuerza iónica, entre otras; en este sentido, el modelamiento de las potenciales reacciones que pueden tomar lugar bajo este tipo de condiciones, cobra una importancia inusitada debido a que evita la formación de especies insolubles o no deseadas, que modifcan la homogeneidad del medio y por tanto la composición del producto fnal. Dicho modelamiento se realizó mediante el empleo del programa Hydra-Medusa (Puigdomenech, 2002), permitiendo evaluar el comportamiento de cada uno de los cationes componentes; inicialmente, en el caso del lantano, se encontró que a pH < 3.0 este catión existe preferentemente en forma de especies La3+ y LaOH2+, al tiempo que el complejo sólido La(OH)3(c) precipita a pH > 10.0 mientras la formación del respectivo compuesto de coordinación de La(Cit), se establece en un intervalo de pH considerablemente amplio entre 2.0 y 10.0; situación consistente con algunas investigaciones en las cuales se ha demostrado que el catión La3+ forma compuestos poliméricos de coordinación con estructura [La(Cit)(H2O)2], los cuales son térmicamente estables por encima de los 15S °C y cristalizan en el grupo espacial monoclínico C2/c con a = 16.765(3) Å, b = 8.822(2) Å, c = 14.04S(3) Å y β = 120.64(3)°. Esta estructura consiste de cadenas de cationes La3+ enlazados por grupos O-C-O con aniones citrato que conforman una estructura pilarizada en la cual el citrato se coordina a tres átomos de lantano, con la formación de quelatos citrato-lantano en una estructura tridimensional compacta, la cual ha sido ampliamente demostrada por análisis elemental, FT-IR, TGA-DTA, y difracción de rayos X (Vanhoyland et al., 2005).
De igual forma, se ha encontrado que el catión estroncio existe en las formas Sr2+ y SrOH+ en un amplio intervalo de pH, sin embargo comienza a precipitar como especie Sr(OH)2 a pH > 8.0 y aunque en la actualidad se conocen diferentes conformaciones poliméricas tipo Sr(Hcit); Sr(H2Cit)+ y SrCit que son estables en intervalos de pH que dependen de factores como el pH y la relación Sr2+:citrato, la estructura cristalina más estable ha sido estudiada y clarifcada por Zacharias y Glusker (1993), según los cuales el catión Sr2+ puede coordinarse con ocho átomos de oxígeno y dos especies citrato, conformando un compuesto de coordinación tridentado tipo [Sr3(C6H5O7)(H2O)2].5H2O, en el que los grupos citrato pueden encontrarse ubicados de forma asimétrica en una conformación extendida favorecida cuando se emplean cationes divalentes como se indica en la Figura 1.
Figura 1. Diagrama de distribución de especies en función del pH para la síntesis del compuesto de LaO.8 SrO.2 CrO3 en presencia de ácido cítrico.
Para el caso del cromo, la situación es más compleja, ya que este no forma quelatos de citrato bajo las condiciones de concentración y temperatura aquíestablecidas, permaneciendo en forma de especies insolubles Cr2O3(cr), las cuales persisten en la mayor parte de la escala de pH (3,4-12); a pesar de esto, reportes recientes (Gabrielet al., 2007) han logrado establecer que bajo determinadas condiciones, el catión Cr3+ puede interactuar con ligandos del ácido cítrico en medios amoniacales, produciendo sistemas binarios de tipo (NH4)4[Cr(C6H4O7)(C6H5O7)].3H2O, que cristalizan en un grupo espacial monoclínico I2/a, con parámetros de celda a = 19.260(10) Å, b = 10.006(6) Å, c = 23.400(10) Å, β = 100.73o y V = 443.1Å3, los cuales han sido ampliamente caracterizados por análisis elemental, FT-IR, TGA-DTA y susceptibilidad magnética, sugiriendo la presencia de un número de especies entre las cuales el compuesto mono-nuclear octaédrico [Cr(C6H4O7) (C6H5O7)]-4 puede favorecerse alrededor de pH 4.0, confrmando que bajo las condiciones trabajadas en el presente trabajo, es posible obtener un compuesto de coordinación de estas características, donde los dos ligandos citrato poseen diferentes estados de desprotonación que se relacionan con la esfera de coordinación del Cr3+, revelando que el pH es un parámetro crucial en la formación de estos compuestos. Similarmente, el modelamiento propuesto permitió identifcar que a pH < 3.0 se presenta una fuerte tendencia a la hidrólisis, formando especies solubles que pueden ayudar en el proceso de consolidación de la fase homogénea buscada en el medio de reacción planteado (Gómez-Cuaspud & Schmal, 2013).
Así, con las condiciones de síntesis ajustadas se procedió a tratar la disolución formada a 120 oC durante 24 horas hasta la formación de un gel, que se trató a 250 oC hasta el inicio del proceso de autocombustión y la subsecuente obtención de un conglomerado de polvos cerámicos.
3.2 Caracterización
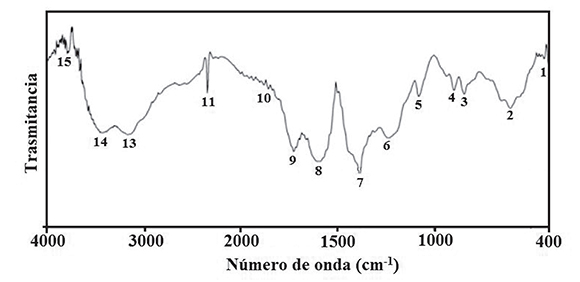
Espectroscopía infrarroja (FTIR): La caracterización del precursor obtenido del proceso de polimerización-combustión, confrmó la obtención de un precursor con grupos funcionales asociados a la presencia de grupos citrato. En la Figura 2, se muestran los diferentes espectros de los sistemas más representativos de la serie sintetizada, junto con sus correspondientes bandas de absorción, que indican una alta homogeneidad composicional entre los diferentes precursores. La banda a 3.791 cm-1, se debe a la vibración del enlace M-OH y la ubicada a 3.413 cm-1 a la vibración del OH libre del grupo citrato, el cual puede desplazarse a mayores frecuencias debido a que genera el fortalecimiento del enlace OH. Además, pueden ser debidas a las vibraciones simétricas y asimétricas de los enlaces OH de moléculas de agua, derivadas del proceso de síntesis del material, típicamente localizadas a 3.413 y 3.163 cm-1.
Figura 2. Espectro infrarrojo del precursor de LaO.8 SrO.2 CrO3 en pastilla de KBr obtenido a 25 oC, con sus principales bandas de absorción
Las bandas ubicadas hacia 2.340 y 2.360 cm-1, corresponden con modos de tensión asociados a la presencia de CO2, ocluido entre los poros del material en el proceso de formación de los precursores, mientras la banda ubicada hacia 1.S55 cm-1, puede identifcarse con vibraciones secundarias y de tensión del enlace C=O.
La banda a 1.729 cm-1, corresponde con el modo de tensión del enlace C=O en dímeros de ácidos carboxílicos alifáticos saturados, relacionada con el aumento del pH del sistema durante la consolidación del precursor. Por otro lado, la señal ubicada a 1.591 cm-1, puede asociarse al modo de tensión asimétrico del COO-de un compuesto de coordinación unidentado, que eventualmente puede desplazarse hacia bajos números de onda que también están relacionados con el mismo modo vibracional, pero en un compuesto de coordinación bidentado tipo puente. La banda a 1.3S5 cm-1, puede corresponder con el modo de tensión simétrico del COO-asociado a compuestos de coordinación bidentados; de igual forma, puede contener información relacionada con el grupo funcional NH4+. Otra banda es la ubicada a 1.231 cm-1, y que corresponde al modo de tensión del enlace C-O, relacionada con ésteres del ácido acético (CH3COOR), que pueden formarse en el proceso de secado de los soles de ácido cítrico. Las señales correspondientes con la banda a 1.07S y S96 cm-1, corresponden con el modo de tensión del enlace C-O, asociado a acetales y alcoholes primarios alifáticos saturados, asícomo a fexiones fuera del plano del enlace C-H, las cuales están presentes en todos los precursores y que pueden contener información sobre el NH4OH adicionado en el proceso de ajuste del pH del medio de reacción. Las bandas ubicadas a bajo número de onda a S43, 667 y 410 cm-1, corresponden con el enlace de los diferentes cationes metálicos de La3+, Sr2+ y Cr3+ con grupos OH y átomos de oxígeno, cuyos modos vibracionales u(O-M-O) pueden verse fortalecidos en función del pH, además de sufrir ligeros desplazamientos hacia longitudes de onda más bajas. Esta situación, confrma que el pH del medio escogido para la síntesis del material, favorece la obtención de especies diméricas de ácidos carboxílicos, asícomo el establecimiento preferente de compuestos de coordinación bidentados por parte del grupo COO-y el fortalecimiento de los enlaces M-O.
La banda a 1.791 cm-1 indica la presencia de un carbonilo neutro, mientras que la banda localizada a 1.591 cm-1 indica un sistema carbonilo con carga de -1, debido a un quelato formado en el proceso de reacción, la banda a 1.231 cm-1 es consistente con el enlace C-O sencillo, confrmando lo observado en la banda a 1.791 cm-1 y, fnalmente, la banda a 1.400 cm-1, es debida a la vibración C-O, confrmando lo observado en la banda a 1.591 cm-1, que posee carga negativa y, por lo tanto, es un sistema resonante.
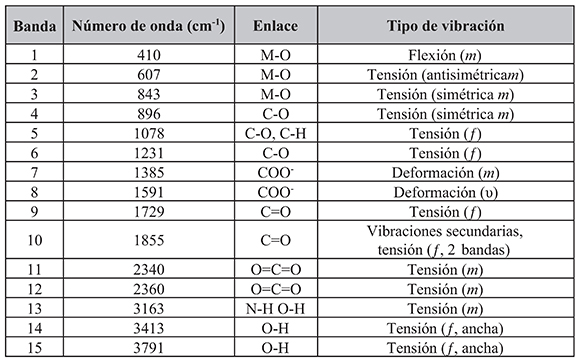
Además, los ésteres poseen un banda, debida a la vibración asimétrica del C=O entre 695 y 600 cm-1, que en los precursores estaría contenida en la banda ancha alrededor de 607 cm-1, junto con la banda a S96 cm-1 que puede contener información del grupo CO-O del éster. Finalmente, a manera de referencia, se muestra una comparación, con la biblioteca espectral de referencia, en la cual se demuestra la presencia de grupos funcionales similares a los mostrados por el precursor obtenido. Comparando la posición de las bandas de absorción observadas en el espectro del ácido cítrico con la tabla 1 de bandas esperadas, se puede realizar la asignación y comprobar algunos grupos moleculares en común presentes en los precursores obtenidos.
Tabla 1. Posición de las bandas de absorción infrarroja en el precursor de LaO.8 SrO.2 CrO3 comparadas con la base de datos SDBS
En función de las principales bandas de absorción identifcadas, fue clara la presencia de especies tipo citrato, confrmadas por la separación de la banda del grupo carboxílico libre (∼ 1.730 cm-1) en dos bandas características, llamadas uOCOasym (∼ 1.590 cm-1) y uOCOsym (∼ 1.3S0 -1.400 cm-1) y por el cambio de la banda asignada a υ(C-OH) a frecuencias más bajas (1.0S0 - 1.070 cm-1) [7, S].
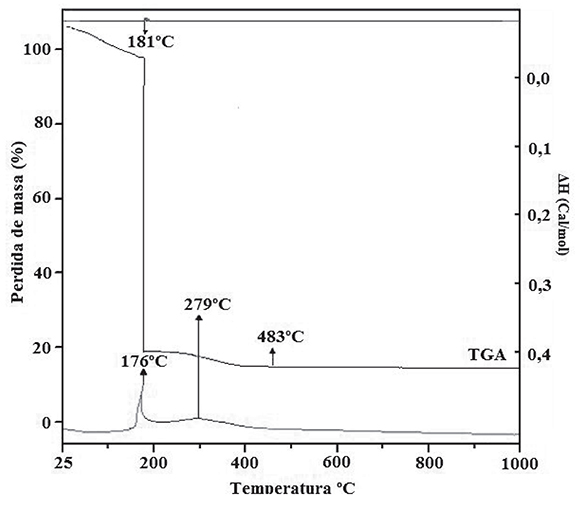
Análisis térmico (TGA-DTA): El análisis mostrado en la Figura 3 confrma una primera etapa de desprotonación entre 25 y 114 oC (zona I) y tiene lugar en dos etapas que sugieren diferencias en el modo de enlace de las moléculas de agua presentes fnalizando en la zona II. Con esto se confrma lo observado en el IR, las bandas alrededor de 3.413 y 3.163 cm-1, son debidas defnitivamente a las vibraciones asimétricas y simétricas de los enlaces OH de las moléculas de agua.
Figura 3. Curva de análisis térmico (TGA) para el compuesto precursor LaO.8 SrO.2 CrO3 obtenido por el método de polimerización-combustión
La deshidratación continúa hasta la eliminación de agua intramolecular a temperaturas cercanas a los 12S oC; al mismo tiempo, se inicia la formación de especies amoniacales entre 130 y 156 oC, acompañada por la eliminación de especies radicales(R-O) (Gómez-Cuaspud, 2015).
Posteriormente, el precursor evoluciona a un máximo, relacionado con la eliminación de materia orgánica (- CH2, CO, CO2 y C3H6 principalmente) entre 15S y 21°C (zona II), mostrando una ligera estabilización en el peso, con pérdidas variables. En este punto, cuando la mayoría de la materia orgánica se ha destruido y la eliminación de las especies carbonatadas se ha completado, puede observarse en la muestra, una señal exotérmica a ≈ 279 °C. Dicho proceso, marca el inicio de la obtención del precursor oxídico necesario para la estabilización de la fase cristalina del compuesto La0.8 Sr0.2 CrO3. La naturaleza de los compuestos que persisten en esta etapa, se han discutido en la literatura (Todorovsky et al., 2002; Milanova et al., 1998) y de acuerdo con diferentes reportes y evidencias, se admite la formación de especies relacionadas con carbonatos, oxocarbonatos metálicos y otros óxidos intermedios formados en el proceso; inclusive, se sabe que estas sustancias, amorfas o cristalinas pueden existir desde los 450 oC hasta los S50 °C. En este sentido, en algunas investigaciones en las cuales se han comparado diferentes curvas de TGA, entre precursores preparados mediante rutas de química húmeda, se ha demostrado que las pérdidas fnales de peso para composiciones similares, pueden darse alrededor de los 800 ºC y corresponden con una señal endotérmica seguida por una de tipo exotérmica que incluso, mediante curvas de DTA en nitrógeno, han mostrado un comportamiento similar, asociado a las pérdidas de peso por presencia de carbonatos inorgánicos (Van et al., 1998; Baythoun y Sale, 1982). Las ligeras variaciones de masa que aparecen entre 500 y 700 oC, corresponden a fenómenos de descomposición de especies secundarias y a procesos de reorganización estructural. En consecuencia, los análisis permitieron localizar una temperatura ideal de tratamiento térmico, que no sólo favoreció la obtención del sistema de La0.8 Sr0.2 CrO3, sino que además evitó la eventual volatilización de especies de cromo asociadas a este compuesto.
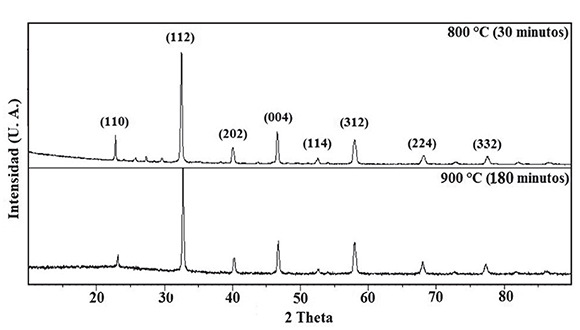
Difracción de rayos X (XRD): El espectro de difracción de rayos X del material calcinado y mostrado en la Figura 4, fue analizado y comparado con la base de datos del programa X`Pert High Score, permitiendo determinar una gran similitud con el material de referencia La0.8 Sr0.2 CrO3 ICSD:01-074-19S0 y el óxido obtenido en el presente trabajo. La caracterización permitió clasifcar el óxido como un material cristalino cúbico de grupo espacial Pm-3m, con parámetros de celda a = 3.860 Å, b =3.860 Å, c =3.860 Å y ángulos α = β = γ = 90.0°.
Figura 4. Patrón de difracción de rayos X indexado del sistema LaO.8 SrO.2 CrO3 obtenido a 8OO °C con presencia de fases secundarias de La2O3 y SrOy sistema tratado a 9OO °C por 3 horas
La indexación y la estimación del tamaño de cristalito se realizaron utilizando las señales más intensas de difracción, usando la ecuación de Debye-Scherrer, tomando el valor medio de pico (β) y una constante de 0.89, resultando en un tamaño medio de 45nm. Las señales en el patrón de difracción, localizadas entre 25° y 30° 2 theta, corresponden con una fase secundaria de óxidos de lantano y estroncio La2O3 y SrO respectivamente, que no se integraron a la estructura cristalina por efectos de las bajas temperaturas de síntesis, lo cual se corrobora una vez el material es sinterizado a 900 °C por 3 horas, logrando la fase cristalina buscada, como se indica en la Figura 4. La determinación del factor de tolerancia del sistema, se realizó mediante el programa SPuDS (Structure Prediction Diagnostic Software), confrmando la estabilidad del grupo espacial Pm-3m con un valor de 0.9672 a una temperatura de 25 °C.
Microscopía electrónica (SEM-TEM) y medida de área superfcial (BET): Los análisis por microscopía electrónica permitieron evaluar la morfología, la textura y las características superfciales del sólido obtenido a 900°C, evidenciando que la técnica de síntesis le confere al material propiedades de importancia a nivel superfcial lo que puede suponer la promoción de reacciones de importancia como se indica en la Figura 5.
Figura 5. Imágenes de microscopía electrónica de barrido para la muestra calcinada de LaO.8 SrO.2 CrO3 obtenidas a diferentes magnifcaciones
Los resultados de microscopía electrónica de transmisión, permitieron desarrollar un conteo estadístico de la estimación del tamaño de los cristalitos nanométricos de morfología regular que conforman el conglomerado de polvos cerámicos sintetizados, orientados de forma preferencial en el plano (1 1 2), con tamaños promedio de 44.8 nm 45.0 nm y distancias interplanares de 0.29 nm para el principal plano de difracción. Las micrografías no evidencian la formación o presencia de residuos carbonosos remanentes del proceso de autocombustión, lo que sugiere la efectividad del proceso propuesto, como se indica en la Figura 6.
Figura 6. Micrografías electrónicas de transmisión y distancia interplanar para la muestra de LaO.8 SrO.2 CrO3
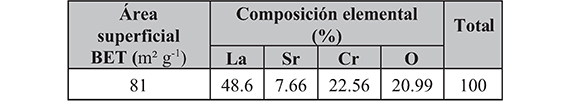
Por otra parte, las medidas de área superfcial logradas a través de la técnica BET por isotermas de adsorción de nitrógeno, permitieron establecer una medida en tamaño de 7.3 nm con un área de 81 m² g-1, dichos resultados, guardan relación con los derivados del estudio por difracción de rayos X y microscopía electrónica, en los cuales puede verse como el método de síntesis le confere al sólido de La0.8 Sr0.2 CrO3 ciertas características texturales y morfológicas específcas, mejorando la microestructura del sólido como se muestra en la Tabla 2.
Tabla 2. Medida de área superfcial para el sistema LaO.8 SrO.2 CrO3 obtenida mediante la técnica de isotermas de adsorción BET y medidas de composición elemental obtenidas por fuorescencia de rayos X
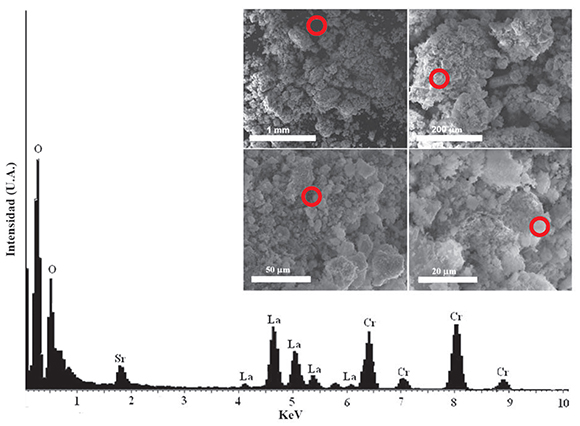
Composición elemental por fuorescencia de rayos X (XRF): Finalmente, la determinación de la composición del sistema, se realizó mediante análisis por fuorescencia de rayos X en la muestra calcinada a 900 °C por tres horas, confrmando una buena correlación entre la composición nominal y obtenida, como se indica en la Tabla 2 y Figura 7.
Figura 7. Espectro de fuorescencia de rayos X para la muestra de LaO.8 SrO.2 CrO3 , obtenido a partir de los análisis de microscopía electrónica de barrido
A partir de estos resultados, es claro que se mantiene una estrecha relación con los valores estequiométricos buscados, lo anterior valida el método propuesto y las temperaturas de calcinación para lograr la fase cristalina sin pérdidas por volatilización de especies de cromo. El espectro de fuorescencia obtenido y los sitios de muestreo aleatorios que se muestran en la Figura 7, donde se grafca el conteo de rayos X en función de la energía de los niveles atómicos de los elementos detectados, las señales encontradas se integraron y normalizaron respecto al elemento de mayor intensidad evidenciando la presencia de los elementos componentes del óxido sintetizado.
4. Conclusiones
En este trabajo queda demostrado que el método de polimerización-combustión con ácido cítrico permite la síntesis a baja temperatura de materiales nanométricos, topotácticamente diseñados no densifcados y con estructura cristalina defnida. Los análisis fsicoquímicos realizados evidencian que el material sintetizado en la primera etapa como precursor metalorgánico presenta bandas de vibración infrarroja características y asociadas con la formación de compuestos de coordinación a manera de citratos, lo cual favorece la obtención de compuestos homogéneos, solubles y de alta pureza, que poseen temperaturas de consolidación de fase cristalina relativamente bajas alrededor de los 483 °C. La caracterización estructural del material mediante difracción de rayos X, evidenció la obtención de un sólido cúbico de estequiometría defnida asociado con el material La0.8 Sr0.2 CrO3 , con parámetros de red coherentes con una fase pura del material.
Finalmente, los análisis microestructurales realizados con microscopía electrónica SEM y TEM, confrmaron la obtención de un material homogéneo y del orden nanométrico alrededor de los 45 nm; hecho que supone su potencial aplicabilidad en el diseño y la construcción de componentes electrodicos para pilas de combustible de óxido sólido, pues supone una mejora en el estado del arte esperado en la síntesis de este tipo de materiales. Al respecto es claro que el modelamiento de las condiciones de síntesis en medio acuoso, evitando la segregación de componentes insolubles y el control sobre la presencia de fases heterogéneas determinaron el éxito de la metodología propuesta en el presente trabajo.
Referencias
Baythoun, M. S., Sale, F. R (1982). Production of strontium substituted lanthanum manganite perovskite powder by the amorphous citrate process. Journal of Materials Science, 17, 2757-2759. [ Links ]
Cao, XG., Jiang, SP., & Li, YY. (2015). Synthesis and characterization of calcium and iron co-doped lanthanum silicate oxyapatites by sol-gel process for solid oxide fuel cells. Journal of Power Sources, 293, 806-814. [ Links ]
Esposito, V., Garbayo, I., Linderoth, S., & Pryds, N. (2015). Solid-oxide fuel cells 15. Epitaxial Growth of Complex Metal Oxides, 443. [ Links ]
Feng, H., Chen, L., Xie, Z., & Sun, F. (2015). Constructal optimization for a single tubular solid oxide fuel cell. Journal of Power Sources, 286, 406-413. [ Links ]
Gabriel, C., Raptopoulou, C. P., Terzis, A., Tangoulis, V., Mateescu, C., & Salifoglou, A. (2007). pH-specifc synthesis and spectroscopic, structural, and magnetic studies of a chromium(III)-citrate species. Aqueous solution speciation of the binary chromium(III)-citrate system. Inorg. Chem., 46, 2998-3009. [ Links ]
Gómez-Cuaspud, J. (2015). Synthesis and characterization of cerium fuorites based on CeLn Osystem (Ln: Nd3+, Sm3+, Eu3+, Gd3+, Dy3+ and Ho3+). Journal of the Chilean Chemical Society, 60(2), 2774-2781. [ Links ]
Gómez-Cuaspud, J. A., y Valencia-Ríos, J. S. (2009). Síntesis de óxidos tipo LaSrCrFeO3 mediante polimerización con ácido cítrico. Rev. Energética, 42(2), 69-72. [ Links ]
Gómez-Cuaspud, J., & Schmal, M. (2013). Nano-structured metal oxides obtained by means polymerization-combustion at low temperature for CO selective oxidation. International Journal of Hydrogen Energy, 38, 7458-7462. [ Links ]
Gorte, R. J., & Vohs, J. M (2003). Novel SOFC anodes for the direct electrochemical oxidation of hydrocarbons. J. Catal. 216, (1-2), 477-486. [ Links ]
Handal, H.T., & Thangadurai, V. (2013). Evaluation of chemical stability, thermal expansion coeffcient, and electrical properties of solid state and wet chemical synthesized Y and Mn-codoped CeO2 for solid oxide fuel cells. Journal of Power Sources, 243, 458-471. [ Links ]
Heidarpour, A., Saidi, A., Abbasi, M. H., & Choi, G. M. (2013). In situ fabrication mechanism of a dense Sr and Ca doped lanthanum chromite interconnect on Ni-YSZ anode of a solid oxide fuel cell during Co-sintering. Ceramics International, 39(2), 1821-1826. [ Links ]
Hong, H. S., Lee, S., & Lee, C. S. (2015). Characterization of (Ni-Cu)/YSZ cermet composites fabricated using high-energy ball milling: effect of Cu concentration on the composite performance. Ceramics International, 41(4), 6122-6126. [ Links ]
Mahato, N., Banerjee, A., Gupta, A., & Omar, S., Balani, K. (2015). Progress in material selection for solid oxide fuel cell technology: A review. Progress in Materials Science, 72, 141-337. [ Links ]
Marrony, M., Ancelin, M., Lefevre, G., & Dailly, J. (2015). Elaboration of intermediate size planar Proton conducting solid oxide cell by wet chemical routes: A way to industrialization. Solid State Ionics, 275, 97-100. [ Links ]
Milanova, M. M., Arnaudov, M. G., Getsova, M. M., & Todorovsky, D. S. (1998). Preparation and characterization of solid state lanthanum titanium citrate complexes. Journal of Alloy Compounds, 264, 95-103. [ Links ]
Oh, TS., Anthony, SY., Adijanto, L., & Gorte, RJ. (2014). Infltrated lanthanum strontium chromite anodes for solid oxide fuel cells: Structural and catalytic aspects., Journal of Power Sources, 262, 207-212. [ Links ]
Puigdomenech, I. (2002). Make equilibrium diagrams using sophisticated algorithms Medusa. Stocholm, Sweden: Royal Institute of Technology. [ Links ]
Shin, T.H., Hagiwara, H., Ida, S., Ishihara, T. (2015). RuO2 nanoparticle-modifed (Ce,Mn,Fe)O2/(La,Sr)(Fe,Mn)O3 composite oxide as an active anode for direct hydrocarbon type solid oxide fuel cell. Journal of Power Sources, 289, 138-145. [ Links ]
Shiyi, C., Noam, L., & Wenguo, X. (2015). Coal gasifcation integration with solid oxide fuel cell and chemical looping combustion for high-effciency power generation with inherent CO2 capture. Applied Energy, 146, 298-312. [ Links ]
Somalu, S.P.S., Shaikh, S.P.S., Muchtar, A., Somalu, M.R. (2015). A review on the selection of anode materials for solid oxide fuel cells. Renewable and Sustainable Energy Reviews, 51, 1-8. [ Links ]
Subotié, V., Schluckner, C., Mathe, J., Rechberger, J., Schroettner, H., & Hochenauer, C. (2015). Anode regeneration following carbon depositions in an industrial-sized anode supported solid oxide fuel cell operating on synthetic diesel reformate. Journal of Power Sources, 295, 55-66. [ Links ]
Todorovsky, D. S., Getsova, M. M., & Vasileva, M. A. (2002). Thermal decomposition of lanthanum titanium citric complexes prepared from ethylene glycol medium. Journal of Materials Science, 37, 4029- 4039. [ Links ]
Van, D., Kruidhof, R. H. E., Nijmeijer, A., Winnubst, A., & Burggraaf, J. (1998). Preparation of perovskite by thermal decomposition of metal EDTA complexes. Journal of Materials Chemistry, 8(9), 2109-2112. [ Links ]
Vanhoyland, G, J. P., D'Haen, J., Mullens, S., & Mullens, S. J. (2005). Characterization and structural study of lanthanum citrate trihydrate La(C6H5O7)(H2O)2].H2O. J. Solid State Chem., 178, 166-171. [ Links ]
Wang, SF., Yeh, CT., Wang, YR., & Wu, YC. (2013). Characterization of samariumdoped ceria powders prepared by hydrothermal synthesis for use in solid state. Journal of Materials Research and Technology, 2(2), 141-148. [ Links ]
Weil, K. S., Hardy, J. S., & Kim, J. Y. (2007). A new technique for joining ceramic and metal components in high temperature electrochemical devices. J. Adv. Mater., 2, 84-94. [ Links ]
Yang, T., Zhao, H., Han, J., Xu, N., Shen, Y., Du, Z. et al. (2014). Synthesis and densifcation of lanthanum silicate apatite electrolyte for intermediate temperature solid oxide fuel cell via co-precipitation method. Journal of the European Ceramic Society, 34(6), 1563-1569. [ Links ]
Zacharias, D. E., & Glusker, J. P. (1993). Structure of strontium citrate pentahydrate. Acta Cryst. C., 49, 1732-1735. [ Links ]

Revista de Ciencias por Universidad del Valle se encuentra bajo una licencia Creative Commons Reconocimiento 4.0.