1 Introducción
El departamento de Norte de Santander, Colombia, se encuentra rodeado por tres grandes cuencas: río Magdalena, río Catatumbo y río Orinoco, 1 que cuentan con una variedad de especies icticas de impacto económico, siendo Prochilodus sp, las especies más representativas a nivel comercial. 2-4.
Prochilodus magdalenae (bocachico), especie endémica de la cuenca del rio Magdalena, 5 se distribuye en las zonas bajas de los rios Magdalena, Sinú y Atrato, hasta los 1,000 m.s.n.m., aproximadamente; y en el río Cauca alcanza a remontar a la cuenca alta hasta los 1,500 m.s.n.m. debido a la pendiente suave. 6 En la década de los años 80 se estableció que la población de bocachico estaba cercana a los límites de aprovechamiento sostenible (tasa de explotación E= 41%). 7 Para la cuenca del Sinú, Valderrama y Solano 2004, 8 determinaron una disminución progresiva de la biomasa desovante durante el periodo 1997-2002, pasando de 279 ton a 32 ton, con mortalidades por pesca (F media anual= 1.9 año-1) muy superiores al punto biológico de referencia (PBR) de mortalidad por pesca al máximo rendimiento por recluta Fmax= 0.9 año-1, indicando altos niveles de sobreexplotación. En razón a su gran importancia económica, P. magdalenae es la especie íctica más investigada del país, no obstante, persisten vacíos de información sobre aspectos reproductivos, genéticos poblacionales, dinámicas poblacional y migratoria en las cuencas del Magdalena y Atrato. Para la cuenca del Sinú se conoce su dinámica migratoria y estructura genética de las poblaciones. 6
Prochilodus reticulatu se encuentra en las cuencas de los ríos Catatumbo y Ranchería, distribuidas en Colombia y Venezuela. 9 En el Catatumbo habita en toda la cuenca desde el Lago de Maracaibo y ciénagas adyacentes de la parte baja, hasta los 1,000 m.s.n.m. En época de aguas bajas remonta el río Catatumbo y demás tributarios como los ríos, Tibú, Tarra, San Miguel, río de Oro, Sardinata, Nuevo Presidente y Zulia, hasta aproximadamente los 1,000 m.s.n.m. 10 Para el Catatumbo, P. reticulatu era la especie de mayor contribución a las capturas totales, según los monitoreos realizados entre 1989 y 1995 por la Asociación Cravo Norte, 11 sin embargo, en la actualidad su aporte ha disminuido.
Se ha observado que los ríos Catatumbo y Magdalena comparten muchas especies de peces, lo que hace suponer un origen común. 9 Shultz 10 consideraba que las cuencas de estos ríos debieron converger en algún momento; el levantamiento de la serranía del Perija, durante el plioceno superior separo en dos, las cuencas del Magdalena y Catatumbo con lo cual poblaciones de peces prácticamente idénticas quedaron aisladas de lado y lado de esta serranía evolucionado por separado. Los endemismos producidos por esta separación no bastan para explicar las diferencias entre la fauna del Magdalena y del Catatumbo. 2 La caracterización genética se convierte en una herramienta importante que permite dar un nuevo enfoque más acorde a la relación filogenética entre estas especies. 12,13 Las metodologías moleculares han revolucionado el análisis genético permitiendo la identificación de especies implementando diversas técnicas moleculares. La técnica para detectar polimorfismo en el ADN amplificado al azar (RAPD) en ictiología, es un método basado en la PCR, en el que se emplea un cebador corto, generalmente de 10 bases, para amplificar secuencias arbitrarias de ADN. 11 Con esta técnica no se busca ningún fragmento de ADN específico, ya que el cebador se adhiere al ADN patrón en secuencias complementarias de ubicación desconocida. En consecuencia, no se conocerá la naturaleza de los productos obtenidos. Los fragmentos de ADN así generados se separan y se detectan mediante electroforesis, produciendo polimorfismos que permiten una caracterización molecular de las especies en estudio. Según Alberti 14 su rapidez, sencillez y bajo costo son los marcadores elegidos para numerosos estudios de diversidad, sobre todo en especies no modelo en las que no se dispone de información previa de secuencia. Silva et al.15, utilizaron de forma exitosa los marcadores RAPD y ADN mitocondrial (mtADN) en el pez Atherinella brasiliensis, determinando su diversidad genética, estructura de la población y el flujo de genes. En otra investigación, Mohapatra et al. 16, evaluaron la variación genética y la filogenia molecular entre y dentro de dos poblaciones de Catla catla implementando la técnica RAPD. Según lo anterior y teniendo en cuenta los estudios de Bardakci y Skibinski 17 en especies de Tilápia, el empleo de marcadores RAPD pueden detectar variaciones interpoblacionales e interespecíficas en poblaciones de peces. Diferentes autores han evaluado la estructura genética de las poblaciones y han caracterizado una gran variedad de peces, que han permitido conocer las relaciones evolutivas de un grupo de especies utilizando los marcadores RAPD. 15-19 Sin embargo, no se han reportados estudios en donde se analicen las relaciones filogenéticas entre las especies P. magdalenae y P. reticulatus. Por tal motivo esta investigación busca caracterizar a nivel molecular las especies P. reticulatus y P. magdalenae, utilizando la técnica RAPD. Posteriormente, se realiza un análisis filogenético utilizando el coeficiente de Jaccard y el método UPGMA para determinar la relación entre las especies trabajadas.
2 Materiales y métodos
Se recolectaron cuatro individuos de cada una de las siguientes poblaciones:
P. magdalenae de la piscícola San Silvestre Barrancabermeja Santander - Colombia (Figura 1A).
P. reticulatus de la piscícola del parque eco turístico Paco Piedra Corponor Zulia Norte de Santander- Colombia (Figura 1B).
Prochilodus. mariae en el río Urivante Orinoco Venezolano. Utilizada como control positivo.
Anodus laticeps del parque eco turístico Paco Piedra Corponor Zulia Norte de Santander - Colombia, como control negativo por ser una especie que no pertenece al genero Prochilodus.
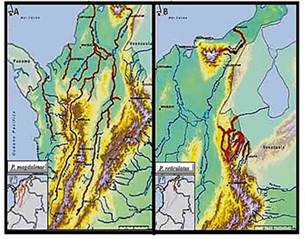
Figura 1 Distribución geográfica de P. magdalenae y P. reticulatus. A. localización de P. magdalenae. B. localización de P. reticulatus. Fuente: Mojica et al.6.
2.1 Extracción de ADN
El ADN fue extraído a partir de la aleta dorsal de dieciséis individuos siguiendo el protocolo de fenol cloroformo por maceración manual descrito por Sambrook et al.20 Posteriormente, se visualizó la cantidad y calidad del ADN en un gel de agarosa al 1%. Las muestras de ADN fueron almacenadas a 4° C hasta su utilización.
2.2 Caracterización molecular mediante RAPD
Se utilizó la metodología propuestas por Hatanaka y Galetti 21 en la estandarización de la mezcla de PCR, las temperaturas y los tiempos para la amplificación arbitraria mediante RAPD de los ADN de P. magdalenae, P. reticulatus, P. mariae y A. laticeps. Los cebadores utilizados fueron OPP-7 GTCCATGCCA, OPP-12 AAGGGCGAGT, A11 CAATCGCCGT y A02 TGCCGAGCTG. 21,22
La PCR se realizó con un paso inicial de desnaturalización a 94° C durante 5 minutos, seguido de 45 repeticiones de 1 minuto a 94° C, 1 minuto a 36° C y 2 minutos a 72° C, con un ciclo final de extensión a 72° C por 15 minutos. Los productos de la PCR se analizaron en geles de agarosa al 1.4%.
3. Estudio Filogenético
Para el estudio filogenético de P. magdalenae y P. reticulatus se utilizaron matrices de presencia y ausencia de bandas de los perfiles de ADN obtenidos por RAPD con cada uno de los cebadores utilizados. Con ellos se hizo un análisis de agrupamiento con el fin de identificar patrones de similitud entre P. magdalenae y P. reticulatus comparado con P. mariae como control positivo y A. laticeps como control negativo. Los datos de perfiles de bandas fueron ordenados de acuerdo a un sistema binario de 0 y 1, donde valores de 0 indican ausencia de una banda y 1 la presencia en una posición determinada. Los perfiles de fragmentos de ADN obtenidos con los 4 diferentes cebadores fueron analizados con el Software estadístico NTSYS 2.2. En este análisis se empleó la técnica de ligamiento por el promedio ponderado o UPGMA. La matriz de similitud fue construida utilizando el coeficiente de Jaccard. 23
4 Resultados y discusión
En el aislamiento de ADN, utilizando el procedimiento propuesto por Sambrook et al.20 , se obtuvo un ADN en adecuada de alta concentración y pureza en las especies P. magdalenae, P. reticulatus, P. mariae y A. laticeps demostrando la eficacia en la extracción de ADN (Figura 2).
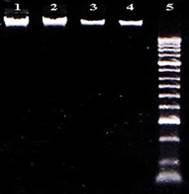
Figura 2 ADN aislado mediante el método de Fenol-Cloroformo con maceración manual. 1: P. magdalenae; 2: P. reticulatus; 3: P. mariae; 4: A. laticeps; 5: Marcador de peso molecular Hyperladder II.
Para la caracterización molecular de P. magdalenae y P. reticulatus todas las amplificaciones realizadas mostraron patrones de bandas definidas y reproducibles. El perfil de bandas que generó cada uno de los cebadores (Figura 3) fue analizado para cada especie mediante el registro de la presencia («1») o ausencia («0») de bandas de ADN de tamaño similar. El criterio utilizado para identificar una banda como polimórfica fue su presencia o ausencia en forma consistente en dos amplificaciones independientes, demostrando la reproducibilidad de la técnica. Estos resultados permitieron construir una matriz binaria que combinó todos los polimorfismos detectados en las especies utilizadas en este estudio.
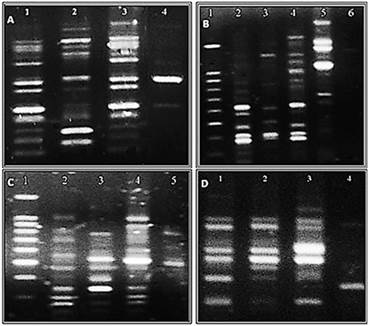
Figura 3 Patrones de amplificación RAPD. A: cebador OPP7 (1: P. reticulatus; 2: P. mariae; 3: P. Magdalenae; 4: A. Leptus). B. cebador OPP12 (1: Marcador de peso molecular 100bp DNA Ladder; 2: P. reticulatus; 3: P. mariae; 4: P. Magdalenae; 5: A. laticeptus) C. cebador A02 (1: Marcador de peso molecular 100bp DNA Ladder; 2: P. reticulatus; 3: P. mariae; 4: P. Magdalenae; 5: A. laticeps. D. cebador A11 (1: P. reticulatus; 2: P. mariae; 3: P. Magdalenae;4: A. Laticeps.
En el análisis filogenético utilizando el cebador OPP7 se observó que el índice de similitud de 0.93 obtenido entre P. reticulatus y P. magdalenae muestra una relación muy estrecha, lo que demuestra que las diferencias a nivel molecular entre estas dos especies son mínimas (Figura 4A). En un estudio realizado por Hatanaka y Galetti 21, en donde establecen una caracterización molecular de P. marggravii distribuidas en diferentes áreas geográficas, la amplificación con el cebador OPP7 mostró un alto grado de polimorfismo, estableciendo una diferenciación genética en los individuos en sus diferentes hábitats. También este cebador ha sido utilizado en estudios de caracterización de algas, hongos, plantas y mamíferos, mostrando un alto grado de polimorfismo. 24
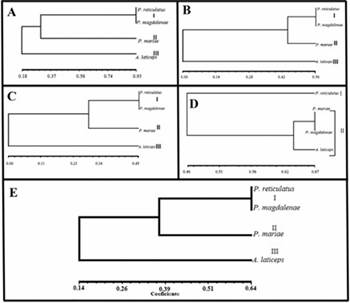
Figura 4 Dendrogramas de similitud usando el coeficiente de Jaccard y el método UPGMA. (A) Cebador OPP-7. (B) Cebador OPP-12. (C) Cebador A11. (D) Cebador A02. (E) Análisis total.
Los cebadores OPP12 y A02 presentaron un porcentaje de similitud de 0.56 y 0.45, respectivamente, entre P. reticulatus y P. magdalenae, mostrando una relación entre estas dos especies. Establecen una diferencia de 0.45 para OPP12 y 0.31 para A02, con el control P. mariae y una diferencia total con los dos cebadores con el control negativo A. laticeps (Figura 4B y 4C). Estos cebadores también han sido utilizados mostrando amplificaciones polimórficas en estudios de caracterización molecular en otros peces, como Piaractus mesopotamicus y Leporinus elongatus,13 y en plantas, como Solanum tuberosum25.
El análisis molecular con el cebador A11 mostro una diferencia con los cebadores anteriores, agrupando al control negativo A. laticeps con P. magdalenae y P. mariae con un coeficiente de similaridad de 0.64. Además, establece una diferencia entre P. reticulatus y las demás especies analizadas (Figura 4D). Este marcador molecular localiza regiones altamente polimórficas no apropiadas para el estudio a nivel de género y especie en la familia Curimatidae, sino probablemente permitiría caracterizar especies en categorías taxonómicas superiores.
Relacionando los cuatro cebadores utilizados mediante un análisis de similitud y agrupamiento se observó la formación de 3 clusters entre las especies comparadas. Todas presentaron un porcentaje de similitud de 0.14. P. mariae exhibe un coeficiente de similaridad de 0.38 con P. reticulatus y P. magdalenae. El porcentaje de agrupamiento entre P. reticulatus y P. magdalenae fue de 0.64 (Figura 4E). Islam et al.19, utilizaron marcadores moleculares RAPD para analizar la diferenciación genética en las poblaciones de C. catla en tres ríos de la india a partir de la combinación de cuatro cebadores aleatorios (OPB03, OPB08, OPB09, OPB15) el coeficiente de similitud varió De 0,025 a 0,052 en las poblaciones de los ríos Halda (0.052) Jamuna y Padma (0.025), demostrando que entre más distantes son geográficamente las poblaciones de C. catla, la distancia genética va a ser mayor. 19 Otro estudio similar con cuatro poblaciones de C. catla, confirman la importancia de los marcadores RAPD para discriminar eficazmente las diferencias genéticas de las poblaciones. 18. Silva et al. 15, implementaron los marcadores RAPD y el ADN mitocondrial (mtADN) para brindar información sobre la diversidad, la estructura y la historia de las poblaciones de A. brasiliensis a lo largo de la costa brasileña. Recientemente, se emplearon exitosamente los marcadores de mtADN para conocer la estructura de las poblaciones y las relaciones filogenéticas del pez Gymnocypris dobula.26 En otras investigaciones, Orozco et al.27, utilizaron los marcadores de microsatélites para determinar la diversidad genética y la estructura poblacional de P. magdalenae en la cuenca del río Magdalena en Colombia, constituyendo una herramienta para una mejor comprensión del comportamiento y biología de esta especie, contribuyendo a la gestión de la pesca y los programas de conservación de P. magdalenae.
El análisis filogenético entre las especies P. reticulatus y P. magdalenae muestra una estrecha relación genética entre estas dos especies. Esta uniformidad genética sugiere que las diferencias encontradas entre P. reticulatus y P. magdalenae pueden considerarse no significativas. Sin embargo, se considera necesario realizar investigaciones en donde se comparen otros marcadores para seguir estudiando la relación entre P. reticulatus y P. magdalenae.
5 Conclusiones
Se caracterizó molecularmente P. reticulatus y P. magdalenae mediante RAPD presentando una estrecha relación entre estas dos especies, con un coeficiente de similitud de 0.64. Sus diferencias fenotípicas pueden resultar no de cambios genéticos, si no, probablemente, de la interacción genotipo y ambiente, que provocarían diferentes manifestaciones del fenotipo, ya que estas especies son grupos de poblaciones naturales con posibilidad de cruzamiento entre sí, pero conservando diferentes barreras en la reproducción que impiden el intercambio genético. 27
Se plantea la posibilidad de realizar un estudio más detallado de la relación entre las especies P. reticulatus y P. magdalenae en donde se puedan utilizar nuevos marcadores moleculares como secuenciación y microsatelites que permitan medir la variación genética y la filogenia entre estas dos poblaciones de P. reticulatus y P. magdalenae, que permitirían aportar una información más detallada.














