Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Facultad de Odontología Universidad de Antioquia
versão impressa ISSN 0121-246X
Rev Fac Odontol Univ Antioq vol.27 no.2 Medellín jan./jul. 2016
https://doi.org/10.17533/udea.rfo.v27n2a10
Articles
REVISIÓN DEL ESTADO ACTUAL DE CEMENTOS DE SILICATO DE CALCIO EN ODONTOLOGÍA RESTAURADORA2
1 DMD, MClinDent, PhD (c) UNESP, Instructor, Department of Restorative Dentistry, School of Dentistry, Universidad de Chile, Chile. Email: camila.corral@u.uchile.cl
2 DMD, PhD, Associate Professor, Department of Restorative Dentistry, School of Dentistry, Universidad de Chile, Chile
3 DMD, PhD, Assistant Professor, Department of Restorative Dentistry, School of Dentistry, Universidad de Chile, Chile
4 DMD, PhD (c) UNESP, Assistant, Department of Restorative Dentistry, School of Dentistry, Universidad de Chile, Chile
5 DMD, MSc, Assistant Professor, Department of Restorative Dentistry, School of Dentistry, Universidad de Chile, Chile
6 DMD, PhD, Adjunct Professor, School of Dentistry, UNESP, Brazil
Los cementos de silicato de calcio se han aplicado como materiales dentales desde hace más de veinte años; sin embargo, su uso en el área de la odontología restauradora es más reciente. Mejores propiedades mecánicas y menores tiempos de endurecimiento le permiten ser indicados para una variedad de aplicaciones en las que este material se utiliza como sustituto dentinario, entre ellas el recubrimiento pulpar directo/indirecto y como base/liner cavitario. A su vez, también se podría utilizar como material para restaurar esmalte de manera temporal. El presente artículo busca revisar la evidencia científica disponible, enfocándola a sus aplicaciones en odontología restauradora. La información se obtuvo a partir de artículos originales de investigación científica y revisiones de literatura, publicados en revistas disponibles en bases de datos como Medline/Pubmed y Scielo, junto a la información técnica otorgada por los fabricantes de estos cementos. El presente trabajo describe la composición, el modo de empleo, la reacción de fraguado y la evidencia científica sobre las aplicaciones de los cementos de silicato de calcio en odontología restauradora.
Palabras clave: cementos de silicato; cementos dentales; materiales dentales; recubrimiento de la pulpa dental
Calcium silicate cements have been used as dental materials for more than twenty years; however, their use in restorative dentistry is more recent. Better mechanical properties and shorter curing times make them suitable for a variety of applications in which they are used as a substitute of dentin, including direct/indirect pulp capping and as cavity base/liner. These materials may also be used to restore enamel temporarily. This article seeks to review the available scientific evidence with a focus on their applications in restorative dentistry. The information was gathered by reviewing original scientific research articles and literature reviews published in journals available in databases such as Medline/Pubmed and Scielo, along with technical information provided by the manufacturers of these cements. This article describes the composition, instructions for use, and curing reaction of calcium silicate cements, as well as the scientific evidence on their applications in restorative dentistry.
Key words: silicate cements; dental cements; dental materials; dental pulp capping
INTRODUCCIÓN
Lentamente, los cementos de silicato de calcio han empezado a abrirse un espacio dentro de la variedad de materiales usados en odontología restauradora. Si bien es cierto que su uso en endodoncia ya es de larga data, su introducción en procedimientos propios de odontología restauradora ha sido más reciente. El Mineral Trioxide Aggregate (MTA) fue el primero de este tipo de materiales en ser desarrollado (patentado en 1995). En respuesta a las favorables propiedades de biocompatibilidad y bioactividad de este primer material, numerosos fabricantes elaboraron productos similares al MTA, como MTA Angelus (Angelus Solucões Odontológicas, Brazil) y Endo CPM Sealer (Egeo, Argentina).1) En general, estos materiales apuntan a su uso en tratamientos endodónticos; sin embargo, también incluyen aplicaciones propias de la odontología restauradora, entre ellas la posibilidad de realizar recubrimiento pulpar directo.1)(2
Posteriormente, en 2011, apareció en el mercado BiodentineTM(Septodont, Saint Maur des Fosses, France), el cual se indica para ser usado como remplazo de dentina tanto coronal como radicular.3) El rápido fraguado de este cemento, en comparación con los silicatos de calcio previos, y la mejora de las propiedades mecánicas, le permiten ser indicado como material de restauración definitiva en remplazo de dentina y como cemento temporal para restituir esmalte.3) Otros materiales, como el TheraCal LC (Bisco Inc, Schamburg, IL, USA), han sido desarrollados más recientemente, proponiendo el uso de silicatos de calcio mezclados con resinas compuestas, dado que, al ser fotopolimerizables, logran controlar el tiempo de endurecimiento.
Una de las grandes ventajas de los silicatos de calcio es la llamada propiedad de bioactividad. Los materiales bioactivos se han definido como aquellos que "provocan una respuesta biológica en la interface de los tejidos con el material, resultando en la formación de una unión entre el material y el tejido".4)(5) Esto se ha visto reflejado en las respuestas favorables observadas cuando el material está en contacto con tejidos blandos como el tejido pulpar y el periodontal, o con tejidos duros como la dentina.6)(7)(8
Los resultados de las investigaciones muestran que estos cementos son capaces de generar una unión íntima con la dentina a través de una zona de infiltración mineral, con formación de tags minerales y difusión de calcio y silicio a la dentina.9)(10) Además, en contacto con tejido pulpar, el material es capaz de estimular la formación de puente dentinario.11) Es por eso que el estudio de estos materiales es de especial interés para la odontología restauradora, por su potencial uso como material restaurador en caso de cavidades dentinarias profundas, y en terapias de recubrimiento pulpar directo e indirecto.
Debido a que los cementos de silicato de calcio han ampliado su rango de indicaciones, incluyendo algunas propias de la odontología restauradora, además de la aparición de nuevos materiales a base de silicato de calcio con importantes variaciones en sus composiciones, se hace necesario revisar la evidencia científica disponible que evalúa su uso en estas aplicaciones, ya que actualmente no existen revisiones que se enfoquen en esta temática en particular. Por ello este artículo de revisión de tema tiene por objetivo revisar la información disponible sobre los cementos de silicato de calcio, enfocándolo a sus posibles aplicaciones en odontología restauradora. De esta manera, se busca actualizar al odontólogo en su conocimiento sobre los cementos de silicato de calcio, ayudándolo a una toma de decisiones clínica más informada.
Se realizó una revisión del tema en la literatura, a través de una búsqueda en las bases de datos Medline/Pubmed y Scielo, ingresando las palabras clave calcium silicate cement, tricalcium silicate cement, Mineral Trioxide Aggregate, BiodentineTM, TheraCal LC y bioactive cements . Junto con ello, se recopiló la información técnica otorgada por los fabricantes de estos cementos. Para el análisis de la información recopilada, se revisaron los resúmenes de los artículos disponibles y se incluyeron aquellos que se consideraron relevantes para el tema a tratar.
MINERAL TRIOXIDE AGGREGATE
El MTA, o Mineral Trioxide Aggregate, es el primer silicato de calcio desarrollado para uso en odontología, el cual fue desarrollado y patentado en 1995 por Torabinejad y White.12) Su principal componente es cemento de Portland tipo I (silicato de calcio), conocido como cemento de Portland ordinario, usado en construcción, al que se le ha agregado óxido de bismuto (Bi2O3) para proveer radiopacidad.12
Composición y modo de empleo
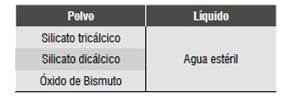
La fórmula original del MTA fue desarrollada en la Universidad de Loma Linda, Estados Unidos, y es fabricada por Dentsply International (ProRoot MTA and Tooth-Colored MTA; Dentsply-Tulsa Dental, Tulsa-USA; Dentsply-Johnson City-USA). Sin embargo, han aparecido una serie de productos similares fabricados por otras compañías.1) Diversos estudios han permitido conocer en más detalle los componentes de los principales tipos de MTA, ProRoot MTA (Grey MTA o GMTA) y Tooth-Colored MTA (White MTA o WMTA).13) Los principales componentes del GMTA están descritos en la Tabla 1, mientras que los componentes de la versión blanca, WMTA, son silicato tricálcico y óxido de bismuto.13) Los estudios que comparan su composición han concluido que la diferencia de color entre estos se debe a la falta de compuestos de hierro en la fórmula de WMTA. También se ha observado un menor tamaño de partículas en WMTA al compararlo con GMTA, lo que se ha propuesto que puede estar relacionado con las mejores propiedades de manipulación que presenta WMTA.13)(14)(15
Estos cementos se preparan mezclando el polvo de MTA con agua estéril en una proporción de polvo y líquido de 3:1.16) Se utiliza una espátula plástica o metálica para mezclar el cemento en una loseta, y esta mezcla se puede aplicar con un instrumento tipo porta amalgama plástico o metálico para llevar el material al sitio de aplicación.16
Reacción de fraguado
La mezcla del polvo con el agua estéril lleva a la formación de un gel coloidal, el cual solidifica.1) Durante la mezcla, se produce una reacción de hidratación de sus componentes, lo que lleva a la formación de un gel de silicato de calcio hidratado (C-S-H) e hidróxido de calcio como subproducto.17) Una vez iniciada la mezcla, el valor de pH aumenta bruscamente, alcanzando pH 12 luego de 20 m, que permanece por tres horas.18)(19) Camilleri ha estudiado los cambios químicos que ocurren cuando se hidrata el cemento. Se ha observado que una alta proporción de iones de calcio es liberada rápidamente, debido a la disolución del hidróxido de calcio y a una progresiva descalcificación de C-S-H. Esto ocurre con mayor rapidez que la liberación de sílice y bismuto. Se piensa que los altos niveles de calcio liberados se relacionan con la biocompatibilidad de este material, debido a que la elución de hidróxido de calcio induce la proliferación celularin vitro.17
El tiempo de endurecimiento de la versión original de MTA, GMTA, es de 165 (+/−5) m;18) mientras que WMTA demora 70 (+/−8,5) m, con un tiempo de trabajo de 5 (+/−0,79) m.20) Este largo tiempo de endurecimiento es una de las principales desventajas de este tipo de materiales, y es una de las razones por las que este material no puede ser usado en procedimientos en una sola sesión.2) Por lo general, los clínicos deben confirmar el endurecimiento del material en una segunda sesión y continuar con la siguiente etapa.
Aplicaciones en odontología restauradora
Dentro de las numerosas aplicaciones relativas a la endodoncia, también se ha propuesto el uso de MTA en tratamientos de recubrimiento pulpar directo.2) La técnica para realizar esta terapia en dientes vitales ha sido descrita en detalle por Whiterspoon.21
Recubrimiento directo
Se han publicado diversos artículos de revisión bibliográfica sobre las aplicaciones clínicas del MTA.2)(21)(22)(23)(24) En 2010, la revisión realizada por Parirokh y Torabinejad señala que el MTA es un material prometedor para preservar la vitalidad pulpar cuando se utiliza como material en recubrimientos pulpares directos.2) Los autores indican que este parece ser el material de elección para terapias de recubrimiento directo, comparado con otros materiales disponibles actualmente para el tratamiento de dientes permanentes.2) En el 2011, Aguilar y Linsuwanont publicaron una revisión sistemática sobre terapia pulpar en dientes permanentes con exposiciones pulpares por caries tratadas con MTA e hidróxido de calcio.22) e encontró que ambos materiales pueden generar resultados satisfactorios en terapias pulpares, como recubrimiento directo y pulpotomía parcial y total. Las tasas de éxito a los 3 años fueron altas: de 72,9% para recubrimiento pulpar directo (en pacientes de 6 a 10 años), 99,4% para pulpotomía parcial (en pacientes de 6 a 27 años) y 99,3% para pulpotomía total (en pacientes de 6 a 70 años).22) Sin embargo, los autores también declaran que la evidencia disponible en ese momento proveía información inconclusa y enfatizan en la necesidad de llevar a cabo más estudios de alta calidad.22
Después de esas revisiones, se han publicado cuatro estudios clínicos en los que se compara el MTA con el hidróxido de calcio (material usado convencionalmente en terapias pulpares vitales de dientes permanentes), los cuales, en su mayoría, han encontrado mejores resultados para el MTA.25)(26)(27)(28) Mente y colaboradores evaluaron 149 pacientes (con un promedio de seguimiento de 27 meses) en los que se realizaron tratamientos de recubrimiento directo posterior a exposición pulpar, con hidróxido de calcio y MTA.27) Obtuvieron una mayor tasa de éxito con MTA (78%) al compararlo con hidróxido de calcio (60%), concluyendo que el MTA parece ser más efectivo en mantener la vitalidad pulpar después de un recubrimiento directo.27) Similares resultados obtuvieron Hilton y colaboradores en su estudio clínico randomizado, en el cual encontraron una menor probabilidad de fracaso en dientes tratados con MTA (19,7%), al compararlo con hidróxido de calcio (31,5%).25) En este estudio se incluyó una muestra extensa de 376 pacientes, que fueron controlados por hasta 2 años.25) Por otro lado, Chailertvanitkul y colaboradores no encontraron diferencias en la tasa de éxito al realizar recubrimientos directos luego de exposiciones pulpares con MTA e hidróxido de calcio, pero sí encontraron una tendencia a una mayor probabilidad de fracaso en exposiciones pulpares mayores a 5 mm2, con un seguimiento de 2 años.26) Leye Benoist y colaboradores no encontraron diferencias significativas en las tasas de sobrevida con MTA e hidróxido de calcio a los 6 meses, pero sí a los 3 meses, con resultados más favorables para MTA.28) Además, se ha publicado un estudio clínico que evalúa la conservación de la vitalidad de los dientes tratados con MTA en recubrimientos directos.29) La tasa de éxito (conservación de la vitalidad) después de 3,6 (+/−1,1) años fue de 91,3%.29
De esta manera, ha ido creciendo lentamente la evidencia científica del uso de MTA en terapias pulpares de recubrimiento directo. Sin embargo, a pesar de los resultados favorables con MTA, todavía la cantidad de estudios clínicos de alta calidad son reducidos en este tópico, con seguimientos a corto y mediano plazo.
BIODENTINE TM
BiodentineTMes un cemento a base de silicato de calcio, el cual ha sido publicitado como "el primer material todo-en-uno para ser usado toda vez que la dentina ha sido dañada".30) Este material ha sido desarrollado en un esfuerzo por crear un silicato de calcio con mejores propiedades mecánicas31) y un menor tiempo de endurecimiento.32
Composición y modo de empleo
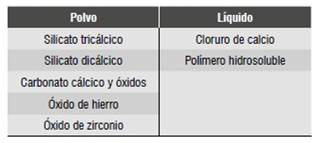
La presentación de BiodentineTMes en forma de una cápsula que contiene el polvo y un líquido contenido en una ampolla. De acuerdo con las instrucciones de mezclado, el contenido de la ampolla debe ser exprimido en la cápsula, luego de lo cual se mezcla en un amalgamador por 30 s. El contenido de la cápsula es, dependiendo de la preferencia, aplicado con un porta amalgama, una espátula o un dispositivo como la Root Canal Messing Gun.33) La Tabla 2 muestra los componentes declarados por el fabricante.32
De acuerdo con el fabricante, la tecnología Active Biosilicate Technology™, usada para producir BiodentineTM, permite asegurar la pureza del silicato de calcio, en contraste a lo ocurrido con otros cementos de silicato de calcio basados en cemento de Portland que contienen intrínsecamente mezclas no purificadas con bajas concentraciones de impurezas metálicas.32) Sin embargo, estudios recientes han encontrado trazas de arsénico, plomo y cromo en BiodentineTM.34) Más aún, los niveles de arsénico encontrado son mayores a los permitidos por ISO 9917. Sin embargo, los mismos componentes se han reportado para MTA, pero, ya que la liberación en solución fisiológica es despreciable, han sido considerados seguros.34
El fabricante ha propuesto que la disminución del tiempo de fraguado (12 m) de este material, comparado con silicatos de calcio tradicionales, como MTA (70 ±8,5 m),20) se debe al menor tamaño de las partículas del polvo, lo que permitiría una mayor área de reacción. Además, el cloruro de calcio adicionado al líquido ha probado ser un potente acelerador de la reacción en estos materiales.35)(36) El fabricante también declara que las mejores propiedades mecánicas se deben a la falta de impurezas, junto a la adición de carbonato de calcio al polvo y la densidad óptima del polvo obtenida en la mezcla.32) El polímero hidrosoluble probablemente cumple un rol importante en lograr una mejor densidad del polvo, dado que se puede obtener una mezcla de fácil manejo con una menor cantidad de agua.32) Finalmente, se presume que se adiciona óxido de zirconio para proveer radiopacidad, ya que se ha usado en otros materiales para este efecto.37) Esta es otra de las diferencias importantes con MTA, en el cual el radiopacificador es óxido de bismuto -un compuesto que, según algunos autores, tiene un efecto adverso en el material-.38
Reacción de fraguado
La reacción de fraguado es similar a la que ocurre en MTA, con producción de silicatos de calcio hidratados e hidróxido de calcio como subproducto,39) pero la velocidad de la reacción es mayor en BiodentineTM.40)(41
La reacción de fraguado inicial toma aproximadamente 12 m.41) Sin embargo, por espectroscopia de impedancia se ha podido observar que la reacción continúa ocurriendo por hasta 14 días.42) El estudio de Villat y colaboradores sugiere que la reacción completa de hidratación de este silicato es mucho más lenta que la observada en la reacción ácido-base de cementos de vidrio ionómero, por lo que concluyen que esta reacción podría continuar por meses, extendiendo el intercambio iónico, disminuyendo la porosidad y aumentando las propiedades mecánicas del material.42
Aplicaciones en odontología restauradora
El BiodentineTM está indicado para ser usado como sustituto de la dentina, tanto en la porción coronal como en la radicular.32) Las indicaciones aplicadas a la odontología restauradoras son:
Restauración temporal de esmalte
Restauración definitiva de dentina
Restauración de lesiones de caries profundas y/o extensas (técnica de sándwich)
Restauración de lesiones cervicales o radiculares profundas
Recubrimiento pulpar directo e indirecto
El fabricante indica que para aplicar el producto no hay necesidad de efectuar ningún tratamiento previo a la aplicación y que, una vez endurecido, el cemento se debe tratar como si fuese dentina sana. En el caso de realizar una restauración tipo sándwich con este material, se recomienda restaurar la cavidad completamente en una primera sesión, y después de una semana a seis meses se remueve la parte más externa para cubrir con resina compuesta.33
Recubrimiento pulpar directo
A la fecha solo se ha publicado un estudio clínico que evalúa BiodentineTMcomo material restaurador en recubrimientos pulpares directos. En el estudio de Nowicka y colaboradores se realizaron perforaciones pulpares en premolares con indicación de extracción por ortodoncia y se hicieron recubrimientos con BiodentineTM(n = 11) y MTA (n = 11). Luego de 6 semanas se observó que la mayoría de los premolares presentaba formación de puente dentinario completo, con ausencia de respuesta pulpar inflamatoria; no se encontraron diferencias significativas entre BiodentineTMy MTA durante el período de observación.11
Otros artículos han evaluado este material en modelos animales y en molares extraídos. El estudio del grupo de Tran y colaboradores fue realizado en ratas y demostró también la formación consistente de puente dentinario en recubrimientos pulpares hechos con BiodentineTMy con MTA.43
En estos casos, el puente formado está localizado en la zona de la injuria, con organización de tipo ortodentina, en contraste con lo observado en las reparaciones realizadas con hidróxido de calcio, las cuales presentaron inclusiones celulares que evocaban osteodentina.43
En el estudio desarrollado por Laurent y colaboradores se utilizaron premolares sanos recién extraídos, que fueron mantenidos en medio de cultivo y a los cuales se les aplicaron procedimientos de recubrimiento directo con BiodentineTM.8) En todos los premolares evaluados (n = 15) se observó la formación de focos de mineralización, que aumentaron de tamaño hasta el día 28, en que se hizo la última observación. También se observó expresión de marcadores de mineralización, lo que sugiere que el material es capaz de inducir la diferenciación a células tipo odontoblastos, involucradas en la formación de tejido dentinario.8
Sin embargo, el nivel de evidencia en los estudios en animales o en modelos exvivo es de menor magnitud que el derivado de ensayos clínicos. Por lo tanto, actualmente existe la necesidad de conducir otros ensayos clínicos que otorguen mayor nivel de evidencia sobre el uso de este material en terapias de recubrimiento pulpar directo.
Recubrimiento pulpar indirecto
Recientemente, un estudio clínico randomizado evaluó el uso de BiodentineTMen procedimientos de recubrimiento pulpar indirecto. En el estudio se evaluaron 72 restauraciones (36 realizadas con BiodentineTMy 36 con vidrio ionómero), con seguimiento de hasta un año, y no se encontraron diferencias entre los materiales al medir la eficacia clínica de conservación de vitalidad pulpar.44) Sin embargo, se observó que la mayoría de los dientes con radiolucidez apical (que no fue detectada en un comienzo con radiografía periapical, pero sí posteriormente con tomografía computarizada) que disminuyeron en tamaño o se eliminaron fueron tratados con BiodentineTM,44) mientras que la mayoría de las nuevas lesiones o su progresión se encontró en dientes tratados con vidrio ionómero. 44 Estos resultados fueron atribuidos a las características bioactivas de BiodentineTM, que se han reportado a partir de estudiosin vitro.6)(7)(8)(45
Restauración permanente de dentina y temporal de esmalte
A la fecha, solo se ha publicado un estudio clínico en el que BiodentineTMse ha usado como material restaurador (de esmalte y dentina).46) Este estudio clínico, multicéntrico, randomizado y con seguimiento de tres años, ha publicado solo los resultados obtenidos durante el primer año.46) Se llevaron a cabo restauraciones (n = 397) clase I y II con BiodentineTMy con resina compuesta.46) La evaluación inicial del producto muestra resultados muy satisfactorios al considerar la forma anatómica, la adaptación marginal y los contactos proximales; sin embargo, luego de seis meses las restauraciones de resina compuesta demostraron un mejor comportamiento clínicos en estos parámetros. Por esta razón, en este estudio se decidió recomendar que después de 6 meses es necesario remover la capa más externa de BiodentineTM, para restaurarla con resina compuesta, dejándolo sólo como material de remplazo permanente de dentina y temporal de esmalte.46
THERACAL LC
TheraCal LC es un cemento de silicato de calcio modificado con resina, desarrollado por Bisco Inc., para uso como barrera y protección del complejo pulpo-dentinario.47) Se presenta en una jeringa que contiene una pasta fotopolimerizable, compuesta de óxido de calcio, partículas de silicato de calcio, vidrio de estroncio, sílice, sulfato de bario, zirconato de bario y resina (BisGMA y PEGDMA). De acuerdo con el fabricante, se indica para uso en recubrimientos pulpares directos e indirectos aplicado como liner cavitario.47
Algunos estudios in vitro han investigado sus propiedades físicas y químicas.48)(49)(50 Camilleri ha observado que, de manera similar a BiodentineTM, TheraCal LC es capaz de permitir el depósito de fosfatos de calcio en su superficie cuando está en contacto con una solución fisiológica;50) sin embargo la liberación de iones de calcio al medio es significativamente menor que la de BiodentineTM.49)(50) Gandolfi ha demostrado que la solubilidad de TheraCal LC es menor que la de MTA y la de hidróxido de calcio; además, presenta una radiopacidad débil (menor a lo requerido según la norma ISO 6976) y es capaz de ser fotopolimerizado en grosores de 1,7 mm.48
Debido a su reciente disponibilidad, no existen estudios clínicos que evalúen su comportamiento, y a la fecha solo se ha publicado un estudio en animales. Cannon y colaboradores llevaron a cabo un estudio en primates, realizando recubrimientos pulpares directos con Thera- Cal LC. Los autores observaron que los dientes tratados con este material presentaban de manera más frecuente formación de puente dentinario, en comparación con el hidróxido de calcio y el vidrio ionómero.51
DISCUSIÓN
Desde hace bastante tiempo, los silicatos de calcio hacen parte de la variedad de materiales dentales disponibles; sin embargo, su uso en odontología restauradora estaba más bien limitado a algunas aplicaciones. El Mineral Trioxide Aggregate (MTA), debido a sus excelentes propiedades de biocompatibilidad y bioactividad, pero con bajas propiedades mecánicas, se indica para procedimientos de recubrimiento directo.1)(2) La evidencia científica disponible, al compararlo con materiales alternativos para estas terapias, muestra resultados muy favorables en su uso en estas indicaciones. Estudios clínicos randomizados y revisiones sistemáticas concuerdan en que el material es capaz de mantener el diente vital, con formación consistente de puente dentinario.2)(22)(26)(27) Las tasas de éxito de las terapias con este material son comparables (y en algunos estudios incluso superiores) a los materiales alternativos convencionales, como el hidróxido de calcio (fraguable utilizado en los estudios de Hilton y colaboradores, Chailertvanitkul y colaboradores, y Leye Benoist y colaboradores; y con pasta de hidróxido de calcio no fraguable en el estudio de Mente y colaboradores).25)(26)(27)(28) Sin embargo, existe la necesidad de llevar a cabo una mayor cantidad de estudios clínicos a largo plazo, que aporten mayor evidencia.
El desarrollo de BiodentineTMamplió las indicaciones de los silicatos de calcio en odontología restauradora. La composición de este material es similar a la de MTA, pero presenta importantes variaciones, que determinan cambios en sus propiedades físicas.32) Las aclamadas mejores propiedades mecánicas y el reducido tiempo de fraguado de BiodentineTMle permiten ser usado en una amplia gama de indicaciones. Se sugiere su uso como material de remplazo dentinario en cavidades clase I, II y V, y como remplazo de esmalte de manera temporal (hasta 6 meses). Estas aplicaciones de BiodentineTMson completamente nuevas entre los silicatos de calcio, por lo que su evaluación es necesaria.
Los resultados de los estudios clínicos realizados son promisorios. BiodentineTM, además de ser un material de fraguado más rápido (en comparación con otros silicatos de calcio), es de fácil manipulación, con presentación en cápsulas, por lo que es posible aplicarlo en el diente de manera limpia y precisa. Este material podría significar una muy buena alternativa para el tratamiento de caries dentinaria profunda, incluyendo casos en los que ya se han generado procesos inflamatorios pulpares reversibles. BiodentineTM, por sus propiedades bioactivas, podría proveer un adecuado sellado pulpo-dentinario, favoreciendo una respuesta pulpar de reparación y cambiando las condiciones de los tejidos afectados por caries.
El cemento TheraCal, de más reciente incorporación al mercado, presenta la ventaja de ser fotopolimerizable.47) Los efectos de esta incorporación de resina a un cemento de silicato de calcio se han investigado en algunos estudiosin vitro;48)(49)(50) sin embargo, a la fecha no se han reportado resultados de estudios clínicos.
La evidencia científica sobre los cementos de silicato de calcio en general está más bien enfocada a materiales que han estado disponibles por más tiempo, como el MTA.11)(44)(46) Los nuevos tipos de cementos de silicato de calcio, debido a su más reciente aparición, no cuentan con un gran número de estudios clínicos.11)(44) Esto impide tener información más consistente para determinar su eficacia clínica. Este nivel de evidencia es sin duda necesario para que emitir juicios sobre estos materiales; por ello es evidente la necesidad de conducir evaluaciones mediante ensayos clínicos aleatorizados, con el fin de otorgarle seguridad al clínico en la toma de decisiones.
CONCLUSIONES
Los silicatos de calcio son una alternativa de materiales dentales para ser usados en indicaciones de recubrimiento directo e indirecto, liner cavitario, remplazo dentinario en cavidades clase I, II y V, y como restauración semipermanente de esmalte.
Su uso en indicaciones de recubrimiento directo e indirecto está avalado por algunos estudios clínicos, especialmente en el caso de MTA para recubrimiento directo. Las nuevas aplicaciones propuestas para estos materiales, como el remplazo de dentina en cavidades clase I, II y V, poseen todavía insuficiente evidencia clínica; sin embargo, los estudios in vitro muestran resultados prometedores.
Las propiedades de biocompatibilidad y bioactividad sitúan a los silicatos de calcio como uno de los materiales restauradores que generan una respuesta más favorable por parte del tejido pulpar.
REFERENCES
1 Parirokh M, Torabinejad M. Mineral trioxide aggregate: a comprehensive literature review. Part I: chemical, physical, and antibacterial properties. J Endod 2010; 36(1): 16-27. [ Links ]
2. Parirokh M, Torabinejad M. Mineral trioxide aggregate: a comprehensive literature review. Part III: Clinical applications, drawbacks, and mechanism of action. J Endod 2010; 36(3): 400-413. [ Links ]
3. Watson TF, Atmeh AR, Sajini S, Cook RJ, Festy F. Present and future of glass-ionomers and calcium-silicate cements as bioactive materials in dentistry: biophotonics-based interfacial analyses in health and disease. Dent Mater 2014; 30(1): 50-61. [ Links ]
4. Hench LL. Bioactive ceramics. Ann N Y Acad Sci 1988; 523: 54-71. [ Links ]
5. Cao WP, Hench LL. Bioactive materials. Ceram Int 1996; 22(6): 493-507. [ Links ]
6. Laurent P, Camps J, De Meo M, Dejou J, About I. Induction of specific cell responses to a Ca(3)SiO(5)-based posterior restorative material. Dent Mater 2008; 24(11): 1486-1494. [ Links ]
7. Kim JR, Nosrat A, Fouad AF. Interfacial characteristics of Biodentine and MTA with dentine in simulated body fluid. J Dent 2015; 43(2): 241-247. [ Links ]
8. Laurent P, Camps J, About I. Biodentine(TM)induces TGF-Β1 release from human pulp cells and early dental pulp mineralization. Int Endod J 2012; 45(5): 439-448. [ Links ]
9. Han L, Okiji T. Bioactivity evaluation of three calcium silicate-based endodontic materials. Int Endod J 2013; 46(9): 808-814. [ Links ]
10. Han L, Okiji T. Uptake of calcium and silicon released from calcium silicate-based endodontic materials into root canal dentine. Int Endod J 2011; 44(12): 1081-1087. [ Links ]
11. Nowicka A, Lipski M, Parafiniuk M, Sporniak-Tutak K, Lichota D, Kosierkiewicz A et al. Response of human dental pulp capped with biodentine and mineral trioxide aggregate. J Endod 2013; 39(6): 743-747. [ Links ]
12. Torabinejad M, White DJ, inventores; Loma Linda University, cecionario. Tooth filling material and method of use. Estados Unidos de Norteamérica US 5415547 A. 1995 May 16. [ Links ]
13. Camilleri J, Montesin FE, Brady K, Sweeney R, Curtis RV, Ford TR. The constitution of mineral trioxide aggregate. Dent Mater 2005; 21(4): 297-303. [ Links ]
14. Camilleri J, Montesin FE, Di Silvio L, Pitt Ford TR. The chemical constitution and biocompatibility of accelerated Portland cement for endodontic use. Int Endod J 2005; 38(11): 834-842. [ Links ]
15. Asgary S, Eghbal MJ, Parirokh M, Ghoddusi J, Kheirieh S, Brink F. Comparison of mineral trioxide aggregate′s composition with Portland cements and a new endodontic cement. J Endod 2009; 35(2): 243-250. [ Links ]
16. Torabinejad M, Chivian N. Clinical applications of mineral trioxide aggregate. J Endod 1999; 25(3): 197-205. [ Links ]
17. Camilleri J. Characterization of hydration products of mineral trioxide aggregate. Int Endod J 2008; 41(5): 408-417. [ Links ]
18. Torabinejad M, Hong CU, McDonald F, Pitt Ford TR. Physical and chemical properties of a new root-end filling material. J Endod 1995; 21(7): 349-353. [ Links ]
19. Oliveira IR, Pandolfelli VC, Jacobovitz M. Chemical, physical and mechanical properties of a novel calcium aluminate endodontic cement. Int Endod J 2010; 43(12): 1069-1076. [ Links ]
20. Asgary S, Shahabi S, Jafarzadeh T, Amini S, Kheirieh S. The properties of a new endodontic material. J Endod 2008; 34(8): 990-993. [ Links ]
21. Witherspoon DE. Vital pulp therapy with new materials: new directions and treatment perspectives--permanent teeth. Pediatr Dent 2008; 30(3): 220-224. [ Links ]
22. Aguilar P, Linsuwanont P. Vital pulp therapy in vital permanent teeth with cariously exposed pulp: a systematic review. J Endod 2011; 37(5): 581-587. [ Links ]
23. Bogen G, Kuttler S. Mineral trioxide aggregate obturation: a review and case series. J Endod 2009; 35(6): 777-790. [ Links ]
24. Naito T. Uncertainty remains regarding long-term success of mineral trioxide aggregate for direct pulp capping. J Evid Based Dent Pract 2010; 10(4): 250-251. [ Links ]
25. Hilton TJ, Ferracane JL, Mancl L. Comparison of CaOH with MTA for direct pulp capping: a PBRN randomized clinical trial. J Dent Res 2013; 92(7 Suppl): 16S-22S. [ Links ]
26. Chailertvanitkul P, Paphangkorakit J, Sooksantisakoonchai N, Pumas N, Pairojamornyoot W, Leela-Apiradee N et al. Randomized control trial comparing calcium hydroxide and mineral trioxide aggregate for partial pulpotomies in cariously exposed pulps of permanent molars. Int Endod J 2014; 47(9): 835-842. [ Links ]
27. Mente J, Geletneky B, Ohle M, Koch MJ, Friedrich-Ding PG, Wolff D et al. Mineral trioxide aggregate or calcium hydroxide direct pulp capping: an analysis of the clinical treatment outcome. J Endod 2010; 36(5): 806-813. [ Links ]
28. Leye Benoist F, Gaye Ndiaye F, Kane AW, Benoist HM, Farge P. Evaluation of mineral trioxide aggregate (MTA) versus calcium hydroxide cement (Dycal(®)) in the formation of a dentine bridge: a randomised controlled trial. Int Dent J 2012; 62(1): 33-39. [ Links ]
29. Marques MS, Wesselink PR, Shemesh H. Outcome of direct pulp capping with Mineral Trioxide Aggregate: a prospective study. J Endod 2015; 41(7): 1026-1031. [ Links ]
30. Septodont. BiodentineTMBrochure [internet]. [Consultado 2014 Nov 3] Disponible en:Disponible en:http://www.septodontusa. com/products/biodentine . [ Links ]
31. Grech L, Mallia B, Camilleri J. Investigation of the physical properties of tricalcium silicate cement-based root-end filling materials. Dent Mater 2013; 29(2): e20-28. [ Links ]
32. Septodont. BiodentineTMActive Biosilicate TechnologyTM[internet]. [Consultado 2014 Mar 2]. Disponible en: http:// Disponible en: http:// www.septodontusa.com/sites/default/files/Biodentine.pdf . [ Links ]
33. Septodont. Biodentine, Active Biosilicate Technology. Package insert. [ Links ]
34. Camilleri J, Kralj P, Veber M, Sinagra E. Characterization and analyses of acid-extractable and leached trace elements in dental cements. Int Endod J 2012; 45(8): 737-743. [ Links ]
35. Kogan P, He J, Glickman GN, Watanabe I. The effects of various additives on setting properties of MTA. J Endod 2006; 32(6): 569-572. [ Links ]
36. Wiltbank KB, Schwartz SA, Schindler WG. Effect of selected accelerants on the physical properties of mineral trioxide aggregate and Portland cement. J Endod 2007; 33(10): 1235-1238. [ Links ]
37. Tanomaru-Filho M, Jorge EG, Guerreiro-Tanomaru JM, Goncalves M. Radiopacity evaluation of new root canal filling materials by digitalization of images. J Endod 2007; 33(3): 249-251. [ Links ]
38. Camilleri J, Montesin FE, Papaioannou S, McDonald F, Pitt-Ford TR. Biocompatibility of two commercial forms of mineral trioxide aggregate. Int Endod J 2004; 37(10): 699-704. [ Links ]
39. Grech L, Mallia B, Camilleri J. Characterization of set Intermediate Restorative Material, Biodentine, Bioaggregate and a prototype calcium silicate cement for use as root-end filling materials. Int Endod J 2013; 46(7): 632-641. [ Links ]
40. Camilleri J. Investigation of Biodentine as dentine replacement material. J Dent 2013; 41(7): 600-610. [ Links ]
41. Gandolfi MG, Siboni F, Polimeni A, Bossù M, Riccitiello F, Rengo S et al. In Vitro screening of the apatite-forming ability, biointeractivity and physical properties of a Tricalcium Silicate Material for endodontics and restorative dentistry. Dent J 2013; 1(4): 41-60. [ Links ]
42. Villat C, Tran XV, Pradelle-Plasse N, Ponthiaux P, Wenger F, Grosgogeat B et al. Impedance methodology: A new way to characterize the setting reaction of dental cements. Dent Mater 2010; 26(12): 1127-1132. [ Links ]
43. Tran XV, Gorin C, Willig C, Baroukh B, Pellat B, Decup F et al. Effect of a calcium-silicate-based restorative cement on pulp repair. J Dent Res 2012; 91(12): 1166-1171. [ Links ]
44. Hashem D, Mannocci F, Patel S, Manoharan A, Brown JE, Watson TF et al. Clinical and radiographic assessment of the efficacy of calcium silicate indirect pulp capping: a randomized controlled clinical trial. J Dent Res 2015; 94(4): 562-568. [ Links ]
45. Hashem DF, Foxton R, Manoharan A, Watson TF, Banerjee A. The physical characteristics of resin composite-calcium silicate interface as part of a layered/laminate adhesive restoration. Dent Mater 2014; 30(3): 343-349. [ Links ]
46. Koubi G, Colon P, Franquin JC, Hartmann A, Richard G, Faure MO et al. Clinical evaluation of the performance and safety of a new dentine substitute, Biodentine, in the restoration of posterior teeth: a prospective study. Clin Oral Investig 2013; 17(1): 243-249. [ Links ]
47. BISCO. Seal and Protect with TheraCal LC Pulp Capping Material and Liner [internet]. [Consultado 2014 17]. Disponible en: Disponible en: http://www.bisco.com/catalog/TheracalLC.pdf . [ Links ]
48. Gandolfi MG, Siboni F, Prati C. Chemical-physical properties of TheraCal, a novel light-curable MTA-like material for pulp capping. Int Endod J 2012; 45(6): 571-579. [ Links ]
49. Camilleri J, Laurent P, About I. Hydration of Biodentine, Theracal LC, and a prototype tricalcium silicate-based dentin replacement material after pulp capping in entire tooth cultures. J Endod 2014; 40(11): 1846-1154. [ Links ]
50. Camilleri J. Hydration characteristics of Biodentine and Theracal used as pulp capping materials. Dent Mater 2014; 30(7): 709-715. [ Links ]
51. Cannon M, Gerodias N, Viera A, Percinoto C, Jurado R. Primate pulpal healing after exposure and TheraCal application. J Clin Pediatr Dent 2014; 38(4): 333-337 [ Links ]
Recibido: 14 de Agosto de 2014; Aprobado: 13 de Octubre de 2015











 texto em
texto em