Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad de Odontología Universidad de Antioquia
Print version ISSN 0121-246X
Rev Fac Odontol Univ Antioq vol.29 no.1 Medellín July/Dec. 2017
https://doi.org/10.17533/udea.rfo.v29n1a10
Articles
USO DE DENTÍFRICOS FLUORADOS EN NIÑOS: BASES CONCEPTUALES EN UN CONTEXTO CONFUSO. REVISIÓN DE TEMA
1 DMD. Master in Medical Microbiology. Professor, School of Dentistry, Universidad de Antioquia, Medellín, Colombia.
2 Pharmaceutical Chemist. PhD in Pharmacology. Professor, Universidad CES and Universidad de Antioquia, Medellín, Colombia.
3 DMD, Universidad de Antioquia, Medellín, Colombia.
Las cremas dentales fluoradas han sido recomendadas ampliamente como parte de la prevención de la caries dental. Resultados controversiales sugieren que su uso inadecuado puede contribuir de manera importante a la ingesta total de fluoruros en niños menores de 3 años, siendo ésta una de las razones por las que han sido relacionadas con el desarrollo de fluorosis dental. La relación costo-beneficio del uso de los dentífricos fluorados en los niños ha generado controversia y ha permitido la evolución de conceptos que cimientan las recomendaciones de uso. En esta revisión de tema se presentan algunos aspectos que determinan el potencial preventivo de las cremas dentales fluoradas, las recomendaciones académicas sobre su uso, distintas normativas gubernamentales de países de América Latina en torno al tema, y una breve descripción de la disponibilidad de productos en el mercado colombiano. Se pretende contribuir así a una mayor comprensión del tema y por tanto a una mejor orientación individual de los pacientes.
Palabras clave: dentífricos; flúor; niño; formas de dosificación; pastas de dientes
Fluoride toothpastes have long been recommended as part of the measures to prevent dental caries. Controversial findings suggest that an inappropriate use of this type of dentifrices can significantly contribute to the total intake of fluoride by children younger than 3 years, being one of the reasons why they have been linked to the development of dental fluorosis. The cost-benefit relationship of using fluoride dentifrices in children has been controversial and has allowed the evolution of concepts that reinforce the recommendations to use them. This topic review discusses some aspects that determine the preventive potential of fluoride toothpastes, the academic recommendations to use them, the various policies in Latin American countries on the issue, and a brief description of the availability of products in the Colombian market. This article seeks to contribute to a better understanding of this issue and therefore to a better orientation of patients.
Key words: dentifrices; fluoride; child; dosage; toothpaste
INTRODUCCIÓN
La utilización de fluoruros es una de las estrategias más comunes para la prevención de la caries dental, y su incorporación a los dentífricos ha permitido grandes alcances en cubrimiento poblacional, así como reducción de la caries dental, con cifras entre el 30 y 70% mayores a las logradas con opciones no fluoradas,(1,2,3,4,5,6) por lo que las mayores concentraciones de flúor se han relacionado con una mejor prevención de la caries.(7,8,9) Sin embargo, el uso de cremas dentales con alto contenido de flúor también está asociado con una mayor predisposición a desarrollar fluorosis dental en niños,(9,10,11,12) especialmente cuando se implementa durante la primera infancia (antes de los 6 años).(13,14,15,16) El flúor presente en las cremas dentales contribuye aproximadamente con el 57 al 81,5% de la ingesta total de flúor en niños con edades comprendidas entre 12 meses y 6 años.(17,18,19,20,21,22,23) Por otro lado, algunos autores han demostrado que en niños de 3 a 8 años la utilización de estos productos se relaciona con un aumento significativo de la concentración de flúor en la orina después del cepillado dental(24,25,26) y a la ingesta de agua fluorada en países como Brasil.(27)
A nivel mundial, se viene observando un aumento en la prevalencia de fluorosis dental, con porcentajes que van de 7,7 a 80,7% en áreas donde se cuenta con agua fluorada, y entre 2,9 a 42% en áreas sin agua fluorada.(28) En Latinoamérica se han realizado diversos estudios que reflejan la prevalencia de fluorosis dental en la región. En México, en el 2004, se reportó una prevalencia de 56% en escolares de 6 a 9 años (45% nivel leve).(29) En Venezuela, en el 2007, se encontró una prevalencia del 16,6% en niños de 8 a 12 años (8,5% nivel leve).(30) En Colombia, en 1998, se reportó una prevalencia de 11,5% (niveles leve y muy leve) en una población de 6, 7, 12 y 15 a 19 años.(31) En el IV Estudio Nacional de Salud Bucal (ENSAB-IV) realizado en el 2014, se informa de un 62,15% a los 12 años y 56,05% a los 15 años.(32)
El Índice Comunitario de Fluorosis de Dean (ICF) en las regiones Atlántica, Oriental, Central, Bogotá y Orinoquia-Amazonia fue de 0,90 a los 12 años, lo cual indica que esta población en su conjunto tiene riesgo leve, por encontrarse en el rango entre 0,6 y 1,0 del ICF de Dean, mientras que en la zona rural dispersa alcanza un valor de 1,05, pasando al nivel de riesgo moderado, lo cual se considera un signo de alarma para la toma de medidas en salud pública; esto ocurre también con la región Pacífica, que presenta un valor de 1,06, lo que pone de relieve la necesidad de analizar los efectos indeseados a largo plazo.(32)
En cuanto a la preocupación sobre el aumento en la prevalencia de la fluorosis dental, es necesario considerar las múltiples fuentes de flúor a las que puede estar expuesto un individuo: cremas dentales, sal de cocina, alimentos sólidos y líquidos de la dieta -especialmente el agua en aquellos países donde se adiciona flúor al agua potable-.(20,33,34,35,36,37,38,39,40,41,42) Autores como Levy et al sugieren que una de las fuentes asociadas a fluorosis dental en la primera infancia es el fluoruro ingerido en la crema dental fluorada utilizada durante el desarrollo de los dientes permanentes,(43) y Lockner et al atribuyen un aumento del riesgo a la aplicación de barnices fluorados simultáneamente con el uso de cremas fluoradas.(26)
Esta revisión de tema pretende aportar información sobre el tipo de flúor terapéutico utilizado en los dentífricos, el abrasivo que acompaña a este flúor, las recomendaciones académicas sobre uso y cantidad a emplear y las variaciones según las distintas normativas gubernamentales de países de América Latina. Se incluyó también una descripción de la disponibilidad de productos en el mercado de Medellín (Colombia), lo cual condiciona el uso y el seguimiento de las recomendaciones clínicas. Esta información puede ayudar a entender algunas particularidades que influyen en el efecto tóxico y el efecto anticaries de los dentífricos fluorados para que su integración permita orientar individualmente a los pacientes, ya que pareciera que las diferencias entre las fuentes de información dejan un vacío que dificulta la selección y el uso de las cremas dentales en niños. Finalmente, esta información se puede utilizar para ayudar a los padres o cuidadores a hacer un uso adecuado, consciente, orientado, controlado y supervisado de las cremas dentales fluoradas y para que los fabricantes de estos productos participen activamente en la educación que necesitan los consumidores.
MÉTODOS
Se realizó la búsqueda de material bibliográfico en las bases de datos Pubmed, LILACS y SciELO, desde el inicio de conformación de las bases de datos hasta las publicaciones realizadas al 30 de mayo de 2017, para garantizar exhaustividad. De acuerdo al algoritmo de cada base de datos, se utilizó una ecuación de búsqueda con los descriptores “pasta dental”, “flúor” y “niño” en inglés y español. La ecuación de búsqueda utilizada en la base de datos Pubmed fue: ((children[Title/Abstract]) AND toothpaste[Title/Abstract]) AND fluoride[Title/ Abstract].
Los registros obtenidos fueron exportados al programa Zotero, donde se aplicaron criterios de inclusión y criterios de exclusión, lo cual dio finalmente un total de 38 artículos para analizar (Figura 1).
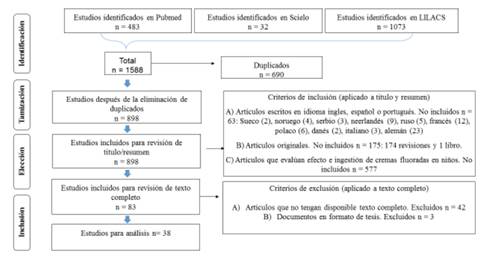
Figura 1 Metodología aplicada para la revisión de tema: bases de datos utilizadas, registros recuperados, criterios de inclusión y exclusión aplicados
Adicionalmente, se realizó la búsqueda de guías y normativas que rigen para el uso de flúor en cremas dentales en archivos gubernamentales y se encontró información relacionada de los ministerios nacionales de salud de Brasil, Colombia, Chile, Perú y Guatemala y de la Secretaría de Salud de México. Se obtuvo además documentación emitida por American Dental Association (ADA), American Academy of Pediatric Dentistry (AAPD), American Academy of Pediatrics (AAP), European Academy of Paediatric Dentistry (EAPD), American Dental Association Council on Scientific Affairs (JADA), World Dental Federation (FDI), la Comunidad Andina y Mercosur.
RESULTADOS
Influencia de los componentes del dentífrico en su capacidad preventiva
El efecto preventivo de los dentífricos depende de sus características químicas y por tanto de los componentes utilizados en su fabricación y de las interacciones entre los mismos.(44) Estos productos contienen una mezcla de sustancias que varían en concentración dependiendo de los objetivos que se pretenda alcanzar, entre ellas se encuentran los abrasivos, los cuales constituyen entre el 25 y el 60% de un dentífrico típico.(45) Los abrasivos son partículas insolubles que ayudan a la remoción mecánica de la placa bacteriana; algunos ejemplos son: fosfato dicálcico (CaHPO4), pirofosfato cálcico (Ca2P4O7), hidróxido de aluminio (Al(OH)3), carbonato de calcio (CaCO3), sílicas, zeolitas y la hidroxiapatita (Ca5(PO4)3OH).(45,46)
Por otro lado, los agentes terapéuticos o activos más empleados en la fabricación de cremas dentales son los fluoruros, dentro de los cuales el más utilizado es el fluoruro de sodio (NaF), seguido del monofluorofosfato (MFP). El fluoruro de sodio es un compuesto altamente ionizable, por lo que se vuelve activo tan pronto se introduce en la boca. En el MFP, el fluoruro se encuentra unido al fosfato en forma covalente y para que este flúor sea activo debe ser liberado por hidrólisis enzimática de la molécula de MFP durante el cepillado por acción de las fosfatasas, enzimas presentes de manera natural en la placa y la saliva; es decir, el fluoruro de sodio libera iones de flúor inmediatamente al entrar en contacto con el ambiente bucal, mientras que el MFP requiere de una acción enzimática previa.(47,48)
Se han presentado discusiones relacionadas con la efectividad de estos dos tipos de flúor en el control de caries dental. Algunos autores, como DePaola et al,(49) Volpe et al,(50) y Basch et al,(51) concluyeron que no existe superioridad de uno sobre otro y que su actividad en el control de la caries es equivalente; sin embargo, Churchley et al indican que hay diferencias significativas en la efectividad anticaries de las cremas dentales con NaF y MFP, y además la remineralización se relaciona con la cantidad de fluoruro presente en el esmalte.(48) Se debe tener en cuenta que la absorción del flúor está condicionada por diferentes excipientes contenidos en la crema dental,(44) debido a que los compuestos de los dentífricos pueden ser activos e inactivos y los ingredientes activos pueden ser inactivados, como en el caso del NaF, que se hace bastante ineficaz como agente anticaries cuando el carbonato de calcio (abrasivo) se une a él.(52)
Con respecto a la concentración de flúor en los dentífricos, y por disposición de la FDA (Food and Drug Administration) de Estados Unidos, estos productos deben tener por lo menos el 60% de su contenido de flúor total, como la suma del ion de flúor soluble y formas iónicas solubles, como flúor y fluorofosfato para el NaF y para el MFP, respectivamente. Entonces el contenido de flúor soluble total depende del calcio contenido en el abrasivo del dentífrico, el cual puede formar sales insolubles que no contribuyen a la remineralización.(53) Dado lo anterior, para el consumidor no es posible conocer la concentración de flúor activo presente en una crema dental, ya que las etiquetas indican la concentración total adicionada al producto.(53)
De acuerdo con la American Dental Association (ADA), una de las condiciones mínimas para que un dentífrico presente capacidad de controlar el proceso de caries es la de mantener flúor soluble y reactivo. La posición general es que los dentífricos deben presentar alrededor de 1000 ppm (concentración promedio), de allí que 14501500 ppm sean consideradas concentraciones altas, y 500 ppm, concentraciones bajas.(54)
La actividad del fluoruro en las formulaciones de los dentífricos debería ser evaluada en el tiempo, ya que parte del fluoruro del MFP es liberado durante el almacenamiento y reacciona con el calcio formando flúor insoluble. Algunas evaluaciones indican que la actividad anticaries de estos productos se mantiene por el tiempo en que van a ser usados por la población,(55,56,57) pero otros trabajos encuentran que en algunos casos el flúor total declarado en las etiquetas no corresponde a la concentración real medida por cromatografía de gases,(58) y en algunos casos esta es inferior a la concentración total de la formulación,(6,59,60) razón de más para pensar en la necesidad de programas de vigilancia y control. Los fabricantes deberían suministrar en las etiquetas la información sobre la concentración de flúor en su forma activa, de manera que garantice la biodisponibilidad dentro del rango de concentración sugerido por la FDA, lo cual permitiría un mejor acercamiento a su verdadero potencial preventivo.(53)
Cantidad y concentración de dentífrico a utilizar en los niños
El consumo diario total de flúor por parte de un individuo resulta de la combinación del flúor contenido en la dieta (sólidos y líquidos) con el flúor de la crema dental y otros suplementos. La cantidad de fluoruro ingerido a partir del dentífrico depende de la cantidad que se coloca en el cepillo y de la concentración de fluoruro en la pasta.(13,61,62) Para reducir el riesgo de desarrollar fluorosis dental, se considera que la dosis no debe exceder 0,07 mg F/kg de peso corporal/día.(63)
Paiva et al(64) realizaron en dos ciudades de Brasil (Ibiá y Piracicaba) un análisis del flúor total ingerido por niños de 19 a 38 meses de edad (período crítico para el desarrollo de fluorosis en incisivos permanentes). Ambas ciudades cuentan con adición de flúor en el agua (0,7 ppm), y en el estudio sólo se incluyeron niños que consumían el agua de suministro público regularmente. Los autores encontraron que la dieta de los niños hacía un aporte de flúor por debajo del límite superior seguro para el desarrollo de fluorosis, con variaciones según la ubicación de los niños, posiblemente por diferencias en los patrones de alimentación. Por el contrario, la cantidad de flúor ingerido procedente de dentífricos fue cercana al límite superior de la dosis aceptada como segura para el desarrollo de fluorosis dental, situación que los autores atribuyeron al uso de una gran cantidad de dentífrico y a una mayor frecuencia de cepillado de los niños brasileros en comparación con los de otras comunidades. Estos resultados son similares a los obtenidos por Lima et al, quienes determinaron que en una ciudad de Brasil con clima tropical (Teresina, Piauí), con acceso a agua fluorada, el 74% de los niños de 3 a 4 años de edad tenían una ingesta de menos de 0,07 mg F/kg de peso corporal/día, con contribuciones variables de la dieta y la pasta dentífrica, lo cual atribuye los mismos factores asociados y sugiere que la cantidad de fluoruro ingerida se considera segura en términos de riesgo de fluorosis dental.(65) Do Nascimento et al(66) estimaron la ingesta de fluoruro a partir de pastas dentales en niños de 2 a 6 años de edad en una ciudad de Brasil sin abastecimiento de agua fluorada (Campina Grande). Estos autores consideran que el uso de dentífricos está relacionado con el riesgo de fluorosis en los niños, debido principalmente al uso inapropiado de las pastas dentales.
En búsqueda de estrategias que den mayor seguridad al uso de dentífricos fluorados en la población infantil, la ADA(54) y la Asociación Americana de Pediatría (AAP)(67) recomendaron en el año 2014 -teniendo en cuenta que 1 pulgada (equivalente a 2.5 centímetros y a 1 gramo) de dentífrico de 1000 ppm contiene 1 mg de fluoruro- usar una pequeña cantidad de dentífrico (0,3 g/cepillada, “similar a una arveja”) en niños de 3 a 6 años, y para niños menores de 3 años una cantidad del tamaño de un “grano de arroz”, empezando tan pronto como salga el primer diente (Figura 2), siempre con supervisión y ayuda de un adulto, quien debe realizar la dosificación del producto, teniendo en cuenta las necesidades individuales, especialmente el riesgo de caries y fluorosis, y aclarando que el odontopediatra puede recomendar su uso en edades más tempranas cuando el riesgo de caries es alto.
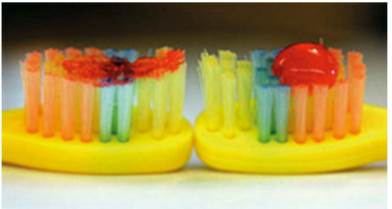
Figura 2 La foto muestra a la izquierda la cantidad de dentífrico recomendada para niños menores de 2 años (0.1 mg de fluoruro) y a la derecha la cantidad correspondiente a una “arveja”, recomendada para niños de 2 a 6 años (0.25 mg de fluoruro). Tomado de: American Dental Association Council on Scientific Affairs, 2014.
Por su parte, la EAPD (European Academy of Paediatric Dentistry) emitió en el año 2009 un documento guía en el que sugiere el uso de dentífricos de 500 ppm en niños de 6 meses a 2 años, de 1000 ppm para niños de 2 a 6 años y de 1450 ppm para niños de 6 años o más. Estas recomendaciones tienen en cuenta la importancia del acompañamiento de los padres en la dosificación y supervisión del cepillado, hasta que el niño aprenda a no deglutir el dentífrico, para evitar así el riesgo de ingesta; también muestra la relevancia de los procesos educativos dirigidos a los padres(68) y señala a los niños menores de 4 años (especialmente entre los 15 y 30 meses) como los de mayor riesgo de desarrollar fluorosis dental en incisivos permanentes y primeros molares.(69)
Los dentífricos con bajas concentraciones de fluoruros (entre 500 y 600 ppm) constituyen una de las formas más recomendadas en la literatura para reducir la ingesta total de fluoruros en los niños.(70,71) Paiva et al(64) argumentan que esta puede ser una medida parcial, considerando que algunos niños degluten cantidades considerables de dentífrico (por encima de 0,181 mg F/kg/día). Estos autores consideran que el 60% del consumo diario total de flúor se le puede adjudicar al dentífrico; entonces un niño expuesto a una dosis de 0,20 mg F/kg de peso corporal/ día de un dentífrico con 50% menos de fluoruro tendrá una exposición a una dosis dos veces mayor al límite superior seguro para el desarrollo de fluorosis (0,07); por lo tanto, se considera que el uso de dentífricos de baja concentración puede reducir el riesgo de fluorosis en la mayoría de la población,(61,63) y que se debe reducir la cantidad de crema dental fluorada (tamaño de un guisante) a los niños pequeños que están en riesgo de ingerir esta sustancia.(72) Se identifica que los dentífricos dirigidos a la población infantil son más costosos y por tanto no alcanzan a cubrir a niños de diferente estatus socioeconómico, lo cual es discriminatorio, ya que la mayoría de los niños seguirían utilizando el mismo dentífrico (menos costoso) que usen sus padres o cuidadores. Argumentan también que, aunque la publicidad puede hacer el producto atractivo para los niños, en realidad no hay un producto que sea especial para ellos.(64)
Las evaluaciones del efecto anticaries de las cremas dentales de baja concentración ante diferentes condiciones indican que, para el caso de niños con caries activa y de individuos con una alta exposición al azúcar (6 a 8 veces/día), o con altos índices de placa, estas cremas tienen menos efectividad que las pastas dentales con flúor convencional (1100 ppm F).(59,73,74,75,76)
Arana y Villa(77) evidencian la utilización generalizada de dentífricos entre familias con niños de 3 a 5 años de edad de los distritos de Pesqueda, Mampuesto y La Esperanza en la provincia de Trujillo, Perú, las cuales contenían NaF, MFP o ambos. La concentración de fluoruros en estos productos era de 1100, 1450 y 1500 ppm, pero los autores encontraron que existe una gran variación en la forma en que se describe la cantidad y la concentración de flúor incorporado en las etiquetas. En su mayoría, los niños se cepillaban los dientes más de dos veces al día con estos dentífricos, lo cual se asemeja a lo identificado en los estudios de Paiva et al(64) y Lima et al(65) en niños de Brasil. La evidencia indica que las pastas dentales con mayores concentraciones de fluoruro confieren mayor protección contra la caries dental, pero es claro que estas también incrementan el riesgo de fluorosis.(77,78,79) Estudios realizados en Colombia y México presentan hallazgos similares a los de Paiva et al,(64) en los cuales la ingesta de flúor a través de los dentífricos aporta hasta el 69% de la ingesta total de flúor y contribuye a ubicarla por encima del valor aceptado como seguro para prevenir la fluorosis.(80,81)
Arana y Villa(77) hacen un llamado a las autoridades sanitarias para que mejoren el control que se ejerce sobre estos productos y uniformicen el formato bajo el cual describen sus contenidos, de manera que se facilite la lectura y la comprensión de las etiquetas -medida necesaria para el consumidor final y para el odontólogo, quien necesita disponer de la mejor información posible para poder orientar y educar-.
El manejo de la cantidad de dentífrico para el control de la ingesta de fluoruros cobra sentido teniendo en cuenta la correlación entre la cantidad usada y la dosis.(64,82) Paiva et al(64) consideran que, si bajo las condiciones evaluadas en su estudio, un niño usa 0,3 g de dentífrico en cada cepillada, tal como lo recomiendan la ADA,(54) la AAPD (American Academy of Pediatric Dentistry)(83) y la AAP,(67) esto puede ser suficiente para reducir la ingesta de fluoruro procedente del dentífrico e incluir con la medida a los niños que acostumbran deglutir grandes cantidades de dentífrico.(64) Sin embargo, hay que considerar que esto resulta contradictorio con lo que muestra la publicidad; algunos de los empaques y otras formas de difusión y divulgación de uso de dentífricos muestran toda la cabeza del cepillo cubierta de crema dental (aproximadamente cuatro veces la recomendación para niños).(51) Aun para un odontólogo bien documentado resulta difícil competir con estrategias publicitarias que tienen tantos años en el mercado, que son de una amplia difusión, en las que se invierten tantos recursos y que dejan la idea de que todos los pacientes tienen iguales necesidades y riesgos en salud bucal.
La frecuencia de uso del dentífrico durante el día influye de manera importante sobre la ingesta total de fluoruros;(64,65,66) en este sentido, la EAPD en el año 2009(68) y la FDI (Federación Dental Internacional)(84) en el 2008 recomiendan usar crema dental fluorada dos veces al día y tener en cuenta que los niños deben escupir durante el cepillado y enjuagarse la boca con un mínimo de agua después del cepillado para disminuir su deglución; recomiendan además mantener la supervisión de los menores de 6 años y seguir las indicaciones de cada autoridad nacional correspondiente, específicas para menores de 3 años.(66,84)
Normativa de países de América Latina sobre condiciones de uso de fluoruros en los dentífricos
Perú, Chile, Guatemala, México y el Bloque Mercosur (Argentina, Uruguay, Paraguay y Brasil) cuentan con normas técnicas en las que se exponen las condiciones de uso de fluoruros en los dentífricos.(85,86,87,88,89,90)
En el caso de Perú, la Norma Técnica del 2001 considera que los dentífricos con 1100 ppm de fluoruro o más son indicados para niños mayores de 6 años y adultos; estas deben presentar como mínimo 600 ppm de flúor soluble al año de fabricación y 450 ppm hasta su expiración. Las cremas dentales indicadas para niños menores de 6 años deberán tener una concentración de fluoruro de 250 a 550 ppm y deben tener como mínimo 60% de flúor soluble hasta su expiración, indicando en el rotulado la advertencia de “no ingerir”; no deben tener frases que incentiven la ingestión del producto y deben consignar la frase “niños menores de 6 años utilizar una pequeña cantidad (tamaño de una lenteja) y ser supervisados por sus padres”. Los dentífricos con 1100 ppm de fluoruro o más deben tener la advertencia “no se recomienda el uso en menores de 6 años”. Los anuncios de los productos de higiene bucal no deben dar a entender que la sola aplicación o uso de los agentes fluorados asegura la inexistencia de caries dental ni controla el total desarrollo de la placa bacteriana, y los dibujos o diseños impresos en los envases no deben incentivar el uso excesivo del producto.(89,90)
Por su parte, la norma guatemalteca establece como parámetro para la concentración de flúor soluble total 1.003 ppm si este proviene de MFP y 1.086 ppm si es de NaF, hasta un límite máximo de 1.500 ppm para ambos ingredientes.(86)
El Bloque Mercosur (Argentina, Uruguay, Paraguay y Brasil) tiene el “Reglamento técnico Mercosur sobre lista de sustancias que los productos de higiene personal, cosméticos y perfumes no deben contener, excepto en las condiciones y con las restricciones establecidas”, el cual indica que las cremas dentales con 0.1-0.15% de MFP o fluoruro de sodio deberán presentar en su rotulado el texto: “niños de 6 años o menores: utilizar una cantidad del tamaño de una arveja bajo la supervisión de un adulto a fin de minimizar el riesgo de ingestión. En caso de recibir un aporte suplementario de flúor a través de otras fuentes, consulte a su odontólogo o médico”, excepto si ya está rotulada como contraindicada para niños (por ejemplo: sólo para adultos).(88)
Para la norma oficial mexicana, la concentración de flúor en un dentífrico no debe exceder 0,2% y en productos para niños menores de seis años debe ser máximo de 0,05%. Señala que los dentífricos con mayor contenido de flúor deben emplearse en cantidades pequeñas (“del tamaño de una gota”) y bajo la supervisión de un adulto. Los productos de uso tópico objeto de esta norma deben cumplir con los requisitos sanitarios y comerciales de etiquetado establecidos en la NOM-137-SSA1-1995; para dentífricos de 1500 ppm, incluir la leyenda: “en menores de 6 años use 5 mm, bajo supervisión de un adulto. Evite su ingestión”, para dentífricos con concentración máxima de 550 ppm, incluir la leyenda: “esta pasta es recomendada para niños menores de 6 años; use 5 mm, bajo supervisión de un adulto. Evite su ingestión”.(85,87)
En Colombia, la concentración máxima de fluoruros en los dentífricos cosméticos debe ser de 1.500 ppm para uso en adultos y 500 ppm para su uso en niños menores de 6 años; cuando está mezclada con otros compuestos fluorados, la concentración del flúor no debe exceder 1500 ppm.(91) La leyenda: “contiene fluoruro de sodio” debe ir en todas las etiquetas y en toda pasta dentífrica que contenga de 0,1 a 0,15% de fluoruro; excepto si ya está etiquetada como contraindicado para los niños, debe tener obligatoriamente el mensaje: “niños de 6 años o menores: utilizar una cantidad del tamaño de un guisante bajo la supervisión de un adulto para minimizar la deglución. En caso de ingesta de flúor a través de otras fuentes, consulte a su dentista o doctor”.(92)
En Chile, la norma técnica de 1993 establecía que las concentraciones de flúor en los dentífricos no debían ser menores a 1000 ppm ni mayores a 1500 ppm para uso en adultos, y que los dentífricos destinados a menores de 6 años debían tener una concentración máxima de 500 ppm.(93)
Esta normatividad fue modificada en 2015 con cambios sobresalientes, como la recomendación de uso de pastas con concentraciones de fluoruros de 1000 a 1500 ppm en el grupo de menores de 6 años.(94) La norma justifica esta modificación en el mayor efecto protector de las cremas de alta concentración comparado con las de baja concentración de flúor (menor a 600 ppm).(2,94,95)
También expresa que la concentración del ion flúor en ppm y el contenido total de flúor deberá declararse en los envases y estuches de las pastas dentales. (94)
Para niños y niñas menores de 6 años sugiere que la higiene bucal debe ser realizada por un adulto, o al menos bajo la supervisión de éste, controlando la cantidad de pasta a utilizar e indicando al niño que no debe tragársela. Explica que, en el cepillo seco, se debe dispensar la pasta dental a lo ancho en un tamaño no superior al de una arveja, aproximadamente 0,5 gramos, y utilizar una menor cantidad en los niños y niñas que no pueden eliminar bien los restos de pasta dental.(94)
Para las pastas con menos de 1000 ppm se sugiere eliminar el rótulo de pasta infantil o para menores de 6 años, y para las pastas con 1000 a 1500 ppm de flúor, se pide incluir la frase “en menores de 6 años, usar una cantidad igual o menor al tamaño de una arveja, supervisado por un adulto, evitando su ingesta”. Indica que los dentífricos no deben contener frases que induzcan su ingesta, como “delicioso sabor”.(94)
La Tabla 1 presenta las concentraciones de fluoruros que según la normatividad de cada país deben ser usadas en adultos y en niños.
Tabla 1 Concentración recomendada de fluoruros en los dentífricos según la normatividad de países de América Latina
| País | Concentración de flúor para dentífricos de adultos | Concentración de flúor para dentífricos de niños |
|---|---|---|
| Perú | Entre 1000 y 1500 ppm | Menor a 600 ppm |
| Chile | Entre 1000 y 1500 ppm | Entre 1000 y 1500 ppm |
| Guatemala | Entre 1003 y 1500 ppm | |
| México | No mayor a 2000 ppm | Máximo 500 ppm |
| Colombia | Máximo 1500 ppm | Máximo 500 ppm |
La evidencia indica que, para los entes gubernamentales de países latinoamericanos,(85,86,87,88,89,90,91,92,93,94) al igual que en territorios de Norte América y Europa, sigue siendo motivo de preocupación el exceso de dispensación de crema dental fluorada en niños pequeños.(96)
Teniendo en cuenta que términos como “guisante”, “gota”, “lenteja” y “arveja” pueden ser equívocos porque no son una medida absoluta y quedan abiertos a interpretación, Creeth et al(96) recomiendan unificar la terminología definida para indicar la cantidad de pasta de dientes al tamaño de “un guisante”, debido a que se demostró que este término correlaciona muy bien el peso en gramos indicado por la normativa (0,25 g). De Moura et al(97) sugieren que también se hace necesario ofrecer educación sobre la prevalencia de la fluorosis dental mediante programas para la salud materno-infantil, incluyendo el asesoramiento sobre la cantidad adecuada de pasta dentífrica fluorada en la primera infancia, debido a que se demostró que los niños cuyos padres participaron en estos programas presentaron menos prevalencia de fluorosis dental.
Características del mercado de los dentífricos en Medellín (Colombia)
Dado que la disponibilidad comercial determina el uso que hace el paciente, se revisaron datos de una base elaborada por el grupo de investigación Patología Oral, Periodoncia y Cirugía Alvéolo-Dentaria (POPCAD) de la Facultad de Odontología de la Universidad de Antioquia, que incluye un listado con las cremas dentales disponibles entre 2013 y 2014 en cinco sedes de uno de los almacenes de cadena más grandes de la ciudad, donde se verificó el tipo de flúor y la concentración consignada en las etiquetas de cada producto. Esta información fue consignada en una hoja de cálculo de Microsoft Excel® 2010 y analizada en el programa estadístico IBM SPSS® versión 22.0 con el fin de explorarla y resumirla (datos no publicados).
Se reportaron 11 marcas de cremas dentales con 45 referencias, entre las cuales se presentan diferentes tipos de flúor (Tabla 2), siendo las concentraciones más utilizadas las de 1450 ppm (44,4%), seguidas por las de 1100 ppm (22,2%), 1100/350 ppm (7,4%) y las inferiores a 1000 ppm (5,6%). Ramírez et al identificaron que, en el municipio de Frontino, Antioquia, las cremas dentales convencionales contenían flúor en concentraciones de 1504 ± 387 ppm,(34) datos similares a los de las cremas dentales comercializadas en el territorio nacional, las cuales poseen concentraciones de flúor entre 1100 y 1500 ppm.(98)
Tabla 2 Tipos de flúor y frecuencia de uso en las cremas dentales más comercializadas en la ciudad de Medellín, Colombia
| Tipo de flúor | Frecuencia | Porcentaje |
|---|---|---|
| Fluoruro de estaño / Fluoruro de sodio | 5 | 9,3% |
| Fluoruro de sodio | 36 | 66,7% |
| Monofluorofosfato | 10 | 18,5% |
| Monofluorofosfato/Fluoruro de sodio | 2 | 3,7% |
| Sin flúor | 1 | 1,9% |
| Total | 54 | 100,0% |
Se encontraron 7 referencias de cremas dentales con presentación especial para niños, con etiquetas que advierten que deben ser utilizadas por niños mayores de 6 años, pero cuya presentación, olor y sabor son atractivos para niños de menor edad. De estos productos, 42,9% no tenían flúor, 42,9% contenían NaF y 14,3% contenían MFP; las concentraciones más utilizadas son las de 0 ppm (42,9%), seguidas de 500 ppm (28,6%), 995 ppm (14,3%) y 1100 ppm (14,3%). Estas concentraciones son similares a las encontradas por Báez-Quintero et al en 17 cremas dentales para niños vendidas en los principales supermercados de Bogotá.(99)
En ese sentido, la norma técnica colombiana no aclara las determinaciones de los excipientes como sí lo hacen los ministerios de salud de Perú y Chile con sus disposiciones técnicas, en las que indican que “las cremas dentales para niños no deben contener en su composición saborizantes, edulcorantes o colorantes que incentiven la ingesta indebida”.(89,94)
Las diversas presentaciones de los fluoruros tópicos para autoaplicación muestran diferencias en la concentración de flúor, volúmenes e indicaciones de uso, por lo que el odontólogo tiene la obligación de conocerlas, de modo que cuente con un mejor criterio al momento de sugerir su uso. En Colombia no se ha estudiado suficientemente el cumplimiento de la normatividad y son escasas las investigaciones que evalúan a los odontólogos sobre los conocimientos acerca de los dentífricos y sus recomendaciones de uso;(4) y aunque hay estudios que buscan evaluar a cuidadores o educadores escolares al respecto, se ha dejado de lado el papel del odontólogo como fuente esencial de información para la comunidad.(100,101,102,103)
Arrieta et al(102) demuestran que existe un nivel deficiente de conocimientos y prácticas sobre fluorosis dental por parte de odontólogos y auxiliares del hospital local de Cartagena de Indias -situación que finalmente repercutía en la orientación que se les daba a los cuidadores de los niños-. En ese mismo año, una situación similar fue descrita por Ramírez et al(101) en un trabajo conjunto con la Alcaldía de Medellín: las personas se mostraban confundidas con los diferentes mensajes transmitidos por odontólogos y personal auxiliar sobre flúor, fluorosis y uso de la crema dental. La información recibida por los cuidadores acerca del tipo de dentífrico que debían usar los niños evidenció la variedad de criterios que tenían los profesionales locales al momento de recomendar una crema dental infantil, así como su relación con las presentaciones comerciales.
CONCLUSIONES
El efecto anticaries de las cremas dentales en los niños está sujeto a variaciones relacionadas con el tipo y la concentración de flúor que contienen dichas cremas. En el caso de niños con caries activa, alta exposición al azúcar o altos índices de placa, se deben utilizar pastas dentales con flúor convencional (1000-1500 ppm F), pero cuando el flúor puede tener un efecto adverso relacionado con la ingestión por parte de niños pequeños, sobrepasando los límites permitidos, se puede acudir al uso de dentífricos fluorados de baja concentración y a la implementación de estrategias educativas que permitan supervisar y controlar adecuadamente la dosificación, concentración y frecuencia del cepillado -variables que son motivo de preocupación en varios países, incluidos algunos latinoamericanos-. En Colombia, el mercado local responde a los criterios de la reglamentación para el uso de cremas dentales, aunque puede mejorarse la contribución si en los empaques se incluye información aclaratoria sobre las concentraciones de flúor biodisponible, la cantidad y frecuencia de uso recomendada según la edad, y el riesgo de caries y de fluorosis, y si se indica la dosificación mediante el uso de una foto como la de la ADA, para agregar elementos de seguridad al uso de estos productos en los infantes. Finalmente, teniendo en cuenta el panorama particular de prevalencia de fluorosis en el país, cabe preguntarse si sería razonable modificar la normatividad siguiendo el ejemplo chileno, además de proponer la utilización de un único término como “guisante” para correlacionar mejor el peso en gramos de crema dental indicado por la normativa para niños menores de 3 años.
REFERENCIAS
1. Marinho VC, Higgins JP, Logan S, Sheiham A. Topical fluoride (toothpastes, mouthrinses, gels or varnishes) for preventing dental caries in children and adolescents. Cochrane Database Syst Rev. 2003; (4): CD002782. DOI:10.1002/14651858.CD002782 [ Links ]
2. Cury JA, Tenuta LMA, Ribeiro CCC, Leme AFP. The importance of fluoride dentifrices to the current dental caries prevalence in Brazil. Braz Dent J. 2004; 15(3): 167-174. DOI:10.1590/S0103-64402004000300001 [ Links ]
3. Jackson RJ, Newman HN, Smart GJ, Stokes E, Hogan JI, Brown C et al. The effects of a supervised toothbrushing programme on the caries increment of primary school children, initially aged 5-6 years. Caries Res. 2005; 39(2): 108-115. DOI:10.1159/000083155 [ Links ]
4. Ellwood RP, Fejerskov O, Cury JA, Clarkson B. Fluoride in caries control. En: Fejerskov O, Kidd E. Dental caries: the disease and its clinical management. 2 ed. Oxford: Blackwell & Munksgaard; 2008: 287-319. [ Links ]
5. Marinho VC. Cochrane reviews of randomized trials of fluoride therapies for preventing dental caries. Eur Arch Paediatr Dent. 2009; 10(3): 183-191. [ Links ]
6. Hashizume LN, Mathias TC, Cibils DM, Maltz M. Effect of the widespread use of fluorides on the occurrence of hidden caries in children. Int J Paediatr Dent. 2003; 23(1): 72-76. DOI:10.1111/j.1365-263X.2012.01231.x [ Links ]
7. Walsh T, Worthington HV, Glenny AM, Appelbe P, MarinhoVC, Shi X. Fluoride toothpastes of different concentrations for preventing dental caries in children and adolescents. Cochrane Database Syst Rev. 2010; 20(1): CD007868. DOI:10.1002/14651858.CD007868.pub2 [ Links ]
8. Noronha MdS, Romão DA, Cury JA, Machado-Tabchoury CP. Effect of fluoride concentration on reduction of enamel demineralization according to the cariogenic challenge. Braz Dent J. 2016; 27(4): 393-398. DOI:10.1590/0103-6440201600831 [ Links ]
9. Milsom K, Mitropoulos CM. Enamel defects in 8-year- old children in fluoridated and non-fluoridated parts of Cheshire. Caries Res. 1990; 24(4): 286-289. DOI:10.1159/000261284 [ Links ]
10. Pendrys DG, Katz RV, Morse DE. Risk factors for enamel fluorosis in a non-fluoridated population. Am J Epidemiol. 1994; 140(5): 461-471. [ Links ]
11. Osuji OO, Leake JL. Chipman ML, Nikiforuk G, Locker D, Levine N. Risk factors for dental fluorosis in a fluoridated community. J Dent Res. 1988; 67(12): 1488-1492. DOI:10.1177/00220345880670120901 [ Links ]
12. Tabari ED, Ellwood R, Rugg-Gunn AJ, Evans DJ, Davies RM. Dental fluorosis in permanent incisor teeth in relation to water fluoridation, social deprivation and toothpaste usage in infancy. Br Dent J. 2000; 189(4): 216- 220. [ Links ]
13. Mascarenhas AK, Burt BA. Fluorosis risk from early exposure to fluoride toothpaste. Community Dent Oral Epidemiol. 1998; 26(4): 241-248. [ Links ]
14. Mascarenhas AK. Risk factors for dental fluorosis: a review of the recent literature. Pediatr Dent. 2000; 22(4): 269-277. [ Links ]
15. Cordeiro MCR, Armonia PL, Scabar LF, Chelotti A. O creme dental fluorado, a escova dental e a idade da criança como fatores de risco da fluorose dentária. J Health Sci Inst. 2007; 25(1): 29-38. [ Links ]
16. Atia GS, May J. Dental fluorosis in the paediatric patient. Dent Update. 2013; 40(10): 836-839. [ Links ]
17. Simard PL, Naccache H, Lachapelle D, Brodeur JM. Ingestion of fluoride from dentifrices by children aged 12 to 24 months. Clin Pediatr (Phila). 1991; 30(11): 614-617. DOI:10.1177/000992289103001101 [ Links ]
18. Levy SM, McGrady JA, Bhuridej P, Warren JJ, Heilman JR, Wefel JS. Factors affecting dentifrice use and ingestion among a sample of U.S. preschoolers. Pediatr Dent. 2000; 22(5): 389-394. [ Links ]
19. Pessan JP, Silva SM, Buzalaf MA. Evaluation of the total fluoride intake of 4-7-year-old children from diet and dentifrice. J Appl Oral Sci. 2003; 11(2): 150-156. [ Links ]
20. Franco AM, Martignon S, Saldarriaga A, González MC, Arbeláez MI, Ocampo A et al. Total fluoride intake in children aged 22-35 months in four Colombian cities. Community Dent Oral Epidemiol. 2005; 33(1): 1-8. DOI:10.1111/j.1600-0528.2004.00164.x [ Links ]
21. Omena LMF, Silva MFdeA, Pinheiro CC, Cavalcante JC, Sampaio FC. Fluoride intake from drinking water and dentifrice by children living in a tropical area of Brazil. J Appl Oral Sci. 2006; 14(5): 382-387. [ Links ]
22. De-Almeida BS, da-Silva-Cardoso VE, Buzalaf MA. Fluoride ingestion from toothpaste and diet in 1- to 3-year- old Brazilian children. Community Dent Oral Epidemiol. 2007; 35(1): 53-63. [ Links ]
23. Oliveira MJ, Martins CC, Paiva SM, Tenuta LMA, Cury JA. Estimated fluoride doses from toothpastes should be based on total soluble fluoride. Int J Environ Res Public Health. 2013; 10(11): 5726-5736. DOI:10.3390/ijerph10115726 [ Links ]
24. Haftenberger M, Viergutz G, Neumeister V, Hetzer G. Total fluoride intake and urinary excretion in German children aged 3-6 years. Caries Res. 2001; 35(6): 451-457. [ Links ]
25. García-Camba-de-la-Muela JM, García-Hoyos F, Valera- Morales M, González-Sanz A. Absorción sistémica de flúor en niños secundaria al cepillado con dentífrico fluorado. Rev Esp Salud Pública. 2009; 83(3): 415-425. [ Links ]
26. Lockner F, Twetman S, Stecksén-Blicks C. Urinary fluoride excretion after application of fluoride varnish and use of fluoride toothpaste in young children. Int J Paediatr Dent. 2017; 27(6): 463-468. DOI:10.1111/ipd.12284 [ Links ]
27. Forte FD, Moimaz SA, Sampaio FC. Urinary fluoride excretion in children exposed to fluoride toothpaste and to different water fluoride levels in a tropical area of Brazil. Braz Dent J. 2008; 19(3): 214-218. [ Links ]
28. Colombia. Ministerio de Salud. Protocolo de vigilancia en salud pública: exposición a fluor (Centinela). Bogotá: Instituto Nacional de Salud; 2007. [ Links ]
29. Soto-Rojas AE, Ureña-Cirett JL, Martínez-Mier EA. A review of the prevalence of dental fluorosis in México. Rev Panam Salud Publica. 2004; 15(1): 9-18. [ Links ]
30. Montero M, Rojas-Sánchez F, Socorro M, Torres J, Acevedo AM. Dental caries and fluorosis in children consuming water with different fluoride concentrations in Maiquetia, Vargas State, Venezuela. Invest Clin. 2007; 48(1): 5-19. [ Links ]
31. Colombia. Ministerio de Salud. III Estudio nacional de salud bucal ENSAB III. Bogotá: Ministerio de Salud de Colombia; 1999. [ Links ]
32. Colombia. Ministerio de Salud y Protección Social. IV Estudio nacional de salud bucal ENSAB IV: Situación de salud bucal: para saber cómo estamos y saber qué hacemos. Bogotá: Ministerio de Salud y Protección Social de Colombia; 2004. [ Links ]
33. Skotowski MC, Hunt RJ, Levy SM. Risk factors for dental fluorosis in pediatric dental patients. J Public Health Dent. 1995; 55(3): 154-159. [ Links ]
34. Ramírez BS, Franco AM, Sierra JL, López RV, Alzate T, Sarrazola AM et al. Fluorosis dental en escolares y exploración de factores de riesgo. Municipio de Frontino, 2003. Rev Fac Odont Univ Antioq. 2006; 17(2): 26-33. [ Links ]
35. Barbachan-e-Silva B, Maltz M. Prevalence of dental caries, gingivitis, and fluorosis in 12-year-old students from Porto Alegre - RS, Brazil, 1998/1999. Pesqui Odontol Bras. 2001; 15(3): 208-214. [ Links ]
36. Menezes LMB, de-Sousa MLR, Azevedo-Rodrígues LK, Cury JA. Autopercepção da fluorose pela exposição a flúor pela água e dentifrício. Rev Saúde Publica. 2002; 36(6): 752-754. DOI:http://dx.doi.org/10.1590/S0034-89102002000700015 [ Links ]
37. Moysés SJ, Moysés ST, Allegretti AC, Argenta M, Werneck R. Dental fluorosis: epidemiological fiction? Rev Panam Salud Publica . 2002; 12(5): 339-346. [ Links ]
38. Peres KG, Latorre MR, Peres MA, Traebert J, Panizzi M. Impact of dental caries and dental fluorosis on 12-year- old schoolchildren’s self-perception of appearance and chewing. Cad Saúde Publica. 2003; 19(1): 323-330. [ Links ]
39. Lima YB, Cury JA. Seasonal variation of fluoride intake by children in a subtropical region. Caries Res. 2003; 37(5): 335-338. DOI:10.1159/000072164 [ Links ]
40. Narvai PC, Frazão P, Roncalli AG, Antunes JL. Dental caries in Brazil: decline, polarization, inequality and social exclusion. Rev Panam Salud Publica. 2006; 19(6): 385- 393. [ Links ]
41. Peres KG, Peres MA, Araujo CL, Menezes AM, Hallal PC. Social and dental status along the life course and oral health impacts in adolescents: a population-based birth cohort. Health Qual Life Outcomes. 2009; 7: 95. DOI:10.1186/1477-7525-7-95 [ Links ]
42. Rodrigues MH, Leite AL, Arana A, Villena RS, Forte FD, Sampaio FC et al. Dietary fluoride intake by children receiving different sources of systemic fluoride. J Dent Res. 2009; 88(2): 142-145. DOI:10.1177/0022034508328426 [ Links ]
43. Levy SM, Broffitt B, Marshall TA, Eichenberger- Gilmore JM, Warren JJ. Associations between fluorosis of permanent incisors and fluoride intake from infant formula, other dietary sources and dentifrice during early childhood. J Am Dent Assoc. 2010; 141(10): 1190-1201. [ Links ]
44. Stovell AG, Newton BM, Lynch RJM. Important considerations in the development of toothpaste formulations for children. Int Dent J. 2013; 63(Suppl 2): 57-63. DOI:10.1111/idj.12083 [ Links ]
45. Batlle-Edo C, De-Conte-Vila O. Dentífricos. Asesoramiento. Farm Prof. 2001; 15(5): 61-69. [ Links ]
46. Weinert W. Oral Hygiene Products. En: Ullmann F, Gerhartz W, Yamamoto S, Campbell T, Pfefferkorn R, Rounsaville J. Ullmann’s encyclopedia of industrial chemistry. 5 ed. California: VCH; 1991: 201-217. [ Links ]
47. Pearce EI, Dibdin GH. The diffusion and enzymic hydrolysis of monofluorophosphate in dental plaque. J Dent Res. 1995; 74(2): 691-697. DOI:10.1177/00220345950740021101 [ Links ]
48. Churchley D, Schemehorn BR. In vitro assessment of a toothpaste range specifically designed for children. Int Dent J. 2013; 63(Suppl 2): 48-56. DOI:10.1111/idj.12071 [ Links ]
49. DePaola PF, Soparkar PM, Triol C, Volpe AR, Garcia L, Duffy J et al. The relative anticaries effectiveness of sodium monofluorophosphate and sodium fluoride as contained in currently available dentifrice formulations. Am J Dent. 1993; 6: S7-S12. [ Links ]
50. Volpe AR, Petrone ME, Davies R, Proskin HM. Clinical anticaries efficacy of NaF and SMFP dentifrices: overview and resolution of the scientific controversy. J Clin Dent. 1995; 6: 1-28. [ Links ]
51. Basch CH, Hammond R, Guinta A, Rajan S, Basch CE. Advertising of toothpaste in parenting magazines. J Community Health. 2003; 38(5): 911-914. DOI:10.1007/s10900-013-9700-2 [ Links ]
52. Davies R, Scully C, Preston AJ. Dentifrices - an update. Med Oral Patol Oral Cir Bucal. 2010; 15(6): e976-e982. [ Links ]
53. Carrera CA, Giacaman RA, Muñoz-Sandoval C, Cury JA. Total and soluble fluoride content in commercial dentifrices in Chile. Acta Odontol Scand. 2002; 70(6): 583-588. DOI:10.3109/00016357.2011.640287 [ Links ]
54. American Dental Association Council on Scientific Affairs. Fluoride toothpaste use for young children. J Am Dent Assoc. 2014; 145(2): 190-191. DOI:10.14219/jada.2013.47 [ Links ]
55. Conde NC, Rebelo MA, Cury JA. Evaluation of the fluoride stability of dentifrices sold in Manaus, AM, Brazil. Pesqui Odontol Bras. 2003; 17(3): 247-253. [ Links ]
56. Cury JA, Tabchoury CPM, Piovano S. Concentration and stability of fluoride in dentifrices market in Buenos Aires. Bol Asoc Argent Odontol Ninos. 2006; 35(2): 4-8. [ Links ]
57. Benzian H, Holmgren C, Helderman WV. Efficacy of fluoride toothpaste over time. Braz Dent J. 2012; 23(4): 311-314. [ Links ]
58. Van-Loveren C, Moorer WR, Buijs MJ, Van-Palenstein- Helderman WH. Total and free fluoride in toothpastes from some non-established market economy countries. Caries Res. 2005; 39(3): 224-230. DOI:10.1159/000084802 [ Links ]
59. Cury JA, Oliveira MJL, Martins CC, Tenuta LMA, Paiva SM. Available fluoride in toothpastes used by Brazilian children. Braz Dent J. 2010; 21(5): 396-400. DOI:10.1590/S0103-64402010000500003 [ Links ]
60. Sebastian ST, Siddanna S. Total and free fluoride concentration in various brands of toothpaste marketed in India. J Clin Diagn Res. 2015; 9(10): ZC09-ZC12. DOI:10.7860/JCDR/2015/13382.6578 [ Links ]
61. Moraes SM, Pessan JP, Ramires I, Buzalaf MA. Fluoride intake from regular and low fluoride dentifrices by 2-3-year-old children: influence of the dentifrice flavor. Braz Oral Res. 2007; 21(3): 234-240. [ Links ]
62. Zohoori FV, Duckworth RM, Omid N, O’Hare WT, Maguire A. Fluoridated toothpaste: usage and ingestion of fluoride by 4 to 6 years old children in England. Eur J Oral Sci. 2012; 120(5): 415-421. DOI:10.1111/j.1600-0722.2012.00984.x [ Links ]
63. Burt BA. The changing patterns of systemic fluoride intake. J Dent Res. 1992; 71(5): 1228-1237. DOI:10.1177/00220345920710051601 [ Links ]
64. Paiva SM, Lima YB, Cury JA. Fluoride intake by Brazilian children from two communities with fluoridated water. Community Dent Oral Epidemiol. 2003; 31(3): 184-191. [ Links ]
65. Lima CV, Cury JA, Vale GC, Lima MD, Moura LdeF, Moura MS. Total fluoride intake by children from a tropical Brazilian city. Caries Res. 2015; 49(6): 640-646. DOI:10.1159/000442029 [ Links ]
66. Do-Nascimento HA, Soares-Ferreira JM, Granville-Garcia AF, de-Brito-Costa EM, Almeida-Cavalcante AL, Sampaio FC. Estimation of toothpaste fluoride intake in preschool children. Braz Dent J. 2013; 24(2): 142-146. DOI:10.1590/0103-6440201302087 [ Links ]
67. Clark MB, Slayton RL, American Academy of Pediatrics (Section on Oral Health). Fluoride use in caries prevention in the primary care setting. Pediatrics. 2014; 134(3): 626- 633. DOI:10.1542/peds.2014-1699 [ Links ]
68. European Academy of Paediatric Dentistry. Guidelines on the use of fluoride in children: an EAPD policy document. Eur Arch Paediatr Dent. 2009; 10(3): 129-135. [ Links ]
69. Evans RW, Stamm JW. An epidemiologic estimate of the critical period during which human maxillary central incisors are most susceptible to fluorosis. J Public Health Dent. 1991; 51(4): 251-259. [ Links ]
70. Horowitz HS. The need for toothpastes with lower than conventional fluoride concentrations for preschool-aged children. J Public Health Dent . 1992; 52(4): 216-221. [ Links ]
71. Wong MC, Glenny AM, Tsang BW, Lo EC, Worthington HV, Marinho VC. Topical fluoride as a cause of dental fluorosis in children. Cochrane Database Syst Rev. 2010; (1): CD007693. DOI:10.1002/14651858.CD007693.pub2 [ Links ]
72. DenBesten P, Ko HS. Fluoride levels in whole saliva of preschool children after brushing with 0.25 g (pea-sized) as compared 1.0 g (full-brush) of a fluoride dentifrice. Pediatr Dent. 1996; 18(4): 277-280. [ Links ]
73. Lima TJ, Ribeiro CC, Tenuta LMA, Cury JA. Low- fluoride dentifrice and caries lesions control in children with different caries experience: a randomized clinical trial. Caries Res. 2008; 42(1): 46-50. DOI:10.1159/000111749 [ Links ]
74. Topping GV. The anticaries effects of low fluoride formulations of toothpaste may be different in caries- active and caries-inactive children. J Evid Based Dent Pract. 2009; 9(1): 30-31. DOI:10.1016/j.jebdp.2008.12.006 [ Links ]
75. Cury JA, Do-Amaral RC, Tenuta LMA, Del-Bel-Cury AA, Tabchoury CP. Low-fluoride toothpaste and deciduous enamel demineralization under biofilm accumulation and sucrose exposure. Eur J Oral Sci. 2010; 118(4): 370-375. DOI:10.1111/j.1600-0722.2010.00745.x [ Links ]
76. Cury JA, Tenuta LMA. Evidence-based recommendation on toothpaste use. Braz Oral Res. 2014; 28(Spec): 1-7. DOI:10.1590/S1806-83242014.50000001 [ Links ]
77. Arana AS, Villa AE. Uso de pasta dental con flúor en niños de 3 a 5 años de la ciudad de Trujillo. Rev Estomatol Herediana. 2006; 16(2): 89-92. [ Links ]
78. O’Mullane DM, Kavanagh D, Ellwood RP, Chesters RK, Schafer F, Huntington E et al. A three-year clinical trial of a combination of trimetaphosphate and sodium fluoride in silica toothpastes. J Dent Res . 1997; 76(11): 1776-1781. DOI:10.1177/00220345970760110901 [ Links ]
79. Stephen KW, Creanor SL, Russell JI, Burchell CK, Huntington E, Downie CF. A 3- year oral health dose- response study of sodium monofluorophosphate dentifrices with and without zinc citrate: anti-caries results. Community Dent Oral Epidemiol. 1988; 16(6): 321-325. [ Links ]
80. Martínez-Mier EA, Soto-Rojas AE, Urena-Cirett JL, Stookey GK, Dunipace AJ. Fluoride intake from foods, beverages and dentifrice by children in Mexico. Community Dent Oral Epidemiol. 2003; 31(3): 221-230. [ Links ]
81. Franco AM, Saldarriaga A, Martignon S, Gonzalez MC, Villa AE. Fluoride intake and fractional urinary fluoride excretion of Colombian preschool children. Community Dent Health. 2005; 22(4): 272-278. [ Links ]
82. Hall KB, Delbem AB, Nagata ME, Hosida TY, de-Moraes FR, Danelon M et al. Influence of the amount of dentifrice and fluoride concentrations on salivary fluoride levels in children. Pediatr Dent . 2016; 38(5): 379-384. [ Links ]
83. American Academy of Pediatric Dentistry. Guideline on infant oral health care. Clinical Guidelines, Reference manual. 2004; 37(6): 15-16. [ Links ]
84. FDI World Dental Federation. Promoting dental health through fluoride toothpaste: original version adopted by the General Assembly in november 2000, Paris, France: revised version adopted by the General Assembly: 26th September 2008, Stockholm, Sweden [Internet]. Stockholm: FDI; 2008. En:http://www.fdiworldental.org/media/11323/Promoting-dental-health-through-fluoride-toothpaste-2008.pdf [ Links ]
85. Estados Unidos Mexicanos. Secretaría de Economía. DECLARATORIA de vigencia de las normas mexicanas NMX-E-053-CNCP-2013, NMX-E-114- CNCP-2013, NMX-E-134-CNCP-2013, NMX-E- 146-CNCP-2013, NMX-E-178-CNCP-2013, NMX- E-234-CNCP-2013, NMX-E-255-CNCP-2013, NMX-K-539-CNCP-2013, NMX-K-541-CNCP-2013, NMX-Q-010-CNCP-2013, NMX-E-122-CNCP-2013 y NMX-E-165-CNCP-2013. En:http://dof.gob.mx/nota_detalle_popup.php?codigo=5347615 [ Links ]
86. Guatemala: Ministerio de Economía. COGUANOR NGO 30 019 1987: norma guatemalteca obligatoria: pasta dental con flúor y pasta dental sin flúor: especificaciones. Ciudad de Guatemala: Ministerio de Economía; 1987. En:http://cretec.org.gt/wp-content/files_mf/coguanorngo_30_019.pdf [ Links ]
87. Estados Unidos Mexicanos. Secretaría de Salud. Norma oficial mexicana NOM-137-SSA1-1995: información regulatoria-especificaciones generales de etiquetado que deberán ostentar los dispositivos médicos, tanto de manufactura nacional como de procedencia extranjera [Internet]. Ciudad de México: Secretaría de Salud de México; 1995. En:http://www.salud.gob.mx/unidades/cdi/nom/137ssa15.html [ Links ]
88. MERCOSUR. Reglamento técnico MERCOSUR sobre lista de sustancias que los productos de higiene personal, cosméticos y perfumes no deben contener, excepto en las condiciones y con las restricciones establecidas 2000[Internet]. En:http://www.anmat.gov.ar/webanmat/mercosur/agregados/AgregadoIII/Cosmeticos/UNI3PRES11_09_REV1_ES.pdf [ Links ]
89. Perú. Ministerio de salud. Norma Técnica Sanitaria para la adición de fluoruros en cremas dentales, enjuagatorios y otros productos utilizados en la higiene bucal. Resolución ministerial Nº 454-2001-SA/DM. Lima, 27 de julio del 2001[Internet]. En:ftp://ftp2.minsa.gob.pe/normaslegales/2001/RM454-2001.pdf. [ Links ]
90. Perú. Ministerio de salud. Resolución ministerial Nº 154- 2001-SA/DM. Lima, 7 de marzo del 2001 [Internet]. En:ftp://ftp2.minsa.gob.pe/normaslegales/2001/RM154-2001.pdf. [ Links ]
91. Colombia: Ministerio de la Protección. Instituto Nacional de Vigilancia de Medicamentos y Alimentos - INVIMA. Acta 08 de 2010, Numeral 2.11.4 de la sala especializada de medicamentos y productos biológicos de la comisión revisora 2010. [Internet]. En:https://www.invima.gov.co/images/pdf/salas-especializadas/Sala_Especializada_de_Medicamentos/acta2010/ACTA082010_SEMPB.pdf [ Links ]
92. Comunidad Andina. Decisión 516 de 2002: armonización de Legislaciones en materia de productos cosméticos [Internet]. En:http://webcache.googleusercontent.com/search?q=cache:http:// w w w . s a l u d c a p i t a l . g o v . c o / D S P / D o c s / Decisi%25C3%25B3n%2520516%2520de%25202002.pdf [ Links ]
93. Chile. Ministerio de Salud. Normas de usos de fluoruros en la prevención odontológica. Norma técnica N° 4.863 del 11 de junio de 1993. Tomo II, Anexos II y III 1998. En:http://web.minsal.cl/portal/url/item/7f2dd0d1a7e8c658e04001011e010fe2.pdf [ Links ]
94. Chile. Ministerio de Salud. Subsecretaría de Salud Pública División de Prevención y Control de Enfermedades, División jurídica. Modifica resolución exenta No 727, de 2008, del Ministerio de Salud, que aprueba norma general técnica No 105 sobre “uso de fluoruros en la prevención odontológica”. Santiago de Chile, 3 de octubre de 2015. Santiago de Chile: Ministerio de Salud de Salud de Chile; 2015 [ Links ]
95. Dos-Santos AP, Nadanovsky P, De-Oliveira BH. A systematic review and meta-analysis of the effects of fluoride toothpastes on the prevention of dental caries in the primary dentition of preschool children. Community Dent Oral Epidemiol. 2013; 41(1): 1-12. DOI:10.1111/j.1600-0528.2012.00708.x [ Links ]
96. Creeth J, Bosma ML, Govier K. How much is a “pea- sized amount”? A study of dentifrice dosing by parents in three countries. Int Dent J. 2013; 63(suppl 2): 25-30. DOI:https://doi.org/10.1111/idj.12074 [ Links ]
97. De-Moura MS, De-Carvalho MM, Silva MC, De-Lima MdeD, De-Deus-Moura LdeF, De-Melo-Simplício AH. The impact of a dental program for maternal and infant health on the prevalence of dental fluorosis. Pediatr Dent. 2013; 35(7): 519-522. [ Links ]
98. Colombia. Ministerio de Salud y Proteccion Social. Documento técnico: perspectiva del uso del fluor vs caries y fluorosis dental en Colombia [Internet]. Bogotá: Ministerio de Salud y Proteccion Social de Colombia; 2006. En:https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/VS/PP/ENT/perspectiva-uso-fluor.pdf [ Links ]
99. Quintero-Báez L, Botazzo-Delbem A, Nagata M, Pessan J. Fluoride concentration in toothpastes and mouthwashes for children distributed in Bogotá, Colombia. Rev Nac Odontol. 2006; 23(12): 41-48. [ Links ]
100. Vásquez P. Conocimientos y prácticas en prevención de caries y gingivitis en educadores de párvulos, JUNJI, Santiago. Rev Chil Salud Pública. 2008; 12 (2): 64-72. [ Links ]
101. Ramírez BS, Franco AM, Ochoa EM. Hábitos de consumo y uso de la crema dental de niños y niñas asistentes a los hogares comunitarios del ICBF y guarderías del Programa Buen Comienzo. Medellín: Secretaría de Salud; 2011 [ Links ]
102. Arrieta K, González FD, Pomares A. Conocimientos y prácticas sobre fluorosis dental en odontólogos y auxiliares hospital local Cartagena de Indias. Rev Colomb Invest Odontol. 2012; 3(7): 1-9. DOI:10.25063/21457735.87 [ Links ]
103. Mattos-Vela MA; Carrasco-Loyola MB, Valdivia-Pacheco SG. Nivel de conocimiento sobre pasta dental fluorada en padres y profesores de preescolares. Int. J Odontostomat. 2013: 7(1): 17-24. DOI:10.4067/S0718-381X2013000100003 [ Links ]
Recibido: 07 de Junio de 2016; Aprobado: 29 de Agosto de 2017











 text in
text in 


