Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Vitae
Print version ISSN 0121-4004
Vitae vol.12 no.2 Medellín Jul./Dec. 2005
EVALUACIÓN DE LA ACTIVIDAD LEISHMANICIDA DE LOS EXTRACTOS ETANÓLICOS DE Rollinia rufinervis SOBRE Leishmania chagasi
EVALUATION OF THE LEISHMANICIDAL ACTIVITY OF THE ETHANOLIC EXTRACTS OF Rollinia rufinervis ON Leishmania chagasi
HERNÁNDEZ C. Jorge E.1*, TENORIO V. José L.1, ROJAS Claudia M. 1 y VALLEJO Gustavo A.2
1 Departamento de Química. Facultad de Ciencias. Universidad del Tolima. A.A 546 Barrio Santa Elena. Ibagué. Tolima. Colombia.
2 Laboratorio de parasitología, Facultad de Ciencias, Universidad del Tolima, A.A 546 Barrio Santa Elena. Ibagué. Tolima. Colombia.
* Autor a quien se debe dirigir la correspondencia: tolijhernandez@hotmail.com
Recibido: abril 4 de 2005 Aceptado: agosto 23 de 2005
RESUMEN
En éste estudio se evalúa la bioactividad de las fracciones obtenidas de los extractos etanólicos de las hojas, de la corteza del tronco y de la corteza de la raíz de Rollinia rufinervis (Annonaceae), las cuales presentan actividad citotóxica y se detecta la presencia de las acetogeninas, que pueden ser responsables de la actividad antiparasitaria. Las fracciones son probadas a concentraciones entre 0.095 µg/mL y 100 µg/mL contra promastigotes de Leishmania chagasi, evaluando la movilidad de los parásitos a las 72 horas. El efecto de las fracciones es contrastado con el medio Schneider-Drosófila sin extracto y con glucantime®, utilizados como control. Las fracciones de Rollinia rufinervis de: acetato de etilo de raíz, éter de petróleo de corteza, acetato de etilo de corteza y acetato de etilo de hojas, presentan actividad leishmanicida. La última fracción es la de mayor actividad causando inmovilidad apreciable o total de los parásitos a lo largo del experimento. De ella se aisló posiblemente el β-sitosterol.
Palabras clave: Annonaceae, Rollinia rufinervis, acetogeninas, leishmaniasis, β-sitosterol
ABSTRACT
In this study the bioactivity of the fractions obtained from the ethanolic extracts of the leaves, of the trunk bark and of the root bark of Rollinia rufinervis (Annonaceae) is evaluated. It is found that they show cytotoxic activity and that the presence of acetogenins can cause the antiparasitaire activity. The fractions are tested at concentration between 0.095 "g/mL and 100 "g/mL against promastigotes of Leishmania chagasi, evaluating the parasite mobility after 72 hours. The effect of the fractions is contrasted with the mediun Schneider- Drosófila without extract and with glucantime®, used as control. The Rollinia rufinervis fractions of: ethyl acetate of the root, petroleum ether of the bark, ethyl acetate of the bark and ethyl acetate of the leaves present leishmanicidal activity. The last fraction has the largest activity causing appreciable or total immobility of the parasites during the experiment. Probably ß-sitosterol is isolated from this fraction.
Keywords: Annonaceae, Rollinia, acetogenins, leishmaniasis, ß-sitosterol
INTRODUCCIÓN
La infección por leishmania tiene una distribución mundial: es encontrada en los cinco continentes; es una enfermedad endémica en las regiones tropicales y subtropicales en 88 países del mundo; se estima que hay 12 millones de casos distribuidos en el mundo; de 1,5 a 2 millones de nuevos casos ocurren cada año. La forma cutánea es la más común (1 a 1,5 millones de casos por año), representando del 50 al 75% de todos los nuevos casos, y 500.000 casos son de leishmaniasis visceral. Hasta la semana epidemiológica 53 del año 2003, se notificaron 9.615 casos de leishmaniasis en Colombia, de los cuales 9420 casos son de leishmaniasis cutánea que corresponden al 98%, la leishmaniasis visceral representa el 1% con 125 casos, y 70 casos son de la leishmaniasis mucosa. En Colombia la enfermedad afecta principalmente a los habitantes de los departamentos de Boyacá, Choco, Sucre, y Antioquia (1). En el departamento del Tolima se han reportado 20 casos de leishmaniasis visceral entre los años 2003- 2005 (2), situación que no deja de ser preocupante ya que la enfermedad se ha propagado por diferentes regiones del departamento del Tolima afectando comunidades de bajos recursos económicos y principalmente a los niños.
La infección es tratada comúnmente con antimonio pentavalente en la forma de stibogluconato de sodio (pentostam®) o antimiato de N-metilglucamina (glucantime®) y con pentamidina o anfotericna- B. Esas drogas son potencialmente tóxicas y generalmente administradas en hospitales (3). En las regiones endémicas, los tratamientos son llevados a cabo empleando la medicina popular aprovechando las propiedades farmacológicas de las biomóleculas presentes en los vegetales disponibles en la zona.
Entre los géneros pertenecientes a la familia Annonaceae que muestran una amplia actividad biológica (antitumoral, antiparasitaria, inmunodepresiva y pesticida) (4), gracias a la diversidad de metabolitos secundarios que poseen (acetogeninas, esteroles, sesquiterpenlactonas, quinonas y alcaloides entre otros) se encuentra el género Rollinia que comprende 65 especies alrededor del mundo (5). En Colombia se encuentran 11 especies entre ellas Rollinia rufinervis (6), de la cual no se encontraron reportes relacionado a la actividad leishmanicida en Leishmania chagasi. En el género Rollinia se encuentran diferentes tipos de metabolitos propios de la familia Annonacea como alcaloides y acetogeninas, a este ultimo grupo de compuestos se les atribuye diversas actividades biológicas, entre ellas la actividad antiparasitaria como lo reporta Cavé y colaboradores (4), al mencionar el aislamiento de acetogeninas de Annonaceas como uleicina de Rollina ulei, senegalene, squamocina y molvizarina de Annona senegalensis las cuales fueron efectivas contra la leishmaniasis.
Con la información aportada a esta investigación por los habitantes de las regiones endémicas del departamento del Tolima, se observó que diversas partes de las plantas de la familia Annonacea entre ellas las pertenecientes a los géneros Rollinia, Annona, Xylopia, son utilizadas de manera empírica para tratar fiebres, gripas y el cocimiento de la corteza y de las hojas la emplean para tratar la leishmaniasis. Los reportes en cuanto la actividad biológica y química del género Rollinia y los pocos estudios que se reportan de Rollinia rufinervis hacen de este vegetal una posible fuente de biomoléculas con actividad biológica.
La contribución de esta investigación fue evaluar la actividad leishmanicida en Leishmania chagasis de las fracciones bioactivas de diferentes partes de Rollinia rufinervis en las que se detectó la presencia de acetogeninas. Además se analizó la composición química de la fracción acetato de etilo de hojas utilizando pruebas químicas, físicas y espectroscópicas. Con ello se avanzó en el estudio de la flora Tolimense, se introdujo a Rollinia rufinervis al índice de especies de la familia Annonaceae con actividad leishmanicida, se mostró la presencia de acetogeninas y se encontró una nueva perspectiva terapéutica contra la leishmaniasis visceral usando fracciones provenientes de los extractos etanólicos de la planta estudiada.
MATERIALES Y MÉTODOS
Procedimientos experimentales generales
Los espectros ultravioleta fueron realizados en un espectrofotómetro Genesis 5. Los espectros IR se corrieron en un equipo Mattson Genesis UNICAM (FT-IR) utilizando un rango de barrido entre 4000 y 600 cm-1.
Material vegetal
La corteza de la raíz, las hojas y la corteza del tronco fueron colectadas en el bosque del municipio de Mariquita, Colombia, con una temperatura media de 26ºC y una altitud de 495 m.s.n.m (7). Los ejemplares colectados fueron confrontados con los depositados en el Herbario TOLI de la Universidad del Tolima (Código 2967).
Material Animal
La prueba citotóxica in vitro se realizó con nauplios maduros de Artemia salina cultivados bajo condiciones estrictas de salinidad 3.8% y temperatura de 25 a 28ºC. Para la prueba leishmanicida se utilizaron formas promastigotes de Leishmania chagasi obtenidas de la cepa MHOM/CO/84/Cl-044B aportadas por el Instituto Nacional de Salud (Bogotá D. C), conservadas y repicadas en el Laboratorio de Parasitología Tropical de la Universidad del Tolima (Ibagué) a una temperatura de 28ºC y a una altura de 1150 m.s.n.m.
Preparación de extractos
A la corteza de raíz, las hojas y la corteza del tronco previamente secas (30-50°C), se les redujo su tamaño de partícula en un molino THOMAS-WILEY, malla 2.0 mm y fueron sometidas separadamente a extracción continua por 48 horas en un soxhlet usando éter de petróleo de punto de ebullición entre 40°C- 70°C. El material vegetal así desengrasado se sometió a una extracción por lixiviación utilizando 250 cm3 de etanol a temperatura ambiente. El solvente se hizo circular por la muestra hasta saturación, después se realizó un proceso igual con otra porción fresca del solvente. El método se repitió hasta agotamiento de la muestra. Los extractos etanólico obtenidos de cada muestra se guardaron en frascos ámbar rotulados y se almacenaron en nevera a 5°C.
A cada extracto etanólico obtenido se le retiró totalmente el solvente y se le sometió a columna de cromatografía (60cm x 4cm) empacada con sílica gel 60F para cromatografía de columna (J.T. Baker), se adaptó a un equipo de vacío y se trató con tres solventes diferentes, el primero fué éter de petróleo, se continuó con acetato de etilo y por último se usó etanol. Las fracciones obtenidas fueron concentradas a presión reducida.
A cada una de las fracciones se les realizó un ensayo sobre CCD (cromatoplacas de sílica 60 GF254). Se utilizó como eluente diclorometano-acetato de etilo-metanol (50: 45: 5.) y como revelador ácido fosfomolíbdico y el reactivo de Kedde para identificar la presencia de las acetogeninas (8). Para detectar esteroles se utilizaron como eluentes: éter de petróleo, benceno, éter de petróleo- acetato de etilo (7:3), benceno-acetato de etilo (7:3), benceno-acetato de etilo (3:7), acetato de etilo, benceno-acetona (9:1) y se usaron como reveladores el Cloruro de Cobalto (CoCl2) y el Ácido sulfúrico 98% (H2SO4) (9).
BIOENSAYOS
Actividad citotóxica
En este ensayo se usaron larvas de Artemia salina y fue aplicado de acuerdo al protocolo reportado por McLaughlin (10).
Actividad leishmanicida
Las formas promastigote de Leishmania chagasi se obtuvieron de cepas cultivadas a 28°C en un medio Schneider-Drosófila, suplementado con suero fetal bovino (10%) inactivado a 56°C, durante 30 minutos. Dicha cepa fue repicada y conservada a 28ºC. Se utilizaron 2x106 promastigotes/mililitro para el ensayo biológico.
Las fracciones de Rollinia rufinervis fueron disueltas en un volumen conocido de dimetilsulfoxido (DMSO) y después en el medio Shneider-Drosofila. A partir de esta solución madre se hicieron soluciones a concentraciones entre 0.095ppm y 100ppm. El conteo se realizó a las 72 horas. Se determinó la actividad observando al microscopio la movilidad del parásito, buena movilidad (extracto no activo), movilidad media (extracto poco activo), baja movilidad (extracto activo) y ninguna movilidad (extracto muy activo). Se realizó la comparación con los controles sin extracto y con glucantime® como medicamento de referencia (11).
RESULTADOS Y DISCUSIÓN
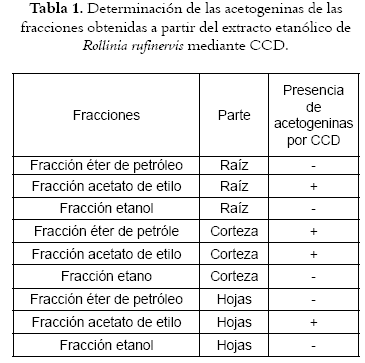
Las fracciones obtenidas a partir del extracto etanólico de las diferentes partes de Rollinia rufinervis (Annonaceae) fueron sometidas a pruebas de CCD para encontrar las fracciones que presentaron acetogeninas (véase tabla 1).
Las fracciones, acetato de etilo raíz, éter de petróleo de la corteza, acetato de etilo de la corteza y acetato de etilo de la hoja en las que se detectó la presencia de las acetogeninas fueron escogidas para realizar la prueba de citotoxicidad utilizando nauplios maduros de Artemia salina.
Actividad citotóxica
Para el ensayo de citotoxicidad se hizo un análisis univariado de varianza (ANOVA) a través de cuatro extractos a cuatro concentraciones, y se estimo la concentración letal media (LC50) (véase tabla 2).
El análisis univariado en este caso es débil ya que se han generado intervalos de confianza muy amplios, y se observan valores de LC50 que tienden a ser altos puesto que la dosis mayor es un valor atípico. De acuerdo a este resultado se pueden sugerir intervalos de concentración constantes para mejorar la consistencia en la respuesta, ya que se observa que las fracciones obtenidas manifiestan actividad frente al organismo. Para estudiar el comportamiento de forma simultanea de las cuatro fracciones obtenidas de la misma planta, se hizo un análisis multivariado de varianza (MANOVA), mediante el cual se estableció a través de la prueba F (P<0.05) que la muerte de los organismos es debido a las biomoléculas presentes en las fracciones y no a causas aleatorias. Por el contrario el valor F (P>0.05) para el blanco indica que el promedio de nauplios muertos no es significativo y que obedece solo a causas aleatorias.
Se realizó el análisis de componentes principales el cual permitió establecer que el factor F1 (Dosis) aporta porcentualmente mayor varianza que el factor F2 (Blanco), esto se puede apreciar en las dosis 100 y 1000 ppm las cuales están aportando en varianza un porcentaje a F1 de 38.45% y 38.18% respectivamente; lo que indica que al hacer aplicaciones de 100 o 1000 ppm de las fracciones, estas ejercen una misma acción biológica. De acuerdo al análisis de componentes principales se podrá encontrar a una concentración de 100 ppm o por debajo de ella una acción biológica causada por los metabolitos secundarios presentes en la planta. Por tal motivo se decidió estimar el intervalo de concentraciones de cada una de las fracciones para el ensayo leishmanicida entre 0.095 y 100 ppm.
Los resultados del ensayo se analizaron a través de los paquetes estadísticos MINITAB-13 y SPSS 9.0.
Actividad leishmanicida
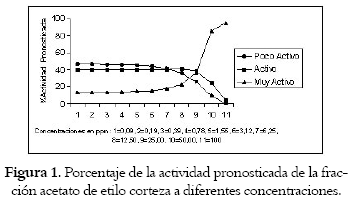
Teniendo en cuenta la presencia de acetogeninas y la citotoxicidad de las fracciones se evaluó la actividad leishmanicida sobre promastigotes de Leishmania chagasi, la actividad antiparasitaria permitió establecer notorias diferencias entre la perdida del movimiento del parasito ocasionada por los metabolitos secundarios presentes en las diferentes fracciones a través de las concentraciones estimadas. El análisis para las fracciones: acetato de etilo corteza, acetato de etilo raíz, éter de petróleo corteza, se realizó mediante el programa estadístico STATGRAPHICS 5.0 a través del cual se desarrollo el modelo de regresión logística multinomial. Este modelo utilizó el estadístico de prueba (Logaritmo de máxima verosimilitud) el cual permitió establecer la idoneidad del modelo (P>0.05), además se reveló que existe una relación significativa entre la variable independiente (dosis) y la actividad del extracto sobre el movimiento del parásito, esto es confirmado por el estadístico de prueba del Wald (P>0.10). El porcentaje de ocurrencia de la actividad biológica originada por la fracción acetato de etilo corteza dada a diferentes concentraciones es de activo con una probabilidad de ocurrencia aproximadamente del 40% a lo largo del experimento, volviéndose muy activa en las tres concentraciones más altas (25 "g/mL, 50 "g/mL y 100 "g/mL) en las cuales el parásito pierde su movimiento (veáse figura 1).
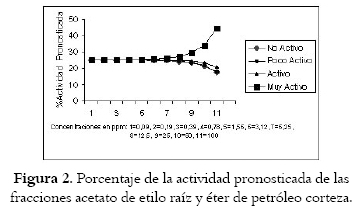
El análisis estadístico hecho por separado a las fracciones acetato de etilo raíz y éter de petróleo corteza, muestra que el efecto de estas fracciones sobre el comportamiento del organismo a lo largo del experimento es igual a pesar de ser fracciones obtenidas de diferente parte de la planta. La actividad pronosticada para las fracciones antes mencionadas dejan ver que a concentraciones inferiores a 12.5 "g/mL no se presenta actividad significativa sobre el organismo, por el contrario las fracciones se hacen muy activas en las concentraciones más altas (12.5 "g/mL, 25 "g/mL, 50 "g/mL y 100 "g/mL) en las cuales se observa que el organismo pierde su movimiento (véase figura 2). De acuerdo a la similitud de la actividad biológica es posible que las acetogeninas de anonáceas presentes en la raíz y en la corteza sean las mismas, causando efecto sobre promastigotes de Leishmania chagasi.
La fracción acetato de etilo-hoja la cual presentó dos actividades (Activo y Muy activo), se analizó estadísticamente a partir del modelo de regresión logística binomial, que utilizó como estadístico de prueba un Chi-Cuadrado que con un P>0.05 permitió establecer la idoneidad del modelo. Al aplicar la fracción acetato de etilo hoja los parásitos pierden su movimiento haciéndose esto más notable a medida que se incrementa la concentración a partir de 1.56 μg/mL hasta 100 μg/mL. El análisis binomial permitió establecer que al encontrarse una probabilidad estimada por encima de 0.5 durante el experimento es decir P (X=i) = 0.5, la fracción tiende a ser muy activa inhibiendo completamente el movimiento del parasito. El pronóstico de ocurrencia de la fracción acetato de etilo hoja sobre los promastigotes de Leishmania chagasi está entre lo activo y lo muy activo, lo que ha demostrado una actividad equivalente o mejor que el glucantime®, medicamento de referencia.
El efecto leishmanicida de las diferentes fracciones obtenidas de Rollinia rufinervis puede ser atribuido a las acetogeninas de Annonaceas entre ellas rolliniastatina, esquamosina (12), annonacina (13) entre otras. Por tal motivo el resultado obtenido en esta investigación es comparable con investigaciones adelantadas por otros autores en géneros pertenecientes a esta familia.
La actividad antiparasitaria en Leishmania chagasi, aunque fue adelantada en formas promastigotes del parásito las cuales se presentan en el tubo digestivo del vector y no en los macrófagos como sucede con los amastigotes que causan la destrucción de la célula, no deja de ser importante, ya que los efectos experimentales observados posiblemente sean semejantes en la forma amastigota, a causa de los metabolitos secundarios presentes en las fracciones activas, especialmente por las acetogeninas de Annonaceas que tienen acción comprobada sobre el sistema mitocondrial que es común en las dos formas del parásito (14,17 ).
Identificación del compuesto aislado
Las pruebas químicas, físicas y espectroscópicas adelantadas al compuesto aislado de la fracción acetato de etilo hoja coinciden con el patrón (Sigma Chemical Co. N° S-5753) del ß-sitosterol (véase tabla 3).
El compuesto aislado tiene un punto de fusión (134°C) que coincide con el del β-sitosterol, además al mezclar el compuesto con el β-sitosterol el punto de fusión no mostró depresión apreciable. La solubilidad del compuesto aislado en los solventes utilizados es igual a lo observado con el patrón.
En las pruebas químicas de Liberman- Bourchard y de Salkowsky, el compuesto se comporta de la misma manera como lo hacen muchos triterpenos y esteroles en especial el β-sitosterol, esto se acompaña con la prueba de Bromo que confirma la presencia de dobles enlaces (18 ).
Para el análisis en CCF el compuesto presentó un Rf que no presenta diferencia significativa con el β-sitosterol. Estos resultados se acompañan de las bandas observadas en el IR caracteristicas de los esteroles así: para OH (3363-3400 cm-1) y para C=C (1601 cm-1) y la banda de 2928 cm-1 para el C- H alifático. Las dos bandas a 1448 y 1267.73 cm-1 son características del β-sitosterol y corresponden a torciones de los enlaces C-H en los grupos -CH2 - y (C(CH3)2) (18 ).
Los anteriores datos nos permiten proponer que el compuesto aislado es el β-sitosterol, faltando el análisis de Resonancia Magnética Nuclear que con- firmaría la presencia de este compuesto en Rollinia rufinervis y seria un aporte de esta investigación al estudio fitoquímico de este vegetal.
Nuestros resultados se convierten en la base para adelantar estudios farmacológicos que permitan evidenciar el poder terapéutico de las fracciones de Rollinia rufinervis contra la leishmaniasis visceral. Además sería conveniente realizar estudios sobre formas amastigotes, evaluando el número de organismos muertos a causa de las fracciones a diferentes concentraciones, para garantizar un mejor resultado de la actividad antiparasitaria que posiblemente generan las acetogeninas de Rollinia rufinervis.
Esta investigación se convierte en el punto de partida para identificar las acetogeninas de Annonaceas en esta especie que posiblemente causen el efecto antiparasitario y determinar si su acción se acentúa cuando se realiza la aplicación de las acetogeninas separadamente o en su defecto actúan todas ellas de manera sinérgica. En términos generales se podría abrir una posibilidad de trabajo científico tendiente a solucionar la problemática de salud pública que origina la leishmaniasis en habitantes del departamento del Tolima.
AGRADECIMIENTOS
Los autores agradecen la financiación otorgada por el Comité Central de Investigaciones de la Universidad del Tolima y a entidades públicas como la Secretaría de Salud del Tolima quienes nos proporcionaron el medicamento de referencia y al Instituto Nacional de Salud Pública quien nos facilitó la cepa de Leishmania chagasi.
También agradecemos al profesor Octavio Rojas por su colaboración en el análisis estadístico y a las profesora Amparo Viña y Yolanda Flórez por sus aportes.
REFERENCIAS BIBLIOGRÁFICAS
1. Instituto Nacional de Salud. Sistema Nacional de Vigilancia en Salud Pública (SIVIGILA). Boletín epidemiológico. [Sitio en Internet]. Disponible en: http://www.col.ops-oms.org/sivigila/2004/BOLE10_04.htm. Consultado: 12 de noviembre de 2004. [ Links ]
2. Instituto Nacional de Salud. Sistema Nacional de Vigilancia en Salud Pública (SIVIGILA). [Sitio en Internet]. Disponible en: http://www.ins.gov.co/vigilancia/nivel2.php?seccion=28#. Consultado: Junio 20 de 2004 [ Links ]
3. Fournet A, Angelo A, Muñoz V, Roblot F, Hocquemiller R, Cave A. Biological and chemical studies of Pera benensis, a Bolivian plant used in folk medicine as a treatment of cutaneous leishmania. J Ethnopharmacol. 1992; 37(2):159-164. [ Links ]
4. Cavé A, Cortés D, Figadére B, Laurens A. Acetogenins from Annonaceae. Nueva York: Springer-Wien; 1997. [ Links ]
5. Do Nascimento F, Diamantino MA, Assunção AC, Santos LP. Acetogeninas de Anonáceas isoladas de Folhas de Rollinia laurifólia. Quim Nova 2003; 26(3):319-322. [ Links ]
6. Montoya G, Osorio E, Jiménez N. Actividad captadora de radicales libres de alcaloides de Rollinia pittieri (Annonaceae) por el método del DPPH. Vitae 2004; 11 (2): 52-53. [ Links ]
7. Gobernación del Tolima. El Tolima y sus Municipios. Ibagué: El Boga; 1990. [ Links ]
8. Ruppercht JK, Hui YH, McLaughlin JL. Annonaceous acetogenins: a review. J Nat Prod 1990; 53(2):237-278. [ Links ]
9. Domínguez X. Métodos de investigación fitoquímica. México: Limusa; 1998. [ Links ]
10. Mc. Laughlin J, Colman-Saizarbitoria T, Anderson J. Tres bioensayos simples para químicos de productos naturales. Revista de la sociedad venezolana de química1. 1995; 18:14-15. [ Links ]
11. Fournet A, Angelo A, Muñoz V, Hocquemiller F, Roblot F, Cave A, et al. Antiprotozoal activity of quinoline alkaloids isolated from Galipea longiflora, a bolivian plant used as a treatment for cutaneous leishmaniasis. Phytother Res. 1994; 8(3):174-178. [ Links ]
12. Organic acids, lipids and acetogenins. [Sitio en Internet]. Disponible en: http://www.userpage.fuberlin.de/~kayser/lipds_and_aliphaticcompounds.htm. Consultado: agosto de 2004
13. Jaramillo MC, Arango GJ, González MC, Robledo SM, Velez ID. Cytotoxicity and antileishmanial activity of Anona muricata pericarp. Fitoterapia. 2000; 71(2):183-186. [ Links ]
14. Zafra-Polo C, Figadére B, Gallardo T. Natural Acetogenins from Annonaceae, síntesis and mechanisms of action. Phytochem. Anal. 1998; 48:1087-1117. [ Links ]
15. Tormo J, González C, Cortes D., et al. Characterization of mitochondrial complex I inhiditods using Annonaceus Acetogenins. Biochem Biophys Res Commun 1999; 369:119-126. [ Links ]
16. Motoyama T, Yabunaka H, Miyoshi H. Essential structural factors of acetogenins, potent inhibitors of mitochondrial complex I. Bioorg Med Chem Lett. 2002; 12(16): 2089-2092. [ Links ]
17. Yabunaka H, Abe M, Kenmochi A, Hamada T, Nishioka T, Miyoshi H. Synthesis and inhibitor with bovine mitochondrial complex I. Bioorg.Med. Chem.Lett. 2003; 13(14): 2385-2388. [ Links ]
18. Tenorio JL. Estudio Químico de Isertia pitteri standi II (Jaboncillo). Universidad del Tolima. Facultad de Ciencias. Departamento de Química, p 15-84. 1992. [ Links ]