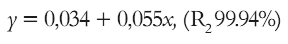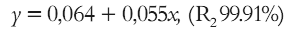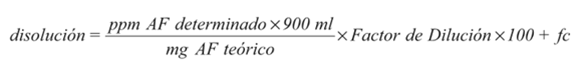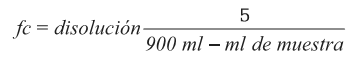Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Vitae
Print version ISSN 0121-4004
Vitae vol.16 no.1 Medellín Jan./Apr. 2009
PRODUCCIÓN FARMACÉUTICA
Desarrollo y caracterización de micropartículas de ácido fólico formadas por secado por aspersión, utilizando goma arábiga y maltodextrina como materiales de pared
Development and characterization of folic acid microparticles formed by spray-drying with gum arabic and maltodextrin
Seneida M LOPERA C.1; Cielo GUZMÁN O. 1; Carlos CATAÑO R.1; Cecilia GALLARDO C.1*
1Grupo de Estudios de Estabilidad de Medicamentos, Cosméticos y Alimentos. Facultad de Química Farmacéutica, Universidad de Antioquia. Calle 67 Nº 53-108, Bloque 2, A.A. 1226. Medellín, Colombia
RESUMEN
El ácido fólico es una vitamina esencial, que participa en la biosíntesis de aminoácidos esenciales y en algunos procesos asociados al ADN. Es una vitamina con limitaciones en su estabilidad frente a factores como la luz, pH y oxígeno. Por esta razón se hace necesario desarrollar estrategias que permitan su estabilización sin afectar su actividad biológica. Así pues, se propone la obtención de micropartículas utilizando mezclas de goma arábiga y maltodextrina, con el método de secado por aspersión, que presenten características adecuadas para actuar como un reservorio del ácido fólico con potencialidades para su estabilización. En este estudio se obtienen micropartículas de ácido fólico utilizando cuatro mezclas diferentes de goma arábiga y maltodextrina, caracterizadas mediante los siguientes parámetros: distribución de tamaño de partícula, porcentaje de humedad, morfología, eficiencia de encapsulación y perfil de disolución. Los resultados de la caracterización muestran diferentes aspectos: la morfología de las micropartículas obtenidas por este método varía con la relación goma arábiga- maltodextrina, la eficiencia de encapsulación es elevada para los cuatro tipos de micropartículas estudiadas, la distribución de tamaño de partícula no cambia con la relación de los materiales de la pared y los perfiles de disolución muestran un porcentaje de disolución limitado, siendo el mejor el que corresponde a micropartículas con la relación goma arábiga- maltodextrina 70-30. La goma arábiga es efectiva para el atrapamiento del ácido fólico y cuando se mezcla con maltodextrina se mejoran las características de morfología, eficiencia y disolución de las micropartículas, lo cual sugiere que existe una mezcla óptima de los dos materiales de pared que optimizan las características de las micropartículas.
Palabras clave: ácido fólico, micropartículas, goma arábiga, maltodextrina.
ABSTRACT
The folic acid is an essential vitamin, it is involved in the essential aminoacids biosynthesis and some process associated to DNA. Folic acid undergoes degradation reactions when is exposed to light, acid or alkaline medium and oxygen atmosphere. For this reason it is necessary to develop strategies to improve its stability not affecting its biological activity. In this connection the obtaining of microparticles by spray drying, using arabic gum and maltodextrin blends is proposed. The microparticles could act as a carrier of folic acid providing it protection. In this study, microparticles of folic acid were obtained using four different blends of arabic gum and maltodextrin. The particles size distribution, morphology, encapsulation efficiency and dissolution profile were assessed for the different types of microparticles. The results showed different aspects: the microparticles morphology changed with the ratio arabic gum - maltodextrine, the encapsulation efficiency was high for four types of studied microparticles, the particles size distribution did not change with the wall materials ratio, the dissolution profiles showed a limited dissolution percentage, and microparticles of arabic gum-maltodextrin 70-30 showed the best profile. The arabic gum favored the encapsulation of folic acid and when it is mixed with maltodextrin the morphology, encapsulation efficiency and dissolution improved. Probably there is an optimum ratio of two wall materials providing optimum properties to microparticles.
Keywords: folic acid, microparticles, arabic gum, maltodextrin.
INTRODUCCIÓN
El ácido fólico (ácido N-[4-[(2-amino-3,4-dihidro-4-oxo-6-pteridinilmetil)-amino]-benzoil] L- ácido glutámico), pertenece al grupo de compuestos conocidos como folatos (del latín folium: hojas). Es una vitamina esencial para los seres vivos, actuando como un cofactor en reacciones de transferencia de carbono (formilo, hidroximetilo y metilo), necesarias para la biosíntesis de nucleótidos (bases purinas y pirimidinas), metabolismo de aminoácidos (metionina, histidina), metabolismo de neurotransmisores (serina, colina), etc (1,2). Los animales y humanos no pueden sintetizar folatos. Por eso es necesario incorporarlos dentro de la dieta a partir de fuentes vegetales o mediante la fortificación de alimentos usando el ácido fólico que corresponde a la forma sintética de los folatos. La deficiencia de ácido fólico en la dieta está relacionada con defectos del tubo neural, enfermedades coronarias y anemia megaloblástica (3).
El ácido fólico (AF) presenta reacciones de degradación de fotólisis e hidrólisis, mediante ruptura del enlace amídico (C9 y N10), dando lugar a 2-amino-4-hidroxi-6-formil-pterina (6-FPT) y p-aminobenzoil-L-acido glutámico (PABG); en la reacción de fotólisis se da lugar a reacciones secundarias donde el 6-FPT es oxidado al correspondiente 6-ácido carboxílico (6-CBPT), y éste posteriormente sufre descarboxilación formando 2- amino-4-hidroxi-pteridina (4,5,6).
Ninguno de los compuestos de degradación presenta actividad biológica; por tanto, durante la formulación de productos farmacéuticos, nutracéuticos o alimentos enriquecidos con AF se hace necesaria la protección del AF ante factores ambientales como la luz y factores de formulación como medios ácidos y medios básicos. La microencapsulación es una alternativa para proteger principios activos lábiles, entre ellos las vitaminas, tanto liposolubles como hidrosolubles (7,8), ya que en las micropartículas el principio activo está confinado dentro de una matriz polimérica constituyendo una barrera física a los factores ambientales y a los de formulación (9).
El AF también puede ser protegido de las interacciones con otras vitaminas por medio de la microencapsulación. Es conocido que el AF es degradado mas rápidamente cuando la riboflavina está presente en la formulación, lo cual se ha explicado por el efecto fotosensibilizante característico de la riboflavina (4).
Existen diferentes técnicas para obtener micropartículas. La mas viable, económica y ampliamente usada por la industria de alimentos es la técnica de secado por aspersión (10). Esta técnica consiste en la adición del principio activo a una dispersión de un polímero formador de pared y un solvente (generalmente agua), formando un sistema fluido, que luego es bombeado a una cámara de aspersión, donde el fluido es atomizado y por acción del aire en circulación, a una temperatura de 150 - 200°C, se produce la eliminación del disolvente y la formación de las micropartículas (11).
Entre los materiales formadores de pared mas frecuentemente usados en la técnica de secado por aspersión se encuentran las gomas (arábiga, carragenina, mesquita, gellan); proteínas (gelatina, caseinato); almidones modificados y maltodextrinas.
La goma arábiga (GA) es un biopolímero obtenido del exudado del árbol acacia, de la familia Leguminosae, originaria de Egipto y de uso milenario. Actualmente es extraída y pulverizada con procesos limpios, a partir de diversas especies de acacia, predominando las especies senegal y seyal. Esta goma ha sido evaluada y reconocida como aditivo alimentario por el Equipo de Expertos del Comité Aditivos Alimentarios -JECFA-del Codex Alimentarius.
La estructura química de la GA corresponde a un complejo polisacárido que contiene pequeñas cantidades de material nitrogenado. El polisacárido es una cadena ramificada, con un peso molecular que puede variar de 47.000 a 3.000.000 g/mol (12). La cadena lineal está compuesta de unidades (1,3) β-D galactopiranolsil y ramificaciones a los lados de (1,6) β-D galactopiranolsil-4 -O metil-glucurónico, las cuales, a su vez, están unidas a ramas más pequeñas compuestas por L- ramnosa - D-acido glucurónico, D- galactosa - (1,3) y L- arabinosa y L- arabinosa (1,3) - L-arabinosa (1,3) L-arabinosa. El material nitrogenado es de carácter proteico, corresponde hasta al 10% del peso total, y en particular en las especies senegal y seyal está alrededor del 2% (13). Por esta razón se ha denominado a la GA como complejo proteico-arabinogalactano. La fracción proteica está constituida por 400 residuos aminoacídicos, con 18 aminoácidos diferentes, de los cuales el 50% corresponde a hidroxiprolina, serina y prolina, y se considera que muy probablemente la unión al polisacárido se presenta por la vía hidroxiprolina unida a residuos de arabinosa (14). La GA o complejo proteico-arabinogalactano, por sus características estructurales presenta un carácter amfifílico, lo que le permite absorber en superficies lipofílicas, actuar como coloide protector y, por ende, como un buen agente formador de películas (15); adicionalmente, presenta baja viscosidad y comportamiento newtoniano a concentraciones inferiores al 35%. En efecto, la GA es uno de los materiales formadores de película más efectivo para microencroencapsular; sin embargo, el costo y su limitada disponibilidad comercial, han restringido su uso a nivel industrial (16).
Por su parte, la maltodextrina (MD) es un polisacárido con un peso molecular promedio de 1800 g/mol (17), no edulcorante, con un aporte nutricional de 4 calorías por gramo, obtenido de la hidrólisis parcial, ácida y/o enzimática del almidón de papa, arroz o maíz. Ha sido reconocida por la FDA como sustancia GRAS (generally recognized as safe). Su composición química consiste en unidades de D-glucosa unidas con enlaces α(1-4) y con un bajo número de enlaces α-(1,6) en posición aleatoria (18). Se caracteriza por tener entre 2 y 20 equivalentes de dextrosa (DE). Se ha determinado que para microencapsulación son mas efectivas las MD con 10-20 equivalentes de dextrosa. La aplicación de la MD en el proceso de encapsulación está asociada a la baja viscosidad a altos contenidos de sólidos, buena solubilidad, capacidad de formar películas y bajo costo (19).
Una alternativa para la encapsulación de principios activos mediante el secado por aspersión, es la utilización de mezcla con hidrocoloides sinergistas, como la goma arábiga y la maltodextrina, ya que permiten compensar el alto costo de la GA y la deficiente actividad interfacial que presenta la MD.
El objetivo de este trabajo fue evaluar la morfología, eficiencia de encapsulación y perfil de disolución del AF a partir de micropartículas obtenidas usando mezclas binarias de GA y MD en cuatro proporciones diferentes.
MATERIALES Y MÉTODOS
Materiales
Para los ensayos de microencapsulación se usó Acido Fólico calidad materia prima farmacéutica, y para los ensayos cuantitativos un estándar secundario de AF. La goma arábiga y la maltodextrina usadas fueron grado alimenticio. El ácido cítrico, el citrato de sodio, el cloruro de potasio, el fosfato de potasio monobásico, el hidróxido de sodio y el ácido clorhídrico fueron adquiridos de Merck. Para todos los ensayos se usó agua purificada.
Preparación de micropartículas por el método de secado por aspersión
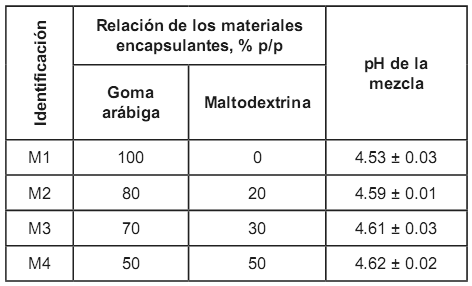
Se preparan inicialmente cuatro suspensiones en cuya composición se mantuvo constante el porcentaje de AF (1% p/p), de agua (66%) y el porcentaje total del material encapsulante (33%), y solo se modificó la relación de los dos materiales encapsulantes, goma arábiga y maltodextrina, en las relaciones que se muestran en la tabla 1. El peso total de cada suspensión preparada fue de 6.065 kg en promedio.
Las suspensiones se prepararon pesando y dispersando los materiales goma arábiga y maltodextrina en agua destilada usando un agitador de hélice (Heidolph®) a 1700 rpm± 300 y 29.52 ± 1.92ºC, durante una hora. Luego se adicionó el AF previamente disperso en agua destilada, y se continuó agitando durante 30 min adicionales. La viscosidad y el pH de la dispersión formada fueron medidos usando un viscosímetro Brookfield® y un pHmetro Methrom®.
Las micropartículas fueron obtenidas secando la suspensión en un secador por aspersión (Niro FU11 model Atomizer) equipado con una boquilla de 0.5 mm de diámetro. La velocidad rotacional fue controlada a 18000 rpm ± 600 y las partículas al salir presentaron una velocidad lineal de 100 a 150 m/s. La temperatura de entrada y salida del secador fue mantenida a 220±5 y 105±10 ºC, respectivamente. La velocidad de alimentación del sistema aspersor fue de 3.3 L/min. Las micropartículas obtenidas fueron colectadas en bolsas de polietileno y almacenadas en cajas de cartón corrugado, observando las buenas prácticas de almacenamiento que la empresa exige en su sistema de control de calidad.
Evaluación del tamaño de la partícula
La distribución del tamaño de las micropartículas fue determinada usando un analizador de tamaño de partícula (MasterSizer 2000, Malvern), usando como accesorio Hydro 2000S(A), obscuración de 6.99%, y se usó agua como agente dispersante para la preparación de la muestra, a una concentración de 0.0023 % p/v. La temperatura de lectura fue 18ºC± 3, se realizaron dos barridos de 106 medidas cada uno, con capacidad de medir un rango ponderado de 0.020 a 2000.000 μm. Se calculó previamente el índice de refracción del agua y del AF.
Determinación de humedad de las micropartículas
Se aplicó el método NTC 529-ISO 712, con principio de secado en estufa (Marca Binder) a una temperatura 130ºC ± 3, con una cantidad de muestra de 5g ±1, la cual fue sometida al secado durante 120 minutos. Seguidamente se introdujo en un desecador durante 30 minutos y luego fue pesada en balanza analítica. El ensayo se realizó por triplicado.
Evaluación de características morfológicas
La estructura de las macropartículas fue evaluada usando microscopía electrónica de barrido (SEM-JSM 5800). Las muestras fueron fijadas a cilindros metálicos por adhesión con cinta de doble faz, luego llevadas a un secador, con la técnica de punto crítico con CO2, a una temperatura cercana a 40ºC, seguida de un recubrimiento con una mezcla oro/platino, procedimiento que se realizó durante 60 minutos. Seguidamente los cilindros que contenían la muestra se llevaron a la cámara de muestras del microscopio. El análisis se efectuó a 12-15Kv de voltaje de aceleración.
Método analítico de determinación del ácido fólico
El AF fue cuantificado midiendo la absorbancia a 280 nm, usando un espectrofotómetro (UV-1601, Shimatzu®). El método fue previamente validado en los parámetros de linealidad, exactitud y precisión en el rango de 5.28-36 ppm.
El proceso de extracción del AF se hizo pesando una cantidad exacta del granulado y adicionando 50 mL de buffer citrato, 0.05 M (pH 5.0), se sometió a calentamiento a 40±0.5ºC por 15 min en baño maría, luego a sonificación en un baño ultrasónico durante 20 min, y finalmente se filtró usando membranas Millipore 0.45μm.
Determinación de la eficiencia de encapsulación
La eficiencia de encapsulación se calculó usando la siguiente ecuación:
Ecuación 1.
Para la determinación del AF encontrado, se pesaron analíticamente 46 mg de micropartículas (conteniendo teóricamente 1.5 mg of AF), se aplicó el método de extracción y el filtrado resultante se analizó por espectroscopia UV a 280 nm y se calculó el % de eficiencia de encapsulación aplicando la ecuación 1. Se realizaron 5 réplicas para cada tipo de micropartículas y la comparación de la eficiencia obtenida con las diferentes mezclas, se estableció usando un modelo de 1 factor con efectos fijos, completamente aleatorizado. El nivel de confianza fue del 95% y la potencia para detectar diferencias significativas, del 90%.
Determinación del perfil de disolución
Para evaluar el perfil de disolución de las micropartículas se utilizó un disolutor (Disolutor SR2- Dissolution Test Station- Hanson Research con 6 vasos). Este ensayo fue desarrollado siguiendo directrices de la USP 31 NF 26 (20), con algunas modificaciones para el tipo de muestra a ensayar.
Como soluciones modelo de fluidos gástrico e intestinal, se prepararon buffer de HCl 0.2 M (pH 1.20±0.05) y fosfato 0.2 M (pH 7.20±0.05) respectivamente, y con estas soluciones se llenaron los vasos del disolutor (900 mL en cada vaso).
Se pesaron 700 mg de micropartículas, equivalentes teóricamente a 20 mg de AF, se envasaron en bolsas de celulosa tipo infusión, las cuales fueron posteriormente selladas y colocadas dentro de las canastillas malla nº 40 del disolutor. El ensayo se llevó a cabo a 75±5 rpm y a 37±1 ºC. Se aplicó un muestreo sin reposición, se extrajeron alícuotas de 5 mL usando una jeringa equipada con un microfiltro con intervalos de 10 minutos y cada alícuota fue analizada por espectrofotometría, midiendo la absorbancia a 280 nm.
Para obtener el perfil de disolución se obtuvieron los valores promedio en cada intervalo de las tres réplicas analizadas para cada tipo de micropartícula y los cálculos se efectuaron en base a una curva de calibración obtenida usando soluciones de AF en el rango 2 - 14.5 ppm a pH 1.2, y 1-20 ppm a pH 7.2.
RESULTADOS Y DISCUSIÓN
Se seleccionaron la GA y MD como materiales formadores de pared, por tener gran aplicación industrial y haber sido reportados como los de mayor utilización en la microencapsulación por secado por aspersión (21); ademàs, son aprobados para la industria de alimentos y resultan más económicos que otros, como alginatos y caseinatos.
Los porcentajes en la composición de las mezclas binarias se seleccionaron teniendo en cuenta que para la formación de micropartículas es fundamental el carácter amfifílico de la GA, por tanto, ésta se mantuvo en concentraciones considerables para favorecer la difusión de GA en la interfase sólido-líquido (21), y por otra parte, también se ha encontrado que la eficiencia de encapsulación y morfología de micropartículas se optimiza cuando el porcentaje de MD es superior a 50% (12).
Un aspecto fundamental que debe tenerse en cuenta durante el desarrollo de las micropartículas es la solubilidad del AF en medio acuoso. Algunos autores clasifican al AF como una vitamina hidrosoluble (2), mientras que otros reportan una solubilidad de 1.6 mg L-1 a 25°C (0.16%) (22, 23), lo cual corresponde a una ligera solubilidad, según la terminología usada en la USP y se reporta que el AF solamente es soluble en soluciones ácidas y alcalinas diluidas (24,25).
Dada esta baja solubilidad, cuando el AF es adicionado a la dispersión inicial del material encapsulante, a una concentración del 1% (0.023 M), se forma una suspensión. Los materiales encapsulantes aportan viscosidad a la suspensión. Las cuatro suspensiones preparadas presentaron viscosidades de 350± 20 cP, la cual fue lo suficientemente alta para estabilizar el sistema minimizando la velocidad de sedimentación, evitando la formación de agregados de AF durante el proceso de microencapsulación que tuvo una duración de una hora, y lo suficientemente baja para permitir el traslado de las suspensiones desde el mezclador hasta el secador.
Los valores de pH de las cuatro suspensiones se muestran en la tabla 1. En ella se observa que el pH disminuye cuando el porcentaje de GA incrementa, lo cual es un resultado esperado dado que la GA se comporta como un polisacárido aniónico por la presencia de ácido glucurónico en su estructura (26), mientras que la MD es un polímero neutro. Los valores de las dispersiones obtenidos son cercanos a los valores de pH de una dispersión de GA, el cual es cercano a 4.5 (27).
Tabla 1. Descripción de las mezclas de materiales encapsulantes y su pH
El porcentaje de humedad en las micropartículas fue 1.69±0.04, 1.87±0.02, 1.99±0.04 y 2.65±0.01 para los ensayos M1, M2, M3 y M4, respectivamente; con este porcentaje de humedad no se favorecen fenómenos de agregación y apelmazamiento durante el almacenamiento, según observaciones experimentales a nivel industrial. El porcentaje de humedad incrementa con el incremento del porcentaje de MD, la cual, como cualquier derivado de almidón, presenta una notable capacidad para atrapar y enlazar moléculas de agua a través del grupo hidroxilo.
La cantidad obtenida fue de 1.8±0.2 Kg para cada ensayo, el rendimiento fue de 89.5±0.5%, y la concentración teórica de AF microencapsulado, de 3.3% p/p.
Evaluación de las características morfológicas de las micropartículas
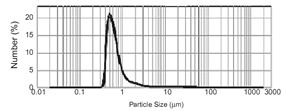
Las micropartículas obtenidas presentaron un color amarillo y su apariencia correspondía a un sólido pulverizado. En la figura 1 se encuentran superpuestos los perfiles de distribución de tamaño de partícula para los cuatro tipos de micropartículas estudiadas, donde el tamaño de partícula se encuentra en el rango 0.2-4 μm, con un promedio de 0.5 μm para los cuatro tipos de micropartículas. Estos resultados permiten concluir que la naturaleza del material encapsulante no influyó en el tamaño de las micropartículas, éste está influenciado por variables de operación del equipo como la velocidad de rotación del atomizador, la cual fue controlada en 18000 rpm para los cuatro tipos de micropartículas. La temperatura de entrada del aire también tiene efectos en la morfología de las micropartículas, y a valores bajos, menores de 150ºC, puede afectar las interacciones partícula-partícula, la flotabilidad y el contenido de humedad final, produciendo aglomeraciones y partículas de mayor tamaño. En el ensayo se trabajó con temperaturas de 220ºC, reportadas como típicas para este tipo de experimento. Igualmente el tamaño de partícula puede aumentar cuando no se controlan variables del proceso como la viscosidad y la velocidad de alimentación de la dispersión (8).
Figura 1. Superposición del análisis de distribución de tamaño de partícula de los cuatro tipos de micropartículas obtenidas.
La morfología y la superfície de las micropartículas fueron evaluadas con imágenes obtenidas por microscopia electrónica de barrido. En la figura 2 se observa una diferencia notable en las micropartículas obtenidas usando como material de pared GA 100%, y las obtenidas con GA-MD 50-50. Las primeras presentan forma irregular y una superfície contraída, con pliegues (Véase figura 2a), mientras que las obtenidas usando como encapsulante mezclas de GA-MD 50-50 presentan forma esférica, con superficie lisa, pero agrietada (Véase figura 2b).
Figura 2. Micrografías de micropartículas de AF por microscopía electrónica de barrido usando una amplificación de 3000 y 7500. Materiales de pared (a) GA:MD (100-0), (b) GA:MD (50-50).
La superficie de las micropartículas de GA se debe probablemente a las propiedades plásticas predominantes en la GA sobre las propiedades vítreas, dado que durante el proceso de secado por aspersión se producen contracciones de las partículas durante las etapas de secado y enfriamiento, la plasticidad de la GA da lugar a pliegues sobre la superficie de las partículas y se previene el agrietamiento de la pared. (28,29)
Las propiedades de superficie de las micropartículas que contenìan como material de pared MD, se deben a las propiedades vítreas de esta, y por lo tanto, durante el secado la pared de MD se opone a los fenómenos de contracción y trata de formar estructuras esféricas (30). Con la combinación de GA y MD se obtienen micropartículas con formas tanto esféricas como irregulares, se encuentran micropartículas fracturados que muestran una cavidad en el centro y se observan fragmentos de pared de gran espesor que sugieren que una doble pared es formada, presentando la pared interna una apariencia flexible, sin rupturas y con pliegues, mientras que la pared externa es lisa y quebradiza, como se observa en la figura 3.
Figura 3. Micrografías de micropartículas de AF por microscopía electrónica de barrido. Materiales de pared (a) GA:MD (100%-0%), (b) GA:MD (80%-20%), (c) GA:MD (70%-30%), (d) GA:MD (50%-50%).
Es posible explicar la doble pared formada, desde la disposición de los hidrocoloides en la suspensión inicial. La GA podría estar absorbida en la interfase sólido-líquido, orientando su pequeña fracción proteica a la superficie de las partículas de AF, y orientando su cadena glicosilada a la fase continua de la suspensión, rodeando de esta manera la partícula de AF y dándole carácter hidrofílico; así, durante el proceso de secado la GA formaría una primera película, mientras que la MD, que no tiene capacidad interfacial, se ubicaría predominantemente en la región mas externa de la partícula, entrelazándose con la cadena glicosilada de la GA, formando así una segunda cubierta en el proceso de secado.
Eficiencia de Encapsulación
Para este ensayo es necesario primero disponer de un método de extracción del AF de las micropartículas, y de un método analítico de cuantificación del AF.
Para el método de extracción se realizaron diferentes ensayos preliminares buscando las condiciones de máxima solubilidad del AF y las condiciones para romper las paredes de las micropartículas y liberar el AF. El pH es un factor fundamental en la solubilidad del AF, dado que éste es una molécula anfótera, con valores de pKa de 3.5 (α-COOH),
4.8 (β-COOH) y 8.3 (amina del grupo pterina) (31). Experimentalmente se encontró que a valores de pH de 5.0, el AF presenta una buena solubilidad para los propósitos de este estudio.
Respecto a la liberación del AF de la matriz polimérica formada por la GA y MD, se encontró que con la aplicación de temperatura y ultrasonido se da lugar a la liberación del AF encapsulado. La eficiencia del método se determinó a través del porcentaje de recuperación, cuyos resultados se describen mas adelante.
Como método analítico se eligió el espectrofotométrico, por su sencillez y exactitud. El AF presenta dos máximos de absorción, a 280 y 350 nm en medios acuosos; el primer máximo se atribuye al ácido aminobenzoico, y el segundo al grupo pteridina. Se seleccionó la absorbancia a 280 nm porque es la que presenta un coeficiente de extinción mayor y, por tanto, la sensibilidad es mayor. En varios estudios anteriores se ha propuesto y usado este método para la cuantificación de AF (32).
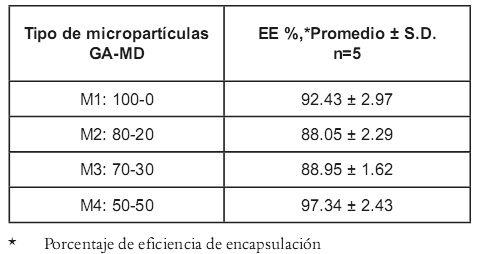
Los resultados al evaluar la eficiencia de encapsulación se describen en la tabla 2, donde se presentan los promedios y los intervalos múltiples de Duncan con un intervalo de confianza del 95%. Los cuatro tipos de micropartículas presentan altos porcentajes de eficiencia de encapsulación, todos superiores al 80%. Las micropartículas obtenidas usando la mezcla GA-MD 50-50 fueron las que mayor eficiencia de encapsulación presentaron, mientras que las mezclas GA-MD 70-30 y 80-20, obtuvieron los resultados mas bajos, muy similares entre sí (estadísticamente no son diferentes de acuerdo a los intervalos de Duncan).
Tabla 2. Eficiencia de encapsulación.
Estos resultados pueden ser explicados por las diferencias en la funcionalidad de los materiales de pared usados. En las micropartículas con 100% de GA, se obtuvo un % EE de 92%, acorde con los resultados obtenidos por otros investigadores (16,33,34), que demuestran la gran habilidad de esta goma para formar películas e inmovilizar principios activos con baja solubilidad en agua, por su capacidad para absorberse en las interfaces sólido-líquido.
En la mezcla equitativa de GA y MD se suman de manera sinérgica la actividad interfacial de la GA y las propiedades ligantes de la MD, dándose lugar a la formación de la doble capa, ya mencionada, donde el AF está convenientemente rodeado de GA y sobre las cadenas glicosiladas de la GA se encuentran interpenetradas las moléculas pequeñas de MD, que actúan como ligante, formando así una doble pared poco porosa que favorece el atrapamiento del AF.
Mientras que en las mezclas de GA-MD 70-30 y 80-20, se presenta una competencia entre la disposición de las GA y la MD en la interfase, formándose una capa interna mas débil que la de GA 100%, y por otra parte, la cantidad de MD en la capa externa no es suficiente para dar lugar a una buena acción ligante. Aparentemente el aumento de la cantidad de MD también favorece el % EE; sin embargo, al evaluar de una manera preliminar MD 100% se obtuvieron micropartículas fracturadas, lo que indica la necesidad de la presencia de GA y la existencia de una mezcla óptima de GA-MD.
Los ensayos de disolución son una prueba fisico-química que determina la cantidad de fármaco que se disuelve por unidad de tiempo, bajo condiciones estandarizadas y determinan la cantidad acumulativa de un principio activo en una solución, como función del tiempo (35)
Los ensayos de disolución in vitro se utilizan como indicadores de la biodisponibilidad del principio activo incorporado en una forma farmacéutica. En este trabajo se realizó el ensayo de disolución, para observar el comportamiento de las micropartículas en un medio con pH similar al gástrico y al intestinal (pH 1.2 y 7.2), atendiendo las recomendaciones de la USP 31 (21).
El ensayo se hizo durante 60 minutos a pH 1.2 y hasta 120 minutos para pH 7.2; a los 60 minutos se presenta, de acuerdo al patrón de motilidad cíclico del estómago e intestino delgado, la transición entre la fase I y la fase II, la cual se caracteriza por inactividad y la presencia de contracciones (36). El estudio de disolución fue aplicado a los 4 tipos de micropartículas, realizando 3 repeticiones para cada uno, y en las condiciones ya descritas en la parte experimental.
Inicialmente se construyeron las curvas de calibración para soluciones de AF a pH 1.2 y 7.2, con tres repeticiones en cada caso y se obtuvieron las ecuaciones 2 y 3, que describen los respectivos modelos lineales de las curvas de calibración:
Ecuación 2.
Ecuación 3.
Se calculó el % de disolución aplicando la ecuación 4, donde fc corresponde al factor de corrección de los mL de buffer extraídos, que se calcula con la ecuación 5.
Ecuación 4.
Ecuación 5.
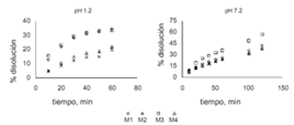
En el ensayo de disolución se obtuvieron los resultados que se muestran en la figura 4, donde se graficaron los promedios de disolución obtenidos para cada tiempo de monitoreo y se obtuvieron los
perfiles de disolución para cada tipo de micropartícula a pH 1.2 y 7.2.
Figura 4. Perfiles de disolución a pH 1.2 y 7.2
Dada la baja solubilidad del AF en soluciones acuosas se espera que la disolución sea baja. Efectivamente, los porcentajes de disolución encontrados se pueden considerar bajos de acuerdo a Ribeiro y colaboradores (37), quienes expresan que porcentajes de disolución cercanos o inferiores a 20%, son bajos, al realizar ensayos durante 60 minutos.
Analizando los resultados se puede concluir que las micropartículas con GA 100% y GA:MD, 50-50 son las que presentan el menor porcentaje de disolución, tanto a pH 1.2 como 7.2. Dado que estos dos tipos de micropartículas justamente corresponden a las que contienen mayor porcentaje de EE, se podría decir que la estructura de la micropartícula formada presenta una pared compacta que favorece el atrapamiento de AF pero impide su liberación.
Las micropartículas con mezclas de GA-MD 70-30 presentan el mejor porcentaje de disolución en ambos valores de pH; siendo ligeramente superior al 20% a los 60 minutos. Como se describió anteriormente, estas podrían presentar una pared débil, posiblemente porosa por la insuficiente acción ligante de la MD, y por tanto se podría explicar que la liberación del AF esté favorecida por tener una pared porosa, por donde puede ingresar agua. Los perfiles de disolución de micropartículas compuestas por materiales de pared tipo polisacáridos están fuertemente influenciados por la capacidad de hinchamiento de estos (38), lo que posiblemente explica las diferencias entre los cuatro tipos de micropartículas en los perfiles de disolución en ambos pH. Posterior al hinchamiento de la pared, el principio activo puede ser liberado por disolución y difusión.
La GA, teóricamente, observa un comportamiento diferente a pH 1.2 y 7.2; a pH 1.2 se esperaría que esta se encuentre bajo una configuración contraída y compacta; debido a su bajo grado de ionización, las interacciones polímero-polímero son favorecidas mas que las interacciones polímero-agua y, por tanto, la hidratación es insuficiente; mientras que a pH 7.2 presentaría una configuración extendida y desenrrollada, debido a la ionización de los grupos glucorónicos terminales, donde se favorecen las interacciones polímero-agua y, por tanto, la GA se hincharía en estas condiciones. En consecuencia, se esperaría que haya un mayor porcentaje de disolución a pH 7.2; sin embargo, la solubilidad del AF es mayor a pH extremos (pH 1.2). En conclusión, si bien a pH 7.2 la liberación se favorecería por la hidratación de la GA, la baja solubilidad del AF contrarresta este efecto. El hinchamiento de la GA y la gradual disolución y difusión del AF dentro de ese gel formado, podrían explicar el hecho de que los perfiles a pH 7.2 no muestren un valor asintótico, aun después de 2 horas de observación, como se observa a pH 1.2.
Las micropartículas de GA-MD 80-20 observan un comportamiento diferente en los dos valores de pH, presentando un perfil similar al de las micropartículas de GA-MD 70-30 a pH 1.2, mientras que su porcentaje de disolución es menor a pH 7.2, lo cual se puede explicar por el mayor contenido de GA.
CONCLUSIONES
La técnica de secado por aspersión en las condiciones aplicadas, permite la formación de micropartículas de ácido fólico con un tamaño de partícula de 0.5 μm. La morfología de las micropartículas obtenidas por este método varía con la relación goma arábiga-maltodextrina: son poco esféricas y con superficie contraída cuando el porcentaje de goma arábiga es alto, y esféricas y con fracturas cuando se aumenta el porcentaje de maltodextrina. La eficiencia de encapsulación es elevada para los cuatro tipos de micropartículas estudiadas, mientras que los perfiles de disolución muestran limitaciones de las micropartículas en la capacidad de liberación del principio activo, siendo el mejor el de las micropartículas con goma arábiga- maltodextrina, 70-30.
AGRADECIMIENTOS
Los autores agradecen el apoyo financiero recibido del CODI-Universidad de Antioquia; igualmente el apoyo de la empresa CI Tecnacol SA, del Laboratorio Especializado de Análisis LEA y del profesor Leonidas Millán.
REFERENCIAS BIBLIOGRÁFICAS
1. Bekaert S, Storozhenko S, Mehrshahi P, Bennett MJ, Lambert W, Gregory JF, et al. Folate biofortication in food plants. Trends in Plant Sci. 2002; 13 (1): 28-35. [ Links ]
2. Avendaño López MC. Introducción a la Química Farmacéutica. Madrid: McGraw Hill; 1993. [ Links ]
3. Erliana G, Jayashree A. High-performance liquid chromatographic determination of naturally occurring folates during tempe preparation. J Agric Food Chem. 2004; 52 (26): 77527758. [ Links ]
4. Ahmad I, Khan MA, Akhtar J.M. Photodegradation of folic acid in aqueous solution. J Pharm Biomed Anal. 1999; 19 (3-4): 269-275. [ Links ]
5. HuaSongQ,ChuHwangK.Directobservationforphotophysical and photochemistry processes of folic acid in DMSO solution. J Photoch Photobiol A. 2007; 185 (1): 51-56. [ Links ]
6. Kristian M, Steidal AE, Porojnicu AC, Juzeniene A, Vorobey A, Johnsson A, et al. Ultraviolet photodegradation of folic acid. J Photochem Photobiol B. 2005; 80 (1): 47-50. [ Links ]
7. Schrooyen PMM, van der Meer R De Kruif CG. Microencapsulation: its application in nutrition. Proc Nutr Soc. 2001; 60 (4): 475-479. [ Links ]
8. Gharsallaoui A. Applications of spray-drying in microencapsulation of food ingredients: An overview. Food Res Int. 2007; 40 (9): 1107-1121. [ Links ]
9. Madziva H, Kailasaphaty K, Phillips M. Evaluation of alginate-pectin capsules in cheddar cheese as s food carrier for the delivery of folic acid. Food Sci Technol. 2006; 39 (2): 146-151. [ Links ]
10. Barbosa MLM, Borsarelli CD, Mercadante AZ. Light stability of spray-dried bixin encapsulated with different edible polysaccharide preparations. Food Res Int. 2005; 38 (8-9): 989-994 [ Links ]
11. Vila-Jato JL. Tecnología Farmacéutica. Madrid: Síntesis; 1997. [ Links ]
12. Pedroza-Islas R, Vernon-Carter EJ, Durán C. Using biopolymer blends for shrimp feedstuff microencapsulation I. Microencapsule particle size, morphology and microstructure. Food Res Int. 1999; 32 (5): 367-374. [ Links ]
13. Pandit N, Badgujar M, Bhaskar C, Rao M. Encapsulation of endoglucanase using a biopolymer gum Arabic for its controlled release. Bioresource Technol. 2007; 98 (2): 368-372. [ Links ]
14. Phillips G, Williams P. Studies on acacia exudates gums. Food Hydrocolloid. 2005; 19 (4): 661-667. [ Links ]
15. Yadav MP, Igartuburu JM, Yan Y, Nothnagel NA. Chemical investigation of the structural basis of the emulsifying activity of gum arabic. Food Hydrocolloid. 2007; 21 (2): 297-298. [ Links ]
16. Kanakdande D, Bhosale R, Singhal RS. Stability of cumin oleoresin microencapsulated in different combination of gum arabic, maltodextrina and modified starch. Carbohyd Polym. 2007; 67 (4): 536-541. [ Links ]
17. Pedroza-Islas R, Alvarez-Ramirez J, Vernon-Carter EJ. Using biopolymer blends for shrimp feedstuff microencapsulation. II: dissolution and floatability kinetics as selection criteria. Food Res Int. 2000; 33 (2): 119-124. [ Links ]
18. Avaltroni F, Bouquerand PE, Normand V. Maltodextrin molecular weight distribution influence on the glass transition temperature and viscosity in aqueous solutions. Carbohyd Polym. 2004; 58 (3): 323-324. [ Links ]
19. Madene A, Jacquot M, Scher J, Desobry, S. Flavour encapsulation and controlled release a review. Int J Food Sci Tech. 2006; 41 (1): 1-21. [ Links ]
20. USP 31 NF 26 The United States Phamacopeia-National Formulary. Official Monographs. Folic Acid; 2007. [ Links ]
21. Pedroza R. Alimentos microencapsulados: particularidades de los procesos para la microencapsulación de alimentos para larvas de especies acuícolas. Avances en nutrición acuícola. Memorias del VI Simposio Internacional de Nutrición, México; 2002. [ Links ]
22. Gangolli S, ed.. The Dictionary of Substances and their Effects, 2ª ed. Cambridge: The Royal Society of Chemistry; 1999. [ Links ]
23. The Merck Index. An encyclopedie of Chemicals, Drugs and Biologicals. 9ª ed. Estados Unidos: Merck; 1989. [ Links ]
24. Arcot J, Shrestha A. Folate: methods of analysis. Trends Food Sci Tech. 2005; 16 (6-7): 253-266. [ Links ]
25. Ruth HJ, Eger K, Troschutz R. Pharmaceutical chemistry. Vol 2: Drug analysis. Inglaterra: Ellis Horwood; 1991. [ Links ]
26. Leong YK, Seah U, Chu SY, Ong BC. Effects of gum arabic macromolecules on surface forces in oxide dispersions. Colloid Surf A-Physicochem Eng Asp. 2001; 182 (1-3): 263-268. [ Links ]
27. Phillips A, Williams PA. Handbook of hydrocolloids. Cambridge (Estados Unidos): Woodhead; 2003. [ Links ]
28. Young DK, Morr ChV. Microencapsulation properties of gum arabic and several food proteins: Liquid Orange oil emulsion particles. J Agric Food Chem. 2006; 44 (5): 1314-1320. [ Links ]
29. Mercadante AZ, Barbosa MLM, Borsarelli CD. Light stability of spray-dried bixin encapsulated with different edible polysaccharide preparations. Food Res Int. 2005; 38 (8-9): 989-994. [ Links ]
30. Loksuwan J, Characteristics of microencapsulated β-carotene formed by spray drying with modified tapioca starch, native starch and maltodextrina. Food Hydrocolloid 2007; 21 (5-6): 928-935. [ Links ]
31. Bryant CN, Sharpless KE, Sander LC. Quantitative determination of folic acid in multivitamin multielement tablets using liquid chromatography/tandem mass spectrometry. J Chromatogr A. 2006; 1135 (2): 203-211. [ Links ]
32. Song Q-H, Hwang K-C. Direct observation for photophysical and photochemical processes of folic acid in DMSO solution. J Photoch Photobiol A. 2007; 185 (1): 51-56. [ Links ]
33. Krishnan S, Kshirsagar AC, Singhal RS. The use of gum arabic and modified starch in the microencapsulation of a food flavoring agent. Carbohyd Polym. 2005; 62 (4): 309-315. [ Links ]
34. Gabas AL, Telis VRN, Sobral PJA, Telis-Romero J. Effect of maltodextrin and arabic gum in water vapor sorption thermodynamic properties of vacuum dried pineapple pulp power. J Food Eng. 2007; 82 (2): 246-252 [ Links ]
35. Nickerson B, Brown CK, Chokshi HP, Reed RA, Rohrs BR y Shah PA. Acceptable Analytical Practices for dissolution testing of poorly soluble compounds. Pharm Tech. [serial en linea] 2004 [citado 2009 febrero 20]; 28 (1-2). Disponible en: http://pharmtech.findpharma.com/pharmtech/data/articlestandard//pharmtech/502004/137424/article.pdf. [ Links ]
36. Ruiz AM. Evaluación de la liberación in vitro-in vivo de la Teofilina a partir de comprimidos matriciales elaborados con copolímeros de metacrilato de metilo y derivados del almidón. [Tesis Doctoral]. Sevilla (España); 2005. [ Links ]
37. Ribeiro AJ, Silva CM, Veiga F, Zerrouk N. Chitosan-reinforced alginate microspheres obtained through the emulsification/internal gelation technique. Eur J Pharm Sci. 2000; 25 (1): 31-40. [ Links ]
38. Benita S, editora. Microenpasulation methods and industrial applications. New York: Tailor & Francis; 2006. [ Links ]
Recibido: Octubre 8 de 2008.
Aceptado: Marzo 30 de 2009.
* Autor a quien se debe dirigir la correspondencia: cgallardo@farmacia.udea.edu.co