Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Vitae
Print version ISSN 0121-4004
Vitae vol.16 no.3 Medellín Sept./Dec. 2009
PRODUCTOS NATURALES
DETERMINACIÓN DEL CONTENIDO DE FENOLES Y EVALUACIÓN DE LA ACTIVIDAD ANTIOXIDANTE DE PROPÓLEOS RECOLECTADOS EN EL DEPARTAMENTO DE ANTIOQUIA (COLOMBIA)
DETERMINATION OF PHENOLIC CONTENT AND EVALUATION OF ANTIOXIDANT ACTIVITY OF PROPOLIS FROM ANTIOQUIA (COLOMBIA)
Lady R. PALOMINO G.1; Carlos M. GARCÍA P. 1; Jesús H. GIL G.1,2; Benjamín A. ROJANO1; Diego L. DURANGO R.1*
1 Grupo de Química de los Productos Naturales y los Alimentos. Escuela de Química. Facultad de Ciencias. Universidad Nacional de Colombia. Calle 59a No. 63-020 Autopista Norte. A.A. 3840. Medellín, Colombia.
2 Departamento de Ingeniería Agrícola y Alimentos. Facultad de Ciencias Agropecuarias. Universidad Nacional de Colombia. Calle 59a No. 63-020 Autopista Norte. A.A. 3840. Medellín, Colombia.
RESUMEN
El propóleo, un producto natural colectado por las abejas a partir de los exudados de las plantas, es ampliamente utilizado en la medicina tradicional por sus reconocidas propiedades terapéuticas. En este estudio se compara la calidad del extracto etanólico de propóleos (EEP) provenientes de diferentes regiones de Antioquia (Colombia), mediante la determinación del contenido de flavonoides y fenoles totales, y la actividad antioxidante in vitro, la cual es establecida empleando las técnicas de captura de los radicales DPPH• (1,1-difenil-2-picrilhidracilo) y ABTS•+ (catión del ácido 2,2'-azino-bis 3-etilbenzotiazolina-6-sulfónico), y la capacidad reductora de hierro (FRAP). Las determinaciones para el contenido total de compuestos fenólicos se encuentran entre 22,11 ± 0,54 y 75,22 ± 1,35 mg GAE/g de EEP y para el contenido total de flavonoides, entre 4,75 ± 0,01 y 34,50 ± 0,07 mg QE/g de EEP. La actividad antiradicalaria varía entre 33,9 ± 9,7 y 324,6 ± 15,0, y entre 455,5 ± 7,8 y 1,091 ± 17,3 µmol TE/g de EEP (TEAC) en los sistemas DPPH y ABTS, respectivamente. En el método FRAP la actividad se encuentra entre 40,9 ± 13,3 y 338,4 ± 22,4 µmol AAE/g de EEP (AEAC). Los resultados muestran una correlación lineal positiva entre la capacidad antioxidante y el contenido de compuestos de naturaleza fenólica. La actividad antioxidante de algunos propóleos indica su potencial como producto nutracéutico.
Palabras clave:propóleo, compuestos fenólicos, flavonoides, DPPH, FRAP.
ABSTRACT
Propolis, a natural product collected by honeybee from exudates of plants, is widely used in traditional medicine due to its known therapeutic properties. In this paper, the quality of ethanol extracts of propolis (EEP) from different regions of Antioquia (Colombia) is compared through the determination of flavonoids and total phenolic compounds content, and the in vitro antioxidant activity, using three assay systems: radical scavenging activity by means of the DPPH• (1-diphenyl-2-picrylhydrazyl) and ABTS•+ (2,2'-azino-bis 3-ethylbenzthiazoline-6-sulfonic acid cation) assays, and ferric reducing antioxidant power (FRAP). Determinations of total phenolic compounds content are found between 22.11 ± 0.54 and 75.22 ± 1.35 mg GAE/g of EEP and total content of flavonoids between 4.75 ± 0.01 y 34.50 ± 0.07 mg QE/g of EEP The radical scavenging activity varies from 33.9 ± 9.7 to 324.6 ± 15.0, and from 455.5 ± 7.8 to 1091 ± 17.3 µmol TE/g of EEP (TEAC) in the DPPH and ABTS system, respectively. In the FRAP method, the activity is found between 40.9 ± 13.3 and 338.4 ± 22.4 µmol AAE/g of EEP (AEAC). Results show a positive linear correlation between antioxidant activity and total phenolic content. The antioxidant activity of some propolis indicates its potential role as nutraceutical.
Key words: propolis, phenolic compounds, flavonoids, DPPH, FRAP.
INTRODUCCIÓN
La palabra propóleo se deriva del griego pro (en defensa de) y polis (la ciudad); con ella se designa la sustancia que recubre la colmena o polis de las abejas y cumple funciones defensivas. El propóleo es una sustancia resinosa y altamente adhesiva, recolectada, transformada y usada por las abejas para sellar los agujeros, fijar los panales de miel, pulir las paredes interiores y proteger la entrada contra los intrusos (1). Su composición química es compleja y depende de la flora presente en el área de recolección; sin embargo, se han identificado como principales componentes: alcoholes, aldehídos, aminoácidos, ácidos alifáticos, ácidos aromáticos, ésteres aromáticos, flavonoides, ácidos grasos, ácidos p-cumáricos prenilados, ácidos cafeoilquínicos, lignanos, ácidos diterpénicos, triterpenos, esteroides y azúcares (2, 3).
Este producto de la colmena ha sido utilizado desde tiempos antiguos por las propiedades farmacéuticas que se le han atribuido, tales como: antibacteriano (4), antifúngico (5), antiviral (6), antiinflamatorio (6), antiúlceroso (7), hepatoprotector (8), antitumoral (9), entre otras. Algunas de estas propiedades han sido relacionadas con el contenido de compuestos fenólicos, especialmente flavonoides, ésteres del ácido caféico, etc (10-12). En la actualidad, el propóleo se emplea en la medicina natural, en apiterapia, como componente de biocosméticos y como alimento saludable para múltiples propósitos (1, 3, 13, 14).
La amplia diversidad en la composición química de este producto apícola y su empleo generalizado en la industria, han traído como consecuencia la necesidad de control de su calidad y su normalización en general. Con este fin se han desarrollado protocolos de trabajo establecidos por diferentes normas internacionales, como la norma IRAM, del Instituto Argentino de Normalización - Subcomité de Productos Agroalimentarios del NOA-2004 (15), la norma Ramal del Ministerio de Agricultura de Cuba-1994 (16), y el reglamento técnico para la fijación de identidad y calidad de propóleos del Ministerio de Agricultura de Brasil-1999 (17).
En Colombia, a pesar de que la información referente a su composición química y su actividad biológica es escasa (18, 19), este material es comercializado ampliamente en tiendas naturistas, como jarabe, tintura y ungüento. Un conocimiento más profundo de sus propiedades permitiría la elaboración de normas de calidad adecuadas, que sirvan como elementos útiles para su control y verificación por parte de las entidades farmacológicas y bromatológicas correspondientes. En este sentido, la concepción más actualizada de su control de calidad consiste en la determinación de sus propiedades físico-químicas y la estimación de su actividad biológica. Para el presente trabajo se llevaron a cabo estudios comparativos mediante la determinación del contenido de fenoles totales y flavonoides, y la evaluación de la actividad captadora de radicales y antioxidante de muestras de propóleos colectadas en diferentes regiones de Antioquia.
MATERIALES Y MÉTODOS
Recolección del propóleo y obtención de los extractosLas muestras de propóleo provenientes de abejas Apis mellifera (africanizada), se obtuvieron en el Departamento de Antioquia (Colombia) en apiarios de los municipios de Caldas (Latitud: 6°06' N, Longitud: 75°38' O; 1.750 msnm), Betania (Latitud: 5°44' N, Longitud: 76°00' O; 1.550 msnm), La Unión (Latitud: 5°59' N, Longitud: 75°22' O; 2.473 msnm), y Medellín (Laboratorio de Investigaciones Melitológicas y Apícolas-LIMA de la Universidad Nacional; Latitud: 6°16' N, Longitud: 75°34' O; 1.479 msnm). La recolección se realizó mediante los métodos de raspado y trampa. En el primero se utilizó una espátula de acero inoxidable para remover el producto adherido en las caras laterales, tapa y entretapa de cada cajón. Mediante este método se recolectaron muestras de propóleo en los Municipios de Caldas (CR) y Betania (BR). Para el método de trampa, se emplearon mallas plásticas matrizadas, las cuales, una vez recubiertas del material, se retiraron y almacenaron a -10°C para facilitar la remoción del producto. Este procedimiento se empleó para obtener los propóleos en los Municipios de Caldas (CT), La Unión (UT) y el apiario LIMA (MT). Todas las muestras se recolectaron en época de lluvias, entre los meses de octubre y diciembre de 2007. El muestreo se efectuó en forma aleatoria de diferentes colmenas de cada apiario para formar una muestra compuesta representativa de cada municipio.
Los diferentes propóleos crudos se maceraron manualmente y se les retiraron trozos de madera, piedras pequeñas y partes de insectos. Luego, 30 g de muestra se sometieron a extracción sucesiva con 100 mL de etanol al 96% v/v (3x100 mL) en un agitador magnético, durante 48 horas, a temperatura ambiente y en ausencia de luz. Posteriormente, el material se filtró en un embudo con placa sinterizada. A los filtrados combinados, se les eliminaron las ceras mediante precipitación y filtración con adición de agua destilada (50 mL) y refrigeración del extracto a -18°C. Finalmente, se evaporó el solvente de los filtrados por destilación al vacío en un evaporador rotatorio a presión reducida a una temperatura de 40°C. Los extractos etanólicos obtenidos (EEP) se almacenaron en viales ámbar y se refrigeraron a -18°C hasta su posterior evaluación.
Absorbancia específica del espectro UV
La absorbancia específica del espectro UV de cada muestra de EEP se obtuvo por el método de Miyataka et al (20). A partir de la absorbancia específica a la longitud de onda de máxima absorción (λmax), determinada en un espectrofotómetro UVvisible Shimadzu UV 1800, se calculó el valor del coeficiente de extinción E1 cm1%.
Contenido de fenoles y flavonoides totales
El contenido de fenoles totales se determinó por el método colorimétrico de Singleton y Rossi (21) con algunas modificaciones. En un tubo de reacción se adicionaron 50 µL de solución etanólica de propóleo, 800 µL de agua y 100 µL de reactivo Folin-Ciocalteu (grado analítico, Merck). Se agitó y luego se dejó en reposo por 8 minutos. Posteriormente se adicionaron 50 µL de Na2CO3 al 20%. Después de 1 hora en la oscuridad se leyó la absorbancia a 760 nm. Se usaron soluciones de ácido gálico (Sigma-Aldrich®) entre 50 - 500 µg/mL para construir la curva de calibración (r2=0,995). Los resultados se expresaron como mg equivalentes de ácido gálico (GAE)/g de EEP; los valores se presentan como la media de los análisis realizados por triplicado ± desviación estándar (DE).
El contenido de flavonoides totales en los extractos etanólicos fue determinado por el método de Kumazawa et al (22). A una alícuota de 0,5 mL de solución de propóleo, se le adicionaron 0,5 mL de solución etanólica de AlCl3 al 2%. Después de una hora de incubación a temperatura ambiente, la absorbancia fue medida a 420 nm. Se usaron soluciones de quercetina (Sigma-Aldrich®) entre 5 - 25 µg/mL, para construir la curva de calibración (r2 = 0,994). El contenido de flavonoides totales fue calculado como mg equivalentes de quercetina (QE)/g de EEP. Este procedimiento se efectuó con cada uno de los propóleos objeto de estudio por triplicado. Los valores presentados corresponden a la media ± desviación estándar (DE).
Actividad antioxidante
Actividad inhibidora del radical libre 1,1-difenil-2-picril hidracilo (DPPH•).
La actividad antioxidante de los extractos sek evaluó mediante la capacidad captadora del radical DPPH• utilizando la metodología de Rojano et al (23). Un volumen de 990 µL de una solución metanólica de DPPH se mezcló con 10 µL de las soluciones etanólicas de propóleos en varias concentraciones; las mezclas se dejaron en reposo y en ausencia de luz durante 30 minutos. Transcurrido este tiempo se leyó la absorbancia a 517 nm en un espectrofotómetro. Los resultados fueron convertidos a porcentaje de inhibición y expresados como capacidad antioxidante en µmol de equivalentes Trolox (ácido 6-hidroxi-2,5,7,8-tetrametilcromo-2carboxílico; TE)/g de EEP (TEAC). Los experimentos se llevaron a cabo usando un bloque de diseño al azar. Dentro de cada bloque cada tratamiento se aplicó 3 veces. El antioxidante sintético butil hidroxitolueno (BHT), se usó como control positivo.
Actividad inhibidora del radical 2,2'-azino-bis (3-etilbenzotiazolina)-6 sulfonato de amonio (ABTS•+).
Se empleó el método propuesto por Aubad et al (24). El radical se generó por una reacción de oxidación del ABTS con persulfato de potasio. Se prepararon soluciones etanólicas de diferentes concentraciones de cada una de las muestras de propóleo, de las cuales se tomaron 20 µL y se mezclaron con 980 µL de la solución de ABTS previamente preparada en una solución buffer fosfato a un pH de 7,4. Las soluciones obtenidas se incubaron en la oscuridad a temperatura ambiente durante 30 minutos y posteriormente se midieron sus absorbancias a 734 nm. Se utilizó una curva de calibración de Trolox como estándar y los resultados se expresaron como capacidad antioxidante en µmol de equivalentes Trolox (TE)/g de EEP (TEAC). Los valores se expresan como la media de tres réplicas. Se usó como referencia el BHT.
Actividad antioxidante reductora de Fe3+: Ensayo FRAP
La evaluación de la actividad reductora se llevó a cabo según el método de Benzie et al (25). Un volumen de 10 µL de las muestras de propóleo en diferentes concentraciones, se mezcló con 90 µL de agua destilada y 900 µL del reactivo FRAP (2,5 mL de la solución 2,4,6-tripiridil-s-triazina a una concentración de 10 µM en HCl 40 mM; 2,5 mL de FeCl3 20 µM y 25 mL de buffer acetato 0,3 µM a un pH de 3.6). La absorbancia fue leída a 593 nm después de 7 minutos. Se utilizó una curva de calibración de ácido ascórbico (AA) y las actividades de los extractos de propóleo se expresaron como µmol de equivalentes de ácido ascórbico (AAE)/g de EEP (AEAC). Los valores se expresan como la media de tres réplicas. Como control positivo se empleó el antioxidante BHT.
RESULTADOS Y DISCUSIÓN
Contenido de fenoles y flavonoides totales
El valor E1 cm1% de la absorción UV es uno de los parámetros fisicoquímicos usados para evaluar el propóleo (20, 26), porque varias de las actividades biológicas de este producto apícola se atribuyen a la presencia de compuestos fenólicos, flavonoides y ácidos caféicos, los cuales presentan absorciones máximas entre las longitudes de onda de 240 y 350 nm. Los valores de E1 cm1% de las muestras de EEP se encontraron entre 72 y 390 (Véase tabla 1). Una λmax cercana a 290 nm, se halló en los propóleos CT, CR, UT, y MT. El mayor valor E1 cm1% lo presentó el propóleo del municipio de Betania, superando incluso los valores reportados por Kumazawa, Hamasaka y Nakayama (22) para propóleos de diferentes regiones del mundo. En este propóleo la longitud de máxima absorción se detectó a 242 nm. Es posible inferir que las diferencias en la λmax corresponden a diversas composiciones de fenoles y flavonoides presentes en los propóleos como consecuencia de sus diferentes orígenes botánicos y geográficos. Por su parte, el menor valor E1 cm1% se halló en el propóleo MT.
Tabla 1. Contenido de fenoles totales y flavonoides totales en las muestras de propóleo.
El contenido de fenoles y flavonoides en propóleos es un parámetro importante que establece tanto la calidad del material como su potencial biológico, en especial para la actividad antioxidante. Se ha reportado que estos compuestos pueden actuar interrumpiendo la reacción de oxidación de lípidos (27), inhibiendo las reacciones de quimioluminiscencia (28), capturando varias especies reactivas de oxígeno (29). Los métodos de Folin-Ciocalteau y de formación del complejo con AlCl3 para determinar el contenido total de compuestos fenólicos y flavonoides, respectivamente, son comúnmente usados para analizar plantas y alimentos (30). En el presente estudio, estos métodos se aplicaron para determinar el contenido de fenoles y flavonoides totales en muestras de propóleo de diferentes municipios de Antioquia. Los métodos fisicoquímicos son útiles para evaluar estos materiales porque el propóleo contiene muchas clases de compuestos fenólicos (30). Se observa que el contenido de fenoles y flavonoides en los extractos varía ampliamente, en un intervalo desde 22,11 ± 0,54 a 75,22 ± 1,35 mg GAE/g de EEP y desde 4,75 ± 0,01 a 42,37 ± 0,18 mg QE/g de EEP, respectivamente (Véase tabla 1). Los extractos etanólicos de los propóleos BR, UT y CT presentan valores altos de contenido de compuestos fenólicos, comparados con las demás muestras.
Normativas como la de Argentina (15) y Brasil (17), han establecido requisitos mínimos de concentración que deben cumplir el propóleo y sus extractos para ser utilizados como materia prima en el desarrollo de productos; para los compuestos fenólicos, el valor mínimo es de 50 mg GAE/g de EEP, y para flavonoides, de 5 mg QE/g de EEP (15). De acuerdo con lo anterior, los propóleos BR, UT, y CT satisfacen los requisitos de calidad establecidos por estas normativas.
El propóleo MT es el que posee los menores niveles de fenoles y flavonoides, siendo de 22,11 ± 0,54 y 4,75 ± 0,01 mg/g de EPP, respectivamente. En este propóleo, Meneses (31) ha reportado la presencia principalmente de diterpenos de tipo labdano. Por otra parte, el propóleo de Betania es el que posee los mayores niveles de contenido de fenoles (75,22 ± 1,35 mg GAE/g) y flavonoides (42,37 ± 0,18 mg QE/g), superando los valores encontrados en los propóleos de otras regiones de Colombia, según lo reportado por Salamanca, Correa y Principal (32). Adicionalmente, todas las muestras presentaron contenidos de compuestos fenólicos y flavonoides inferiores a los reportados para propóleos de origen europeo, asiático y norteamericano (33), lo cual sugiere que la composición de los propóleos analizados difiere de la encontrada en regiones templadas, debido a la influencia y diversidad del origen botánico a partir de la cual las abejas los elaboran en cada una de las zonas biogeográficas (2, 3). Los propóleos de zonas templadas poseen como principales constituyentes compuestos fenólicos (flavonoides, ácidos cinámicos, y derivados), cuya fuente principal son los exudados de álamos (Populus spp.), abedules (Betula alba), entre otros (34). En regiones tropicales, carentes de este tipo de vegetación, las abejas deben usar otras plantas como fuente para su producción (35).
Capacidad antioxidante
La actividad antioxidante de los extractos fue evaluada por tres métodos diferentes, pues se sabe que los antioxidantes pueden actuar por múltiples mecanismos, dependiendo del sistema de reacción o la fuente radicalaria u oxidante (36). Los resultados fueron expresados en equivalentes Trolox (TEAC) y equivalentes de ácido ascórbico (AEAC). El valor TEAC compara la capacidad captadora de radicales ABTS•+ o DPPH• del extracto bajo investigación con respecto al antioxidante sintético Trolox; un análogo soluble en agua de la vitamina E (37). Por su parte, el valor AEAC confronta la habilidad del propóleos evaluado para reducir Fe3+ a Fe2+, con respecto a la del ácido ascórbico. De esta manera, altos valores TEAC y/o AEAC representan una actividad antioxidante superior; indicando respectivamente, mayor capacidad para captar radicales libres mediante transferencia de hidrógeno, y/o para reducir Fe3+ a Fe2+.
Actividad captadora de radicales
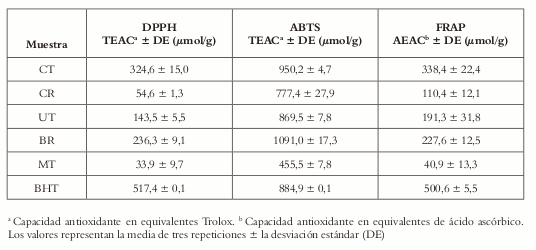
Los resultados de la actividad captadora de radicales DPPH• y ABTS•+ para los diferentes propóleos, variaron entre 33,9 ± 9,7 y 324,6 ± 15,0; y entre 455,5 ± 7,8 y 1091 ± 17,3 µmol de TE/g de EEP (TEAC), respectivamente (Véase tabla 2). De los cinco extractos, los más promisorios, los que demostraron actividad significativa en las dos técnicas evaluadas, son CT y BR. Teniendo en cuenta que cada técnica tiene diferentes condiciones de reacción y solubilidad, es posible inferir que los extractos contienen diversos compuestos con potencial antioxidante.
Tabla 2. Actividad antioxidante de los extractos etanólicos de los propóleos.
Los resultados muestran que para todos los extractos, los valores de ABTS expresados como TEAC son mayores que en la técnica con DPPH, debido a la baja selectividad del ABTS •+, que reacciona con cualquier compuesto aromático hidroxilado, independientemente de su potencial antioxidante real (38). Por otro lado, si la capacidad antioxidante de los extractos EEP se debe a la presencia de ácidos fenólicos, flavonoides y otro tipo de polifenoles, como se reporta generalmente en la literatura (33, 39-41), se debe tener en cuenta que el DPPH es más selectivo que el ABTS•+ y, a diferencia de este último, no reacciona con los flavonoides carentes de grupos hidroxilo en el anillo B, ni con ácidos aromáticos que contengan un solo grupo hidroxilo (38). Este hecho explica los valores TEAC inferiores en el método DPPH con respecto al ABTS.
La mayor actividad captadora del radical DPPH• se registró en el extracto etanólico CT seguido de BR, mientras que para el radical ABTS•+ el orden se invierte. Para el ensayo ABTS, ambos propóleos presentan una actividad superior a la observada para el antioxidante sintético BHT. Por otro lado, el extracto MT exhibió una débil actividad captadora de radicales. En los propóleos provenientes de Caldas se encontraron diferencias en la capacidad captadora de radicales, dependiendo del método de recolección.
Actividad antioxidante reductora de Fe3+ (FRAP)
El ensayo FRAP está basado en la habilidad de los compuestos fenólicos para reducir Fe3+ a Fe2+ (42). En presencia de 2,4,6-tripiridil-s-triazina, la reducción se encuentra acompañada de la formación de un complejo coloreado de Fe2+. Los valores de la actividad antioxidante FRAP se encontraron entre 40,9 ± 13,3 y 338,4 ± 22,4 µmol de AAE/g de EEP (AEAC) (Véase tabla 2). Los extractos CT y BR, que presentaron la mayor actividad captadora de los radicales DPPH• y ABTS•+, también exhibieron la mayor capacidad antioxidante, con valores AEAC de 338,4 ± 22,4 y 227,6 ± 12,5, respectivamente. Estos valores estuvieron por debajo del encontrado para el antioxidante BHT. El extracto EEP, proveniente del apiario LIMA, MT, que presentó una débil actividad captadora de radicales, también demostró ser el menos activo en el ensayo FRAP.
Correlación entre la capacidad antioxidante y el contenido de fenoles y flavonoides totales
El propóleo contiene una amplia variedad de compuestos fenólicos, principalmente flavonoides. La variación en el contenido de flavonoides del propóleo se puede atribuir principalmente a la diferencia en la vegetación circundante a la colmena. Se ha sugerido que el contenido de flavonoides y otras sustancias fenólicas juega un papel preventivo en el desarrollo del cáncer y las enfermedades del corazón (43). Estudios concernientes a la composición del propóleo han reportado ácidos carboxílicos aromáticos, tales como cafeico, p-cumárico, 3,4-dimetoxicinámico, y sus ésteres, y los flavonoides quercetina, pinobanksina-5-metileter, apigenina, kaempferol, crisina, pinocembrina, galangina, sakuranetina, entre otros (2,3).
Se observó que los extractos CT y BR, que presentaron los mayores contenidos de fenoles y flavonoides, a su vez exhibieron altos valores de TEAC y AEAC (Véanse tablas 1 y 2). Estos extractos, a su vez, poseen valores de E1 cm1% superiores a los encontrados en los otros propóleos. Por otro lado, el extracto MT, cuyo valor E1 cm1%, contenido de fenoles y flavonoides totales es pequeño, exhibió una débil actividad captadora de radicales y antioxidante, lo que sugiere que posiblemente los principales componentes de este propóleo son diferentes a los de los otros municipios.
El análisis de la relación entre la actividad captadora de radicales, DPPH y ABTS, y antioxidante de los extractos de los propóleos, y el contenido de fenoles, muestra una correlación positiva media (Véase tabla 3).
Tabla 3. Análisis de la correlación entre los parámetros de actividad captadora de radicales y antioxidante, y el contenido de fenoles y flavonoides.
Las correlaciones no son completamente lineales porque el método de Folin-Ciocalteu es específico para compuestos fenólicos, y la actividad antioxidante también puede ser exhibida por compuestos no fenólicos (44, 45). Además es posible que se presenten interacciones antagonistas o sinergistas entre los compuestos fenólicos y otros metabolitos que pueden afectar la actividad (46). La relación entre el contenido de fenoles y la capacidad captadora de radicales DPPH (r2 = 0,60), ABTS (r2 = 0,69) y antioxidante FRAP (r2 = 0,68), sugiere que entre 60 y 69% de la actividad evaluada para los propóleos de Antioquia resulta de la contribución de los compuestos fenólicos.
Adicionalmente se aprecia una relación positiva débil entre la actividad y el contenido de flavonoides. Nieva Moreno et al (47), han reportado que la correlación entre el contenido de flavonoides y la actividad antioxidante es significativa, pero otros factores están involucrados. Asimismo, Yamauchi (48) describió que otros constituyentes diferentes a los flavonoides también toman parte en la actividad antioxidante del propóleo.
Una mayor correlación se encontró entre la actividad y el contenido de fenoles que cuando se correlacionaron esta actividad y los niveles de flavonoides, lo que sugiere que otros compuestos fenólicos diferentes a los flavonoides, por ejemplo derivados del ácido caféico, juegan un papel importante en la actividad antioxidante del propóleo recolectado en Antioquia. Sin embargo, es necesario un análisis cualitativo y cuantitativo más detallado de los compuestos con actividad antioxidante para elucidar la actividad antioxidante del propóleo.
CONCLUSIONES
En el presente trabajo se determinó el contenido de fenoles y flavonoides totales mediante métodos espectrofotométricos, y la actividad antioxidante de propóleos provenientes de diversas regiones de Antioquia-Colombia. Se estableció que los extractos etanólicos de los propóleos (EEP) provenientes de los municipios de Betania BR, y Caldas CT, exhibieron un mayor contenido de compuestos fenólicos, los cuales podrían estar relacionados con la capacidad antioxidante de los mismos. En BR también se detectó el mayor contenido de flavonoides. Los valores encontrados cumplen con aquellos establecidos por diferentes normatividades técnicas para la fijación de identidad y calidad de propóleos. En general, los propóleos con actividad antioxidante FRAP también exhibieron la mayor actividad captadora de los radicales DPPH y ABTS; se encontró una buena correlación entre estas actividades y el contenido de fenoles de los extractos. La alta actividad antioxidante de los propóleos de Betania y Caldas, su alto contenido de fenoles y su origen natural, los hacen promisorios como aditivos nutricionales para la dieta humana
AGRADECIMIENTOS
Los autores agradecen el apoyo de la Universidad Nacional de Colombia y de la Dirección Nacional de Investigación para llevar a cabo esta investigación.
REFERENCIAS BIBLIOGRÁFICAS
1. Burdock GA. Review of the biological properties and toxicity of bee propolis (propolis). Food Chem Toxicol. 1998; 36 (4): 347-363. [ Links ]
2. Marcucci MC. Propolis: chemical composition, biological properties and therapeutic activity. Apidologie. 1995; 26 (2): 83-99. [ Links ]
3. Bankova VS, de Castro SL, Marcucci MC. Propolis: recent advances in chemistry and plant origin. Apidologie. 2000; 31 (1): 3-15. [ Links ]
4. Marcucci MC, Ferreres F, García-Viguera C, Bankova VS, de Castro SL, Dantas AP, et al. Phenolic compounds from Brazilian propolis with pharmacological activities. J Ethnopharmacol. 2001; 74 (2): 105-112. [ Links ]
5. Garedew A, Schmolz E, Lamprecht, I. Microbiological and calorimetric investigations on the antimicrobial actions of different propolis extracts: an in vitro approach. Thermochim Acta. 2004; 422 (1-2): 115-124. [ Links ]
6. Kujumgiev A, Tsvetkova I, Serkedjieva Y, Bankova V, Christov R, Popova S. Antibacterial, antifungal and antiviral activity of propolis of different geographic origin. J Ethnopharmacol. 1999; 64 (3): 235-240. [ Links ]
7. Hu F, Hepburn H, Yinghua L, Chen M, Radloff S, Daya S. Effects of ethanol and water extracts of propolis (bee glue) on acute inflammatory animal models. J Ethnopharmacol. 2005; 100 (3): 276-283. [ Links ]
8. Primon de Barros M, Lemos M, Maistro EL, Freire Leitec M, Barreto Sousac JP, Bastos KJ, et al.Evaluation of antiulcer activity of the main phenolic acids found in Brazilian Green Propolis. J Ethnopharmacol. 2008; 120 (3): 372-377. [ Links ]
9. Shimizu K, Ashida H, Matsuura Y, Kanazawa K. Antioxidative bioavailability of artepillin C in Brazilian propolis. Arch Biochem Biophys. 2004; 424 (2): 181-188. [ Links ]
10. El-Khawaga OA, Salem TA, Elshal MF. Protective role of Egyptian propolis against tumor in mice. Clin Chim Acta. 2003; 338 (1-2): 11-16. [ Links ]
11. Russo A, Longo R, Vanella A. Antioxidant activity of propolis: role of caffeic acid phenethyl ester and galangin. Fitoterapia. 2002; 73 (S1): S1-S29. [ Links ]
12. Banskota AH, Tezuka Y, Kadota S. Recent progress in pharmacological research of propolis. Phytother Res. 2001; 15 (7): 561-571. [ Links ]
13. Matsuda S. Propolis-health care food. Foods and Food Ingredients Journal of Japan. 1994; 160: 64-73. [ Links ]
14. Wollenweber E, Buchmann S. Feral honey bee in the Sonoran Desert: propolis sources other than Poplar (Populus spp.). Z Naturforsch. 1997; 52c (7-8): 530-535. [ Links ]
15. Argentina. Norma IRAM 15935-1 Scheme 1. Buenos Aires: Instituto Argentino de Normalización - Subcomité de productos agroalimentarios del NOA; 2004. [ Links ]
16. Cuba. Ministerio de Agricultura. Norma Ramal Cubana: Apicultura NRAG-1135-94 (Propóleos Materia Prima), Especificaciones. La Habana: El Ministerio; 1994. [ Links ]
17. Ministerio de Agricultura de Brasil. Regulamentos Técnicos Para a Fixação de Identidade e Qualidade de Extrato de Própolis. Revista Mensagem Doce. [Serial en linea] 1999 [citado 2009 agosto 20]; 52 (1). Disponible en: http://www.apacame.org.br/mensagemdoce/52/msg52.htm. [ Links ]
18. Salamanca GG, Ramírez C, Rubiano L. Contenido mineral de los propóleos colectados en algunas zonas biogeográficas colombianas. Rev Inst Univ Tecn del Chocó. 2004; 20 (1): 79-85. [ Links ]
19. Moreno Z, Martínez P, Figueroa J. Efecto antimicrobiano in vitro de propóleos argentinos, colombianos y cubano sobre Streptococcus mutans ATCC 25175. Nova. 2007; 5 (7): 70-75. [ Links ]
20. Miyataka H, Nishiki M, Matsumoto H, Fujimoto T, Matsuka M, Satoh T. Evaluation of propolis I. Evaluation of Brazilian and Chinese propolis by enzymatic and physico-chemical methods. Biol Pharm Bull. 1997; 20 (5): 496-501. [ Links ]
21. Singleton VL, Rossi JA. Colorimetry of total phenolics with phosphomolybdic-phosphotungstic acid reagents. Am J Enol Vitic. 1965; 16: 144-158. [ Links ]
22. Kumazawa S, Hamasaka T, Nakayama T. Antioxidant activity of propolis of various geographic origins. Food Chem. 2004; 84 (3): 329-339. [ Links ]
23. Rojano B, Saez J, Schinella G, Quijano J, Vélez E, Gil A, et al. Experimental and theoretical determination of the antioxidant properties of isoespintanol (2-isopropyl-3,6-dimethoxy-5methylphenol). J Mol Struct. 2008; 877 (1-3): 1-6. [ Links ]
24. Aubad P, Rojano B, Lobo T. Actividad antioxidante en musgos. Scientia Et Technica. 2007; 13 (033): 23-26. [ Links ]
25. Benzie IF, Strain JJ. The ferric reducing ability of plasma (FRAP) as a measure of "antioxidant power": The FRAP assay. Anal Biochem. 1996; 239 (1): 70-76. [ Links ]
26. Miyataka H, Nishiki M, Matsumoto H, Fujimoto T, Matsuka M, Isobe T, et al. Evaluation of propolis II: Effects of Brazilian and Chinese propolis on histamine release from rat peritoneal mast cells induced by compound 48/80 and concanavalin A. Biol Pharm Bull. 1998; 21 (7): 723-729. [ Links ]
27. Torel J, Cillard J, Cillard P. Antioxidant activity of flavonoids and reactivity with peroxy radical. Phytochemistry. 1986; 25 (2): 383-385. [ Links ]
28. Krol W, Sheller S, Czuba Z, Matsumo T, Zydowicz G, Shani J, et al. Inhibition of neutrophils' chemiluminescence by ethanol extract of propolis (EEP) and its phenolic components. J Ethnopharmacol. 1996; 55 (1): 19-25. [ Links ]
29. Bors W, Séller W, Michel C, Saran M. Flavonoids as antioxidants: Determination of radical-scavenging efficiencies. Method Enzymol. 1990; 186: 343-355. [ Links ]
30. Marquele FD, di Mambro VM, Georgetti SR, Casagrande R, Valim YM, Fonseca MJ. Assessment of the antioxidant activities of Brazilian extracts of propolis alone and in topical pharmaceutical formulations. J Pharmaceut Biomed. 2005; 39 (3-4): 455-462. [ Links ]
31. Meneses EA. Caracterización química y evaluación de la actividad antifúngica del propóleos recolectado en el apiario de la Universidad Nacional de Colombia Sede Medellín. [Tesis de Maestría]. Colombia: Universidad Nacional de Colombia-Sede Medellín; 2006. [ Links ]
32. Salamanca G, Correa IL, Principal J. Perfil de flavonoides e índices de oxidación de algunos propóleos colombianos. Zootecnia Tropical. 2007; 25 (2): 95-102. [ Links ]
33. Kumazawa S, Hamasaka T, Nakayama T. Antioxidant activity of propolis of various geographic origins. Food Chem. 2004; 84 (3): 329-339. [ Links ]
34. Park YK, Alencar SM, Aguiar CL. Botanical origin and chemical composition of Brazilian propolis. J Agric Food Chem. 2002; 50 (9): 2502-2506. [ Links ]
35. Bankova V, Dyulgerov A, Popov S, Evstatieva L, Kuleva L, Pureb O, et al. Propolis produced in Bulgaria and Mongolia: phenolic compounds and plant origin. Apidologie. 1992; 23 (1): 79-85. [ Links ]
36. Prior RL, Wu X, Schaich K. Standardized methods for the determination of antioxidant capacity and phenolics in foods and dietary supplements. J Agric Food Chem. 2005; 53 (10): 4290-4302. [ Links ]
37. Morales G, Sierra P, Paredes A, Loyola L, Borquez J. Constituents of Helenium atacamense Cabr. J Chil Chem Soc. 2006; 51 (1): 769772. [ Links ]
38. Roginsky V, Lissi EA. Review of methods to determine chainbreaking antioxidant activity in food. Food Chem. 2005; 92 (2): 235-254. [ Links ]
39. Russo A, Cardile V, Sánchez F, Troncoso N, Vanella A, Garbarino JA. Chilean propolis: antioxidant activity and antiproliferative action in human tumor cell lines. Life Sci. 2004; 76 (5): 545-558. [ Links ]
40. Choi YM, Noh DO, Cho SY, Suh HJ, Kim KM, Kim JM. Antioxidant and antimicrobial activities of propolis from several regions of Korea. LWT Food Sci Technol. 2006; 39 (7): 756-761. [ Links ]
41. Ahn MR, Kumazawa SA, Usui YA, Nakamura J, Matsuka MB, Zhu FC, et al. Antioxidant activity and constituents of propolis collected in various areas of China. Food Chem. 2007; 101(4): 1383-1392. [ Links ]
42. Pulido R, Bravo L, Saura-Calixto F. Antioxidant activity of dietary polyphenols as determined by a modified ferric reducing/antioxidant power assay. J Agric Food Chem. 2000; 48 (8): 3396-3402. [ Links ]
43. Kahkonen MP, Hopia AI, Vuorela HJ, Rauha JP, Pihlaja K, Kujala TS, et al. Antioxidant activity of plant extracts containing phenolic compounds. J Agric Food Chem. 1999; 47(10): 3954-3962. [ Links ]
44. MacDonald-Wicks LK, Wood LG, Garg ML. Methodology for the determination of biological antioxidant capacity in vitro: a review. J Sci Food Agric. 2006; 86(13): 2046-2056. [ Links ]
45. Asami DK, Hong YJ, Barrett DM, Mitchell AE. Comparison of the total phenolic and ascorbic acid content of freeze-dried and air-dried marion-berry, strawberry, and corn grown using conven-tional, organic, and sustainable agricultural practices. J Agric Food Chem. 2003; 51 (5): 1237-1241. [ Links ]
46. Odabasoglu F, Aslan A, Cakir A, Suleyman H, Karagoz Y, Bayir Y, et al. Antioxidant activity, reducing power and total phenolic content of some lichen species. Fitoterapia. 2005; 76 (2): 216-219. [ Links ]
47. Nieva Moreno MI, Isla MI, Sampietro AR, Vattuone MA. Comparison of the free radical-scavenging activity of propolis from several regions of Argentina. J Ethnopharmacol. 2000; 71 (1-2): 109-114. [ Links ]
48. Yamauchi R, Kato K, Oida S, Kanaeda J, Ueno Y. Benzyl caffeate, an antioxidative compound isolated from propolis. Biosci Biotech Bioch. 1992; 56 (8): 1321-1322. [ Links ]
Recibido: Agosto 15 de 2009; Aceptado: Septiembre 28 de 2009
* Autor a quien debe dirigir la correspondencia: dldurango@unal.edu.co