INTRODUCCIÓN
Actualmente, existe un gran interés en el uso de pigmentos naturales como una alternativa al empleo de colorantes sintéticos, siendo el tinte extraído del arilo de las semillas de una planta tropical denominada comúnmente como achiote (Bixa orellana L.), uno de los colorantes naturales mundialmente reconocido, al haber sido utilizado en el pasado por los Aztecas para colorear alimentos, textiles, y sus cuerpos, siendo seguro para los humanos 1. Estos pigmentos, además de las aplicaciones como colorante de alimentos y bebidas, presentan propiedades medicinales asociadas a la presencia de sustancias denominadas carotenoides, que desempeñan diversas funciones en el organismo, destacándose su actividad antioxidante 2. A pesar de que dichos compuestos presentan propiedad biológica de gran interés para la industria de alimentos y de fármacos, su uso puede estar limitado debido a su baja solubilidad en agua 3, y a su inestabilidad en presencia de luz, aire, humedad y altas temperaturas 4.
Una alternativa para contrarrestar esta desventaja, es su acomplejamiento con ciclodextrinas (CDs), que permite proteger los pigmentos naturales en el medio ambiente contra la descomposición inducida por la luz, y también lograr una controlada liberación 5. Las ciclodextrinas son macromoléculas, producidas por la reacción de ciclación de pequeñas cadenas de glucopiranosa, unidas por enlaces α-1-4 mediante la acción enzimática de glucosiltransferasa. Tienen una superficie externa hidrofílica y una superficie interna hidrofóbica, característica responsable de la inclusión total o parcial de moléculas orgánicas, que interactúan con estas por enlaces de hidrógeno o fuerzas de Van der Waals 6, favoreciendo la estabilidad física y la solubilidad acuosa de las moléculas incluidas.
Tenemos que la formación de complejos, puede alterar las características físicoquímicas y biológicas (actividad antioxidante) de los compuestos incluidos 7, y hasta el momento se desconoce si la inclusión del extracto de semilla de Bixa orellana en la cavidad interna de la β-CD por el método de fluido supercrítico afecta la actividad antioxidante de los pigmentos extraídos de la planta. Por ello, para la presente investigación se planteó determinar las condiciones apropiadas de temperatura y presión de la extracción por fluido supercrítico para la obtención de un extracto de semillas de achiote (Bixa orellana L.) con una mayor actividad antioxidante, y evaluar el efecto de la inclusión en β-CD de los pigmentos sobre la capacidad captadora del radical sintético 2,2-difenil-1-picril-hidrazilo (DPPH).
MATERIALES Y MÉTODOS
Material vegetal
Se colectaron semillas de una variedad roja de Bixa orellana L., en el Jardín Botánico de Tuluá, Valle del Cauca, región con una temperatura promedio entre 24 y 27°C, ubicada a 960 m.s.n.m y con una precipitación anual media de 900 mm. Las semillas fueron sacadas de su cápsula, y sometidas a secado en un horno a una temperatura de 38°C durante 24 h. Las semillas enteras se enfriaron con nitrógeno líquido, y fueron inmediatamente trituradas en un molino con tornillo sinfín y almacenadas a -4°C en frascos ámbar para protegerlas de la luz difusa.
Condiciones de extracción supercrítica
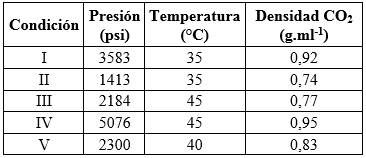
Se tomaron 11 g de semillas de Bixa orellana molidas, y se realizó la extracción con CO2 supercrítico a una pureza de 99,9 %. Se compararon cinco condiciones experimentales de extracción (Tabla 1), de acuerdo con lo reportado por Silva y colaboradores 8.
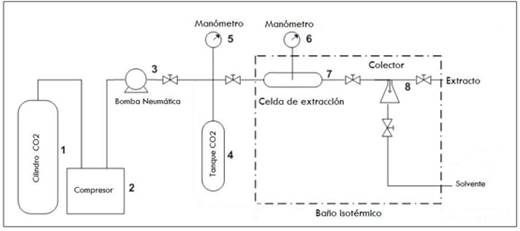
El tiempo de extracción fue de aproximadamente 45 min, debido a que después de este tiempo, el aumento del rendimiento fue mínimo. La unidad de extracción por fluido supercrítico (Figura 1) utilizada en el experimento fue diseñada en la Universidad del Valle, y consta de un cilindro de CO2 [1] con sifón, el cual abastece al equipo de tal fluido, dirigido hacia un compresor [2] que permite enfriar el CO2, a temperaturas aproximadamente de -10°C. El CO2 es bombeado con el pistón de una bomba neumática [3], hasta el cilindro de alta presión [4], cuya presión puede ser monitoreada gracias a un manómetro [5]. El tanque de alta presión se encuentra ubicado entre dos válvulas que permiten la entrada y salida del CO2. Una vez se alcanza la presión deseada, el fluido va a la celda de extracción [7] donde se ha depositado previamente la muestra y el cual también cuenta con un manómetro [6], que permite visualizar la presión de la celda de extracción. El flujo se controla manualmente por una válvula micrométrica, a medida que la extracción se lleva a cabo. El extracto y el fluido se dirigen a un colector [8], en el cual ocurre la separación del extracto y del solvente, pasando este último a estado gaseoso. Tanto la celda de extracción como el colector se encuentran sumergidos en un baño isotérmico a la temperatura de extracción deseada.
Evaluación de la actividad antioxidante de los extractos
La capacidad de captura de radicales es determinada usando el radical sintético 2,2-difenil-1-picril-hidrazilo (DPPH), el cual fue adquirido del laboratorio CALBIOCHEM, con pureza mayor a 90 %. Se prepararon por triplicado soluciones de los extractos obtenidos por FSC en metanol con concentraciones de 500, 100, 50 y 10 μg/mL. Para realizar el monitoreo de la reacción del DPPH y el extracto, se implementó el método propuesto por Pérez y colaboradores 9, mezclando 2,4 mL de la disolución metanólica de DPPH con 1,2 mL de cada solución de extracto preparada, y realizando lectura del decrecimiento de la absorbancia a 515 nm en un espectrofotómetro Thermo Spectronic Génesis 20, durante 2 h desde el tiempo cero de la reacción, tiempo durante el cual la reacción ha alcanzado el estado estacionario. Como patrón de referencia se utilizó ácido ascórbico (vitamina C), evaluándose su actividad antioxidante con las mismas condiciones descritas para las muestras. A partir de los datos obtenidos, se determinó el valor de la concentración de la muestra requerido para reducir a la mitad la concentración de DPPH (IC50), y el porcentaje de inhibición. Se realizó un análisis de varianza (ANOVA) de un factor, y un Pos-ANOVA de mínima diferencia significativa utilizando el software Minitab Statistical, para demostrar las diferencias estadísticamente significativas (p<0,01) entre los IC50 de los extractos obtenidos bajo las cinco diferentes condiciones de extracción por FSC.
Preparación del complejo de inclusión extracto y β-Ciclodextrina
Para el encapsulamiento con β-CD se eligieron como muestras, los extractos de Bixa orellana obtenidos por fluido supercrítico que presentaron la mayor actividad antioxidante, dada por el valor IC50 y por el porcentaje de inhibición. La inclusión del extracto de Bixa orellana con β-CD se realizó por fluido supercrítico con CO2. Las condiciones empleadas para la inclusión (5076 psi y 45°C) fueron aquellas en donde la densidad del CO2 fue más alta, y aquellas que dieron extractos de achiote con una mayor actividad antioxidante. Para la inclusión, se homogenizó en un mortero una mezcla de 1g de β-CD, 0,1g de extracto y 14 % de agua. Esta mezcla se vertió en un vial de vidrio, el cual fue introducido dentro de la celda de extracción. Utilizando el mismo equipo empleado para la extracción, este es presurizado lentamente una vez se alcanzó la temperatura deseada. El tiempo de contacto a presión constante fue de 6 h, de acuerdo con lo planteado por Lai y colaboradores 10 para la inclusión de Imazalil, donde se evidencia que a tiempos entre 2 y 6 h, se obtiene un aumento en la eficiencia de encapsulamiento al aumentar el tiempo de contacto.
Caracterización del complejo de inclusión
A los complejos de inclusión, se realizaron análisis espectroscópicos IR, UV-Visible, 1H - RMN, y análisis térmico DSC, cuya comparación con los análisis del extracto libre, permite evidenciar cambios que expliquen la formación del complejo de inclusión. El análisis de espectroscopia infrarroja con Transformada de Fourier (FTIR), se realizó en un instrumento FTIR- IRAfinity-1 Shimadzu, por el método de dispersión en pastilla de KBr, para los complejos de inclusión. El IR del extracto fue tomado en una placa de KBr para líquidos. Los espectros UV-Visible fueron obtenidos en un espectrofotómetro UV-Vis Shimadzu modelo 1700, en metanol, tanto para el extracto como para el complejo. Los espectros de RMN fueron adquiridos de un espectrómetro BRUKER 400 Ultrashield. Las muestras se prepararon en DMSO-d6. Los análisis de DSC se llevaron a cabo en un instrumento de la firma TA- Instruments modelo 2920, y analizados con el software Universal Analysis 2000 Versión 4.1D.41. Las medidas espectrofotométricas se realizaron en un espectrofotómetro Thermo Spectronic 20. Se realizó la calorimetría diferencial de barrido (DSC) a la β-CD, al extracto, y al complejo β-CD/Extracto preparado por FSC, con un aumento de temperatura de 10°C/min bajo atmósfera de nitrógeno. El intervalo de barrido de temperatura está comprendido entre -50 y 350°C.
Determinación de la capacidad antioxidante del complejo de inclusión
El complejo obtenido por FSC, fue disuelto en metanol, hasta lograr una concentración de 2 mg/mL, reportado como concentración de extracto, esto con el fin de realizar diluciones de 500, 100, 50 y 10 μg/mL como se hizo para los extractos libres (sin acomplejar) y de esta forma realizar comparaciones de actividad antioxidante entre el extracto libre y acomplejado en β-ciclodextrina. El procedimiento para determinar la capacidad antioxidante es el mismo que se reportó para los extractos.
RESULTADOS
Evaluación de la actividad antioxidante de los extractos
La Figura 2 muestra el porcentaje de inhibición del radical DPPH por parte de la vitamina C (VitC) control, y de los extractos de Bixa orellana obtenidos a diferentes condiciones de presión y temperatura por el método de extracción FSC.
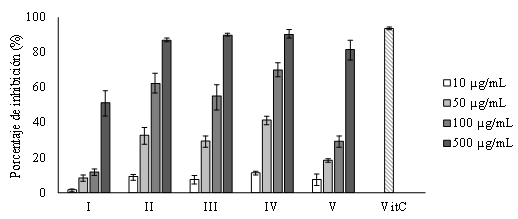
Figura 2 Porcentaje de inhibición del radical DPPH de la vitamina C (VitC), y de los extractos de Bixa orellana bajo cinco condiciones diferentes de extracción por FSC después de 30 min de reacción.
Los resultados obtenidos sugieren que el porcentaje de inhibición del radical DPPH presenta una relación directa con la concentración de las soluciones metanólicas de extracto de Bixa orellana. Por otro lado, se puede observar la mayor inhibición por parte de los extractos obtenidos por FSC a 5076 psi y 45°C (condición de extracción IV), y el menor porcentaje de inhibición bajo las condiciones de extracción No. I (3583 psi y 35°C).
En la Tabla 2, se observa que los extractos obtenidos bajo las condiciones II, III y IV presentaron similar IC50, siendo la condición IV la que presentó la mayor actividad antioxidante con un IC50 de 23,55 µg/mL. Al realizar las comparaciones estadísticas de la capacidad reductora del radical sintético DPPH de los extractos de Bixa orellana encontramos que existen diferencias significativas de las condiciones de extracción I y V respecto al resto de condiciones, las cuales presentaron la menor actividad antioxidante entre los diferentes extractos obtenidos.
Tabla 2 Actividad antirradicalaria de los extractos de Bixa orellana L., obtenidos a diferentes condiciones de presión y temperatura por FSC.
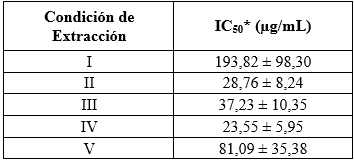
* Promedio ± Desviación Estándar. (n = 3)
Caracterización del complejo de inclusión del extracto de Bixa orellana en β-Ciclodextrina
Espectroscopia Infrarroja con Transformada de Fourier (FTIR)
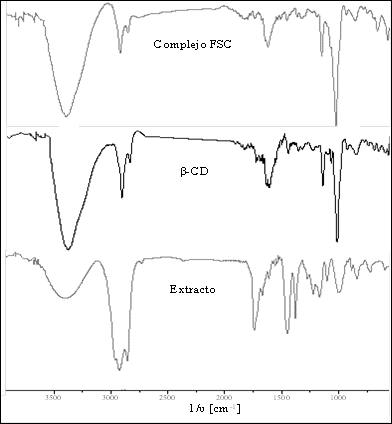
El espectro IR del extracto muestra bandas de tensión y deformación que corresponden a grupos funcionales carbonilo, O-H asociado, tensión C-H de metilos, entre otras (Figura 3).
El espectro del extracto de Bixa orellana de la figura 3 muestra bandas de absorción de tensión O-H (3378 cm-1) y C-H (2925 cm-1). Se observó una tensión C=O en 1741 cm-1, mientras que en 1449 cm-1 y 1169 cm-1 existe una deformación y estiramiento de CO/CC, respectivamente. Una deformación =C-H se puede observar en 1003 cm-1. El espectro FT-IR de la β-CD muestra bandas de absorción a 3396,79 cm-1 (Estiramiento O-H), 2923,25 cm-1 (Tensión C-H), 1646,32 cm-1 (Deformación H-O-H), 1627,99 cm-1 (Flexión O-H), 1156,38 y 1029,07 cm-1 (Estiramiento CO/CC). El espectro del complejo de inclusión obtenido por FSC (Figura 3), es muy similar al de β-CD. Ocurre un desplazamiento de la banda de deformación O-H del interior de la cavidad de la ciclodextrina, de 1646 cm-1 a 1627,99 cm-1 en el complejo de inclusión, lo que evidencia la inclusión.
Análisis térmico por Calorimetría Diferencial de Barrido (DSC)
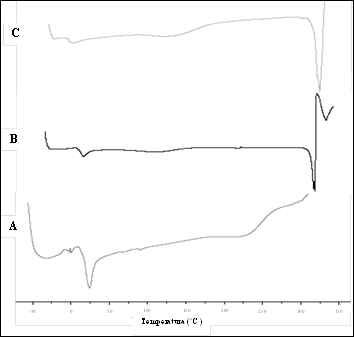
Las curvas térmicas del extracto de Bixa orellana, la β-CD y del complejo extracto/β-CD obtenido por FSC se muestran en la Figura 4.
La transición térmica del extracto a 24,32°C (Figura 4A) es debido a evaporación de los compuestos más volátiles del extracto, y aquella a 227,94°C es asignada a la descomposición del extracto; es una banda amplia que representa el gran intervalo de temperaturas de descomposición de la mayoría de moléculas que componen el extracto.
La curva DSC de la β-CD en la Figura 4.B, muestra dos picos endotérmicos: a 14,17°C correspondientes a la cristalización y otro a 111,80°C, debido a la evaporación de las moléculas de agua asociadas a la β-CD. La fusión ocurre a 220,05°C, y el pico asignado a la descomposición es más pronunciado y se localiza a 313°C. El análisis térmico para el complejo obtenido por FSC mostrado en la Figura 4.C, presenta un pico a 1,90°C correspondiente a cristalización, y a 133,91°C debido a la evaporación de moléculas de agua. La fusión ocurre cerca de 300°C e inmediatamente comienza el pico correspondiente a la descomposición en 317,49°C.
Espectroscopía de Resonancia Magnética Nuclear (RMN)
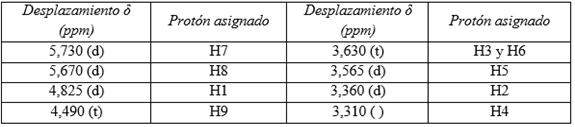
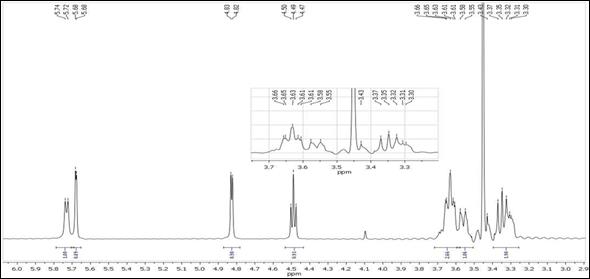
El espectro de protones de la β-CD permite asignar las señales de los protones de las unidades de α -D-glucopiranosa que conforman a esta supramolécula. Los desplazamientos se ilustran en la Tabla 3 y en la Figura 5 se observa el espectro.
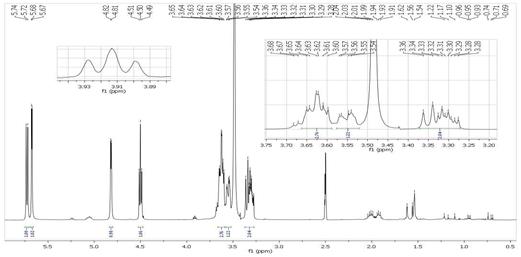
El espectro del complejo de inclusión realizado con CO2-SC (Figura 6), muestra las señales procedentes de los protones de la β-CD, y además permite ver señales de protones del extracto, sin embargo ocurre algo interesante, algunas señales desaparecen en la región de 3,9 a 4,0 ppm, pertenecientes a protones del extracto. Las señales de los protones internos de la β-CD, H3 y H5, se desplazan un poco a campo alto, el triplete que se encuentra originalmente en la β-CD correspondiente a los protones H3 y H6, se ha desplazado, se observan entonces dos tripletes desfasados, lo cual confirma que la inclusión ha tenido lugar.
Espectroscopía UV-Visible
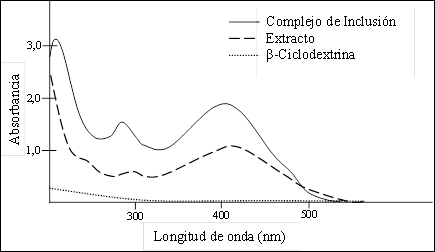
En la Figura 7 se muestra que la β-CD no presenta absorción en el rango visible del espectro; su absorción está en la región ultravioleta. Para el espectro UV-visible del extracto disuelto en metanol, se muestran dos bandas en la región ultravioleta a 211 y 296 nm, y una banda en la región visible a 422 nm. La absorción en el visible se debe a transiciones electrónicas tipo π(π*, de los dobles enlaces conjugados de las moléculas de los carotenoides presentes en el extracto. El espectro para el complejo de inclusión obtenido por FSC, presenta claramente un desplazamiento hipsocrómico o desplazamiento hacia el azul de la longitud de onda de absorción de 296 nm (extracto) a 286 nm (complejo FSC) y de 422 nm (extracto) a 399 nm (complejo FSC) relacionadas a interacciones débiles del extracto con la β-CD, de tipo enlaces de hidrógeno y fuerzas de Van der Waals, lo cual es una clara evidencia de que ha ocurrido la inclusión.
Determinación de la capacidad antioxidante del complejo de inclusión
El cálculo del IC50 del complejo de inclusión β-CD/Extracto obtenido por FSC a 5076 psi y 45°C, arrojó un valor de 104,84 µg/mL, que en comparación con el valor del extracto libre de Bixa orellana (23,55 µg/mL), este presentó un decrecimiento considerable en su capacidad antioxidante, después de la inclusión en la β-ciclodextrina.
DISCUSIÓN
La reacción del radical DPPH frente a los extractos de Bixa orellana (Figura 2) tiene su efecto, por la presencia de diversos compuestos, entre éstos la bixina, la cual es un carotenoide que actúa como antioxidante, y que ha demostrado tener capacidad de desactivar radicales y detener reacciones en cadena de la oxidación in vivo e in vitro11. La aparición de estas sustancias antioxidantes en el extracto se debe a que las propiedades de solubilidad del CO2 favorece la obtención en mayor proporción de sustancias lipídicas, las cuales se extraen a partir de densidades de CO2 de 0,4 g.mL-1, que llevan consigo sustancias solubles como tocoferoles, carotenos o esteroles 12.
Estos resultados concuerdan con la literatura, donde se expone que los metabolitos mayoritarios en las semillas de Bixa orellana son los apocarotenoides, bixina y norbixina; además, la solubilidad de la bixina es mayor en los lípidos provenientes de las mismas semillas, de acuerdo a lo reportado por Silva et al . ( 8, quienes indican que los lípidos de las semillas actúan como co-solventes en la extracción con CO2 supercrítico, incrementando la solubilidad de la bixina en CO2 más de diez veces que cuando se encuentra en estado puro.
La mayor actividad antioxidante dada en los extractos obtenidos por FSC bajo la condición IV de mayor presión y temperatura, 5076 psi y 45°C respectivamente, puede deberse a que el aumento de la temperatura a presión constante por encima de 28 MPa (4061 psi) en la extracción con CO2 supercrítico, contribuye favorablemente el aumento de la solubilidad del extracto 8, llevando consigo una mayor cantidad de los componentes necesarios para que se dé el proceso de reducción del radical DPPH.
Por otro lado, el complejo del extracto con la β-CD muestra poca actividad antioxidante, la cual pudo verse afectada por el modo de formación del complejo, al existir un enmascaramiento de los grupos funcionales específicos para el efecto antioxidante 13. La formación del complejo entre el extracto y la β-CD fue evidenciada por la completa desaparición de señales por IR del extracto en el complejo de inclusión realizado por FSC, lo cual pueden deberse a que la relación β-CD/extracto es muy grande y por ello es muy difícil verlas, ya que las señales de β-CD pueden enmascararlas. El comportamiento del complejo de inclusión obtenido por FSC, puede ser explicado admitiendo que la señal del grupo carbonilo que desaparece en el complejo de inclusión se debe a la interacción intermolecular de las moléculas del extracto incluidas con el interior de la β-CD estableciendo un nuevo enlace de hidrógeno. Las moléculas insertadas en el interior de la cavidad pueden experimentar variación del momento dipolar. Considerando que la estructura de las sustancias puras ha sufrido completamente un re-arreglo en la estructura del complejo, se pueden presentar señales de intensidad reducida o éstas pueden desaparecer completamente en el complejo, por el efecto protector de la β-CD.
Los datos del análisis térmico también permiten determinar que el fenómeno de inclusión se ha efectuado ya que han desaparecido los procesos térmicos relacionados con el extracto, de acuerdo con lo reportado en la literatura por Sauceau et al.14.
CONCLUSIONES
Los extractos de Bixa orellana obtenidos por fluido supercrítico presentaron una respuesta diferencial en su actividad antioxidante por las variaciones en el proceso de extracción, logrando un extracto óptimo a 5076 psi de presión y 45°C de temperatura. La actividad antioxidante del complejo entre el extracto de Bixa orellana y la β-CD, considerablemente inferior a la capacidad antioxidante del extracto puro, permite inferir la protección de la β-CD al extracto del ataque de radicales como el DPPH, al hacerlo menos disponible y/o menos reactivo, retardar de ésta forma la reacción oxidativa. Se confirmó la inclusión de las moléculas del extracto en la cavidad de la β-CD, mediante las técnicas espectroscópicas de IR, UV-Visible, 1H - RMN y con el análisis térmico DSC.