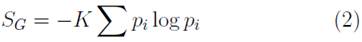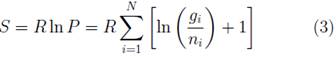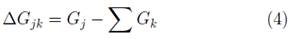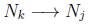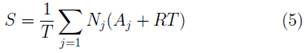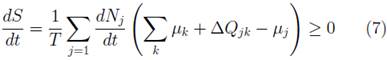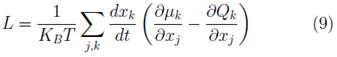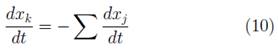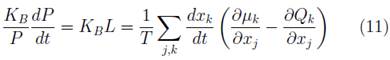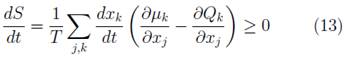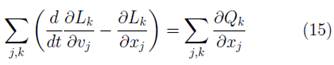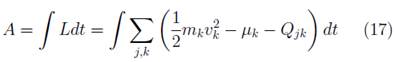Introducción
Con el desarrollo de la termodinámica estadística, se ha podido describir la evolución de sistemas termodinámicos. En los últimos anos, se ha propuesto que los sistemas termodinámicos evolucionan hacia estados de menor energía libre, contribuyendo de esta manera al incremento de la entropía del universo [1,2]. Asimismo, se ha desarrollado la teoría de la evolución biológica de Darwin; sin embargo, esta teoría no integra los principios termodinámicos en sus postulados. Por lo tanto, se ha venido desarrollando una teoría termodinámica de la evolución biológica [3,4]. En definitiva, este trabajo presenta algunos de los planteamientos de la teoría termodinámica de la evolución biológica; asimismo, se plantea una hipótesis que explica la rápida evolución de los sistemas biológicos.
Termodinámica y evolución biológica
En el siglo XIX, Ludwig Boltzmann desarrollo un modelo matemático que describe las propiedades macroscópicas de la materia. En este sentido, Boltzmann, explicó la heterogeneidad molecular en términos estadísticos; por tanto, planteó el concepto de entropía. Segán Boltzmann la entropía de un sistema es [5]:
Donde K es la constante de Boltzmann y W es el número de microestados [5].
Por otro lado, Willard Gibbs describió la entropía en términos probabilísticos, introduciendo la siguiente ecuación [5].
Donde ρi es la probabilidad de que una partícula este en un microestado i [5].
Por lo anteriormente expuesto, el modelo de Boltzmann presenta la evolución en términos cuantitativos, y representa una explicación mecanicista de la evolución de los sistemas termodinámicos. En contraste a este modelo, la teoría de la evolución biológica de Darwin describe la evolución como un proceso dinámico, donde distintas especies compiten por recursos y espacio a lo largo del tiempo. En este proceso se generan mutaciones que permiten la adaptation de organismos vivos al medio en el que viven. Asimismo, se desarrolla la selección de organismos con rasgos fenotípicos que se adaptan mejor a su medio ambiente, proceso conocido como selección natural [5].
Esta aparente discordancia entre la termodinámica y la teoría de la evolución biológica, ha llevado al desarrollo de planteamientos matemáticos que tratan de explicar la evolución biológica en términos termodinámicos [3].
Termodinámica de la evolución biológica
La teoría termodinámica de la evolución biológica es una serie de planteamientos, de diversos autores, que describe la evolución de sistemas biológicos; mediante modelos matemáticos [3,4,6]. De forma similar a la ecuación 2, la relación entre probabilidad y entropía en un sistema homogéneo, puede ser descrita por la siguiente ecuación [3].
Donde N = Σ n i , N representa el número de partículas en el nivel de energía E i ; R es la constante de los gases ideales; g es la degeneración que puede existir entre las diferentes partículas, degeneración es un término que denota varias partículas en un mismo nivel energético [3].
El concepto entropía, planteando en este trabajo, se refiere a los gradientes energéticos que existen entre los sistemas abiertos en el universo. Por lo tanto, que un sistema abierto tenga entropía alta se refiere a que tiene baja energía potencial en comparación con sus alrededores, por lo que está en equilibrio; por el contrario un sistema abierto con entropía baja posee alta energía potencial y tiende a evolucionar hacia un estado de equilibrio [3].
Se considera que la probabilidad para que una determinada reacción química se lleve a cabo, es dependiente de la disponibilidad de determinado sustrato Nk. Por lo tanto, la variación de la energía libre de Gibbs de la reacción ((Gjk) será [3]:
Donde Gj es la energía libre de Gibbs del producto y Gk es la energía libre del sustrato [3].
Para una mejor description de la evolución de un sistema abierto; consideremos la evolución de un sistema abierto en un estado inicial k de mayor energía libre Gibbs a un estado j de menor energía libre. Por lo que se puede representar dicha evolución como [3]:
La entropía de este sistema estará definida por [3]:
Donde la afinidad (A j ) = Σ μk + (Qjk - μj, μ es el potencial químico, (Qjk es la energía externa que puede acoplarse, R es la constante de gases ideales y T es la temperatura [3].
De acuerdo con la segunda ley de la termodinámica, la entropía en el universo tiende a elevarse. Por tanto, la entropía puede ser expresada como [3]:
Donde S es la entropía y t es el tiempo [3]. En resumen tenemos que [3]:
Como observamos en la última ecuación, las reacciones químicas avanzan hacia estados de menor energía libre de Gibbs; con la conversión de sustratos más reactivos en productos más estables, suele liberarse energía (reacciones alergénicas) [3]. Por lo tanto, existe en la naturaleza la tendencia a degradar la energía potencial de los sistemas abiertos [2].
Principio de mínima acción, disipación y evolución biológica
Los sistemas abiertos evolucionan en el tiempo, disminuyendo los gradientes energéticos que los caracterizan, mediante flujo de energía [7].
Consideremos la densidad energética (k, donde densidad energética se entiende como la energía potencial de un sistema, en la posición xk; este sistema evoluciona en un tiempo t hacia una densidad energética ( j · en la position X j . De acuerdo con la segunda ley de la termodinámica, descrita en términos de probabilísticos [7]:
Donde P es probabilidad, t es tiempo y L es definido por la siguiente ecuación [7]:
Donde μ es el potencial químico, Q es la disipación, K B es la constante de Boltzmann, T es temperatura y el cambio de la position (dx k /dt) es descrita por la ecuación [7]:
Reemplazando la ecuación 9 en 8, tenemos que [7].
Reemplazando la ecuación 6 en la ecuación 8, tenemos que [7]:
Por tanto reemplazando la ecuación 11 en la ecuación 12 y 6, tenemos que [7]:
La ecuación 13 describe la evolución de un sistema abierto, podemos ver que cuando existe una diferencia en el potencial químico de un sistema con sus alrededores; el potencial μK tiende a disminuir hasta alcanzar un equilibrio donde [7]:
Por otro lado, la ecuación Euler-Lagrange describe el movimiento disipativo [7]:
Donde Lk (L k = Kk - Uk) es el lagrangiano, K es la energía cinética, U es la energía potencial y vj es descrita por la ecuación [7]:
Por último, se ha descrito la acción de un sistema abierto como [7]:
Donde 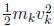 es la energía cinética en la position x
k
, μ es el potencial químico y Q es la disipación. Siendo la disipación (Q) : Q = Kk + Uk. En esta ecuación podemos ver que en la evolución de un sistema abierto, este evoluciona hasta un estado donde el gradiente químico o gradiente energético se ha nivelado con sus alrededores [7].
es la energía cinética en la position x
k
, μ es el potencial químico y Q es la disipación. Siendo la disipación (Q) : Q = Kk + Uk. En esta ecuación podemos ver que en la evolución de un sistema abierto, este evoluciona hasta un estado donde el gradiente químico o gradiente energético se ha nivelado con sus alrededores [7].
Por lo tanto, el principio de mínima disipación impulsa a los sistemas con potenciales químicos altos a evolucionar hacia sistemas con un potencial químico mas bajo, y de esta manera alcanzar un equilibrio con sus alrededores [7].
Los sistemas biológicos no están exentos a estos eventos, ya que son considerados como sistemas abiertos. De la misma manera que los sistemas abióticos, los sistemas biológicos evolucionarían hacia un estado de mínima disipación [2,7].
Recientemente se ha propuesto una cuarta ley de la termodinámica, la cual señala que los sistemas que no están en equilibrio tienden a evolucionar hacia el equilibrio. En este proceso estos sistemas incrementan la entropía de sus alrededores y su velocidad de generación de entropía. Simultáneamente se forman estructuras organizadas y complejas. Por lo tanto, este estudio propuso que los sistemas biológicos evolucionarían hacia a un estado con mayor velocidad de generación de entropía [8].
Por otro lado, se ha planteado que los sistemas disipativos, entiéndase este término como sistemas abiertos que incrementan la entropía de sus alrededores, mantienen su estado de desequilibrio mediante la continua generación de entropía en sus alrededores. Por lo que el desorden generado fuera del sistema produce estructuras organizadas y complejas dentro del sistema [9].
Hipótesis del mínimo recorrido
En este apartado describiré una hipótesis que pretende explicar la rápida evolución de los sistemas biológicos. Consideremos una molécula con elevada reactividad (lo cual se entiende como elevada energía potencial 3, dicha molécula posee una energía potencial U, al entrar en contacto con su medio reaccionaría con otras moléculas, y transferiría parte de su energía potencial hacia otros sistemas. Esta interacción con otros sistemas, generaría un movimiento; por lo que parte de su energía potencial se transformaría en energía cinética K [10,11]. Por lo tanto, las moléculas con energía potencial tienden a disminuir sus gradientes energéticos, y esta diminución seria consecuencia de la segunda ley de la termodinámica [2].
De acuerdo con el principio de mínima acción, el recorrido que toma esta molécula siempre es el que tiene la mínima acción [7]. Por tanto, podríamos preguntarnos ¿cual es el recorrido que toma un sistema abierto?
Siguiendo con el ejemplo, una molécula con alta energía potencial, puede tomar una serie de caminos; sin embargo, solo toma el camino en cual disminuye más rápido los gradientes energético [7]. Por lo tanto, se puede resumir el principio del tiempo mínimo con el siguiente enunciado:
La evolución de sistemas abiertos con energía potencial siempre se da en el menor tiempo [12].
Por lo tanto, para todo proceso evolutivo, la entropía final siempre es mayor que la inicial [7]; la variación de la entropía de un sistema abierto, en un estado de desequilibrio con sus alrededores, podría ser descrita por la siguiente ecuación [7]:
Donde S es entropía y t es el tiempo [7].
Para una mejor descripción de la hipótesis planteada, en este trabajo, introduciré el término eficiencia en la degradación de gradientes energéticos (EDGE). Donde EDGE, es la velocidad de transformación de sistemas abiertos, con energía potencial alta, de sus alrededores en sistemas abiertos con menor energía potencial.
Consideremos un sistema biológico X i evoluciona hacia uno Xf (Figura 1). De acuerdo con lo planteando, el sistema Xi tendría menor EDGE, por lo que en este estado inicial existe un mayor gradiente energético en sus alrededores. Por tanto de acuerdo con lo planteado, este sistema evolucionaría hacia un estado de mayor EDGE. En definitiva, este sistema podrá tomar una serie de caminos desde X i a X f; sin embargo, de acuerdo con el principio del tiempo mínimo, este recorrido siempre será rectilíneo.
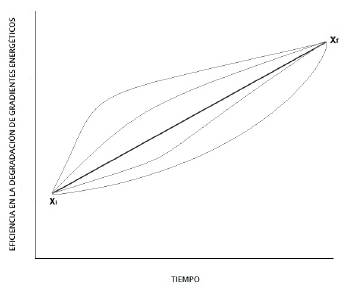
FIGURA 1 Se observan algunas posibles curvas que pueden unir los puntos (Xi y X f ). Cada punto representa un estado en la evolución de un sistema biológico. El eje horizontal representa el tiempo y el vertical, la eficiencia en la degradación de gradientes energéticos. De acuerdo con lo planteado, el camino que tomarla el sistema biológico X i sería una línea recta.
En conclusión, la hipótesis del mínimo recorrido plantea que en un proceso evolutivo, un sistema biológico incrementa su EDGE; y este incremento es directamente proporcional al tiempo. De esta manera, los sistemas biológicos transforman los sistemas abiertos de sus alrededores e incrementan la entropía del universo. Por lo que se satisface la segunda ley de la termodinámica.
Discusión
Los organismos biológicos se rigen por las mismas leyes termodinámicas que rigen los cuerpos inanimados; por tanto se esperaría que siguieran la misma evolución. Sin embargo, la complejidad de estos sistemas hizo pensar por mucho tiempo que seguían principios distintos; estos principios fueron unificados en la teoría de la evolución biológica de Darwin [3,7].
En las últimas décadas se ha desarrollado una teoria que explica la evolución biológica, como un proceso en donde los seres vivos utilizan los recursos de su medio ambiente para generar complejidad estructural, mantener y reproducir dicha complejidad. En el marco de esta teoría, se considera la evolución biológica como un proceso en el que se reducen los potenciales energéticos [3].
El concepto EDGE, introducido en este trabajo, es similar al concepto de velocidad de generación de entropá (introducido en la cuarta ley de la termodinámica). Asimismo, ambos experimentan un incremento en función al tiempo [8]. Sin embargo, el concepto EDGE se sustenta en la segunda ley de la termodinámica y el principio de mínima acción.
De acuerdo con la hipótesis planteada, en este trabajo, el tiempo que le tomaría a un organismo en evolucionar es el mínimo. Este hecho guarda relación con el surgimiento, en los últimos 60 años, de resistencia a diferentes antimicrobianos [13]. Asimismo, la presencia de regiones de ADN no codificante, por ejemplo transposones, en la mayoría de eucariotas; ha llevado a pensar que su presencia se debería a que serían blanco de mutaciones o al ser ADN móvil podrían transferirse a otras regiones de ADN y convertirse en genes. Por lo tanto, la presencia de ADN no codificante podrá ser una ventaja evolutiva [14]. Probablemente, la presencia de regiones de ADN no codificante conlleve a una mayor probabilidad de adquirir, en el futuro, una mayor capacidad para degradar gradientes energéticos [15].
Por otro lado, una energía libre de Gibbs negativa no nos proporciona información sobre el tiempo que demoran en convertirse los sustratos en productos; ya que para que ocurra una reacción química se debe superar una energía de activación. Esto explica por qué muchas reacciones químicas necesitan de catalizadores. Numerosas reacciones bioquímicas suelen ser termodinámicamente favorables, por ejemplo la combustión de la glucosa; sin embargo, estas reacciones suelen ser lentas en condiciones no enzimáticas. Por tanto la aparición de las enzimas posibilito el desarrollo de la vida. Teniendo en cuenta que muchas de las mutaciones se dan en genes que codifican enzimas; por lo que estas mutaciones favorecerá el desarrollo de enzimas más eficientes. Lo que se entiende como enzimas que catalizan reacciones químicas en un menor tiempo [16]. En definitiva, la aparición de las enzimas será consecuencia de la hipótesis planteada.
Conclusiones
La hipótesis planteada, en este trabajo, explica la rápida evolución de los sistemas biológicos. Asimismo, los gradientes energéticos determinan el curso de la evolución, desde sistemas con alta energía potencial a menor energía potencial.
Un mayor entendimiento de los principios y leyes termodinámicas nos conducirán a una teoría termodinámica que explique la evolución biológica y el origen de la vida.