Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Ingeniería
Print version ISSN 0121-4993
rev.ing. no.30 Bogotá July/Dec. 2009
Relación entre el efecto hidrofóbico superficial de carbones activados y la entalpía de inmersión en soluciones acuosas de fenol, 4-nitro fenol y 3-cloro fenol
Relation between Surface Hydrophobic Effect of Activated Carbons and the Immersion Enthalpies in Phenol, 4-Nitro Phenol and 3-Chloro Phenol Aqueous Solutions
Liliana Giraldo
PhD. Profesora Asociada. Departamento de Química, Facultad de Ciencias. Universidad Nacional de Colombia. Bogotá D.C., Colombia.
lgiraldogu@unal.edu.co
Juan Carlos Moreno
PhD. Profesor Titular. Departamento de Química. Facultad de Ciencias. Universidad de los Andes. Bogotá D.C., Colombia.
jumoreno@uniandes.edu.co
Recibido 8 de abril de 2008, modificado 24 de agosto de 2009, aprobado 31 de agosto de 2009.
PALABRAS CLAVES
Adsorción de fenoles, acidez y basicidad, calorimetría de inmersión, pHPZC, entalpía de inmersión.
RESUMEN
Para cinco carbones activados, obtenidos de materiales lignocelulósicos, se determinan las entalpías de inmersión en soluciones fenólicas. Los carbones activados son de carácter básico con valores del pH en el punto de carga cero, pHPZC, entre 7.4 y 9.7. Se determina la entalpía de inmersión de los carbones activados en CCl4 y agua; a partir de estos resultados, se calcula el factor hidrofóbico, fh, que varía entre 2.98 y 6.75. Las entalpías de inmersión de los carbones activados en soluciones de fenol, 4-nitro fenol y 3-cloro fenol están entre 7.6 y 13.9; 12.7 y 20.5; 6.8 y 11.4 Jg-1 respectivamente.
KEY WORDS
Acidity and basicity, immersion calorimetry, pHPZC, immersion enthalphy, phenols adsorption.
ABSTRACT
For five activated carbons, obtained from lignocellulosic materials the, immersion enthalpies in phenolic solutions are determined. The activated carbons have basic character with values of pH in the point of zero charge, pHPZC, between 7.4 and 9.7. The immersion enthalpies of activated carbons in CCl4 and water are determined, from these results the hydrophobic factor, hf, are calculated, that change between 2.98 and 6.75. The immersion enthalpies of the activated carbons in phenol, 4-nitro phenol and 3-chloro phenol solutions are between 7.6 y 13.9; 12.7 y 20.5; 6.8 y 11.4 Jg-1 respectively
INTRODUCCIÓN
Las entalpías de inmersión de sólidos porosos en líquidos polares, con los que no interactúan, se pueden relacionar con el área superficial del sólido considerado a través de los modelos desarrollados por Dubinin y Stoeckli [1, 2].
Cuando se utiliza otro tipo de líquido de inmersión, se logra información sobre las interacciones con la superficie química producidas entre el sólido y el líquido; esta situación se presenta cuando se utilizan soluciones con diferentes solutos, que pueden ser ácidos, bases, compuestos orgánicos e iones metálicos, como líquido de inmersión; en este caso, el valor del calor determinado involucra las interacciones del líquido y de las sustancias disueltas con los grupos funcionales superficiales, que son de tipo específico y, por tanto, de magnitud diferente que cuando se usa un solvente no interactuante [3].
La calorimetría es una técnica que permite obtener información con respecto a las interacciones que se producen entre un sólido y diferentes líquidos de inmersión. La intensidad del efecto de calor lleva a establecer comparaciones y relaciones entre diferentes características de los sólidos porosos. De esta forma, la determinación del calor de inmersión, en unas condiciones específicas, constituye un parámetro adicional en la caracterización de los sólidos, tal como lo son el área superficial, el volumen de poros, el contenido de sitios activos, entre otros [4, 5].
Una de las aplicaciones de los carbones activados es la de remover compuestos orgánicos de aguas. Para esta aplicación particular, uno de los aspectos que tiene mayor influencia en la adsorción es la química de la superficie, que depende del contenido de heteroátomos, principalmente grupos con oxígeno que determinan en los carbones activados la carga de la superficie, la hidrofobicidad y la densidad electrónica de las capas grafénicas [6, 7].
En este trabajo se estudian cinco muestras de carbón activado, obtenidas mediante activación física, con porcentajes de activación alrededor de 20%, a los que se les determina el punto de carga cero, el contenido total de grupos ácidos y básicos, la entalpía de inmersión en CCl4 y en agua, la adsorción y entalpía de inmersión en soluciones acuosas de fenol, 4-nitro fenol y 3-cloro fenol. Con los resultados obtenidos, se calcula un factor hidrofóbico que indica cómo influye la condición de la superficie del carbón activado en la interacción entre éste y las soluciones acuosas de los solutos orgánicos.
METODOLOGÍA
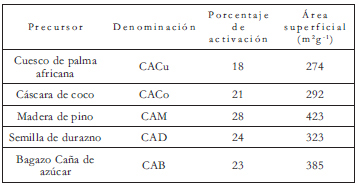
Los carbones activados que se emplean en este trabajo se han obtenido por activación física de distintos materiales lignocelulósicos en las mismas condiciones experimentales, de tal forma que las características superficiales finales de cada uno de éstos se deba a la naturaleza del material precursor [8]. En la Tabla 1 se presentan: el material precursor, la denominación, el porcentaje de activación y el área superficial de los carbones activados que se estudian en este trabajo.
Tabla 1. Características de los carbones activados.
DETERMINACIÓN DE LOS SITIOS ÁCIDOS Y BÁSICOS
Se determinan la acidez y la basicidad total de los carbones activados por el método de Boehm [9]. Se pesa 1.000 g de cada sólido, tanto para determinar sitios ácidos como sitios básicos. Una muestra de carbón activado se coloca en un frasco de vidrio con tapa esmerilada con 50.0 mL de NaOH, 0.1 N y otra muestra se coloca en un recipiente con 50.0 mL de HCl, 0.1N. Las soluciones permanecen con agitación y a temperatura constante de 25.0°C, durante 5 días. Se toman muestras de 10.0mL de cada una de las soluciones y se titula con la solución estándar de hidróxido de sodio o ácido clorhídrico, según sea el caso; se mide durante la titulación el pH de la solución con un pH meter CG 840B Schott.
DETERMINACIÓN DEL PUNTO DE CARGA CERO, PCZ. MÉTODO DE TITULACIÓN DE MASAS
Se pesan cantidades de los carbones activados en un rango de 0.010 a 0.600 g, cada una de las cuales se coloca en un frasco de vidrio de 50.0 mL y se le agrega 20.0 mL de NaCl, 0.1 M. Los frascos se tapan y se dejan en agitación a temperatura constante de 25.0°C durante 48 horas, para que las cargas del carbón se equilibren. Pasadas las 48 horas, se mide el pH de cada una de las soluciones con un pH meter CG 840B Schott [10].
DETERMINACIÓN DE LA CANTIDAD DE FENOL Y 4-NITRO FENOL ADSORBIDOS
Para determinar la cantidad que adsorbe cada carbón activado de los compuestos fenólicos se colocan 0.500g de éstos en frascos de vidrio y 250 mL de las soluciones acuosas de fenol, 4-nitro fenol y 3-cloro fenol con una concentración de 100 mg.L-1. Las muestras se agitan y mantienen a una temperatura de 25.0°C, durante 72 horas. La concentración de equilibrio en las soluciones después de la adsorción se determina, previa calibración, con un equipo espectrofotométrico uv-vis Milton Roy Co. Spectronic Genesys SN.
DETERMINACIÓN DE LAS ENTALPÍAS DE INMERSIÓN
En este trabajo se realizan determinaciones del calor de inmersión de los carbones activados en distintos líquidos calorimétricos, que son: CCl4, agua y soluciones acuosas de los compuestos fenólicos de 100 mg.L-1, para determinar la interacciones energéticas cuando el carbón activado está en contacto con soluciones que tienen dichos compuestos. A continuación, se hace una descripción general de la forma en que se llevan a cabo estas determinaciones.
Para determinar los calores de inmersión se usa un microcalorímetro de conducción de calor con una celda calorimétrica en acero inoxidable [11]. Se colocan en la celda 30 mL de la solución que se va a utilizar, los cuales se han mantenido en un termostato a 25.0°C; se pesa una muestra de carbón activado del orden de 0.500 g y se coloca dentro de la celda calorimétrica en una ampolleta de vidrio, se ensambla el microcalorímetro. Cuando el equipo alcanza una temperatura de alrededor 25°C, se inicia el registro de potencial de salida por un periodo de aproximadamente 15 minutos; se toman lecturas de potencial cada 20 segundos, se procede a realizar el rompimiento de la ampolleta de vidrio, se registra el efecto térmico generado y se continua con las lecturas de potencial por aproximadamente 15 minutos más; finalmente, se calibra eléctricamente.
RESULTADOS Y DISCUSIÓN
Los carbones activados se han preparado mediante carbonización en atmósfera de nitrógeno y posterior activación con CO2 a 900 °C por un período de 2 horas. En estas condiciones se obtienen materiales con porcentajes de activación del orden de 20-30 %, como es el caso de este trabajo, que corresponde a un desarrollo de área superficial moderado [12]. El análisis se centra, entonces, en la química superficial de los carbones activados que depende, en buena parte, de su contenido de heteroátomos; éstos determinan la carga de la superficie, su hidrofobicidad, acidez total y basicidad total. Tales factores intervienen en la capacidad de adsorción del carbón activado [13]; por esta razón, se han cuantificado: el contenido de grupos superficiales, el pH en el punto de carga cero, pHPZC, y la entalpía de inmersión de los carbones activados en CCl4 y en agua para relacionarlos con la adsorción de los fenoles en solución acuosa.
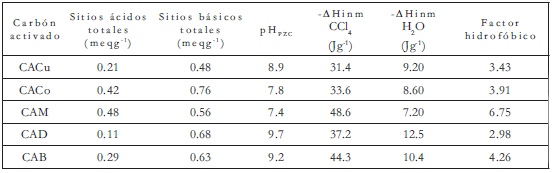
A partir de las entalpías de inmersión en CCl4 y en agua, se calcula el factor hidrofóbico, fh, que se obtiene de la relación entre la entalpía de inmersión de la muestra en CCl4 y el respectivo valor de la entalpía de inmersión en agua. De esta forma, valores altos de fh indican que la superficie del carbón activado interactúa menos con el agua. En la Tabla 1 se presentan los resultados obtenidos para la acidez y basicidad total, en meqg-1, el pH en el punto de carga cero, pHPZC, las entalpías de inmersión en CCl4 y en agua, en Jg-1 y el factor hidrofóbico fh.
Como se observa en la Tabla 2, las cinco muestras de carbones activados presentan contenidos de acidez en un rango aproximado de 0.10 a 0.50 meqg-1. La basicidad total varía entre 0.48 y 0.76 meqg-1 que muestra el carácter básico de los carbones activados obtenidos térmicamente en las condiciones descritas; sin embargo, las diferencias entre la acidez y la basicidad no son grandes y es un comportamiento comparable con los obtenidos en otros trabajos y por otros autores [14,15].
Tabla 2. Características químicas superficiales de los carbones activados
En lo referente al pH en el punto de carga cero, pHPZC, para todos los carbones activados éste es el que los clasifica como carbones activados tipo H; de tal forma que, si los sólidos se ponen en contacto con soluciones cuyo pH sea menor que el pHPZC, la carga de su superficie será en promedio positiva, que es lo que ocurre en este trabajo dado que las determinaciones de cantidad de adsorción y calorimetría de inmersión se hacen sin ajuste del pH.
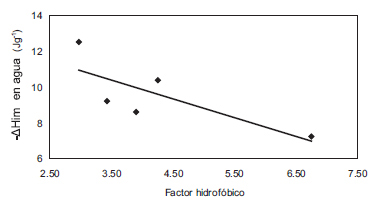
Los valores para las entalpías de inmersión son mayores en todos los casos cuando el líquido es CCl4; esto se debe al tipo de interacciones que presenta el agua con la superficie. Rutherford [16] presenta un modelo en el que las moléculas de agua ocupan sitios activos y promueven la adsorción sobre éste y sus vecindades. En la Figura 1, se presenta la relación entre las entalpías de inmersión agua en función del factor hidrófobico; se observa que a medida que aumenta el factor hidrofóbico disminuye la entalpía de inmersión en agua; el carbón activado que presenta el valor del factor hidrofóbico más alto, de 6.75, es CAM, que a su vez presenta un contenido de sitios ácidos y básicos similar.
Figura 1. Entalpías de inmersión en agua en función del factor hidrofóbico.
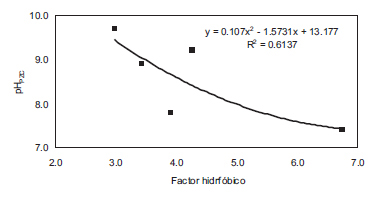
La Figura 2 muestra la relación que se establece entre el pH en el punto de carga cero, pHPZC, y el factor hidrofóbico, fh. Se observa que, a medida que los valores de fh se hacen más grandes, el pHPZC tiende a alcanzar un valor neutro ya sea porque el contenido de sitios ácidos y básicos es semejante o porque el contenido de sitios básicos es mayor y éstos se asocian a regiones ricas en electrones μ en el interior de las capas grafénicas que actúan como bases de Lewis [7]. La línea de tendencia que se traza para promediar el comportamiento de los puntos experimentales corresponde a un polinomio de segundo grado, con un coeficiente de correlación de 0.614 dada la dispersión de las muestras CACo y CAB, con respecto a la línea de tendencia
Figura 2. Relación entre el pHPZC y el factor hidrofóbico.
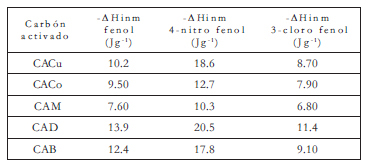
En la Tabla 3 se resumen los resultados obtenidos para la entalpía de inmersión, ΔHinm, en soluciones acuosas de los compuestos fenólicos con una concentración de 100 mg.L-1, en Jg-1.
Tabla 3. Adsorción y entalpía de inmersión de soluciones acuosas de fenol y 4-nitro fenol en carbones activados.
Las entalpías de inmersión, de carácter exotérmico, son mayores cuando se realiza la inmersión de los carbones activados en la solución de 100 mg.L-1 de 4-nitro fenol. Dado que las determinaciones se han realizado en condiciones experimentales similares, se presenta una mayor interacción entre los carbones activados estudiados y la solución de 4-nitrofenol.
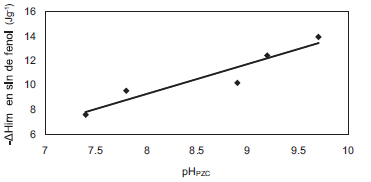
En la Figura 3, se representan la entalpía de inmersión de los carbones activados en solución de fenol y el valor del pH en el punto de carga cero, pHPZC. La entalpía de inmersión aumenta cuando el pHPZC aumenta con una tendencia lineal, que indica que la adsorción en las condiciones experimentales del trabajo se favorece cuando los carbones activados poseen valores de pHPZC más altos; es decir, cuando las características de la superficie son básicas. Cundo se observa la relación entre estos dos parámetros para la inmersión de los carbones activados en soluciones de 4-nitro fenol y de 3-cloro fenol, la entalpía de inmersión y el valor del pHPZC poseen un comportamiento semejante, lo cual indica que la adsorción para estos compuestos es mayor en los carbones activados con carácter básico.
Figura 3. Entalpía de inmersión de los carbones activados en solución acuosa de fenol y pHPZC
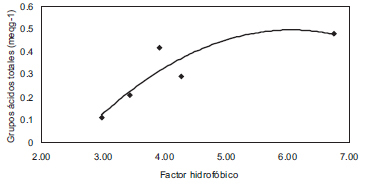
La Figura 4 muestra la relación entre el factor hidrofóbico, fh, y el contenido de grupos ácidos totales de los distintos carbones activados. La gráfica indica que, a medida que aumenta el factor hidrofóbico, el contenido de grupos ácidos también lo hace, a excepción del carbón activado obtenido a partir de cáscara de coco, CAco, que presenta un contenido de grupos ácidos de 0.42 meqg-1 y un factor hidrofóbico de 3.9, de tal forma que se sale de la tendencia general que presentan los otros carbones activados.
Figura 4. Grupos ácidos totales en función del factor hidrofóbico
Al aumentar el contenido de grupos ácidos en la superficie del carbón activado, ésta será menos hidrófoba; sin embargo, hay que tener en cuenta también el contenido de grupos básicos y el pHPZC, dado que el conjunto de estos factores determina las interacciones en superficie con los solventes CCl4 y agua, que determinan el factor hidrofóbico. Para la muestra CAM se obtiene un valor de 6.75 para el factor hidrofóbico y un contenido de grupos ácidos de 0.48 meqg-1; pero, a su vez, es la muestra que tiene menor entalpía de inmersión en agua, por tanto, se debe tener en cuenta la diferencia en la porosidad, tal como lo sugiere Cosnier [17] en su trabajo en el que se hidrofobizan varios carbones activados.
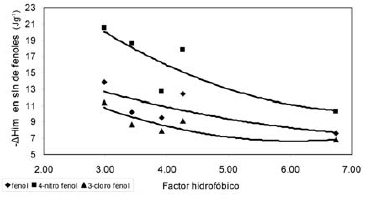
Finalmente, en la Figura 5, se presenta la relación entre las entalpías de inmersión de los carbones activados en las soluciones de los compuestos fenólicos y el factor hidrfóbico. Se observa que, a medida que el factor hidrofóbico aumenta, el calor de inmersión para las soluciones de los compuestos disminuye; esto se debe a que la interacción de la superficie del carbón con una fase acuosa se hace menor, dado que se cambia la relación de los grupos químicos en la superficie. Resultados similares se presentan en trabajos con carbones activados con valores de área superficial superiores a los de este estudio [18].
Figura 5. Relación entre el factor hidrofóbico y el calor de inmersión de carbones activados en soluciones acuosas de fenol y 4-nitro fenol
CONCLUSIONES
Se estudia las interacciones entre cinco muestras de carbón activado, obtenidas a partir de diferentes materiales lignocelulósicos con grado de activación moderado, y soluciones acuosas de fenol, 4-nitro fenol y 3-cloro fenol mediante la determinación de las entalpías de inmersión.
Se establece que los carbones activados obtenidos son de carácter básico y presentan valores para el pH en el punto de carga cero, pHPZC, que varían entre 7.4 y 9.7 y contenidos de basicidad total mayores en todos los casos que los valores obtenidos para la acidez total.
Igualmente, se determina la entalpía de inmersión de los carbones activados en CCl4 y en agua con valores mayores para la entalpía de inmersión en CCl4; a partir de los valores de las entalpías de inmersión se calcula el factor hidrofóbico, fh, que varía entre 2.98 y 6.75 para los carbones activados estudiados.
Las entalpías de inmersión en solución de fenol se hallan entre 7.6 y 13.9 Jg-1, para el 4-nitro fenol se encuentran entre 12.7 y 20.5 Jg-1 y para el 3-cloro fenol están entre 6.8 y 11.4 Jg-1; con valores mayores para todas las muestras para la inmersión en el segundo compuesto.
Se observa que el efecto de calor producido entre los carbones activados y las soluciones de compuestos fenólicos adsorbidos disminuye con el contenido de grupos ácidos y que la entalpía de inmersión de los carbones activados en soluciones acuosas de los compuestos mencionados aumenta cuando se incrementa el valor del pHPZC. Con respecto al factor hidrofóbico el calor de inmersión de las muestras disminuye al aumentar dicho parámetro, debido a que la interacción entre las fases es menor.
AGRADECIMIENTOS
Los autores agradecen al Convenio Marco entre la Universidad de los Andes y la Universidad Nacional de Colombia y al Acta de Acuerdo entre los Departamentos de Química de las dos Universidades.
REFERENCIAS BIBLIOGRÁFICAS
[1] H.F. Stoeckli and F. Kraehnbuehl. The enthalpies of immersion of active carbons, in relation of the Dubinin theory for the volume filling of micropores. Carbon. Vol. 19, No. 5, 1981, pp. 353-356. [ Links ]
[2] J. Silvestre-Albero, C. Gómez, A. Sepúlveda- Escribano and F. Rodríguez-Reinoso. Characterization of microporous solids by immersion calorimetry. Colloids and Surfaces A: Physicochemical and Engineering Aspects. Vol. 187-188, 31 August 2001, pp. 151- 165. [ Links ]
[3] M.V. López-Ramón, H.F. Stoeckli, C. Moreno- Castilla and F. Carrasco-Marín. On the Characterization of Acidic and Basic Surface Sites on Carbons by Various Techniques. Carbon. Vol. 37, No. 8, 1 January 1999, pp. 1215-1221. [ Links ]
[4] F. Stoeckli, A. Guillot, A.M. Slasli, D. Hugy-Cleary. The comparison of experimental and calculated pore size distribution of activated carbons. Carbon. Vol. 40, No. 3, March 2002, pp. 383-388. [ Links ]
[5] S. Villar-Rodil, R. Denoyel, J. Rouquerol, A. Martínez-Alonso and J.M.D. Tascón. Characterization of aramid based activated carbon fibres by adsorption and immersion techniques. Carbon. Vol. 40, No. 8, July 2002, pp. 1376-1380. [ Links ]
[6] M.J. McGuire and I.H. Suffet (eds.). Treatment of Water By Granular Activated Carbon. American Washington D.C.: Chemical Society, 1983, pp. 29-33 [ Links ]
[7] C. Moreno-Castilla. Adsorption of organic molecules from aqueous solutions on carbon materials. Carbon. Vol. 42, No. 1, 2004, pp. 83-94. [ Links ]
[8] B.A. Amaya, D.O. Rangel. Obtención de carbón activado a partir de residuos lignocelulósicos y diseño en adsorbedor para la remocion de Cr+6 y Pb+2 en corrientes acuosas. Tesis de maestría. Bogotá: Facultad de Ingenieria, Universidad de los Andes, 2004. [ Links ]
[9] H.P. Boehm. Advances in Catalysis. Eds. E.D.H.Pines, P.B.Weisz. New York: Academic Press, 1966, pp. 192 [ Links ]
[10] L. Giraldo, J.C. Moreno. Determinación de la entalpía de inmersión y capacidad de adsorción de un carbón activado en soluciones acuosas de plomo. Rev. Colomb. Quim. Vol. 33, No. 2, 2004, pp. 87-97. [ Links ]
[11] L. Giraldo, J.C. Moreno and J.I. Huertas. Heats Conduction Micro-Calorimeter With Metallic Reaction Cells. Instrumentation Science & Technology. Vol. 30, No. 2, pp. 177-186, 2002. [ Links ]
[12] F. Rodríguez-Reinoso. Activated carbon: structure, characterization, preparation and applications. Introduction to carbon technologies. Alicante, España: Universidad de Alicante (Publicaciones), 1997, pp. 60. [ Links ]
[13] L.R. Radovic, C. Moreno-Castilla and J. Rivera- Utrilla . Carbon Materials as Adsorbents in Aqueous Solutions. Chemistry and Physics of Carbon. A Serie of Advances. Vol. 27, New York, Marcel Dekker, 2000, pp. 227-405. [ Links ]
[14] C.M Diaz, N. Briceño, M.C. Baquero, L. Giraldo and J.C. Moreno. Influence of temperature in the processes of carbonization and activation with CO2 in the obtainment of activated carbon from African Palm pit. Study of the modification of characterization parameters. Internet Journal of Chemistry. Vol. 6, No. 1, 2003, pp- 1-15. [ Links ]
[15] C.A. Toles, W.E. Marshall and M.M. Johns. Surface functional groups on acid-activated nutshell carbons. Carbon. Vol. 37, No. 8, 1999, pp. 1207-1214. [ Links ]
[16] S.W. Rutherford. Application of cooperative multimolecular sorption theory for characterization of water adsorption equilibrium in carbon. Carbon. Vol. 41, No. 3, 2003, pp. 622-625. [ Links ]
[17] F. Cosnier, A. Celzard, G. Furdin, D. Begin, J.F. Mareche and O. Barres. Hydrophobisation of active carbon surface and effect on the adsorption of water. Carbon. Vol. 43, No. 12, October 2005, pp. 2554-2563. [ Links ]
[18] K. Laszlo. Adsorption from aqueous phenol and aniline solutions on activated carbons with different surface chemistry. Colloids and Surfaces A: Physicochemical and Engineering Aspects. Vol. 265, No. 1-3, 1 September 2005, pp. 32-39. [ Links ]