Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Ingeniería
Print version ISSN 0121-4993
rev.ing. no.31 Bogotá Jan./Jun. 2010
Efecto de la heterogeneidad sobre las isotermas de adsorción de carbones activados
The Effect of Heterogeneity on the Adsorption Isotherms in Activated Carbon
Jose Carlos Alexandre de Oliveira
Ingeniero Químico. Becario Postgrado FONCYT, alumno de Doctorado, Universidad Nacional de San Luis. San Luis, Argentina. alex@unsl.edu.ar
Deicy Barrera
Ingeniera Química. Becaria Postgrado FONCYT, alumna de Maestría. Universidad, Nacional de San Luis. San Luis, Argentina. deicybarrera@unsl.edu.ar
Juan Pablo Toso
Licenciado en Física. Tesista de Maestría, Instituto de Física Aplicada INFAP, Universidad Nacional de San Luis. San Luis, Argentina. jtoso@unsl.edu.ar
Raúl H. López
PhD. en Física. Investigador asistente, Instituto de Física Aplicada INFAP (CONICET), Universidad Nacional de San Luis. San Luis, Argentina. rlopez@unsl.edu.ar
Karim Sapag
PhD. en Física. Investigador adjunto, Instituto de Física Aplicada INFAP (CONICET), Profesor asociado, Universidad Nacional de San Luis. San Luis, Argentina. ksapag@gmail.com
Giorgio Zgrablich
PhD. en Física. Director, Instituto de Física Aplicada INFAP, Universidad Nacional de San Luis. San Luis, Argentina. giorgio.unsl@.gmail.com
Recibido 17 de Septiembre de 2009, modificado 8 de Junio de 2010, aprobado 15 de Junio de 2010.
RESUMEN
Los carbones activados (CA) son materiales microporosos que poseen gran capacidad de adsorción. La heterogeneidad de cualquier adsorbente, en particular la de los CA, puede ser separada en dos grandes familias: energética (o superficial) y estructural. La heterogeneidad estructural es causada por la presencia de poros de diferentes tamaños y formas, y por su posible interconexión; mientras que la heterogeneidad energética se origina por las irregularidades superficiales, así como por la presencia de grupos funcionales y/o impurezas. En este trabajo se discutirán diferentes modelos de heterogeneidad superficial en materiales con poros de geometría, tipo placas paralelas, y su efecto sobre las isotermas de adsorción y en las distribuciones de tamaño de poros.
PALABRAS CLAVES
Carbones activados, distribuciones de tamaño de poros, heterogeneidad, isotermas de adsorción.
ABSTRACT
Activated carbons (AC) are microporous materials that have high adsorptive capacity. The heterogeneity of any adsorbent, in particular of the AC, can be separated into two large families: energetic and structural. Structural heterogeneity is caused by the presence of pores of different sizes, shapes and how they are interconnected, while the energy heterogeneity is caused by surface irregularities, as well as by the presence of functional groups and / or impurities. In this paper we discuss different models of surface heterogeneity in materials with slit pores and its effect on adsorption isotherms and the pore size distributions (PSD).
KEY WORDS
Activated carbons, adsorption isotherms, heterogeneity, pore size distributions.
INTRODUCCIÓN
Las innumerables aplicaciones que poseen los materiales microporosos, como los carbones activados, han motivado un continuo interés sobre ellos, el cual se evidencia en la gran cantidad de estudios dedicados a la comprensión de sus propiedades y características. Una de sus principales aplicaciones es su uso como material adsorbente de líquidos y gases en una innumerable cantidad de procesos industriales; por ejemplo, la purificación y separación de gases, el tratamiento de aguas para su potabilización tanto a gran escala como en usos domésticos, etc.
Los carbones activados poseen una red interna de poros altamente desarrollada y una gran superficie específica, lo que los hace especialmente aptos en su aplicación como adsorbentes. Su utilidad en una aplicación en particular depende de cuatro factores: las dimensiones que tiene su red interna de poros, el volumen total de la porosidad, la extensión de su superficie interna y la magnitud de las interacciones entre el sólido y el adsorbato.
Es usual aproximar el sólido real por una colección de poros independientes de distintos tamaños y geometrías. Elegida la geometría, una de las características más importantes que el modelo busca asignar al sólido es la Distribución de Tamaño de Poros (PSD, por sus siglas en inglés) [1, 2]. Uno de los métodos utilizados para obtener la PSD de una muestra es: a partir de su isoterma experimental y utilizando un banco de isotermas de distintos tamaños obtenidas por simulación de Monte Carlo, se hace un ajuste por mínimos cuadrados entre las isotermas simuladas y la experimental, por lo que se obtiene la PSD a partir de la isoterma simulada ajustada. La adopción de un modelo geométrico de poros para modelar la estructura interna de los carbones activados es una hipótesis común; el modelo de poros usualmente adoptado para dichos materiales es el modelo de caras planas paralelas, cuyas paredes están constituidas por placas grafíticas [3]. Si bien existen numerosas cantidades de estudios sobre el proceso de adsorción en este modelo, no es aún claro que sus características sean suficientes para explicar los diferentes tipos de evolución que poseen las isotermas de adsorción en dichos materiales. Así mismo, tampoco se ha determinado claramente si el modelo de poros de placas planas paralelas puede explicar el comportamiento de los calores de adsorción de los diferentes tipos de carbones activados. Vinculada a esta cuestión se encuentra la pregunta sobre si es necesario suponer la presencia de heterogeneidad energética superficial en la interacción adsorbato-sólido, conjuntamente con la heterogeneidad estructural de dichos materiales, para explicar el comportamiento de los calores de adsorción [4].
La heterogeneidad de cualquier adsorbente, en particular la de los carbones activados, puede ser separada en dos grandes familias: energética (o superficial) y estructural. La heterogeneidad estructural es causada por la presencia de poros de diferentes tamaños y formas, y por cómo están interconectados; mientras que la heterogeneidad energética se origina por las irregularidades superficiales, así como también por la presencia de grupos funcionales y/o impurezas.
En este trabajo se discutirán modelos de heterogeneidad superficial en poros de geometría tipo placas paralelas y su efecto sobre las isotermas de adsorción y en las distribuciones de tamaño de poros.
ISOTERMA EXPERIMENTAL
SÍNTESIS DEL CARBÓN ACTIVADO
Se utilizó un carbón activado (CA) obtenido a partir de la pirolisis de cáscara de coco, el cual se activó físicamente con una mezcla de gas inerte (N2) y vapor de agua. El carbón primario se introdujo en un portamuestras y se hizo circular una corriente de N2 para desplazar el O2 presente. Luego, la muestra se calentó hasta una temperatura de 800 °C, manteniendo el suministro de N2. Finalmente, se incorporó el vapor de agua manteniendo esta mezcla activante a esta temperatura durante 1 h [5].
PROPIEDADES TEXTURALES
A partir de la isoterma de adsorción – desorción de N2 a 77 K en un equipo de adsorción volumétrico AUTOSORB-1MP (Quantachrome), se determinaron las propiedades texturales del material. El área superficial específica se estimó mediante el método de Brunauer, Emmet y Teller BET [6] y se obtuvo un valor de 860 m2/g. A partir del modelo de Dubinin Radushkevich [7] se consiguió un volumen de microporos de 0.33 cm3/g. El volumen total de poros se logró mediante la regla de Gurvich a una presión relativa de 0.98 [1] y reveló un valor de 0.36 cm3/g.
SIMULACIÓN MOLECULAR DE LA ADSORCIÓN DE COMPONENTES PUROS
Uno de los métodos más utilizado para la simulación molecular aplicada a los problemas de adsorción es el de Monte Carlo en el Gran Canónico (GCMC), debido a que en condiciones de equilibrio permite el cálculo directo de la fase adsorbida. Los fundamentos para la aplicación de este método de simulación están bien establecidos y documentados [8, 9].
En este trabajo, se modelaron las moléculas del adsorbato como esferas y se las identificó por la posición de su centro. Con esta suposición, se pueden reproducir datos experimentales para cada adsorbato con una exactitud razonable. Evidentemente, para problemas más exigentes son necesarios potenciales de interacción más precisos.
El potencial gas-gas se considera como un potencial de Lennard-Jones (LJ):
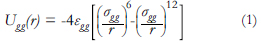
donde εgg y σgg son parámetros de energía y geometría de LJ, y r es la distancia entre moléculas. Los valores de todos los parámetros, incluso los potenciales de interacción, están dados en la Tabla 1.
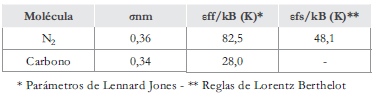
Tabla 1. Parámetros usados en la simulación
El potencial gas-sólido utilizado para el poro plano fue la superposición de dos potenciales tipo "Steele" [10], uno por cada plano infinito:
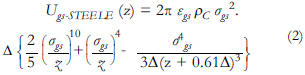
donde Δ es la distancia entre las placas de grafito, ρC es la densidad de los átomos de carbono en el grafito, z es la distancia desde el núcleo de los átomos de carbono en la superficie del plano grafito, y εgs y σgs son los parámetros de potencial de LJ utilizados en la interacción sólido-fluido. Los parámetros combinados de LJ son determinados al usar las reglas de Lorentz-Berthelot (la media aritmética del diámetro de colisión y la media geométrica de la energía εgs).
La elección del conjunto Gran Canónico como marco del esquema de simulación [9] se debe a que éste tiene como variables independientes para describir el estado del sistema al potencial químico μ (la presión p), la temperatura T y el volumen V. Este conjunto de variables es particularmente conveniente, debido a que las isotermas de adsorción simuladas (ρL) para diferentes "diámetros de poros" se pueden obtener en forma directa al evaluar para cada valor de μ(p) y para un mismo valor de la temperatura, el número medio de moléculas adsorbidas en el interior del poro. Cada paso de Monte Carlo involucra la realización de tres tipos de acciones de un estado inicial I a un estado final J: desplazamiento de una molécula preabsorbida, adsorción de una nueva molécula y desorción de una molécula. Utilizando el procedimiento de inspección de Metrópolis, las respectivas probabilidades de transición son:
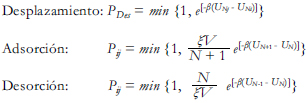
Dónde U es la energía total de interacción del adsorbato, N es el número de moléculas adsorbidas y ξ la longitud de onda de De Broglie. Las dimensiones laterales de la celda de simulación fueron de 10 nm, con condiciones de borde periódicas en esa dirección. El radio de "cutoff", distancia de corte esférica para las interacciones gas-gas fue de 5 diámetros moleculares y los tiempos de relajación fueron del orden de 1x10 7 pasos de Monte Carlo.
OBTENCIÓN DE LA PSD A PARTIR DE LA ISOTERMA DE ADSORCIÓN
Obtener la Distribución de Tamaños de Poros (DTP) de un carbón activado es de fundamental importancia en la caracterización del material, para su posterior utilización en un proceso industrial. Por lo general, el material contiene una colección de poros de diferentes tamaños S, caracterizada por una distribución f(S)dS que indica la probabilidad de tener un poro con tamaño entre S y S + dS. El problema de la caracterización del material consiste en obtener la PSD, dada por f(S)[cm3/gÅ], a partir del análisis de una isoterma de adsorción experimental realizada en ese material.
Si los poros adsorben independientemente uno de otro, la isoterma de adsorción, n [mmol/g], puede escribirse como una "superposición" de isotermas correspondientes a cada tamaño de poro, llamadas "isotermas locales", ρL[mmol/cm3], cada una con el peso correspondiente a la PSD:
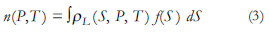
Esta ecuación puede ser discretizada al substituir la integral por una sumatoria; de tal forma que, para un punto de la isoterma correspondiente a una presión Pi, se tiene:
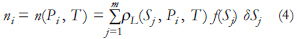
donde el intervalo de integración se ha dividido en m intervalos de tamaños δSj (que pueden ser diferentes entre sí).
Utilizando el método de minimización, se ajusta cada isoterma experimental con el banco de isotermas simuladas. Primero, se utiliza la familia de isotermas para poros planos homogéneos y, luego, con heterogeneidad para distintos cubrimientos.
La heterogeneidad superficial (en esta primera etapa) se introdujo mediante la adsorción aleatoria e irreversible de moléculas esféricas sobre la superficie interna de los poros a distintos cubrimientos θ. Dichas moléculas interactúan con las de nitrógeno mediante un potencial tipo esfera rígida y sus parámetros son iguales a los de las moléculas de carbono que forman las placas grafíticas.
RESULTADOS Y DISCUSIÓN
En la Figura 1 se observan los "snapshots" del proceso de llenado de los poros a diferentes presiones, para un determinado diámetro de poro con heterogeneidades. Puede verse cómo la presencia de la heterogeneidad desordena levemente el llenado por capas.
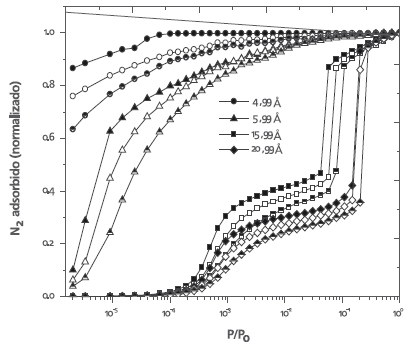
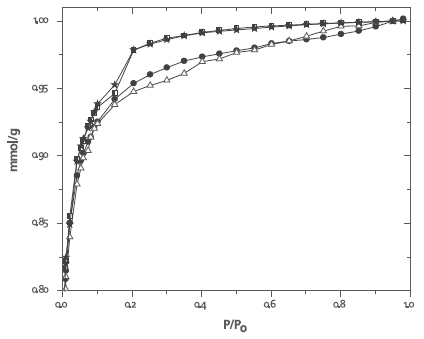
En la Figura 2 se muestra parte de las isotermas simuladas correspondientes a poros con y sin heterogeneidad. Como era de esperar, la presencia de esta clase de heterogeneidad disminuye la capacidad de adsorción del sólido, no sólo por la presencia de sitios ya ocupados, sino también por el desorden que se introduce. Dado que el mínimo de la energía gas-sólido es monótonamente decreciente hacia un valor de saturación de 2 kcal/mol para poros planos, las isotermas de adsorción se desplazan hacia mayores valores de presión conforme crece el tamaño de poro [11]. En la Figura 3 se aprecia la isoterma experimental y los respectivos ajustes al utilizar el banco de isotermas de poros homogéneos y el banco de isotermas para poros planos con heterogeneidades. Se observa claramente que los mejores ajustes se obtienen cuando se supone la presencia de una heterogeneidad al 5%.
En la Figura 4 se muestran las PSD obtenidas por la simulación de MC. Las Figura 4a representa la contribución de los poros planos homogéneos y las 4b y 4c, las correspondientes a los poros con heterogeneidad. Se destaca que las PSD obtenidas son diferentes, por lo que se tendría que usar algún criterio para escoger la más real. Dado que la isoterma que mejor ajusta a la experimental es la obtenida con una heterogeneidad del 5%, ésta sería la PSD más adecuada para esta muestra.
CONCLUSIONES
Los CA son habitualmente modelados como materiales con una única geometría del tipo placas paralelas. Esta suposición produce PSD con un aparente exceso de ultra-microporos [12]. En los resultados encontrados, podemos corroborar que esos ultramicroporos existen y que, en todo caso, el modelo que hemos denominado "homogéneo" no los presenta en exceso. La incorporación de heterogeneidad permite arribar a resultados más concordantes con la isoterma experimental, aunque es claro que habría que realizar mayores ajustes.
Figura 1. "Snapshot" del proceso del llenado para un diámetro de 16.99 Å, con heterogeneidad de 10%. Las moléculas no están en escala.
Figura 2. Isotermas simuladas: poro homogéneo (símbolos llenos), poro con heterogeneidad de 5% (símbolos vacío), poro con heterogeneidad de 10 % (símbolos semilleno)
Figura 3. Isoterma experimental (círculos) e isotermas ajustadas con los bancos de isotermas para poros planos perfectos (cuadrados), con heterogeneidades del 5% (triángulos) y 10% (estrella)
Los resultados del presente trabajo muestran que, al utilizar este simple modelo de adsorción con heterogeneidad, las PSD obtenidas están influenciadas por los sitios ocupados. Se debe destacar que en las distribuciones aparecen "huecos", alrededor de los 10 Å, lo que nos indica que el método debe ser refinado. Resultados preliminares, aún no acabados, muestran que ajustando el nivel de heterogeneidad se puede ajustar mejor la isoterma experimental y el hueco en esta región tiende a desaparecer.
Figura 4. Distribución de tamaños de poros (PSD): a) poros homogéneos, b) poros con heterogeneidad de 5%, c) poros con heterogeneidad de 10%
GLOSARIO
b Constante de Boltzmann
Δ Separación entre capas de grafito
δS Intervalo entre los tamaños de poro
ξ Longitud de onda de De Broglie
εgg Potencial de interacción gas-gas de Lennard Jones
εgs Potencial de interacción gas-sólido (Reglas de Lorentz Berthelot)
f(S) Distribución del tamaños de poro
µ Potencial químico
N Número de moléculas adsorbidas
pdes Probabilidad de transición de desplazamiento
pij Probabilidades de transición de adsorción o desorción
P Presión
π Número pi
r Separación molecular
ρc Número de átomos de carbono por unidad de volumen de grafito
ρL Isoterma simulada para un tamaño de poro
σgg Diámetro de Colisión gas-gas de Lennard Jones
σgs Diámetro de Colisión gas-sólido (Reglas de Lorentz Berthelot)
S Tamaño del poro
T Temperatura
Ugg Potencial gas-gas
Ugs Potencial gas-sólido
U Energía total de interacción del adsorbato
V Volumen accesible para el fluido
z Distancia del centro de una molécula a la placa grafítica
REFERENCIAS BIBLIOGRÁFICAS
[1] F. Rouquerol, J. Rouquerol, K. Sing. Adsorption by Powders and Porous Solids. San Diego, Academic Press, 1999. [ Links ]
[2] S. J. Gregg, K. S. W. Sing. Adsorption, Surface Area and Porosity. London, New York: Academic Press, 1982. [ Links ]
[3] H. Marsh, F. Rodríguez-Reinoso. Activated Carbon, London: Elsevier, 2006. [ Links ]
[4] G. R. Birkett and D. D. Do. "Characteristic Heats of Adsorption for Slit Pore and Defected Pore Models". Langmuir. Vol. 24, No. 9, March 2008, pp. 4853-4856. [ Links ]
[5] J.P. Toso, R. Aja Muñiz, A. Vallone, A. Fernández Rodríguez, C. R. Castillo, K. Sapag, G. Zgrablich. "Influencia del Tiempo de Activación en el Desarrollo de la Porosidad de Carbones Activados Físicamente". Anales AFA 2008, Vol. 18, pp. 208-212. [ Links ]
[6] S. Brunauer, P.H. Emmett and E. Teller. "Adsorption of gases in multimolecular layers". J. Amer. Chem. Soc. Vol. 60, No. 2, 1938, pp.309-319. [ Links ]
[7] P.A. Webb, and C. Orr. Analytical methods in fine particle technolog y. Micromeritics Instrument Corporation, Norcross, 1997. [ Links ]
[8] D. Nicholson and N. G. Parsonage. Computer Simulation and the Statistical Mechanics of Adsorption. London: Academic Press, 1982. [ Links ]
[9] M.P. Allen and D.J. Tildesley. Computer Simulation of Liquids. Oxford: Clarendon Press, 1990. [ Links ]
[10] W. A. Steele. The Interaction of Gases with Solid Surfaces. Oxford, U.K: Pergamon, 1974. [ Links ]
[11] D.C.S. Azevedo, R.B. Rios, R.H. López, A.E.B. Torres, C.L. Cavalcante, J.P. Toso, G. Zgrablich. "Characterization of PSD of Activated Carbons by Using Slit and Triangular Pore Geometries". Applied Surface Science, Vol. 256, No. 17, 15 June 2010, pp. 5191-5197. [ Links ]
[12] GM. Davies, N.A. Seaton and V.S Vassiliadis. "Calculation of Pore Size Distribution of Activated Carbon from Adsorption Isotherms". Langmuir, Vol. 15, No. 23, 1999, pp. 8235-8245. [ Links ]