Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Ingeniería
Print version ISSN 0121-4993
rev.ing. no.32 Bogotá July/Dec. 2010
Peroxidacion y flotación electrolítica de vinazas de destilería
Flotation and Peroxidation of Distillery Vinasse
Javier Andrés Dávila Rincón
M.Sc., Instructor. Departamento de Ingeniería Química, Universidad de los Andes, Bogotá D.C., Colombia. ja.davila1982@uniandes.edu.co
Fiderman Machuca Martínez
Ph.D. en Ingenieria Química, Vicedecano de Investigaciones, Universidad del Valle. Cali, Colombia. fiderman@univalle.com
Nilson Marrianga Cabrales
M.Sc. en Ingeniería Química. Profesor titular, Escuela de Ingeniería Química, Universidad del Valle. Cali, Colombia. marriaga@univalle.com
Recibido 26 de agosto de 2009, modificado 21 de septiembre de 2010, aprobado 23 de septiembre de 2010
RESUMEN
Se estudió el desempeño de la peroxidación y flotación electrolítica de vinazas empleando electrodos de acero en configuración monopolar. Se evauló la influencia de: pH inicial de la suspensión, densidad de corriente (DC) y concentración de H2O2 mediante la metodología Taguchi. Se lograron disminuciones del orden de: 63% en sólidos totales (ST), 57% en carbono orgánico total (COT) y 99,7% en turbidez. Las variables que mas infuyeron en el proceso fueron: la concentración de H2O2 y el pH inicial.
PALABRAS CLAVES
Electrofenton, electroflotación, peroxidación, Taguchi, Vinaza.
ABSTRACT
The perfonmance of the electrolytic flotation and peroxidation of vinasse was studied using steel electrodes in monopolar configuration. The influence of: initial of the suspension, density of current (DC) and concentration of H2O2 by Taguchi methodology were evaluated. Reductions were achieved in the order of 63% in total solids (TS), 57% total organic carbon (TOC) and 99.7% in turbidity. The most influential variables in the process were: the concentration of H2O2 and the initial pH.
KEY WORDS
Cane vinasse, electrofento, electroflotación peroxidation, waste distillery, Taguchi.
INTRODUCCIÓN
En Colombia, las plantas de alcohol carburante producen cerca de 11 millones de litros/día de vinaza diluida (7%-11% sólidos) con alta carga contaminante (DQO superiores a 50.000 ppm). Cerca del 60% de la vinaza producida se recircula a los fermentadores y el resto se concentra por evaporación (23%-25%), para luego destinarse a la producción de biofertilizantes mediante compostaje. Sin embargo, este esquema de procesamiento presenta alto consumo de energía térmica y elevados tiempos de residencia.
Los tratamientos electrolíticos y los procesos avanzados de oxidación de aguas residuales industriales representan alternativas promisorias para la remoción o degradación de contaminantes. Por ejemplo, combinando electrocoagulación y electroflotación [1] para el tratamiento de aguas residuales provenientes de restaurantes se alcanzaron eficiencias de remoción de 99, 9% en demanda química de oxígeno (DQO). En la electrocoagulación de aguas de la industria textil, se logró obtener remoción en turbidez y DQO de 98% y 75% respectivamente [2]; de igual forma, la remoción de boro de aguas residuales por electrocoagulación y utilizando cloruro de calcio como electrolito soporte logró eficiencias de 97% [3].
Asimismo, se ha logrado la remoción completa de nitratos en aguas superficiales por electrocoagulación y electrorreducción [4]. Se logró remover también el 99% de arsénico de aguas subterráneas usando electrocoagulación [5].
Vinazas biológicamente tratadas han sido ensayadas por métodos electrolíticos y se han alcanzado remociones superiores a 90% en DQO, DBO, COT y turbidez usando una combinación de floculación química y oxidación electrolítica [6]. Vinaza previamente tratada por evaporación y centrifugación (DQO inferior a 5.000 ppm) también ha sido sometida a tratamiento electrofenton logrando disminuciones del orden de 93% en DQO [7].
Igualmente, se trató vinaza (DQO inferior a 28.000 ppm) por electrocoagulación combinada con un adsorbente (carbón activado) obteniendo remociones de 99% en turbidez y superiores al 80% en DQO y DBO usando electrodos de acero inoxidable [8]. Se ha ensayado la electrodiálisis para reducir la deposición de sales sobre los tubos de los evaporadores durante la concentración de vinazas, disminuyendo hasta en 85% la concentración de sales [9, 10]. Estudios exploratorios [11, 12] muestran el potencial de esta técnica para el tratamiento de vinazas de destilerías colombianas.
Arienzo et al. [13] aplicaron la peroxidación para la remediación de sistemas acuosos contaminados con metales pesados y lograron remover más del 95% de la contaminación. Posteriormente, Arienzo et al. [14] también utilizaron la misma técnica para descontaminar aguas que contenían arsénico y lograron una remoción del 98%.
El propósito del presente estudio fue establecer el desempeño de la peroxidación y flotación electrolítica aplicada a vinazas provenientes de destilerías. Particularmente, se estableció el efecto de las variables: pH inicial, densidad de corriente y la concentración de H2O2 sobre la disminución en la concentración de sólidos totales y en la carga contaminante (COT y DQO).
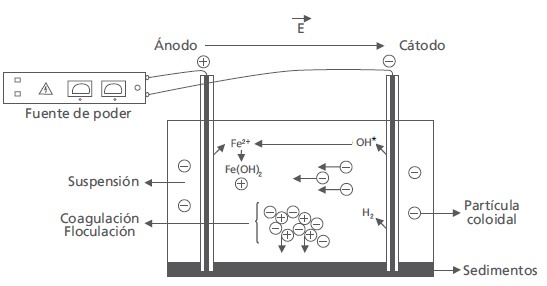
En la Figura 1 se presenta el proceso de peroxidación y electroflotación electrolítica, el cual involucra las siguientes etapas sucesivas [15, 16]:
Figura 1. Esquema conceptual de la peroxidación y electroflotación electrolítica
Además, pueden ocurrir otras reacciones fisicoquímicas como:
Por otro lado, la metodología Taguchi enfatiza la búsqueda del juego de condiciones que logren que el comportamiento del proceso esté menos influenciado por variables que no pueden controlarse (ruido); para esto, se usa la relación señal/ruido (S/N). Entre menor sea el valor de S/N, el proceso estará más afectado por variables que no pueden controlarse (N alto), por lo que se deben escoger condiciones en las que la relación S/N sea alta y se asegure así que el proceso sea lo más robusto posible [17, 18 y 19].
MATERIALES Y MÉTODOS
La vinaza cruda presentó un contenido de sólidos totales de 23%, pH de 4,3, conductividad eléctrica de 28,4 mS/cm y DQO de 160.000 ppm.
Se utilizó una celda electrolítica de 500 ml con ánodos de acero galvanizado y cátodos de acero inoxidable. Los electrodos fueron conectados en arreglo monopolar con un espaciamiento de 1 cm. El área anódica total fue de 32 cm2 y se empleó un agitador magnético fijando una velocidad de agitación de 110 rpm. Los electrodos de acero galvanizado fueron previamente decapados químicamente con el fin de remover la capa superficial de zinc empleando HCl y lijando posteriormente con lija No. 400.
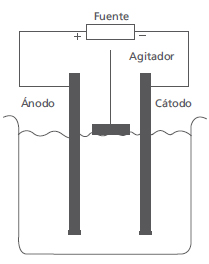
Para el suministro de corriente se dispuso una fuente de corriente GPS-S Serie INSTEK. Previo a cada ensayo, se ajustó el pH inicial de la vinaza adicionando NaOH y se ajustó igualmente la concentración de H2O2. En la Figura 2 se esquematiza el montaje experimental implementado.
Figura 2. Montaje experimental
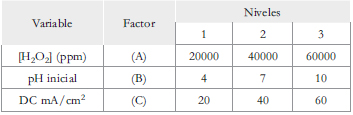
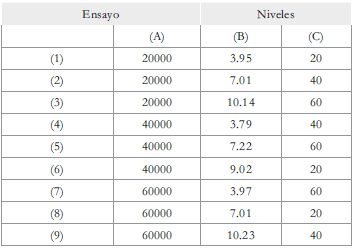
Se ejecutó un diseño experimental Taguchi L9(33), es decir, 9 ensayos con tres variables en tres niveles. Este diseño permite evaluar muchas variables en diferentes niveles con pocas medidas experimentales [20, 21, 22 y 23]. El diseño corresponde a un arreglo ortogonal, lo que significa que por cada par de columnas existen todas las combinaciones posibles de los niveles escogidos y sus factores. La Tabla 1 muestra los factores y sus niveles; la Tabla 2 resume la combinación de éstos para este diseño.
Tabla 1. Condiciones de operación del método Taguchi
Tabla 2. Combinación de factores y niveles
Se estableció el contenido de sólidos totales por medio de evaporación a 105°C en una balanza termoanalítica. Al finalizar los ensayos, se obtuvo abundante espuma en la parte superior de la celda debido a la electroflotación y un líquido clarificado remanente en la celda. Se midió el pH final y la conductividad eléctrica para el líquido formado, una vez la espuma colapsó, y para el clarificado. Para los dos ensayos con mejor remoción en sólidos totales se realizaron medidas de DQO, COT y turbidez.
RESULTADOS Y ANÁLISIS
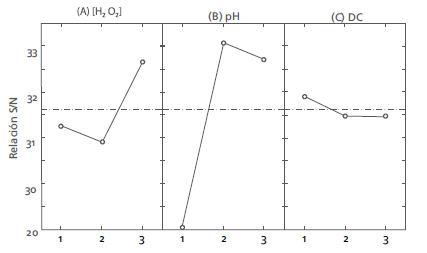
En la Figura 3 se muestra la relación S/N para cada variable sobre la remoción de sólidos totales (%RST). Las relaciones S/N indican que la variable más significativa es el pH inicial (B) y que la combinación apropiada de niveles para la prueba comprobatoria es: nivel 3 para la variable (A), nivel 2 para la variable (B) y nivel 1 para la variable (C). Esta prueba pertenece al diseño planteado y corresponde al punto (8) (60.000 ppm de H2O2, pH de 7 y 20 mA/cm2 ).
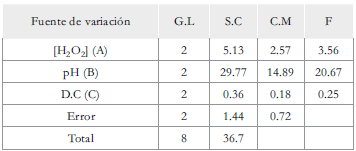
La Figura 3 concuerda con el análisis de varianza ANOVA; la Tabla 3, por su parte, muestra el análisis de varianza para el diseño planteado. La variable pH inicial (B) tuvo la mayor influencia sobre la recomición de solidos totales (por el valor de F), seguida por la concentración de H2O2 (A). Mientras que la densidad de corriente (C) tuvo poca influencia sobre la variable tal como lo indica la relación S/N de la Figura 3.
Tabla 3. Análisis de varianza
Figura 3. Relaciones S/N para cada variable y nivel (la línea a trazos indica la media)
EFECTO DEL PH
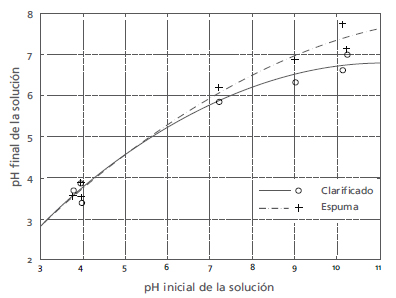
El comportamiento del pH final de la suspensión clarificada y de la espuma se representa en la Figura 4. Se evidencia una mayor disminución del pH cuando se trabaja bajo condiciones alcalinas que cuando se trabaja bajo condiciones ácidas.
Figura 4. Comportamiento del pH final de la solución
Esto sugeriría que existe una alta formación de hidróxidos insolubles de hierro que precipitan en medio básico [24]. Partiendo de condiciones alcalinas se lograron mejores remociones en DQO indicando la efectividad de la formación de compuestos o complejos básicos y su eliminación por flotación [6].
EFECTO DE LA DENSIDAD DE CORRIENTE
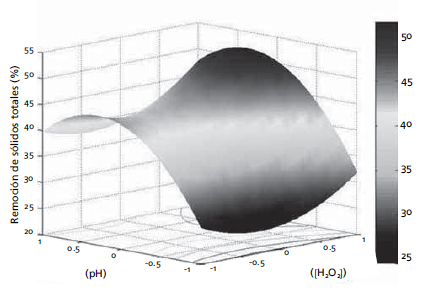
Aunque la densidad de corriente fue la variable menos influyente en la remoción de sólidos totales, determina la cantidad de iones metálicos que pasan a la suspensión. La Figura 5 muestra la superficie de respuesta para una densidad de corriente de 20 mA/cm2, condición en la que se obtuvo la máxima remoción de sólidos totales.
Figura 5. Superficie de respuesta para %RST a DC = 20 mA/cm2
Las condiciones que favorecieron la disminución de sólidos corresponden a concentraciones altas de H2O2 y condiciones alcalinas (pH superior a 7). Se lograron remociones de sólidos totales más altos con densidades de corrientes bajas, debido a que la eficiencia de la corriente disminuye a medida que ésta aumenta.
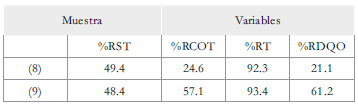
La Tabla 4 muestra la remoción de sólidos totales (%RST), turbidez (%RT), COT (%RCOT) y DQO (%RDQO) para las muestras (8) y (9), las cuales presentaron la mayor remoción de sólidos totales, 49,4% y 48,4% respectivamente.
Tabla 4. Porcentajes de remoción de COT, turbidez y DQO para los ensayos (8) y (9)
CONCLUSIONES
Combinando la peroxidación y la flotación electrolítica se consiguió reducir el contenido de sólidos totales en 63%, el contenido de carbono orgánico total (COT) en 57%, en turbidez cerca de 93% y en DQO cerca de 61% a partir de vinaza concentrada de destilería (23% sólidos).
Para la disminución de DQO, COT, turbidez y sólidos totales fue necesario emplear altas concentraciones de peróxido de hidrógeno; sin embargo, si se requiere conseguir altas reducciones de COT y DQO se pue de usar concentraciones intermedias de peróxido de hidrógeno pero es necesario usar pH alto (alrededor de 9-10) y densidades de corriente bajas (cercanas a 20 mA/cm2), lo que favorecería un menor consumo de electricidad.
REFERENCIAS BIBLIOGRÁFICAS
[1] C. Xueming, C. Guohua, P. L. Yue. "Separation of pollutants from restaurant wastewater by electrocoagulation". Separation and Purification Technology, Vol. 19, No. 1-2, 1 June 2000, pp. 65-76. [ Links ]
[2] K. Mehmet, T. C. Orhan, B. Mahmut. "Treatment of textile wastewaters by electrocoagulation using iron and aluminum electrodes". Journal of Hazardous Materials, Vol. 100, No. 1-3, 27 June 2003, pp. 163-178. [ Links ]
[3] A.E. Yilmaz, R. Boncukcuoglu, M,M. Kocakerim, B.Keskinler. "The investigation of parameters affecting boron removal by electrocoagulation method". Journal of Hazardous Materials, Vol. 125, No. 1-3, 17 October 2005, pp. 160-165 [ Links ]
[4] A.S. Koparal and U.B. Ogutveren. "Removal of nitrate from water by electroreduction and electrocoagulation". Journal of Hazardous Materials, Vol. 89, No. 1,4 January 2002, pp. 83-94. [ Links ]
[5] R. J. Parga, D. L. Cocke, J. L. Valenzuela, J. A. Gomez, M. Kesmez, G. Irwin, H. Moreno, M. Weir. "Arsenic removal via electrocoagulation from heavy metal contaminated groundwater in La Comarca Lagunera Mexico". Journal of Hazardous Materials, Vol. 124, No. 1-3, 30 September 2005, pp. 247-254. [ Links ]
[6] T. Zayas, V. Romero, L. Salgado, M. Meraz, U. Morales. "Applicability of coagulation/flocculation and electrochemical processes to the purification of biologically treated vinasse effluent". Separation and Purification Technology, Vol. 57, No. 2, 15 October 2007, pp. 270-276. [ Links ]
[7] Y. Yavuz. "EC and EF processes for the treatment of alcohol distillery wastewater". Separation and Purification Technology, Vol. 53, No. 1, 15 February 2007, pp. 135-140. [ Links ]
[8] N. Kannan, G. Karthikeyan, N. Tamilselvan. "Comparison of treatment potential of electrocoagulation of distillery effluent with and without activated areca catechu nut carbon". Journal of Hazardous Materials, Vol. 137, No. 3, 11 October 2006, pp. 1803-1809. [ Links ]
[9] M. Decloux, A. Bories, R. Lewandowski, C. Fargues, A. Mersad, M. L. Lameloise, F. Bonnet, B. Dherbecourta and L. Nieto Osuna. "Interest of electrodialysis to reduce potassium level in vinasses. Preliminary experiments". Desalination, Vol. 146, No. 1-3, 10 September 2002, pp. 393-398. [ Links ]
[10] J. A. Milewski, P. P. Lewicki. "Demineralisation of vinasse by electrodialysis". Journal of Food Engineering, Vol. 7, No. 3, August 1988, pp. 177-196. [ Links ]
[11] C. Becerra, D. M. Gómez. Estudio exploratorio de la remoción de DBO y DQO en vinazas mediante electrocoagulación. Trabajo de grado en Ingeniería Química. Cali: Universidad del Valle, 2007. [ Links ]
[12] J. A. Dávila. Electrocoagulación-electroflotación de vinazas de destilería. Tesis de maestría en Ingeniería Química. Cali. Universidad del Valle, 2007. [ Links ]
[13] M. Arienzo, J. Chiarenzelli and R. Scrudato. "Remediation of metal-contaminated aqueous systems by electrochemical peroxidation: an experimental investigation". Journal of Hazardous Materials. Vol. 87, No. 1-3, 12 October 2001, pp. 187-198. [ Links ]
[14] M. Arienzo, P. Adamo, J. Chiarenzelli, M. Bianco and A. De Martino. "Retention of arsenic on hydrous ferric oxides generated by electrochemical peroxidation". Chemosphere, Vol. 48, No. 10, September 2002, pp. 1009-1018. [ Links ]
[15] A. K. Golder, A. N. Samanta, S. Ray. "Removal of trivalent chromium by electrocoagulation". Separation and Purification Technology, Vol. 53, No. 1, 15 February 2007, pp. 33-41. [ Links ]
[16] G. Chen. "Electrochemical technologies in wastewater treatment". Separation and Purification Technology, Vol. 38, No. 1, 15 July 2004, pp. 11-41. [ Links ]
[17] S. Irdemez, Y.S. Yildiz and V. Tosunoglu "Optimization of phosphate removal from wastewater by electrocoagulation with aluminum plate electrodes". Separation and Purification Technology, Vol. 52, No. 2, December 2006, pp. 394-401. [ Links ]
[18] J. Z. Zhang, J. C. Chen and E. D. Kirbyb. "Surface roughness optimization in an end-milling operation using the Taguchi design method". Journal of Materials Processing Technology, Vol. 184, No. 1-3, 12 April 2007, pp. 233-239. [ Links ]
[19] H. H. Tung, C. H. Su, W. L. Liu. "Parameters optimization of a nano-particle wet milling process using the Taguchi method, response surface method and genetic algorithm". Powder Technology, Vol. 173, No. 3, 30 April 2007, pp. 153-162. [ Links ]
[20] K.K. Prasad, S.V.Mohan, R.S. Rao, B.R. Pati, P.N. Sarma. "Laccase production by Pleurotus ostreatus 1804: Optimization of submerged culture conditions by Taguchi DOE methodology". Biochemical Engineering Journal, Vol. 24, No. 1, 15 May 2005, pp. 17-26. [ Links ]
[21] M. Levent, Ö. Kaya, M. Kocakerim, V. Yigit, Ö. Kücük. "Optimization of desulphurization of Artvin-Yusufeli lignite with acidic hydrogen peroxide solutions". Fuel, Vol. 86, No. 7-8, May 2007, pp. 983-992. [ Links ]
[22] S. Madaeni, S. Koocheki. "Application of taguchi method in the optimization of wastewater treatment using spiral-wound reverse osmosis element". Chemical Engineering Journal, Vol. 119, No. 1, 1 June 2006, pp. 37-44. [ Links ]
[23] M. Jiang, R. Komanduri. "Application of Taguchi method for optimization of finishing conditions in magnetic float polishing (MFP)". Wear, Vol. 213, No. 1-2, 30 December 1997, pp. 59-71. [ Links ]
[24] I.A. Sengil, M. Ozacar, B. Omurlu. "Decolorization of C.I. Reactive Red 124 Using the Electrocoagulation Method". Journal of Hazardous Materials, Vol. 161, No. 2-3, 30 January 2009, pp. 1369-1376. [ Links ]
[25] M. Nalbant, H. Gökkaya, G. Sur. "Application of Taguchi method in the optimization of cutting parameters for surface roughness in turning". Materials and Design, Vol. 28, No. 4, March 2007, pp. 1379-1385. [ Links ]