Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Med
versão impressa ISSN 0121-5256versão On-line ISSN 1909-7700
rev.fac.med v.17 n.1 Bogotá jan./jun. 2009
ARTÍCULO DE REVISIÓN
ACTUALIZACIÓN DEL MARCO CONCEPTUAL Y MANEJO DE LA SEPSIS, SEPSIS SEVERA Y SHOCK SÉPTICO
UPDATE IN THE CONCEPTUAL FRAMEWORK AND MANAGEMENT OF SEPSIS, SEVERE SEPSIS AND SEPTIC SHOCK
ATUALIZAÇÃO DO CONCEITO E TRATAMENTO DA SEPSE, SEPSE GRAVE E CHOQUE
JUAN CARLOS GÓMEZ RODRÍGUEZ, M.D.a*
a Residente del Programa de Cirugía General, Universidad Militar Nueva Granada, Bogotá, D.C.
* Correspondencia: juancgomezr@hotmail.com. Dirección postal: 800 West Avenue Apt.915 Miami Beach, Fl 33139, USA.
Recibido: Mayo 5 de 2009. Aceptado: Junio 30 de 2009.
Resumen
Si bien la sepsis es tan antigua como el sistema inmune, solo hasta el siglo XIX se identificó una relación de causalidad de entre los organismos infecciosos y la infección per se. Y aunque después de ello se han producido grandes avances, tan sólo en los últimos veinte años se ha iniciado el proceso que pretende disminuir su mortalidad, que supera incluso el 50% en casos de sepsis severa, convirtiéndose en la décima causa de muerte en países industrializados. El subregistro epidemiológico de la sepsis se asocia a deficiencias en la estandarización y a las definiciones de los términos asociados: sepsis, sepsis severa y choque séptico. La comprensión de los mecanismos fisiopatológicos en la última década ha logrado crear herramientas diagnósticas y terapéuticas que han producido un impacto altamente positivo, con iniciativas que buscan su divulgación y uniformidad y de ésta forma estandarizar protocolos de tratamiento. En esta revisión se discuten las guías de manejo recientemente actualizadas, dirigidas a que se homogenice el tratamiento de la sepsis desde la sala de urgencias hasta la Unidad de Cuidado Intensivo y a que se establezcan cifras que permitan su evaluación y la medición del impacto real de este ominoso proceso.
Palabras clave: sepsis, choque séptico, infección, terapia
Abstract
Even though sepsis is as old as our immune system, it was not until the XIX century that a causality relation between infectious organisms and the infection per se was identified. Although great advances have taken place after this, it was not until the last 20 years that a process was initiated to try and diminish the mortality, which surpasses 50% in cases of severe sepsis, becoming the tenth most common cause of death in industrialized countries. The epidemiologic sub registry is marred by deficiencies in the standardization and the definitions of the associated terms: sepsis, severe sepsis and septic shock. The understanding of the physiopathologic mechanisms in the last decade has helped to create diagnostic and therapeutic tools that have produced a highly positive impact, with initiatives created to establish uniformity, to publicize them and to standardize the treatment protocols. This is a discussion and review of the management guidelines, which were recently updated, in an attempt to obtain homogenization of the treatment of sepsis from the emergency room to the Intensive Care Unit and to establish data to evaluate sepsis and the real impact of this ominous process.
Key words: sepsis, septic shock, infection
Resumo
Embora a sepse seja tão antiga quanto o sistema imune, só até o século XIX identificou-se uma relação da causalidade entre os organismos infecciosos e a infecção per se. E mesmo depois que houve grandes avanços apenas nos últimos vinte anos começo o processo que tenta reduzir sua mortalidade que supera incluso o 50% em casos do sepse grave, tornando-se a décima causa de morte nos países industrializados. A sub notificação epidemiológica da sepse é associada às deficiências na estandardização e as definições dos termos associados: sepse, sepse grave e choque séptico. A compreensão dos mecanismos fisiopatológicos na última década conseguiu criar ferramentas diagnosticas e terapêuticas que têm produzido um impacto altamente positivo, com iniciativas que visam a sua divulgação e uniformidade e assim padronizar protocolos de tratamento. Nesta revisão discutimos as guias do manejo atualizadas recentemente, dirigidas para que se homogênese o tratamento desde na sala de urgências ate as unidades de terapia intensiva e que se estabeleçam cifras que permitam a sua evacuação.
Palavras-chave: sepse, infecção, choque séptico
Introducción
La palabra sepsis se origina del vocablo griego seps (shy) que significa putrefacción y se empezó a utilizar mucho antes de que se relacionara a la infección con los microorganismos. Es la décima causa de muerte en los Estados Unidos (1), una importantísima causa de morbilidad y mortalidad preoperatoria y postoperatoria y el 20% de quienes la desarrollan son pacientes quirúrgicos. Se estima que más de 750.000 casos de sepsis se presentan al año, con aproximadamente 225.000 muertes en el mismo periodo (2). La variación epidemiológica inexorablemente tiende a aumentar esas cifras y también su relación con los casos quirúrgicos (3). El uso del término "septicemia" fue desaconsejado en la Conferencia de Consenso de 1991(4), por no tener correspondencia exacta con ninguna de las categorías actuales (5), pues al referirse a la presencia de microorganismos patógenos -o sus toxinas- en la sangre, junto con un síndrome de respuesta inflamatoria sistémica (SRIS) atribuido a la infección y también a la disfunción aguda de órganos (sepsis grave) y al shock séptico, dejaba por fuera un número indeterminado de casos de sepsis sin bacteriemia, lo cual resultaba impreciso (5). Sin embargo, aun se mantiene en la Clasificación Internacional de Enfermedades (ICD-10 o CIE-10) y también como término MeSH en la base de datos Medline.
La relación entre bacteriemia y sepsis grave merece mención especial, pues se produce sepsis grave en uno de cada cuatro episodios de bacteriemia (6), y a la inversa, se documenta bacteriemia en el 25% de los casos de sepsis grave. La frecuencia de bacteriemia aumenta en cada uno de los estadios de la sepsis (7) y mientras que la mortalidad de bacteriemia y de sepsis grave por separado sería alrededor de un 25%, la de sepsis grave bacteriémica sería superior al 50%. La bacteriemia, como otras infecciones, presenta un espectro de gravedad muy variable, sin que su presencia resulte en criterio adecuado para clasificar a los pacientes con sepsis (6).
Aspectos epidemiológicos
En 1990, el CDC (Centers for Disease Control) realizó uno de los principales estudios epidemiológicos sobre pacientes con sepsis, encontrando que la incidencia de "septicemia" había aumentado en Estados Unidos entre 1979 y 1987 desde 73,6 hasta 175,9 por 100.000 (habitantes y año), un aumento del 139% (8), el cual era aún mayor en personas mayores de 65 años (de 326,3 a 854,7 por 100.000, un 162%). A pesar de que en este periodo de tiempo la mortalidad de los pacientes con "septicemia" disminuyó desde el 31% hasta el 25,3%, la tasa de mortalidad aumentó de 22,8 a 44,5 por 100.000 habitantes y el riesgo relativo de morir en los pacientes con "septicemia" con respecto a los enfermos hospitalizados por otro motivo fue de 8,6 (IC 95%: 8,14- 9,09), lo que atestigua la letalidad de la enfermedad (5). Angus y col. (2), basándose en la revisión retrospectiva de una amplia muestra de los diagnósticos de alta hospitalaria estadounidense según la clasificación ICD-9, encontraron una incidencia de sepsis grave de 300 casos por 100.000 habitantes y año, una mortalidad global de la sepsis grave del 28,6% y del 34,1% para los pacientes ingresados en las unidades de cuidado intensivo (UCI). En cifras absolutas, calcularon que cada año se producen en Estados Unidos 751.000 casos nuevos de sepsis grave, de los cuales 400.000 ingresan a UCI; estas estimaciones prevén un aumento anual del 1,5% en la incidencia de sepsis grave, con lo que se alcanzaría el millón de episodios anuales en la próxima década. El número de muertos por sepsis calculado fue de 215.000 por año, similar al de fallecidos por infarto de miocardio (211.000 anuales), lo que significa que en Estados Unidos, la sepsis grave fue la causa de la muerte de casi el 10% de todos los fallecimientos de 1995 (9).
El estudio del CDC de 1990 (4) ya había puesto de manifiesto que la incidencia de septicemia era mucho mayor en sujetos de edad avanzada y que el ritmo de crecimiento en este grupo de edad era además más acelerado que en el resto de la población. El estudio de Angus (2) mostró también una relación exponencial entre la incidencia de sepsis grave y la edad, poniendo de manifiesto que esta es cien veces más frecuente en mayores de 85 años (2.620 por 100.000) que en niños (20 por 100.000), disparándose a partir de la sexta década de vida. La mortalidad también aumentó con la edad, esta vez de forma lineal, desde porcentajes inferiores al 15% por debajo de los 30 años, hasta alcanzar el 40% a partir de los 85 años, porcentajes que se incrementan en pacientes inmunocomprometidos ó con cáncer (10). Martin y col. (11), también en Estados Unidos, recogieron una muestra aleatoria de informes de alta hospitalaria entre 1979 y 2000, encontrando un aumento en la incidencia anual de sepsis del 8,7%, desde 83 hasta 240 casos por 100.000, un ritmo de crecimiento mucho más elevado que el estimado por Angus.
La sepsis es ahora más grave que hace 20 años: la proporción de pacientes con sepsis que presentan algún fallo de órganos se ha duplicado en este periodo, desde el 16,8% hasta el 33,6%: en la actualidad uno de cada tres pacientes con sepsis tienen sepsis severa (12). Los órganos que fallaron más a menudo fueron los pulmones (18%), los riñones (15%), y los sistemas cardiovascular (7%) y hematológico (6%), con una mortalidad que aumentó con cada órgano adicional fallado. En la actualidad, la frecuencia con que los supervivientes requieren permanecer en centros de rehabilitación o de dependencia ha aumentado considerablemente, del 16,8% al 31,8%. Mientras que las tendencias norteamericanas no difieren mucho de las mostradas en estudios europeos, con cifras escandalosas en incidencia y mortalidad (13-16), en los países latinoamericanos hay pocos datos acerca de la epidemiología de la sepsis grave. Recientemente investigadores brasileros publicaron el estudio BASES (17), un estudio multicéntrico de cohortes, que prospectivamente incluyó 1.383 pacientes adultos ingresados en cinco unidades de cuidado intensivo, encontrando una incidencia de sepsis, sepsis grave y shock séptico de 61, 36 y 30 casos por 1.000 pacientes-días de UCI, respectivamente. La mortalidad fue del 24,3% para los pacientes con SIRS, 34,7% con sepsis, 47,3% con sepsis grave y 52,2% con shock séptico. Los autores realizaron una comparación entre los hospitales privados y públicos, que evidenció en los primeros una menor mortalidad (12,5% frente a 28,9%; p< 0,0005). Los pacientes de los hospitales públicos presentaban con mayor frecuencia sepsis grave y shock séptico que los de hospitales privados y tuvieron una mayor mortalidad dentro de cada uno de los estadios de sepsis, a igualdad de gravedad de disfunción de órganos, medida mediante el sistema SOFA. En el estudio se destaca claramente la influencia del nivel socioeconómico tanto en la incidencia como en la mortalidad de la sepsis (9,18). Desafortunadamente el registro epidemiológico colombiano sigue siendo deficiente respecto a éste y a otros procesos, deficiencia facilitada, entre otras cosas, por errores en la codificación de enfermedades, por la asignación de códigos de enfermedad diferentes en los sistemas de registro hospitalarios, por la falta de sistematización de los mismos, por los inadecuados parámetros de estandarización en los reportes epidemiológicos e incluso, por la aceptación de los estándares internacionales; sin embargo, la experiencia empírica muestra que los datos nacionales no difieren de los hallazgos mundiales anteriormente mencionados.
En cuanto a la relación foco de infección - microorganismo causante - mortalidad de la sepsis, los estudios epidemiológicos ha demostrado una interacción significativa entre foco de infección y microorganismo causante, lo que hace considerarlos como factores de influencia pronóstica (9). Recientemente el grupo europeo de Cohen publicó una extensa revisión que analizó más de 50.000 episodios de infección, encontrándose diferencias notables en la mortalidad de los seis principales focos de infección: bacteriemia, meningitis, neumonía, infecciones de piel y tejidos blandos, peritonitis e infecciones urinarias (19).
Es importante resaltar que la carga económica que supone la asistencia de los enfermos con sepsis grave es muy elevada. En un estudio retrospectivo de cohortes que incluyó más de 16.000 pacientes hospitalizados con sepsis grave, de los cuales el 81,2% tenían 65 años o más (20) y realizado en los Estados Unidos entre los años 1991-2000, se encontró que la mortalidad hospitalaria fue del 21,2%, la mortalidad al año del 51,4% y a los cinco años del 74,2%. El costo de atención médica fue de US$44.600 durante el ingreso hospitalario inicial, de US$78.500 al año y de US$118.800 a los cinco años, correspondiendo la mayor parte a costos de hospitalización (21).
Bases fisiopatológicas
La inflamación es la respuesta inespecífica inicial ante la lesión tisular producida por estímulos mecánicos, químicos o microbianos (22). Es una respuesta rápida, humoral y celular, muy amplificada pero controlada, en la que las cascadas del complemento, coagulación fibrinólisis, junto con citoquinas y quininas, se disparan en conjunto cuando elementos bacterianos, para este caso, activan los macrófagos (Mφ) y las células endoteliales. Esta respuesta local, considerada benigna y adecuada en tanto el proceso inflamatorio sea correctamente regulado, tiene componentes pro-inflamatorios y anti-inflamatorios y en ocasiones estos últimos son iguales o mayores que los primeros.
En condiciones normales la respuesta inmune ante un agente bacteriano es correctamente controlada y funciona de forma efectiva para limitar la infección y promover posteriormente la reparación tisular. Existe un balance entre citoquinas pro-inflamatorias como el factor de necrosis tumoral-α (TNFα), la interleuquina 1 (IL-1), la interleuquina 12 (IL-12) y el interferón γ (IFN- γ) y citoquinas anti-inflamatorias como la interleuquina 10 (IL-10), la interleuquina 4 (IL-4) y la interleuquina 6 (IL-6), el factor transformante de crecimiento β (TGF- β), antagonista del receptor de IL-1 y algunas prostaglandinas (PGE), que resulta de una activación efectiva, con la subsiguiente resolución de la respuesta inflamatoria. Sin embargo, en algunos casos el no control de la respuesta inflamatoria puede originar una inflamación sistémica severa, denominada Síndrome de Respuesta Inflamato ria Sistémica (SRIS) (5), que no siempre tiene un origen infeccioso. Al contrario, cuando predomina la respuesta anti-inflamatoria, se puede desarrollar un estado de inmunosupresión relativa, fenómeno que se puede observar después de un trauma mayor, de una lesión térmica o de un estado post-sepsis que se denomina Síndrome de Respuesta Compensadora Anti-inflamatoria (SRCA), el cual hace susceptible a las complicaciones infecciosas a quienes lo desarrollan. Esta secuela adversa de la sepsis que induce inmunosupresión se logra revertir con la administración del interferón d, citoquina que restaura la producción de TNFα por los Mφ, mejorando la superviviencia de los pacientes con sepsis (23). Tanto la disfunción multiorgánica, como la insuficiencia orgánica y la muerte, pueden ocurrir todas consecuencia de SIRS, o de infecciones graves en casos de SRCA (24).
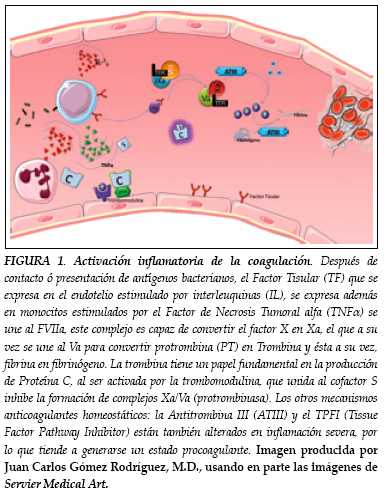
En la actualidad, el conocimiento de la interrelación entre inflamación y coagulación y los varios mecanismos que actúan en el balance hemostático produciendo tendencia a un estado pro-coagulante está esclarecido, junto con las citoquinas que lo median. Esa interrelación se manifiesta en tres vías (figura 1): en primera instancia interviene la antitrombina, una proteasa y principal inhibidora de la trombina y del factor Xa, que se ve marcadamente disminuida durante la respuesta inflamatoria grave debido a su consumo, a una síntesis deficiente y a su degradación. En segunda instancia participa el sistema de la proteína C, vía que ha mostrado una importante implicación terapéutica (25). La proteína C es activada por el complejo trombina-trombomodulina y potenciada por la unión al receptor endotelial de proteína C (REPC), regulando los cofactores Va y VIIIa. En procesos inflamatorios graves se altera su producción y su degradación, sumándose al déficit de su actividad la falla endotelial. En tercer lugar está la vía del factor tisular, cuyos mecanismos son aun desconocidos, creyéndose que la concentración de inhibidor de la vía del factor tisular (IVFT) puede ser insuficiente para regular la activación de la coagulación (26,27). Sumado a esto, cada vez hay mayor evidencia acerca de la relación directa entre las alteraciones genéticas y las presentaciones clínica y pronóstico de los pacientes que sufren de sepsis, de sepsis severa y de shock séptico (28), de tal forma que se considera que las enfermedades poligénicas (o multifactoriales) pueden ser factor de riesgo o indicador pronóstico en casos de sepsis y disfunción multiorgánica, entre otras. Recuérdese que son los estudios genéticos los que permiten establecer las bases moleculares de la respuesta a los fármacos (farmacogenética) y los blancos futuros de la terapia génica (5).
Definiciones y estandarización
Los estudios publicados en los años 80 mostraban cifras muy dispares sobre la mortalidad de los pacientes con sepsis, debido en parte a las diferentes definiciones que se empleaban en cada estudio y a la ausencia de datos epidemiológicos fiables. Durante muchos años se tuvo como requisito la bacteriemia para hablar de sepsis, centrándose demasiado la investigación en los subgrupos de las infecciones por bacilos Gram negativos (29). En 1989, Bone y cols. (30) hicieron un intento notable en unificar el concepto y definición de sepsis, para lo cual propusieron el término "Síndrome Séptico" con base en datos fisiológicos que finalmente fueron inconsistentes, por lo que fue reemplazado posteriormente por las definiciones que actualmente se utilizan, en el desarrollo de la Conferencia de Consenso de 1992 (6) que patrocinó el American College of Chest Physicians (ACCP) y la Society of Critical Care Medicine (SCCM). En ella se introdujo además el novedoso término de Síndrome de Respuesta Inflamatoria Sistémica (SRIS), una respuesta generalizada del organismo ante determinados estímulos, no necesariamente de origen infeccioso. Mientras que el SIRS es la respuesta del organismo a una variedad de estímulos, incluyendo el infeccioso, la sepsis es la respuesta del organismo a la infección (8).
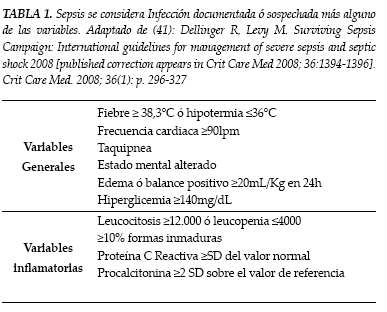
Los criterios propuestos de SIRS por la conferencia de consenso ganaron aceptación por su sencillez y han sido empleados y validados en multitud de ensayos clínicos desde entonces. Aún así, falencias asociadas a esa simplicidad se pusieron de manifiesto en la Conferencia de Consenso celebrada diez años después (31), en la que se modificaron los criterios diagnósticos de SIRS y se adicionaron variables que representaban mejor la respuesta clínica a la infección (tabla 1). Si bien los marcadores no son infalibles y sean muchos los pacientes con sepsis que no muestran todas las características y lo contrario, pacientes que sin ella muestren algunas, indefectiblemente la presencia de estos marcadores debe llevar a una alta sospecha a la búsqueda sistemática de un foco infeccioso (32). Un concepto importante que se introdujo fue el de sepsis y sus secuelas (disfunción y fallo de órganos) como un espectro continuo de gravedad, por lo que los distintos síndromes sépticos se consideran ahora estadios de la sepsis: sepsis, sepsis grave y shock séptico (tabla 2). Cada uno tiene una morbilidad y mortalidad mayores que el anterior (33). Además, se consideran otros factores con influencia pronóstica, como el número de órganos fallados y las puntuaciones de gravedad (APACHE-II, SAPS-II, y otras). En el análisis de subgrupos del estudio PROWESS (34) sobre tratamiento de la sepsis grave con proteína C activada, se encontró eficacia del tratamiento solo en los pacientes con fallo de dos o más órganos o con puntuación APACHE-II igual o superior a 25 puntos en las últimas 24 horas; ambos puntos de corte parecieron ser los que mejor discriminaban un riesgo alto de morir. Ambos grupos de se han denominado sepsis grave de alto riesgo, aunque la denominación tiene interés exclusivo en la decisión de emplear o no dicho tratamiento.
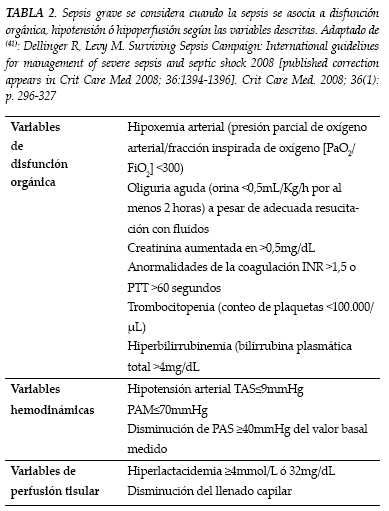
Por último, existe también un espectro de gravedad en la disfunción/fallo de órganos, reservándose el término "fallo" para los niveles de más gravedad. Entre los distintos sistemas de valoración de la disfunción de órganos (LODS, MODS, SOFA) el que más amplia aceptación ha logrado en adultos es el sistema SOFA ("Sepsis-related Organ Failure Assessment", o "Sequential Organ Failure Assessment" (35), un sistema sencillo diseñado específicamente para la sepsis y para ser evaluado de forma repetida a lo largo de la evolución del enfermo (36). Incluye la valoración de la función de seis órganos, con puntuaciones para cada uno de de 0 a 4, denominándose "disfunción" cuando se asignan 1 o 2 puntos y "fallo" del órgano cuando alcanza puntuación de 3 ó 4. De los órganos que evalúa el SOFA el cardiovascular es el de mayor importancia pronóstica (37), lo que apoya la clasificación de la sepsis, incluyendo el shock séptico, como estadio independiente y no sólo como un órgano disfuncionante más.
Tratando de definir sepsis, no menos importante resultó la definición de infección (puesto que en cada una se encuentra implícito el significado de la otra), lo que hizo necesario estandarizar este término. Para ello se reunió un panel de expertos en la Conferencia de Consenso del 2005 organizada por el Foro Internacional de Sepsis y generaron un documento (32) en el que se definen las seis más frecuentes causas de infección en pacientes sépticos. Si bien esas definiciones tienen como objetivo marcar pautas para la inclusión de pacientes en estudios clínicos, no cabe duda que pueden usarse para una aproximación diagnóstica y terapéutica en las UCI.
Manejo
Rivers y cols. le dieron un viraje importante a la aproximación terapéutica del paciente con sepsis severa y shock séptico. En su artículo publicado en el 2001 (38) expusieron lo que ahora se convierte en paradigma en el manejo y que fundamenta las guías de manejo más recientes: la terapia de resucitación temprana basada en metas (Early Goal-Directed Therapy ó EGDT). La EGDT (figura 2) se refiere a la resucitación dirigida por protocolos para alcanzar metas predefinidas ajustando la precarga cardiaca, la poscarga y la contractilidad, en los pacientes con sepsis severa o hipoperfusión inducida por sepsis. La resucitación hemodinámica es necesaria para combatir las anormalidades circulatorias que acompañan la transición de sepsis a sepsis severa y a shock séptico, como respuesta a las citoquinas proinflamatorias y a otros mediadores en la cascada séptica. La disminución en la resistencia vascular sistémica, el aumento de la capacitancia venosa, la depresión miocárdica, la depleción del volumen intravascular y el metabolismo aumentado, pueden llevar a un disbalance entre la entrega y la demanda de oxígeno sistémico, lo que eventualmente puede resultar en hipoxia tisular, o en falla o disfunción orgánica reversible.
Parece haber acuerdo en que la optimización hemodinámica antes del inicio de la disfunción orgánica es crítica y tiene impacto en la mortalidad (39), de manera que la EGDT se debe empezar tan temprano como sea posible, incluso en el departamento de urgencias, sin esperar a que estos esfuerzos de resucitación se inicien en la UCI (3). La intervención hemodinámica temprana es capaz de restaurar la perfusión antes de que la disfunción celular pase de reversible a irreversible, previéndose así la falla orgánica o la muerte, como lo evidenció, entre otros estudios, el metaanálisis Kern & Shoemaker (40). La Campaña "Sobrevivir la Sepsis" (Surviving Sepsis Campaign) publicó en 2008 una actualización de las Guías Internacionales de Manejo de la Sepsis Severa y el Shock Séptico (41), como forma racional de manejo basado en la evidencia disponible. Tomando como base este documento y en asocio con el Institute for healthcare improvement (IHI), se desarrollaron "paquetes" de manejo para facilitar la implementación sistemática, rápida y consistente de las recomendaciones de las guías, de manera que en las primeras seis horas se implemente el paquete de resucitación y en las 24 horas el paquete de manejo. Con esta información se pretende que cada médico se aproxime al manejo del paciente con sepsis severa o shock séptico aún desde la sala de urgencias.
Además, se han creado herramientas que aseguren el cumplimiento de los objetivos de las guías, la medición de los resultados y la penetración en el ambiente clínico de la estandarización. Por ejemplo, tarjetas, pósteres educativos y hasta programas basados en el sistema operativo Palm® para dispositivos portátiles, lo que permitan al tratante recordar y aplicar sistemáticamente las guías de manejo. Esas herramientas, incluyendo el software, pueden bajarse en forma gratuita de la internet (42).
Paquete de resucitación (seis primeras horas)
Comprende las medidas que deben completarse y puntuarse dentro de las primeras seis horas de identificación de sepsis grave, por lo que su inicio debe ser lo antes posible y cumplir en un 100% en estos pacientes. Hay algunos elementos que aunque pueden no realizarse si la situación clínica no lo requiere (p.ej.: la monitorización de la presión venosa central o la saturación central de oxígeno en ausencia de shock o lactato > 4 mmol/L ó 36mg/dL), se considera que todos sean puestos en práctica (43).
1. Medición del lactato sérico. La hiperlactacidemia es frecuente en los pacientes con sepsis grave o shock séptico, indicando habitualmente metabolismo anaerobio e hipoperfusión, aunque también puede deberse a un aclaramiento reducido de lactato en casos de insuficiencia hepática, o a disfunción metabólica celular sin hipoperfusión global. Diversos estudios han reportado que los niveles de lactato tienen un valor pronóstico independiente de la hipotensión, especialmente cuando persisten elevados tras la resucitación inicial. La hiperlactacidemia puede ser el único indicador de hipoperfusión en pacientes normotensos, e indica la necesidad de llevar a cabo una resucitación agresiva, al igual que la presencia de hipotensión.
Aunque en los paquetes de medidas SSC/IHI no se especifica el momento de la determinación de lactato, salvo que es una medida a realizar en las seis primeras horas, se ha establecido que preferiblemente se haga en las dos primeras horas, con la primera determinación analítica y la toma de hemocultivos, teniendo en cuenta que su resultado puede modificar la actitud terapéutica inicial, pues es criterio que guía la resucitación hemodinámica. Usualmente los Analizadores de Gases Arteriales estándar realizan medidas eficaces (44,45). Se recomienda:
- Que en todos los centros hospitalarios la determinación urgente de lactato arterial esté incluida en el protocolo de sepsis grave y que se considere como un estándar asistencial. Para ello deben adoptarse medidas concretas en los puntos asistenciales que lo precisan más a menudo (urgencias, cuidados intensivos).
- Que al poderse realizar de inmediato la determinación de lactato y mientras se resuelve esta urgencia, se emplee el déficit de bases como medida equivalente.
2. Obtención de hemocultivos antes de iniciar el tratamiento antibiótico. Son indicaciones para obtener hemocultivos cualquiera de los criterios que califiquen un paciente con sospecha de sepsis grave, al igual que la presencia aislada de fiebre, escalofríos, leucocitosis con desviación izquierda, neutropenia, o disfunción de órganos sin otra causa obvia. El porcentaje de hemocultivos positivos en pacientes con sepsis grave o shock séptico es del 30% al 50% y la toma de las muestras antes de iniciar el tratamiento antibiótico ofrece la mejor oportunidad para identificar el microorganismo causante; cuando estas se obtienen después de iniciada la antibioticoterapia se puede retrasar o impedir la identificación porque en cuestión de horas las muestras potenciales se pueden esterilizar.
Las normas concretas de extracción de hemocultivos se deben acordar con el laboratorio de microbiología de la institución; habitualmente se recogen dos o tres hemocultivos de sangre periférica obtenidos por venopunción lo antes posible desde la sospecha de sepsis grave y cuando se sospecha de sepsis por catéter puede resultar útil la obtención de pares de muestras, obtenidas simultáneamente por venopunción y por extracción a través del catéter sospechoso. Se recomienda:
- Incluir en el protocolo de sepsis grave la obligatoriedad de la obtención de hemocultivos, previa al inicio de la antibioticoterapia.
- Colocar avisos que recuerden la necesidad de obtener hemocultivos, en lugares próximos a los de almacenamiento de antibióticos.
- Obtener sólo dos o tres hemocultivos de punciones separadas y sin intervalo entre las extracciones, reduciendo así el retraso hasta el inicio de la antibioticoterapia.
- Realizar por vía percutánea al menos uno de los hemocultivos.
- Hacer cultivo de cada uno los dispositivos de acceso que lleven más de 48 horas.
3. Administración precoz de antibióticos de amplio espectro. Teniendo en cuenta que el inicio correcto y precoz de la antibioticoterapia de amplio espectro reduce la mortalidad de los pacientes con sepsis grave o con shock séptico (46,47), esta debe iniciarse en las tres primeras horas si el paciente es atendido en urgencias y en la primera hora si ingresa directamente en UCI. Aunque los dos focos más frecuentes de sepsis grave y shock séptico son el pulmonar y el abdominal, se deben considerar los seis más frecuentes del Consenso de Definiciones en Infección (32).
La elección del tratamiento antibiótico se debe guiar por la susceptibilidad de los patógenos probables en la comunidad y en el hospital, así como por las características individuales del paciente (foco, comorbilidades, edad, lugar de adquisición, etc.). Como casi siempre el inicio del tratamiento es empírico mientras se conoce el microorganismo causal, se debe recurrir a antibióticos de amplio espectro con cobertura para todos los patógenos probables, incluyendo siempre microorganismos Gram positivos y Gram negativos, revalorando siempre el tratamiento entre las 48 y 72 horas de su inicio. Posteriormente, al identificar el microorganismo causal y su sensibilidad a los antibióticos, se debe valorar la conveniencia o no de mantener un tratamiento de combinación, frente a la monoterapia. La reducción de la cobertura antibiótica reduce costos, toxicidad y la posibilidad del desarrollo de patógenos resistentes. Mientras que la duración del tratamiento antibiótico debe ser entre siete y diez días, guiado por la respuesta clínica, las dosis e intervalos de administración se pautarán de acuerdo a las características farmacocinéticas del fármaco y a las alteraciones fisiológicas del paciente (43). Se recomienda:
- Establecer en el protocolo de sepsis grave la administración empírica de antibióticos de amplio espectro en las tres primeras horas cuando el paciente es atendido inicialmente en urgencias y en la primera hora cuando ingresa directamente a UCI.
- Disponer del suministro de antibióticos de amplio espectro tanto en urgencias como en la UCI, evitando así retrasos.
- Administrar simultáneamente los antibióticos por varias vías, asegurando la rapidez en las entradas.
- Cubrir microorganismos Gram positivos y Gram negativos, hasta que se disponga de los resultados del cultivo. Cuando se trate de pacientes neutropénicos, cubrir a los con más de un antibiótico para ambos tipos de germen.
- Considerar las características individuales del paciente en lo que respecta a su infección, procedencia y patrones de resistencia de cada lugar.
- Considerar cobertura antibiótica doble frente a Pseudomonas, cuando existe sospecha clínica de esta bacteria (esta recomendación no cuenta con un consenso amplio).
- Aunque la duración de la terapia debe ser entre siete y diez días, aumentarla en casos de respuesta lenta, cuando hay focos no drenables, o en deficiencias inmunológicas.
4. Presencia de hipotensión o de niveles de lactato mayores a 4 mmol/L. Cuando el paciente con sepsis grave desarrolla hipotensión, o cuando sus valores de lactato son mayores de 4 mmol/L, la resucitación con líquidos debe ser inmediata, sea con cristaloides o coloides, en la ubicación inicial del enfermo mientras se prepara su traslado a la UCI, o al sitio en que se le realizarán las pruebas imaginológicas. Esta expansión volumétrica se realiza con un mínimo de 20 mL/Kg de cristaloides o con dosis equivalente de coloides, pudiendo también administrar albúmina o coloides artificiales (48) en volúmenes y ritmos de infusión equivalentes, teniendo en cuenta que hay meta-análisis y reportes recientes que respaldan su uso, sin que se haya demostrado diferencias en la mortalidad (49,50). Habitualmente se requiere de la canulación de dos vías periféricas de grueso calibre, una para la extracción de muestras y hemocultivos (si éste no se había realizado previamente) y la otra para la administración inmediata de antibióticos de amplio espectro; este procedimiento no debe demorar ni alterar la administración de fármacos vasopresores a los pacientes hipotensos que no responden de forma rápida. Una vez en la UCI, los pacientes requieren de canulación arterial para el monitoreo de la presión arterial.
Para asegurar la infusión rápida de volumen (hasta 500 o 1.000 ml de cristaloides en los primeros 30 minutos, 1.500 a 2.000 ml en la primera hora, 500 a 1.000 ml por hora después) generalmente se requiere de bombas de infusión volumétricas, sirviendo las dos primeras para el suministro inicial de antibióticos. Es indispensable protocolizar estas medidas teniendo en cuenta las rutinas de cada centro hospitalario, si se desea alcanzar el máximo de efectividad en la resucitación volumétrica inicial (43). Se recomienda:
- Establecer en el protocolo de sepsis grave con hipotensión o hipoperfusión los cuatro componentes de la expansión volumétrica: A) tipo de fluido (cristaloides o coloides), B) ritmo de infusión (≥1.000 mL de solución salina normal (SSN) ó solución de Ringer en los primeros 30 minutos, 20 mL/kg en la primera hora, 500 a 1.000 mL / hora después), C) objetivos de la expansión (tensión arterial media superior a 65 o 70 mmHg), D) límites de seguridad (aparición de signos de edema pulmonar, PVC superior a 14 mm Hg).
- La resucitación con líquidos debe iniciarse de inmediato en todos los casos, independiente de la ubicación del enfermo y tampoco se debe retrasar por la colocación del catéter venoso central.
- Cuando no hay respuesta a loa resucitación con líquidos, pensar en otras causas como disfunción miocárdica, insuficiencia suprarrenal, neumotórax a tensión, taponamiento cardiaco, etc.
5. Tratar la hipotensión con vasopresores durante y después de la resucitación con líquidos. En ocasiones se consigue la estabilización hemodinámica con la expansión inicial de volumen, pero en otros casos no se logra mantener ni la presión arterial ni la perfusión tisular, por lo que se debe iniciar un rápido suministro de vasopresores (noradrenalina o dopamina). Conseguir cuanto antes una tensión arterial media superior a 65mmHg (o mayor en sujetos previamente hipertensos) se considera esencial para mejorar la perfusión tisular y para prevenir deterioro en la función de órganos. La consecución de niveles adecuados de tensión mediante el uso precoz de vasopresores no debe dar la falsa sensación de que la resucitación ha concluido y por el contrario, se debe continuar con la expansión de volumen guiada por la presión venosa central (43). Se recomienda:
- Incluir el uso precoz de vasopresores en el protocolo de tratamiento del shock séptico para mantener una TA media superior a 65 mmHg.
- Asegurar que todo el personal de urgencias y UCI esté familiarizado con el manejo y dosificación de los vasopresores habituales.
- No esperar a que se finalice la resucitación con líquidos para administrar vasopresores si existe hipotensión profunda.
- Si no se puede prescindir de los vasopresores, considerar diagnósticos alternativos, como disfunción miocárdica, insuficiencia suprarrenal, neumotórax a tensión o taponamiento cardiaco.
- Al ser esencial una medición exacta y una monitorización continúa de la presión arterial en pacientes que reciben vasopresores, es indispensable un catéter arterial lo antes posible.
6. En presencia hipotensión persistente a pesar de la resucitación con fluidos o con niveles de lactato superiores a 4 mmol/L. En esta situación de debe alcanzar una PVC ≥8mmHg y una ScvO2 ≥70% o SvO2 ≥65%. Las medidas aquí especificadas se basan exclusivamente en el estudio de Rivers (38) y sus limitaciones constituyen el principal punto débil de los paquetes de manejo en sepsis.4 El principal mérito del estudio está en que se destaca la importancia de tres factores: A) La precocidad de la resucitación; B) La agresividad de la misma; C) El uso de protocolos de actuación en los que se especifiquen objetivos hemodinámicos precisos que guíen el tratamiento. Se recomienda:
- Incluir en el protocolo de sepsis grave, cuando el paciente siga hipotenso, la colocación de catéter venoso central (CVC), para medir la PVC y la ScvO2 (51). Si se emplea un catéter de Swan-Ganz con otro propósito, se pueden medir la PCP y la SvO2. La colocación del CVC no debe sufrir retrasos ni esperar el traslado del paciente a UCI.
- Mantener la tensión arterial con fármacos vasoactivos, o cuando presenta elevación del lactato > 4 mmol/L.
- Asegurar la disponibilidad inmediata de kits preparados para el CVC, así como de profesionales capacitados para la cateterización, para la medición de PVC y ScvO2 y para resolver los problemas y complicaciones que se puedan derivar del CVC.
- En presencia de shock séptico o lactato > 4 mmol/L, mantener la PVC en 8-12mmHg, o en 12-15mmHg si el paciente está en ventilación mecánica, hipertensión abdominal o disfunción diastólica (52). El protocolo de sepsis grave debe incluir explícitamente el objetivo de PVC 8-12 mmHg.
- Destacar la importancia de priorizar el uso de líquidos para lograr la PVC propuesta, seguido de la posterior administración de concentrados de hematíes si existe anemia.
- Asegurar la educación del personal de urgencias en la importancia de una correcta técnica de medición de PVC, en la colocación del transductor y en la técnica exacta para mediciones manuales (aun frecuentes en Colombia).
- Una vez conseguida la PVC ≥ 8 mmHg, mantener la ScvO2 ≥ 70% (o SVO2 ≥65%) mediante transfusión si el hematocrito ≤ 30% y dobutamina si el hematocrito > 30%
- Incluir en el protocolo la medición del hematocrito y la determinación del grupo sanguíneo y realización de pruebas cruzadas.
- Incluir en el protocolo la monitorización de ScvO2 (o SvO2) en pacientes con shock séptico o lactato > 4 mmol/L.
- Incluir en el protocolo la transfusión de hematíes si tras conseguir la PVC con líquidos y vasopresores, la ScvO2 es menor del 70% y el hematocrito es menor del 30%.
- Incluir en el protocolo la administración de dobutamina si la ScvO2 sigue inferior al 70% una vez conseguidos los objetivos de PVC y hematocrito.
- Destacar la importancia de la prioridad de la administración de líquidos y transfusiones antes de la dobutamina. Asegurar la formación del personal de urgencias en el uso de inotrópicos.
- Ajustar la dosis de inotrópicos para mantener la ScvO2 > 70%.
- No esperar al ingreso en UCI para administrar la dobutamina, esta se recomienda a máximo 20mg/Kg/min.
- No esperar al traslado a UCI para iniciar la monitorización.
Medidas a implementar en las primeras 24 horas
Una vez identificada la sepsis grave, estos elementos se deben completar dentro de las primeras 24 horas, cumpliéndolos todos en el 100% de los casos (41). Algunos de los cambios en las guías de 2008 respecto a los anteriores, del 2004, se centran precisamente en los manejos descritos a continuación:
1. Administrar corticoides a dosis bajas en caso de shock séptico. Posterior al estudio CORTICUS (Corticosteroid Therapy for Septic Shock) (53), se bajó el grado de recomendación para el uso de corticoides en adultos con shock séptico que no respondían adecuadamente a resucitación con fluidos y a terapia vasopresora. Tampoco se debe usar el test de estimulación de ACTH para identificar los pacientes que se podrían beneficiar de la hidrocortisona (41), porque entre otras cosas, el etomidato, fármaco empleado en la secuencia rápida de intubación traqueal, produce insuficiencia suprarrenal que puede persistir hasta 24 horas después de una dosis única y también altera la prueba de ACTH (aumento de cortisol de >9mg/dL en 30 a 60 minutos posterior a la administración de ACTH), empleada con frecuencia para determinar la existencia de disfunción suprarrenal en casos de shock séptico y para valorar la interrupción del tratamiento con hidrocortisona. Se recomienda:
- Incluir en los protocolos de manejo de shock séptico el uso de hidrocortisona, con necesidad de vasopresores después de una adecuada resucitación con líquidos en las primeras 24 horas, SOLAMENTE en los pacientes adultos en quienes se ha confirmado una pobre respuesta a los fluidos y a los vasopresores. Las dosis deben ser bajas (200-300 mg/día, divididos en tres o cuatro dosis) durante cinco a siete días. Nunca usar dosis superiores, comparables o iguales a 300mg de hidrocortisona al día.
- No retrasar el uso de corticoides por temor de agravar la infección o de provocar inmunosupresión y descontinuar su uso una vez el paciente no requiera de vasopresores.
- No realizar la prueba de ACTH para identificar pacientes que se pueden beneficiar de la terapia con hidrocortisona. Recordar que el uso de etomidato en las horas previas invalida los resultados porque suprime el eje hipotálamo-hipofisiario-adrenal.
- Considerar la adición al tratamiento de mineralocorticoides (fludrocortisona oral) en pacientes para quienes la hidrocortisona no estaba disponible y cuando el corticoide usado no tiene actividad mineralocorticoide. Es opcional cuando se usa hidrocortisona.
- No usar esteroides en pacientes con sepsis sin shock.
2. Administrar Proteína C activada en la sepsis grave de alto riesgo. Las guías de práctica clínica recomiendan que se administre Proteína C activada recombinante humana (rhAPC) [drotrecogina alfa activada], SOLAMENTE en pacientes adultos con sepsis grave y alto riesgo de muerte sin contraindicaciones absolutas ni relativas(41), es decir, cuando hay disfunción aguda de dos o más órganos inducida por sepsis, o cuando la puntuación APACHE-II es ≥ 25 puntos en las 24 horas previas. La Proteína C Activada recombinante humana no está indicada en pacientes pediátricos ni en pacientes adultos de riesgo bajo (puntuación APACHE-II < 25 puntos y fallo de un solo órgano). Se excluyen del tratamiento los pacientes con contraindicaciones absolutas y los que teniendo contraindicaciones relativas, a juicio del clínico exceden el beneficio potencial del tratamiento.
Como el más grave efecto adverso relacionado con la rhAPC es la hemorragia, en pacientes a quienes se les ha realizado, o se les planea realizar un procedimiento quirúrgico mayor, la rhAPC no se debe administrar sino hasta doce horas después del procedimiento. Como la vida media de la rhAPC es corta y la interrupción de su infusión restaura los niveles previos de hemostasia en dos horas, el tratamiento con rhAPC se debe interrumpir dos horas antes de cualquier procedimiento quirúrgico. Para procedimientos menos invasivos, como una canulación venosa central, o la colocación de un drenaje torácico, o una punción lumbar, el tratamiento se debe interrumpir dos horas antes y reanudarse una o dos horas después, una vez se comprueba la ausencia de hemorragia. El riesgo de hemorragia es especialmente alto si hay trombocitopenia grave, con recuento plaquetario inferior a 30.000/mm3, por lo que está contraindicado el uso de rhAPC en estos casos, incluso después de elevarse el recuento de plaquetas por medio de transfusión.
En los casos de coagulación intravascular diseminada (CID) la rhAPC si está indicada, salvo si hay consumo acusado de factores (menos de 30.000 plaquetas/mm3, fibrinógeno menor de 100 mg/dL, actividad de protrombina inferior al 30%). La rhAPC reduce, por su efecto anticoagulante, el consumo de factores pero no el de plaquetas, por lo que el recuento de plaquetas se debe vigilar estrechamente si se utiliza rhAPC en presencia de CID. El uso simultáneo de heparina puede reducir la eficacia de la rhAPC, por lo que se recomienda no emplear heparina ni HBPM mientras dura el tratamiento con rhAPC. Los pacientes tratados en los últimos siete días con anticoagulantes orales no deben recibir rhAPC, sin embargo, no se encontró relación entre el aumento de PTT, TP o INR y el riesgo de hemorragia en el PROWESS (34). Se recomienda:
- Desarrollar conjuntamente con el Servicio de Farmacia de cada Centro Hospitalario, un protocolo con las indicaciones de uso de la rhAPC, acordes con las aprobadas por el Ministerio de Protección Social y el INVIMA.
- El protocolo de actuación de la sepsis grave debe incluir la valoración de la indicación de rhAPC en las primeras 24 horas de evolución.
- Entrenar al personal de UCI en la administración, efectos secundarios y alteraciones de laboratorio de la rhAPC.
- Incluir en el protocolo un listado de elementos que califican o descalifican a un paciente para el uso de rhAPC, asegurando así que no se administre de manera inapropiada ni que se deje de administrar cuando está indicada.
3. Mantener la glucemia entre 70 y 150 mg/dL. El papel del control estricto de las glucemias no se ha estudiado específicamente para la sepsis grave y la recomendación se basa exclusivamente en los trabajos de Van den Berghe(54) (55), realizado predominantemente en pacientes quirúrgicos de menor gravedad. En la actualidad se viene desarrollando un ensayo clínico que puede dar una respuesta definitiva a esta cuestión. Como en estos pacientes la administración subcutánea de insulina puede ser menos fiable por el edema, o por los trastornos circulatorios, el tratamiento se debe iniciar mediante infusión continua intravenosa. El empleo de protocolos de administración ha demostrado eficacia y seguridad en el control estricto de las glucemias dentro del rango de la normalidad en pacientes críticos. Se recomienda:
- Incluir en el protocolo de sepsis grave la necesidad de mantener las cifras de glucemia por debajo de 150 mg/ dl desde las primeras 24 horas.
- Desarrollar conjuntamente con enfermería un protocolo de administración de insulina en infusión (0,04 U/Kg/h), permitiendo el ajuste por el equipo de enfermería.
- Asegurar la administración de glucosa IV (9g/h – 19kCal/Kg/d) o nutrición enteral con medición frecuente de glucemias y un protocolo específico para tratar la hipoglucemia.
4. Adoptar una estrategia de ventilación protectora en pacientes que reciben ventilación mecánica. La mayoría de los enfermos con sepsis grave y shock séptico requieren intubación traqueal y ventilación mecánica y casi el 50% con sepsis grave desarrolla lesión pulmonar aguda (Acute Lung Injury - ALI), o síndrome de distrés respiratorio agudo (ARDS) en las primeras 24 horas de evolución. Los pacientes con ALI o ARDS tienen infiltrados bilaterales, una paO2:FiO2 inferior a 300mmHg (ALI) o 200mmHg (ARDS) y, cuando se mide, una PCP (Pulmonary Capillary Wedge Pressure - PCWP) inferior a 18 cmH20. En los pacientes con ALI/ARDS la ventilación protectora, con limitación del volumen corriente (Tidal Volume) a 6 mL/kg de peso predicho y de la presión meseta (Plateau Pressure) ≤30 cmH2O, reduce la mortalidad.
La mayoría de las veces la ventilación protectora produce hipercapnia, que debe tolerarse dentro de determinados límites (pH > 7,20). Salvo en pacientes con hipertensión endocraneal, en la mayoría de los casos se requiere de profundos grados de sedación (hipercapnia permisiva). Es recomendable el empleo de las combinaciones de FiO2 y PEEP empleadas en el estudio del ARDS-Network (56) y no se ha encontrado que el uso de niveles mayores de PEEP mejore el pronóstico de los pacientes. Se recomienda:
- Incluir en el protocolo para pacientes con sepsis grave que requieren ventilación mecánica. el uso de un volumen corriente ≤ 6 ml/kg de peso predicho y presión meseta ≤30 cmH2O en las primeras 24 horas.
- Desarrollar un protocolo de ventilación protectora en ALI y SDRA que forme parte del protocolo de sepsis y que incluya la limitación de volumen corriente y presión meseta.
- Emplear modos mandatorios de ventilación (CMV o PCV) durante la fase aguda de la enfermedad, evitando SIMV y PSV, para evitar volúmenes corrientes espontáneos grandes.
- Salvo en acidemia marcada (pH < 7,20), no preocuparse del pCO2. Cuando exista disfunción renal que dificulte la compensación metabólica, se puede administrar bicarbonato en infusión.
- Ajustar la PEEP para evitar colapso pulmonar extenso al final de la espiración.
- Posicionar en prono a los pacientes que requieran niveles potencialmente perjudiciales de FiO2 o presión meseta que no tengan consecuencias adversas por este posicionamiento.
- Considerar el uso de ventilación no invasiva con máscara SOLAMENTE para pacientes con ALI/SDRA e hipoxemia leve a moderada, estables hemodinámicamente, que pueden expulsar secreciones o que se manejan fácilmente.
- Instaurar protocolos de extubación y evaluar diariamente a través de pruebas de ventilación espontanea si el paciente está hemodinámicamente estable, si hay riesgos adicionales potenciales, si están conscientes o alertables y si tienen bajos parámetros ventilatorios.
- Establecer protocolos conservadores de fluidos en pacientes con ALI.
Discusión
Es claro que la incidencia de la sepsis en cualquiera de sus presentaciones aumenta a medida que lo hace la expectativa de vida y que la gran cantidad de procesos y de procedimientos que la originan, sean clínicos, quirúrgicos o traumáticos, no muestran una posibilidad real de ser prevenidos. Los logros en los últimos veinte años se resumen en una limitada disminución de la mortalidad, de la misma forma en que la incidencia ha aumentado de manera inversa y de que la amenaza, inexorablemente se incrementará. Los esfuerzos por definir la entidad han sido grandes en los países desarrollados, en contraste con los del tercer mundo, en los que aun se ignoran las estadísticas más importantes respecto a este proceso, con un alto grado de sub-registro en naciones como Colombia. Partiendo de ello, la probabilidad de evaluar algún tipo de progreso sigue alejado de la realidad.
Las herramientas para lograr la estandarización de la sepsis, gracias a los esfuerzos de organizaciones internacionales y profesionales dedicadas a ello son cada vez más claras, acertadas y fáciles de usar y los resultados de las campañas correspondientes a esta última década están a próximos a revelarse. La literatura respecto a sepsis, sepsis grave y shock séptico abunda, redundando en esfuerzos que actualmente demuestran que con medidas sencillas se pueden lograr grandes resultados. El conocimiento de la historia de la sepsis y los avances de las últimas décadas para estandarizarla y controlarla permite intuir que en el próximo lustro y ante el llamado las instituciones internacionales, así como a la constante especialización de los profesionales de la salud, Colombia podrá participar activamente en una lucha enfocada a la disminución de la actual e inaceptable mortalidad de la sepsis, desarrollando y aplicando programas de estandarización y protocolización.
Todo proceso de cambio y de construcción de futuro empieza por el conocimiento, cimiento que se ha querido tratar en este documento. Los objetivos que se consigan dependerán de la voluntad del lector, de su disposición y motivación para traducir los conocimientos en medidas individuales, colectivas e institucionales que lleven a iniciar el recaudo de estadísticas, la implementación de los procesos y las recomendaciones y su adaptación a las características individuales del medio. En este documento se reunieron los avances actuales y se incluyeron herramientas que se pueden poner a funcionar de manera fácil en instituciones de carácter público y privado y si bien es cierto, hay medidas que se salen de las posibilidades locales, como es el uso de la rhAPC, todas las demás si pueden estar al alcance de cualquier institución hospitalaria del nivel adecuado.
Agradecimientos
Al Dr. Antonio Marttos, Cirujano General – Cuidado Intensivo Quirúrgico y Cirugía de Trauma Ryder Trauma Center – Jackson Memorial Hospital, Miami, Florida, EEUU.
Referencias
1. Miniño A.M, et al. Deaths: final data for 2000. Natl Vital Stat Rep. 2002 Sep 16;50(15):1-119. [ Links ]
2. Angus D.C, et al. Epidemiology of severe sepsis in the United States: analysis of incidence, outcome and associated costs of care. Crit Care Med. 2001 Jul;29(7):1303-10. [ Links ]
3. Howell G, Tisherman S.A. Management of sepsis. Surg Clin North Am. 2006 Dec;86(6):1523-39. [ Links ]
4. Bone R.C, et al. Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. The ACCP/ SCCM Consensus Conference Committee. American College of Chest Physicians/Society of Critical Care Medicine. Chest. 1992 Jun;101(6):1644-55. [ Links ]
5. Briceño I. Sepsis: definiciones y aspectos fisiopatologicos. Medicrit 2005; 2(8):164-178 [ Links ]
6. Brun-Buisson C. Bacteremia and severe sepsis in adults: a multicenter prospective survey in ICUs and wards of 24 hospitals. Am J Respir Crit Care Med - 01-SEP-1996; 154(3 Pt 1): 617-24 [ Links ]
7. Rangel-Frausto M.S, et al. The natural history of the systemic inflammatory response syndrome (SIRS). A prospective study. JAMA. 1995 Jan 11;273(2):117-23. [ Links ]
8. Centers for Disease Control. Current trends increase in hospital discharge survey rates for septicaemia: United States, 1979-1987. MMWR. 1990; 39: 31-34. [ Links ]
9. Palencia E. Epidemiología de la sepsis. REMI 2004; 4 (7): 1B. [ Links ]
10. Williams M.D, et al. Hospitalized cancer patients with severe sepsis: analysis of incidence, mortality, and associated costs of care. Crit Care. 2004; 8(5): R291–R298. [ Links ]
11. Martin G.S, et al. The Epidemiology of Sepsis in the United States from 1979 through 2000. N Engl J Med 2003;348:1546-54. [ Links ]
12. Annane D, et al. Current epidemiology of septic shock: the CUB-Réa Network. Am J Respir Crit Care Med. 2003 Jul 15;168(2):165-72. [ Links ]
13. Brun-Buisson C, et al. Incidence, Risk Factors, and Outcome of Severe Sepsis and Septic Shock in Adults A Multicenter Prospective Study in Intensive Care Units. JAMA. 1995;274(12):968-974. [ Links ]
14. Brun-Buisson C, et al. EPISEPSIS: a reappraisal of the epidemiology and outcome of severe sepsis in French intensive care units. Intensive Care Med. 2004 Apr;30(4):580-8. Epub 2004 Mar 2. [ Links ]
15. Padkin A, Goldfrad C, Brady A.R, et al. epidemiology of severe sepsis occurring in the fi rst 24 hrs in intensive care units in england, wales nd northern ireland. crit care med, 2003;31:2332-2338. [ Links ]
16. Van Gestel A, e al. Prevalence and incidence of severe sepsis in Dutch intensive care units. Crit Care. 2004; 8(4): R153–R162. [ Links ]
17. Silva E, et al. Brazilian sepsis epidemiologic study (BASES). Critical Care 2004, 8:R251-R260. [ Links ]
18. Linde-Zwirble W, Angus D. Severe sepsis epidemiology: sampling, selection and society. Critical Care 2004, 8:222-226. [ Links ]
19. Teres D, et al. Effects of severity of illness on resource use by survivors and nonsurvivors of severe sepsis at intensive care unit admission. Crit Care Med. 2002 Nov;30(11):2413-9. [ Links ]
20. Cohen J, et al. New method of classifying infections in critically ill patients. Critical care medicine. 2004, vol. 32, no7, pp. 1510-1526. [ Links ]
21. Weycker D, et al. Long term mortality and medical care charges in patients with severe sepsis. Crit Care Med. 2003 Sep;31(9):2316-23. [ Links ]
22. Opal S. The Uncertain Value of the Definition for SIRS. Chest 1998;113;1442-1443. [ Links ]
23. Hotchkiss R, Karl I. The Pathophysiology and Treatment of Sepsis. N Eng J Med. 2003; 348: p. 138-150. [ Links ]
24. Sherwood E.R. Current Concept of The Inflammatory response. The American Society of Anesthesiologists.2002;30:169-184. [ Links ]
25. MATTHAY M. Severe sepsis: a new treatment with both anticoagulant and antiinflammatory properties. N Engl J Med. 2001; 344: p. 759-762. [ Links ]
26. Levi M. et al. Pathogenesis of Disseminated Intravascular Coagulation in Sepsis. JAMA. 1993;270(8):975-979. [ Links ]
27. Levi M. The Coagulant Response in sepsis. Clinics in Chest Medicine, Volume 29, Issue 4, December 2008, Pages 627-642 [ Links ]
28. Kellum J.A, Angus D.C. Genetic variation and risk of sepsis. Minerva anestesiologica 2003, vol. 69, no4, pp. 245-253. [ Links ]
29. Palencia E. La sepsis: definiciones y estadios. Revista Electrónica de Medicina Intensiva Artículo no. C1. Vol 4 no. 6, junio 2004. [ Links ]
30. Bone R. Sepsis syndrome: a valid clinical entity. Methylprednisolone Severe Sepsis Study Group. Crit Care Med - 01-MAY-1989; 17(5): 389-93. [ Links ]
31. Levy M.M, et al. 2001 SCCM/ESICM/ACCP/ATS/SIS International Sepsis Definitions Conference. Crit Care Med. 2003 Apr;31(4):1250- 6. [ Links ]
32. Calandra T, et al. The international sepsis forum consensus conference on definitions of infection in the intensive care unit. Crit Care Med. 2005 Jul;33(7):1538-48. [ Links ]
33. Vincent J.L, et al. Defining Sepsis. Clinics in Chest Medicine, Volume 29, Issue 4, December 2008, Pages 585-590. [ Links ]
34. Bernard G, et al. Efficacy and safety of recombinant human activated protein c for severe sepsis. N Engl J Med 2001;344:699-709. [ Links ]
35. Vincent JL, de Mendonca A, Cantraine F, Moreno R, Takala J, Suter PM, Sprung CL, Colardyn F, Blecher S. Working group on "sepsis-related problems" of the European Society of Intensive Care Medicine. Use of the SOFA score to assess the incidence of organ dysfunction/failure in intensive care units: results of a multicenter, prospective study. Crit Care Med 1998; 26: 1793-800. [ Links ]
36. Ferreira F, et al. Serial Evaluation of the SOFA Score to Predict Outcome in Critically Ill Patients. JAMA. 2001;286:1754-1758 [ Links ]
37. Moreno R, et al. The use of maximum SOFA score to quantify organ dysfunction/failure in intensive care. Results of a prospective, multicentre study. Working Group on Sepsis related Problems of the ESICM. Intensive Care Med. 1999 Jul;25(7):686-96. [ Links ]
38. Rivers E, et al. Early goal-directed therapy in the treatment of severe sepsis and septic shock. N Engl J Med 2001;345:1368-77. [ Links ]
39. Gunn S, et al. Equipment review: The success of early goal-directed therapy for septic shock prompts evaluation of current approaches for monitoring the adequacy of resuscitation. Critical Care 2005, 9:349-359 [ Links ]
40. Kern J.W, Shoemaker W.C. Meta-analysis of hemodynamic optimization in high-risk patients. Crit Care Med. 2002 Aug;30(8):1686-92. [ Links ]
41. Dellinger R, et al. Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock: 2008. Intensive Care Med (2008) 34:17–60. [ Links ]
42. Handhelddoc. Handhelddoc.com. (Online). (cited 2008 12 21). Available from: http://www.handhelddoc.com [ Links ]
43. ESICM/ISP/SCCM. Surviving Sepsis Campaign. (Online).; 2009 (cited 2009 01 05. Campana finalizada). Available from: http://www.survivingsepsis.org/ [ Links ]
44. Vincent J.L, Gerlach H. Fluid resuscitation in severe sepsis and septic shock: an evidence-based review. Crit Care Med. 2004 Nov;32(11 Suppl):S451-4. [ Links ]
45. Herrejón E. Tratamiento del enfermo con sepsis grave. Revista Electrónica de Medicina Intensiva Artículo no. C3. Vol 5 no. 3, marzo 2005. [ Links ]
46. Kollef M, et al. Inadequate Antimicrobial Treatment of Infections A Risk Factor for Hospital Mortality Among Critically Ill Patients. CHEST 1999; 115:462–474. [ Links ]
47. Ibrahim E, et al. The Influence of Inadequate Antimicrobial Treatment of Bloodstream Infections on Patient Outcomes in the ICU Setting. CHEST 2000; 118:146–155. [ Links ]
48. The SAFE Study Investigators. A Comparison of Albumin and Saline for Fluid Resuscitation in the Intensive Care Unit. N Engl J Med 2004;350:2247-56. [ Links ]
49. The SAFE Study Investigators. A Comparison of Albumin and Saline for Fluid Resuscitation in the Intensive Care Unit. N Engl J Med 2004;350:2247-56. [ Links ]
50. Schierhout G, Roberts I. Fluid resuscitation with colloid or crystalloid solutions in critically ill patients: a systematic review of randomized trials. BMJ 1998;316:961–4. [ Links ]
51. Reinhart K, Bloos F. The value of venous oximetry. Curr Opin Crit Care. 2005 Jun;11(3):259-63. [ Links ]
52. Rivers E, et al. Early and innovative interventions for severe sepsis and septic shock: taking advantage of a window of opportunity. CMAJ 2005;173(9):1054-65. [ Links ]
53. Sprung C, et al. Hydrocortisone Therapy for Patients with Septic Shock. N Engl J Med 2008; 358:111-24. [ Links ]
54. Van Den Berghe G, et al. Intensive insulin therapy in critically ill patients. N Engl J Med 2001;345:1359-67. [ Links ]
55. Van Den Berghe G, et al. Outcome benefit of intensive insulin therapy in the critically ill: Insulin dose versus glycemic control. Crit Care Med. 2003 Feb;31(2):359-66. [ Links ]
56. The National Heart, Lung and Blood Institute/ National Institute of Health. ARDS Network. (Online).; 2008 (cited 2008 12 10). Available from: http://www.ardsnet.org/ [ Links ]














