Introducción
La tos ferina, también llamada coqueluche o tos convulsiva es una enfermedad respiratoria de notificación obligatoria y prevenible por vacuna, que afecta a todos los grupos de edad especialmente a menores de un año. Su agente causal se relaciona al género bacteriano Bordetella, cuya principal especie implicada es el B. pertussis, sin embargo, se pueden identificar otras especies como B. parapertussis, B. holmesii y B. bronchiseptica este último conocido como un patógeno animal pero que rara vez puede infectar a personas inmunocomprometidas 1. El Síndrome coqueluchoide a diferencia de la tos ferina es un término que se ha utilizado para incluir aquellos pacientes que presentan un cuadro clínico indistinguible de tosferina, con diferentes etiologías infecciosas o no infecciosas. Los agentes involucrados pueden incluir virus y bacterias, entre los que destacan Haemophilus influen-zae, Moraxella catarrhalis, Mycobacterium pneumoniae, Adenovirus, Influenza virus, Parainfluenza 1-4, Virus sincitial respiratorio, citomegalovirus y virus de Epstein Barr1,2.
Bordetella pertussis es un cocobacilo Gram negativo, capsulado, inmóvil, aerobio facultativo que tiene al ser humano como único reservorio. Las diferentes especies comparten un elevado grado de homología en el ácido desoxirribonucleico (ADN) entre los genes relacionados con la virulencia. Tan solo B. pertussis expresa la toxina de la tos ferina o toxina pertussis (TP), la cual es considerada la proteína más virulenta. La división en serotipos depende de los aglutinógenos termolábiles K y de los 14 existentes, 6 son específicos de B. pertussis. Los seroti-pos cambian según la región geográfica y a lo largo del tiempo 1.
B. pertussis produce una serie de sustancias activas biológicamente, muchas de las cuales juegan un papel importante en la enfermedad, la inmunidad y su forma de transmisión. Con respecto a esta ultima caracteristica, se ha documentado que, en la exposición a aerosoles, la he-maglutinina filamentosa y la pertactina son importantes elementos de anclaje a las células del epitelio respiratorio ciliado 3.
La tos ferina es una enfermedad muy contagiosa, con tasas de ataque de hasta el 80 % en personas susceptibles. Esta patología ocupa el quinto puesto en las causas de muerte prevenible por vacunas en menores de 5 años, según datos de la Organización Mundial de la Salud (OMS) 4. Actualmente representa una reemergencia mundial por múltiples causas como: mayor reconocimiento de la enfermedad en la comunidad médica, sospecha clínica en adultos, mejor vigilancia del evento, el uso de técnicas moleculares en el diagnóstico, coberturas de vacunación no adecuadas, eficacia de la vacuna, ausencia de refuerzo en población adolescente y adulta, cambios genéticos del agente causal, entre otras; de ahí que resalta la importancia de su oportuno diagnóstico y tratamiento.
Método
Se realizó una revisión bibliográfica sobre los aspectos epidemiológicos, clínicos y moleculares que engloban tanto la tos ferina como su agente causal, Bordetella pertussis, mediante la búsqueda electrónica de literatura empleando bases de datos como PubMed, ScienceDirect, SciELO, Redalyc; y búsqueda en portales de salud, utilizando las palabras clave: "Bordetella pertussis", "Aden-ylate cyclase toxin-hemolysin", "cAMP intoxication", "Pertussis vaccine", "Genetic changes Bordetella pertussis". Se incluyeron artículos escritos tanto en inglés con en español; se seleccionaron un total de 79 artículos de los cuales 69 fueron obtenidos de PubMed; 6 obtenidos de ScenceDirect; 2 artículos desde SciELO; 2 obtenidos de Redalyc. Ademas se incluyó información de portales web de centros de referencia internacional en epidemiología como Centers for Disease Control and Prevention (CDC), World Health Organization (WHO).
Resultados
Epidemiología
Hipócrates, desde el año 400 A.C. denominó "quintas" a accesos de tos característicos del proceso; en 1578 se produjo una primera descripción clínica en relación con una epidemia en París. En 1669 se realizó la descripción de síndrome tos ferinoso como pertussis (tos severa) y en 1906 Bordet y Gengou lograron el aislamiento del agente Bordetella Pertussis de expectoraciones de niños y diseñaron una relación entre la sintomatología y el agente etiológico; en 1916 se recomendó el examen de placa tosida y en 1964 se produjo la demostración de los adenovirus tipo 2 como agentes de síndrome tos ferinoso, pertusoide o coqueluchoide; en 1966 Collier y otros describieron manifestaciones clínicas semejantes a la tos ferina en dos hermanos, aislando el adenovirus tipo 5 y llamando este cuadro síndrome pertussis; en 1975 Islur y otros hicieron referencia a un síndrome de tos ferina en 201 niños, en 139 de ellos se aisló B. Pertussis junto con adenovirus, y en los restantes 62 pacientes, encontraron adenovirus lo que ratifica lo establecido por Klenk y otros tres años antes, acerca de que una infección mixta bacteriana y viral pudiera estar presente en el síndrome tosferinoso o coqueluchoide 5,6.
Sin embargo, alrededor de 1974 los ingleses, dejaron bruscamente de confiar en la vacuna contra la tos ferina e interrumpieron la vacunación, a raíz de la muerte de varios niños de corta edad; muchos médicos aconsejaron a los padres la no vacunación de sus hijos argumentando la escasa fiabilidad de la vacuna. Hasta entonces más del 85% de la población vacunaba a sus hijos; aquel año y los años siguientes la cifra descendió al 65%. La enfermedad, que prácticamente había desaparecido, volvió a resurgir y dos grandes epidemias, en 1978-1979 y 1982-1983, causaron miles de víctimas 7.
A pesar de esto, los resultados de la reunión internacional celebrada en Copenhage durante 1988 confirmaron la gran utilidad de la vacunación contra la tos ferina. Confirmando su eficacia por el hecho de que un aumento de la tasa de vacunación, no se produjo la epidemia prevista para 1986. 8,9.
Actualmente a pesar de las estrategias de vacunación a nivel mundial, B. pertussis se ha convertido en un problema de salud pública y sigue siendo una de las enfermedades menos prevenibles por vacunación en todo el mundo, aún en países desarrollados con amplia cobertura de vacunación; el 95% de los casos de tos ferina ocurren en países de medianos y bajos ingresos con un estimado de 16 millones de casos y 200.000 muertes a nivel mundial cada año 10. En la última década se ha presentado un aumento en la incidencia de la enfermedad en países desarrollados, reportándose epidemias en Europa, Australia y Estados Unidos 11,12.
Estudios posteriores revelan que ni la infección, ni la vacunación inducen una inmunidad protectora, ocasionando reinfecciones frecuentes en cualquier época de la vida, siendo los infantes menores de un año el grupo más afectado, con una mayor proporción de casos en menores de 6 meses que aún no han sido vacunados o no han completado el esquema de vacunación primaria 13.
La tos ferina es una infección reemergente en países con amplia cobertura de inmunización a infantes; de acuerdo al Centro de Control y Prevención de enfermedades, Estados Unidos experimentó en el año 2012 el brote de tos ferina más grande reportado en los últimos 50 años, con más de 48000 casos reportados a escala nacional 14,15.
La reemergencia de la tos ferina puede ser atribuida a diferentes factores, entre éstos, cambios a nivel genético en las cepas circulantes de B. pertussis, una mayor circulación bacteriana entre los adolescentes y adultos, relacionado con una disminución en la inmunidad 16.
La disminución de la inmunidad inducida por la vacuna ha desplazado el pico de incidencia en los neonatos hacia los adolescentes y adultos; por otro lado, los brotes nosocomiales de la enfermedad no son infrecuentes y los trabajadores en el cuidado de la salud al ser expuestos se convierten en fuente de infección especialmente a infantes con pobre desarrollo inmunológico, como es el caso de los neonatos prematuros 17,18.
Los programas de vacunación para adultos aún no han sido implementados en muchos países; se ha demostrado que las infecciones en adultos pueden ser debido a un esquema de vacunación incompleta en la niñez, ya que éstos se van volviendo susceptibles a las infecciones a medida que aumentan la edad, además, la probabilidad de encontrar anticuerpos inducidos por la vacunación desde la infancia disminuye con el tiempo. En un estudio reciente realizado por Oksuz et al., se determinó la positividad de anticuerpos IgG anti-pertussis por el método ELISA en adultos, encontrando el 60,4% de la población en estudio negativos, y el 39,6 % positivos, de estos últimos, el 47,6% pertenecían al grupo de edad de los 51-65 años, estudios como estos recomiendan la imple-mentación de una dosis única de la vacuna contra la tos ferina para adultos con el fin de disminuir las fuentes de infección en infantes susceptibles 19.
Los neonatos a menudo contraen la infección por parientes infectados, miembros del hogar o personal del cuidado de la salud, quienes carecen de síntomas típicos; éstos últimos son los responsables de la mayoría de brotes reportados por tos ferina, ocasionando un impacto sobre neonatos, infantes hospitalizados y colegas; frente a esto, la restricción de visitantes, el uso de medicamentos inhalados y la vacunación a los trabajadores sanitarios se proponen como mecanismos eficaces contra la transmisión de la enfermedad, logrando evitar brotes intra-hospitalarios, además de la identificación temprana de un posible paciente fuente 20.
De acuerdo a lo anterior, en un estudio reciente, en el cual se realizó detección serológica de B. pertussis en personal encargado del cuidado de la salud, se encontró que el 77% del personal no poseen anticuerpos contra la bacteria; y según otros estudios, solo un tercio de los niños de escuela primaria tiene anticuerpos frente a este microorganismo, que a su vez van disminuyendo en la población adolescente y adulta, lo cual se encuentra estrechamente relacionado con la reaparición de la enfermedad 21.
Por otra parte, entre el año 2008 y 2010 Urbiztondo y cols. reclutaron 460 trabajadores del cuidado de la salud de centros de atención primaria, con el fin de determinar la susceptibilidad a B. pertussis, midiendo anticuerpos IgG (anti-pertussis), en búsqueda de anticuerpos contra la toxina pertussis (PT) y la hemaglutinina filamentosa (FHA), obteniendo resultados positivos con más de una técnica específica, cuya prevalencia fue del 51%, además de reportar títulos altos anti-PT en el 15% del personal seropositivo demostrando su reciente contacto con B. pertussis13,22.
Clínica de la enfermedad
La tos ferina es altamente contagiosa y puede esparcirse rápidamente de persona a persona mediante el contacto con aerosoles producidos al toser o estornudar por el individuo infectado, cuya bacteria se aloja inicialmente en la nasofaringe 23.
De acuerdo a estudios de enfermedades infecciosas, para valorar la transmisión de una enfermedad se tiene en cuenta el número reproductivo básico (R0), el cual estima la velocidad con que una enfermedad puede propagarse en una población; teniendo en cuenta el R0, la tos ferina es considerada una enfermedad infecciosa más contagiosa que el polio, sarampión, rubeola, paperas y difteria; en la que una persona infectada puede transmitir la bacteria a otros 12-17 individuos susceptibles 24,25.
En pacientes infectados con B. pertussis, se presenta un periodo de incubación usualmente entre 7-10 días, sin embargo, pueden llegar a presentarse hasta por 4 semanas. Esta enfermedad se caracteriza por accesos incontrolables de tos, acompañados de sibilancias respiratorias; a pesar de esto, la manifestación de signos y síntomas pueden variar dependiendo si se presenta en lactantes o adolescentes; en lactantes y niños hasta los 9 años, puede manifestarse como una enfermdad asinto-mática, hasta una presentación severa del tracto respiratorio superior con tos persistente y progresiva contínua durante semanas o meses 26.
Los síntomas clásicos consisten en tos rápida y violenta con la consecuente expulsión de aire de los pulmones, seguida de una inspiración intensa y ruidosa provocada por el espasmo de la glotis. El curso clínico de la enfermedad progresa a través de tres estadios consecutivos después de la infección y la incubación: estadio catarral, paroxístico y de convalecencia; cada uno de ellos con una duración aproximada de 1-3 semanas, y el paciente no se recupera completamente sino hasta 2-3 meses después 27.
En la primera fase se produce la infección o colonización, en la cual la bacteria llega hasta las células ciliadas del revestimiento epitelial del aparato respiratorio, donde logra la multiplicación. En lactantes a menudo se presenta sin alteración de la temperatura corporal o con febrícula, malestar general, dolor faríngeo, congestión nasal, rinorrea, lagrimación, estornudos y tos seca leve. Durante este estadio, el diagnóstico es frecuentemente pasado por alto, ya que los signos y síntomas pueden ser comunes con otras enfermedades infecciosas de origen viral como rinovirus, coronavirus e influenza; y a menudo durante esta fase los pacientes son tratados de forma ambulatoria sin un diagnóstico preciso, convirtiéndose en focos de transmisión para los contactos familiares, en escuelas y jardines infantiles 28.
En un segundo estadio se resume la enfermedad propiamente dicha, producida por la secreción de toxina que ocasionan los síntomas de la tos ferina, caracterizados por accesos violentos de tos (5-10 tos/paroxismos) que pueden durar varios minutos seguido de gritos inspira-torios, asociado a cianosis, proptosis, protrusión de la lengua, producción de salivación espesa, lagrimación e ingurgitación de las venas del cuello 29.
Los paroxismos de tos se deben al efecto de la toxina que produce el espesamiento del moco, lo cual dificulta el paso de aire por la tráquea, bronquios y bronquiolos; bloqueando las vas respiratorias y provocando asfixia y la muerte; dichos paroxismos pueden ser desencadenados por estímulos como la risa, el llanto o la deglución; ocurren más frecuentemente en la noche y su frecuencia se incrementa durante la primera a segunda semana del estadio paroxístico, con su posterior disminución gradual. Durante esta fase los pacientes pueden manifestar emesis (emesis post-tusiva), fatiga y agotamiento respiratorio 26,30.
En el tercer estadío, de convalecencia, los síntomas disminuyen en frecuencia, duración y severidad. Sin embargo, la tos no paroxística, leve y crónica, puede durar hasta 6 semanas. Al transcurrir esta fase, los pacientes ya han recibido terapia antibiótica y de soporte adecuados. La tos ferina puede ser altamente sospechada en casos de tos persistente por más de 3 semanas, independientemente si evidencia paroxismo 31.
Las complicaciones pueden suceder en todos los grupos de edad, pero más comúnmente en los lactantes quienes requieren hospitalización en aproximadamente el 50% de los casos; un 50-70% experimentan apnea; 20-23% pueden presentar neumonía y el 12% manifiestan pérdida de peso. Entre las complicaciones vistas en adolescentes y adultos se incluye la apnea (27-44%), pérdida de peso (3-33%) e incontinencia urinaria (328%). Por otro lado, han sido reportadas manifestaciones neurológicas que incluyen convulsiones, descritas en todos los grupos de edad, aunque son más comunes en los infantes 26.
Virulencia de Bordetella pertussis
B. pertussis causa una infección persistente del tracto respiratorio, que puede durar semanas o meses en los lactantes, y a menudo se asocia con infecciones secundarias y neumonía, ya que la bacteria ha desarrollado estrategias para sobrevivir y multiplicarse dentro de diferentes entornos tanto intracelulares como extracelulares 32.
La regulación y modulación en la expresión de los factores de virulencia de B. pertusis se genera principalmente en respuesta a cambios en las condiciones ambientales mediante un sistema de transducción de señales conformado por un sensor/activador (BvgAS: Bordetella virulence gene activador/sensor): las adhesinas, autotrans-portadores y toxinas, que son los principales factores de virulencia regulados por dicho sistema 33.
La invasión de la bacteria se produce por la adhesión a las células ciliadas del epitelio nasofaríngeo y del árbol traqueo-bronquial a través de moléculas de adhesión como: hemaglutinina filamentosa (FHA), fimbrias, pertactina (PRN) y otras proteínas de superficie, además de las toxinas secretadas: toxina pertussis (PT), citotoxina traqueal (CTT), toxina dermonecrótica (TDN) y la toxina adenilato ciclasa-hemosilina (ACT; CyaA), como factores importantes en su patogenicidad 34 (Figura 1).
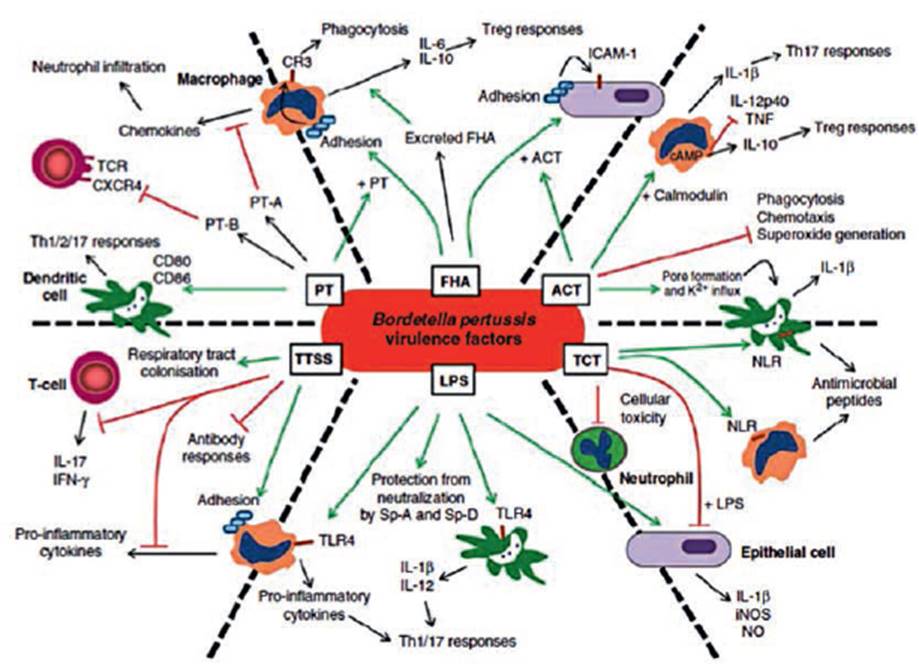
Figura 1 Efectos inmunomoduladores de los factores de virulencia de Bordetella pertussis. Este microorganismo cuenta con diferentes mecanismos para la evasión de la respuesta inmune del huésped, como factores de virulencia: Hemaglutinina filamentosa (FHA), toxina pertussis (PT), citotoxina traqueal (TCT), toxina adenilato ciclasa (ACT), sistema de secreción tipo III (TTSS) y lipopolisacáridos (LPS). Las flechas verdes indican un efecto regulador positivo hacia la célula blanco. Las líneas rojas indican un efecto modulador negativo en la célula. ICAM-1, molécula de adhesión intracelular 1; IL, interleuquina; iNOS, óxido nítrico sintetasa inducible; NLR, receptor de nucleótidos y dominio de oligomerización (NOD); NO, óxido nítrico; SP, proteína tensioactiva; TCR, receptor de células T; Th, T helper; TNF, factor de necrosis tumoral; Treg, células T reguladoras. Tomado de: Higgs R, Higgins S, Ross P, Mills K. Immunity to the respiratory pathogen Bordetella pertussis. Mucosal Immunology. 2012; 5(5):485-500. DOI:10.1038/mi.2012.54 PUBMED
B. pertussis es un patógeno no invasivo que causa infección limitada a la mucosa respiratoria; las manifestaciones sistémicas se deben a la acción de las toxinas secretadas como la toxina pertussis, la cual se encuentra relacionada con la adhesión y anclaje a los cilios respiratorios 26.
La toxina pertussis (PT) es un factor de virulencia secretado que consiste en un monómero A con actividad ribosiltransferasa de ADP, cataliza la transferencia de un grupo ADP-ribosil a las proteínas de unión a GTP reguladoras de las células el mamífero, impidiendo de esta manera la interacción del receptor acoplado en la membrana celular y su consiguiente comunicación intracelular; por otra parte, se compone de un oligómero B, que se une a las glicopro-teínas superficiales en una variedad de células huésped. La exposición a dicha toxina puede inhibir la función de varias células importantes del sistema inmune, incluyendo neutrófilos, macrófagos, monocitos y linfocitos 35.
La subunidad A inactiva proteínas G citoplasmáticas, inhibiendo varias vías de señalización de quimiocinas y conduce a la alteración de quimiotaxis de macrófa-gos, neutrófilos y linfocitos; por otro lado, el oligómero B activa varias moléculas de señalización asociadas a receptores de células T, incluyendo Zap70 y la Proteína Cinasa C, lo cual promueve posteriormente la inmunosupresión mediante desensibilización cruzada del receptor de células T y le receptor de quimioquinas CXCR4 36.
Esta toxina se compone de 5 tipos de subunidades, S1 (28 kDa), S2 (23kDa), S3 (22 kDa), S4 (11.7 kDa), y S5 (9.3 kDa). S1 demuestra la actividad enzimática de la toxina; las subunidades S2 a S5 forman el pentámero B. Dicha toxina ingresa a las células blanco por endocitosis y viaja por vía retrógrada a través del aparato de Golgi al retículo endoplasmático (RE). Del RE ingresa al citoplasma disfrazándose como una proteína huésped mal plegada y entrando en la vía de degradación asociada a RE; una vez en el citosol, la subunidad S1 cataliza la transferencia de Adenosina 5'Difosfato (ADP)-ribosa de la Nicotinamida Adenina Dinucleótido (NAD) a la subunidad inhibitoria alfa de la proteína G (Gi α). La ADP-ribosilación de Gi previene la inhibición de la ade-nilato ciclasa y conduce a un aumento sostenido de la concentración intracelular de Adenosina Monofosfato Cíclico (cAMP) (37). (Figura 2.)
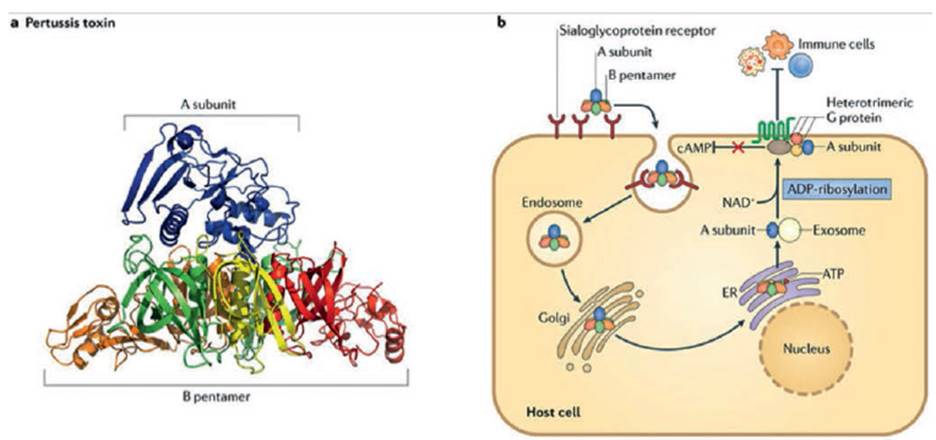
Figura 2 a. Toxina pertussis (PT; Protein Data Bank (PDB) acceso 1PRT): es una toxina tipo AB 5 compuesta por una subinidad catalítica (subunidad A) y un pentámero de unión a la membrana o subunidad transportadora (pentámero B). PT es ensamblada en el periplasma bacteriano y exportado por el sistema de secreción tipo IV. b. Después de la unión al receptor celular de sialogli-coproteina. PT es endocitada y llevada a través del apartato de Golgi y el Retículo endoplasmático (ER). En el ER, el pentámero B se une al ATP y se disocia d ela subunidad A. Esta última, es luego transportada dentro del citoplasma y circula dentro de exosomas hasta la membrana plasmática, donde ocurre ADP-ribosilación de la subunidad-α de la proteína G heterotrimérica. Estas modificaciones alteran la habilidad de la proteína G de regular múltiples rutas enzimáticas, incluyendo la habilidad de inhibir la formación de AMPc. El resultado conjunto de esas modificaciones es la supresión inicial de la producción de citoquinas inflamatorias y la inhibición del reclutamiento de células de la respuesta inmune al sitio de la infección. Tomado de: Bordetella pertussis pathogenesis: current and future challenges. Melvin J, Scheller E, Miller J, Cotter P. Nature. 2014: 12; 274-288.
Por otro lado, la Toxina Adenilato Ciclasa (ACT; CyaA) está involucrada en la colonización temprana del tracto respiratorio. Esta toxina invade las células eucariotas y ocasiona sobreproducción de los niveles de cAMP, alterando la fisiología celular, con la supresión de la respuesta inmune del huésped llevando finalmente a la muerte celular 38.
La toxina cataliza la formación de niveles suprafisiológi-cos de AMPc, lo cual inhibe la función antibacteriana de los macrófagos y suprime la secreción de las citocinas inflamatorias IL-12p70 y TNF-α y promueve la secreción de IL-10, que junto con la IL-10 inducida por FHA, promueven el desarrollo de células Treg Tr1 antígeno-específicas, las cuales revierten la respuesta inmune del huésped y retrasan la eliminación bacteriana 39
Además de sus funciones inmunomoduladoras, el dominio C-terminal promueven la formación de poros en la membrana de la célula diana, produciendo un flujo de K+, lo cual genera la formación y activación del complejo de inflamasoma NLRp3, que resulta en la activación de la caspasa-1 y la liberación de IL-1B desde las células dendríticas, citoquina importante en la protección del huésped y el aclaramiento bacteriano mediante la inducción de células Th17 (IL-17) 40.
Esta es una proteína bifuncional y toxina AB, pero a diferencia de las enterotoxinas AB5 como la PT, se compone de un único polipéptido de 1706 aminoácidos que presenta dos dominios; uno de ellos con actividad adenilato ciclasa (AC) sensible a calmodulina (CaM), ubicado dentro de los 400 aminoácidos próximos al extremo NH2-terminal; el otro dominio RTX (Repeat-in-ToXins) ó hemolítico (Hly) hace parte de los aminoácidos restantes (1306), involucrados en la unión de la toxina a las células diana y la entrada del dominio catalítico al citosol, además de promover la formación de poros en la membrana de las células diana 41.
Esta toxina pertenece a la familia de toxinas citolíticas formadoras de poros (hemolisina RTX), análoga a las toxinas citolíticas formadoras de poros dependientes de Ca+2, producidas por bacterias patogénicas gram negativas, tales como la α-hemolisina de Escherichia coli y leucotoxina de Pasteurella hemolítica42.
El dominio catalítico de CyaA está compuesto a su vez por dos subdominios conocidos como T25 y T18; en ausencia de CaM, este dominio se encuentra en estado de desorden estructural, en el cual su estructura terciaria es compacta e hidratada; una vez que el dominio C-Termi-nal de la CaM interactúa con el subdominio T18 de la toxina, el extremo NH2-terminal adquiere una conformación extendida y deshidratada, proporcionándole cambios en sus propiedades hidrodinámicas 43.
Por otra parte, el extremo RTX (C-Terminal) de la toxina contiene el dominio de unión al receptor (RD, en los residuos 1006 a 1706); esta región es rica en aspartato y glicina, además de repeticiones en tandem de nonapéptidos de unión al calcio, lo cual es una de las características de la gran familia de toxinas citolisinas bacterianas conocidas como RTX (Repeat-in-ToXin). El dominio RD se caracteriza por un alto nivel de desorden estructural y cargas principalmente negativas, las cuales son parcialmente neutralizadas por la unión al calcio, lo cual favorece la transición del desorden, al orden estructural; por otro lado, el calcio induce el plegamiento del dominio RD requerido para la actividad biológica de la toxina 44. Este dominio, RTX, puede subdividirse en 4 regiones: 1) una región en la que se ubican varios segmentos hidrofóbicos que se insertan en la membrana plasmática adoptando estructuras alfa-hélice, 2) otra región donde ocurre la palmitoilación de la Lys, 3) una región de 38 a 42 repeticiones de los motivos RTX, 4) una señal de secreción carboxi-terminal no procesada 45.
El extremo C-Terminal sufre un cambio conformacional en presencia de Calcio, en el cual varios motivos se pliegan formando hélice B, y en cada giro B, el Calcio se une al grupo carbonilo de la cadena lateral del aspartato; es necesaria la unión de 30 a 40 iones de Calcio para llevar a cabo el plegamiento y actividad de la toxina; la unión del calcio permite conservar la capacidad de la toxina frente a la permeabilización y actividad hemolítica de la forma monomérica de CyaA, hCyaAm, bajo un ambiente rico en dicho cofactor, además, la unión del dominio C-terminal al calcio permite la fuerte estabilidad de regiones N-terminal 46.
El calcio es un cofactor esencial tanto para la toxina CyaA, como para los otros miembros de la familia de toxinas RTX; ya que se une a los segmentos repetidos RTX y es de vital importancia para llevar a cabo las diferentes funciones de la toxina, incluyendo la secreción, la unión al receptor celular y/o membrana de la célula blanco, la formación de poros y actividad hemolítica, y finalmente para el ingreso del dominio catalítico de la toxina a través de la membrana plasmática 47.
La toxina adenilato ciclasa (ACT) se sintetiza como un precursor inactivo (proCyaA) codificado por el gen CyaA, que es convertido a su forma activa CyaA, ya que el dominio RTX alberga los sitios de activación, que se produce gracias a la palmitoilación de la Lisina 860 y Lisina 983 (Lys 860; Lys 983), mediada por la aciltransferasa CyaC. Estas dos modificaciones postraducciona-les son esenciales para la actividad citotóxica de CyaA y también para el replegamiento de la toxina en un estado holo-monomérico ya que las acilaciones mejoran significativamente el rendimiento de recuperación de monómeros frente a oligómeros y multímeros 48.
CyaA penetra las células blanco mediante una serie de pasos: en una fase inicial dicha toxina se une a la superficie celular, posiblemente a gangliósidos, para lo cual es necesaria la integridad del extremo C-terminal de la toxina y de la palmitoilación de la Lys; dicho proceso de ingreso puede resumirse en tres pasos consecutivos que incluyen la inserción, la translocación y el clivaje intracelular; una vez la toxina es insertada en la membrana de la célula blanco, la porción NH2-terminal es translocada al otro lado de la membrana mediante la creación de un canal proteico por el dominio C-terminal de la toxina 49 (Figura 3).
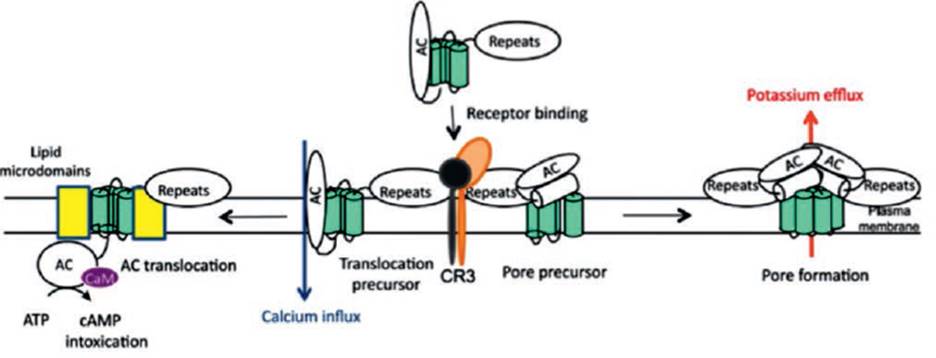
Figura 3 Representación esquemática de la función de CyaA. La invasión celular y la formación de poros por la toxina parecen ser funciones independientes, pero se efectúan en paralelo sobre la membrana de la célula blanco. La toxina está conformada por dos dominios, uno de ellos permite la translocación y la entrega de la región catalítica de la toxina a través de la bicapa lipídica, y a su vez provoca la afluencia concomitante de iones de calcio en las células. El otro dominio permite la formación del poro provocando el flujo de potasio en la célula diana que promueve liberación de IL-1S. Tomado de: Masin J, Osicka R, Bumba L, Sebo P. Bordetella adenylate cyclase toxin: a unique combination of a pore-forming moiety with a cell-invading adenylate cyclase enzyme. FEMS Pathogens and Disease, 2015; 73(8): ftv075.
Luego de ser secretada, el dominio RD se une de manera dependiente de calcio a la integrina CD11b/CD18 expresada en células mieloides, tales como macrófagos, células dendríticas, neutrófilos y células NK, siendo este tipo de células los principales blancos de la toxina CyaA in vivo50.
Esta unión de alta afinidad se realiza principalmente al complejo CD11b/CD18, que pertenece a los receptores aMp2 de la subfamilia de receptores leucocitarios, conocidos como receptores de complemento-3 (CR3); sus cadenas a y β equivalen a glicoproteínas transmembrana de 165 kDa y 95 kDa respectivamente, usualmente expresados en la superficie de células mieloides, ocasionando que la función de dichas células efectoras de la respuesta inmune se encuentre alterada 51.
A pesar de que la toxina utiliza para su ingreso la vía principal a través de dicho receptor, ésta también puede ingresar a una gran variedad de células de forma independiente del mismo, a través de otros receptores específicos independiente de acilaciones post-translacionales de la toxina, o mediante la interacción directa gracias al potencial de membrana 52.
El dominio catalítico de la toxina es conducido hacia el citoplasma mediante la formación de un poro mediado por el dominio C-terminal, proceso llamado translocación o intoxicación, durante esta fase hay un incremento rápido de los niveles de cAMP; por otro lado, la entrada de la toxina es independiente de la acidificación de las vesículas endocíticas; estudios han demostrado que la toxina CyaA, tiene la capacidad única entre las toxinas enzimáticamente activas, de cruzar directamente la membrana citoplasmática de la célula y llegar al citosol sin necesidad de endocitosis; como se ha reportado in vitro, la toxina es capaz de penetrar con eficacia una variedad de tipos celulares incluyendo los eritrocitos de mamíferos que carecen de mecanismos de endocitosis de membrana 46,53,54.
Una vez dentro de la célula, el dominio catalítico, es activado por la calmodulina y cataliza la conversión de ATP a cAMP, molécula clave que actúa como segundo mensajero provocando deterioro en las funciones bactericidas de los fagocitos como la quimiotaxis, la fagocitosis, o la producción de superóxido además de promover la apoptosis de los macrófagos 55-57.
La hemaglutinina filamentosa (FHA) son estructuras similares a bastones de aproximadamente 220.000 Da, que median la adhesión a las células ciliadas del epitelio respiratorio, a través de una integrina (RGD con secuencia arginina, glicina y ácido aspártico) (58), además de un dominio de reconocimiento a carbohidratos y de unión a heparinas se encuentra expresada en la superficie de la célula bacteriana, pero también es secretada al medio extracelular. Su papel en la adherencia al epitelio respiratorio se intensifica en presencia de ACT y balsas lipídicas de colesterol 59.
Por otro lado, promueve la fagocitosis de B. pertussis por los macrófagos y polimorfonucleares; además de su papel en la adherencia bacteriana y fagocitosis, también tiene importantes funciones inmunomoduladoras, incluyendo la producción de IL-6 e IL-10, la supresión de la producción de IL-12 por los macrófagos y CDs, lo cual conduce a la generación de células Treg y la producción consecuente de IL-10, a su vez, éste suprime la formación de IFN- γ y por tanto inhiben la formación y función de células Th-1 60.
La pertactina (PRN) es una proteína autotransportadora de la membrana externa de 69 kDa, la cual tiene un papel importante en la adherencia de B. pertussis a mono-citos y células epiteliales; hace parte de las proteínas de membrana externa con motivo RGD y su expresión es modulada por el locus vir, el cual controla la expresión de los otros factores de virulencia bacteriana 61.
PRN es también un blanco importante para los anticuerpos inducidos tanto en la infección natural como por la vacuna, ya que es uno de los componentes de la mayoría de las vacunas acelulares en uso actual 62.
Sin embargo, investigaciones reportan aislados de B. pertussis con una baja producción de PRN en hallazgos realizados en diferentes países donde ha sido introducida la vacuna acelular (aP) contra la tos ferina. Recientes estudios han demostrado que las cepas deficientes en PRN colonizan el tracto respiratorio de forma más efectiva que las cepas productoras de la proteína, en ratones vacunados con la vacuna aP. Se ha demostrado que los aislamientos de la bacteria, que no producen PRN son capaces de mantener una infección más duradera en comparación con los aislados productores de la misma, en un modelo in vivo inmunizado con la vacuna aP; por tanto, la pérdida de la producción de PRN podría proporcionar una ventaja selectiva de estas cepas, lo que explica el aumento de dichos aislados en la población 63-65.
Respuesta Inmune Del Hospedero
B. pertussis cuenta con una gama de toxinas y otros factores de virulencia críticos para la invasión y producción de la enfermedad, los cuales son dianas antigénicas para anticuerpos y células T. Además de su replicación extracelular, lo hace también en células del epitelio respiratorio, de igual forma puede sobrevivir al interior de los macrófagos; lo anterior sugiere que tanto la inmunidad celular como la humoral son necesarias para la eliminación de la bacteria en el tracto respiratorio 41.
La bacteria se une a células del epitelio ciliado tanto de la tráquea, bronquios, bronquiolos y de manera intracelular se encuentra en células epiteliales ciliadas y macrófagos alveolares; los macrófagos infiltrados y residentes, son las primeras células de la respuesta inmune innata en detectar y responder a la infección; posteriormente es seguido por un flujo de neutrófilos, luego de células NK y finalmente de células T α/β; en cuanto a la inmunidad humoral, la IgA secretora y la IgG han sido reportadas en experimentos de modelos murinos 41.
Modelos animales de infección por B. pertussis, así como estudios in vitro, han demostrado que la bacteria puede ingresar, sobrevivir y persistir en los macrófagos, sugiriendo que estas células permiten la propagación y la diseminación de la infección a nuevos huéspedes. Una alta proporción de bacterias fagocitadas son destruidas dentro de los compartimentos ácidos de los macrófagos, pero otra cantidad pueden evadir su destrucción y reproducirse 66.
A diferencia de los macrófagos, los neutrófilos no son buenos reservorios para B. pertussis, debido a su corta vida media, sin embargo, juegan un papel crucial en la fagocitosis bacteriana. A pesar de esto, los factores de virulencia permiten la evasión de esta respuesta y la supervivencia del microorganismo. La toxina pertussis parece modular la respuesta inmune temprana a B. pertussis, retrasando la infiltración de neutrófilos; del mismo modo la ACT puede inhibir la función de los neutrófilos por la disminución en su capacidad de fagocitosis, la generación de superóxido y la inhibición de la quimiotáxis 67.
Por otro lado, las CDs permiten la presentación de an-tígenos a las células T y proveen una fuente de citoqui-nas innatas que promueven la diferenciación de células T naive; el reconocimiento de los factores de virulencia de B. pertussis generan fuertes señales proinflamato-rias que son cruciales para desencadenar la producción temprana de citoquinas y quimiocinas, seguido por la activación de la respuesta de células T 68.
Los lipopolisacáridos (LPS) bacterianos se unen a los Toll-like receptor 4 (TLR-4) en las CDs e incentivan su maduración y la secreción de IL-12 e IFN- γ, que impulsa la inducción de células Th1, y éstas a su vez median el aclaramiento bacteriano. Además, la activación de CDs por la ACT, también promueve la inducción de células Th1. Los otros factores de virulencia como FHA, generan respuestas antiinflamatorias, incluyendo la producción de IL-10 por CDs, que conduce a la producción de células Treg, las cuales evidencian un papel protector esencial, ya que estudios han demostrado que la ausencia de células Treg productoras de IL-10 aumentan la mortalidad mediada por excesiva inflamación en los pulmones ocasionada por la infección de B. pertussis69 (Figura 4).
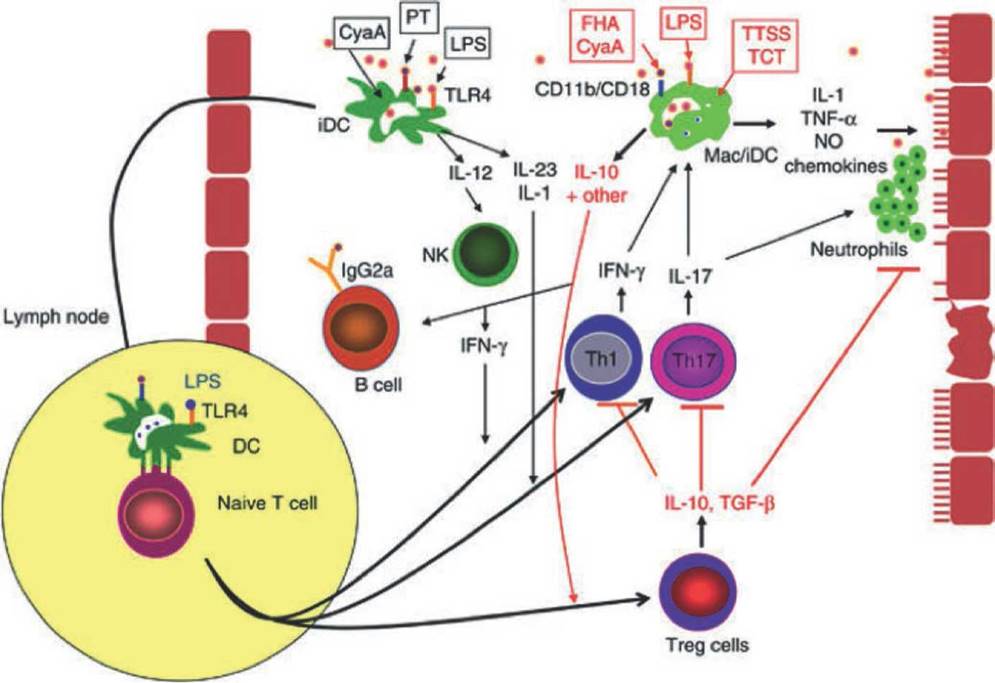
Figura 4 Respuesta inmune del hospedero frente a la infección por B. pertussis. Una vez B. pertussis ingresa en el tracto respiratorio, ésta se une a las células epiteliales ciliadas, donde migran células de la respuesta inmune innata, como macrófagos (Mac) y células dendríticas (iDC). Las DC presentan antígenos bacterianos a las células T. Se genera la producción de interleucina IL-12 por células de la respuesta innata y se impulsa la producción de células T helper tipo 1 (Th1); la e IL-23 promueven la diferenciación de células Th17. Sin embargo, en la infección temprana, la acción de las células T locales es suprimida por células innatas que secretan IL-10 como respuesta a la hemaglutinina filamentosa (FHA), la toxina de adenilato ciclasa (ACT) y por la acción de las células T reguladoras (Treg). El óxido nítrico (NO) y las citoquinas pro-inflamatorias, IL-1 y el factor de necrosis tumoral TNF-α, son inducidos por toxinas bacterianas, especialmente lipopolisacárido (LPS), citotoxina traqueal (TCT), ACT y toxina pertussis (PT), que además contribuyen a la eliminación bacteriana, también median la patología pulmonar local y son responsables de muchas de las consecuencias sistémicas y neurológicas de la infección. El interferón (IFN) -γ secretado tempranamente en la infección por células DC y natural killer (NK); de modo más tardío en la infección, las células Th1, estimulan el reclutamiento y la activación de macrófagos y neutrófilos. La IL-17 secretada por células Th17 promueve la producción de proteína 2 inflamatoria de macrófagos y el reclutamiento y activación de neutrófilos. Las bacterias opsoniza-das o no opsonizadas son absorbidas por neutrófilos y macrófagos, que son destruidos por el NO o intermedios reactivos de oxígeno. Las flechas negras representan respuestas inmunes inflamatorias/efectoras y las flechas rojas representan respuestas antiinflamatorias e inmunosupresoras. TGF, Factor de Crecimiento Transformante; TLR4, Receptor tipo Toll 4. Tomado de: Higgs R, Higgins S, Ross P, Mills K. Immunity to the respiratory pathogen Bordetella pertussis. Mucosal Immunology. 2012; 5(5):485-500. DOI:10.1038/mi.2012.54 PUBMED
Estudios en modelos murinos muestran que los mecanismos de la respuesta inmune innata involucran células dendríticas (CDs), macrófagos, neutrófilos, células Natural Killer y péptidos antimicrobianos que ayudan al control de la infección; por otro lado, el aclaramiento bacteriano requiere de la respuesta inmune mediada por células. Investigaciones ha revelado diferencias mecánicas en el tipo de respuesta inmune celular inducida con los distintos tipos de vacunas: de células enteras (wP), como la acelular (aP); la vacuna wP, a pesar de su propensión a causar reacciones adversas en los receptores, es capaz de inducir una fuerte respuesta inmune celular; estudios en años recientes demuestran que tanto la infección natural como la vacuna wP, inducen predominantemente respuesta vía Th1 con presencia de IFN-γ e IL-17 por células Th17 en menor proporción; por el contrario, la vacuna aP, induce principalmente respuesta Th2 y Th17, con una débil respuesta de Th1 70.
Una inmunidad mediada por células Th17, es necesaria para brindar protección contra bacterias extracelulares ya que la IL-17 promueve el reclutamiento de neutrófilos 73. Por otro lado, se ha demostrado que el INF-γ es necesario para el control de la infección en el tracto respiratorio, ya que los ratones que carecen de esta citoquina o de su receptor, desarrollan infección letal y diseminadora 41.
En un trabajo llevado a cabo por Ross et al., en el 2013, se demostró la contribución de las células Th1 y Th17 en la respuesta inmune adaptativa frente a B. pertussis, ya que ambos tipos de células permitieron la eliminación la infección primaria en ratones previamente vacunados con wP; y por otro lado, mediante el uso de la vacuna aP con sales de aluminio como adyuvante, logró inducir respuestas de tipo Th17 así como de tipo Th2. Se plantea que la respuesta mediada por Th17, requiere de la activación de señalización IL-1R en células de la inmunidad innata y su protección se asocia con el reclutamiento, activación y muerte celular a nivel pulmonar después de la estimulación con B. pertussis, mediado por neutrófilos 71.
Tradicionalmente se han aceptado las sales de aluminio (alumbre) como adyuvantes en las vacunas aP que aumentan la respuesta inmune a los antígenos de la vacuna y facilitan la retención del antígeno en el sitio de inyección promoviendo la respuesta de anticuerpos y la captación del antígeno por las células presentadoras para el posterior cebado de las células T en los ganglios linfáticos; por otro lado, se ha reportado que el alumbre promueve la respuesta celular tipo Th2, las cuales proveen la protección mediada por anticuerpos contra bacterias extracelulares; más recientemente, ha sido demostrada la función del alumbre en la activación del inflamasoma NLRp3, involucrado en la mediación de cambios confor-macionales que permiten el reclutamiento de la proteína adaptadora ASC (apoptosis-asociated speck-like protein containing a caspase recruitment domain), importante para el reclutamiento y activación de caspasa-1, responsable de la maduración y obtención de las formas activas de IL-1β e IL-18 72,73.
Avances en inmunización
La combinación triple de toxoides diftérico-tetánico y componentes de B. pertussis (células enteras o acelula-res) es una de las vacunas más utilizadas en todo el mundo (131 países con una cobertura de >90% en 2012) en una serie primaria de 3 dosis y refuerzo en el segundo año de vida 74.
Frente a la necesidad de inmunizar adolescentes, además de proporcionar seguridad concerniente a la vacuna wP y problemas en su fabricación, condujo el desarrollo, autorización e introducción de vacunas acelulares contra la tos ferina (aP) en los años 90'. Esta vacuna reemplazó rápidamente la vacuna wP para la inmunización a recién nacidos, además de la inmunización de refuerzo para los adolescentes en países desarrollados y luego su introducción como refuerzo para los adultos. La aP está compuesta por proteínas purificadas de B. pertussis, en partirucular la toxina pertussis (PT), hemaglutinina filamentosa (FHA), pertactina (PRN) y agluninogenos fin-briales FIM2 y FIM3. A comparación de otras vacunas, la protección eficiente de aP parece necesitar al menos tres antígenos en la formulación; estudios clínicos de la vacuna aP muestran que la eficacia de tres o más componentes vacunales es comparable con la vacuna wP, mientras que uno o dos componentes fueron reportados menos eficaces 75-77.
Las últimas estrategias incluyen el uso de la vacuna ace-lular, la cual induce inmunidad específica contra pocos factores de virulencia entre los cuales la pertactina es incluida en tres de cinco componentes acelulares 78. A pesar de la efectividad de ésta, se ha reportado un incremento en la prevalencia de aislados B. pertussis no productores de PRN; en algunos países como Francia, se usa una vacuna aP de dos componentes que incluye la toxina Pertussis (PT) y la hemaglutinina filamentosa (FHA), o vacuna aP de tres componentes (aP-3), incluyendo PT, FHA y PRN; ésta última vacuna se utiliza para la inmunización de lactantes y adolescentes, en la cual una elevada proporción de la vacuna induce inmunidad dirigida frente a PRN 78.
Sin embargo, estudios han reportado que aislados clínicos deficientes en PRN, resisten la inhibición in vitro de la citotoxicidad celular cuando se incuban junto con anticuerpos específicos anti-PRN, lo cual podría ser una ventaja selectiva ya que los aislados deficientes en PRN, podrían resistir la actividad opsonofagocítica mediada por anti-PRN bajo dichas condiciones 79.
Uno de los interrogantes es si la falta de producción de pertactina podría ser beneficiosa in vivo, en inmunizaciones con aP-3 que promueva la formación de anticuerpos anti-PRN debido a los mecanismos antes mencionados 75. Estudios de evaluación de asociación entre la producción de PRN y la inmunización, sugieren que las personas vacunadas tienen una mayor susceptibilidad a las cepas deficientes en pertactina comparado con las cepas productoras; aquellas cepas deficientes en PRN (PRN-) se sospecha que evaden la inmunidad inducida por la vacuna o alteran la gravedad de la enfermedad; en un reciente estudio realizado por Martin y et al. Se evaluó de manera retrospectiva la asociación entre la producción de pertac-tina (PRN-, PRN+), la presentación clínica de la enfermedad y el historial vacunal; el 85% de los aislados fueron PRN-; se concluyó que existe una asociación significativa entre la inmunización y la producción PRN+, lo cual sugiere que la probabilidad de que se haya desarrollado la enfermedad causada por las cepas PRN- es mayor en los pacientes vacunados 80.
En estudios recientes, han utilizado formulaciones de pro-teoliposomas de B. pertussis (PLBp), toxoide tetánico y difteria (DT-PLBpI), evaluándose como vacuna trivalente candidata en ratones BALB/c; con lo cual se evidenció una reducción total de UFC a nivel pulmonar a los 7 días después del inoculado intranasal de B. pertusis, además de inducir la producción de anticuerpos > 2UI/mL contra tétano y difteria 81.
Los proteoliposomas son estructuras vesiculares nano-particuladas que contienen proteínas, lípidos y lipopo-lisacáridos nativos (LPS), gracias a sus propiedades in-munoestimulantes y adyuvantes, las hacen moléculas atractivas para el desarrollo de vacunas contra varias enfermedades 82.
En la actualidad, las vacunas acelulares contra la tos ferina no proporcionan una inmunidad protectora adecuada y estudios demuestran cambios significativos en las poblaciones de B. pertussis, lo que sugiere la adaptación, la persistencia y el resurgimiento bacteriano frente a la evasión de la presión ocasionada por las vacunas; estos cambios incluyen divergencia antigénica con las cepas vacunales y el aumento en la producción de toxina pertussis; la divergencia antigénica afecta principalmente la memoria inmune y la eficacia de los anticuerpos, mientras que los niveles altos de la toxina pueden aumentar la supresión del sistema inmune innato y adquirido 83-85.
Finalmente, debe considerarse la contribución de los cambios genéticos de las cepas circulantes de B. pertussis, a la enfermedad; es claro que éstos han ocurrido en diferentes antígenos bacterianos, los cuales han llevado a que el microorganismo eluda la inmunidad inducida por la vacuna o sea más virulento; dichos cambios pueden atribuirse a la presión selectiva ejercida por la vacuna a lo largo del tiempo. Estudios genéticos demuestran pérdida de regiones en el genoma de diferentes cepas circulantes; de acuerdo con esto, en un trabajo realizado por Kallonen y et al. en el 2011, se encontraron diferencias en el contenido genómico de B. pertussis aislada antes y después de la introducción de la vacuna contra la tos ferina en cuatro países europeos; mediante técnicas moleculares, los autores compararon el genoma de 39 cepas vacunales y aislados clínicos antiguos colectados de los diferentes países, observando pérdida de tres regiones genómicas en los aislados analizados, además de describir un nuevo alelo promotor de la toxina pertusis (ptxP3), que reemplazó los aislados con el alelo ptxP1 en los países evaluados; dichos hallazgos demuestran que las cepas circulantes en Europa en la época pre-vacunal y sus genomas eran distintos a las cepas de referencia correspondiente a los aislados recientes, lo que sugiere que dichas diferencias genómicas podrían deberse a la presión inducida por la introducción de la vacuna 86.
Como lo han demostrado otros estudios, se ha producido una pérdida progresiva de genes en los aislamientos B. pertussis, en países como Finlandia, posterior al inicio de la vacunación contra la tos ferina en dicho país desde 1952; los resultados de dichos estudios confirman que las cepas circulan de manera dinámica y evolucionan continuamente, lo que sugiere que la bacteria puede usar la pérdida de genes como una estrategia para adaptarse a poblaciones altamente imnunizadas 87.
En una investigación reciente se compararon los reordenamientos en el genoma entre 257 aislados de B. pertussis para evaluar la estructura cromosomal, en la cual se identificaron cambios discretos que diferenciaron el genoma de las cepas de referencia de la vacuna y varios aislados clínicos; entre los reordenamientos observados fueron principalmente grandes inversiones centrados en el origen de replicación y flanqueados por un elemento genético móvil > 240 copias por genoma (IS481), y previamente reportado como mediador de reordenamientos y deleciones por recombinación homóloga; dichos datos sugieren que la evolución del genoma estructural de B. pertussis no se limita a la pérdida de regiones en el ge-noma, sino que también incluye reordenamientos, y aunque los genomas de los aislamientos clínicos se evidencia heterogeneidad estructural, se conservan cambios específicos en el orden de los genes, posiblemente debido a la selección positiva, lo que proporciona información novedosa para futuras investigaciones en el resurgimiento de la enfermedad 88
Hacia un futuro, con la ayuda de técnicas moleculares, de proteómica y metabolómica, se pretende dar un enfoque más integrado del problema, incluyendo las características de las vacunas, las poblaciones de B. pertussis y la interacción entre éstas.
Discusión
Después de la exposición a B. pertussis, la patogenia de la enfermedad depende de cuatro etapas: fijación, evasión de defensas del huésped, daño local y enfermedad sistémica. La aparición de la enfermedad, que implica la unión al epitelio respiratorio, la existencia de lesiones locales y la absorción sistémica de toxinas depende de la alteración y desaparición de los mecanismos de defensa del huésped (cilios y neutrófilos). Está claramente demostrado que la vacunación no proporciona protección para toda la vida contra la tos ferina 89,90.
Estudios recientes demuestran que la citotoxina traqueal, el factor dermonecrótico y la adenilato ciclasa, son en su mayoría las responsables del daño epitelial local que da lugar a los síntomas respiratorios y facilita la absorción de la Toxina Pertussis, que a su vez posee numerosas actividades biológicas, sensibilidad a la histamina, la secreción de insulina, la disfunción leucocitaria y otras, algunas de las cuales pueden explicar las manifestaciones sistémicas de la enfermedad.
La clínica de la tos ferina es diferente en adolescentes respecto a los lactantes, aunque en general es menos grave, también se observan casos graves y complicaciones. Una tos persistente puede ser el único síntoma, tos de más de 4 semanas de evolución, tos nocturna o que se exacerba al comer o beber es igualmente típico en adolescentes 91,92.
Para el desarrollo de nuevas vacunas contra la tos ferina, múltiples estudios han realizado aportes que permitan una vacuna más eficiente, y entre las características más importantes para su desarrollo, al igual que para cualquier otra vacuna, se encuentran: 1) inducir un patrón de respuesta inmunitaria similar a la infección natural, 2) mostrar un perfil reactogénico mejor que las vacunas tradicionales, 3) ser multi-antigénicos con el fin de eludir la presión de la vacuna, 4) ser asequible tanto para los países desarrollados como para los países en desarrollo 93.
Actualmente se le da mucho valor al criterio clínico de tos ferina ya que la confirmación debe realizarse con métodos auxiliares de diagnóstico como el cultivo o la reacción en cadena de la polimerasa (PCR), no siempre disponible 93.














